ANTECEDENTES
Con el envejecimiento, el sistema inmunológico experimenta cambios adaptativos conocidos como inmunosenescencia. El proceso de adaptación deficiente provoca mayor susceptibilidad a enfermedades infecciosas, autoinmunes, inflamatorias y neoplásicas en los adultos mayores.1 En algunos casos aparece un estado proinflamatorio, caracterizado por aumento en la producción de citocinas (IL-1, IL-3, IL-6, TNF-α/β y proteína C reactiva), así como disminución en la función de linfocitos T reguladores, T citotóxicos, células Natural Killer, linfocitos T vírgenes y sus receptores. Estos cambios se han denominado por algunos autores como inflammaging.2,3
En los adultos mayores, el hígado, los pulmones, intestinos y, especialmente, la piel, producen citocinas proinflamatorias de manera continua.4 Dentro de los factores implicados con la senescencia cutánea y el inflammaging se encuentran: edad avanzada, tabaquismo, exposición a la luz ultravioleta, contaminación ambiental y estados de malnutrición.5 Los trastornos nutricionales son comunes en la población adulta mayor; entre el 50 y 80% consumen menos del 75% de las cantidades diarias recomendadas de nutrientes, lo que sugiere que un tercio de las personas mayores de 65 años tiene déficit nutricional.6
La hipersensibilidad retardada se ha estudiado en humanos de diferentes edades, y se ha observado que en adultos mayores de 60 años existe una disminución en la respuesta intradérmica, debido al declive de los linfocitos T asociado con la edad y exposición al estrés crónico.7,8 La deficiente respuesta a diversos antígenos, conocida como anergia, puede detectarse de manera oportuna y, potencialmente, mejorar la tasa de morbilidad y mortalidad.9 Por lo tanto, es crucial estudiar la interrelación entre vejez, nutrición e inmunidad, ya que estos factores son determinantes para la calidad de vida de los adultos mayores.10
El objetivo de este estudio fue: analizar la relación entre la respuesta inmune celular, evaluada a través de pruebas intradérmicas de hipersensibilidad retardada, y el estado nutricional de mujeres adultas mayores.
MÉTODOS
Estudio observacional, de correlación, efectuado en mujeres adultas mayores jubiladas de un Hospital Regional. Se incluyeron pacientes sin infección activa, previo consentimiento informado. El proyecto fue dictaminado y aprobado por los comités de investigación y ética en investigación del Hospital Regional ISSSTE Puebla y otorgaron número de registro 615.2023.
Se aplicaron pruebas de intradermorreacción en el antebrazo no dominante, con una distancia de 5 cm entre cada uno, utilizando 0.1 mL de:
Antígeno de candidina (Monilia Skin test Antigen): Dilución 1:100 en solución salina al 0.9%.
Antígeno de bacterias Gram (+) [Staphylococcus aureus 180 UFC/mL, Streptococcus pneumoniae 22.5 UFC/mL, Klebsiella pneumoniae 22.5 UFC/mL, Branhamella catarrhalis 22.5 UFC/mL, Haemophilus influenzae 22.5 UFC/mL] (Alergomex). Dilución 1:10 en solución salina al 0.9%.
Antígeno de Escherichia coli: Para obtener los antígenos se seleccionaron cepas sensibles a partir de urocultivos. El cultivo se llevó a una concentración de 0.5 McFarland (1 × 108/mL bacterias). Posteriormente para la aplicación de los antígenos, las bacterias fueron esterilizadas en UV durante 30 min (se confirmó la falta de crecimiento en medio de cultivo), y finalmente para la prueba de intradermorreacción se aplicó una concentración de 1 × 109/mL bacterias.
Antígenos de tétanos/difteria: Dilución 1:10 en solución salina al 0.9%.
La respuesta se midió a las 4, 24, 48, 72 horas, y posteriormente a las 96 horas de la aplicación. La induración se consideró positiva con una medida > 5 mm.
Se utilizaron las escalas: 1) MNA (Mini Nutritional Assessment) para evaluar el estado nutricional,11 y 2) Lawton-Brody para valoración de la funcionalidad. Se colectaron los datos de laboratorio (biometría hemática, química sanguínea, examen general de orina) a partir del expediente clínico.
Para el análisis estadístico se implementaron coeficientes de correlación r de Pearson o Rho de Spearman, según la distribución de las variables. Para la predicción de malnutrición se calculó el área bajo la curva ROC, y se consideró estadísticamente significativo el valor de p > 0.5 y p < 0.05.
Responsabilidades éticas
Todos los procedimientos realizados durante el desarrollo de esta investigación se realizaron conforme al reglamento de la Ley General de Salud en materia de investigación para la salud, así como la Declaración de Helsinki. El número de aprobación por los comités de investigación, ética en investigación y bioseguridad del Hospital Regional ISSSTE Puebla, fue el 615.2023.
RESULTADOS
Se registraron 36 mujeres con promedio de edad de 69.2 ± 5.9 años; el 66.7% tuvo sobrepeso y 27.8% diabetes. El 83.3% mostró un estado nutricional normal y el 16.7% con riesgo de malnutrición. La escala MNA reportó un puntaje de 25.6 ± 2.7 (0 a 29). La induración mayor de 5 mm, posterior a 48 horas de los diferentes antígenos fue: bacterias Gram + 21 (58.3%), tétanos-difteria 14 (38.9%), candidina 24 (66.7%), y Escherichia coli 0 (0%; Cuadro 1). Luego de 48 horas, excepto Escherichia coli, el promedio de la induración fue mayor de 5 mm. Cuadro 2
Respecto de la coexistencia de bacteriuria asintomática, apareció en el 33.3% de las pacientes con riesgo de malnutrición versus 30.8% con estado nutricional normal (p = 0.7). La respuesta a candidina fue más frecuente en las mujeres adultas mayores con riesgo de malnutrición (OR: 1.3; IC95%: 1.1 - 1.7; p = 0.05). Cuadro 3
La correlación de induración entre las diferentes mediciones de los mismos antígenos fue: candidina a las 4 h con candidina a las 72 h mostró una correlación moderada: +0.42 (p = 0.01); la induración de bacterias Gram (+) a las 4 h con bacterias Gram + a las 72 h mostró correlación fuerte: +0.62 (p = 0.001); la induración con E. coli a las 4 versus 96 h tuvo correlación moderada: +0.41 (p = 0.01), y la induración de tétanos-difteria a las 4 h versus 72 horas reportó correlación fuerte: +0.64 (p = 0.001). Además, la correlación entre la induración de los diferentes antígenos mostró una correlación débil: +0.39 (p = 0.02) de candidina con la induración de bacterias Gram (+), ambas a las 72 horas. Figura 1
En cuanto a la correlación entre induración de los diferentes antígenos con el puntaje de nutrición (MNA), se observó que la induración de Escherichia coli a las 72 h mostró una correlación moderadamente negativa de -0.5 (p = 0.002), mientras que la induración de candidina a las 72 h tuvo un área bajo la curva ROC de 0.75 (IC95%: 0.57 - 0.94; p = 0.05) y punto de corte de 7 mm para predecir el riesgo de malnutrición. Figura 2 y Figura 3
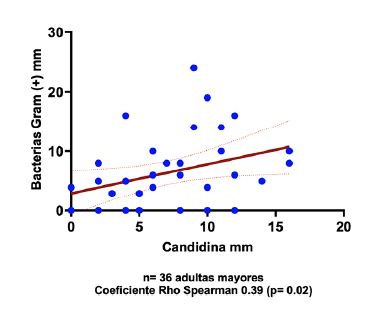
Figura 1 Correlación entre induración a las 72 h de candidina y bacterias Gram (+) en mujeres adultas mayores
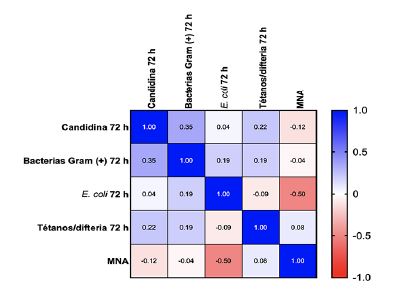
Figura 2 Coeficiente de correlación de Spearman (p) entre los antígenos microbianos y el estado nutricional en mujeres adultas mayores.
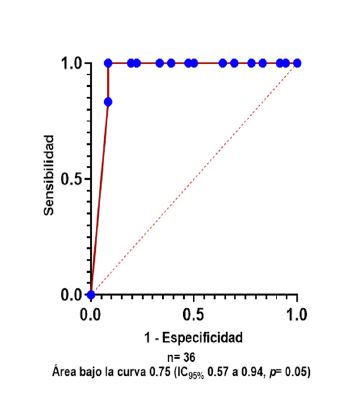
Figura 3 Curva ROC de la induración de candidina a las 72 h para predecir el riesgo de malnutrición en mujeres adultas mayores.
Cuadro 1 Comorbilidades, estado nutricional, funcionalidad y respuesta de hipersensibilidad retardada de mujeres adultas mayores
| Variables | n = 36 |
|---|---|
| Frecuencia (%) | |
| Edad en años x̅ ± DE | 69.2 ± 5.9 |
| IMC kg/m2 x̅ ± DE | 27.1 ± 5.3 |
| Sobrepeso y obesidad | 24 (66.7) |
| Diabetes Mellitus Tipo 2 | 10 (27.8) |
| Hipertensión | 16 (44.4) |
| Enfermedad tiroidea | 10 (27.8) |
| Cardiopatía | 2 (5.6) |
| Estado nutricional | |
| Normal | 30 (83.3) |
| Riesgo de malnutrición | 6 (16.7) |
| Funcionalidad | |
| Independencia total | 36 (100) |
| Análisis clínicos | |
| Hemoglobina g/dL x̅ ± DE | 13.5 ± 1.8 |
| Leucocitos 103/μL x̅ ± DE | 7.2 ± 0.5 |
| Linfocitos 103/μL x̅ ± DE | 1.9 ± 1.0 |
| Neutrófilos 103/μL x̅ ± DE | 4.3 ± 1.7 |
| Monocitos 103/μL x̅ ± DE | 0.5 ± 0.2 |
| Eosinófilos 103/μL x̅ ± DE | 0.1 ± 0.7 |
| Plaquetas 103/μL x̅ ± DE | 258 ± 68.2 |
| Glucosa mg/dL x̅ ± DE | 122.6 ± 55.9 |
| Colesterol total mg/dL x̅ ± DE | 197.0 ± 30.3 |
| Triglicéridos mg/dL x̅ ± DE | 141.5 ± 35.4 |
| Bacteriuria asintomática | 5 (19.5) |
| Respuesta de hipersensibilidad a las 48 h (induración mayor a 5 mm) | |
| Bacterias Gram + | 21 (58.3) |
| Tétanos/difteria | 14 (38.9) |
| Candidina | 24 (66.7) |
| Escherichia coli | - |
Cuadro 2 Resultados de las pruebas diagnósticas para rinitis alérgica
| Antígeno | 4 h n = 36 x̄ ± DE | 24 h n = 36 x̄ ± DE | 48 h n = 36 x̄ ± DE | 72 h n = 36 x̄ ± DE | 96 h n = 36 x̄ ± DE |
|---|---|---|---|---|---|
| Candidina (mm) | 4.2 ± 3.2 | 7.4 ± 3.6 | 7.3 ± 4.0 | 7.1 ± 4.4 | 4.9 ± 4.4 |
| Bacterias Gram (+)*(mm) | 6.6 ± 4.9 | 11.8 ± 7.9 | 9.1 ± 7.0 | 6.4 ± 6.0 | 3.2 ± 4.9 |
| Escherichia coli (mm) | 0.5 ± 1.1 | 0.4 ± 1.1 | 0.3 ± 0.9 | 0.1 ± 0.7 | 0.1 ± 0.7 |
| Tétanos y difteria (mm) | 4.3 ± 4.0 | 6.3 ± 4.9 | 5.4 ± 4.5 | 4.4 ± 4.1 | 2.6 ± 3.7 |
**Bacterias Gram (+): Staphylococcus aureus, Streptococcus pneumoniae, Klebsiella pneumoniae, Branhamella catarrhallis, Haemophilus influenzae
Cuadro 3 Pruebas cutáneas positivas por grupo de alérgenos
| Antígeno evaluado | Nutrición normal n = 30 (%) | Riesgo de malnutrición n = 6 (%) | OR (IC95%) | *p |
|---|---|---|---|---|
| Bacterias Gram + | ||||
| Sin respuesta | 13 (43.3) | 2 (33.3) | 0.6 (0.1 a 4.1) | 0.5 |
| Con respuesta | 17 (56.6) | 4 (66.6) | ||
| Candidina | ||||
| Sin respuesta | 12 (40.0) | - | 1.3 (1.1 a 1.7) | 0.05 |
| Con respuesta | 18 (60.0) | 6 (100) | ||
| Tétanos-difteria | ||||
| Sin respuesta | 20 (66.6) | 2 (33.3) | 0.3 (0.04 a 1.6) | 0.1 |
| Con respuesta | 10 (33.1) | 4 (66.6) | ||
| Escherichia coli | ||||
| Sin respuesta | 30 (100) | 6 (100) | 1 | 1 |
| Con respuesta | - | - |
**Bacterias Gram (+): Staphylococcus aureus, Streptococcus pneumoniae, Klebsiella pneumoniae, Branhamella catarrhallis, Haemophilus influenzae
DISCUSIÓN
La prueba de hipersensibilidad retardada permite evaluar la memoria inmunológica y la respuesta celular frente a diferentes antígenos. La edad avanzada, el estado nutricional y la senescencia de las células inmunológicas y cutáneas pueden deteriorar este tipo de respuesta. En nuestro estudio aplicamos diversos antígenos microbianos (bacterias, toxoides y hongos) a un grupo de mujeres adultas mayores, y relacionamos la respuesta obtenida con su estado nutricional. El mayor porcentaje de respuesta se observó con la candidina; la mitad de las pacientes respondió a bacterias Gram positivas, una tercera parte mostró respuesta a tétanos y difteria, y ninguna respondió a Escherichia coli. Estos resultados son similares a los reportados por Cainzos y colaboradores, quienes encontraron que la candidina es uno de los antígenos con mayor respuesta, con prevalencia del 58%, incluso detectaron anergia en mujeres mayores de 70 años.12
En nuestro estudio la intensidad de respuesta a la candidina se asoció con mayor probabilidad de malnutrición. Es posible que esta relación se deba a una mayor senescencia y a un estado de inflammaging en la piel. En este sentido, Vukmanovic y su grupo, al aplicar el antígeno de varicela zoster, identificaron en cortes histológicos de piel de adultos mayores escasa induración, disminución en la cantidad de células CD11c+ (dendríticas), CD4+ y CD8+, y menor expresión de E-selectina. Además, demostraron que la inflamación excesiva en la piel retrasa la respuesta inmune específica al antígeno, lo que puede relacionarse con aumento en las concentraciones de proteína C reactiva, IL-6 y TNF-α en el sistema vascular.13
Las diferentes dimensiones de la respuesta inmune (constitutiva, innata y adquirida) pueden evaluarse in vivo a través de la piel. Los queratinocitos, que expresan el complejo principal de histocompatibilidad clase II, y las células de Langerhans, ubicadas en el estrato basal de la epidermis, interactúan con los linfocitos TCD4+ y TCD8+. Esta interacción forma un vínculo crucial para la regulación de la respuesta inmune adquirida.14-16
A medida que avanza la edad, la capacidad defensiva de la piel puede afectarse debido a la disminución de la vasculatura, sensibilidad y producción de ácidos grasos, así como al aumento del pH y la alteración de diversas moléculas que mantienen la funcionalidad de los queratinocitos. Dentro de estos cambios se observa disminución del receptor sensible al calcio (CaSR) en los queratinocitos, reducción de la E-cadherina y de las moléculas de adhesión, y del coactivador PGC-1α (coactivador 1 del receptor activador gamma proliferador de peroxisomas). Incluso se incrementa la actividad del factor de transcripción NF-κB y disminuye la expresión de la acuaporina 3 (AQP3).17-20
La respuesta celular inicial depende del reconocimiento de patrones moleculares asociados con microorganismos y, al parecer, los receptores de reconocimiento de patrones TLR2 y TLR4 experimentan disfunción con el envejecimiento.21 Sin embargo, la capacidad de las células dendríticas para fagocitar y reconocer antígenos a través de TLR2 y TLR4, específicamente frente a Candida albicans, se mantiene intacta a pesar de la edad.22 Este hecho podría explicar la alta prevalencia de respuestas positivas a la candidina observada en nuestros pacientes. En contraste con el estudio de Pence y colaboradores, los adultos mayores con respuesta a candidina se relacionaron con menor cantidad de proteína C reactiva en suero, lo que sugiere la relación con disfunción en la respuesta inmune en el adulto mayor.23
Es importante exponer que, en el análisis de la respuesta a los antígenos de tétanos y difteria, casi la mayoría de los pacientes no mostraron respuesta adecuada. Es probable que muchos de estos individuos no hayan recibido las inmunizaciones correspondientes, o quienes sí fueron inmunizados carezcan de memoria inmunológica suficiente para generar una respuesta efectiva.
La intensidad de la respuesta en las pruebas de hipersensibilidad depende de varios factores: edad avanzada, estado de salud de la persona y variabilidad geográfica.24 La edad avanzada suele asociarse con menor respuesta inmunológica. Coincidimos con Cainzos y su grupo en que es necesario estandarizar los valores de estas pruebas, considerando los diferentes grupos de edad, estado de salud, estilo de vida y hábitats.12
Una de las principales limitaciones de nuestro estudio es que se enfocó exclusivamente en mujeres. Sin embargo, la evidencia sugiere que en la posmenopausia, la respuesta inmune es similar a la observada en hombres de la misma edad.25 Otra limitación es la falta de correlación entre la respuesta celular in vivo e in vitro, como los estudios de proliferación linfocitaria. Incluir estos datos puede fortalecer nuestros resultados. Es crucial emprender estudios complementarios que integren biomarcadores inflamatorios (proteína C reactiva, IL-6 o TNF-α), y continuar con líneas de investigación que permitan determinar el estado de inflammaging. Hasta la fecha, este es el primer estudio que reporta la relación entre la respuesta inmune celular a la candidina y el riesgo de malnutrición en mujeres adultas mayores.
Este estudio aporta evidencia significativa de la relación entre la respuesta inmune celular a la candidina y el riesgo de malnutrición en mujeres adultas mayores, un área poco explorada en la bibliografía actual. Los hallazgos refuerzan la importancia de considerar el estado nutricional y los factores inmunológicos en el tratamiento integral de la salud en esta población.
Los estudios futuros deben incluir a hombres y mujeres para evaluar si la diferencia de género influye en la respuesta inmunológica, incluso incluir a pacientes adultos o pediátricos como grupo control para comparar dicha respuesta inmune conforme avanza la edad, al igual que la determinación de biomarcadores inflamatorios que refuercen la comprensión del estado de inflammaging.











 nueva página del texto (beta)
nueva página del texto (beta)



