Introducción
El cáncer gastrointestinal representa hasta el 35% de las muertes relacionadas con cáncer1-4. Tiene un alta morbimortalidad, derivada de una detección tardía, más acentuada en Latinoamérica5-9, a pesar de los esfuerzos para una detección temprana10-12.
La resección endoscópica mucosa (REM) y la disección endoscópica submucosa (DES) son pilares en el manejo de lesiones premalignas o malignas gastrointestinales tempranas y de lesiones subepiteliales (LSE)13,14; la REM para lesiones < 1.5 cm15 y la DES para lesiones de mayor tamaño16, y esta última con mejores tasas de resección total comparada con la REM (92-98 vs. 78-81%; p < 0.001)17,18 y con menor morbimortalidad al compararla con tratamientos quirúrgicos convencionales19,20.
La DES es una técnica segura y efectiva21, que representa el método de referencia para el tratamiento de lesiones neoplásicas tempranas (LNT) y de LSE de entre 2 y 4 cm, específicamente los tumores del estroma gastrointestinal (GIST)22,23. La recurrencia es menor que con la REM (1-2 vs. 6-10%; p < 0.05)1,2,12. Su adopción en México y Latinoamérica es menor que en Oriente24,25; entre los factores relacionados están los relacionados con el procedimiento (dificultad, eventos adversos potencialmente graves y tiempo de realización prolongado) y con el médico (experiencia limitada, gran conocimiento del equipo y de los materiales, carencia de centros de entrenamiento y prevalencia e incidencia bajas que limitan la curva de aprendizaje)26-28.
Por lo que derivado de las ventajas de la DES en el tratamiento de LNT y LSE, es necesaria su incorporación para ser utilizada en nuestro país, por lo que nuestro objetivo es describir nuestra experiencia en el uso de la DES para el tratamiento de LNT y LSE en un centro de tercer nivel de atención en México.
Método
Estudio retrospectivo realizado entre enero de 2008 y octubre de 2022. Se incluyeron pacientes mayores de 18 años con sospecha de LNT o LSE en el tubo digestivo. En LNT se excluyeron los pacientes con histología mal o pobremente diferenciada, datos endoscópicos sugestivos de invasión profunda o de lesión avanzada, y en LSE se excluyeron los pacientes con factores de mal pronóstico (necrosis, ulceración, metástasis ganglionares). Se obtuvo el consentimiento informado en todos los casos.
Se documentaron las características demograficas de los pacientes, los procedimientos y los análisis histológicos. Los procedimientos fueron realizados por los autores, ambos médicos endoscopistas que cuentan con experiencia previa en DES (> 200 procedimientos cada uno).
Evaluación previa al procedimiento y equipo
La evaluación endoscópica de todos los casos se realizó con equipos marca Olympus modelos GIF-H-180 y GIF- H180 J (Olympus, Tokio, Japón) o Fujinon modelos EG-450WR5 H, EG-590WR, EG-600 WR y EG-760R (Fujinon, Tokio, Japón), y para la colonoscopía se utilizaron equipos marca Olympus modelos CF-Q180 y CF-H190L (Olympus, Tokio, Japón) o Fujinon modelos EC-450WR5, EC-590WR, EC-600 WR, EC-760R y EC-760R-VL (Fujinon, Tokio, Japón).
LNT
Se caracterizaron las lesiones utilizando cromoendoscopia vital o digital con NBI (Narrow Band Imaging, Olympus, Tokio, Japón) o BLI (Blue Light Imaging, Fujinon, Tokio, Japón), según el equipo. Se utilizaron las clasificaciones de la Sociedad Esofágica Japonesa, la clasificación del grupo internacional de NBI en Barrett (BING), el algoritmo simplificado de endoscopia con magnificación para cáncer gástrico (MESDA-G) y las clasificaciones de Kudo y NICE para la evaluacion del cáncer esofágico escamoso, del esófago de Barrett, del cáncer gástrico temprano y de las lesiones colónicas, respectivamente. Para definir la morfología de todas las lesiones gastrointestinales encontradas se utilizó la clasificación de París29-35 (Fig. 1).

Figura 1 Algoritmo diagnóstico de lesiones epiteliales candidatas a disección endoscópica submucosa.CEE: Cáncer esofágico escamoso; CGT: Cáncer gástrico temprano; DES: disección endoscópica de la submucosa; EB: esófago de Barrett; HGD: displasia de alto grado; EIM: Endoscopia con imágen mejorada; TNE: tumor neuroendocrino; TAC: tomografia axial computarizada; USE: ultrasonido endoscópico; TCL: Tumor de crecimiento lateral+ Endoscopìa con imagen mejorada: uso de cromoendoscopia digital y vital asi como magnificación.aUso de USE se restringe solo en caso de sospecha de invasion submucosa profiunda a pesar de una evaluación endoscópica minuciosa.# IA=Indicaciones abosultas; IE = indicaciones extendidas de tratamiento para CGT: IA = cáncer bien/moderadamente diferenciado, no úlcerado, ≤ 2 cms. IE = Cáncer bien/moderadamente diferenciado > 2 cms, lesiones úlceradas ≤ 3 cms, cáncer no diferenciadas y no ulceradas ≤ 2 cms, cáncer con invasión submucosa < 500 micras, bien diferenciado y ≤ 3 cms.
LSE
Se realizó ultrasonido endoscópico lineal para la caracterización y se realizó confirmación histológica. El algoritmo de tratamiento se muestra en la figura 2.
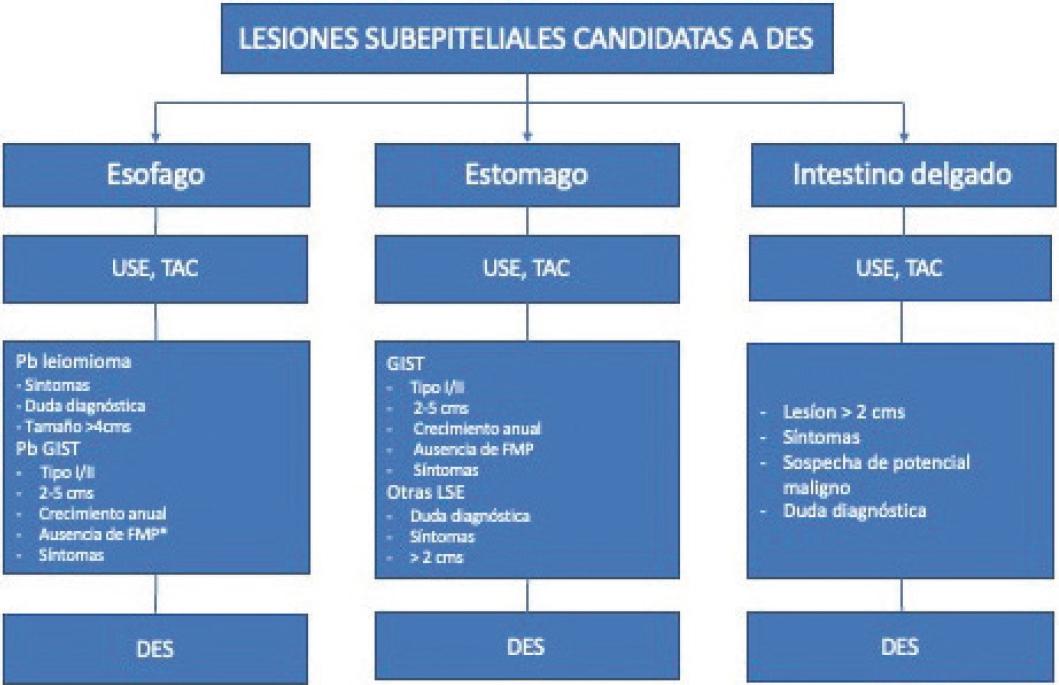
Figura 2 Algoritmo diagnóstico de lesiones subepiteliales candidatas a disección endoscópica submucosa.GIST: Tumor del estroma gastrointestinal; DES: disección endoscópica de la submucosa; FMP: factores de mal pronóstico; LSE: lesiones subepiteliales; TAC: tomografia axial computarizada; USE: ultrasonido endoscópico.*FMP=Factores de mal pronostico en GIST: lesiones úlceradas y/o presencia de bordes irregulares, focos hipocecogénicos (necrosis); focos hiperecogénicos (sangrado), reforzamiento heterogeneo, presencia de METS a distancia o ganglionares por USE/TAC.
DES en LNT
Se utilizó CO2 en todos los casos, con bomba de insuflación ENDOstratus (Medivators, Minneapolis, Minnesota, USA), unidad electroquirúrgica marca ERBE (ERBE, VIO-200D, 300-D o VIO-3, Tübingen, Alemania), cuchillos tipo I, O o T acoplados a la unidad ERBEJET (ERBE, Tübingen, Alemania), BT-knife de 2.0 o 2.5 mm (Fujifilm, Tokio, Japón) y Coagrasper (Olympus, Tokio, Japón) para hemostasia de vasos. La elevación submucosa se realizó con solución salina al 0.9% o hidroxipropil metilcelulosa (Lagricel, Laboratorios Sophia, México), combinados con azul de metileno al 0.5% o índigo carmín al 0.1-0.3%. Se realizaron los cinco pasos de la técnica original:
Marcaje: puntos realizados con coagulación monopolar a 5 mm externos a la lesión (coagulación suave, efecto 4 a 80 W).
Inyección submucosa: elevación con azul de metileno al 0.5% combinado con solución salina.
Incisión circular: disección con modo endocut I (intervalo 3, duración 3 y efecto 3) a 5 mm externos del marcaje.
Disección submucosa, resección total de la lesión en el plano submucoso; en caso de hemostasia, se realizó coagulación suave a 80 W, efecto 4.
Extracción del espécimen, fijación y revisión del área tratada en búsqueda de datos de lesión muscular, y en caso de ameritar manejo endoscópico se utilizaron hemoclips (Boston Scientific, Natick, Massachusetts, USA) u OTS clip (Over-The-Scope clip, Tübingen, Alemania), a criterio del médico (Fig. 3).
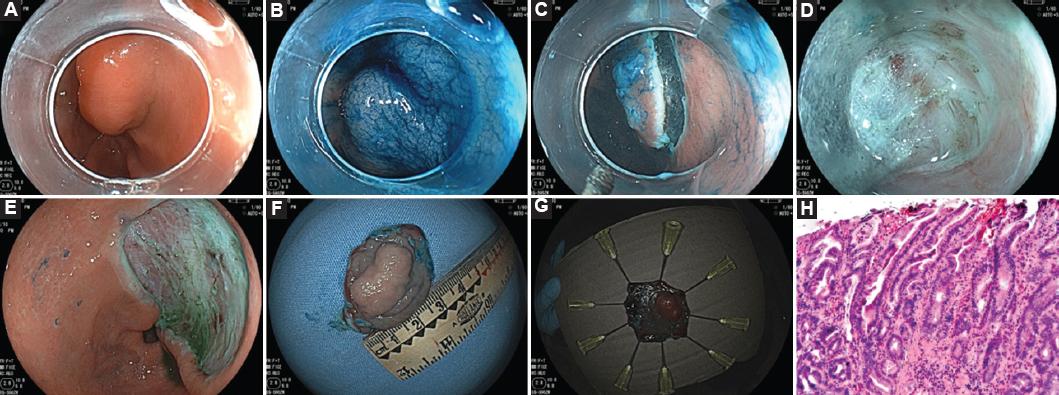
Figura 3 Disección endoscópica submucosa realizada en un adenoma gástrico. A: lesión localizada en la región prepilórica. B: cromoendoscopia con azul de metileno. C: incisión circunferencial. D: disección submucosa. E: lecho quirúrgico posdisección. F y G: espécimen obtenido. H: histología mostrando displasia de bajo grado.
DES en LSE
De acuerdo con el tamaño, la localización y las características de la lesión, se utilizó la misma técnica de DES que en las lesiones epiteliales, o se realizó la modificación con combinación con tunelización o REM (Fig. 4).
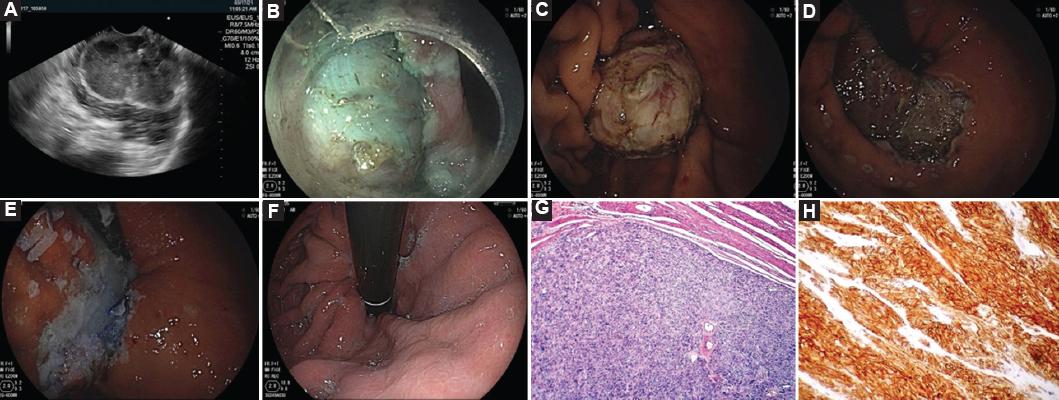
Figura 4 Disección endoscópica combinada con tunelización para la resección de un tumor subespitelial. A: lesión subepitelial dependiente de la cuarta ecocapa con degeneración quística y calcificaciones de 65 × 43 mm de diámetro. B: lesión submucosa expuesta. C: lesión disecada. D: lecho de resección. E: cierre de lecho quirúrgico con clips OVESCO y cianoacrilato. F: revisión 5 meses después de la disección endoscópica submucosa. G: histología con tinción de hematoxilina y eosina. H: inmunohistoquímica con CD-117 positivo.
Análisis histológico
Se realizó el análisis histológico de las piezas en lesiones epiteliales (LE) confirmando la presencia de puntos de marcaje, y en LSE la integridad de la cápsula. Se realizó una fijación con formalina y cortes cada 2 mm. Se clasificó como R0 (resección total con márgenes laterales y profundos negativos), R1 (positividad de alguno de los márgenes), R2 (presencia macroscópica de tumor residual) y RX (no es posible la valoración de resección total).
Eventos adversos
Tanto en LE como en LSE se documentaron los eventos adversos antes, durante y después del procedimiento, así como el tipo de manejo (endoscópico, conservador o quirúrgico). En los casos de neumoperitoneo clínicamente significativo (alteración en la mecánica ventilatoria o circulatoria) se realizó una descrompresión abdominal o torácica, según procediera, con aguja de Veress. En caso de perforación o daño muscular, se dio el manejo apropiado a criterio del endoscopista.
Objetivos
El objetivo del presente trabajo fue documentar la seguridad, la eficacia, el tiempo operatorio, los eventos adversos, el éxito clínico y la recurrencia del tumor en pacientes sometidos a DES para el tratamiento tanto de LNT como de LSE en el tubo digestivo.
Análisis estadístico
El cálculo del tamaño de muestra se realizó con base en la eficacia de la DES en el tratamiento de LNT y LSE, que de acuerdo con estudios previos12,16,23,25 es mayor del 90%. Con un error alfa del 5% y asumiendo un intervalo de confianza del 95%, se requirió un mínimo de 138 pacientes, utilizando un programa estadístico validado (EpiInfo,USA). Se documentaron las características generales de los pacientes y los procedimientos. La expresión fue con media y desviación estándar, o con mediana y rangos intercuartilares, de acuerdo con su distribución, para las variables cuantitativas, y con frecuencias y porcentajes para las cualitativas. La comparación bivariada se realizó con Kruskal-Wallis, y asociación lineal por lineal. Una p < 0.05 se consideró como estadísticamente significativa. Se utilizó el programa SPSS 27 (IBM, Chicago, Il, USA).
Resultados
Características generales de los pacientes y los procedimientos
En el periodo comprendido entre enero de 2008 y octubre de 2022 se realizaron 246 procedimientos (137 LNT y 109 LSE). No hubo diferencias en cuanto a sexo ni edad entre ambos grupos. La diabetes no dependiente de insulina fue la comorbilidad más común (LNT 54.7% y LSE 58.7%). Se demostró diferencia en la histología previa a la DES entre ambos grupos por razones inherentes al tipo de patología epitelial o subepitelial (p = 0.01). El estómago fue el lugar más frecuente para la realización de DES, con 128 lesiones (52%). La mediana de tamaño para LNT y LSE fue de 22.1 y 25.7 mm, respectivamente (p = 0.22). La técnica clásica fue la más comúnmente realizada en ambos grupos y la resección en bloque fue similar entre LNT y LSE (97.1 vs. 96.3%; p = 0.53). La estancia intrahospitalaria fue similar en ambos grupos, con una mediana de 2 días (Tabla 1).
Tabla 1 Características generales de los pacientes y de los procedimientos de acuerdo con el tipo de lesión
| Características | LNT (n = 137) | LSE (n = 109) | p |
|---|---|---|---|
| Sexo masculino, n (%) | 74 (54) | 61 (55.9) | 0.21a |
| Edad (años), mediana, RIQ | 55 (16-93) | 52 (22-78) | 0.35b |
| Comorbilidad, n (%) | |||
| Diabetes | 75 (54.7) | 64 (58.7) | 0.88c |
| Hipertensión arterial | 64 (46.7) | 55 (50.4) | |
| Insuficiencia renal crónica | 42 (30.6) | 21 (19.2) | |
| Cardiopatía isquémica | 31 (22.6) | 32 (29.3) | |
| Enfermedad autoinmunitaria | 18 (13.3) | 12 (11) | |
| Otras | 4 (2.9) | 5 (4.6) | |
| Anticoagulación, n (%) | 26 (18.9) | 18 (16.5) | 0.35a |
| Uso de ASA, n (%) | 46 (33.5) | 35 (32.1) | 0.12a |
| Alcohol, n (%) | 28 (20.4) | 22 (20.1) | 0.45a |
| Tabaquismo, n (%) | 65 (47.4) | 33 (30.2) | 0.51a |
| Histología pre-DES, n (%) | |||
| MI con DBG | 8 (3.3) | - | 0.01c |
| MI con DAG | 25 (10.2) | - | |
| ACG | 16 (6.5) | - | |
| AC | 12 (4.9) | - | |
| LST-G | 29 (11.8) | - | |
| LST-NG | 12 (4.9) | - | |
| Barrett con DBG | 8 (3.3) | - | |
| Barrett con DAG | 8 (3.3) | - | |
| CE | 6 (2.4) | - | |
| TNE | 13 (5.3) | - | |
| Pb leiomioma | - | 16 (14.6) | |
| Pb (GIST) | - | 93 (85.4) | |
| Localización, n (%) | |||
| Esófago | 28 (20.4) | 20 (18.4) | 0.02c |
| Estómago | 73 (53.4) | 55 (50.4) | |
| Duodeno | 8 (5.8) | 5 (4.6) | |
| Colon | 28 (20.4) | 29 (26.6) | |
| Tamaño (mm), mediana (RIQ) | 22.1 (6.5-81.2) | 25.7 (14.5-65.5) | 0.22b |
| Técnica, n (%) | |||
| DES clásica | 82 (59.8) | 55 (50.4) | 0.37c |
| DES + tunelización | 44 (32.1) | 41 (37.6) | |
| DES + REM | 11 (8.1) | 13 (12) | |
| Tiempo operatorio (min), mediana (RIQ) | 71.5 (27.8-348.1) | 78.5 (35.5-188.9) | 0.91b |
| Resección en bloque, n (%) | 133 (97.1) | 105 (96.3) | 0.53a |
| Estancia intrahospitalaria (días), mediana (RIQ) | 2 (1-4) | 2 (1-6) | 0.15b |
AC: adenoma de colon; ACG: adenocarcinoma gástrico; ASA: aspirina; CE: carcinoma esofágico; DAG: displasia de alto grado; DBG: displasia de bajo grado; DES: disección endoscópica submucosa; GIST: tumor del estroma gastrointestinal; LNT: lesión neoplásica temprana; LSE: lesión subepitelial; LST-G: tumor de crecimiento lateral variedad granular; LST-NG: tumor de crecimiento lateral variedad no granular; MI: metaplasia intestinal; Pb: probable; REM: resección endoscópica mucosa; RIQ: rango intercuartilar; TNE: tumor neuroendocrino.
aU de Mann-Whitney.
bPrueba de χ2.
cAsociación lineal por lineal.
Eventos adversos
El neumoperitoneo se presentó en 74 pacientes (33 LNT y 41 LSE), de los cuales 12 (16.2%), requirieron punción descompresiva con aguja de Veress. La hemorragia transprocedimiento se presentó en 45 casos (18.3%), siendo más frecuente en LSE (23.8 vs. 13.8%; p = 0.04); el manejo endoscópico logró el control en todos los casos. En 17 pacientes (6.9%) se presentó hemorragia después de las 24 horas (10 LNT y 7 LSE; p = 0.55), realizando revisión endoscópica en todos y requiriendo manejo endoscópico 7 pacientes (3 hemoclips, 2 coagulación monopolar y 2 tratamiento combinado), obteniendo el control total en todos. La perforación se presentó en 17 pacientes (6.9%) (8 LNT y 9 LSE; p = 0.34) y fue tratada endoscópicamente en 14 (6 hemoclips, 3 OTS clip, 2 cianoacrilato y 3 tratamiento combinado) y quirúrgicamente en 3. Cinco pacientes requirieron exploración quirúrgica 24 horas posteriores a la DES, por datos sugestivos de perforación (1 en el duodeno, 2 en el colon y 2 gástricos), y se confirmó en un caso. No hubo ningún caso de mortalidad trans- ni posprocedimiento (Tabla 2).
Tabla 2 Eventos adversos de la disección endoscópica submucosa de acuerdo con el tipo de lesión
| Evento adverso | LNT (n = 137) | LSE (n = 109) | p |
|---|---|---|---|
| Síndrome pospolipectomía, n (%) | 2 (1.4) | 2 (1.8) | 0.21a |
| Neumoperitoneo, n (%) | 33 (24.1) | 41 (37.6) | 0.26a |
| Ninguno, n (%) | 25 (18.2) | 31 (28.4) | 0.09a |
| Neumomediastino, n % | 15 (10.9) | 13 (11.9) | 0.11a |
| Hemorragia durante el procedimiento, n (%) | 19 (13.8) | 26 (23.8) | 0.04a |
| Perforación, n (%) | 8 (5.8) | 9 (8.3) | 0.34a |
| Hemorragia > 24 h, n (%) | 10 (7.3) | 7 (6.4) | 0.55a |
| Dolor abdominal, n (%) | 8 (5.8) | 15 (13.7) | 0.19a |
| Mortalidad, n (%) | 0 (0) | 0 (0) | 0.08a |
| Necesidad de cirugía, n (%) | 3 (2.1) | 2 (1.8) | 0.71a |
aPrueba de χ2.
Histología
Se encontraron lesiones benignas/premalignas en el 74.4% y malignas en el 25.6%. El GIST con bajo riesgo de progresión fue la lesión más frecuente, con 60/183 (24.5%) pacientes, y el adenocarcinoma gástrico bien diferenciado en las lesiones malignas con 22 pacientes (8.8%). Las LNT se presentaron en 137/246 casos (55.7%), la mayoría a nivel de SM1, en 120/137 (87.6%) pacientes. La resección en bloque fue de 239/246 (97.2%), con resección completa (R0) en 233/246 (94.7%; 130 LNT [94.8%] y 103 LSE [94.5%]), R1 en 12/246 (4.9%; 7 LNT y 5 LSE) y R2 en 1/246 (0.4%; 1 LNT). Finalmente, la resección curativa se alcanzó en 211/246 (85.8%; 117 LNT [85.4%] y 96 LSE [86.2%]). La correlación entre la histología pre- y pos-DES se encontró en el 91% de los casos (126 LNT [91.6%] y 99 LSE [90.8%]) (Tabla 3).
Tabla 3 Hallazgos histológicos finales
| Características | (n = 246) |
|---|---|
| Lesiones benignas o premalignas, n (%) | 183 (74.4) |
| Barrett con DBG | 5 (2) |
| Barrett con DAG | 13 (5.3) |
| MI con DBG | 10 (4) |
| MI con DAG | 14 (5.7) |
| Adenoma tubulovelloso con DBG | 15 (6.1) |
| Adenoma tubulovelloso con DAG | 24 (9.7) |
| Adenoma velloso con DBG | 4 (1.6) |
| Adenoma velloso con DAG | 4 (1.6) |
| GIST muy bajo, bajo o intermedio | 60 (24.5) |
| Leiomioma | 30 (12.3) |
| Tumor de células granulares | 2 (0.8) |
| Lipoma | 2 (0.8) |
| Lesiones malignas, n (%) | 63 (25.6) |
| CE bien diferenciado | 2 (0.8) |
| CE mal diferenciado | 2 0.8) |
| ACG bien diferenciado | 22 (8.8) |
| ACG mal diferenciado | 3 (1.2) |
| AC bien diferenciado | 4 (1.6) |
| AC mal diferenciado | 2 (0.8) |
| GIST con datos de alto riesgo | 16 (6.5) |
| TNE | 12 (4.9) |
| Profundidad de invasión LNT, n (%) | 137 (100) |
| Mucosa y SM1 | 120 (87.6) |
| > SM2 | 17 (12.4) |
| Resección completa (R0), n (%) | 233 (94.7) |
| LNT | LNT 130/137 (94.8) |
| LSE | LSE 103/109 (94.5) |
| Resección curativa final, n (%) | 211 (85.8) |
| LNT | LNT 117/137 (85.4) |
| LSE | LSE 96/109 (86.2) |
| Correlación histológica pre- vs. post-DES, n (%) | 224/246 (91) |
| LNT | LNT 126/137 (91.6) |
| LSE | LSE 99/109 (90.8) |
AC: adenoma de colon; ACG: adenocarcinoma gástrico; CE: carcinoma esofágico; DAG: displasia de alto grado; DBG: displasia de bajo grado; DES: disección endoscópica submucosa; GIST: tumor del estroma gastrointestinal; LNT: lesión neoplásica temprana; LSE: lesión subepitelial; MI: metaplasia intestinal; SM1: submucosa superficial; SM2: submucosa profunda.
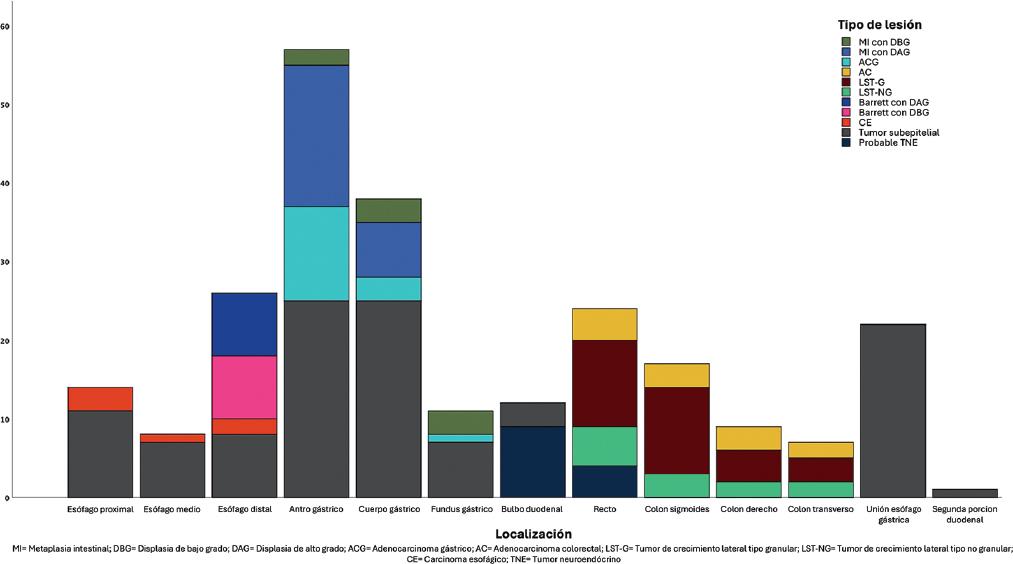
Distribución de las lesiones
La región con mayor frecuencia de procedimientos fue el estómago (128/246; 52%). En el esófago, el leiomioma fue la lesión más común, con 21 casos (43.8%); en el estómago, el GIST con bajo grado de malignidad, con 52 casos (40.6%); en el colon, la lesión de crecimiento lateral variedad no granular con displasia de alto grado, con 24 casos (42.1%), y en el duodeno, el tumor neuroendocrino, con 8 casos (61.5%) (Fig. 5).
Recurrencia al seguimiento
De los 239/246 pacientes en quienes se realizó la resección en bloque (97.2%), fue R0 en 233/246 (94.7%). La mayoría de las recurrencias se presentaron en los primeros 5 años en 12 pacientes (7.29%), y hasta octubre de 2022 (177 meses pos-DES) un total de 22 (9.44%), de las cuales 12 fueron LNT y 10 fueron LSE. El tratamiento ofrecido fue endoscópico en 8 (exitoso en 6) y las otras 14 recurrencias requirieron cirugía y terapia neoadyuvante en todos los casos. La resección curativa fue de 211/246 (85.8%; LNT 85.4% y LSE 86.2; p = 0.45), no hubo lesiones avanzadas en el seguimiento y la mortalidad fue del 8.1% a 177 meses, pero sin relación con la recurrencia tumoral (Tabla 4 y Fig. 6).
Tabla 4 Recurrencia durante el seguimiento
| Características | Recurrencia acumulada (n = 233) |
|---|---|
| 3 meses, n (%) | 1 (0.42) LNT 1/LSE 0 |
| 6 meses, n (%) | 2 (0.85) LNT 1/LSE 1 |
| 12 meses, n (%) | 3 (1.28) LNT 2/LSE 1 |
| 24 meses, n (%) | 6 (2.57) LNT 3/LSE 3 |
| 36 meses, n (%) | 9 (3.86) LNT 5/LSE 4 |
| 48 meses, n (%) | 12 (5.15) LNT 7/LSE 5 |
| 60 meses, n (%) | 17 (7.29) LNT 11/LSE 6 |
| 177 meses (último corte), n (%) | 22 (9.44) LNT 12/LSE 10 |
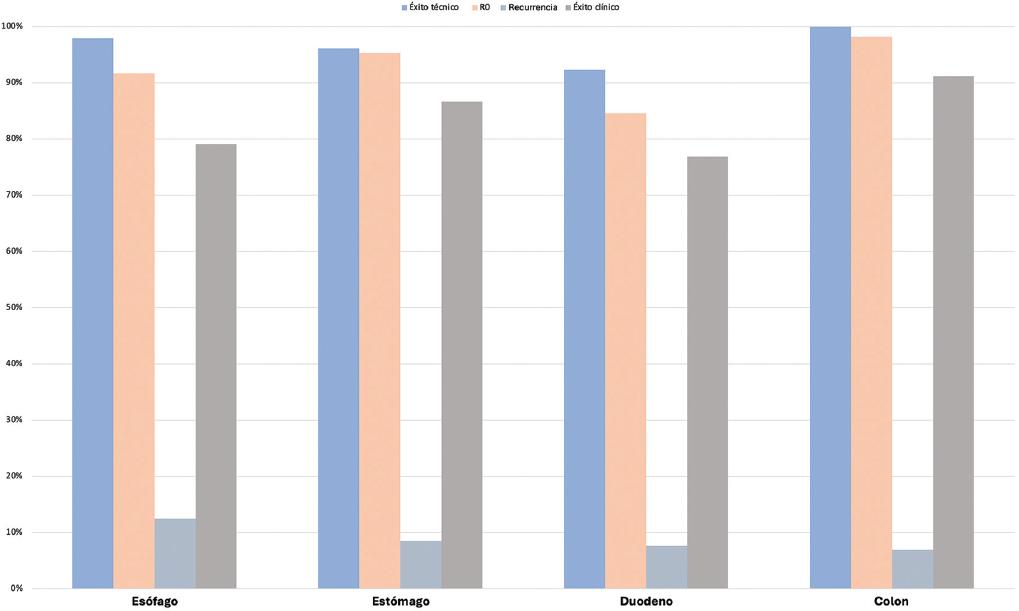
Disección endoscópica submucosa con relación al órgano
El mayor tamaño de lesiones resecadas fue en el colon, comparadas con el duodeno (26.5 vs. 10.3 mm; p < 0.001), obteniendo también los mayores tiempos de resección (95.4 vs. 55.6 min; p < 0.001). No hubo diferencias en los días de estancia intrahospitalaria, la tasa de resección en bloque, R0 ni el tipo de lesión (LNT vs. LSE). La hemorragia fue más frecuente en el estómago, con 11 pacientes (8.6%), y la perforación lo fue en el colon, con 5 pacientes (8.8%) (Tabla 5).
Tabla 5 Características de la disección endoscópica submucosa según las regiones del tubo digestivo
| Características | Esófago (n = 48) | Estomago (n = 128) | Duodeno (n = 13) | Colon (n = 57) | p |
|---|---|---|---|---|---|
| Tamaño (mm), mediana, RIQ | 17.5 (8.1-40) | 24.1 (10.1-65.1) | 10.3 (6.5-15) | 26.5 (8.4-81.2) | < 0.001a |
| Tiempo (min), mediana, RIQ | 62 (34.5-96) | 78.1 (33.1-278) | 55.6 (27.8-88) | 95.4 (28.1-348) | < 0.001a |
| Estancia hospitalaria (días), mediana, RIQ | 1 (1-5) | 3 (2-7) | 3 (2-6) | 2 (1-8) | 0.22a |
| Resección en bloque, n (%) | 47 (97.9) | 123 (96.1) | 12 (92.3) | 57 (100) | 0.25b |
| Eventos adversos graves, n (%) | |||||
| Hemorragia grave | 3 (6.3) | 11 (8.6) | 1 (7.7) | 2 (3.5) | 0.04b |
| Perforación | 1 (2.1) | 10 (7.8) | 1 (7.7) | 5 (8.8) | |
| R0, n (%) | 44 (91.7) | 122 (95.3) | 11 (84.6) | 56 (98.2) | 0.94b |
aKruskal-Wallis.
bAsociación lineal por lineal.
Discusión
El objetivo del presente trabajo fue evaluar la experiencia de la DES para el tratamiento de LNT y LSE. Confirmamos que es una técnica segura, efectiva y reproducible en nuestro medio. Se ha consolidado como una técnica segura y efectiva12,13,36-39, aunque su incursión en Latinoamérica y México ha sido lenta14,16,40. A pesar de esto, países como Brasil, Chile, Perú y Colombia han publicado buenos resultados de la DES para el tratamiento de las LNT y LSE, similares a los documentados en Oriente9,24,27,40-45. En nuestro país, el grupo de Carames et al.46 reportó el uso de la DES en 32 pacientes con metaplasia intestinal, obteniendo buenos resultados.
En el presente estudio incluimos 246 lesiones (137 LNT y 109 LSE), siendo el sexo masculino más predominante (54% y 55.9%, respectivamente) en ambos grupos, de modo similar a lo reportado por diversos autores latinoamericanos (52-66%), como Emura et al.43 y otros27,41,44. La edad y demás factores demográficos también son similares a los reportados por otros autores, como Medina et al.47, que utilizaron esta técnica para el tratamiento de LNT y LSE.
Las lesiones de mayor tamaño requirieron mayor tiempo de DES y fueron más frecuentes en el colon (26.5 mm y 94.5 min), lo cual es similar a lo reportado por otros autores, como Arantes et al.9 y Palacios et al.27, y también a lo encontrado en centros orientales por Su et al.48 y Jiao et al.49. Estos hallazgos son claros para LNT, donde las lesiones son epiteliales y los retrasos en la disección se relacionan con la presencia de hemorragia transprocedimiento, localización y fibrosis, a diferencia de las LSE, donde los tiempos de resección son también muy variables, pero similares a los de otros trabajos de DES en LNT y LSE41,44,48,49.
La perforación se presentó en 17 casos (LNT 5.8% y LSE 8.3%) y la hemorragia transprocedimiento fue discretamente mayor en LSE (23.8 vs. 13.8% en LNT), probablemente relacionado con la localización y la vascularización mayor de las LSE comparadas con las LNT. Sin embargo, los eventos adversos fueron controlados endoscópicamente, de modo similar a lo reportado en otros centros de Asia y Latinoamérica, donde la resolución endoscópica tuvo una eficacia mayor del 80%1,9,10,13,16,49,50, como en nuestra cohorte (82.5%).
Nuestra casuística es la mayor documentada en Latinoamérica, con una tasa de resección en bloque del 97.2% (LNT 97.1% vs. LSE 96.3%; p = 0.53), similar a los observado por otros autores, como Arantes et al.9 y Palacios et al.27, con R0 para LNT gástricas en el 96.3% y el 99%, respectivamente. Estos datos también son similares a los publicado por Saito et al.50 en Oriente, quienes en un estudio multicéntrico para el tratamiento de lesiones colorrectales observaron un tamaño de 34.2 mm, un tiempo operatorio de 90 min y una resección en bloque del 95.4%, similares a los nuestros (26.5 mm, 95.4 min y 100%).
El principal beneficio de la DES es que permite ofrecer un pronóstico a mediano y largo plazo muy similar a lo observado con los tratamientos quirúrgicos habituales36,42,48. En el cáncer gástrico se ha confirmado una reducción en la mortalidad de hasta el 63%50. Esto se obtiene con una adecuada resección en bloque y R0, que en nuestro caso fue del 94.7% en general, siendo más baja en el duodeno, con un 84.6%, pero congruente con lo recomendado por los expertos orientales, que sugieren que sea mayor del 80% en esta región50 y variable dependiendo de la región y de la histología de las lesiones resecadas. Esto es, en el estómago se han documentado R0 en el 94.7-95.1%, en el colon en el 92-95.3%, y en el esófago en el 91.5-93.9%; resultados similares a los de nuestra cohorte (95.3, 98.2 y 91.7%, respectivamente) y mayores que los reportados por otros autores en Latinoamérica, como Arantes et al.9, que tuvieron una tasa de resección en bloque del 95.5%, R0 del 88.8% y resección curativa del 76.1%.
La recurrencia global en nuestra cohorte fue del 9.44% a 177 meses, de los cuales 12 casos fueron LNT y 10 LSE, y un éxito clínico del 85.8% (LNT 85.4% y LSE 86.2%), lo cual, aunque es distinto a otros centros, se puede explicar por la heterogeneidad de las lesiones resecadas. Sin embargo, en el subanálisis por región, encontramos que la DES para LNT gástricas y colorrectales, en nuestra cohorte, fue del 1.4% y el 2.1%, respectivamente, y la mayor recurrencia fue en lesiones del tipo GIST, lo cual es similar a lo obtenido por otros autores27,37,39,42,44.
Las debilidades de nuestro trabajo derivan del sesgo inherente a su naturaleza retrospectiva, ser unicéntrico, su realización por dos médicos y su limitada aplicabilidad en otros centros; esto último derivado de que, si bien nuestros resultados son comparables a los de grandes centros de Oriente, esto se debe a que, al tratarse de un centro de referencia, el número de casos y la experiencia son mayores en comparación con otros centros mexicanos donde no se cuenta con esta ventaja, por lo cual los resultados podrían ser distintos. Sin embargo, nuestras fortalezas incluyen ser la cohorte más grande reportada en Latinoamérica, la inclusión de LNT y LSE, la evaluación y el seguimiento a largo plazo de los pacientes, y la documentación clara y específica de los procedimientos, los eventos adversos y la histología.
Conclusiones
En los pacientes con LNT o LSE que cumplan con una adecuada indicación clínica, la DES representa el tratamiento de primera línea, con excelentes resultados a corto, mediano y largo plazo, siempre y cuando sea realizada en centros que cuenten con la infraestructura y la experiencia adecuadas.











 nueva página del texto (beta)
nueva página del texto (beta)