Introducción
La carne bovina aporta gran valor nutricional a la dieta por ser fuente de proteínas y grasas de alto valor biológico, además de micronutrientes como ácido fólico, hierro, selenio y vitaminas A, B12; sin embargo, durante las últimas décadas, se ha relacionado a mayor riesgo de enfermedades crónicas, como la diabetes tipo II, enfermedades cardiovasculares y cáncer, debido a su alto contenido de grasa (Wolk 2017). Dentro de los componentes asociados, se encuentran algunos de los ácidos grasos saturados (SFA) (Calder 2015), los cuales, además de su efecto negativo en la salud, también influyen desfavorablemente en la calidad sensorial, que va desde la apariencia visual, la cual influye en la decisión de compra, hasta las propiedades organolépticas durante el consumo (Frank et al. 2016, Motoyama et al. 2016). Por el contrario, algunos ácidos grasos monoinsaturados (MUFA) se han asociado con efectos positivos en la salud al reducir la concentración de lípidos en sangre, y mejorar el sabor de la carne (O’Quinn et al. 2016). Adicionalmente, los ácidos grasos poliinsaturados (PUFA) presentes en la carne, tienen una función importante sobre el metabolismo de lípidos, sensibilidad a la insulina y se han asociado con la reducción de triglicéridos y presión arterial (Vela-Vásquez et al. 2021). Debido a lo anterior, los consumidores prefieren carne con mayores cantidades de MUFA y menores de SFA, por lo que se busca mejorar las proporciones MUFA/SFA y PUFA/SFA en la carne bovina.
La vía de la proteína cinasa activadas por mitógenos (AMPK) actúa como sensor del estado energético celular; se activa por aumentos en la proporción celular AMP/ATP causado por estrés metabólico que interfiere con la producción de ATP. Una vez activada, la vía AMPK conduce a la inhibición de las vías biosintéticas que consumen energía, como la síntesis de proteínas, ácidos grasos (FA) y glucógeno; por otro lado, induce a la activación de las vías catabólicas productoras de ATP, como la oxidación de los FA y la glucólisis (Garcia y Shaw 2017). En este amplio rango de procesos metabólicos, participan múltiples genes polimórficos que regulan el metabolismo de los FA y, por ende, la composición en la carne. Conocer la arquitectura genética de las características relacionadas con estos procesos metabólicos propone una vía de mejoramiento de la calidad de los productos cárnicos y lácteos. La selección asistida por marcadores (MAS) se centra en la incorporación de información molecular para seleccionar las variantes génicas beneficiosas que subyacen a esos rasgos complejos (Hasan et al. 2021). Con la disponibilidad de estudios de genoma completo se ha reportado mayor evidencia en rutas como la del AMPK, en las cuales existen genes candidatos que albergan marcadores moleculares que se han asociado a modificar la composición de FA en carne y leche. Desde su descubrimiento algunos marcadores dentro de DGAT1, FASN y SCD1 han sido estudiados en múltiples razas como Angus, Hanwoo, Holstein y Negro japones donde se han mantenido asociaciones coherentes, además, existen otros marcadores que no reflejan el mismo efecto entre diferentes razas, y otros más que solo se han analizado en una raza. En México diversas razas son utilizadas para la producción de carne, sin embargo, la raza bovina Negro japonés (Wagyu), originaria de Japón, destaca por la capacidad de generar carne con gran porcentaje de grasa intramuscular, la cual es símbolo de calidad organoléptica (Gotoh et al. 2018); y por presentar mayor contenido MUFA/SFA en comparación las razas Angus, Hanwoo, Negro Jeju (Lee et al. 2020, Vázquez-Mosquera et al. 2023). El conjunto de estos atributos ha permitido una gran aceptación de la carne Wagyu en ciertos nichos de consumo en distintas partes del mundo. En México la raza Wagyu se cría a través de cruzas con razas cárnicas, con la intención de mejorar características de la canal y adaptabilidad a las condiciones de producción. Actualmente la carne del ganado Wagyu es comercializada bajo el nombre Wagyu-Cross. Por lo anterior, el objetivo de este estudio fue estimar y comparar las frecuencias alélicas de 27 polimorfismos de un solo nucleótido (SNP) en 22 genes de la ruta AMPK, en poblaciones de ganado Wagyu y sus cruces (Wagyu-Cross).
Materiales y métodos
Muestras
Se colectaron 111 muestras de carne del músculo Longissimus dorsi, entre la 11a y 12a costilla, de animales provenientes de la ganadería Rancho “Exhacienda Cañas” (Canatlán, Durango, México), sacrificados en rastros Tipo Inspección Federal (TIF), considerando todas las normas de manejo y bienestar animal. Con la base de datos proporcionada por el productor, las muestras se agruparon por grupo genético en: Wagyu (WAG, n = 39) y sus cruzas con Angus (WAN, n = 18), Beefmaster (WBM, n = 12), Brangus (WBR, n = 29) y Hereford (WHF, n = 13).
Selección de SNP
Los SNP se escogieron por su ubicación en genes que participan en la ruta AMPK (Figura 1) y/o por su previa asociación al perfil de los FA en carne o leche. Se seleccionó un panel de 24 SNP localizados en 19 genes de la ruta AMPK y tres SNP en genes fuera de la vía AMPK previamente asociados a FA en ganado bovino. En la Tabla 1 se muestran los SNP seleccionados. Se realizó la extracción de ADN de las muestras con el kit comercial Genelute Mammalian Genomic DNA Cat. G1N350 (Sigma-Aldrich®, St. Louis, MO). La tipificación se realizó en la compañía NEOGEN Corp. con la tecnología Sequenom massARRAY® system (Agena Bioscience, San Diego, CA) con una tasa de éxito de 98.06%.
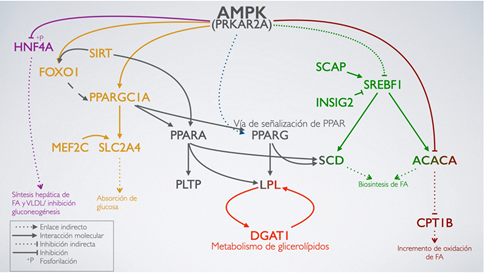
Figura 1 Red de interacción genética dentro de la vía AMPK. NCBI (Sayers et al. 2023), STRING (Szklarczyk et al. 2023), KEGG (Kanehisa et al. 2023), UniProt (The Uniprot Consortium 2023).
Tabla 1 Panel de 27 SNP en 22 genes de la ruta AMPK.
| Ch | Gen | SNP ID | Ubicación SNP1 | A1/A2 | Cambio AA | Referencia | |
|---|---|---|---|---|---|---|---|
| 2 | INSIG2 | ss252452236 | 73137048 | I2 | C/T | Rincón et al. 2011 | |
| ss252452234 | 73136642 | I2 | C/G | ||||
| 5 | CPT1B | ss65363345 | G/C | Sevane et al. 2011 | |||
| PPARA | ss65362714 | C/T | Sevane et al. 2011 | ||||
| 6 | PPARGC1A | c.1892+19 | I9 | T>C | Weikard et al. 2005 | ||
| SCD5 | ss252452202 | 101280113 | E3 | C/T | Sinónimo | Rincón et al. 2011 | |
| 7 | MEF2C | ss38329156 | 90725014 | G/T | Sevane et al. 2011 | ||
| ss65449641 | G/T | Sevane et al. 2013 | |||||
| 8 | LPL | ss65478732 | T/C | Sinónimo | Sevane et al. 2011 | ||
| 9 | IGF2R | ss77831885 | G/A | Williams et al. 2009 | |||
| 12 | FOXO1 | ss65611802 | T/C | Sevane et al. 2013 | |||
| 13 | HNF4A | ss61961144 | 73576499 | UTR | C/T | Sevane et al. 2013 | |
| PLTP | ss77832104 | 75428449 | 3’UTR | G/A | Williams et al. 2009 | ||
| 14 | DGAT1 | K232A | E8 | K>A | Lys/Ala | Grisart et al. 2002 | |
| 19 | ACACA | ss64381883 | G/A | Sevane et al. 2011 | |||
| SLC2A4 | ss62538460 | G/A | Sevane et al. 2011 | ||||
| SREBF1 | ss62543518 | T/C | Sevane et al. 2011 | ||||
| 22 | PPARG | ss62850198 | 57468357 | 5’UTR | A/G | Sevane et al. 2011 | |
| PRKAR2A | ss62837580 | 51717613 | T/C | Sevane et al. 2013 | |||
| ss62837667 | 51710370 | T/C | |||||
| SCAP | ss62839002 | 52816252 | A/G | Sevane et al. 2013 | |||
| 26 | SCD1 | g.10153 G>A | E5 | A<G | Sinónimo | Taniguchi et al. 2004 | |
| g.10213 C>T | E5 | T<C | Sinónimo | ||||
| g.10329 T>C | E5 | C<T | Val/Ala | ||||
| 28 | MYOZ1 | ss77831945 | 29004608 | T/C | Williams et al. 2009 | ||
| SIRT1 | ss61550598 | G/A | Sevane et al. 2013 | ||||
| 29 | SRPRA | 4150 | C/G | Medrano y Rincón 2009 | |||
Ch: Cromosoma; A1/A2: Alelo 1/ Alelo 2; AA Aminoácido; 1: Btau_4.0 genome assembly; En negrita ubicación en el gen, I: Intrón, E: Exón; UTR: Región no traducida.
Análisis estadísticos
Se estimaron las frecuencias alélicas de los SNP estudiados, se analizó el desequilibrio de ligamiento entre loci mediante una prueba de razón de verosimilitud exacta (prueba G), se examinó el equilibrio de Hardy-Weinberg (H-W) de cada locus estudiado por grupo genético usando una prueba exacta de Fisher, y se realizó un análisis de diferenciación génica utilizando pruebas de Fst entre los grupos considerando la hipótesis nula de que las frecuencias entre grupos eran iguales. Todos los análisis se realizaron en el software GENEPOP 4.7 (Rousset 2008).
Resultados
El SNP SCD g.10153 está ligado a SCD g.10213, y ambos muestran ligamiento con SCD g.10329 (P = 0.0001). Asimismo, los SNP ss62837667 y ss62837580, localizados en el gen PRKAR2A, presentaron un ligamiento significativo (P = 0.0083). El análisis del equilibrio de H-W mostró desviaciones significativas en los loci HNF4 ss61961144 (P = 0.0001) y SCD g.10213 (P = 0.0383). Adicionalmente, se determinaron las frecuencias alélicas de 27 SNP analizados en la población de ganado Wagyu y Wagyu-cross (Tabla 2). La genotipificación mostró que los marcadores CPT1B ss65363345, FOXO1 ss65611802, INSIG2 93867, MEF2C ss65449641, PPARA ss65362714, SCAP ss62839002 y SIRT1 ss61550598 fueron monomórficos en todos los grupos analizados, sin embargo, algunos resultaron monomórficos solo en ciertos grupos: ACACA ss64381883 e INSIG2 93461 en WAN, WBM y WBR; LPL ss65478732 en WHF; y SLC2A4 ss62538460 en WBR.
Tabla 2 Frecuencia del alélica en la población Wagyu por grupo genético.
| Gen | ID SNP | A1/A2 | Frecuencia alélica | |||||
|---|---|---|---|---|---|---|---|---|
| WAG | WAN | WBM | WBR | WHF | General | |||
| n = 39 | n = 18 | n = 12 | n = 29 | n = 13 | n = 111 | |||
| ACACA | ss64381883 | G/A | 0.9744 | 1.000 | 1.000 | 1.000 | 0.9615 | 0.9865 |
| CPT1B | ss65363345 | G/C | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 |
| DGAT1 | K232A | K>G | 0.6923a | 0.3889b | 0.375b | 0.5345ab | 0.5385ab | 0.5827 |
| FOXO1 | ss65611802 | T/C | 0.000 | 0.000 | 0.000 | 0.000 | 0.000 | 0.000 |
| HNF4A | ss61961144 | T/C | 0.1410 | 0.3056 | 0.2727 | 0.1379 | 0.2778 | 0.1934 |
| IGF2R | ss77831885 | G/A | 0.8462ab | 0.75b | 0.7083b | 0.9138a | 0.8077ab | 0.8288 |
| INSIG2 | ss252452236 | C/T | 0.000 | 0.000 | 0.000 | 0.000 | 0.000 | 0.000 |
| INSIG2 | ss252452234 | C/G | 0.0132 | 0.000 | 0.000 | 0.000 | 0.0385 | 0.0091 |
| LPL | ss65478732 | T/C | 0.0256 | 0.0278 | 0.0417 | 0.0517 | 0.000 | 0.0315 |
| ME2FC | ss65449641 | G/T | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 |
| MEF2C | ss38329156 | G/T | 0.8718 | 0.7222 | 0.6667 | 0.7069 | 0.8846 | 0.7838 |
| MYOZ1 | ss77831945 | T/C | 0.4615a | 0.2647ab | 0.5000ab | 0.4444a | 0.1818b | 0.3960 |
| PLTP | ss77832104 | G/A | 0.7727 | 0.800 | 0.8750 | 0.8269 | 0.6364 | 0.7849 |
| PPARA | ss65362714 | C/T | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 | 1.000 |
| PPARG | ss62850198 | A/G | 0.2179 | 0.1667 | 0.3333 | 0.2069 | 0.1923 | 0.2162 |
| PPARGC1A | c.1892+19 | T>C | 0.1282 | 0.2778 | 0.2083 | 0.2586 | 0.1154 | 0.1937 |
| PRKAR2A | ss62837580 | T/C | 0.4615b | 0.6667a | 0.5417ab | 0.5345ab | 0.5385ab | 0.5315 |
| PRKAR2A | ss62837667 | T/C | 0.1538b | 0.1667b | 0.4167a | 0.2143ab | 0.0769b | 0.1909 |
| SCAP | ss62839002 | A/G | 0.000 | 0.000 | 0.000 | 0.000 | 0.000 | 0.000 |
| SCD1 702 | g.10153 | A<G | 0.6974 | 0.6389 | 0.5833 | 0.6724 | 0.6250 | 0.6619 |
| SCD1 762 | g.10213 | T<C | 0.7027 | 0.5938 | 0.6500 | 0.6724 | 0.8125 | 0.6800 |
| SCD1 878 | g.10329 | C<T | 0.6447a | 0.4167b | 0.5833ab | 0.6852a | 0.5000ab | 0.5926 |
| SCD5 | 134718 | C/T | 0.2179ab | 0.3889a | 0.25ab | 0.1724b | 0.2083ab | 0.2364 |
| SIRT1 | ss61550598 | G/A | 1.0000 | 1.0000 | 1.0000 | 1.0000 | 1.0000 | 1.0000 |
| SLC2A4 | ss62538460 | G/A | 0.9744 | 0.9167 | 0.9583 | 1.0000 | 0.9615 | 0.9685 |
| SREBF1 | ss62543518 | T/C | 0.1154 | 0.1944 | 0.0833 | 0.1724 | 0.2692 | 0.1577 |
| SRPRA | 4150 | C/G | 0.141ab | 0.2500a | 0.2500ab | 0.0862b | 0.1538ab | 0.1577 |
A: Alelo; WAG: Wagyu, WAN: Wagyu x Angus. WBM: Wagyu x Beefmaster. WBR: Wagyu x Brangus. WHF: Wagyu x Hereford. Alelo en negrita: Previa asociación favorable ab: diferencia génica significativa. Alelo silvestre < alelo variante
Solo ocho SNP presentaron diferencia génica entre grupos. En DGAT1 ss77831745, WAG presentó la frecuencia más alta del alelo K (0.6923) y se encontró diferencia génica con WAN (0.3889) y WBM (0.3750) (P = 0.0088 y 0.0045, respectivamente). En general en IGF2R ss77831885, se observó una alta segregación del alelo G, sin embargo, WBR presentó la frecuencia más alta (0.9138) y se encontró diferencia génica significativa respecto a WAN (0.75) y WBM (0.7083) (P = 0.0399 y 0.0354, respectivamente). Respecto a MYOZ1 ss77831945, WHF tuvo la frecuencia más baja del alelo G (0.181), donde se observó una diferencia génica significativa con WAG y WBR (P= 0.0262 y 0.0370, respectivamente). Las frecuencias en PRKAR2A ss62837580 aparentan ser iguales, sin embargo, se encontró una diferencia génica donde WAN, presentó mayor frecuencia del alelo T (0.666 7) respecto a WAG (P = 0.048 6). En este mismo gen, ss62837667, la frecuencia del alelo T en WBM (0.4167) fue notoriamente más alta al resto y se observó diferencia respecto a WAG, WAN y WHF (P = 0.0223, 0.0428 y 0.0079, respectivamente). En SCD g.10329, la frecuencia alélica más alta se observó en WBR (0.685) y WAG (0.645), donde se encontró una diferencia génica respecto a WAN (0.417) (P = 0.0165 y 0.024, respectivamente). Respecto a SCD5 rs109937152 y SRPRA 4150 se observó una baja segregación de los alelos C, sin embargo, en ambos alelos, se encontró una diferencia génica entre WAN que mantuvo una frecuencia más alta (0.388 9 y 0.25) y WBR que mantuvo las frecuencias más bajas (P = 0.029 5 y 0.040 2, respectivamente).
Discusión
La proteína quinasa activada por AMP (AMPK) se activa cuando hay disminuciones de ATP y por lo tanto aumentos de AMP o ADP. En respuesta, AMPK promueve vías catabólicas para generar más ATP e inhibe las vías anabólicas que la consumen (Garcia y Shaw 2017). En los mamíferos, las subunidades α y β de AMPK tienen dos isoformas cada una, y la subunidad γ de AMPK tiene tres isoformas. Esto sugiere la presencia de 12 combinaciones potenciales de AMPK (Sang-Min 2016). Esta proteína, se ha relacionado a la oxidación de los FA en la mitocondria (Herms et al. 2015). Los SNP ss62837667 y ss62837580 se encuentran presente dentro del gen PRKAR2A el cual sintetiza la subunidad reguladora alfa de la proteína quinasa tipo II dependiente de AMPc que constituye a AMPK. En este estudio se encontró que los SNP están desequilibrio de ligamiento y diferencia génica entre grupos. Debido a su previa asociación y los resultados obtenido en este estudio, ambos SNP son útiles para buscar variaciones en el perfil lipídico entre diferentes razas de ganado bovino. Múltiples áreas de la ciencia investigan desde distintos enfoques a esta proteína, lo que reafirma la importancia que tiene sobre el metabolismo, sin embargo, específicamente, no se tienen reportes de estos SNP asociados a FA en ganado bovino.
AMPK inhibe directamente a HNF4A. Este factor de transcripción regula la expresión de genes implicados en el transporte y metabolismo de la glucosa, la secreción de insulina, y la síntesis de ácidos grasos (FA) y lipoproteínas de muy baja densidad (VLDL) en el hígado (Tucker et al. 2019).
Cercano a este gen se encuentra el SNP HNF4A ss61961144, en la población Wagyu-Cross se observó desviaciones significativas en el equilibrio H-W, donde el alelo C, fue el que predomino. En ganado bovino español (Holstein, Simmental, Marchiniga, Avileña-Negra Iberica), se encontró una frecuencia aún más alta del alelo C y se encontró que este SNP influye en la actividad de la enzima isocitrato deshidrogenasa (ICDH), que está relacionada con el potencial oxidativo de las fibras musculares para catabolizar los FA (Sevane et al. 2013). Recientemente se descubrió que HNF4A regula la expresión de SCD1 (Pan et al. 2021), el cual es un gen clave en metabolismo de MUFA, por lo que el SNP ss61961144podría influir sobre la composición FA en carne bovina. Las previas asociaciones del gen y su función metabólica postulan a este SNP como candidato para el estudio de la arquitectura lipídica en la carne bovina.
La proteína de unión al elemento regulador de esterol (SREBP), se une a la membrana como factor de transcripción y activa genes que codifican las enzimas necesarias para la síntesis de colesterol, FA, triglicéridos y fosfolípidos (Eberlé et al. 2004). AMPK inhibe específicamente a SREBF1, la cual es una subunidad de SREBP. De igual manera, a altas concentraciones de esteroles, INSIG2 se une a SREBP para bloquear su función (Lee et al. 2020) (Figura 1). Por otra parte, SCAP actúa como chaperona de SREBP, la cual, en condiciones de bajas concentraciones de colesterol, induce la translocación desde el retículo endoplásmico al aparato de Golgi, lo que le permite regular los niveles celulares de triglicéridos y colesterol (Lee et al. 2020). En la población Wagyu-Cross, el SNP SREBF1 ss62543518, presentó una baja segregación del alelo T. A pesar de estar dentro de un regulador de la homeostasis de lípidos, ss62543518 no ha sido ampliamente estudiado, y no se ha asociado a FA. En ganado Holstein, se encontró el SNP rs41912290 en SREBF1 altamente vinculado a la composición de grasa en leche (Rincon et al. 2012). En la raza Hanwoo se encontró otro polimorfismo (inserción/deleción) dentro de este gen, el cual se asoció a la composición de ácido esteárico (C18:0), ácido linoleico (C18:2n6) y PUFA (Bhuiyan et al. 2009). Esta inserción/deleción también se ha asociado a múltiples FA en ganado canadiense, español y raza Simmental (Han et al. 2013, Xu et al. 2013, Gamarra et al. 2021). La raza Hanwoo y la Wagyu tienen ascendencia en común (Smith et al. 2009), por lo que los polimorfismos presentes dentro de SREBF1 son buenos candidatos para el estudio de FA en ganado. En el intrón dos de INSIG2 se encuentran los SNP ss252452236 y ss252452234 que se encuentran en desequilibrio de ligamiento. En ss252452236 no se encontró ningún alelo C, mientras que en ss252452234, la frecuencia del alelo C fue inferior a 0.01. En ganado Holstein, ambos alelos C se relacionaron a menor concentración de SFA y mayores de MUFA y PUFA en leche (Rincón et al. 2011). En ganado porcino, se encontró en INSIG2 el SNP c.-5527C>G con efecto sobre el contenido de ácido linoleico (C18:2) y ácido eicosanoico C20:0 FA en carne (Grzes et al. 2016). En la población Wagyu-Cross el SNP SCAP ss62839002 fue monomórfico con la fijación del alelo G. En ganado Holstein, Jersey, Asturiana de los valles y Avileña-Negra Ibérica se encontraron frecuencias del alelo A, y en carne de ganado español, se asoció a mayor concentración del ácido docosatetraenoico (22:4n−6) (Sevane et al. 2011, Sevane et al. 2013).
En la biosíntesis de FA, SREBP activa a ACACA y SCD (Figura 1). SCD sintetiza la proteína es Estearoil-CoA desaturasa. La variante SCD1 responde considerablemente a la dieta, desempeñando un papel fundamental en el metabolismo lipídico general y el equilibrio energético. Dentro de este gen, se analizaron los marcadores g.10153, g.10213 y g.10329, los cuales se encuentran en desequilibrio de ligamiento. En SCD g.10329 se encontró una diferencia génica donde WAG y WBR presentaron una frecuencia más alta del alelo C en comparación con WAN. Este SNP es el único no sinónimo, el cual ocasiona una sustitución Val/Ala en el aminoácido 293. Previamente Sánchez-Ramos et al. (2023) analizaron estos SNP en esta población Wagyu-Cross y encontraron múltiples efectos sobre múltiples FA. El desequilibrio de ligamiento entre los tres SNP de SCD1, la desviación en el equilibrio de H-W de SCD g.10213 y la asociación de estos SNP a distintos FA, puede sugerir una selección sobre el haplotipo ATC de estos SNP en la población Wagyu-Cross. Estos SNP se han analizado en ganado autraliano, coreano, italiano, y razas como Angus, Fleckvieh, Hanwoo, Holstein, Qinchuan y se ha encontrado un amplio rango en las frecuencias alélicas y similitudes entre las asociaciones a FA. Específicamente el alelo C de g.10329 se ha asociado a incrementos de MUFA ácido palmitoleico (C16:1n-7) y ácido oleico (C18:1n-6) y disminuciones ácido palmítico (C16:0) y ácido esteárico (C18:0) en carne y leche. SCD5 es la segunda isoforma del gen, la cual se expresa principalmente en el páncreas. En la población Wagyu-Cross, el SNP SCD5 ss252452202 se encontró una diferencia génica donde WAN presentó una frecuencia más alta del alelo C en comparación con WBR. En la raza Holstein, el alelo C de este SNP se asoció a menor deposición de SFA y mayor MUFA en leche (Rincón et al. 2011), por otro lado, en carne de ganado Hereford, el alelo T se asoció a mayor PUFA (Branda et al. 2014). Estas asociaciones concuerdan con la función de SCD, el cual cataliza la inserción de un doble enlace cis en la posición delta-9 en sustratos grasos de acil-CoA dando lugar al ácido palmítico (C16:1n-7) y ácido oleico (C18:1n-6) a partir de sus respectivos saturados (Sánchez-Ramos et al. 2023). ACACA es una enzima citosólica que cataliza la carboxilación de acetil-CoA a malonil-CoA, el cual es el primer paso de la biosíntesis de novo de FA. El SNP ss64381883 ha sido estudiado en razas españolas y Wagyu-Cross donde se ha encontrado una alta segregación del alelo G, sin embargo, no se han encontrado asociaciones a FA. Previamente se realizó un análisis en distintas razas donde ocho SNP dentro de ACACA, se asociaron a múltiples efectos en distintos FA (Zhang et al. 2010). Se han reportado varios SNP con efecto en la composición de FA en leche dentro de este gen (Pegolo et al. 2016, Azis et al. 2020, Kęsek-Wozniak et al. 2020). El malonil-CoA producto de ACACA inhibe a CPT1B la cual es una enzima ubicada en la membrana mitocondrial externa que transporta FA de cadena larga hacia las mitocondrias para la β-oxidación. El SNP CPT1B ss65363345 es monomórfico en la población Wagyu-Cross, previamente se reportó una baja frecuencia del alelo C en razas españolas (Sevane et al. 2013). Recientemente dentro de CPT1B, se encontraron dos SNP asociados a la grasa dorsal y al ácido araquidónico (C20:4n-6) en carne de ganado Simmental (He et al. 2022).
AMPK también regula diversos genes implicados en la captación de glucosa. SIRT1 es una desacetilasa dependiente de NAD+ que funciona como un sensor maestro de lipólisis. Es conocida por sus actividades de desacetilación y modulación de varias proteínas reguladoras de genes, como PGC-1α y SREBP-1, así como por la activación de la oxidación de FA e inhibición de la lipogénesis (Gui et al. 2019). SIRT1 desacetila y modula la actividad de FOXO1, el cual es un factor de transcripción que es el objetivo principal de la señalización de la insulina y regula la homeostasis metabólica en respuesta al estrés oxidativo (Hadar et al. 2017). Ambos SNP analizados en estos genes resultaron monomórficos. Se han identificado dos SNP en SIRT1 y uno en FOXO1 asociados a grasa intramuscular (IMF) en ganado Qinchuan (Gui y Jia 2018, Gui et al. 2019).
La proteína codificada por el gen PPARGC1A es un coactivador transcripcional que regula los genes implicados en el metabolismo energético. Interactúa con PPARG, lo que permite la interacción de esta proteína con múltiples factores de transcripción, además proporciona un vínculo directo entre los estímulos fisiológicos externos y la regulación de la biogénesis mitocondrial (Charos et al. 2012). En el intrón 9 de este gen se encuentra el SNP c.1892+19, donde la población Wagyu-Cross presentó una frecuencia del alelo T visiblemente inferior en todos los grupos genéticos. Previamente se reportó en esta población un efecto aditivo del alelo C a incrementos del ácido linoleico (C18:2n-6) (Sánchez-Ramos et al. 2023). En carne de ganado Holstein se encontró una frecuencia alélica similar, y el homocigoto CC se asoció a menores concentraciones de ácido palmítico (C16:0) y SFA en contraste con el heterocigoto (Bartoň et al. 2016). En otro estudio el alelo C se asoció a menor rendimiento de la grasa en leche (Weikard et al. 2005). Otros estudios han confirmado la asociación entre este SNP y FA. Adicionalmente se han reportado otros SNP asociados a diferentes características en leche Holstein (Schennink et al. 2009, Lee et al. 2015). La función principal de MEF2C es actuar como activador de la transcripción dependiente de la ARN polimerasa II mediante su unión al ADN. Además, esta proteína, miembro de la familia de factores potenciadores de miocitos 2, presenta actividad de unión al dominio de caja HMG, interacción con histona desacetilasa y reconocimiento del elemento MEF2 en las regiones reguladoras de numerosos genes específicos del músculo (Yu y Guttride 2018). Dentro de este gen se analizaron dos SNP, sin embargo, solo MEF2C ss38329156 fue polimórfico, con mayor frecuencia del alelo G. Previamente se reportó en esta población que el homocigoto GG redujo el ácido mirístico (C14:0) en comparación con el heterocigoto en carne Wagyu-Cross (Sánchez-Ramos et al. 2023). SLC2A4 permite la transferencia del enantiómero D del monosacárido hexosa glucosa del exterior de la membrana hacia el citosol. Dentro de este gen, en el SNP ss62538460 se encontró una frecuencia inferior al 5% del alelo A, previamente se reportó en esta población, que el heterocigoto GA está relacionado a menor contenido de SFA y mayor de MUFA y MUFA/SFA en comparación con GG (Sánchez-Ramos et al. 2023). En otros estudios se ha demostrado que algunos FA como el ácido oleico (C18:1) y el ácido linoleico (C18:2n-6) son potentes inhibidores de la expresión de SLC2A4/GLUT4 en células musculares (Poletto et al. 2015).
Los receptores activados por proliferadores de peroxisomas (PPAR) son factores de transcripción activados por ligandos de la superfamilia de receptores de hormonas nucleares (Figura 1). Dentro de esta familia se encuentra PPARA, el cual es uno de los principales reguladores de la oxidación de FA libres y el transporte de FA (Chiazza y Collino 2016). Al igual que en ganado español (Sevane et al. 2013), en este estudio, el SNP ss65362714 fue monomórfico en la población Wagyu-Cross, sin embargo, previamente se reportó polimorfismo en las razas Pasigea, Pirenaica, Asturiana de los Valles (Sevane et al. 2011). PPARG regula la diferenciación de adipocitos, y mejora la expresión de varios genes que codifican proteínas implicadas en el metabolismo de la glucosa y los lípidos (Ferst et al. 2020). Cerca de este gen se encuentra PPARG ss62850198, donde el alelo G se asoció previamente a incrementar PUFA omega-3 en razas españolas (Sevane et al. 2013, Sevane et al. 2014), en la población Wagyu-Cross se encontró alta segregación del alelo G muy similar a la reportada en las razas españolas. Dentro de PPARG existen otros SNP asociados a la composición de múltiples FA en carne de ganado coreano (Lee et al. 2015). PPARA regula directamente a PLTP el cual transfiere fosfolípidos de las lipoproteínas de muy baja densidad (VLDL) a lipoproteínas de alta densidad (HDL). Cerca de este gen se encuentra el PLTP ss77832104, donde el alelo G fue asociado a aumentar omega-6/omega-3 en carne de razas españolas (Dunner et al. 2013, Sevane et al 2014); en ganado Wagyu-Cross se encontró una mayor segregación del alelo G y previamente se encontró un efecto aditivo del alelo G a la reducción de ácido palmítico (C16:0) (Sánchez-Ramos et al. 2023), este resultado es consistente con otro estudio, donde se encontró una relación entre el nivel de ARNm de PLTP y C16:0 y SFA (Qin et al. 2015).
En el exón 8 de DGAT1 se encuentra el marcador DGAT1 K232A, el cual es una sustitución de dinucleótidos ApA/GpC provocando un cambio en el aminoácido 232 K/A. En la población Wagyu-Cross se encontró diferencia génica, donde WAG presentó la mayor segregación del alelo K. Este marcador ha sido estudiado en múltiples razas y se ha encontrado gran variabilidad en la frecuencia alélica y asociaciones del alelo A al incremento de grasa en leche o IMF en carne. El conjunto de asociaciones reportadas muestra un comportamiento en el que el aumento de grasa en la leche o IMF en carne es gracias a los SFA, reduciendo así la proporción MUFA/SFA. DGAT1 participa en el metabolismo de glicerolipidos, sintetizando triglicéridos a partir de diacilglicerol y acil Co-A (Samuel et al. 2023). A su vez LPL cataliza la hidrólisis de los triglicéridos de los quilomicrones circulantes y VLDL (Lund et al. 2021). En el exón dos de LPL se encuentra el SNP ss65478732, el cual presentó en la población Wagyu-Cross una frecuencia del alelo T inferior al 5%. Estos valores se asemejan a lo reportado en múltiples razas; adicionalmente, en carne de razas españolas, se asoció el alelo T al aumento del ácido dihomo-gamma-linolénico neutro (20:3n−6) y ácido araquidónico (20:4n−6) (Sevane et al. 2011, Sevane et al. 2013, Sevane et al. 2014). Dentro del mismo exón 2, se han reportado dos SNP asociados a múltiples FA en IMF de ganado coreano (Oh et al. 2013).
Fuera de las rutas metabólicas mencionadas existen algunos genes que no intervienen directamente en el metabolismo de FA, pero se han relacionado a su composición. El gen IGF2R interviene en el transporte de enzimas lisosomales fosforiladas desde el complejo de Golgi y la superficie celular a los lisosomas. El SNP IGF2R ss77831885 se asoció previamente en esta población Wagyu-Cross a la concentración de C16:0, siendo el heterocigoto el que presentó menor concentración respecto con el homocigoto AA (Sánchez-Ramos et al. 2023). En este estudio se encontró alta segregación del alelo G y diferencia génica, siendo WBR el que presentó mayor segregación del alelo G en comparación con WAN y WBM. En carne de razas españolas este polimorfismo fue asociado al sabor de la carne (Dunner et al. 2013, Sevane et al. 2014). MYOZ1 es una proteína de unión de a-actinina, c-filamina y teletonina de las líneas Z del músculo esquelético y se expresado principalmente en el músculo esquelético (Ma et al. 2015). En el SNP ss77832104 se encontró diferencia génica, siendo WAG y WBR los grupos con mayor segregación del alelo T en comparación con WHF. Recientemente se reportó en esta población que el homocigoto CC contiene mayores niveles de ácido heptadecenoico (C17:1n-8) en comparación con el homocigoto TT (Sánchez-Ramos et al. 2023). El producto de SRPRA participa en la dirección y translocación de proteínas secretoras y de membrana nacientes a la membrana del retículo endoplásmico, lo que ayuda al control espacial de la síntesis de proteínas (Kim et al. 2016). En el marcador SRPRA 4150 se encontró una baja segregación del alelo C en todos los grupos, además se encontró diferencia génica, siendo WAN el que presenta mayor segregación del alelo C en comparación con WBR. En otro estudio se encontró una asociación entre los homocigotos CC a mayores niveles de MUFA, menores de SFA y otros aspectos de interés (Medrano y Rincón 2009). Otro SNP dentro del mismo SRPRA se asoció a efectos similares a los reportados (Branda et al. 2014).
La composición de los FA en la carne es un factor determinante en la calidad sensorial (Frank et al. 2016) y nutricional (Vela-Vásquez et al. 2021). Desde el punto de vista nutricional el alto consumo de SFA se asocia a enfermedades cardiovasculares, cáncer, diabetes entre otras (Bouvard et al. 2015, Mota et al. 2021). Por otro lado, los MUFA se asocian positivamente con la calidad sensorial (Khan et al. 2015) y beneficios de la salud del consumidor (Vela-Vásquez et al. 2021). En general los MUFA producen efectos benéficos que conducen a la prevención del cáncer, enfermedades autoinmunes e inflamatorias (Wang et al. 2020). Entre ellos, el ácido palmitoleico (C16:1n-7) y ácido oleico (C18:1n-9) son de gran importancia en la composición de MUFA en la carne. Los aumentos de PUFA se asocian principalmente a una disminución en los niveles de colesterol en sangre y una reducción en la incidencia de enfermedades cardiovasculares. Sin embargo, una dieta alta ω-6 y deficiente de ω-3, también contribuye a un mayor riesgo de enfermedades cardiovasculares al promover un estado protrombótico y proinflamatorio que predispone a trastornos, tales como como hipertensión y disfunción neurológica (Wood y Enser 2017).
Recientemente en la población Wagyu-Cross se asoció el marcador SLC2A4 ss62538460 a las proporciones de SFA y MUFA llegando a ser un marcador destacable, sin embargo, se necesitan otros análisis de asociación para comprobar su efecto. Como en el caso de SLC2A4 ss62538460 existen otros cinco marcadores que también necesitan validación (Sánchez-Ramos et al. 2023). En el gen SREBF1 se ha identificado un polimorfismo que no se ha analizado en la raza Wagyu, pero si en Hanwoo, el cual se ha asociado a acido esteárico (C18:0), acido linoleico (C18:2n-6) y PUFA. Existen otros genes como ACACA, PPARG, LPL y SRPR que albergan otros polimorfismos que se han asociado a algún FA, pero no se han analizado en ganado Wagyu. Generalmente en las estrategias de selección se busca mejorar el perfil lipídico junto con el aumento de IMF. Sin embargo, hay que dejar en claro que se tratan de características diferentes. DGAT1 K232A es un marcador que se ha asociado a IMF en múltiples razas, el incremento en el IMF se ve principalmente por SFA, disminuyendo la proporción de MUFA. Existen otros SNP con asociaciones de FA en leche y que aún no se han estudiado en carne que podrían ser útiles para mejorar las proporciones. El uso de marcadores con efectos sobre FA en la carne permite identificar como se distribuyen las frecuencias de alelos favorables en los distintos grupos de cruces y predecir la efectividad de cruces en las características de interés. Esta herramienta se puede utilizar en cualquier etapa de vida del animal, permitiendo ahorrar costos y tiempo durante el intervalo generacional. Sin embargo, es necesario validar estos marcadores en la raza Wagyu y sus cruces, para cerciorar que los SNP reportados en otras razas, también sean validas en ésta.
Conclusiones
De los 27 SNP analizados en la población Wagyu-Cross, se encontraron 20 SNP polimórficos, de los cuales ocho de ellos presentaron una diferencia génica entre grupos, y de estos, cinco han sido asociados a FA. Cuatro de los ocho SNP con diferencia génica se encontraron entre WAN y WBR, y tres entre WAG y WAN, colocando a WAN como el grupo con mayor diferencia al resto. La frecuencia alélica del alelo C en SCD1 g.10329 fue mayor en WAG y WBR. En general las frecuencias alélicas de los grupos genéticos de la población Wagyu-cross, no muestran grandes diferencias. El marcador. SCD1 g.10329 es un excelente marcador que, debido a su respaldo, es útil para MAS, y para inferir algunas características de la carne. Adicionalmente se propone a MYOZ1 ss77831945, IGF2R ss77831885, DGAT1 K232A, SCD5 ss252452202, SLC2A4 ss62538460, PPARGC1A c.1892+19 y PLTP ss77832104 a someterse a pruebas de asociación a FA, debido a que tienen cualidades para ser implementados en MAS, sin embargo, necesita cerciorarse su efecto.











 nueva página del texto (beta)
nueva página del texto (beta)



