Introducción
El zinc es un metal de vital importancia en la industria moderna debido a sus diversas propiedades y aplicaciones. Este metal se emplea en múltiples sectores industriales, desde su uso en recubrimientos para proteger estructuras metálicas de la corrosión, hasta su aplicación en baterías y aleaciones [1]. La creciente demanda de zinc a nivel global plantea la necesidad de desarrollar métodos de producción eficientes y sostenibles que garanticen el suministro a largo plazo [2].
Los procesos tradicionales para la obtención de zinc se basan en procesos pirometalúrgicos, los cuales implican el uso de altas temperaturas y la emisión de gases contaminantes. Por lo tanto, es fundamental adoptar prácticas que minimicen el impacto ambiental y optimicen la utilización de los recursos minerales [3].
En respuesta a los desafíos ambientales y tecnológicos, el proceso hidrometalúrgico emergió como una alternativa prometedora para la producción de zinc, ya que evita la emisión de gases contaminantes a la atmósfera [4]. La ruta hidrometalúrgica consiste en un conjunto de métodos que utilizan medios acuosos para obtener el elemento en forma metálica a partir de minerales y concentrados. Este proceso se fundamenta en la disolución selectiva del zinc y la posterior recuperación del metal mediante electrólisis [5].
En este artículo se abordan las etapas operativas del proceso hidrometalúrgico de zinc y los desafíos que representan desde el punto de vista económico y ambiental. Además, se presentan las principales aplicaciones industriales y la demanda de zinc proyectada para el año 2050. Asimismo, se discuten las estrategias relacionadas con la recuperación de zinc a partir de recursos secundarios mediante el enfoque de la economía circular. La revisión será útil para brindar información acerca del estado actual de los procesos hidrometalúrgicos, los avances tecnológicos y los estudios en respuesta a las tendencias futuras de la industria del zinc.
Hidrometalurgia del zinc
En la naturaleza, el zinc se encuentra principalmente en minerales como la esfalerita (ZnS), zincita (ZnO), franklinita (ZnO(Fe, Mn)2O3), calamina (Zn2(OH)2SiO3) y marmatita (Zn, Fe)S. Los principales minerales de ganga son la pirita (FeS2), magnetita (Fe3O4), calcopirita (CuFeS2) y pirrotita (Fe(1-x)S) [6]. La extracción de zinc se basaba tradicionalmente en procesos pirometalúrgicos. Sin embargo, en 1917 se desarrolló de manera comercial el proceso hidrometalúrgico para la obtención de zinc, en la actualidad, representa casi el 85 % de la producción mundial [7]. Este proceso tiene varias ventajas sobre el pirometalúrgico, por ejemplo:
Permite procesar minerales y concentrados complejos de baja ley, es decir, con bajas concentraciones de elementos valiosos [8].
Se pueden recuperar diferentes metales (e.g., Cd, Pb, Au y Ag) como subproductos.
El ácido sulfúrico (H2SO4) utilizado en la lixiviación puede regenerarse mediante la conversión del dióxido de azufre (SO₂(g)) mejorando la economía del proceso [9].
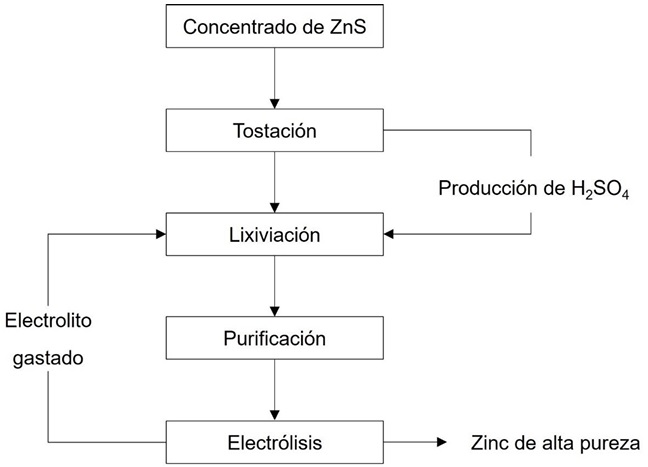
En la Figura 1 se presenta un esquema conceptual del proceso hidrometalúrgico para la obtención de zinc metálico [10]. El proceso convencional involucra cuatro etapas principales: tostación, lixiviación, purificación y electrólisis. Por otra parte, se llevan a cabo operaciones secundarias en las que se destacan la producción de ácido sulfúrico a partir del dióxido de azufre generado durante la tostación y la reutilización del electrolito gastado a la etapa de lixiviación. Estas prácticas promueven el desarrollo sostenible al permitir la reutilización de los subproductos generados en lugar de descartarlos como residuos.
Tostación
La primera etapa del proceso consiste en la tostación de los concentrados de sulfuro de zinc (ZnS). La conversión de los sulfuros a óxidos es necesaria, ya que como sulfuros no pueden ser lixiviados en medios ácidos o básicos. La tostación normalmente se lleva a cabo en hornos de lecho fluidizado a temperaturas de entre 800 y 1300 °C para producir una calcina (ZnO) [11]. Sin embargo, durante la tostación ocurren varias reacciones químicas y es común la formación de ferrita de zinc (ZnFe2O4). Además, si hay presencia de sílice (SiO2) en la estructura mineral, una parte del zinc puede reaccionar para formar silicato de zinc (Zn2SiO4) [12]. Las reacciones químicas del proceso de tostación se presentan en las ecuaciones (1-3) [4].
Producción de ácido sulfúrico
Durante la etapa de tostación, el azufre presente en la materia prima en forma de sulfuro se oxida a dióxido de azufre (SO2(g)) (ver ecuación 1). Generalmente, el SO2(g) se recupera para producir ácido sulfúrico (H2SO4) como subproducto mediante el método de contacto (Figura 2) [13, 14]. El proceso incorpora tres operaciones básicas. En la primera, el SO2(g) se alimenta a una operación unitaria de conversión catalítica. En esta etapa, el SO2(g) se mezcla con aire a 450 °C y una presión de entre 101.3 y 202.6 kPa (i.e., entre 1 y 2 atm) en presencia de un catalizador de vanadio para producir trióxido de azufre (SO3(g)) (ecuación 4).
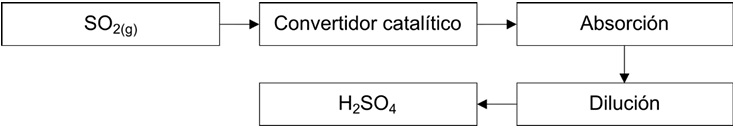
Figura 2 Diagrama de flujo simplificado de la producción de ácido sulfúrico, modificado de Zaker [14].
El trióxido de azufre se absorbe en ácido sulfúrico (H2SO4) al 98 % para producir ácido disulfúrico, también conocido como óleum (H2S2O7) (ecuación 5). Este método se emplea porque la adición directa de agua al trióxido de azufre provoca una reacción altamente exotérmica [15]. Finalmente, el ácido disulfúrico formado en la etapa de absorción se diluye con agua para obtener ácido sulfúrico (ecuación 6), el cual es empleado en la etapa de lixiviación del proceso.
La conversión del SO2(g) en ácido sulfúrico proporciona una fuente interna de materia prima, reduciendo los costos asociados con el suministro de este reactivo. Además, este proceso reduce notablemente las emisiones de gases contaminantes, lo que facilita el cumplimiento de normativas ambientales, especialmente en regiones con estrictas regulaciones sobre la calidad del aire y el manejo de sustancias químicas peligrosas.
Estas prácticas representan un avance significativo hacia el modelo de la economía circular a través del uso eficiente de los recursos y la disminución de los residuos mediante la reutilización y recuperación de subproductos, los cuales pueden ser comercializados a otras industrias.
Lixiviación
La lixiviación de los productos sólidos generados durante la tostación se lleva a cabo en dos etapas. En la primera, el óxido de zinc (ZnO) se disuelve utilizando una solución diluida de ácido sulfúrico con un pH de entre 5 y 6, generando una solución rica de sulfato de zinc (ZnSO4) (ecuación 7). Generalmente, se añade el electrolito gastado proveniente del proceso de electrólisis, el cual contiene entre 100 y 150 g/L de H2SO4. No obstante, compuestos como la ferrita de zinc (ZnFe2O4) y los silicatos de zinc (Zn2SiO4) permanecen insolubles bajo estas condiciones, lo que hace necesario realizar una segunda etapa de lixiviación [7]. Los residuos sólidos resultantes de la primera etapa son trasladados a una serie de tanques donde se lleva a cabo la lixiviación a una temperatura de 90 °C y pH de entre 3 y 2. Las reacciones químicas que ocurren durante esta etapa de lixiviación se detallan en las ecuaciones 8 y 9 [16].
Purificación
El lixiviado de la etapa de disolución ácida contiene iones de hierro (Fe3+) y otras impurezas como cadmio, níquel, cobre, cobalto, arsénico y antimonio, por lo que deben eliminarse para evitar efectos adversos en la electrólisis posterior. Para lograrlo se utilizan diferentes métodos: precipitación de jarosita, goethita y/o hematita [17].
El proceso de precipitación de jarosita se desarrolló en la década de 1960 y ha sido ampliamente utilizado sobre los otros métodos debido a la simplicidad y bajo costo del proceso. La jarosita es un sulfato de hierro básico, cuya fórmula general es representada por AFe3(SO4)2(OH)6, en donde, A representa cationes monovalentes como K+, NH4 +, Na+ y H3O+. Generalmente, la precipitación se lleva a cabo mediante la adición de un álcali o amoníaco a los lixiviados, el ajuste del pH se realiza mediante la adición de calcina hasta lograr estabilizarlo entre 3 y 2 [18].
La generación de compuestos tipo jarosita es de aproximadamente 0.5 toneladas por cada tonelada de zinc producido [19]. Por lo tanto, uno de los problemas centrales radica en la gran cantidad de jarositas generadas, las cuales se consideran residuos mineros peligrosos debido a su contenido en metales pesados. Por lo anterior, varios países han prohibido la implementación del método jarosítico, aunque en México aún se utiliza de manera parcial.
Electrólisis
La etapa de electrólisis a partir de la solución de sulfato de zinc purificada consiste en reducir los iones de zinc (Zn2+) a zinc elemental (Zn0) en el cátodo de una celda electrolítica abierta. El agua se descompone en el ánodo para liberar oxígeno, formar iones de hidrógeno y liberar electrones. Las reacciones que describen este proceso se presentan en las ecuaciones (10-12) [4].
Reacción anódica:
Reacción catódica:
La ecuación global del proceso es la siguiente:
Por lo general, se utilizan cátodos de aluminio y ánodos a base de plomo, ya que estos electrodos tienen una buena estabilidad durante el proceso cuando se opera adecuadamente; sin embargo, cuando se tiene un alto sobrepotencial se favorece la evolución de oxígeno y aumenta significativamente el consumo de energía [20]. Scott, Pitblado, Barton y Ault [21], estudiaron las condiciones óptimas de operación de la celda de electrodeposición y determinaron que las mejores condiciones incluyen un voltaje total de la celda de 2.6 V, 70 g/L Zn2+, 180 g/L H2SO4, 400 A/m2 y 45 °C durante 72 h. Sin embargo, en los últimos años, las condiciones típicas de operación han variado y es común que se utilicen: 55 g/L Zn2+, 170 g/L H2SO4, 500 A/m2 y 40 °C durante 48 h [22].
Avances en la hidrometalurgia del zinc
Ruta de procesamiento para la obtención de zinc y hierro elemental
En el proceso hidrometalúrgico de zinc, el hierro disuelto (Fe3+) presente en las soluciones de lixiviación es una de las principales impurezas y obstaculiza la obtención de zinc elemental. A pesar de que los métodos de precipitación permiten remover o reducir el contenido de hierro, estos presentan algunas limitantes como la generación de grandes volúmenes de residuos sólidos.
Por otra parte, aunque en las operaciones unitarias de la etapa de lixiviación existen varias áreas de oportunidad para contribuir al desarrollo de procesos sostenibles, uno de los principales retos radica en disminuir la cantidad de agua utilizada. Por lo tanto, no solo es necesario proponer esquemas que requieran bajos consumos de agua, sino que también favorezcan las tres R (reusar, reciclar y recuperar). Aunque una de las alternativas más obvias de acuerdo con Lapidus [23] es incrementar la relación sólido-líquido, esto no siempre es posible debido a la baja solubilidad de algunas especies.
Desde la perspectiva de una economía circular, las operaciones unitarias de electrólisis y extracción por solventes (SE, por sus siglas en inglés) son preferibles a las operaciones de precipitación, ya que estos métodos destacan por su capacidad de reutilizar el agua de proceso, promoviendo una gestión más sostenible de los recursos hídricos [23]. Este enfoque no solo disminuye el impacto ambiental asociado al proceso tradicional de obtención de zinc, sino que también optimiza la eficiencia del ciclo operativo.
En la Figura 3 se presenta un esquema conceptual en donde se propone la sustitución del proceso de precipitación de jarosita por el método de extracción por solventes (SE). Esta metodología ofrece una alternativa más eficiente para purificar las soluciones de lixiviación, al mismo tiempo que permite recuperar el hierro en su forma elemental mediante electrólisis, evitando la precipitación del hierro como jarosita. Las etapas principales de este proceso conceptual incluyen: tostación, lixiviación, separación, purificación mediante extracción por solventes (SE) y electrólisis.
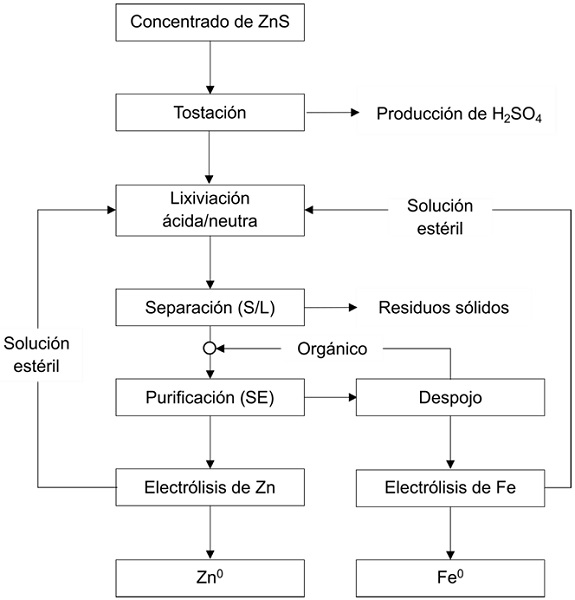
Figura 3 Ruta de procesamiento para la obtención de Zn y Fe elemental mediante extracción por solventes y electrólisis.
De acuerdo con diversos autores [24, 25], la extracción por solventes es uno de los métodos más útiles para la concentración de iones metálicos o impurezas después de la lixiviación y la separación sólido-líquido. En esta etapa se puede producir un electrolito de zinc de alta pureza y un refinado orgánico. El empleo de extractantes orgánicos, como el ácido di-(2-etilhexil) fosfórico (D2EHPA), ha demostrado ser particularmente eficiente en el tratamiento de soluciones que contienen sulfato y hierro disuelto, ya que permite extraer selectivamente el Fe3+ de la solución cargada [26].
En la etapa de despojo, algunos estudios han demostrado que el uso de ácido clorhídrico (HCl) es eficaz para separar el hierro de la fase orgánica, permitiendo su recuperación mediante electrólisis [27]. Por otro lado, la fase orgánica purificada puede recircularse al proceso, mientras que el electrolito gastado (o solución estéril) puede emplearse en la etapa de lixiviación.
En base a lo anterior, la integración del método de extracción por solventes como etapa de purificación representa una estrategia innovadora y prometedora. En este sentido, su implementación a escala industrial requiere de investigación continua, que aborde, entre otros aspectos, el estudio de los extractantes orgánicos y la optimización de los parámetros operativos, con el fin de reducir los costos y maximizar la eficiencia del proceso. Los avances enfocados en la selectividad y estabilidad de extractantes, junto con ajustes en pH, temperatura y condiciones de despojo, podrían ampliar la viabilidad de esta alternativa consolidándola como una tecnología sostenible en la industria hidrometalúrgica [28, 29].
Lixiviación directa de los concentrados de zinc
En los últimos años, se ha investigado la implementación de un proceso de lixiviación directa de concentrados de ZnS como una alternativa para eliminar la etapa de tostación en el proceso convencional de extracción de zinc. La introducción del proceso de lixiviación a presión, que tuvo su inicio en Trail, British Columbia, Canadá, en 1981, ha permitido enfrentar el desafío ambiental que representa la producción de zinc y el control del hierro como impureza. Este método se ha destacado como una de las aplicaciones más exitosas de la hidrometalurgia [30].
El proceso consiste en la lixiviación directa a presión de los concentrados, evitando las operaciones pirometalúrgicas (tostación). Este proceso se lleva a cabo en diferentes etapas a temperaturas de entre 80 y 150 °C y a presiones de entre 400 y 1034 kPa en autoclaves horizontales [31]. Durante el proceso de lixiviación a presión, los sulfuros presentes en la materia prima reaccionan con ácido sulfúrico y oxígeno, generando una solución de sulfatos y azufre elemental. Esto evita la formación de ácido sulfúrico, lo cual no es posible mediante el proceso de tostación. Las reacciones que describen el proceso son las descritas por las ecuaciones (13-16), [32].
El lixiviado se bombea a una etapa combinada de neutralización y reducción. La solución se neutraliza hasta pH 4 con una baja concentración de ácido sulfúrico (< 20 g/L H2SO4), generalmente se emplea el uso del electrolito gastado producido en la etapa de electrólisis. Posteriormente, la solución se calienta a temperaturas de 150 °C bajo presión de oxígeno en una autoclave hasta 1034 kPa aproximadamente. Durante esta etapa el Fe2+ se oxida a Fe3+ y se precipita el hierro de la solución como hematita (Fe2O3), un residuo sólido mucho más estable que la jarosita (ecuación 17) [18]. El precipitado de hematita generalmente contiene entre un 60 y 65 % de Fe, 1 % de S y 0.6 % de Zn. Después de remover el hierro y otras impurezas mediante separación sólido- líquido, la solución cargada se transfiere a la etapa de electrólisis [32].
Entre las principales limitaciones de este método se encuentran los elevados costos de capital asociados al uso de autoclaves, lo que ha restringido su adopción generalizada en la industria. Sin embargo, una ventaja significativa radica en la producción del precipitado de hematita, cuya versatilidad lo convierte en un subproducto valioso. Este material tiene un importante mercado en el sector de la construcción, donde puede ser empleado como materia prima para la fabricación de cemento y otros compuestos [33].
Usos y demanda del zinc
Usos industriales del zinc
El zinc tiene una amplia gama de aplicaciones industriales debido a sus propiedades físicas y químicas. En la Figura 4 se muestra una gráfica con los principales usos del zinc de acuerdo con la Asociación Internacional de Zinc (IZA, por sus siglas en inglés) [34]. Actualmente, alrededor del 60 % de la producción de zinc se utiliza como recubrimientos anticorrosivos mediante galvanizado. Otra parte se utiliza para la manufactura de aleaciones; esta aplicación incluye aleaciones de fundición de zinc-aluminio, zinc-plomo, zinc-hierro y zinc-cobre (17 %), así como aditivo de aleación principalmente en latones y bronces (aproximadamente 9 %). La tercera aplicación importante del zinc es la elaboración de productos semiacabados de zinc como ánodos y láminas (6 %). Una participación similar se destina a la elaboración de productos químicos, siendo el óxido de zinc el más importante en cuanto al volumen de producción.
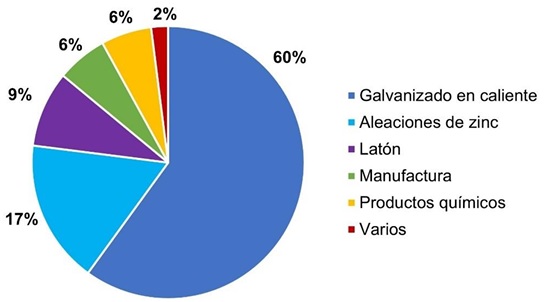
Figura 4 Principales usos del zinc, construida con datos de la Asociación Internacional de Zinc [34].
Demanda de zinc hacia el 2050
La producción anual de zinc es de alrededor de 13.8 millones de toneladas por año y entre los principales países productores se encuentran Australia, Canadá, Perú, Estados Unidos, México, Irlanda, Rusia, España, Suecia, Corea del Norte, China y Japón [35]. Sin embargo, las medidas gubernamentales impuestas debido al estallido de la pandemia mundial por COVID-19 y la subsecuente caída de los precios del zinc provocaron una disminución de la producción minera en muchos países, especialmente en América del Sur. A pesas de esto, se espera que la demanda de metales a nivel mundial aumente en las próximas décadas [36].
La demanda del zinc está impulsada por el crecimiento de la población mundial, el desarrollo tecnológico y la transición energética. La Asociación Internacional de Zinc proyectó un escenario de oferta y demanda para el 2050 utilizando un modelo de existencias y flujos globales de zinc [37]. A través de este modelo, se simuló un escenario de demanda basado en el crecimiento poblacional y la evolución del producto interno bruto (PIB) global, conforme a lo descrito por la Organización para la Cooperación y el Desarrollo Económico (OCDE) en el estudio titulado Global Material Resources Outlook to 2060. Se prevé que el requerimiento total de zinc alcance 28 millones de toneladas anuales en 2050 (ver Figura 5a).
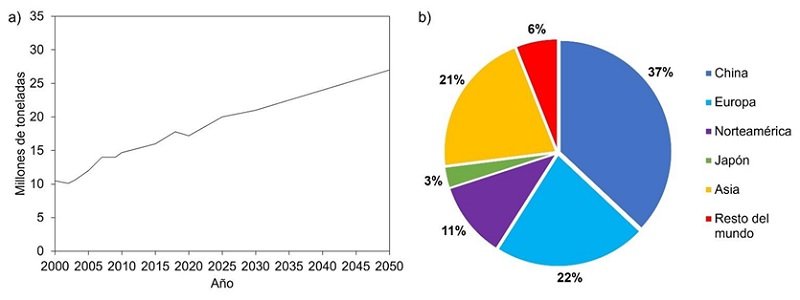
Figura 5 a) Demanda de zinc para el año 2050 y b) participación regional en el consumo mundial de zinc refinado en 2023 [37, 38].
La Figura 5b presenta la participación regional en el consumo mundial de zinc refinado correspondiente al año 2023. En dicho periodo, China se posicionó como el principal consumidor global, representando el 37 % del total, seguida de la región europea con un 22 %. Este patrón de consumo está estrechamente relacionado con los avances en la infraestructura. Se espera que en los próximos 5 años se presenten cambios significativos en el patrón de la demanda regional, lo que plantea la necesidad de incrementar las capacidades de fundición y refinación para satisfacer los requerimientos futuros [38].
Las proyecciones de la demanda estimada por la IZA son consistentes con las descritas en otras fuentes bibliográficas. Backman [39] informa que la demanda de zinc para el año 2050 alcanzará los 27 millones de toneladas. Otros estudios señalan que la demanda mundial de zinc podría variar entre 14.5 y 38.8 millones de toneladas al año, con un promedio de 26 millones de toneladas [40]. Asimismo, un análisis reciente realizado por Rostek, Tercero Espinoza, Goldmann y Loibl [41] estima que la demanda aumentará de 17.5 millones de toneladas en 2019, a 28 millones de toneladas para el año 2050.
El incremento constante en la demanda resalta la importancia de desarrollar tecnologías avanzadas para la gestión y recuperación de subproductos o fuentes secundarias. Esto adquiere especial relevancia si se considera que la corteza terrestre contiene aproximadamente 1.9 billones de toneladas métricas de zinc en total, de las cuales 63 millones de toneladas son recursos extraíbles y alrededor de 250 millones de toneladas son reservas probadas y probables que cumplen con los criterios de producción para alcanzar las demandas actuales del mercado [42].
Recuperación de zinc a partir de recursos secundarios
El fomento de estrategias de economía circular ha cobrado cada vez mayor relevancia, ya que estas se perfilan como una solución viable para enfrentar el agotamiento de los recursos debido a la creciente demanda de materiales y la generación de residuos. Estas estrategias permiten reducir los impactos ambientales de la producción primaria de zinc, debido a los altos consumos energéticos, particularmente en la etapa de electrólisis. En este proceso, el sobrepotencial producido durante la generación de oxígeno (gO2) representa aproximadamente el 20 y 25 % del voltaje total de la celda. Dado el incremento en los costos de energía y la preocupación por las emisiones de gases de efecto invernadero, reducir el sobrepotencial de generación de oxígeno (gO2) es una oportunidad clave para mejorar la eficiencia energética en la industria de obtención de zinc [43].
De acuerdo con el informe publicado por la Bureau of International Recycling (BIR) en 2016 [45], el requerimiento total de energía para la producción secundaria de zinc representa el 75 % de la energía consumida para la producción de zinc a partir de minerales, con una reducción simultánea de las emisiones de dióxido de carbono (CO2(g)) en un 40 %. Esta mayor eficiencia energética y menor huella de carbono, hacen que la adopción de métodos hidrometalúrgicos sea cada vez más relevante, ya que facilitan el aprovechamiento de fuentes secundarias en las que la mayoría de los compuestos pueden disolverse en soluciones ácidas o alcalinas. Además, estos métodos tienen diversas ventajas, como la posibilidad de realizar procesos a pequeña escala sin generar gases contaminantes [46, 47].
De acuerdo con algunos informes [34, 48] la disponibilidad de recursos de zinc en fuentes secundarias a nivel global es de alrededor de 247 millones de toneladas, casi el mismo orden de magnitud que el considerado como reservas probadas y probables. El estudio de la recuperación de zinc a partir de estos materiales ha llevado al desarrollo de un área del conocimiento conocida como minería urbana. Esta área se basa en la valorización de materias primas secundarias de fuentes antropogénicas a través del uso de procedimientos físicos, químicos, biológicos e insumos tecnológicos [49].
La recuperación de zinc a partir de chatarra electrónica representa una fuente secundaria con gran potencial. Esta categoría abarca dispositivos como teléfonos móviles, computadoras, grabadoras de vídeo, televisores entre otros equipos similares [50]. La vida útil limitada de estos desechos electrónicos ha contribuido al crecimiento exponencial de los mismos, lo que ha generado una preocupación ambiental significativa. Las cifras globales de generación de chatarra electrónica indican una producción de 50 millones de toneladas por año, con una proyección de 74.7 millones de toneladas para el año 2030 [51].
La chatarra electrónica comúnmente presenta contenidos importantes de elementos como Cr, Pd, Ni, Pb, Cu, Al, Zn, Ag, Au, entre otros. Cuando reciben un tratamiento y reciclaje apropiados, este tipo de desechos adquiere un valor económico gracias a sus componentes. La investigación y los estudios no se han limitado únicamente al reciclaje, sino que también han abordado la creación de valor comercial a través de enfoques diversos, como la reutilización y la extracción de los metales mediante procesos hidrometalúrgicos.
Por otro lado, uno de los recursos secundarios de zinc más comunes son las pilas de carbono (Zn-carbono) y alcalinas (Zn-MnO2). Generalmente en plantas de pequeña escala el proceso involucra cuatro etapas principales: conminución, lixiviación, purificación y recuperación. Según la revisión realizada por Sadeghi, João y Soares [52], se han logrado avances significativos en el reciclaje de pilas gastadas de Zn-carbono y Zn-MnO₂ mediante procesos hidrometalúrgicos en medios ácidos y alcalinos. Los resultados indican que las estrategias alcalinas son altamente selectivas para la extracción de zinc, con una extracción de apenas el 1 % de manganeso y rendimientos de lixiviación que varían entre el 38 % y el 83 %. En contraste, la lixiviación ácida no fue selectiva (se extrajo entre 13 y 40 % de Mn) y se registraron extracciones de Zn de aproximadamente 86 %.
Otros recursos secundarios que han sido ampliamente estudiados son los polvos (cenizas) y lodos generados en el alto horno (BF, por sus siglas en inglés) y el horno de arco eléctrico (EAF, por sus siglas en inglés). Estos residuos presentan un alto contenido de zinc, lo que hace que su extracción sea económicamente viable. Los procesos propuestos para tratar estos subproductos siderúrgico tienen similitudes con los procesos utilizados en la industria del zinc, como la tostación y la lixiviación [53].
De acuerdo con la Asociación Internacional del Zinc [34], en 2023 aproximadamente el 13.8 % del zinc refinado a nivel mundial se obtuvo a partir de materiales secundarios. Estos incluyen chatarra, polvo de horno de arco eléctrico, residuos generados durante procesos de galvanización, láminas de zinc, piezas fundidas a presión y componentes de latón. Se estima que para el año 2050, el reciclaje de zinc alcance 9 millones de toneladas anuales, elevando la tasa de reciclaje global al 29 % [54].
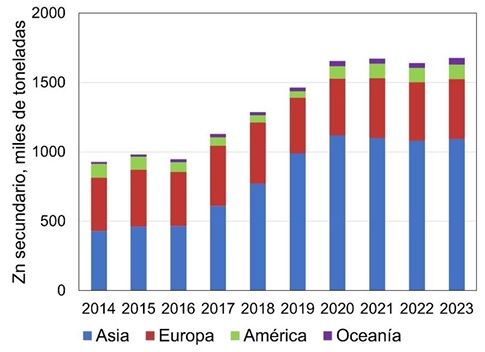
La Figura 6 muestra la producción secundaria de zinc refinado por continentes, entre 2014 y 2023. Asia lidera con una producción de aproximadamente 1 millón de toneladas anuales en los últimos cinco años, consolidándose como el principal productor de zinc secundario. Europa ha mantenido una producción relativamente estable, contribuyendo entre 100 000 y 200 000 toneladas anuales en el mismo período.
En América, el reciclaje de zinc secundario ha experimentado un crecimiento significativo, impulsado principalmente por Estados Unidos. En 2018, este país recicló 32 000 toneladas de zinc secundario provenientes de residuos de galvanización y óxido de zinc crudo generado a partir del polvo de horno de arco eléctrico (EAF). Esta tendencia mejoró considerablemente en 2020 y 2021, con un aumento en la producción secundaria gracias a la reapertura de la planta de American Zinc Recycling en Mooresboro, Carolina del Norte. Por otro lado, Oceanía ha mostrado un crecimiento en la producción de zinc secundario en los últimos años, aunque en menor medida en comparación con América. Sin embargo, presenta una tendencia al alza en su contribución [55].
Conclusiones
La hidrometalurgia del zinc es una alternativa más sostenible en comparación con la pirometalurgia tradicional, gracias a su capacidad para procesar minerales complejos y de baja ley, reducir emisiones de gases contaminantes y reutilizar subproductos, lo que contribuye significativamente al desarrollo de una economía circular. La incorporación de procesos innovadores como la extracción por solventes y la recuperación de hierro elemental fomenta la reutilización y el reciclaje de recursos, optimizando el uso de materiales y reduciendo la generación de residuos peligrosos, como la jarosita, en las operaciones metalúrgicas.
El reciclaje de zinc a partir de materiales secundarios, como chatarra electrónica, baterías gastadas y residuos siderúrgicos, se posiciona como una estrategia clave para satisfacer la creciente demanda global, aportando beneficios significativos como la reducción del consumo energético en un 75 % respecto a la producción primaria y una disminución de las emisiones de CO2 en un 40 %. Con una demanda global proyectada de hasta 28 millones de toneladas anuales de zinc para 2050, esta revisión resalta la necesidad de desarrollar tecnologías más eficientes y sostenibles que permitan gestionar la disponibilidad de recursos primarios y secundarios, asegurando el equilibrio entre el desarrollo industrial y el cuidado ambiental.











 nueva página del texto (beta)
nueva página del texto (beta)