Introducción
En las últimas décadas, se han incrementado los casos de infertilidad humana, afectando a más de 70 millones de personas a nivel mundial, se ha reportado que un 20% de los que se presentan en el género masculino como causa única, y un 50% asociado al género femenino1. Sin embargo, la Organización Mundial de la Salud (OMS) refiere que la prevalencia de infertilidad masculina sigue en aumento llegando a un 50% de los casos2,3.
La infertilidad es un problema médico y social que afecta al 15% de parejas en el mundo y puede afectar tanto a hombres como mujeres5. La infertilidad se refiere a la incapacidad de lograr un embarazo en el lapso de un año, en parejas con vida sexual activa y sin el uso de métodos anticonceptivos. El hombre es considerado como factor único del problema de infertilidad en un 30% de los casos, de los 186 millones de personas infértiles, más de la mitad son pacientes masculinos6,7. Para que la fertilidad sea normal intervienen muchos procesos fisiológicos en los que participan diferentes sistemas, por ejemplo, endocrino, nervioso, e inmunológico, etc., los cuales ayudan a llevar a cabo la espermatogénesis de manera correcta y por ende observar una buena calidad espermática. Existen muchos factores que pueden afectar la calidad del semen y con ello, afectar la fertilidad masculina. Dentro de los factores de riesgo asociados a la infertilidad están los estilos de vida que promueven sobrepeso, obesidad, estrés, ansiedad, así como la exposición a agentes infeccioso2,4. Sin embargo, el estrés crónico es uno de los factores que ha sido poco estudiado.
En esta revisión, nos enfocaremos en estudiar el factor nutricional y el estrés, debido a que diversas enfermedades están en parte provocadas por malos hábitos nutricionales o trastornos alimentarios que han sido asociados a patologías metabólicas, cardiovasculares, etc.; ello debido al papel esencial de los nutrientes en el sistema neuro-inmuno-endocrino8,9,10. De acuerdo con la Organización Mundial de la Salud, la mayoría de las enfermedades podrían prevenirse con un estilo de vida dietético saludable, incorporando en nuestra dieta alimentos que contengan nutrientes tales como triptófano, vitamina B6, vitamina B12, ácido fólico (folato), fenilalanina, tirosina, histidina, colina y ácido glutámico, por mencionar algunos, son necesarios para la producción de neurotransmisores como la serotonina, la dopamina y la norepinefrina, que están involucrados en la regulación del estado de ánimo, el apetito y la cognición11,12. Con relación al impacto de la nutrición sobre la infertilidad, se ha descrito que la deficiencia o exceso de nutrientes esenciales en la dieta puede afectar la salud y el funcionamiento de los órganos reproductivos, lo que puede llevar a problemas de fertilidad. Por otro lado, un exceso de peso y una dieta poco saludable también pueden afectar la fertilidad. Se ha demostrado que el sobrepeso y la obesidad reducen la fertilidad tanto en hombres como en mujeres8,13,14.
Con relación al estrés como factor de riesgo de infertilidad, este se puede definir como alteraciones físicas y psicológicas que desequilibran el balance homeostático, estos factores que cambian o afectan dicha homeostasis se llaman estresores y dependiendo de la intensidad de estos es como se generara una respuesta ante dicho estimulo15. El estrés puede ser agudo o crónico, por un lado, el estrés agudo es único y la exposición es en tiempo limitado, mientras que el estrés crónico es prolongado o de exposición continua durante un largo periodo16,17. Se ha considerado al estrés agudo como un estrés “bueno” o adaptativo ya que se refiere a aquellas respuestas fisiológicas de experiencias relacionadas a enfrentar un estímulo estresante para asumir un riesgo que finalmente resuelve de manera exitosa una situación, a diferencia del estrés crónico que es un estrés “negativo” o al que no podemos adaptarnos debido a que al estar expuesto a estos estímulos estresores durante un largo periodo desencadenan diversos tipos de respuestas neuro-inmuno-endocrinas, que si no se controlan pueden afectar directamente a distintos órganos o descontrolar ciertas funciones fisiológicas18. Dichos estímulos estresores activarán una serie de reacciones que involucran respuestas conductuales y fisiológicas (nerviosas, metabólicas y neuroendocrinas) que permite al organismo responder frente al estresor lo mejor posible19,20. El estrés propicia la activación del eje hipotalámico-pituitario-adrenal (HPA), el cual ejerce una inhibición sobre el eje hipotalámico-pituitario-gonadal (HPG), afectando la esteroidogénesis y suprimiendo la espermatogénesis debido a los bajos niveles de testosterona, generando alteraciones morfológicas y funcionales sobre las células de Sertoli, y la barrera hematotesticular21. Estudios realizados en humanos han demostrado que el estrés genera disminuciones significativas en el conteo espermático, morfología y motilidad, lo que contribuye a una condición de infertilidad21.
A nivel celular y molecular, la generación de especies reactivas de oxígeno (ROS), tienen efectos tanto positivos como negativos sobre la función reproductiva. Las ROS, específicamente H2O2 son necesarias para la capacitación de los espermatozoides mediante la producción de monofosfato de adenosina cíclico (AMPc) que inhibe la tirosina fosfatasa provocando así la fosforilación de la tirosina, de esta forma se estimula la capacitación espermática, este mecanismo también modula la reacción acrosomal, la hiperactivación; además promueve la unión de la membrana del espermatozoide a la proteína ZP-3 de la zona pelúcida necesario para la fusión del espermatozoide con el ovocito, por lo tanto, las ROS desempeñan mecanismos importantes para el proceso de fertilización y reproducción en el hombre22,23,24,25,26,27,28. Los mecanismos pueden ser negativos, debido principalmente a que la membrana de los espermatozoides es rica en ácidos grasos poliinsaturados, por lo que se vuelven aún más susceptible al ataque de ROS. La producción excesiva de ROS de igual forma puede desencadenar apoptosis mediante la activación de caspasas o causar daños directamente en el ADN, generando roturas al ADN, enlaces cruzados y/o reordenamientos cromosómicos, que a su vez se asocia con infertilidad o defectos genéticos hereditarios29,30,31,32,33.
En la actualidad los estilos de vida del hombre moderno pueden estar asociados con una mala nutrición y con el aumento de estímulos estresores que pueden estar impactando de manera significativa en la fertilidad masculina, por lo que el objetivo de la presente revisión sistemática es analizar las evidencias científicas asociadas a los efectos de la suplementación nutrimental con el estrés y la infertilidad masculina.
Materiales y métodos
El presente estudio fue realizado siguiendo los lineamientos y criterios de la guía PRISMA 2020 para revisiones sistemáticas. Para la búsqueda de información sistemática, se utilizaron las bases de datos PubMed, Cochrane y Redalyc durante el periodo de diciembre de 2019 a enero de 2023, las palabras clave utilizadas en la búsqueda fueron “infertilidad masculina” o “male infertility”, “estrés fisiológico” o “physiological stress”, “nutrición o nutrition”, “fertilidad o fertility” validadas en el MeSH del NCBI, así como los operadores booleanos “and (y)” e “or (o)”.
Los criterios de inclusión consideraron artículos en inglés que incluyeran la población de estudio y la temática de interés, así como estudios epidemiológicos y ensayos clínicos que fueran textos completos gratuitos no mayores de 5 años de antigüedad y que fueran en adultos jóvenes.
Los criterios de exclusión consideraron la eliminación de los artículos de metaanálisis, revisiones, revisiones sistemáticas, libros, capítulos de libros, así como artículos que no fueran de libre acceso, además después de la revisión del título se analizó minuciosamente el contenido del texto completo de la literatura restante.
Los criterios de exclusión aplicados a los artículos: títulos sin relación con el contenido, que no tuvieran las palabras clave y estudios realizados en población adulta, artículos con pacientes con comorbilidades derivados de la infertilidad o asociados a otra enfermedad, estudios de ciencias básicas; discusiones clínicas, recomendaciones y guías, artículos sin resultados de pacientes informados. Los resúmenes de los artículos se revisaron y analizaron de manera independiente por los autores para seleccionar los más relevantes. La discrepancia fue discutida por los autores y finalmente, la inclusión y exclusión de artículos se acordó por unanimidad para someterlos al instrumento de calidad.
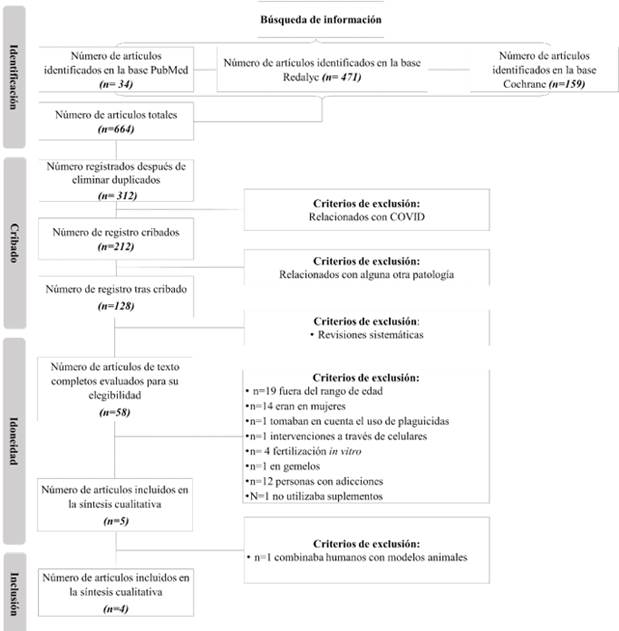
En la figura 1, se observa el diagrama de flujo de búsqueda de información y cribado. Los buscadores utilizados para realizar nuestra búsqueda fueron PubMed, Redalyc y Cochrane. En estos buscadores, al implementar la declaración PRISMA, se obtuvieron 664 artículos. Tras excluir duplicas, el total fue de 312. Se procedió a eliminar aquellos relacionados al COVID, se eliminaron 100 artículos. También, se limitaron a aquellos que no estuvieran relacionados con alguna otra patología como diabetes, hipertensión, cáncer, enfermedades cardiacas, etc.; teniendo así, un total de 128 artículos. De ellos, se eliminaron 70 artículos más que correspondían a revisiones sistemáticas. Finalmente, se aplicaron los criterios de inclusión y exclusión, resultando en un total de 4 artículos. Los motivos para la exclusión fueron: 19 artículos estuvieron fuera del rango de edad pues eran niños y adultos mayores, 14 evaluaban el impacto de la fertilidad en mujeres, 1 tomaban en cuenta el uso de plaguicidas, 1 no utilizaba algún suplemento, 1 era una intervención a través de celular, 4 fueron fertilizaciones in vitro, 1 estaba diseñado en gemelos, 12 eran pacientes infértiles, pero con adicciones y 1 más estaba diseñado en un modelo combinado.
Resultados
Posterior al proceso de cribado, a los artículos seleccionados se les evaluó su calidad siguiendo los criterios de Yepes-Núñez y colaboradores,38 los resultados mostraron que solo un artículo es de calidad baja, 1 de los artículos es de calidad media y los otros 2 son de calidad alta. se procedió a la revisión del texto completo de los 4 artículos que fueron seleccionados 34,35,36,37.
Evidencias del impacto de la nutrición en la fertilidad masculina
Los estudios que se incluyeron en esta revisión sistemática se muestran en la tabla 1. De manera general, podríamos decir que, a pesar de obtener una amplia gama de artículos disponibles en la modalidad de libre acceso, la gran mayoría se asocia a otras patologías asociadas que condicionaban la infertilidad por lo que al final solo 4 artículos fueron considerados para esta investigación. No obstante, es evidente el interés que existe por saber la implicación que tiene la nutrición en la regulación de procesos endocrinológicos que a su vez se relacionan con los efectos derivados del estrés fisiológicos.
Tabla 1 Características de los artículos incluidos
| AUTOR AÑO | PAÍS PERIODO TIPO DE ESTUDIO | POBLACIÓN | OBJETIVO | RESULTADOS |
|---|---|---|---|---|
| Eslamian et al; 2020. | Tehran, Iran. Abril 2013 - mayo 2015. Tipo de estudio: Aleatorizado, de doble ciego y ensayo controlado con placebo. | Hombres sanos, voluntarios, diagnosticados con astenozoospermia idiopática, 20 a 45 años, sin hijos no deseados durante ≥1 año con la misma pareja femenina, función endocrina normal y con concentración y porcentaje de espermatozoides morfológicamente normales según la OMS. | Determinar si el aumento de vitamina E mejora la eficacia del DHA para la motilidad del esperma en pacientes con astenozoospermia al reducir la extensión del daño oxidativo. | La motilidad progresiva de los espermatozoides (27.9 ± 2.8), conteo (p = 0.001) y concentración (p = 0.044) espermática aumentaron en el grupo DE (DHA+Vit. E) en comparación con los otros 3 grupos. Las concentraciones séricas de PUFAs aumentaron en los grupos DE y DP (DHA + Placebo) (p<0.05). |
| Busetto et al; 2020. | Roma Diciembre 2014 - junio 2015. Tipo de estudio: Aleatorizado, de doble ciego y ensayo controlado con placebo. | 104 pacientes infértiles con oligo y/o asteno y/o teratozoospermia, entre los 18 y 48 años, pertenecientes a la clínica de Andrología del Departamento de Ciencias Ginecológicas-Obstétricas y Ciencias Urológicas de la Universidad ''Sapienza'' de Roma. Se incluyen 52 pacientes con varicoceles de grado I-III y 52 pacientes sin varicocele. | Evaluar el efecto de la suplementación antioxidante con compuestos naturales seleccionados sobre la calidad del esperma. | Se observó una diferencia significativa en la eficacia de la suplementación para la motilidad total (p = 0.0272) y progresiva (p = .0159) en pacientes con varicocele e IMC < 25. Este estudio sugiere que la suplementación es más efectiva en sujetos con varicocele menores de 35 años con IMC < 25. |
| Kopets et al; 2020. | Ucrania. Septiembre 2018 - abril 2019. Tipo de estudio: Ensayo clínico multicéntrico, aleatorizado, de doble ciego, controlado con placebo, prospectivo, de brazos paralelos (proporción de asignación 1:1). | Pacientes entre los 21 y 50 años, con infertilidad masculina idiopática, oligo y/o asteno y/o teratozoospermia. | Estudiar la influencia de un suplemento dietético de nutrientes con componentes múltiples en los parámetros espermáticos y las tasas de embarazo en la infertilidad masculina idiopática (IMI) con oligo, asteno y teratozoospermia | Todos los varones terminaron el estudio. En el mes 4, 69% varones en el grupo con suplemento tenían espermiogramas normales (p < 0.001). El porcentaje de embarazos espontáneos en el grupo suplementado fue mayor que en el grupo placebo (p= 0.017). |
| Schisterman E et al; 2020. | EE. UU. Junio de 2013 - diciembre de 2017. Tipo de estudio: Ensayo clínico aleatorizado multicéntrico. | La población fue de 2370 parejas (hombres ≥18 años y mujeres de 18 a 45 años) que planeaban un tratamiento de infertilidad. | Determinar el efecto de la suplementación diaria con ácido fólico y zinc sobre la calidad del semen y los nacidos vivos. | Los nacidos vivos no fueron diferentes entre los grupos de tratamiento (34 %) en el grupo de ácido fólico y zinc vs 35 % en el grupo de placebo. Todos los parámetros de calidad espermática no fueron diferentes después de 6 meses. La prueba de permutación para los parámetros de calidad mostró una calidad general del semen más baja en el grupo de ácido fólico y zinc (p=0.03). Se observó un aumento en el índice de fragmentación del ADN con suplementos de ácido fólico y zinc en general 29.7% vs 27.2% para el grupo de placebo. |
Fuente: Elaboración propia
El artículo de Eslamian y colaboradores en el 2020, reportan que existen diversas enzimas, antioxidantes y lípidos en el semen que participan y juegan un papel importante en la fertilidad masculina. Particularmente demuestran que el consumo de la vitamina E combinando con ácido docohexanoico (DHA) (465 mg DHA y 600 IU vitamina E) mejora el conteo total espermático (p=0.002), así como la concentración (p <0.001) y movilidad (p=0.002) espermática. No obstante, el consumo aislado tanto de DHA como de vitamina E, también tienen un efecto benéfico en el conteo (p=0.006; p<0.001, respectivamente), la concentración (p<0.001, para ambos casos) y movilidad espermática (p=0.002; p<0.001, respectivamente). Con ello, se puede establecer que la combinación de ambos suplementos en dosis efectivas, tienen una fuerte influencia en el mejoramiento de la calidad espermática.
Además, en el mismo año (2020), Busetto y colaboradores, también demuestran que utilizar un suplemento compuesto (1000 mg de L-carnitina, 725 mg de fumarato, 500 mg de acetil-L-carnitina, 1000 mg de fructosa, 50 mg de ácido cítrico, 50 µg de selenio, 20 mg de coenzima Q10, 90 mg de vitamina C, 10 mg de zinc, 200 µg de ácido fólico y 1,5 µg de vitamina B12) mejora el conteo espermático total (p<0.0001), aun cuando sean pacientes con varicocele (p=0.006). De la misma manera, se incrementó la movilidad progresiva tanto en los grupos suplementados, como en los suplementados con varicocele (p=0.0012, p=0.0311; respectivamente). Los efectos más evidentes fueron en el grupo con varicocele, pero con un IMC <25, tanto para el conteo espermático total (p=0.0272) como para la movilidad progresiva (p=0.0159). Con todos estos datos podríamos inferir que la suplementación con antioxidantes parece ser efectiva en mejorar diversos aspectos de la calidad espermática pero solo en personas con menos de 35 años y con un IMC <25.
En el estudio de Kopets y colaboradores (2020), utilizando una sola pastilla de 12 Kcal, con 1990 mg L-carnitina/L-acetil-carnitina, 250mg L-arginina, 100mg de glutatión, 40mg coenzima Q10, 7.5 mg zinc, 234mcg vitamina B9, 2mcg vitamina B12, 50mcg selenio, así como excipientes de sorbitol, maltodextrina, colorante naranja/betacaroteno, sacárido, acesulfame de potasio y dióxido de silicio; muestran que el consumo de estos antioxidantes tiene un efecto positivo en todos los parámetros del espermiograma, a los 2 o 4 meses de tratamiento, excepto por la morfología que en el segundo mes no hubo diferencias significativas. De igual manera, el estudio de Williams y colaboradores en el 2020, demostraron que el suplemento con lactolicopeno para tratar de mejorar la calidad espermática, aumenta significativamente el porcentaje de espermatozoides con movilidad progresiva (p=0.006) y el porcentaje de espermatozoides con morfología normal (p<0.001) pero no hubo diferencias significativas en el porcentaje de espermatozoides con daño al ADN.
En contraste con estos estudios, en esta revisión se encontró un solo artículo que muestra que la suplementación diaria combinada de zinc y ácido fólico durante 6 meses, como posible tratamiento contra la infertilidad en varones, no mejora la calidad espermática ni la tasa de bebes nacidos vivos. Además, los parámetros de la calidad del semen, la concentración de espermatozoides, la motilidad, la morfología y el conteo total de espermatozoides móviles fue más baja en el grupo que consumió ácido fólico y zinc (p=0.03) y con relación al índice de fragmentación, no hubo diferencias entre los grupos (Schisterman y cols. 2020).
Evidencias del impacto del estrés en la fertilidad
Se ha reportado que, dentro de los múltiples factores de mayor relevancia, debido a su prevalencia epidemiológica, que pueden afectar la fertilidad están la nutrición y el estrés por separado y que, en conjunto suman para afectar principalmente la calidad espermática. Sin embargo, en esta revisión sólo encontramos una evidencia científica sobre los efectos del estrés puberal en la fertilidad en un modelo animal de rata. Al respecto, el estudio de Hernández y colaboradores en el 2020 demuestra que el grupo estresado por aislamiento social tuvo una menor motivación sexual, bajos niveles séricos de testosterona y mayor actividad electroencefalográfica en la amígdala en ratas macho en presencia de una hembra receptiva, aunque el grupo control sin estrés no tuvo una mayor actividad prefrontal.
Discusión
La calidad espermática puede estar influenciada por diversos factores, como la nutrición y el estrés. Una dieta equilibrada y saludable puede mejorar la calidad del esperma, mientras que una dieta poco saludable y el sobrepeso pueden reducirla. Por otro lado, el estrés fisiológico puede tener un impacto significativo en la nutrición y la salud. En respuesta al estrés, el cuerpo libera hormonas como el cortisol, que pueden aumentar el apetito y la ingesta de alimentos ricos en grasas y azúcares. Además, el estrés también puede afectar la absorción y el metabolismo de los nutrientes, lo que puede tener consecuencias negativas para la salud a largo plazo. Además, el estrés oxidativo generando por el estrés fisiológico no controlado, también afecta de manera negativa calidad del esperma, lo que puede resultar en daño celular y reducir la fertilidad. Por lo tanto, es importante mantener una dieta saludable, hacer ejercicio regularmente, reducir el estrés, para prevenir los efectos negativos de la nutrición y el estrés en la fertilidad. Aunado a ello, es importante consultar a un especialista en fertilidad en caso de tener problemas para concebir para identificar el problema específico y buscar una solución.
Este estudio sistemático, sugiere que el uso de suplementos dietéticos elaborados a base de diferentes nutrientes puede coadyuvar en mejorar la fertilidad en hombres, específicamente los parámetros de calidad espermática y con ello el aumento de la probabilidad de embarazo en sus parejas respectivamente38. Con la información obtenida, se demuestra que una dieta mediterránea en conjunto con ejercicio moderado puede mejorar tanto los parámetros espermáticos como la capacidad antioxidante en hombres sanos. Sin embargo, esto no define la capacidad de fertilización, por ello se han realizado estudios que muestran la efectividad el uso de un suplemento conformado con L-carnitina, L-arginina, glutatión, zinc, ácido fólico, etc., que además de mejorar la calidad espermática en hombres con infertilidad idiopática, aumentó la tasa de embarazo39. Existen otros factores que pueden influir en la fertilidad masculina tales como la edad y el peso, en el estudio de Busetto y cols. (2020), evaluaron la eficacia de un suplemento rico en antioxidantes relacionado al índice de masa corporal (IMC) y la edad. Los resultados mostraron que los hombres menores de 35 años y con un IMC <25 tuvieron una mejor respuesta a la suplementación. Por otro lado, resultados contradictorios obtuvieron Schisterman y cols. (2020) quienes aplicaron una suplementación combinada de ácido fólico con zinc en hombres, en los que no se observó una mejoría ni en la calidad del semen ni en la tasa de nacidos vivos de sus respectivas parejas.
El estrés es un factor de importancia dentro de las causas de infertilidad en hombres, se sabe que propicia alteraciones hormonales y modifica el comportamiento sexual al generar alteraciones en la funcionalidad cerebral. Las hormonas sexuales juegan un importante papel en la maduración sexual, la testosterona está involucrada en cambios morfológicos durante este proceso, por lo cual niveles bajos de esta hormona durante la pubertad genera una disminución de la motivación sexual38. A nivel cerebral existen regiones que son sensibles a los niveles de hormonas, el área prefrontal y la amígdala poseen receptores a andrógenos, se ha demostrado que durante el cortejo sexual la activación de estas regiones es un factor clave para la ejecución de las conductas sexuales, una disminución en los niveles de andrógenos podrías estar disminuyendo la actividad cerebral haciendo que los animales estresados pierdan el interés hacia las hembras receptivas afectando su fertilidad4,40.
Sin duda alguna existen suplementos nutricionales y antioxidantes que pueden mejorar la calidad espermática, pero es importante consultar a un profesional de la salud antes de utilizarlos. El impacto de la nutrición y el estrés psicológico sobre la fertilidad son dos de los factores en los que dichas investigaciones han abordado su interés41. Se ha estudiado que el estilo de vida influye de manera positiva o negativa en la calidad del semen y con ello aumentar la probabilidad de éxito de embarazo39. Sin embargo, la información disponible aún sigue siendo limitada, lo que evidencia la necesidad de realizar más estudios que aborden esta problemática y que en un futuro forme parte de aplicaciones clínicas.
También es importante remarcar que nuestros resultados respaldan como estos estudios pueden influir en políticas de salud pública y prácticas clínicas. En términos de política, a través de la prevención primaria de la infertilidad masculina, basándose en la identificación de nutrientes específicos que reduzcan el impacto del estrés sobre la fertilidad y esto a su vez, nos llevaría a implementar programas de suplementación poblacional. Por otro lado, en la práctica clínica, se podrían desarrollar protocolos de tratamiento personalizados con un enfoque integral en la salud reproductiva masculina, incluyendo estrategias para reducir el estrés fisiológico.
Conclusión
El análisis mostró que el uso de suplementos alimenticios coadyuva en mejorar la calidad espermática y por ende la fertilidad masculina. Sin embargo, esto depende del tipo de nutrientes, ya que el suplemento con ácido fólico y zinc no mejora la fertilidad masculina. El estrés es un factor importante que afecta la conducta sexual, por lo que el uso de suplementos alimentarios que disminuyan el estrés podría coadyuvar en disminuir la infertilidad masculina. De igual manera, deben tomarse en cuenta otros factores como el estilo de vida, edad, peso, patologías, uso de medicamentos, entre otros, para poder brindar de manera integral más información para futuros posibles tratamientos para mejorar la infertilidad masculina.











 nueva página del texto (beta)
nueva página del texto (beta)