Introducción
El trastorno del espectro autista (ASD, por sus siglas en inglés) es un trastorno del neurodesarrollo caracterizado por dificultades en la comunicación e interacción social, así como por comportamientos e intereses repetitivos, restringidos y estereotipados.1 La manifestación de síntomas varía en cada paciente, es por ello que se define como “espectro” para enfatizar el alcance de sus dimensiones. El autismo incluye al síndrome de Asperger, al trastorno generalizado del desarrollo no especificado, síndrome de Rett, entre otros.2 Pero para el Manual Diagnóstico y Estadístico de los Trastornos Mentales versión V (DSM-V) todos estos trastornos pasan a englobarse bajo el término ASD, y dividiéndose en tres grados de severidad.3
La mayoría de casos son de naturaleza idiopática, presentando una etiología específica en sólo el 5 a 10% de casos.4 Cuenta con una prevalencia de 1 a 2% en la población mundial.5 La ausencia de marcadores biológicos ha sido un obstáculo para la innovación de tratamientos, por lo que existen escasos tipos, particularmente en la población de 13 a 30 años.5 Se han realizado estudios post mortem de neuroimagen, los cuales han demostrado un desarrollo cerebral atípico; de igual modo, existen múltiples factores genéticos y ambientales asociados. No obstante, se ha logrado un avance en los fundamentos neuroanatómicos, estableciendo los componentes neurales que subyacen a él, abarcando áreas como regiones frontotemporales y frontoparietales, partes de los ganglios basales, y la corteza prefrontal dorsolateral (DLPFC, en inglés).2
Hasta la actualidad, los tratamientos conductuales y farmacológicos se han encaminado a reducir los síntomas de comorbilidades asociadas con el ASD, como la catatonia y depresión. De modo que no existe tratamiento farmacológico que sea efectivo para los síntomas centrales.2 Es debido a la falta de tratamientos que se han realizado investigaciones basadas en los nuevos avances tecnológicos, las cuales proporcionen a los pacientes con ASD nuevas alternativas de tratamiento.
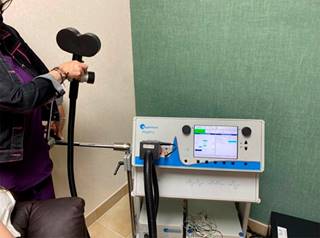
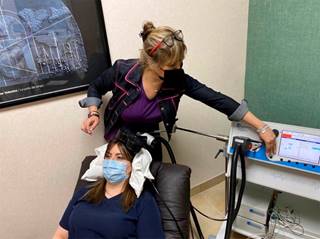
La estimulación magnética transcraneal (TMS) es una técnica no invasiva para la modulación cerebral usada en diferentes enfermedades y trastornos neurológicos y psiquiátricos. Existen varios tipos según los parámetros utilizados: estimulación magnética transcraneal repetitiva (rTMS), theta burst y directa.6 También se dividen de acuerdo con su frecuencia, en baja frecuencia (1 Hz) y alta frecuencia (5 Hz en adelante). Se considera que la de baja frecuencia puede producir una disminución en la excitabilidad corticoespinal; mientras que la alta, genera un aumento de la misma.7 Además, la TMS produce alteración en la plasticidad sinóptica y la potenciación o depresión a largo plazo para producir efectos neurales duraderos.8
En la TMS en ASD se han propuesto diferentes estructuras anatómicas, pero la más importante parece ser la DLPFC para tratar la depresión y mejorar funciones ejecutivas. Estudios previos han demostrado que la rTMS de baja frecuencia sobre la DLPFC podría mejorar los comportamientos repetitivos y modular las funciones ejecutivas en niños, adolescentes y adultos con ASD, mientras que los efectos terapéuticos sobre los déficits sociales son no concluyentes.5
En el presente artículo se discutirá sobre los ensayos clínicos realizados en los últimos años sobre los efectos que tiene la TMS en los pacientes con ASD, y los resultados que se han obtenido en relación al mejoramiento de las estructuras y funciones cerebrales.
Material y métodos
Se realizó una búsqueda de la literatura en PubMed y Google Académico durante el periodo de 2017 a 2022, mediante los términos “transcranial magnetic stimulation”, “autism spectrum disorder”, “autism”, “ASD” y “TMS”. Estos términos fueron combinados con los operadores booleanos AND y OR. Se emplearon las normativas establecidas en las directrices para conducción de estudios observacionales (STROBE). Se incluyeron estudios de pacientes diagnosticados con ASD, de acuerdo con los criterios del manual DSM-IV y DSM-V, cuyo tratamiento consistió en la aplicación de TMS, los cuales incluyeran resultados medibles mediante una escala clínica validada. Los artículos fueron revisados de forma independiente por dos investigadores, quienes se encargaron de evaluar la calidad metodológica de los ensayos clínicos controlados de forma simultánea. Se seleccionaron los estudios que cumplieron con: artículos “originales” en inglés, correspondientes a ensayos clínicos realizados en humanos con ASD, sin comorbilidad. Se excluyeron los estudios piloto y estudios con muestras menores a 10 participantes.
Resultados
La búsqueda combinada, eliminando los artículos duplicados, arrojó un total de 104; tras la evaluación detallada, se seleccionaron siete estudios que informaron datos suficientes para el análisis (Figura 1). Se identificaron 181 casos procedentes de seis países distintos. El tiempo de evolución del tratamiento de TMS fue aproximadamente de seis meses.2,5-10
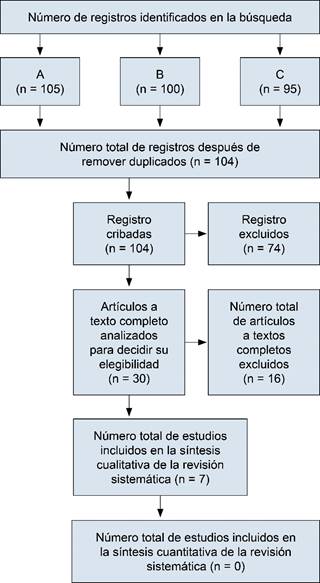
Figura 1: Esquema tipo STROBE que se utilizó para esta revisión sistemática. Búsqueda A con 105, búsqueda B con 100 y búsqueda C con 95.
Los artículos fueron analizados de acuerdo al año de publicación, número de pacientes incluidos, diagnóstico de base, parámetros de estimulación, resultados medidos con algún instrumento psicométrico y sus efectos colaterales. Se encuentran descritos en la Tabla 1.
Tabla 1: Síntesis de resultados obtenidos de los estudios seleccionados.
| Nombre | Año | Autor | n | Criterios de inclusión | Parámetros | Resultados | Efectos colaterales |
|---|---|---|---|---|---|---|---|
| Non-invasive brain stimulation for children with autism spectrum disorders: a short-term outcome study | 2017 | Gómez L, et al | 24 | ASD Niños > 10 años ADI-R y CARS, sin epilepsia recurrente |
rTMS, DLPFC, L izquierdo 90% 1 Hz, 1,500 pulsos por sesión dividido en 4, 375 pulsos con intervalo de 1 min, 20 sesiones | ABC: Z = 3.823, p = 0.0001 ADI: Z = 3.3337, p = 0.0008 ATEC: Z = 3.723, p = 0.0002 Wilcoxon test Sin diferencia entre rTMS y tDCS Reducción en conducta repetitiva y restrictiva Efectos por 6 meses Aumentó la actividad gamma según el EEG CCPT pre: 101.69, post: 57.90 |
Sin efectos adversos |
| The impact of single session intermittent theta-burst stimulation over the dorsolateral prefrontal cortex and posterior superior temporal sulcus on adults with autism spectrum disorder | 2017 | Ni H, et al | 25 | ASD, Asperger PDD-NOS 18-29 años |
Bilateral DLPF pSTS, 80%, 50 Hz, 600 pulsos, 20 veces cada 10 s |
WCST Pre: 12.53, post: 11.21 Perseveración y errores decrecieron en DLPFC, pero aumentaron en pSTS Y-BOCS Obsesiones Pre: 3.89, post: 2.27 Compulsiones Pre: 3.25, post: 1.56, disminuyeron en pSTS SRS sólo decreció la subescala de comunicación social 8 horas después |
Contracciones musculares alrededor de los ojos |
| Intermittent theta-burst transcranial magnetic stimulation for autism spectrum disorder: an open-label pilot study | 2018 | Abujadi C, et al | 10 | ASD 50 puntos mínimos en la escala WISC-III, EEG y MRI normales |
DLPFC derecha 100%, por 300 s, con dadas a 5 Hz en 30 trenes de
10 ráfagas con 8 s encendido y 2 s apagado 15 sesiones |
RBS-R Pre: 27.40, post: 13.30 WSCT Wilcoxon test, p = 0.02, Cohen’s d = 0.54, disminuye perseveración Test de Stroop Pre: 97.30, post: 17.33 Y-BOCS Subescala de compulsión: pre: 0.30, post: 8.50 |
Sin efectos adversos |
| Study of the effect of repetitive transcranial magnetic stimulation on a sample of children with autism spectrum disorder | 2019 | Abd Alrahman AI, et al | 30 | Niños de 4 a 10 años, diagnostica dos con ASD CARS |
rTMS, DLPFC izquierda 90%, 1 Hz, 6 sesiones | CARS Post: 31.4, pre: 40,2 Mejora en severidad de síntomas clínicos |
Sin efectos adversos |
| Treatment of Executive Function Deficits in autism spectrum disorder with repetitive transcranial magnetic stimulation: A double-blind, sham-controlled, pilot trial | 2020 | Ameis SH, et al | 40 | 16 a 35 años ASD CI de 70 (WAIS-IV) |
rTMS, PFDL, Sham 90% 20 Hz, 20 sesiones, 4 semanas |
BRIEF-MCI score Prueba exacta de Fisher p < 0.0001 No hubo diferencias significativas entre la rTMS activa y la sham en el rendimiento de la función ejecutiva |
Efectos adversos leves o moderados |
| The sensory abnormality mediated partially the efficacy of repetitive transcranial magnetic stimulation on treating comorbid sleep disorder in autism spectrum disorder children | 2021 | Gao L, et al | 39 | 2 a 18 años ASD | rTMS DLPFC izquierda a 10 Hz DLPFC derecha a 1 Hz Ambas a 25% diario 8 semanas 32 s, 32 veces |
CSHQ: pre: 4.59, post: 6.26 RBQ-2: F = 2.425, p = 0.093 SSP: pre: 4.88, post: 6.52, cambios en sensibilidad táctil y filtrado auditivo F = 6.345, p = 0.003 SDQ: pre: 2.65, post: 4.83, sin cambios en las subescalas de hiperactividad, inatención y problemas con sus pares |
Sin efectos adversos |
| 5-day multi-session intermittent theta burst stimulation over bilateral posterior superior temporal sulci in adults with autism-a pilot study | 2022 | Ni HC, et al | 13 | 25 participantes mayores de 18 años, ASD No comorbilidad |
Theta burst DLPFC Surco posterior superior temporal 80% 3 pulsos 50 Hz Una semana de intervalo entre cada sesión |
Sin cambios significativos entre pSTS vs sham Sin cambios significativos en el total de WCST Tampoco AQ-padres o AQ-paciente |
Tres participantes presentaron espasmos musculares alrededor de los ojos. Ningún otro efecto adverso |
rTMS = estimulación magnética transcraneal repetitiva. tDCS = estimulación de corriente directa. ABC = autism behavior checklist. ATEC = autism treatment evaluation checklist. ADI = autism diagnostic interview. CCPT = Conner’s continuous performance test. STSP = surco temporal superior-posterior. WCST = Wisconsin card sorting test. DLPC = dorsolateral prefrontal cortex. SRS = social responsiveness scale. RBS-R = repetitive behavior scale revised. Y-BOCS = Yale brown obsessive compulsive scale. CSHQ = children’s sleep habits questionnaire. RBQ-2 = repetitive behavior questionnaire. SSP = short sensory profile. SDQ = strengths difficulties questionnaire.
En el estudio de Gómez y colaboradores compararon la TMS y la TDCS en la DLFC sin una diferencia significativa entre ambas.9
En el estudio de Abujadi, Croarkin, Bellini asociados se comprobó si era viable la rTMS por 15 sesiones diarias, habiendo reducción en todas las escalas, pero en el postest (tres meses después), los sujetos volvieron a subir en síntomas en todas las escalas.10
En el estudio de Gao y su grupo se aplicó estimulación en niños con ASD y con comorbilidad de trastorno del sueño, habiendo disminución en la resistencia para acostarse, ansiedad ante el sueño y somnolencia durante el día, parasomnias y sonambulismo, pero no hubo mejoría en respiración alterada durante el sueño y retraso en el inicio del sueño. Mencionan que la estimulación sería un tratamiento más eficaz que los actuales tratamientos conductuales, ya que los problemas de sueño en esta población se deben a una producción disregular de melatonina, a la organización de sus ondas cerebrales, a los genes del ritmo circadiano, entre otros.6
Los límites de este estudio es que existen pocos artículos con información homogénea, lo que redunda en una población pequeña. Adicionalmente, son pocos los estudios con diseño de ensayo aleatorizado y cegado y pocos correlatos neurofisiológicos. Debido a la heterogeneidad presentada en los resultados, no se empleó estadística inferencial, por lo que nuestro estudio se limita a la descripción de las características demográficas, variables de estimulación, áreas anatómicas estimuladas y los resultados clínicos obtenidos.
Variables
La mayoría de los protocolos de TMS (Figuras 2 y 3) se realizaron mediante alta frecuencia;5-8,10,11 sólo tres estudios aplicaron baja frecuencia;2,6 la rTMS fue la más utilizada,2,5,6,9 siguiendo la theta-burst.7,8,10 El número total de sesiones osciló entre seis y 32, con un tiempo de duración variable según el número de pulsos, variando desde 600 a 4,375 pulsos por sesión; la intensidad osciló entre 80 y 90% del umbral motor. En todos los ensayos clínicos se proporcionaron las evaluaciones clínicas y cognitivas. Además, los pacientes recibían alternadamente tratamiento farmacológico y/o conductual.2,5-10
Escalas de evaluación y medición de resultados
Se emplearon diferentes escalas clínicas para medir hiperactividad, inatención, patrones en conducta repetitiva, restrictividad, irritabilidad, aspectos sociales de comunicación y otros síntomas clínicos del ASD.2,5-10 Algunas de las escalas más utilizadas fueron la escala obsesiva compulsiva de Yale Brown (Y-BOCS) y la escala de evaluación del autismo infantil (CARS).2,5-10 Estas dos escalas se emplearon como referente comparativo, independientemente de que no fueran las variables de salida principales. Los resultados en la subescala de errores de comisión no son estadísticamente significativos, es así que los resultados de los estudios no son homogéneos entre sí, de modo que no se presentan resultados concluyentes.
Discusión
En los artículos recabados no hay parámetros concluyentes que permitan llevar a lo clínico estos resultados, ya que existen diferentes factores que lo impiden: el más frecuente es la población pequeña de cada estudio; otro factor es la amplia heterogeneidad del espectro o diferencias estructurales y funcionales de cada paciente. Los parámetros más utilizados fueron de 1, 5, 20 y 50 Hz.
Otros factores limitantes fueron los tratamientos concomitantes que cada estudio llevó (terapias conductuales) y los fármacos neuroactivos. Además de falta de sham (grupo control o placebo) en el diseño experimental y la severidad de disfuncionalidad no es considerada.
Se aprecia ausencia o brevedad del seguimiento después de la estimulación. Para futuras investigaciones, es necesario tomar como variable el sexo de los sujetos al ser posible que en el ASD existan alteraciones etiológicas y neurobiológicas dependiendo de éste.12 A su vez, la presentación conductual del ASD y las características cognitivas relacionadas, incluidas las funciones ejecutivas, difieren en parte en mujeres frente a hombres. Según el estudio de Ameis y colaboradores, las mujeres respondieron mejor que los hombres a la estimulación en función ejecutiva, por lo que se debe proponer una línea de investigación de ASD con TDAH y de su tratamiento farmacológico con el potencial de influenciar las funciones ejecutivas.5
Los protocolos theta burst tienden a ser excitatorios, mientras los de rTMS inhibitorios y se ha demostrado que ambos tienen efectos que no son observables en conductas, pero sí a la hora de aplicar tests neuropsicológicos.13
Sin embargo, es indudable que hay beneficios tanto en la rTMS de alta frecuencia como de baja frecuencia. Los sujetos con ASD muestran una respuesta facilitadora a la estimulación theta-burst continua en la niñez y pubertad, pero se vuelve inhibitoria conforme maduran, proceso que llega a su pico a los 21 años.1
Cabe volver a señalar que, en todos los estudios revisados, al igual que en Sokhadze y colaboradores, en donde hay una menor mejoría es en el aspecto social y menos cuando ya hay un deterioro significativo, sobre todo en adultos autistas.13











 nueva página del texto (beta)
nueva página del texto (beta)