Introducción
En México, las plantaciones de Theobroma cacao forman un agroecosistema arbolado, debido a la diversidad de plantas que se asocian a este cultivo (Oporto et al., 2015). Estas plantaciones se encuentran establecidas en el sureste de México, donde se cultivan 52,449 ha. La mayor superficie sembrada se encuentra en el estado de Tabasco con 34,266 ha, distribuidas en 10 municipios (SIAP, 2023). De acuerdo con Rice y Greenberg (2000) y Torres-de la Cruz y Ortiz-García (2019), este agroecosistema provee servicios ambientales y contribuye de forma importante a conservar la biodiversidad.
En el estado de Tabasco, diversos estudios han documentado la biodiversidad presente en los agroecosistemas de cacao, abarcando una amplia gama de grupos biológicos como aves, plantas, anfibios, reptiles, insectos y arañas (de la Cruz-Pérez, 2015; Martínez-López et al., 2011; Pérez-de la Cruz et al., 2009; Muñoz et al., 2005; Córdova-Ávalos et al., 2001; Ibarra et al., 2001; Greenberg et al., 2000). Sin embargo, a pesar de esta riqueza en estudios sobre diferentes taxones, la diversidad fúngica asociada a las patologías del cacao sigue siendo un aspecto poco explorado en la región, con investigaciones limitadas como la de Torres-de la Cruz et al. (2015).
A nivel mundial, los hongos fitopatógenos son considerados entre los factores limitantes de mayor importancia de la producción del cacao (Antolinez-Sandoval et al., 2020). Así, la enfermedad con mayor distribución es la mancha negra, cuyo agente causal son diferentes especies del género Phytophthora; la cual se halla en todos los países que cultivan cacao en el mundo (Kroon et al., 2012). En América se han reportado diversos hongos causantes de patologías en T. cacao: Moniliophthora perniciosa (escoba de bruja), M. roreri (moniliasis del cacao), Phytophthora spp. (mancha negra), Lasiodiplodia theobromae (pudrición café), Ceratocystis cacaofunesta (marchitez), diversas especies de Colletotrichum (antracnosis), Fusarium descemcellulare (bubas), Rizoctonia noxia (Mal de hilachas) y Rosellina pepo (llaga blanca) (Phillips-Mora y Cerda-Bustillo, 2009).
En el estado de Tabasco, el hongo M. roreri causa la enfermedad fúngica que más limita de la producción, después de la mancha negra, causada por P. capsici (Ortiz-García, 1996; Torres-de la Cruz et al., 2020). Diversos trabajos mencionan la presencia de especies fúngicas putativas a patologías de T. cacao en el estado de Tabasco (López-Andrade et al., 1996; Córdova-Ávalos, 2001; Tadeo-Sánchez, 2020); sin embargo, se requieren estudios que confirmen su presencia en este agroecosistema. Por tanto, el objetivo del presente estudió fue caracterizar la diversidad fúngica asociada a patologías de T. cacao en el estado de Tabasco, México. Este trabajo muestra la riqueza de especies fúngicas que pueden encontrarse asociadas a patologías de T. cacao en Tabasco, aportando al conocimiento de la biodiversidad. Además, este trabajo puede servir como referencia para investigaciones futuras sobre patogenicidad, incidencia y severidad de los diversos hongos en el cultivo del cacao en México.
Materiales y métodos
Sitios de muestreos y obtención de material vegetal
Los sitios de muestreo se establecieron en tres subregiones productivas del estado de Tabasco, que concentran los 10 municipios en los que se cultiva T. cacao: Subregión Chontalpa con los municipios Cunduacán, Cárdenas, Comalcalco, Paraíso y Huimanguillo; subregión Centro con los municipios Nacajuca, Centro, Jalpa de Méndez, y la Subregión Sierra con dos municipios Tacotalpa y Teapa. Las localidades y sus referencias geográficas se presentan en la Tabla 1.
Tabla 1 Localidades de muestreo y aislamientos fúngicos asociados a patologías de Theobroma cacao en el estado de Tabasco, México.
Table 1: Sampling localities and fungal isolates associated with Theobroma cacao pathologies in the state of Tabasco, Mexico.
| Municipio | Localidad | Latitud Norte | Longitud Oeste | Aislamientos | Número de aislamientos |
| Jalpa de Méndez | Hermenegildo Galeana 2 | 18° 10' 33.4" | 93° 08' 48.5" | PCT06, PCT05, PCT07, PCT65, PCT68, PCT08. PCT10, PCT11, PCT12 | 9 |
| Cunduacán | La Piedra 1 | 18° 07' 45.2" | 18° 07'45.2" | PCT56, PCT57, PCT59, PCT60, PCT66 | 5 |
| Comalcalco | Finca Cholula | 18° 17' 04.8" | 93° 12' 39.7" | PCT17, PCT18, PCT64 | 3 |
| Cárdenas | Ocampo | 18° 01' 49.3" | 93° 21' 29.7" | PCT01, PCT02, PCT03, PCT63 | 4 |
| Tacotalpa | Zunú y patastal | 17° 28' 10.3" | 92° 50' 56.7" | PCT53, PCT46, PCT49, PCT50, PCT51 | 5 |
| Teapa | Allende | 18° 09' 38.1" | 93° 02' 00.8" | PCT27, PCT28, PCT30, PCT31 | 4 |
| Centro | Plátano y cacao 4 | 17° 59' 04.2" | 93° 10' 07.9" | PCT13, PCT14, PCT15, PCT16, PCT24 | 5 |
| Paraíso | Oriente | 18° 22' 19.3" | 93° 13' 42.4" | PCT34, PCT35, PCT36, PCT37, PCT38, PCT39, PCT41, PCT48, PCT61, PCT67 | 10 |
| Nacajuca | Rivera Alta | 18° 10' 51.0" | 93° 02' 15.0" | PCT19, PCT20, PCT21, PCT62, | 4 |
| Huimanguillo | Paredón 1 | 17° 44' 59.6" | 93° 23' 57.8" | PCT43, PCT44, PCT45 | 3 |
En cada municipio y localidad se escogió una plantación de cacao, en la cual se efectuaron muestreos dirigidos para localizar signos y síntomas de enfermedades. Se colectaron tres muestras de cada signo y síntoma observado, incluyéndose tallos, ramas, hojas y frutos. El muestreo se efectuó de octubre a diciembre de 2017. Las muestras, colocadas en bolsas de plástico y en neveras, se transportaron para su procesamiento al Laboratorio de Entomopatógenos de la División Académica de Ciencias Biológicas, Universidad Juárez Autónoma de Tabasco.
Aislamientos y purificación
Trozos del material enfermo se cortaron en secciones de 0.5 cm2 y se lavaron con agua destilada estéril (ADE). Las muestras se desinfestaron con hipoclorito de sodio al 2 % por 2 min y se enjuagaron con ADE. Bajo entorno aséptico, cinco fragmentos, del tejido desinfestado de cada muestra, se colocaron en cajas de Petri conteniendo medio de cultivo papa dextrosa agar (PDA). Las cajas se incubaron durante cinco a siete d. Después, un trozo del medio de cultivo con micelio se transfirió a una caja de Petri con medio PDA. De cada aislamiento poliespórico se obtuvo aislamientos monospóricos de acuerdo con Estrada et al. (1997).
Identificación morfológica
Los hongos se identificaron a nivel de género y especie con base en las estructuras reproductivas, según Samson (1981), Humber (1997), Engelbrecht y Harrington (2005), Phillips-Mora et al. (2006), Phillips-Mora (2013), Weir et al. (2012) y el manual de laboratorio de Fusarium de Leslie y Summerell (2006). Para ello, se utilizaron aislamientos 14 d, crecidos en medio PDA. Se determinó el tamaño, forma y conidiación de las colonias. Además, se inoculó una suspensión de esporas sobre fragmentos de PDA de 0.5 cm de diámetro, al cual se le colocó un cubreobjetos para obtener estructuras microscópicas. Los fragmentos inoculados se clocaron en cámaras húmedas y se incubaron a 25 °C durante 5 d. La morfología de peritecios, picnidios, conidióforos, conidios, esporangios y clamidosporas se observó en microscopio ZEISS Scope.A1; además, estas estructuras se fotodocumentaron por digitalización de imágenes. Para la micrometría se utilizó el software Image® Tool 3.00.
Identificación Molecular
Un aislamiento de cada morfotipo fue seleccionado para la identificación molecular. El ADN genómico se obtuvo a partir de micelio de colonias de 72 h de incubación, sembradas en medio PDA. El micelio se homogeneizó en 400 µL de buffer PBS, contenido en tubo Eppendorf de 1.5 mL. El ADN se obtuvo con el protocolo del Kit AxyPrep Multisource Genomic ADN Minipep (Axigen®). La calidad de ADN se evaluó en gel de agarosa al 1% (Agarosa Ultra Pure, Invitrogen®) y se cuantificó en un espectrofotómetro Perkin Elmer® (Lambda BIO 10®). Las regiones ITS1, ITS2 y 5.8 del ARN ribosomal se amplificaron por PCR con los iniciadores ITS4 (TCC TCC GCT TAT TGA TAT GC) e ITS5 (GGA AGTAAA AGT CGT AAC AAG G) (White et al., 1990). Para el hongo Phytophthora sp. se amplificó el gen 18S de acuerdo con Acosta-Pérez et al., (2012); utilizando los oligonucleótidos iniciadores universales: LV1 (5’CCTGCCAGTAGTCATATGCTTGTCT3’) y LV2 (5’ CACCTACGGAAACCTTGTTACGACT3’. La amplificación se realizó según el protocolo de Ahrens y Seemüller (1992), con modificaciones en las reacciones de PCR cuyo volumen final fue de 25 µL: agua ultrapura estéril (16.05 µL), solución amortiguadora Buffer 10X (2.5 µL), MgCl2a 50 mM (1.25 µL), dNTP mezcla a 10 mM (0.5 µL), iniciadores ITS4 e ITS5 a 10 pmol (1.25 µL de cada uno), TaqDNA polimerasa (Invitrogen®) a 1U (0.2 µL) y ADN blanco a 50 ng (2 µL).
La PCR consistió en un ciclo de 95°C durante 4 min, 35 ciclos de 95°C por 1 min, 35 ciclos de 58°C durante 1 min, 35 ciclos de 72°C por 2 min y un ciclo de 72°C durante 10 min. Con los productos de PCR se realizó electroforesis en gel de agarosa para visualización y medida de la especificidad. La cuantificación del ADN se realizó por espectrofotometría (NanoDrop 2000, Thermo Scientific®). Los productos se enviaron a la Unidad de Síntesis y Secuenciación de ADN del instituto de Biotecnología de la Universidad Nacional Autónoma de México para secuenciación, y las secuencias obtenidas se compararon con la base de datos del banco de genes del National Center for Biotechnology Information (NCBI, 2014) (www.ncbi.nlm.nih.gov/). Para la comparación de los valores generados con la secuencia de estudio se consideró una similitud ≥ 97 % (Stackebrandt y Goebel, 1994). La sinonimia se basó en Enciclopedia de la vida (http://eol.org/pages/192915/names/synonyms), MycoBank (www.mycobank.org) e Index Fungorum (www.indexfungorum.org/).
Análisis de la diversidad
La riqueza específica y la abundancia de hongos asociados a patologías de T. cacao fueron analizadas. La riqueza se calculó con el índice de diversidad de Margalef (DMg), a nivel de estado: DMg = (S - 1)/log N, donde S el número de especies y N el número total de individuos. Este índice representa la riqueza de especies en función del número total de individuos obtenidos. La abundancia se obtuvo mediante el índice de diversidad de Shannon-Wiener: H’ = - Σ i p i (log p i ), en donde p i es la proporción del número total de individuos que aparece representada en la especie i. Este índice (H’) proporciona un indicador de la relación entre el número de especies en cada sitio estudiado, y sus respectivas abundancias numéricas (Magurran, 1991).
Para comparar la composición de la comunidad fúngica encontrada, con comunidades fúngicas reportadas en otros estudios de hongos asociados en patologías de T. cacao, se obtuvo el índice de similitud de Sorensen (ISS). El ISS se calculó de acuerdo con Mueller-Dombois (1981): ISS = [(2C)/(A + B)*100], donde A representa todas las especies de la primera muestra, B representa todas especies de la segunda muestra y C es el número de especies comunes a las dos muestras. Además, se calculó la frecuencia de constancia, de acuerdo con Heredia (1999), a fin de conocer la presencia de las especies fúngicas en los diferentes sitios muestreados.
Resultados y discusión
Se obtuvieron un total de 48 aislamientos fúngicos a partir de muestras de tejidos de plantas de T. cacao con síntomas y signos de patologías (Tabla 1). Entre estos aislamientos, tres mostraron afinidad morfológica con Lasiodiplodia theobromae (Figura 1), nueve con Moniliophthora roreri (Figura 2) y dos con Ceratocystis cacaofunesta (Figura 3) (Tabla 2). Asimismo, veintiún aislamientos presentaron afinidad morfológica con Colletotrichum gloeosporioides (Figura 4), cuatro con Fusarium descemcellulare (Figura 6) y dos con Cophinforma sp. (Figura 6) (Tabla 2). Además, siete aislamientos mostraron afinidad morfológica con el pseudohongo Phytophthora capsici (Figura 7). En total, se identificaron siete especies morfológicas (Tabla 2).
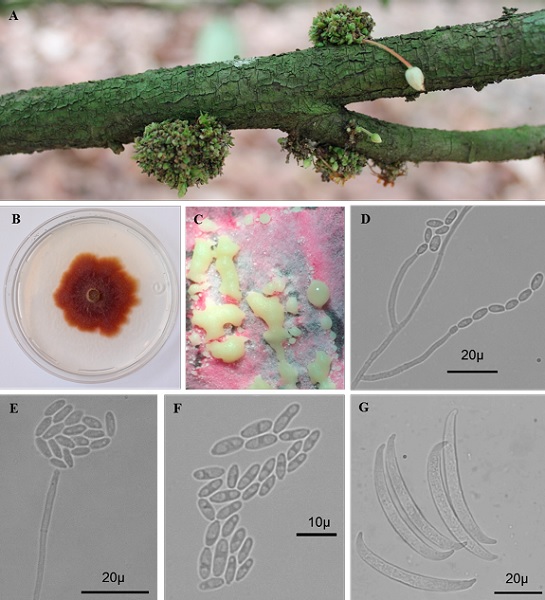
Figura 1 Lasiodiplodia theobromae. A) Fruto con necrosis café y conidiación de aspecto carbonoso. B) Clorosis de hojas, C, D) Necrosis y rayas necróticas en tejido vascular, E) Colonia en medio papa dextrosa agar, F) corte transversal de un picnidio, con conidios inmaduros, G) conidio inmaduro (amerospora), H) conidio maduro (didimospora).

Figure 1: Lasiodiplodia theobromae. A) Fruit with brown necrosis and carbonaceous conidiation, B) Leaf chlorosis, C, D) Necrosis and necrotic streaks in vascular tissue, E) Colony in potato dextrose agar medium, F) cross-section of a pycnidium, with immature conidia, G) immature conidia (amerospore), H) mature conidia (didimospore).
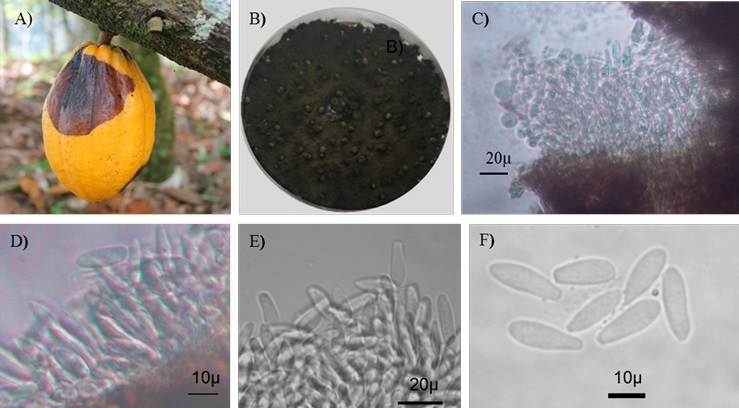
Figura 2 Moniliophthora roreri A) Fruto con deformaciones (jibas), B) fruto necrosado (mancha chocolate), C) fruto colonizado externamente por micelio, D) pseudocarpo con esporas en la superficie del fruto y h) fruto momificado. E) Colonia en medio V8 clarificado, F) conidióforos y formación de conidios en cadena, G) conidios globosos, subglobosos y elipsoidales.

Figure 2: Moniliophthora roreri A) Fruit with deformations (jibas), B) necrotic fruit (chocolate spot), C) fruit externally colonized by mycelium, D) pseudocarp with spores on the surface of the fruit, and h) mummified fruit. E) colony in clarified V8 medium, F) conidiophores and chain conidia formation, G) globose, subglobose and ellipsoidal conidia.
Figura 3 Ceratocystis cacaofunesta. A) árbol de cacao con amarillamiento y marchitez, B) árbol de cacao con hojas secas, C) Colonia en medio papa dextrosa agar, D) peritecio, E) hifas ostiolares y ascosporas, F) ascosporas, G) conidióforos con aleuroconidios, H) endoconidios cilíndricos (primarios), I) endoconidióforos produciendo endoconidios.
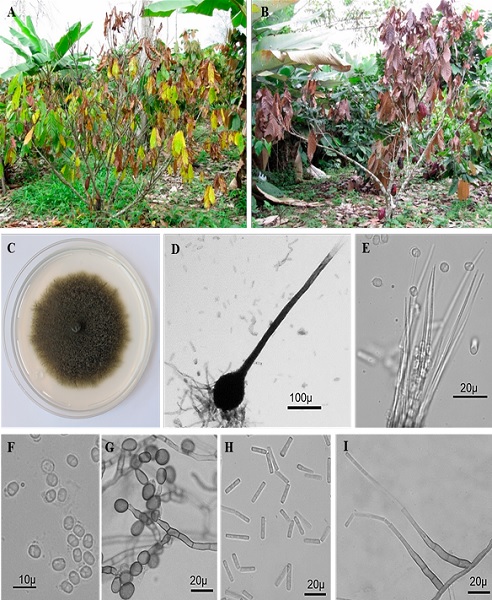
Figure 3: Ceratocystis cacaofunesta. A) cacao tree with yellowing and wilting, B) cacao tree with dry leaves, C) colony in dextrose agar medium, D) perithecium, E) ostiolar hyphae and ascospores, F) ascospores, G) conidiophores with aleuroconidia, H) cylindrical (primary) endoconidia, I) endoconidiophores producing endoconidia.
Figura 4 Colletotrichum gloeosporioides. A) Manchas necróticas con halos cloróticos, B) mancha café extendida del ápice hacia las nervaduras y peciolo, C) frutos juveniles con manchas necróticas hundidas, D) manchas necróticas hundidas en renuevos, E) Colonia en medio papa dextrosa agar, F) conidios, G) apresorios.
Tabla 2 Especies de micromicetos aislados a partir de patologías de Theobroma cacao, identificados por taxonomía clásica.
Table 2: Micromycete species isolated from Theobroma cacao pathologies, identified by classical taxonomy.
| Especie morfológica | Aislamientos | No. de aislamientos |
| Lasiodiplodia theobromae | PCT37, PCT41, PCT61 | 3 |
| Moniliophthora roreri | PCT03, PCT05, PCT13, PCT17, PCT19, PCT34, PCT43, PCT46, PCT56 | 9 |
| Ceratocystis cacaofunesta | PCT01, PCT48 | 2 |
| Colletotrichum gloeosporioides | PCT02, PCT08, PCT10, PCT11, PCT12, PCT15, PCT16, PCT20, PCT21, PCT24, PCT28, PCT30, PCT31, PCT35, PCT49, PCT50, PCT51, PCT44, PCT45, PCT59, PCT60 | 21 |
| Fusarium descemcellulare | PCT07, PCT14, PCT18, PCT27 | 4 |
| Cophinforma sp. | PCT06, PCT57 | 2 |
| Phytophthora capsici | PCT62, PCT63, PCT64, PCT65, PCT66, PCT67, PCT68 | 7 |
En relación con los morfotipos seleccionados para la identificación molecular, se amplificaron regiones específicas en los siguientes aislamientos: el aislamiento PTC41, correspondiente a L. theobromae, mostró una región de 512 pb; el aislamiento PTC13, correspondiente a M. roreri, presentó una región de 852 pb; el aislamiento PTC48, correspondiente a C. cacaofunesta, mostró una región de 520 pb; el aislamiento PTC10, correspondiente a C. gloeosporioides, también presentó una región de 520 pb; la cepa PTC27, identificada como F. descemcellulare, obtuvo una región de 510 pb; el aislamiento PTC06, correspondiente a Cophinforma sp., mostró una región de 538 pb; y el aislamiento PTC62, correspondiente a P. capsici, presentó una región de 1730 pb. Las secuencias obtenidas coincidieron con secuencias del GenBank, mostrando homologías del 99 al 100 % (Tabla 3), confirmando así la identidad de los géneros y especies. En el caso de Cophinforma sp., el análisis molecular reveló que corresponde a C. atrovirens. Por lo tanto, se confirmó que la micobiota asociada a las patologías de T. cacao incluye seis hongos y un pseudohongo (Tabla 3).
Tabla 3 Especies de micromicetos asociados a patologías de Theobroma cacao, en Tabasco, México; identificados por amplificación de los espaciadores transcritos internos y el gen 18S (en el caso del género Phytophthora), en Tabasco, México.
Table 3: Micromycete species associated with pathologies in Theobroma cacao, in Tabasco, Mexico; identified by amplification of internal transcribed spacers and the 18S gene (in the case of the genus Phytophthora), in Tabasco, Mexico.
| Aislamiento | Identificación | Identidad | Cepa de referencia |
| molecular | (%) | (Gen Bank) | |
| PTC41 | Lasiodiplodia theobromae | 99 | KF466497 |
| PTC13 | Moniliophthora roreri | 100 | GU108605 |
| PTC01 | Ceratocistys cacaofunesta | 100 | AY157951 |
| PTC10 | Colletotrichum gloeosporioides | 100 | MF540884 |
| PTC27 | Fusarium descemcellulare | 99 | KU377469 |
| PTC06 | Cophinforma atrovirens | 99 | MF436146 |
| PTC62 | Phytophthora capsici | 99 | AY742748 |
El número de especies asociadas a patologías de T. cacao resulto en un DMg = 1.55 y un H’ = 1.6. La especie más abundante fue C. gloeosporioides (43.7 %), seguido de M. roreri (18.7 %) y P. capsici (14.6 %). Las especies menos abundantes fueron C. cacaofunesta y C. atrovirens (Tabla 4). Nuestros resultados difieren con lo reportado en Cuba, donde las especies más abundantes fueron L. theobromae, seguido de P. palmivora y C. gloeosporioides (Martínez-de la Parte y Pérez-Vicente, 2015). La comunidad de especies asociadas a patologías de T. cacao en Tabasco, fue un 66.6% similar a la reportada en el estado de Chiapas, donde las especies similares fueron: M roreri, P. capsici, C. gloeosporioides y C. cacaofunesta (Hernández-Gómez et al., 2015). Por otro lado, la comunidad de especies reportadas en este trabajo fue 46 % similar a la reportada en plantaciones de cacao en Cuba, donde las especies similares fueron: L. theobromae, C. gloeosporioides y F. descemcellulare (Martínez-de la Parte y Pérez-Vicente, 2015). En cuanto a la presencia de las especies en las localidades evaluadas, C. gloeosporioides y M. roreri mostraron una frecuencia de constancia (FC) del 90 %. La especie P. capsici mostró una FC del 60 %. Las tres especies restantes manifestaron una FC menor al 50 %. La especie con menor FC fue C. atrovirens (Tabla 4). En un estudio realizado en plantaciones de caco en Cuba, P. palmivora mostró una FC del 60%; C. gloeosporioides y L. theobromae mostraron una FC del 55 %, y F. descemcellulare mostró una FC del 10% (Martínez-de la Parte y Pérez-Vicente, 2015). En este estudio, a nivel de subregiones, las especies M. roreri, C. gloeosporioides, F. descemcellulare mostraron un FC del 100 %. Por su parte, L. theobromae y P. capsici mostraron una FC del 67 %; C. cacaofunesta y C. atrovirens presentaron la menor FC (33 %). Los valores del índice de riqueza específica (DMg) y el de abundancia (H’), obtenidos en esta investigación, pueden ser referencias para futuras investigaciones sobre diversidad de hongos asociados a patologías en diversos cultivos.
Tabla 4 Frecuencia de constancia y abundancia de micromicetos asociados a patologías de Theobroma cacao, en 10 localidades del estado de Tabasco, México.
Table 4: Frequency of constancy and abundance of micromycetes associated with Theobroma cacao pathologies in 10 localities of the state of Tabasco, Mexico.
| Especie | Subregión/Localidad | Frecuencia de constancia (%) | Abundancia (%) | |||||||||
| Chontalpa | Centro | Sierra | ||||||||||
| LP | FC | OC | OR | PA | PC | HG | RA | AL | ZP | |||
| Lasiodiplodia theobromae | 0 | 0 | 0 | 1 | 0 | 0 | 0 | 0 | 1 | 0 | 20 | 6.2 |
| Moniliophthora roreri | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 0 | 1 | 90 | 18.7 |
| Ceratocistys cacaofunesta | 0 | 0 | 1 | 1 | 0 | 0 | 0 | 0 | 0 | 0 | 20 | 4.2 |
| Colletotrichum gloeosporioides | 1 | 0 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 90 | 43.7 |
| Fusarium descemcellulare | 0 | 1 | 0 | 0 | 0 | 1 | 1 | 0 | 1 | 0 | 40 | 8.3 |
| Cophinforma atrovirens | 0 | 0 | 0 | 0 | 0 | 0 | 1 | 0 | 0 | 0 | 10 | 4.2 |
| Phytophthora capsici | 1 | 1 | 1 | 1 | 0 | 0 | 1 | 1 | 0 | 0 | 60 | 14.6 |
LP= R/a. La Piedra 1, HG = R/a. Hermenegildo Galeana 2, OR= R/a. Oriente, ZP= Ejido Zunuy y patastal, AL= R/a. Allende, OC= R/a. Ocampo, PC= R/a. Plátano y cacao 4, FC= Finca Cholula, RA= R/a. Rivera Alta, PA= R/a. Paredón 1.
De las especies asociadas a patologías de T. caco, el hongo L. theobromae (Ascomycota: Dothideomycetes) ha sido reportado como el agente causal de la pudrición café de la mazorca y la muerte regresiva de T. cacao en diferentes países (Huda-Shakirah et al., 2022; Mbenoun et al., 2008). De acuerdo con Picos-Muñoz et al. (2015) L. theobromae se registró por primera vez atacando T. cacao en México en el año 1976; sin embargo, no se ha evaluado su incidencia y severidad en este cultivo, en México. L. theobromae posee más de 500 especies vegetales hospederas (Farr y Rossman, 2021) y presenta una amplia distribución en las regiones tropicales y subtropicales (Rodríguez-Gálvez, 2017). Este hongo ha tomado relevante importancia en los diferentes países como Malasia, India, y Cameroon, donde este patógeno ha causado muerte regresiva de árboles de cacao con incidencia de hasta el 20 %, 56 % y 100 %, respectivamente (Huda-Shakirah et al., 2022; Kannan et al., 2010; Mbenoun et al., 2008). En Malasia se ha reportado incidencia en frutos del 25% (Huda-Shakirah et al., 2022). En plantas de cacao, L. theobromae afecta las ramas jóvenes causándoles la muerte, sin afectar las ramas principales, y las ramas afectadas presentan estrías necróticas en el tejido vascular. Cuando el patógeno coloniza tejidos de ramas y tallos, provoca clorosis y marchitez en todo el follaje; posteriormente la planta muere (Figura 1) (Kannan et al., 2010). En frutos, este hongo provoca manchas color café en el exocarpo (Figura 1), y esta necrosis puede extenderse hasta los granos del cacao (Moreira-Morillo et al., 2021).
Otra de las especies fúngicas encontradas fue M. roreri (Basidiomycota: Agaricomycetes) (Figura 2), agente causal de la enfermedad conocida como moniliasis del cacao (Phillips-Mora y Wilkinson 2007). Esta patología se considera la enfermedad más restrictiva de la producción de cacao en América. M. roreri se reportó por primera vez en México en el año 2005 (Phillips-Mora et al., 2006). En México, M. roreri ocasiona pérdidas en la producción de hasta el 75 % (Torres-de la Cruz et al., 2020); en Colombia, Ecuador y Costa Rica se han reportado pérdidas superiores al 80 % (Hidalgo et al., 2003). Actualmente este patógeno está restringido al continente americano; sin embargo, el riesgo de su introducción accidental en África occidental es preocupante, debido al potencial parasítico que muestra este patógeno (Leandro-Muñoz et al., 2017). M. roreri infecta sólo a los frutos, durante todo su desarrollo; sin embargo, los frutos jóvenes son más susceptibles. Este hongo induce hipertrofia, necrosis interna, madurez prematura y manchas necróticas externas de bordes irregulares; sobre la mancha crece un estroma blanco con masas de esporas infectivas (Figura 2) (Torres-de la Cruz et al., 2020).
Por su parte, el hongo C. cacaofunesta (Ascomycota: Sordariomycetes) (Figura 3) ha sido reportado como el agente causal de la marchitez por ceratocystis o mal del machete en T. cacao (Engelbrecht y Harrington, 2005; Phillips-Mora y Cerda-Bustillos, 2009). Esta enfermedad se encuentra distribuida sólo en países de Sudamérica y Centroamérica, de donde es nativa; además, en las islas Haití, República Dominicana y Trinidad (Silva et al., 2007; Engelbrecht et al., 2007; Marín-Montoya y Wingfield, 2006; Baker et al., 2003). Este patógeno ingresa a la planta por medio de las heridas causadas por escarabajos (Scolytinae) y por las herramientas de trabajo. El hongo invade el xilema y causa necrosis vascular, amarillamiento, marchitez y muerte del árbol en pocas semanas (Figura 3). Las hojas muertas permaneces adheridas a la planta por un tiempo largo después de la muerte del árbol (Figura 3) (Silva et al., 2004; Engelbrecht et al., 2007). Este hongo no ha sido reportado afectando frutos; sin embargo, en Nigeria, Umana et al. (2014) reportaron a la especie Ceratocystis paradoxa infectando frutos de cacao. De acuerdo con Engelbrecht et al. (2007), la marchitez por C. cacaofunesta está resurgiendo como enfermedad importante, debido al movimiento de material clonal en los programas de reproducción de cacao, dado que este patógeno puede diseminarse eficientemente a través de esquejes. A pesar de la importancia de este patógeno, en México no existe evaluación de su incidencia y severidad en plantaciones de cacao, ni de los factores que favorecen la enfermedad.
En el caso de C. gloeosporioides (Ascomycota: Sordariomycetes) (Figura 4), este ha sido reportado como el agente causal de la antracnosis en flores, frutos, hojas y brotes tiernos de T. cacao (Phillips-Mora y Cerda-Bustillos, 2009). Este hongo fue descrito por primera vez atacando a T. cacao en el año 1905 en las colonias francesas de África y está presente en todas las zonas productoras de cacao en el mundo (Reyes y Capriles, 2000). Este hongo induce manchas foliares color café extendidas desde el ápice hasta el peciolo de las hojas; manchas necróticas dispersas rodeadas de un halo clorótico, manchas necróticas secas, manchas necróticas húmedas en ramas, manchas necróticas en flores, manchas café hundidas en frutos (Figura 4) (Phillips-Mora y Cerda-Bustillos, 2009). En plantas de vivero, C. gleosporioides causa lesiones similares y defoliación, así como lesiones hundidas en el tallo (Phillips-Mora y Cerda-Bustillos, 2009). De acuerdo con Martínez-de la Parte y Pérez-Vicente (2015), C. gloeosporioides es un patógeno importante en el cultivo de cacao en Cuba, y se ha encontrado atacando principalmente hojas y en menor grado a frutos. Por otro lado, Aoudou y Second (2017) reportaron predominancia de este patógeno en frutos de cacao en Camerún. De acuerdo con Phillips-Mora y Cerda-Bustillos (2009), en Costa Rica, el principal daño por C. gloeosporioides es en las hojas, lo cual provoca defoliación; esto estimula la emisión de ramas nuevas, las cuales también son infectadas, dando finalmente el síntoma de escobas pequeñas. En México, este patógeno ha sido confirmado atacando a T. cacao en Chiapas (Hernández-Gómez et al., 2015); sin embargo, no se ha evaluado su incidencia en los distintos órganos que afecta.
Fusarium descemcellulare (Ascomycota: Sordariomycetes) (Figura 5) fue otra especie asociada a patologías de T. cacao en Tabasco. Este hongo se ha reportado como el causante del crecimiento de bubas o agallas en los cojinetes florales del árbol de cacao. De acuerdo con Wood y Lass (1985), esta patología se reportó por primera vez en Guyana en 1905; posteriormente se reportó en Nicaragua, Costa Rica Colombia, Papúa Nueva Guinea, Venezuela, y actualmente se encuentra distribuida en casi todos los países productores de cacao del mundo (Reyes y Capriles, 2000). Este hongo induce tumores y desorganización meristemática que afecta principalmente los cojines florales y causa disminución de la producción de frutos (Reyes y Capriles, 2000). En caso de ataques muy severos, los cojines florales no muestran formación de frutos (Enríquez 2010). Los árboles afectados por este hongo pueden presentar 60 % de pérdidas de la producción, tornarse improductivos, y constituirse en fuente de infección (Enríquez, 1985; Parra et al., 2009). Al respecto, Moya y Borbón (2015) reportaron una incidencia del 86 % con severidad alta en plantaciones de cacao en República dominicana. Estos autores mencionaron que las bubas causadas por F. descemcellulare pueden ser de puntos verdes, floral, abanico, perilla, lobular y disco; sin embargo, en este estudio sólo se encontraron bubas de puntos verdes, las cuales consistieron en tumoraciones globosas formadas por agrupamiento de yemas verdes, compactas, caedizas, con aspecto de coliflor, que se unen a la planta por un pedúnculo central corto y leñoso (Figura 5). La incidencia y severidad de esta enfermedad no se ha evaluado en México.
Otro de los hongos asociados a patologías de T. cacao en Tabasco fue C. atrovirens (Ascomycota: Dothideomycetes) (Figura 6). Este hongo fue aislado de manchas necróticas en frutos maduros (Figura 6). Aunque este es el primer reporte de Cophinforma atrovirens asociado a patologías de T. cacao en México, Mohali-Castillo y Stewart (2017) ya habían documentado su asociación con la antracnosis del fruto de cacao en el estado de Mérida, Venezuela. Además, C. atrovirens ha sido reportado en Brasil como el agente causal de la pudrición del tallo y la muerte regresiva del marañón (Anacardium occidentale) (Cardoso et al., 2019). En el sur de China, se ha identificado a C. atrovirens como el agente causal de cancro del tallo y tizón de la rama en plantaciones de eucalipto (Zhu et al., 2018). Dado estos antecedentes, es importante evaluar la patogenicidad e incidencia de C. atrovirens en T. cacao en México.
Otra de las especies fúngicas encontradas fue Phytophthora capsici (Oomycota: Oomycetes) (Figura 7). Este pseudohongo ha sido reportado como el agente causal de la mancha negra del cacao (MNC) en México, particularmente en Tabasco y Chiapas (Ortiz-García, 1996; Hernández-Gómez et al., 2016). La enfermedad provocada por P. capsici es actualmente la segunda enfermedad más destructiva del cacao en el sureste de México; con pérdidas de hasta el 25 % en la producción de frutos (Torres- de la Cruz et al., 2023). En otros países se han reportado incidencias de hasta el 70 % (Ndoumbe-Nkeng et al., 2009); sin embargo, en cada país donde se cultiva T. cacao, la MNC es causada por diferentes especies de Phytophthora. En América latina y el Caribe se ha reportado a P. capcisi, P. parasítica y P. palmivora, P. tropicalis y P. theobromicola (Ortiz-García, 1991; Bahía et al., 2015; Decloquement et al., 2021; Aragaky y Uchida, 2021). De acuerdo con Matos et al. (2011), P. megakarya es la especie más agresiva en los campos de cacao en África; sin embargo, no se ha reportado la presencia de esta especie atacando a T. cacao en el Continente Americano. Phytophthora capsici induce manchas necróticas en tejido foliar y en frutos. El daño más frecuente es en el fruto, con manchas circulares de borde regular, de color café oscuro, que se extienden por la superficie hasta cubrir totalmente la mazorca y los granos (Figura 7A, B). Un estudio de la situación actual del género Phytophthora en T. cacao en México es necesaria.
Conclusiones
En el presente trabajo se identificaron siete especies fúngicas asociadas a patologías de T. cacao en Tabasco, México, donde la especie con mayor abundancia fue C. gloeosporioides, seguido de M. roreri y P. capsici. Cophinforma atrovirens se reporta por primera vez asociada a T. cacao en México. Los resultados de este trabajo demuestran la riqueza de especies fúngicas que pueden encontrarse asociadas a patologías de T. cacao en Tabasco, México; aportando también al conocimiento de la biodiversidad. Los resultados de este estudio proveen referencias para investigaciones futuras relacionadas con patogenicidad, incidencia y severidad de los hongos presentes en el cultivo del cacao en México.











 nueva página del texto (beta)
nueva página del texto (beta)