Introducción
La araña roja Tetranychus urticae Koch (Acari: Tetranychidae) es una plaga polífaga que se hospeda en más de 1200 especies de plantas en todo el mundo, atacando árboles frutales, ornamentales, fabáceas, hortalizas y cucurbitáceas donde disminuye el rendimiento en un 10 a 50 % y una perdida en un 50 % (Monroy-Reyes et al., 2015; Brust, 2018; Assouguem et al., 2022; Talib et al., 2023). El daño causado por T. urticae es al momento de alimentarse, ya que inserta su estilete en el mesófilo y las células epidérmicas de las hojas, causando una alteración en la fotosíntesis y transpiración disminuyendo el crecimiento afectando la floración y rendimientos en los cultivos (Abdallah et al., 2019; Shaabow et al., 2019; Golec et al., 2020), pero cuando las condiciones son favorables se incrementa la densidad poblacional y los daños pueden ser severos ya que causa necrosis y muerte de las plantas (Goff et al., 2014; Golec et al., 2020).
La principal forma de controlar la araña roja es mediante el uso de acaricidas convencionales (Van Leeuwen et al., 2010; Rincón et al., 2019), sin embargo, el uso excesivo de estos productos ha causado resistencia a poblaciones de T. urticae, debido a su ciclo de vida corto y alta fecundidad (Van Leeuwen et al., 2010). Dentro de las estrategias utilizadas para el manejo de ácaros fitófagos se ha reportado en varios estudios que extractos de diversas plantas (extractos acuosos, extractos etanólicos, aceites esenciales y aceites orgánicos) tienen alta efectividad en la supresión de la densidad poblacional de T. urticae logrando ser una de las alternativas para el manejo de ácaros fitófagos (Yáñez et al., 2014; Wakgari y Yigezu, 2018; Rincón et al., 2019). De igual manera, Premalatha et al. (2018) evaluaron 20 extractos de plantas de diferentes especies, de las cuales ocho tuvieron efecto tóxico agudo sobre T. urticae. También, se reportó que los extractos de Citratus sinensis, Datura stramonium, Ficus carica, Hyoscoyamus muticus, Jatropha curcas, Mentha pulegium, Morus rubra y Trichilia havanensis tienen efectos letales sobre T. urticae (Abou-Shosha, 2020; Alpkent et al., 2023; Rivera-Hernández et al., 2023).
Con respecto al efecto de los acaricidas botánicos comerciales, se ha demostrado que los acaricidas botánicos a base de Azadirachta indica (Juss) causan mortalidad del 65 % hasta 100 % en adultos de T. urticae y T. evansi (Nag et al., 2020; Azandémè-Hounmalon et al., 2022). A su vez, los acaricidas a base de Capsicum annum L. y Allium sativun L. reducen en 60 % la densidad poblacional de de T. urticae en cultivos de Platanus orientalis (Platanaceae) (Fatemi et al., 2021). Así también, en evaluaciones en otras especies de ácaros, se documentó que los extractos de Cinnamomum zeylanicum y aceite de Glycine max disminuyen la densidad poblacional de Oligonychus sp. y Raoiella indica en campo (Nexticapan-Garcéz et al., 2021).
Los extractos vegetales (extractos acuosos, extractos etanólicos) y acaricidas botánicos comerciales ofrecen una alternativa útil para el control de ácaros fitófagos, por su efectividad, poca persistencia en el ambiente y baja toxicidad a organismos benéficos. Estos acaricidas actúan en varios sitios de acción, desde el sistema nervioso central hasta la respiración mitocondrial, y el sistema endocrino durante el crecimiento (Regnault-Roger et al., 2012; Rincón et al., 2019; Abdel-Khalik et al., 2023). Por tanto, el objetivo de estudio es evaluar el efecto de extractos etanólicos (EE) de Ardisia compressa (Myrsinaceae) y acaricidas botánicos comerciales sobre T. urticae en condiciones de laboratorio e invernadero.
Materiales y métodos
Establecimiento de colonia de T. urticae
T. urticae se obtuvo de plantas de papaya (Carica papaya L.) cultivadas en el municipio de Conkal, Yucatán, México. La colonia de ácaros se estableció sobre plantas sanas de berenjena (S. melongena L.), donde se recolectaron hojas infestadas con ácaros que se fijaron con clips a la parte apical de plantas sanas de berenjena de dos meses de edad, establecidas en un invernadero en el Instituto Tecnológico de Conkal (21° 4’ latitud N y 89° 31’ longitud O). Posterior a tres semanas de la infestación inicial de las hojas, se tuvieron colonias de T. urticae con individuos de diferentes estados de desarrollo para los bioensayos.
Preparación de extractos etanólicos y acaricidas botánicos probados
Para el estudio se usaron dos grupos de productos vegetales, cada grupo se evaluó de manera separada: un grupo correspondió a extractos etanólicos de Ardisia y otro grupo correspondió a acaricidas botánicos comerciales.
Los extractos acuosos se prepararon con base a la metodología propuesta por Cruz-Estrada et al. (2013), donde muestras de hojas de diferentes poblaciones se recolectaron en diferentes municipios de Chiapas, México (Tabla 1) y se secaron a 45 °C por 10 d y se molieron hasta obtener polvo fino (MAN mod. MLU-9090, México). Para la preparación de los extractos etanólicos (EE), se utilizaron muestras con 50g de material pulverizado, a las que se adicionó 500 mL de etanol (grado reactivo). Durante 72 h se mantuvieron en agitación constante a temperatura de 25º. Posteriormente se filtraron en papel Whatman no. 1 para remover el material vegetal. Cada muestra se depositó en un rotavapor a presión de vacío constante para obtener la pasta-extracto de cada población de Ardisia (Yamato B0400. Yamato VR300, USA.).
Tabla 1 Poblaciones silvestres de Ardisia compressa Kunth, recolectadas en cuatro municipios del Estado de Chiapas.
Table 1: Populations of wild Ardisia compressa Kunth, collected in four municipalities of the state of Chiapas.
| ID Extracto | Localidad, Municipio | Altitud (m) | Coordenadas |
| Ardisia YRP | Río Pupiltillo, Yajalón | 500 | 17º 10' 14.00ʺ N, 92º 19' 49.00ʺ W |
| Ardisia YBG | Banco de grava, Yajalón | 915 | 17º 10' 00.00ʺ N, 92º 19' 00.00ʺ W |
| Ardisia CJC | Joybé carretera, Chilón | 972 | 17º 01' 07.00ʺ N, 92º 09' 19.66ʺ W |
| Ardisia CJR | Joybé río, Chilón | 900 | 17° 01' 11.77ʺ N, 92° 09' 41.76ʺ W |
| Ardisia CLC | Las Canchas, Chilón | 850 | 17° 00' 19.07ʺ N, 92º 06' 52.92ʺ W |
| Ardisia CTia | Tiaquil, Chilón | 1141 | 17° 11' 99.00ʺ N, 92º 52' 58.61ʺ W |
| Ardisia TCA | Coquijaz alto, Tila | 1800 | 17° 17' 05.40ʺ N, 92° 28' 46.20ʺ W |
Para la realización de los bioensayos, la pasta-extracto de cada población de Ardisia se diluyó en una solución de etanol y tween 80, a una relación de 1:1:1 (peso/volumen/volumen). Posteriormente, se diluyó en agua destilada (100 mL) hasta obtener una concentración final de 0.2 % (p/v) de la pasta-extracto en la mezcla de aplicación de extractos etanólicos (EE). Para el caso de los bioensayos de los acaricidas botánicos comerciales se utilizaron las concentraciones recomendadas por el fabricante. Se utilizó el insecticida químico abamectina como control positivo y agua destilada como control negativo. Los nombres comerciales, dosis y detalles de los acaricidas botánicos comerciales se describen en la Tabla 2.
Table 2: Botanical acaricides and application rates tested in this study.
| Tratamiento | Nombre comercial (ingrediente activo) | Tasa de aplicación / ha (Cantidad 400 L-1) | Empresa |
| Aceite de Glycine max | EPA-90® (Aceite vegetal de Glycine max) | 3 L | Biokrone S.A. de C.V., México |
| Aceite de Zea mays | Cimax® (Aceite vegetal de Zea mays) | 4 L | Ultraquimia agrícola, S.A. de C.V. |
| Extracto de Cinnamomum zeylanicum | CinnAcar® (Extracto de Cinnamomum zeylanicum) | 3 L | Promotora Técnica Industrial, México. |
| Extracto de Azadirachta | Mix Protectivee-N® (Extracto de Azadirachta indica) | 6 L | Agrosanidad S.A. de C.V. |
| Extracto de Argemone + Ricinus | Star agricola® (Extracto de Argemone mexicana + Ricinus communis) | 2 L | Ultraquimia agrícola, S.A. de C.V. |
| Extracto de Cinnamomun + Azadirachta + Heliposis | Cinanim® (Extracto de Cinnamomum zeylanicum + Azadirachta indica + Heliopsis longipes) | 2 L | BioKrone México, S.A de C.V. |
| Abamectina | Abakrone® Abamectina (1.80 %) | 0.4 L | BioKrone México, S.A de C.V. |
| Control | Agua destilada |
Evaluación de toxicidad letal aguda de T. urticae en laboratorio
Se hicieron dos experimentos, uno para evaluar los EE de Ardisia y otro para evaluar los acaricidas botánicos comerciales. Los ensayos de toxicidad letal se hicieron en adultos de T. urticae, para lo cual se cortaron discos foliares de berenjena (Solanum melongena) de 5 cm de diámetro y se sumergieron por 5 s en los EE de Ardisia o en los acaricidas botánicos comerciales preparados de forma individual en vasos de precipitado de 100 mL. Después de la inmersión, los discos foliares se secaron a temperatura ambiente por 30 minutos. A continuación, los discos foliares se colocaron con el lado adaxial hacia arriba sobre algodón humedecido en cajas de Petri (9 cm de diámetro y 1.5 cm de profundidad). Los bordes de los discos foliares se cubrieron con algodón húmedo para evitar que los ácaros escaparan. Se transfirieron 15 adultos de T. urticae en cada disco foliar y se registró la mortalidad a las 6 y 12 h después de la aplicación. Las cajas Petri se mantuvieron en el laboratorio a 24 ± 30 °C y fotoperiodo de 14 h de luz y 10 h de oscuridad. Se consideraron ácaros muertos, aquellos que no se movían después de ser tocados con un pincel fino. Una caja Petri con 15 ácaros representó una repetición. Se evaluaron 10 repeticiones por cada tratamiento (Cua-Basulto et al., 2022).
Evaluación de la supresión poblacional de T. urticae en invernadero
Para las evaluaciones en invernadero se utilizaron plantas de berenjena de dos meses de edad. La evaluación se hizo en un invernadero con techo de plástico y malla lateral antiáfidos bajo condiciones ambientales fluctuantes (25 - 35°C de temperatura y 55 - 75% de humedad relativa). Las plantas de berenjena se infestaron con adultos de T. urticae y tres semanas después, cuando se había establecido la colonia de ácaros, se realizaron las aplicaciones de los tratamientos, dirigiendo la aspersión a ambos lados de las hojas en cobertura total hasta punto de goteo, utilizando un atomizador manual (Klintek ATO-100). La densidad poblacional de T. urticae se determinó antes de la aspersión y a los 1, 2 y 3 d después de la aplicación de los tratamientos. Para tales efectos, se cortó una hoja joven por planta y se llevó al laboratorio para contar el número de ácaros (adultos, ninfas y huevos) con la ayuda de un estereoscopio (40x). El área de cada hoja evaluada se midió con un integrador de área foliar (LI-COR®, USA, modelo LI-300C). Una planta representó una réplica. Se evaluaron diez réplicas por cada tratamiento (Cua-Basulto et al., 2022).
Análisis de datos
Se usó un diseño completamente al azar para todos los experimentos. Los datos se sometieron a análisis de varianza después de verificar la normalidad y la homocedasticidad (prueba de Shapiro-wilk). Los efectos se consideraron estadísticamente significativos si P < 0,05. Todos los análisis se realizaron en el paquete estadístico Statgraphics.
Resultados
Toxicidad aguda de EE de A. compressa y acaricidas botánicos en T urticae
Los extractos EE de Ardisia tuvieron efectos moderados pero significativos sobre la mortalidad de T. urticae a las 6 h (F = 135.77, gl = 8, 781, P < 0.0001) y a las 12 h (F = 104.99, gl = 8, 81, p < 0.0001) después de la aplicación. El EE de Ardisia YRP tuvo el efecto más alto (34.6 - 38.6 % de mortalidad) en ambos periodos de evaluación. El EE de Ardisia CTia tuvo efecto significativo, pero a las 12 h de su aplicación (35.3 % de mortalidad). Los demás EE de Ardisia causaron entre 18 y 27 % de mortalidad a las 12 h después de su aplicación, en comparación con la abamectina que causo el 100 % de mortalidad a las 6 y 12 h (Figura 1).
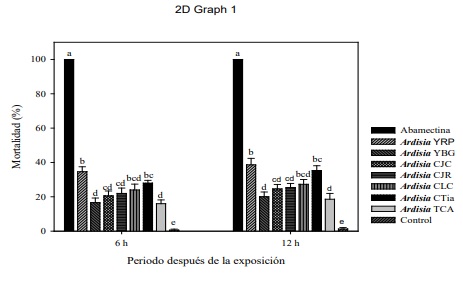
Figura 1 Mortalidad (medias ± error estándar) de adultos de T. urticae en laboratorio. Las medias para cada periodo (horas) después de la exposición que no comparten la misma letra son significativamente diferentes (Tukey P<0.05). Los estadísticos del análisis del efecto se presentan para cada periodo (horas) después de la exposición (HDE). Figure 1. Mortality (means ± standard error) of T. urticae adults in the laboratory. The means for each period (hours) after exposure that do not share the same letter are significantly different (Tukey P<0.05). Effect analysis statistics are presented for each period (hours) after exposure (HDE).
Los acaricidas botánicos comerciales tuvieron efectos significativos sobre la mortalidad de T. urticae a las 6 h (F = 182.1, gl = 7, 72, p < 0.0001) y 12 h después de la exposición (F = 165.89, gl = 7, 72, p < 0.0001). El acaricida botánico a base de aceite de Zea mays tuvo el efecto más alto (62 - 81 % de mortalidad) desde las 6 y 12 h después de la aplicación, mientras que el aceite de Glycine max causó 54 % de mortalidad hasta las 12 h después de su aplicación en comparación con la abamectina que causo el 100 % de mortalidad a las 6 y 12 h. Los otros acaricidas botánicos causaron entre 17 y 26 % de mortalidad (Figura 2).
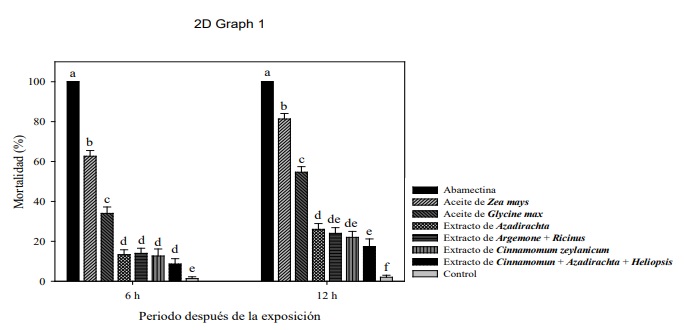
Figura 2 Mortalidad (medias ± error estándar) de adultos de T. urticae en laboratorio. Las medias para cada periodo (horas) después de la exposición que no comparten la misma letra son significativamente diferentes (Tukey P < 0.05). Los estadísticos del análisis del efecto se presentan para cada periodo (h) después de la exposición (HDE). Figure 2. Mortality (means ± standard error) of T. urticae adults in the laboratory. The means for each period (hours) after exposure that do not share the same letter are significantly different (Tukey P < 0.05). Effect analysis statistics are presented for each period (h) after exposure (HDE).
Supresión de la densidad poblacional en invernadero
Todos los EE de Ardisia causaron supresión de la densidad poblacional de T. urticae a los 1, 2 y 3 d después de la exposición. En adultos, los EE de Ardisia YRP y Ardisia CTia redujeron entre 4.0 a 6.4 adultos por cm2 (Figura 3A). En ninfas entre 6.8 y 7.6 por cm2 (Figura 3B) y en huevos entre 11.7 a 15.3 huevos por cm2 (Figura 3C).
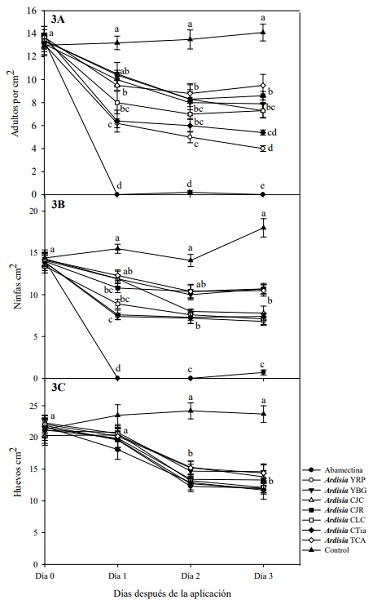
Figura 3 Supresión de la densidad poblacional (media ± error estándar) de adultos (A), ninfas (B) y huevos (C) de T. urticae en invernadero. Las medias para el mismo periodo (día) posteriores a la exposición que no comparten la misma letra son significativamente diferentes (Tukey P < 0.05). Figure 3. Suppression of population density (mean ± standard error) of adults (A), nymphs (B) and eggs (C) of T. urticae in a greenhouse. The means for the same period (day) after exposure that do not share the same letter are significantly different (Tukey P < 0.05).
Para el caso de los acaricidas botánicos comerciales a base de Zea mays y Glycine max, minimizaron la densidad poblacional de adultos registrando valores entre 1.5 y 3.2 adultos por cm2 (Figura 4A). En ninfas entre 2.4 a 3.0 por cm2 (Figura 4B). Del mismo modo en huevos con valores de 13.0 a 18.0 huevos por cm2 después de la aplicación Figura 4C). El extracto de Azadirachta indica, extracto Argemone mexicana + Ricinus y extracto de Cinnamomum + Azadirachta + Heliopsis causaron una reducción intermedia en la densidad poblacional con valores en adultos (2.9 a 5.5 por cm2), en ninfas (4.0 a 5.9 por cm2) y huevos (15.0 a 21.5 por cm2),
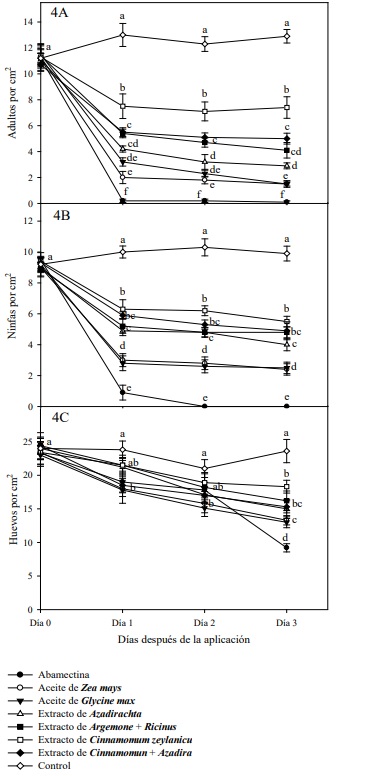
Figura 4 Supresión de la densidad poblacional (media ± error estándar) de adultos (A), ninfas (B) y huevos (C) de T. urticae en invernadero. Las medias para el mismo periodo (día) posteriores a la exposición que no comparten la misma letra son significativamente diferentes (Tukey P < 0.05). Los estadísticos del análisis del efecto se presentan por cada periodo (día) después del tratamiento acaricida (DDT). Figure 4. Suppression of population density (mean ± standard error) of adults (A), nymphs (B) and eggs (C) of T. urticae in a greenhouse. The means for the same period (day) after exposure that do not share the same letter are significantly different (Tukey P < 0.05). The effect analysis statistics are presented for each period (day) after acaricidal treatment (DDT).
Discusión
En el presente estudio se evaluó el efecto tóxico letal y la supresión poblacional de extractos etanólicos (EE) de hojas de A. compressa y acaricidas botánicos comerciales en T. urticae. En la evaluación de efecto tóxico letal (6 y 12 h) se observó que los EE de Ardisia YRP y Ardisia CTia fueron los más tóxicos (35 - 38 % de mortalidad) y en el caso de los acaricidas botánicos comerciales los aceites de Zea mays y Glycine max fueron los más efectivos (54 - 81 % de mortalidad). Se podría considerar entonces que los EE de Ardisia tuvieron efectos tóxicos letales intermedios y los acaricidas botánicos comerciales tuvieron efectos altos. En trabajos con extractos vegetales experimentales se ha visto hasta 70 % de mortalidad de adultos de T. urticae, como es el caso de los extractos etanólicos de Chenopodium quinoa y Solanum nigrum (Harder et al., 2016; Vergel et al., 2016). Incluso, extractos metanólicos de Ardisia japónica causaron mortalidad del 75. 6 % en T. urticae, pero hasta las 48 h después de la aplicación (Lee et al., 2011). El efecto tóxico letal en los extractos de Ardisia se puede atribuir a la presencia de metabolitos secundarios como polifenoles, saponinas, triterpenoides y quinonas (De Mejía y Ramírez-Mares, 2011; Amin et al., 2015). Estos grupos de metabolitos secundarios han mostrado efectividad sobre especies de ácaros fitófagos (Sivira et al., 2011; Ebadollahi et al., 2016).
Para el caso de los acaricidas a base de aceite de Zea mays y Glycine max tuvieron efectos tóxicos letales altos. El aceite orgánico de especies vegetales se ha usado para el desarrollo de acaricidas o insecticidas químicos. por ejemplo, el aceite de oliva (Olea europaea), clavo (Syzygium aromaticum) y ricino (Ricinus communis), pueden ocasionar hasta 100 % de mortalidad de T. urticae en las primeras 72 h después de la aplicación (Bashiri et al., 2021; Meteab et al., 2021). En los últimos 20 años el aceite a base de Glycine max ha mostrado actividad tóxica contra ácaros, y al igual que en el presente estudio se ha documentado hasta 85 % de mortalidad entre las 24 a 72 horas de su aplicación (Moran et al., 2003; Baker et al., 2018; Bashiri et al., 2021). La alta efectividad del aceite de Glycine max en la supresión poblacional de ácaros ha sido documentada en varios estudios (Lancaster et al., 2002; Nexticapan-Garcéz et al., 2021), ya que el efecto toxico letal sobre los ácaros puede estar relacionado con la asfixia por el bloqueo de espiráculos de adultos e inmaduros (Umetsu y Shirai, 2020) o metabolitos secundarios presentes en los aceites, como taninos, terpenos, fenoles (Mex-Álvarez et al., 2016; Nawaz et al., 2018), flavonoides y saponinas (Dixit et al., 2011; De la Rosa et al., 2012; Da Graca et al., 2016), donde se ha observado que estos compuestos tienen alta efectividad en ácaros fitófagos (Tak e Isman, 2017; Heinz-Castro et al., 2021).
Con respecto a las evaluaciones en invernadero los EE de Ardisia YRP y Ardisia CTia, nuevamente resultaron ser los más efectivos en la supresión de la densidad poblacional de adultos y ninfas de T. urticae. Para el caso de los acaricidas botánicos comerciales nuevamente los acaricidas a base de aceites Zea mays y Glycine max tuvieron los efectos más altos. Existe poca información sobre extractos etanólicos en condiciones de invernadero o campo, sin embargo, se ha podido documentar en estudios de laboratorio que extractos etanólicos de Ardisia japónica, Magnolia alejandrae y Moringa oleífera son efectivos manteniendo su efecto al día 1 hasta 3 días posterior a su aplicación (Lee et al., 2011; Heinz-Castro et al., 2021; Olazaran-Santibañez et al., 2024), de igual manera los aceites Zea mays y Glycine max su efecto puede mantenerse al día 1 a 14 días posteriores a su aplicación (Nexticapan-Garcéz et al., 2021; Cua-Basulto et al., 2023), estos resultados sugieren el potencial de extractos etanólicos y acaricidas botánicos para el manejo de ácaros fitófagos.
Con base en los resultados de este estudio, el uso de EE de Ardisia y aceites botánicos comerciales a base de Zea mays y Glycine max son eficaces para el manejo de T. urticae y es necesario continuar con evaluaciones de campo en varios cultivos para validar la efectividad de los tratamientos.
Conclusiones
Los EE de Ardisia YRP y Ardisia CTia y los acaricidas botánicos comerciales a base de aceite Glycine max y Zea mays causaron alta mortalidad de adultos de T. urticae en laboratorio. Estos tratamientos también tuvieron alta efectividad en la supresión de la densidad poblacional de adultos, ninfas y huevos de T. urticae en condiciones de invernadero. Los extractos etanólicos de Ardisia compressa y los aceites botánicos comerciales son una alternativa efectiva para el manejo de T. urticae en la agricultura.











 nueva página del texto (beta)
nueva página del texto (beta)



