Presentación del caso
Paciente varón de 67 años, hipertenso con más de 20 años de evolución que a los 44 años de edad padeció infarto de miocardio con elevación del segmento ST de localización ínfero-posterior, no reperfundido. En angiografía coronaria se detectó enfermedad coronaria grave trivascular y luego fue intervenido de cirugía de revascularización miocárdica (arteria mamaria interna izquierda a descendente anterior, arteria radial izquierda a descendente posterior y vena safena a arteria del margen obtuso), sin embargo, con evolución hacia insuficiencia cardiaca avanzada con fracción de eyección del ventrículo izquierdo 18% e hipocinesia global. Tras cuatro hospitalizaciones por insuficiencia cardiaca, a los 57 años (agosto del 2013) fue intervenido de trasplante cardiaco ortotópico bicaval, con buena evolución clínica postoperatoria y adecuada tolerancia a fármacos inmunosupresores (tacrolimús, micofenolato de mofetilo y prednisona).
Tres semanas posteriores a la cirugía se realizó biopsia endomiocárdica (BEM) (Fig. 1A), por abordaje femoral, con obtención de seis muestras del septum interventricular (medial y apical) de ventrículo derecho, cuyo resultado arrojó rechazo leve tipo 1 Quality 2, realizándose seguimiento clínico estrecho. La ventriculografía posbiopsia descartó complicaciones inmediatas (Fig. 1B). Tres semanas después de la primera BEM se realizó angiografía coronaria invasiva (ACI) (Fig. 1 C D) con hallazgo de dos pequeños aneurismas sobre arteria descendente anterior y fístula coronaria que comunicó arteria descendente anterior con el ventrículo derecho; descartándose estenosis coronaria significativa. El paciente no presentó síntomas asociados, por lo cual se decidió seguimiento clínico.
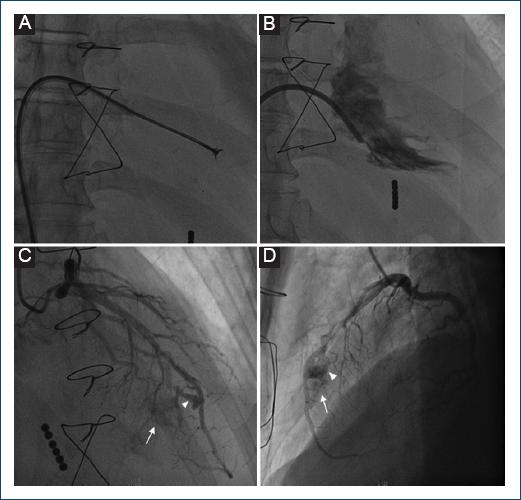
Figura 1 A: toma de biopsia endomiocárdica (BEM) en septum de ventrículo derecho (apical y medio). B: ventriculografía posbiopsia. C y D: angiografía coronaria invasiva (ACI) en el año 2013. Dos pequeños aneurismas (puntas de flecha) de dimensiones 5.9 x 2.8 y 3.1 x 1.5 mm sobre arteria descendente anterior y fístula coronaria (flecha) que comunica sus ramos septales con el ventrículo derecho.
Entre los años 2013 y 2018 se realizaron siete BEM con el mismo resultado patológico de la primera biopsia, sin complicaciones durante la intervención. Asimismo, en 2017 se realizó nueva ACI (Fig. 2 A B). En el año 2023 se realizó nueva BEM y ACI de rutina (Fig. 2 C D). La ecocardiografía transtorácica no logró determinar derivación izquierda-derecha significativa, con tamaño de cavidades cardiacas dentro del rango de normalidad y adecuada función biventricular.
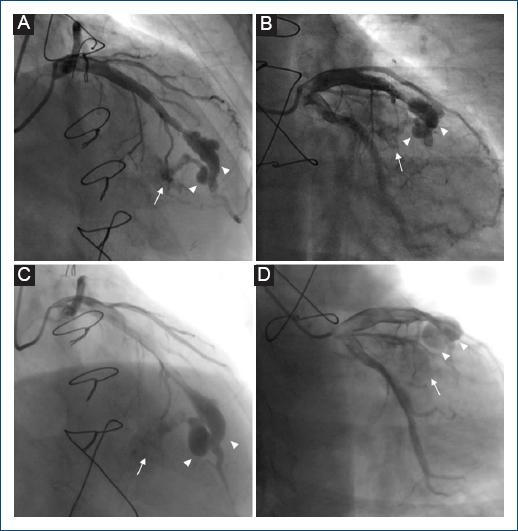
Figura 2 A y B: angiografía coronaria invasiva (ACI) en el año 2017. Aneurismas (puntas de flecha) de dimensiones 20.6 x 7.6 mm y 7.2 x 4.5 mm sobre arteria descendente anterior y fístula coronaria (flecha) que comunica sus ramos septales con el ventrículo derecho. C y D: angiografía coronaria invasiva (ACI) en el año 2023. Aneurismas (puntas de flecha) de dimensiones 21.5 x 7.9 mm y 14.9 x 8.8 mm sobre arteria descendente anterior y fístula coronaria (flecha) que comunica sus ramos septales con el ventrículo derecho.
En este reporte ilustramos la evolución angiográfica de 10 años de seguimiento de aneurismas y fístula coronarios secundarios a biopsia endomiocárdica en un paciente postrasplantado cardiaco, con evolución asintomática, en el cual se decidió tratamiento médico y seguimiento clínico.
Discusión
Las fístulas coronarias son conexiones (congénitas o adquiridas) entre una arteria coronaria y otra estructura (vaso sanguíneo o cavidad cardiaca) que producen derivación sanguínea desde la cavidad de mayor presión a la de menor presión1. Las fístulas coronarias adquiridas son una complicación rara de las cirugías cardiacas, sin embargo se pueden presentar en entre el 8-20% de los casos dentro del primer año postrasplante cardiaco. El mecanismo que las produce es incierto, pero se propone la activación de factores de crecimiento endoteliales y vasculares por injuria. Además, el tratamiento con tacrolimús y micofenolato de mofetilo se destacó como factor asociado1,2.
Las conexiones adquiridas más frecuentes son las de la arteria coronaria derecha (55%) o la descendente anterior (39%) hacia cavidades de baja presión (90%) como el ventrículo derecho, la arteria pulmonar, la aurícula derecha y venas sistémicas. El origen en circunfleja (6%), tronco de coronaria izquierda (< 1%) o puente de arteria mamaria interna (< 1%) es anecdótico. La participación del ventrículo izquierdo (3%) es infrecuente y se asocia a complicaciones (médicas y quirúrgicas) graves en el postoperatorio de trasplante cardiaco2.
La BEM es un procedimiento que se realiza en promedio 14 veces durante el primer año postrasplante para la detección y seguimiento del rechazo del injerto3. Pese a que la tasa de complicaciones en general (0.71%) y específicamente de fístulas coronarias hacia el ventrículo derecho (0.2%) relacionadas con BEM es baja, el riesgo de padecer una fístula coronaria posterior a BEM varía del 5 al 14% por paciente a lo largo del seguimiento4.
Existen discrepancias en relación con la mejor técnica para realizar la BEM. Algunos operadores defienden el abordaje venoso yugular sobre el femoral, debido a la posición septal baja que adopta el biotomo con el fin de disminuir el riesgo de perforación/taponamiento. Asimismo, la BEM guiada por imágenes (resonancia magnética y tomografía por emisión de positrones) ha demostrado disminuir la tasa de complicaciones al evitar toma de muestras en zonas de infiltración grasa o adelgazamiento/aneurismas del ventrículo derecho. Otros autores promueven el abordaje retrógrado (arterial) en lugar del anterógrado (transvenoso) para pacientes con riesgo de perforación miocárdica5. Además, es probable que un número mayor de muestras tomadas en cada procedimiento pueda predisponer a tasas más altas de este tipo de complicaciones1. El carácter repetitivo del procedimiento en pacientes trasplantados incrementa la incidencia de fístulas coronarias.
La presencia de aneurisma (dilatación luminal y localizada de la arteria coronaria ≥ 1.5 veces del diámetro de referencia normal adyacente) asociado a fístula coronaria en pacientes trasplantados posterior a BEM es un hallazgo infrecuente. Probablemente el desarrollo temprano de vasculopatía del injerto influya en la génesis de los aneurismas en estos pacientes. En algunos casos los aneurismas coronarios pueden presentarse como el principal hallazgo de vasculopatía del injerto6.
A pesar de que la forma más frecuente de vasculopatía del injerto es el remodelamiento negativo; algunos pacientes pueden desarrollar remodelamiento positivo y aneurismas. En cuanto a las bases biomoleculares, se sabe que la expresión de TH1, bajo el estímulo de interferón Ȣ (y otras citocinas) desarrolla remodelado negativo a expensas de tres procesos: incremento del tono de la media, hiperplasia de la íntima y fibrosis de la adventicia; cuya consecuencia es estenosis concéntrica y difusa del lecho vascular. Por otro lado, y menos frecuentemente, la expresión de TH2, que media la influencia de IL-4, promueve la sobreexpresión de metaloproteinasas de matriz (MMP 3, 9 y 12), las cuales degradan excesivamente los componentes de matriz extracelular resultando en remodelado positivo y eventualmente la formación de aneurismas7.
Cada vez son mayores los esfuerzos por diagnosticar y tratar tempranamente a los pacientes con vasculopatía del injerto con fenotipo obstructivo, pero poco se ha descrito acerca de la descripción, estadificación y progresión de la vasculopatía con remodelado positivo y formación de aneurismas8.
En la actualidad existe mucha discusión en relación con el manejo de los aneurismas coronarios. El control de los factores de riesgo cardiovasculares y el tratamiento médico (estatinas, inhibidores de la enzima convertidora de angiotensina, antiagregantes), suele indicarse cuando coexiste ateroesclerosis, una asociación frecuente. La doble antiagregación o anticoagulación podría tener lugar en pacientes con síndrome coronario agudo y coronarias francamente ectásicas. En pacientes con oclusión coronaria, restablecer el flujo es mandatorio, estando indicado el tratamiento percutáneo (incluso considerando el riesgo inminente de no reflujo y embolia distal), la trombólisis (mecánica/farmacológica) o los inhibidores IIb/IIIa. En pacientes con angina estable en relación clara con aneurisma coronario, se debe evaluar el riesgo/beneficio de la intervención; podrían tener lugar los stents cubiertos y la exclusión con espirales asistida con stents. Aunque con escasa evidencia, la intervención quirúrgica tendría lugar en aneurismas gigantes, complejos o que comprometen el tronco de la coronaria izquierda9.
Trasladar todas estas indicaciones a los pacientes con aneurismas postrasplante no sería adecuado, debido a las diferencias en los procesos fisiopatológicos y a que no existe evidencia clara para intervenir los aneurismas coronarios diagnosticados incidentalmente y que no producen síntomas.
Algunos estudios demostraron que la gran mayoría de aneurismas-fístulas postrasplante cardiaco presentan curso asintomático y entre el 1 y 2% se cierran espontáneamente1,3. La aparición de nuevos síntomas, el deterioro hemodinámico y de la clase funcional suelen ser la principal indicación para el cierre por intervención. En algunos reportes la inducción de isquemia significativa también apoyó la decisión de intervenir10.
Se reportaron algunos casos exitosos de exclusión de aneurismas-fístulas coronarias hacia cavidades derechas con stents cubiertos4,10.
En este reporte describimos la evolución a lo largo de diez años de dos aneurismas coronarios en crecimiento asociados a una fístula que drena en cámara cardiaca derecha, en un paciente con corazón trasplantado, asintomático y sin repercusión hemodinámica; para el cual las indicaciones de intervención (percutánea o quirúrgica) aún no son claras.











 nueva página del texto (beta)
nueva página del texto (beta)


