Introducción
El cáncer es una enfermedad que ha acompañado al ser humano en el transcurso de su historia. A Hipócrates, (460-375 a.C.), se le atribuye el acuñar el término “cáncer” del griego Καρκίνος (karkinos), quien lo utilizó para hacer referencia a su aspecto clínico, al visualizar masas tumorales que al ulcerarse asemejaban la forma y consistencia de un cangrejo (Hajdu, 2011).
Con el paso del tiempo, al cáncer finalmente se le define como un conjunto de neoplasias malignas que tienen en común la proliferación celular sin control, de forma autónoma y en más de un caso invaden no sólo el tejido local sino otros tejidos distantes. También, se sabe que en la génesis del cáncer participan una serie de protooncogenes y genes supresores de tumores, que codifican para los componentes que participan en múltiples vías de transducción de señales. Tradicionalmente, se les ha atribuido a estos elementos un papel importante en la regulación del ciclo celular y mantenimiento de las señales proliferativas que contribuyen a evadir la supresión del crecimiento y la muerte celular (Mendiola & Soto, 2014).
No obstante, en los últimos años con el conocimiento adquirido y la evidencia, se han desarrollado propuestas que señalan como principal función, de los oncogenes y de los genes supresores de tumores, a la reprogramación del metabolismo celular. Esto debido a que la alteración del metabolismo energético es una de las principales diferencias que existen entre las células normales y las células cancerígenas. A diferencia de las células normales, las células tumorales utilizan principalmente la glucólisis anaerobia para producir energía incluso en presencia de suficiente oxígeno, evento conocido como efecto Warburg (Herrera-González, Martínez-García & Mejía-Jiménez, 2015).
Metabolismo del cáncer
La historia actual, sobre el conocimiento de los factores que participan en el desarrollo del cáncer, es producto de un largo proceso en el que han intervenido diversos investigadores y criterios. Es así que, en décadas más recientes, el estudio del cáncer tiene como objetivo el encontrar las bases moleculares que lo desarrollan mediante la búsqueda de alteraciones genéticas y con el apoyo de las nuevas tecnologías llevar a cabo un análisis genómico, especialmente, la secuenciación genómica a gran escala. Para realizarlo, se creó un proyecto internacional llamado el Atlas del Genoma del Cáncer (TCGA, por sus siglas en inglés, The Cancer Genome Atlas) (Green, Watson & Collins, 2015). Los investigadores al analizar los datos del TCGA, encontraron un grado de heterogeneidad intra e inter-tumoral muy elevado. Los resultados dificultaron identificar una mutación única o combinaciones de mutaciones indispensables para el inicio de la enfermedad (Reiter et al., 2019). Este hallazgo puso de manifiesto que los tumores son entidades más complejas y que, además de la participación de las mutaciones, también intervienen otras funciones celulares. Sin embargo, el conocimiento de cómo operan las mutaciones ha ayudado tanto en el diagnóstico como en el tratamiento de la enfermedad (Seol et al., 2012). Es así, que los investigadores y médicos además de considerar al cáncer como una enfermedad genética, retoman el concepto de una enfermedad metabólica, un aspecto que se propuso el siglo pasado (Warburg, 1956).
Efecto Warburg
Otto Warburg, científico alemán y ganador del premio Nobel en 1931, es reconocido por experimentar con la fermentación de glucosa y el consumo de oxígeno en las células tumorales. Durante sus investigaciones, Warburg midió el consumo de oxígeno en los tejidos normales del hígado y del riñón de rata, que comparó con los tejidos del trasplante de un tumor en las vesículas seminales. En sus experimentos encontró pocas diferencias entre la respiración de los tejidos tumorales y los tejidos normales. También, estudió la producción de lactato como una medida de la tasa de fermentación y encontró que bajo condiciones anaeróbicas todos los tejidos mostraban un aumento en la producción de este metabolito. En contraste, bajo condiciones aeróbicas el comportamiento de los tejidos tumorales produjo una tasa elevada de lactato y los tejidos normales no. Warburg, también observó que las células cancerosas no producían más ni menos energía que las células normales, porque la acción se realiza diferente. Posteriormente, descubrió que el metabolismo del cáncer es deficiente en todos los tipos de células tumorales, sin excepción. Al estar seguro de ello, concluyó que es la causa principal de los efectos secundarios.
Por consiguiente, el paso de la generación de energía aeróbica a la anaeróbica es otra diferencia entre las células cancerosas y las normales. A este hallazgo, se le nombró glucólisis aeróbica por la fermentación de la glucosa, incluso, en la presencia de abundante oxígeno. Situación que se confirmó en la mayoría de las neoplasias, de forma que, con el paso del tiempo, se ha propuesto que esta característica se utilice como un pronóstico de la enfermedad e incluso como blanco farmacológico en la oncoterapia (Dayton, Jacks & Vander Heiden, 2016; Otto, 2016).
Efecto Warburg y el cáncer como patología metabólica
Una de las interrogantes a lo largo del tiempo ha sido el papel del metabolismo energético de las células en el desarrollo del cáncer. Como ya se mencionó, se ha observado que en las células cancerosas el metabolismo energético debe reajustarse como respuesta a las nuevas demandas de una proliferación excesiva; las células normales en condiciones aeróbicas utilizan la fosforilación oxidativa como principal fuente de energía. En el proceso oxidativo de una molécula de glucosa a CO2 se obtiene como resultado final alrededor de 30-32 moléculas de adenosina trifosfato (ATP), diferente a las células en condiciones anaerobias -fermentación láctica- que generan sólo 2 moléculas de ATP. Este último mecanismo es muy utilizado por las células neoplásicas (Vazquez, Liu & Oltvai, 2010; Lehninger, Nelson & Cox, 2019; Bose, Zhang & Le, 2021).
Por otra parte, a nivel celular existe un estrecho vínculo entre la biología del cáncer y la glucosa, puesto que el procesamiento de esta última se encuentra meticulosamente regulado a través de la activación y el silenciamiento de múltiples genes tumorales que conducen a la proliferación desmedida, al arresto del ciclo celular, y al envejecimiento de la célula (Vander Heiden & DeBerardinis, 2017). Las células neoplásicas pierden muchos de sus puntos de control, por la inactivación o mutación de los genes supresores de tumores, y por la amplificación de los oncogenes; todas estas alteraciones resultan en una transcripción aberrante con regulación al alza de las cinasas dependientes de la ciclina (CDKs) cuyo resultado es una progresión del ciclo celular y una mitosis descontroladas (Icard, Fournel, Wu, Alifano & Lincet, 2019). A este respecto, es importante mencionar que p53 es uno de los genes con mutaciones muy frecuentes en las células cancerosas, además de ser un regulador positivo de la respiración mitocondrial y un regulador negativo de la glucólisis. Por lo tanto, estos y más factores conducen a la sobreexpresión de los transportadores de glucosa y de diversas enzimas de la vía que ayudan a explicar la absorción de este azúcar y las alteraciones que se producen durante su uso (Matoba et al., 2006; Bensaad et al., 2006).
Bioquímica y biología molecular de la PKM2
En las células cancerosas la glucólisis aeróbica es una vía metabólica cuya acción predomina debido a su capacidad para desviar la producción del ATP hacia la síntesis de componentes con el fin de satisfacer las altas demandas de proliferación de la enfermedad. Una de las enzimas de la glucólisis es la piruvato cinasa (PK), regulada a detalle, para catalizar el último paso irreversible de la glucólisis, es decir, media la transferencia de un grupo fosforilo del fosfoenolpiruvato (PEP) a la adenosina difosfato (ADP) para producir piruvato y energía en forma de ATP (Hsu & Hung, 2018), (Figura 1).
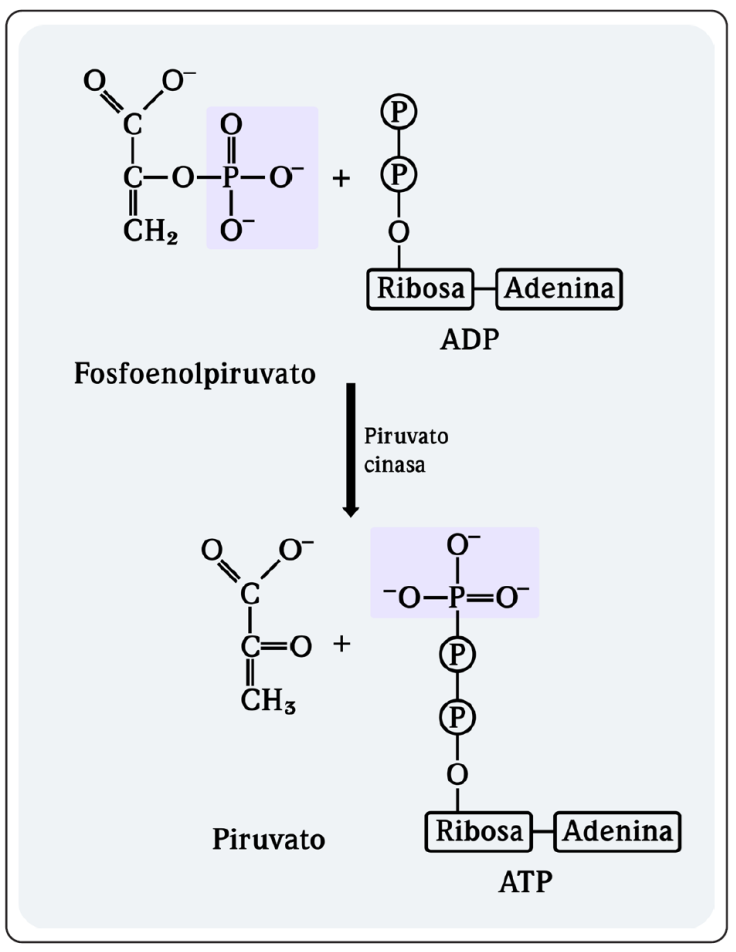
Figura modificada de Lehninger, Nelson & Cox, 2019.
Figura 1 El último paso de la glucólisis es la transferencia del grupo fosforilo desde el fosfoenolpiruvato al ADP catalizado por la PK.
La concentración de oxígeno determina los dos caminos que sigue el piruvato, ya sea a través de la vía de la fosforilación oxidativa o a través de la enzima lactato deshidrogenasa. En las células normales y condiciones aeróbicas, el piruvato es captado en las mitocondrias, y posterior a la descarboxilación oxidativa, se convierte en acetil-CoA, entra al ciclo del ácido cítrico donde ocurre la oxidación y se transforma en CO2 y H2O. Por otra parte, en las células normales en condiciones anaeróbicas, el piruvato es reducido a lactato a través de la enzima lactato deshidrogenasa (Murray, Bender & Bothman, 2013).
En los mamíferos existen 4 isoformas, de la PK, codificadas por dos genes: el gen PKLR que codifica para PKL y PKR. El gen PKL que se expresa principalmente en los hepatocitos, en algunas células del páncreas, en el intestino y el riñón, diferente al gen PKR que se expresa sólo en los eritrocitos (Figura 2A). El gen PKM codifica a la PKM1 y la PKM2 (exon 9 para la PKM1 y exon 10 para la PKM2), mediante un proceso de splicing alternativo de exones mutuamente excluyentes que son idénticos en tamaño, pero que a su vez codifican a una región de 56 aminoácidos de los que 22 residuos son distintos. A pesar de esta diferencia, ambas isoformas realizan la misma función catalítica: el paso irreversible de PEP a piruvato. La principal diferencia consiste en que PKM1 es una enzima tetramérica constitutivamente activa que se expresa principalmente en el corazón, el músculo esquelético, el músculo liso, el cerebro, la médula adrenal y los espermatozoides maduros. En lo que concierne a la PKM2 se manifiesta durante la embriogénesis, los procesos regenerativos y el cáncer, lo que sugiere el desempeño de un papel importante en las células con una alta tasa proliferativa. Aunque también se puede encontrar en los leucocitos, las células del túbulo distal del riñón, el parénquima pulmonar, el intestino, el timo, en las células de los islotes pancreáticos, la grasa blanca, el bazo, los ovarios, la médula adrenal y los testículos (Hsu & Hung, 2018), (Figura 2B).
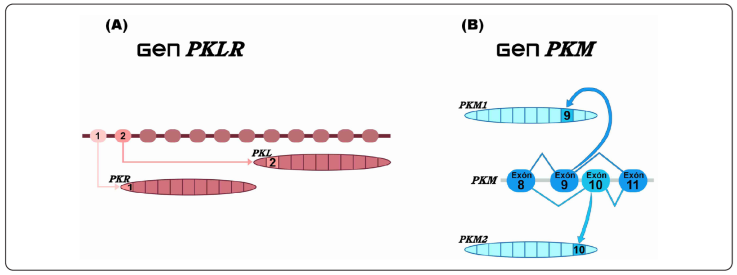
Figura modificada de Dayton, Jacks & Vander Heiden, 2016.
Figura 2 (A) El gen PKLR codifica las isoformas PKL y PKR a través de promotores específicos en cada tejido. (B) El gen PKM codifica a las isoformas PKM1 y PKM2 a través de un splicing alternativo de los exones 9 y 10 mutuamente excluyentes.
La expresión de la PKM2 puede oscilar entre una alta actividad en su forma tetramérica y menor actividad catalítica en su forma dimérica. Se ha descrito que si es tetramérica se encuentra en las células normales como las descritas previamente y tanto la dimérica como la tetramérica están en las células tumorales (Liu et al., 2019).
PKM2 y el oncometabolismo
Las PKs en la glucólisis catalizan la transferencia de un grupo fosforilo del PEP al ADP, lo que genera una molécula de ATP y otra de piruvato que en el Ciclo de Krebs producen acetil-CoA y citrato.
Se ha comprobado que en las células tumorales existe la presencia de la PKM2 tetramérica, sin embargo, la PKM2 dimérica es más importante en el oncometabolismo, debido a que la enzima PKM2 dimérica tiene una actividad catalítica significativamente menor, lo que conduce a una restricción de la ruta metabólica. Este -freno previo al último paso de la glucólisis- genera una acumulación de metabolitos intermediarios que producen abundantes macromoléculas celulares requeridas en la biosíntesis, para una rápida proliferación de las células tumorales (He et al., 2017), (Figura 3).
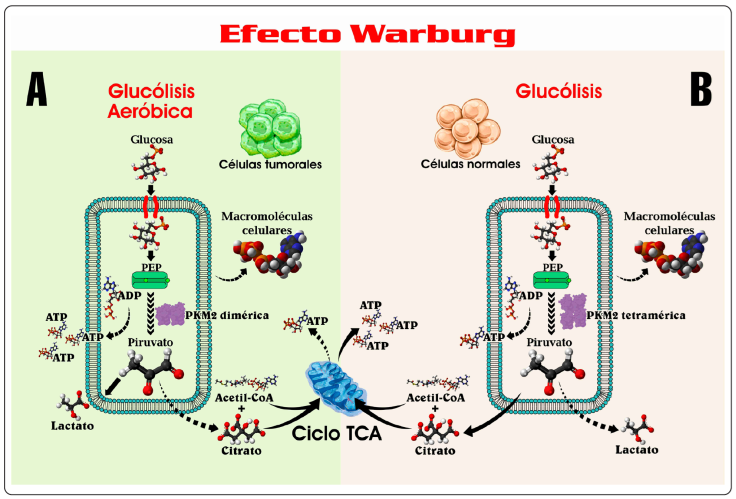
Figura modificada de He et al., 2017.
Figura 3 Efecto Warburg. (A) El dímero de la PKM2 media la glucólisis aeróbica para producir más ácido láctico en las células tumorales. (B) El tetrámero de la PKM2 en las células normales cataliza la producción del ATP y el piruvato para el TCA posterior. Abreviaturas: ADP: Adenosina Bifosfato; ATP: Adenosina Trifosfato; PEP: Fosfoenolpiruvato; PKM2: Piruvato Cinasa Isoforma M2; TCA: Ciclo de los Ácidos Tricarboxílicos.
También existen una serie de modificaciones que afectan la función de la PKM2 y el resultado es un ambiente propicio para el crecimiento tumoral. Como se mencionó, esta enzima es más activa como tetrámero. Por lo tanto, la regulación alostérica se consigue mediante la estabilización o desestabilización de su conformación tetramérica, por lo que se han descrito diversas modificaciones postraduccionales y/o proteicas que actúan transformando a la PKM2, estos cambios se describen en la Tabla I. Por lo que se refiere a la forma dimérica se localiza en distintas zonas intracelulares, por ejemplo: ingresa al núcleo para regular la expresión génica y se une a la membrana externa mitocondrial para mantener su función. Así mismo, la transición entre el dímero y el tetrámero es regulada alostéricamente, en la que el dímero presenta la actividad más baja y la unión de su activador, la fructosa 1,6 bisfosfato (FBP), promueve la formación del tetrámero activo (Zhang et al., 2019).
Tabla I Moléculas que interactúan con la PKM2 y sus funciones en el metabolismo del cáncer.
| Molécula | Función |
|---|---|
| Receptor del Factor de Crecimiento de Fibroblastos (FGFR) | La fosforilación en residuos de tirosina 105 (Y105) por FGFR actúa reduciendo la actividad de la enzima PKM2 y provoca la liberación de la FBP (Hitosugi et al., 2009) |
| v-Src | La fosforilación de la PKM2 en Y105 por v-Src provoca una disminución de la afinidad que posee la PKM2 por su sustrato (PEP). Por lo que, la FBP tampoco puede unirse al tetrámero de la PKM2 y por lo tanto disminuye además de su estabilidad, así como se reduce su capacidad glucolítica (Wong, Ojo, Yan & Tang, 2015) |
| Acetiltransferasa PCAF | La acetilación de la lisina 305 (K305) reduce la actividad de la PKM2 y promueve su degradación en los lisosomas a través de la autofagia mediada por chaperonas (Lv et al., 2011) |
| Proteína E7 | La proteína oncogénica E7, del virus del papiloma humano, induce la acetilación de la PKM2 en la K433 e inhibe la unión de FBP que a su vez también disminuye la actividad glucolítica de la PKM2 así como su potencial proliferativo en las células tumorales (Lv et al., 2013) |
| Rapamicina | La inhibición con rapamicina, de forma directa, a mTOR o a alguno de sus precursores en la vía PI3K-AKT-mTOR es causa de una expresión disminuida de la PKM2 (DeBerardinis & Chandel, 2016; Xiaoyu et al., 2018) |
| Proteína de la leucemia promielocítica citosólica (PML) | Reduce la actividad de la PKM2 tetramérica; probablemente estimula el metabolismo del cáncer (Gupta & Bamezai, 2010) |
| Receptor de prolactina | Inhibe la actividad de la PKM2; incrementa la glucólisis aeróbica y la proliferación celular (Wong et al., 2015) |
| MUC1-C | La oncoproteína mucina 1 (MUC1-C) que fosforila en Y46 se une a la PKM2 en la K433 e inhibe la actividad de la PKM2 y aumenta la glucólisis aeróbica (Kosugi, Ahmad, Alam, Uchida & Kufe, 2011) |
| HIF-1 | HIF-1 se une a un elemento de respuesta a la hipoxia dentro del primer intrón de la PKM2 y activa directamente su transcripción (Guo et al., 2019) |
| Oct-4 | A nivel nuclear, la PKM2 se une a Oct-4 a través de su región C-terminal y mejora la transcripción mediada por Oct-4; promueve la autorrenovación y la proliferación de las células tumorales (Lee, Kim, Han & Kim, 2008) |
| β-catenina | A nivel nuclear, la β-catenina se asocia con la PKM2 e inducen la transactivación de CCND1 y MYC, lo que origina la proliferación tumoral (Wong et al., 2015) |
| Histona H3 | PKM2 se une a la histona H3 en la posición T11 y se activa la Ciclina D1 y MYC (Yang et al., 2012) |
| Vitamina D | Disminuye la expresión de la PKM2 y otras proteínas relacionadas con el efecto Warburg tanto in vivo como in vitro (Yiyan, Yang, Li & Li, 2022) |
PKM2 en la carcinogénesis
Angiogénesis
Uno de los factores clave en el desarrollo tumoral es la angiogénesis, ésta se define como la generación de nuevos vasos sanguíneos provenientes de los ya preexistentes. Es un proceso en extremo complejo, pero necesario para generar el microambiente de las células tumorales. Está conformado por la disrupción de la matriz extracelular, la migración y la proliferación de las células endoteliales, reguladas por múltiples factores como, el del crecimiento vascular endotelial (VEGF) (Viallard & Larrivée, 2017).
La presencia en sangre de la PKM2 dimérica promueve la angiogénesis tumoral al aumentar la proliferación de las células endoteliales, la migración y la adhesión de las células a la matriz extracelular que por lo general facilitan el crecimiento tumoral (Li, Zhang, Qiao, Yang & Liu, 2014). Así mismo, la hipoxia favorece la translocación de la PKM2 y p65 al núcleo, promueve la transcripción de HIF-1α y sus genes blanco, entre ellos VEGF-A, el resultado es un aumento en la formación de los vasos sanguíneos que a su vez, también, contribuyen al crecimiento tumoral. Existen varios RNAs no codificantes que regulan la expresión de PKM, incluidos miR-148a, miR -152, miR-199a, miR-222, miR-138 y let-7a. Estos RNAs no codificantes se unen directamente a la región no traducida (UTR) 3’ de los RNA mensajeros de la PKM2 y disminuyen la síntesis de la proteína PKM2, pero en el cáncer la región del DNA que codifica para los RNAs no codificantes se encuentra hiper- metilada. El silenciamiento de miR-148a/152 contribuye a la sobreexpresión de la PKM2, NF-κB o IGF-IR en algunas células cancerosas. La interrupción del circuito de retroalimentación negativa PKM2/NF-κB/miR-148a/152 regula el crecimiento de las células cancerosas y la angiogénesis, esto se ha visto en las células de cáncer de mama triple negativo, uno de los tumores más agresivos (Xu et al., 2015; Zahra, Dey, Ashish, Mishra & Pandey, 2020).
Metástasis
Las neoplasias malignas se caracterizan por infiltrarse a los tejidos subyacentes y a la metástasis. En las células DLD1, la sobreexpresión de la PKM2, especialmente en su forma dimérica muestra un incremento en los niveles de metaloproteinasa 2 y 9 (MMP-2, MMP-9) y Snail-2, diferente a los niveles de E-cadherina que han disminuido. Además, se ha reportado que dentro del núcleo celular la sobreexpresión de la PKM2 aumenta la sobreexpresión del gen STAT3 que codifica a la proteína del mismo nombre, clave en la migración, en la invasión y en la motilidad de las células tumorales. Por lo tanto, STAT3 facilita la invasión tumoral y la metástasis a través de un aumento en la expresión de MMP-2 y MMP-9 (Yang, Li, Fu, Wu & Li, 2014). Estos resultados son de suma importancia, al existir más evidencia del potencial metastásico de la PKM2, lo que conlleva a que en algunos años se desarrollen objetivos terapéuticos más selectivos.
Apoptosis
El microambiente celular de los tejidos neoplásicos tiene una alta concentración de especies reactivas de oxígeno (ROS) producto de un mal funcionamiento mitocondrial y una alta tasa de actividad metabólica. Situación que en condiciones normales conducen a la célula a la apoptosis, sin embargo, en las células tumorales existen una serie de mecanismos adaptativos que les permiten soportar estas condiciones que inhiben la apoptosis. El primer paso es la interacción de la PKM2 con la proteína chaperona HSP90 en el citoplasma, lo que altera la conformación estructural de la enzima y se trasloca dentro de la mitocondria donde fosforila a Bcl2 en T69. La fosforilación de Bcl-2 evita la unión con E3 ligasa y la subsecuente degradación, de esta forma evade una de las vías de la apoptosis. Además, la sobreexpresión de la PKM2 estabiliza la subunidad p65 de NFkB al promotor Bcl-XL (proteína anti-apoptótica), inhibe la apoptosis y promueve el crecimiento celular como el de las células tumorales gástricas, en las que se vieron las funciones descritas (Kwon et al., 2012; He et al., 2017).
Oncoterapia
El proceso del desarrollo del cáncer es complejo e implica una serie de mecanismos que dan como resultado la proliferación celular descontrolada, el papel que tiene la PKM2, especialmente en su forma dimérica, es crucial para que esto suceda. Debido al protagonismo que la PKM2 tiene en las neoplasias de rápido crecimiento, es que desde hace varios años se ha buscado utilizarla como blanco farmacológico en la oncoterapia (Figura 4). Por lo que se han estudiado distintos activadores e inhibidores descritos a continuación:
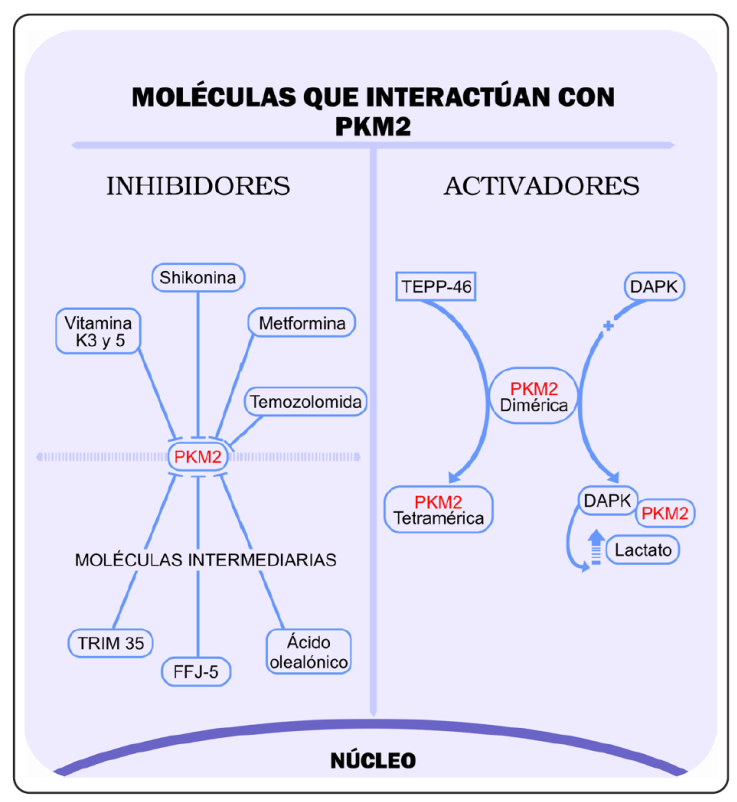
Figura, creatividad personal.
Figura 4 Esquema que representa las diferentes interacciones de diversas moléculas con la PKM2.
Activadores e inhibidores de la PKM2
Activadores de la PKM2
La mayor parte de los compuestos activos que interactúan con la PKM2 inhiben su actividad, sin embargo, se ha propuesto que los activadores de la PKM2 incrementarían su actividad, para ser comparable con la PKM1 a través del cambio de dímero a tetrámero, la molécula con esta capacidad es conocida como TEPP-46, sin embargo, sólo se ha estudiado en los ratones. Otra de las moléculas implicadas en la activación de la PKM2 es la Proteína Cinasa Asociada a la Muerte (DAPK), una serina-treonina cinasa que se une a la PKM2 y aumenta su actividad, mecanismo por el que disminuye la producción de intermediarios útiles en el crecimiento celular (Mor, Carlessi, Ast, Feinstein & Kimchi, 2012). Estudios recientes demuestran que la molécula sintetizada 15n (una imidazopirimidina), actúa como un activador de la PKM2 en algunos tipos de células cancerosas con una AC50 de 90 nM. Estudios de dinámica molecular mostraron que 15n estabiliza a la interfaz dimérica de la PKM2, lo que promueve la formación del tetrámero; la forma, biológica, más activa. El tratamiento de la línea celular de cáncer de mama MCF-7 con 15n promueve la disminución de la concentración del lactato, lo que demuestra que la forma dimérica se convierta en tetramérica. Con base en estos resultados, se propone que para una terapia efectiva contra el cáncer se usen moléculas pequeñas como 15n que se unan a la PKM2 para una conformación tetramérica de alta actividad, pero también a la par se pueden utilizar moléculas inhibidoras de la actividad enzimática (Patel et al., 2022).
Inhibidores de la PKM2
a) Inhibidores directos
La shikonina es el principal componente bioactivo extraído de las raíces de Lithospermum erythrorhizon. Múltiples estudios confirman que la shikonina tiene un efecto antitumoral en varios tipos de cáncer. Su acción se manifiesta en la inhibición de la proliferación celular, la inducción a la apoptosis y a la supresión de la migración e invasión celular a través de distintas rutas moleculares. La inhibición de la PKM2 suprime la proliferación de las células cancerosas al disminuir el ATP intracelular. Estudios realizados en el cáncer de colon y en las líneas celulares HCT116 y SW620, mostraron una disminución en la proliferación celular con el uso de la shikonina. Sustancia que actúa en la activación y expresión del factor inducible por hipoxia subtipo alfa (HIF-1α). HIF-1α regula la expresión de la PKM2 mediante la unión de elementos de respuesta a la hipoxia, localizados dentro del primer intrón del gen de PKM2. De igual forma, la shikonina ha demostrado, también su eficacia, en una línea celular de cáncer de esófago al decaer la proliferación celular a través de la vía HIF-1α/PKM2 (Guo et al., 2019). Así mismo, en las líneas celulares de cáncer de vejiga y en presencia de diferentes concentraciones de glucosa, se ha demostrado que las incubaciones con shikonina atenúan la proliferación celular y favorecen la conversión de la forma dimérica a la tetramérica de la PKM2 (Liu et al., 2019).
Las biguanidas son uno de los grupos de fármacos más usados para el tratamiento de la diabetes mellitus, especialmente la metformina. Además de su papel en el control de la glucemia, existe evidencia de que las biguanidas funcionan en sinergia con algunas intervenciones terapéuticas en los pacientes con cáncer. Se ha descubierto que mejoran el efecto citostático durante la privación celular de serina. Este efecto está relacionado con la idea de que las biguanidas también pueden limitar la acumulación de intermediarios glicolíticos y del Ciclo de Krebs, lo que sugiere que los activadores de la PKM2 comprometen la síntesis de serina al privar a estas vías de intermediarios glicolíticos (van Niekerk & Engelbrecht, 2018). Se sabe que una reducción en los niveles de la PKM2 inducidos por la metformina mejoran la eficiencia de la pirarubicina, una antraciclina utilizada en el tratamiento del cáncer de vejiga (Su et al., 2018).
Existen otros fármacos como la vitamina K y la temozolomida que inhiben en algún grado la actividad de la PKM2. Las vitaminas K3 y K5 tienen un efecto sinérgico en los tratamientos quimioterapéuticos por influir en la disminución de la velocidad de crecimiento de las células tumorales a través de la inhibición de la PKM2 (Su et al., 2019). Asimismo, se ha demostrado que la temozolomida, altera la expresión de la PKM2, al provocar cambios en el metabolismo del piruvato. Lo que muestra la importancia de la PKM2 en la respuesta al daño del DNA (Park et al., 2014).
b) Inhibidores indirectos
Además de las moléculas antes mencionadas y que actúan directamente en la actividad de la PKM2, existen otros inhibidores que de forma indirecta aminoran levemente el efecto de la PKM2 a través de moléculas intermediarias. Entre ellos, el selumetinib, el TRIM35, el FFJ-5, el FFJ3 y el ácido oleanólico que representan los mejor descritos (He et al., 2017), (Figura 4).
PKM2 como biomarcador
El National Institutes Health (NIH) en su documento virtual “Biomarkers, EndpointS, and other Tools” (BEST) define al biomarcador como “Una característica definida que se mide como un indicador de procesos biológicos normales o patológicos, o bien como respuesta a una exposición o intervención” (FDA-NIH Biomarker Working Group. BEST).
Existen diferentes tipos de biomarcadores: los de diagnóstico, los de seguimiento, los de pronóstico y los terapéuticos. Incluso, un solo biomarcador cumple con varios criterios para diferentes usos (Califf, 2018).
A este respecto se ha utilizado de forma experimental a la PKM2 como un biomarcador de diagnóstico en ciertas neoplasias, o de pronóstico (Novotný et al., 2008).
Diagnóstico
Diferenciar entre cáncer u otra entidad nosológica es en ocasiones complicado, por requerir de procedimientos invasivos de acuerdo con el diagnóstico de una patología con diferente solución. Por esta razón, la búsqueda de marcadores serológicos es indispensable para facilitar el diagnóstico clínico y un tratamiento oportuno. Es el caso de la pancreatitis crónica y el cáncer de páncreas, en los que diferenciar un cuadro del otro es complejo. En 2008 Novotny y colaboradores (Novotný et al., 2008) investigaron a la PKM2 como un posible marcador tumoral para distinguir entre el cáncer de páncreas, la pancreatitis crónica y los controles sanos. En ese estudio, se encontró el nivel sérico más alto de la PKM2 en pacientes con adenocarcinoma de páncreas avanzado. Los niveles resultantes fueron significativamente más altos que en los pacientes con adenocarcinoma de páncreas temprano, pancreatitis crónica y controles sanos. Sin embargo, no se encontró diferencia entre estas dos enfermedades, por lo que aún no se considera a PKM2 como un biomarcador adecuado para la detección temprana del adenocarcinoma de páncreas (Kunovsky et al., 2018). Shastri y colaboradores compararon la prueba inmunológica de sangre oculta en heces (IFOBT, por sus siglas en inglés) -y la establecieron como un marcador más preciso, para la detección del cáncer colorrectal, que es la prueba tradicional basada en guayaco- contra la PKM2 en heces. Como resultado se encontró que la prueba IFOBT, es específica, con valor predictivo positivo y una razón de verosimilitud más altos en comparación con los resultados de la PKM2 que mostró un menor rendimiento contra la IFOBT (Shastri et al., 2008). Sin embargo, parece haber cambiado, con estudios recientes, la opinión de la utilidad de la PKM2 en un grupo de pacientes con cáncer de colon, al mostrar que los niveles plasmáticos de la PKM2 resultaron más altos, que en sujetos sanos o con otras lesiones de colon. Por lo que sugieren que la PKM2 es un biomarcador con potencial rápido y no invasivo para el diagnóstico temprano en este tipo de cáncer (Ghoniem, Elghamry, Abobakr, Khidr & Alboraie, 2022). Asimismo, en el cáncer de pulmón se ha reportado una detección simultánea de los marcadores PKM2 y CEA (antígeno carcinoembrionario) que ayudarían a los médicos a decidir si se obtienen muestras citológicas o histológicas que son más invasivas (Zhang, Liu, Li, Jue & Xu, 2022). Estudios preliminares en un grupo de pacientes con cáncer de vejiga mostraron niveles elevados de la PKM2 en orina, por lo que proponen que la PKM2 se utilice como biomarcador en este tipo de cáncer (Liu et al., 2019).
Pronóstico
Se define a la palabra pronóstico como una predicción del curso futuro de una enfermedad después de su inicio. Es decir, el término se refiere a los posibles resultados de una enfermedad y a la frecuencia en que puede producirse (Pimentel-Nieto & Morales-Carmona, 2010) . En pacientes oncológicos, el pronóstico representa una condición de suma importancia al momento de recibir el diagnóstico y durante el curso de su tratamiento puesto que el cáncer es una de las enfermedades que mayor impacto generan en las personas (Campagne, 2019). Por ello, la importancia de tener biomarcadores fiables que puedan generar confianza en el valor de un pronóstico.
Yang y colaboradores llevaron a cabo el meta-análisis más grande hasta ahora publicado, con el objetivo de evaluar la expresión de la PKM2 y su correlación con el pronóstico de tumores sólidos. En este meta-análisis se realizaron 24 ensayos observacionales cuyos datos sobre la supervivencia general pertenecen a diez tipos de cáncer. Los resultados demostraron que la sobreexpresión de la PKM2 está relacionada con un incremento en la mortalidad. En el análisis estratificado por tipo de tumor, los niveles altos de la PKM2 se correlacionaron con una mortalidad general menor en pacientes con cáncer de mama, cáncer de células escamosas de esófago, cáncer de vesícula biliar y carcinoma hepatocelular. No obstante, la sobreexpresión de la PKM2 en cáncer gástrico y cáncer de páncreas no tiene ningún efecto sobre la mortalidad. Estos resultados sugieren que la enzima puede ser un biomarcador de pronóstico potencial y que utilizarla con fines terapéuticos es prometedor para tratar tumores sólidos en una variedad de tipos de cáncer (Yang et al., 2017).
Conclusiones
La función de la isoforma PKM2 es cada vez más relevante en los estudios que abordan la reprogramación del metabolismo, como uno de los puntos fundamentales en la oncogénesis. En las células con tasas elevadas de proliferación, se requiere direccionar el metabolismo celular hacia un incremento en la biosíntesis, por lo tanto, la selección de la PKM2, por encima de las otras isoformas de PKs, es con la finalidad de promover esta reprogramación a través de una disminución en la velocidad de la catálisis, que es posible con el cambio conformacional que lleva PKM2, de su forma dimérica a tetramérica. En particular la actividad reducida de la PKM2 ha sido propuesta para dirigir los intermediarios glicolíticos hacia otras rutas en la biosíntesis como la vía de las pentosas fosfato y la síntesis de serina.
Otro aspecto importante es un conocimiento más amplio sobre la estructura y función de la PKM2, ya que por un lado se propone como un posible blanco farmacológico en la oncoterapia y por otro lado como un biomarcador potencial, rápido y no invasivo, para el diagnóstico temprano en algunos tipos de cáncer.
Por último, cabe resaltar que la actividad de la PKM2 está implicada en diversas funciones del organismo, como el desarrollo embrionario, la respuesta inmune a infecciones y la reparación de heridas, entre otras, lo que motiva a continuar el estudio de esta enzima, relacionada con diversos aspectos de la biología humana.











 nueva página del texto (beta)
nueva página del texto (beta)


