Introducción
Las plantas son organismos sésiles que en el medio ambiente se enfrentan a condiciones o factores favorables o desfavorables para su supervivencia, que aparecen repentina, y repetidamente. En general estos factores estresantes se dividen en bióticos o abióticos. El estrés biótico surge de la infección por patógenos o el ataque de herbívoros. El estrés abiótico incluye factores relacionados con el clima y la actividad humana como la sequía, el frío, la salinidad del suelo, el calor, la contaminación con metales pesados, la radiación ultravioleta (UV), y las inundaciones (Praveen, Dubey, Singh & Sharma, 2023).
Las plantas tienen la capacidad de protegerse ante la escasez de agua provocada por las sequías, las heladas y la salinidad a través de la reactivación de diversas funciones temporales (Claeys & Inze, 2013). Su objetivo es superar o evitar el estrés mediante un equilibrio entre la absorción y la pérdida de agua. La absorción de agua se favorece con la acumulación de solutos que reducen el potencial hídrico del tejido y mejoran el crecimiento de la raíz (Claeys & Inze, 2013); el cierre de los estomas para evitar la pérdida de agua; la restricción en el crecimiento de los brotes; la aceleración de la senescencia de la hoja; la desviación de carbono y energía para el almacenamiento y la biosíntesis de compuestos osmoprotectores como la prolina (Claeys & Inze, 2013). A nivel celular, el acceso limitado a una fuente de agua incrementa la producción de especies reactivas de oxígeno (ERO) con daño a los cloroplastos, las mitocondrias y los peroxisomas (Rodriguez, Cordoba, Ortega & Taleisnik, 2004). Para evitar el daño celular severo se activan mecanismos como la desintoxicación de las ERO, la síntesis de ácido abscísico (ABA), la acumulación de proteínas protectoras, como las proteínas de la Embriogénesis Tardía (LEA), y varios Factores Transcripcionales (FT) como los Elementos de Respuesta a la Sequía (DREB) (Claeys & Inze, 2013). Además, se ha observado que el Ca2+ y las moléculas que lo perciben, regulan una variedad amplia de blancos celulares, como transportadores, FT, cinasas y fosfatasas, proteínas del citoesqueleto y proteínas de unión al DNA. Estos componentes están implicados en la respuesta de defensa ante el estrés provocado por la escasez de agua (Pirayesh, Giridhar, Ben Khedher, Vothknecht & Chigri, 2021).
Ante el estrés hídrico, también las proteínas se dañan y al acumularse alteran la homeostasis celular. Por esto, el reciclaje intracelular es esencial para el control de estas circunstancias y al eliminar las moléculas u organelos dañados se reponen los nutrientes esenciales necesarios para el crecimiento y mantenimiento celular (Masclaux-Daubresse et al., 2014). Las dos vías principales de degradación y reciclamiento de los componentes celulares en los organismos eucariotas son la autofagia y el proteasoma. La autofagia (“comerse a sí mismo”) es la degradación masiva de proteínas citosólicas de vida larga y organelos; el sistema degradador ubiquitina-proteasoma es el principal responsable de la degradación y el reciclaje de proteínas de vida corta (Yin, Pascual & Klionsky, 2016). Por lo hasta aquí expuesto, se analizan en esta revisión los posibles vínculos entre el hidrotropismo, la autofagia y el ion calcio en la resistencia de las plantas a la escasez de agua.
Metodología
La revisión bibliográfica se inició a partir del año 1998 hasta el año 2023. Se consultaron las páginas TAIR (https://www.arabidopsis.org), Plant Promoter Database (https://ppdb.agr.gifu-u.ac.jp/ppdb/cgi-bin/index.cgi) y Plant Pan (http://plantpan.itps.ncku.edu.tw/plantpan4/index.html).
El hidrotropismo y la respuesta hidrotrópica
Los órganos de las plantas se mueven o desplazan en busca de agua, nutrientes y luz, factores esenciales para su crecimiento y desarrollo. En contraste, se alejan cuando se enfrentan a situaciones nocivas. A estos movimientos lentos y en ocasiones imperceptibles que permiten que las plantas se adapten al medio ambiente se les denomina tropismos e implican el crecimiento dirigido de ciertos órganos de las plantas en respuesta a estímulos como la gravedad (gravitropismo), la luz (fototropismo), el contacto (tigmotropismo) y el agua (hidrotropismo). Darwin, fue uno de los pioneros en el estudio de los tropismos. En la actualidad, el estudio de ellos impacta en temas como la mecánica vegetal, estrategias de manejo de cultivos, biología de sistemas y en genómica vegetal (Dietrich et al., 2017); estos movimientos involucran la curvatura o flexión de los órganos de la planta e incluso la regulación del crecimiento, hacia o lejos del estímulo percibido (Cassab, Eapen & Campos, 2013).
En el caso de las raíces, los tropismos condicionan la dirección y el grado de crecimiento hacia o en contra de estímulos como la gravedad, la luz, los gradientes de agua, los nutrientes, los patógenos o los cambios en la temperatura y ayudan al desarrollo del sistema radicular, fundamental para el anclaje de la planta al suelo y la adquisición del agua y los nutrientes, que es importante para evitar los efectos negativos de la sequía (Moriwaki, Miyazawa, Fujii &Takahashi, 2014). Por consiguiente, cuando las plantas perciben escasez de agua, se condiciona el crecimiento de la parte aérea, y del sistema radicular, aunque en algunos casos el crecimiento de la raíz es para optimizar la búsqueda del agua (Sharp et al., 2004). El hidrotropismo es el tropismo que responde al estrés hídrico, lo que implica el movimiento genéticamente regulado de las raíces en busca de ambientes con un contenido óptimo o con menos limitantes de agua (Moriwaki et al., 2014). La respuesta hidrotrópica, es el movimiento que realizan las raíces de las plantas durante el hidrotropismo visible como la curvatura de las raíces en reacción a los gradientes de humedad o al potencial hídrico (Moriwaki et al., 2014).
En el hidrotropismo las hormonas vegetales tienen un papel fundamental para un funcionamiento correcto. El ácido abscísico (ABA), es la hormona por excelencia y un pequeño número de genes, que codifican a los transductores de la señal del ABA, GNOM/MIZ2, y el gen específico del hidrotropismo MIZ1 intervienen en la respuesta hidrotrópica de Arabidopsis thaliana (Arabidopsis) (Miyazawa & Takahashi, 2020). Además, las auxinas que regulan el hidrotropismo en Arabidopsis y en otros tipos de plantas, también participan en la división celular y el alargamiento de los órganos vegetales como la raíz, el tallo, la hoja, y el fruto; reprimen la senescencia y participan en el gravitropismo (movimiento de las raíces relacionado con la gravedad) (Garay-Arroyo, de la Paz Sánchez, García-Ponce, Álvarez-Buylla & Crisanto, 2014). En el chícharo, el pepino, el arroz, el maíz y Lotus japonicus, estudiosos en el tema mencionan que la inhibición del transporte de auxinas cancela las respuestas hidrotrópica y gravitrópica, (Miyazawa & Takahashi, 2020) y que, en el chícharo y el maíz, la cofia de la raíz se requiere para la percepción de los estímulos que dirigen la respuesta hidrotrópica y gravitrópica, y con su eliminación se suprime toda reacción (Jaffe, Takahashi & Biro,1985), (Takahashi & Scott, 1993). Igual observaron que en las raíces de las plántulas de arroz, al cortar la cofia de las raíces se impedía la respuesta gravitrópica, aunque esto no tuvo efecto en la respuesta hidrotrópica (Nakajima et al., 2017). En las raíces de L. japonicus, al retraerse la síntesis de auxinas, mediante el uso de quinurenina, aunque se evitó el desarrollo de la curvatura hidrotrópica, no se afectó el crecimiento de las raíces (Nakajima et al., 2017). En general, estas observaciones en los diferentes tipos de plantas mencionadas dieron lugar a pensar en la probable existencia e intervención de otros mecanismos en la distribución diferencial de las auxinas, incluso en ausencia de las células de la cofia de la raíz.
El hidrotropismo en Arabidopsis thaliana
Los genes MIZU-KUSSEI1 (MIZ1) y GNOM/MIZ2 son esenciales para el hidrotropismo en Arabidopsis (Kobayashi et al., 2007) (Miyazawa, Takahashi, Kobayashi, Kaneyasu, Fujii & Takahashi, 2009). MIZ1 se localiza en la corteza de la zona de elongación de la raíz y es indispensable para el hidrotropismo, ya que permite la acumulación de Ca2+ en el citoplasma, necesario para la curvatura (Kobayashi et al., 2007; Shkolnik, Nuriel, Bonza, Costa & Fromm, 2018). GNOM/MIZ2 se expresa en la epidermis, en la corteza y en la estela de la raíz. La proteína que codificada este gen está relacionada con el tráfico vesicular cuya función mejor conocida es el transporte polar de las proteínas PIN (relacionadas al transporte de auxinas) a la membrana plasmática (Miyazawa et al., 2009).
En las plantas silvestres y en la presencia de un gradiente de humedad, la raíz de Arabidopsis se curva hacia la zona con mayor disponibilidad de agua; esto no sucede en las raíces de las mutantes miz-1 y miz-2. Sin embargo, las mutaciones en estos genes reducen el fototropismo porque las hojas de la planta no giran para evitar el exceso de luz, por esto los autores del estudio consideran que MIZ1 y GNOM/MIZ2 regulan el hidrotropismo y el fototropismo en Arabidopsis (Moriwaki et al., 2014). Adicionalmente, otros autores demostraron que en las células de la corteza de la zona de elongación se perciben los cambios en el gradiente del potencial hídrico mediante un mecanismo aún desconocido que, al provocar la curvatura de la raíz, se le relaciona con la actividad de la cinasa SnRK2.2 y de la proteína MIZ1; ambas localizadas en las células de la corteza de la zona de elongación (Dietrich et al., 2017).
El balance de especies reactivas de oxígeno (ERO) regula el hidrotropismo
Como se mencionó, el suministro limitado de agua incrementa la producción de las ERO, como el peróxido de hidrógeno (H2O2), el ion superóxido (O2-) y el radical hidroxilo (OH-) que se producen en los cloroplastos, las mitocondrias y los peroxisomas dañándolos, igual que a otros organelos celulares (Rodriguez et al., 2004). A nivel molecular, el aumento en la concentración de las ERO afecta la estructura de las macromoléculas celulares como las proteínas, los lípidos y los ácidos nucleicos. Efectos que dañan a los lípidos de las membranas y ocasionan una fuga de moléculas que normalmente no la cruzan sino a través de canales específicos; también se presenta una inactivación de receptores y de enzimas debido a la carbonilación de las proteínas, haciéndolas más susceptibles a degradarse (Moller, Jensen & Hansson, 2007), y una reducción de la síntesis de proteínas que afecta el crecimiento y el desarrollo de todo el organismo por oxidación del DNA (Tuteja, Singh, Misra, Bhalla & Tuteja, 2001). Por otra parte, se ha descrito que las ERO también funcionan como moléculas señalizadoras que regulan las rutas de entrada del Ca2+ a través de la membrana plasmática (MP) (Demidchik, Shabala, Coutts, Tester & Davies, 2003). En las raíces de Arabidopsis, el H2O2 extracelular regula en específico la activación de los canales de Ca2+ de la MP de las células epidérmicas maduras, así como también el de las células de la corteza y en menor grado en las células de la epidermis de la zona de elongación (Demidchik et al., 2003). Igual el OH - extracelular provoca una entrada mayor de Ca2+ a través de la MP en las células de la epidermis que en el periciclo (Demidchik et al., 2003), (Foreman et al., 2003).
En los experimentos con Arabidopsis las raíces que actúan hidrotrópicamente no tienen una distribución asimétrica transitoria de las ERO (Krieger, Shkolnik, Miller & Fromm, 2016) y estas al retraerse mediante el uso de un antioxidante como el ascorbato de sodio o un inhibidor de la generación de las ERO como el yoduro de fenilo, el gravitropismo se atenúa en contraste con un incremento del hidrotropismo (Krieger et al., 2016). También, las mutantes en la NADPH oxidasa RBOH C revelan una mayor curvatura hidrotrópica (Krieger et al., 2016), con la posibilidad de que el H2O2, promueva el gravitropismo y frene el hidrotropismo (Krieger et al., 2016).
El Ca2+ es un segundo mensajero que regula la respuesta hidrotrópica
El calcio es esencial para el funcionamiento de las plantas y transformado el ion Ca2+ es un mensajero intracelular dinámico. Una diversidad de estreses bióticos y abióticos, así como diversos procesos del desarrollo, provocan un aumento en los niveles de Ca2+ en el citosol con su entrada controlada desde las reservas externas, el apoplasto e internas, el RE (Kudla, Batistic & Hashimoto, 2010; McAinsh & Pittman, 2009; Batistic & Kudla, 2012). Además, la señalización de Ca2+ no se limita al citosol, también ocurre en los organelos que son: el núcleo, los cloroplastos, las mitocondrias, los peroxisomas y el sistema de endomembranas.
El Ca2+ es una molécula que actúa como segundo mensajero. Los segundos mensajeros son pequeñas moléculas o iones que transmiten señales recibidas por los receptores de la superficie celular a las proteínas efectoras. El Ca2+ participa en la señalización de numerosos procesos del desarrollo y la defensa, específicamente, se le relaciona con la regulación de diferentes respuestas al estrés de las plantas (Carroll & Peralta, 1998).
La célula tiene una serie de bombas y canales que regresan el Ca2+ a sitios de almacenamiento como RE, el apoplasto, la vacuola, el aparato de Golgi, el cloroplasto, el peroxisoma y el núcleo (Pirayesh et al., 2021). La señalización de Ca2+ se caracteriza por una serie de eventos: i) un aumento transitorio o sostenido en su concentración libre inducido por un estímulo, ii) la detección de sus cambios a través de proteínas sensores de Ca2+, iii) una respuesta celular río abajo desencadenada por la acción de estas proteínas sensores y iv) la remoción del Ca2+ localizado en el citosol al terminar con el proceso de señalización que produjo su cambio transitorio. El movimiento del Ca2+ hacia el interior (influjo) y el exterior (eflujo) de la célula, así como desde el citosol a los organelos que lo almacenan se encuentra regulado por canales iónicos localizados en las membranas celulares. Los canales de calcio son proteínas transmembranales que constituyen la vía más importante para su ingreso a la célula.
En resumen son cuatro las acciones de la participación del Ca2+ como un segundo mensajero en un proceso celular: primero, la célula percibe un estímulo como la escasez de agua, el exceso de iluminación o la infección por un patógeno, lo que origina un aumento transitorio o sostenido de su concentración en el citosol; segundo, la detección de cambios en sus niveles citosólicos por proteínas que se le unen como las calmodulinas (CaMs), las proteínas similares a la calmodulina (CML), las proteínas cinasas que dependen de él (CDPK), proteínas similares a la calcineurina B (CBL) o la proteína cinasa interactiva (CIPK); tercero, el desencadenamiento de procesos celulares relacionados al metabolismo, la transcripción de genes o la modificación de proteínas; y cuarto, el regreso a los niveles basales de Ca2+ en el citosol que oscilan alrededor de los 50-100 nM mediante su influjo en los diferentes compartimientos de la célula en donde se almacena (Pirayesh et al., 2021).
En Arabidopsis, se han identificado familias de canales iónicos permeables al Ca2+ que son responsables del influjo de este ion. Entre éstos se incluyen a las anexinas (Richards et al., 2014), los canales activados por nucleótidos cíclicos (CNGC) (Hamilton, Schlegel & Haswell, 2015), los receptores de glutamato (GLR) (Price, Jelesko & Okumoto, 2012), los canales de dos poros (TPC) (Morgan & Galione, 2014) y los canales mecano -sensibles, éstos últimos constituidos por los canales iónicos mecano-sensibles (MSC), los de actividad complementaria Mid1 (MCA), los canales Piezo (Hamilton et al., 2015) y el canal reductor de la hiper-osmolalidad activado por un aumento en la concentración de Ca2+ intracelular (OSCA), (Yuan et al., 2014). Previamente se describieron tres tipos diferentes de canales con base en los cambios en el potencial de membrana, a los que se les denominó canales activados por hiperpolarización (HACC), canales activados por depolarización (DACC) y canales independientes del voltaje (VICC). Estos canales se localizan en la MP de las células de la epidermis de la zona de elongación de la raíz de Arabidopsis y se activan por las ERO que se producen en situaciones de estrés abiótico (Wilkins, Matthus, Swarbreck & Davies, 2016). En los estudios reportados se propone que los HACC pueden ser anexinas y los VICC, GLR y DACC canales activados por CNGC (White & Broadley, 2003; Swarbreck, Colaco & Davies, 2013), (Figura 1; Tabla I).
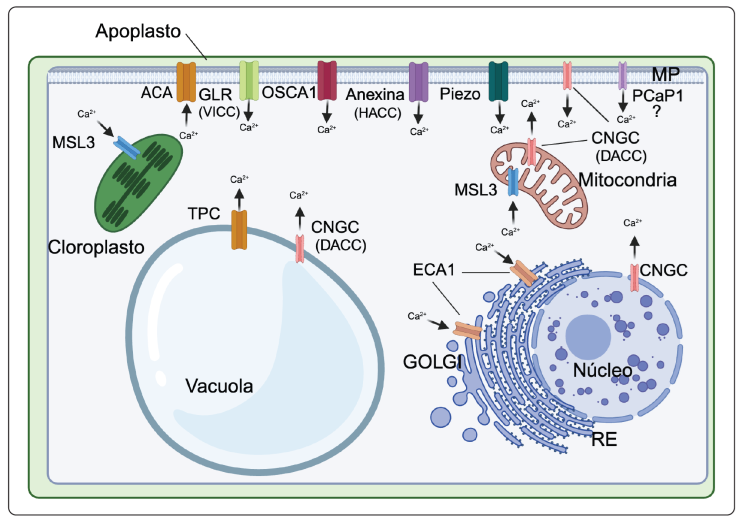
Imagen creada con Biorender.com.
Figura 1 Proteínas transportadoras de Ca2+ en Arabidopsis thaliana. En la Figura se muestra a las proteínas relacionadas con la señalización de Ca2+ de varios organelos descritos en el texto. GLR (receptores de Glu), CNGC (canales activados por nucleótidos cíclicos), TPC (canal de dos poros), ANEXINA, canales tipo Piezo, MSL3 (canal mecano- sensible3), ECA (Ca2+ -ATPasa), ACA (Ca2+-ATPasas auto-inhibida), PCaP1 (Proteína de unión a Ca2+ asociada a la membrana plasmática) y OSCA (Canal reductor de la hiper-osmolalidad inducida por un aumento de concentración de Ca2+ en el citosol). Las flechas indican la dirección del flujo del Ca2+. Se ha descrito que las anexinas GLR, CNGC y TPC1 son HACC, VICC y DACC como se indica en esta Figura y en la Tabla I. ECA1 (Shkolnik et al., 2018), PCaP1 (Tanaka-Takada et al., 2019) y Osca1 (Yuan et al., 2014) están relacionados con la respuesta hidrotrópica o el estrés hídrico.
Tabla I Papel de las proteínas transportadoras de Ca2+ en Arabidopsis thaliana. Se sugiere que las anexinas, GLR, CNGC y TPC1 son HACC, VICC y DACC como se indica en el cuerpo de la Tabla.
| Proteínas transportadoras de Ca2+ | Número de genes en Arabidopsis | Localización | Proceso Biológico | Flujo | Referencias |
|---|---|---|---|---|---|
|
|
20 |
|
|
Influjo | (Lee et al., 2004; Wilkins et al., 2016) |
|
|
20 |
|
|
Influjo | (Gobert, Park, Amtmann, Sanders & Maathuis, 2006; Jammes, Yang, Xiao & Kwak, 2011; Duszyn, Swiezawska, Szmidt-Jaworska & Jaworski, 2019; Wang et al., 2013; Wilkins et al., 2016) |
|
|
1 |
|
|
Influjo | (Morgan & Galione 2014; Wilkins et al., 2016) |
|
|
8 |
|
|
Influjo | (Lee et al., 2004; Zelman, Dawe, Gehring & Berkowitz, 2012; Wilkins et al., 2016) |
|
|
10 |
|
|
Eflujo | (Hamilton, et al., 2015; Lee et al., 2016; Peyronnet et al., 2008; Veley, Maksaev, Frick, January, Kloepper & Haswell, 2014) |
|
|
4 |
|
|
Eflujo | (García Bossi et al., 2020; Shkolni et al., 2018) |
|
|
10 |
|
|
Eflujo | (García Bossi et al., 2020; Yu, Yan, Du & Hua, 2018) |
|
|
1 |
|
|
Influjo | (Tanaka-Takada et al., 2019) |
|
|
15 |
|
|
Influjo | (Yuan et al., 2014; Akita & Miyazawa, 2022) |
Para recuperar el nivel de Ca2+ basal, existen en la célula sistemas que lo bombean a través de alguna membrana celular utilizando ATP o H+ como fuente de energía. Estos transportadores son: los intercambiadores de Ca2+/H + (CAX) (Manohar, Shigaki & Hirschi, 2011) y las ATPasas de Ca 2+ tipo P, que incluyen a la Ca2+-ATPasas auto-inhibida (ACA), la Ca2+-ATPasas de RE (ECA) y la ATPasa 1 de metales pesados, P1-ATPasa (Bonza & De Michelis, 2011), (Figura 1; Tabla I). Las ATPasas de Ca2+, como ACA y ECA son transportadores de alta afinidad (Km = 0,1-2 μM) pero de baja capacidad, distintos a los CAX que son transportadores de baja afinidad (Km = 10-15 μM) pero de alta capacidad (Bose, Pottosin, Shabala, Palmgren & Shabala, 2011). Además, una de las principales diferencias entre ACA y ECA son sus afinidades por el Ca2+, que están en el rango micromolar para ACA y en el rango nanomolar para ECA (Bonza & De Michelis, 2011), (Meneghelli, Fusca, Luoni & De Michelis, 2008). Estos intercambiadores tienen diferentes especificidades para los cationes divalentes: ACA es altamente selectivo y transporta solo Ca2+, sin embargo, ECA también pueden transportar Cd2+, Mn2+ y Zn 2+ (Meneghelli et al., 2008). A ECA se le puede inhibir con el ácido ciclopiazónico (CPA) (Meneghelli et al., 2008), ACA es particularmente sensible a la inhibición con los derivados de la fluoresceína como la eritrosina B o la eosina Y (Bonza & De Michelis, 2011).
En general la señalización intracelular de Ca2+ en el citosol está determinada por la amplitud, duración y oscilación de su concentración en el citosol. La percepción de las señales genera rápidamente sus elevaciones transitorias que activan de manera concertada tanto su influjo pasivo a través de canales, como de sistemas activos de eflujo mediante bombas y transportadores, que temporalmente definen espacialmente su dinámica comúnmente denominada la firma del calcio (McAinsh & Pittman, 2009). Esta firma está impulsada por la apertura de canales localizados en la membrana plasmática permeables al Ca2+. Una vez que el estímulo cesa los intercambiadores y las Ca2+-ATPasas transportan el exceso de su concentración en el citosol al RE, a la vacuola o al apoplasto, recuperándose así la concentración basal en el citosol (McAinsh & Pittman, 2009). A continuación, se describe su regulación del influjo y eflujo durante el hidrotropismo.
Canales mecano-sensibles de Ca2+
En Arabidopsis los estudios indican que los canales similares a los mecano-sensibles de Ca2+ 2 y 3 se activan es respuesta al estrés osmótico (MSL2 y MSL3). MSL2 y MSL3 actúan como válvulas de seguridad para regular la homeostasis osmótica en los plastidios durante el crecimiento y el desarrollo de la planta (Hamilton et al., 2015; McAinsh & Pittman, 2009; Peyronnet, Haswell, Barbier-Brygoo & Frachisse, 2008). La doble mutante msl2/msl3 es más sensible a la limitación de agua. En apoyo a los datos, que están publicados, en nuestros estudios también hemos encontrado un incremento en la expresión de MSL3 en las plantas de Arabidopsis silvestres creciendo en condiciones de estrés osmótico comparando con plantas cuyo desarrollo es en condiciones normales (datos no publicados), lo que sugiere una movilización de Ca 2+ a través de MSL3 para contender con el estrés hídrico. MSL3 se localiza en la membrana externa del cloroplasto y la mitocondria. Sugerimos que en el cloroplasto su función puede estar relacionada con el cierre de los estomas que impide pérdida de agua, y en la mitocondria su función podría ser regular a las ERO producidas durante el estrés hídrico.
El canal permeable al Ca2+ OSCA1.1 participa en la regulación del hidrotropismo
OSCA1.1 es un canal catiónico no selectivo que se encuentra localizado en la membrana plasmática de las células guardia de los estomas de las hojas y también en las células de la epidermis de la raíz de Arabidopsis (Yuan et al., 2014). En estudios realizados con la mutante osca1.1 hubo una disminución de la concentración de Ca2+ en la raíz y las hojas, en respuesta al estrés osmótico generado con un gradiente de sorbitol. Además, la falta de función de OSCA1.1 redujo el influjo de Ca2+ en las células guardia y de la raíz en general, lo que ocasionó que la transpiración aminorara igual que el crecimiento de las raíces, bajo condiciones de estrés hiperosmótico generado con sorbitol (Yuan et al., 2014). osca1.1 mostró un incremento de 10 grados de curvatura hidrotrópica comparada con la planta silvestre (Akita & Miyazawa, 2022). Resultados de un análisis transcripcional indicaron que OSCA1.1 es un regulador negativo de MIZ1 , ya que los niveles del mRNA de MIZ1 se incrementaron en la mutante osca1.1 (Akita & Miyazawa, 2022). Con base en estos resultados los investigadores consideran que OSCA1.1 es relevante para el influjo del Ca2+ del apoplasto hacia el citosol no solamente en el hidrotropismo sino como una respuesta general al estrés hídrico (Yuan et al., 2014).
PCaP1 es una proteína de unión al Ca2+ requerida para la curvatura hidrotrópica
La proteína de unión al Ca2+ asociada a la membrana plasmática (PCaP1) es otro elemento involucrado en el hidrotropismo de las raíces de Arabidopsis (Tanaka-Takada, Kobayashi, Takahashi, Kamiya, Kinoshita & Maeshima, 2019). La mutante pcap1 presentó un decremento en la curvatura hidrotrópica en comparación a la planta silvestre en condiciones de estrés hídrico (Tanaka-Takada et al., 2019). PCaP1-GFP además de estar en el citosol se encontró asociada con la membrana plasmática en la mayoría de las células de la raíz con excepción de las células de la endodermis de la zona de la curvatura. Por lo tanto, la re-localización de PCaP1 en el citosol de las células de la endodermis tiene un papel en el hidrotropismo (Tanaka-Takada et al., 2019). La sobreexpresión de MIZ1 en la mutante pcap1 complementó el fenotipo no hidrotrópico de está mutante lo que indicó que PCaP1 no está río abajo de la señalización de MIZ1 (Tanaka-Takada et al., 2019). Con base en estos resultados la localización de PCaP1 en las células de la endodermis de la zona de elongación de la raíz está involucrada en el proceso hidrotrópico; sin embargo, no se descarta la posibilidad de que PCaP1 contribuya al hidrotropismo a través de una vía independiente de MIZ1 (Tanaka-Takada et al., 2019).
La proteína transportadora de Ca2+ ECA1 regula la curvatura hidrotrópica
ECA1 es una ATPasa que participa en el movimiento del Ca2+ del citosol hacia el RE, permitiéndole a la célula regresar a la homeostasis. En respuesta a las diferencias de potencial hídrico, los autores del estudio observaron el movimiento de una señal de Ca2+ lenta, asimétrica y de larga distancia desde la punta de la raíz hasta la zona de elongación (Figura 2, panel B número 7) . Mediante ensayos de dos híbridos en levadura, vieron que al interactuar MIZ1 con ECA1 disminuye su actividad de transportar Ca 2+ al RE (Shkolnik et al., 2018); esto generó un aumento de la concentración de Ca2+ en el citosol detectable en la zona de elongación, y ocasionó la curvatura hidrotrópica (Shkolnik et al., 2018).
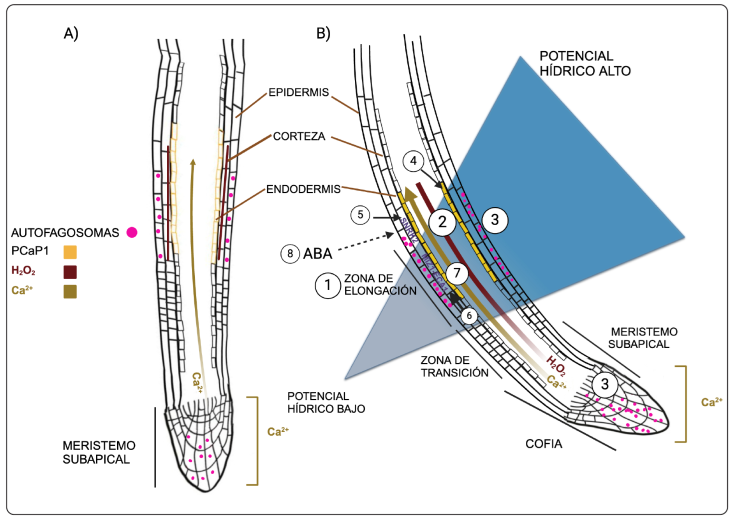
Figura 2 Descripción general de las moléculas y de las vías metabólicas y de señalización involucradas en el hidrotropismo de la raíz de Arabidopsis thaliana.
La numeración se hizo para facilitar el entendimiento del proceso, no implica que este sea el orden en que suceden los eventos señalados. A) y B) indican el estado de la raíz previo y durante el proceso de percepción de la escasez de agua, respectivamente. La descripción de los párrafos numerados se muestra en el panel B.
La zona de elongación tiene dos funciones en la respuesta hidrotrópica: detecta un gradiente de potencial hídrico y posteriormente experimenta un crecimiento diferencial que ocasiona la curvatura hidrotrópica (raíz y triángulo azul) (Dietrich et al., 2017).
Acumulación de H2O2 en la curvatura de la raíz. Utilizando la línea Hyper que expresa un detector de H2O2, se encontró a éste en la zona de la curvatura de la raíz (línea marrón) (Jimenez-Nopala et al., 2018).
Acumulación de autofagosomas en la curvatura de la raíz. Empleando la línea transgénica GFP-ATG8a se observó la acumulación de autofagosomas en la zona de la curvatura de la raíz que coincide con la zona de elongación a un tiempo similar al de la aparición de H2O2 (círculos rosas) (Jimenez-Nopala et al., 2018).
PCaP1se moviliza de la membrana plasmática hacia el citosol en las células de la endodermis de la raíz durante la respuesta hidrotrópica (Tanaka-Takada et al., 2019).
El hidrotropismo depende de la cinasa SnRK2.2 regulada por ABA. SnRK2.2 y MIZ1, proteína específica del hidrotropismo, que dan lugar a la curvatura hidrotrópica en respuesta al estrés hídrico. Ambas proteínas se localizan únicamente en las células de la corteza de la zona de elongación de la raíz (Dietrich et al., 2017).
MIZ1 se une a ECA1 e inhibe su actividad. Esta unión modifica el equilibrio entre la entrada y salida de Ca2+ en el citosol. La acumulación de Ca2+ en el citosol regula la curvatura de la raíz (Shkolnik et al., 2018).
El gradiente de potencial hídrico genera una señal citosólica de Ca2+ lenta y asimétrica de larga distancia en el floema, que alcanza su punto máximo en la zona de elongación, dispersándose lateral y asimétricamente a las células de la periferia de la zona convexa de la raíz, donde se produce el alargamiento celular y la curvatura de la raíz hacia la zona con mayor contenido de agua (Shkolnik et al., 2018) (línea dorada).
Los estudios de expresión tejido-dirigida mostraron que la curvatura hidrotrópica depende de la señalización de ABA a través de regular a la cinasa SnRK2.2 y a MIZ1, ambas actuando específicamente en las células corticales de la zona de elongación (Dietrich et al., 2017). Imagen creada con Biorender.com.
Con base en lo anterior, la inhibición de ECA1 por MIZ1 cambia el equilibrio entre la entrada y salida del Ca2+ citosólico y genera la señal de Ca2+ citosólico que regula la curvatura de la raíz hacia la zona más húmeda del medio (Shkolnik et al., 2018) . Hasta la fecha, MIZ1 es el único regulador de las ATPasas tipo IIA transportadoras de Ca2+ identificado en plantas, por lo que sería muy interesante estudiar si MIZ1 puede unirse y controlar también otras bombas ATPasas tipo IIA transportadoras de Ca2+ en diferentes contextos biológicos y ante diferentes estímulos.
La autofagia como un mecanismo de defensa celular
La autofagia es un proceso catabólico conservado en la mayoría de las células eucariotas, a través del cual el material citosólico no deseado o disfuncional, como las proteínas, los complejos proteicos, los agregados de ácidos nucleicos e incluso los organelos completos, se transporta para su degradación y reciclaje al lisosoma en los animales y a la vacuola en la levadura y en las plantas (Bassham et al., 2006).
Los genes ATG (AuTophaGy), que codifican a las proteínas para la maquinaria de la autofagia, se describieron inicialmente en Saccharomyces cerevisiae y están prácticamente conservados en las células eucariotas. El estudio de los mutantes de Arabidopsis deficientes en los genes ATG confirmó que las proteínas ATG son necesarias para el desarrollo adecuado de la planta (Bassham et al., 2006).
La característica más destacada de la autofagia es la formación de una estructura llamada autofagosoma, que consiste en una vesícula de doble membrana que se encuentra formando una copa conocida como fagóforo que se alarga y rodea a la carga o componentes citosólicos que posteriormente serán degradados en la vacuola (Marshall & Vierstra, 2018).
En las levaduras, los autofagosomas se forman próximos a la membrana vacuolar, y en los mamíferos, las estructuras autofagosómicas tempranas se forman en el RE y en los sitios de contacto entre el RE y las mitocondrias (Yla-Anttila, Vihinen, Jokitalo & Eskelinen, 2009), (Hailey et al., 2010). También, en las células de los mamíferos, la membrana plasmática contribuye directamente a la formación de precursores tempranos de autofagosomas (Ravikumar, Moreau, Jahreiss, Puri & Rubinsztein, 2010). Con base en la detección de la interacción de clatrina que es una proteína estructural participante en la formación de vesículas localizada en la membrana plasmática, y Atg16L1, un componente del complejo de elongación de la autofagia, se vio la formación del fagóforo, una estructura que marca el inicio de la aparición del autofagosoma (Ravikumar et al., 2010). También se menciona que la existencia de esta estructura desde la membrana plasmática puede ser importante durante períodos en los que se requiere de una cantidad importante de autofagosomas, ya que por ser un gran reservorio de membrana permite a las células la generación de autofagosomas a niveles más altos que en condiciones basales, sin comprometer otros procesos celulares (Ravikumar et al., 2010).
En resumen, se presume que en las células de los mamíferos los sitios de formación de los autofagosomas y las fuentes de membrana podrían variar en distintas condiciones fisiológicas y tipos de células (Rubinsztein, Shpilka & Elazar, 2012). En las plantas se considera que estos fragmentos provienen del RE, la mitocondria o la membrana plasmática (Yang & Bassham, 2015), (Zhuang et al., 2017).
Una vez formado el autofagosoma con su carga, su membrana externa se fusiona con el tonoplasto (la membrana vacuolar) y entra al lumen de la vacuola, como una estructura de una sola membrana denominada cuerpo autofágico, que se lisa junto con su carga para reciclar los productos de la degradación (Soto-Burgos, Zhuang, Jiang & Bassham, 2018). En cada uno de los pasos de la autofagia participan varios complejos proteicos conformados por las proteínas ATG (Porta & Jimenez-Nopala, 2019).
En las plantas se han descrito tres tipos distintos de degradación: El primer tipo, la microautofagia, se caracteriza por una invaginación directa del tonoplasto para absorber los componentes celulares destinados a la degradación. El segundo tipo, la macroautofagia (denominada autofagia), es la forma predominante de la autofagia y la más estudiada, tanto en las levaduras, como en los animales y en las plantas. Una vertiente de la macroautofagia es la autofagia selectiva que es un proceso que involucra el engullimiento en autofagosomas de sustratos marcados específicamente para su deterioro como, por ejemplo: las proteínas (proteafagia), los peroxisomas (pexofagia), las mitocondrias (mitofagia) o los ribosomas (ribofagia) (Bu, Yang, Guo, Huang & Chen, 2020). La autofagia selectiva al igual que la autofagia canónica forma autofagosomas para la degradación de su carga en la vacuola y contribuyen a la homeostasis celular y al control de calidad de las proteínas y los organelos (Zaffagnini & Martens, 2016).
El tercer tipo de autofagia es la mega autofagia, una forma extrema de autofagia que hasta ahora solo se ha descrito en las plantas (van Doorn & Papini, 2013). Durante la mega autofagia, la membrana vacuolar se permeabiliza y se rompe, liberando grandes cantidades de hidrolasas en el citosol, lo que provoca una degradación indiscriminada de los materiales citosólicos (van Doorn & Papini, 2013). A diferencia de la autofagia canónica, la mega autofagia no implica la captura de componentes celulares en la vacuola y aparentemente no participan genes ATG (Bassham, 2009).
Regulación de la autofagia por el calcio
Dentro de las proteínas de unión al calcio que participan en la percepción de este ion se han reportado proteínas similares a la calmodulina relacionadas con la regulación de la autofagia (Tsai, Koo, Delk, Gehl & Braam, 2013). Empleando cultivos de células de tabaco hubo una interacción de CML24, un canal mecano- sensible de unión al Ca2+, con la proteína de la autofagia ATG4b (Tsai et al., 2013). En la secuencia primaria de ATG4b se identificaron dos sitios de unión a CaM; sin embargo, se desconoce si éstos son relevantes para la interacción con CML24 (Tsai et al., 2013). Adicionalmente, en las mutantes de CML24 aumentó la formación de autofagosomas caracterizados por GFP-ATG8e (Tsai et al., 2013). Cabe destacar que la mutante cml24 de Arabidopsis muestra una mayor acumulación de autofagosomas en comparación con la planta silvestre, lo cual sugiere que CML4 actúa como un regulador negativo de la autofagia (Tsai et al., 2013). Mediante técnicas de expresión transitoria y ensayos de dos híbridos en la levadura el Ca2+ no regula esta interacción. Sin embargo, es posible que la unión de Ca2+ con CML24 regule su actividad y su función indirectamente (Tsai et al., 2013). ATG4 es una proteasa de cisteína con una función dual tanto en la “lipidación” como en la deslipidación de autofagosomas para el reciclaje de ATG8. ATG8 es esencial para la biogénesis del autofagosoma (Perez-Perez, Lemaire & Crespo, 2021). La regulación de la autofagia por Ca2+ es un campo de investigación novedoso y estos procesos en conjunto impactarían en el hidrotropismo.
La autofagia y las ERO se activan durante la respuesta hidrotrópica
La autofagia tiene un papel central en la respuesta hidrotrópica de Arabidopsis. El hecho es que las plantas de Arabidopsis portadoras de mutaciones en genes de la autofagia como atg2, atg5, atg9, atg8b y atg8i no desarrollaron la curvatura hidrotrópica característica al utilizar un gradiente de agua generado con agar-sorbitol (Jimenez-Nopala et al., 2018). Así mismo, mediante el uso de una línea transgénica que expresaba constitutivamente el gen GFP-ATG8a , observaron la acumulación de autofagosomas en la zona de la curvatura utilizando en el mismo sistema hídrico estresante generado con sorbitol (Jimenez-Nopala et al., 2018). Estos resultados señalan que la autofagia está en la vía de señalización que induce la respuesta hidrotrópica (Jimenez-Nopala et al., 2018).
Mediante el uso de la línea transgénica Hyper, que expresa una molécula detectora de H2O2, los autores de la investigación encontraron una acumulación de ésta ERO y de autofagosomas en la zona de la curvatura de la raíz a un tiempo similar (Jimenez-Nopala et al., 2018). La acumulación simultánea del H2O2 y de autofagosomas denota que la autofagia regula el daño oxidativo al degradar los productos oxidados por acumulación de H2O2 (Jimenez-Nopala et al., 2018).
Se tiene el conocimiento de que en la levadura Saccharomyces y en el alga verde Chlamydomonas reinhardtii la proteinasa ATG4 se activa por reducción y se inhibe reversiblemente por oxidación, indicativo de una modificación redox postraduccional (Perez-Perez et al., 2021). En detalle, la Cys-proteasa ATG4 escinde a la proteína ATG8 en el extremo C-terminal, liberando así un residuo de cisteína en ATG8. Este proceso permite la conjugación de ATG8 con fosfatidiletanolamina (PE) a través del sistema de conjugación similar a la ubiquitinación, compuesto por ATG7 y ATG3. La conjugación de ATG8-PE es crucial para la integración de ATG8 en la doble membrana del autofagosoma. Posteriormente, en el autofagosoma maduro, ATG4 libera a ATG8 de su membrana externa. Esta liberación permite la fusión de la membrana externa del autofagosoma con el tonoplasto lo que libera y degrada al cuerpo autofágico en la vacuola. Así concluye el proceso de la autofagia. Este proceso se describe como la “lipidación” y deslipidación de ATG8, respectivamente y se regula por modificaciones redox de ATG4 (Perez-Perez et al., 2021). Las proteínas ATG4 se han conservado a través de la evolución en diferentes eucariotas, por lo tanto, es muy probable que este mecanismo de regulación de ATG4 por el sistema redox se encuentre conservado en Arabidopsis y en otras plantas.
Conclusiones
La información analizada en esta revisión señala la participación de las ERO y del Ca2+ en la regulación de la autofagia y del hidrotropismo. En la Figura 2 se muestra un modelo de la curvatura hidrotrópica con los componentes que participan en su regulación. La producción de las ERO y la liberación de Ca2+ son respuestas básicas de la célula que modulan mecanismos de defensa como lo muestran las modificaciones que sufre la curvatura hidrotrópica cuando hay un desbalance de las ERO o un aumento en la concentración de Ca2+ en el citosol (Jimenez-Nopala et al., 2018; Shkolnik et al., 2018). Así mismo, OSCA1.1 y PCaP1 contribuyen a la respuesta hidrotrópica, sin embargo, lo hacen de manera independiente de la vía de señalización que incluye a MIZ1 y ECA1 (Akita & Miyazawa, 2022), (Tanaka-Takada et al., 2019).
En la zona de la curvatura de la raíz coinciden la acumulación de las ERO, de autofagosomas y de Ca2+ (Figura 2, panel B, números 2, 6 y círculos color rosa), por consiguiente, la autofagia canónica contiende con las macromoléculas y organelos oxidados, y por tanto dañados, durante la respuesta hidrotrópica (Jimenez-Nopala et al., 2018). Por otra parte, la interacción entre ECA1 y MIZ1 regula el tránsito de regreso del Ca2+ del citosol al RE (Dietrich et al., 2017), lo que parece indicar que la autofagia selectiva (reticulofagia) participa en la regulación de la homeóstasis de Ca2+ a través de la interacción de ECA1 o MIZ1 con las proteínas ATG8, para el tránsito de regreso del Ca2+ del citosol al RE, a través de la generación o liberación de ECA1.
Así mismo, la región reguladora de la transcripción de algunos genes de la maquinaria de la autofagia contiene sitios hipotéticos de unión a la calmodulina, proteína de unión al Ca2+, lo que indica una posible regulación de la autofagia por el Ca2+. El descubrimiento futuro de la interacción entre la autofagia, el Ca2+ y el H2O2 durante la respuesta hidrotrópica serán elementos clave que aporten una mayor información del comportamiento de la raíz en condiciones de escasez de agua y con elementos que permitan una mejor selección de plantas resistentes a esta.











 nueva página del texto (beta)
nueva página del texto (beta)


