Introducción
Una gran parte de los agroquímicos que se aplican en los campos de cultivo se movilizan a través del aire, el suelo y el agua hacia los ecosistemas terrestres y acuáticos como ríos, lagos y zonas costeras (García-Hernández et al., 2018) (Figura 1). La Laguna El Tóbari (LT), no es la excepción, ya que recibe el aporte de aguas residuales que incluyen agroquímicos, nutrientes, metales y metaloides provenientes de una de las zonas agrícolas más importantes del estado de Sonora, el Valle del Yaqui (VY) (Cantu-Soto et al., 2011; Arreola-Lizárraga, 2013). En este valle agrícola se encuentran residuos de Compuestos Orgánicos Persistentes (COPs) en suelos a concentraciones que varían desde los no detectables (ND) hasta los 3.13 µg/g con mayores concentraciones de 1,1,-dicloro-2,2-bis(p-clorofenil) etileno(4,4’-DDE) (Macías-Zamora, Sánchez-Osorio & Ramírez-Álvarez, 2011). También se ha reportado la presencia de diclorodifeniltricloroetanos (∑DDT) en músculo de peces de la LT (N.D. a 0.084 µg/g) y en hígado (ND a 0.185 µg/g) (Macías-Zamora, Sánchez-Osorio & Ramírez-Álvarez, 2011). Por lo tanto, es necesario determinar la presencia de estos contaminantes en otras especies y evaluar los efectos que tienen en los ecosistemas costeros receptores de aguas residuales agrícolas del VY.
Las aves de acecho y de sondeo se alimentan de una amplia variedad de presas en los hábitats acuáticos (Oliveira-Brito & Bugoni, 2015). Su movilidad en los ecosistemas, el nivel trófico que ocupan, además del uso de hábitats agrícolas, puede resultar en una alta exposición a contaminantes ambientales persistentes, incluyendo los COPs, los bifenilos policlorados (BPC’s), los metales y los metaloides (Berny et al., 2002; Fasola, Movalli & Gandini, 1998). Es por ello que las aves acuáticas son utilizadas como bioindicadores de la salud de los ecosistemas y por su consecuente capacidad de bioacumulación (Fasola et al., 1998; Bekhit et al., 2011; Champoux, Rail, Lavoie & Hobson, 2015).
En la evaluación de la concentración de los COPs en las aves, son ampliamente utilizadas las muestras no invasivas como las plumas y los huevos. Las hembras en reproducción tienen la capacidad de transferir algunos contaminantes a los huevos, transportados directamente de la madre vía el metabolismo de lípidos. El muestrear huevos de aves, en lugar de otro tipo de tejido, como, por ejemplo, sangre, implica menos estrés y perturbación a las aves, una unidad puede ser considerada estadísticamente representativa de la puesta y el hecho de retirar una pieza no afecta significativamente los parámetros de la población, ya que los adultos rara vez pueden criar toda la nidada. Además, la etapa de reproducción en las colonias facilita el muestreo (Huertas, Grimalt, Jover, Sanpera & Ruiz, 2016; Fasola, 1998).
En los estudios realizados por Ohlendorf, Custer, Lowe, Rigney & Cromartie, 1988; Ohlendorf & Marois, 1990, se reportó que las poblaciones de Garzón Gris (Ardea herodias) en las costas de California han disminuido y que hubo polluelos con anormalidades en el desarrollo; se encontraron concentraciones promedio de 24 µg/g peso húmedo de 4,4’-DDE en los huevos y una correlación significativa entre las concentraciones del contaminante y el adelgazamiento del cascarón. Así mismo, este contaminante se detectó en más del 10% de los huevos de Pedrete Corona Negra (Nycticorax nycticorax), con concentraciones de >8 µg/g peso húmedo, niveles que han sido asociados con alteraciones en la reproducción. Un estudio de monitoreo de las aves de colonia, en el lago Salton, California, durante un periodo de 6 años, demostró que las especies Garzón Gris, Garza Ganadera (Bubulcus ibis) y Cormoran Orejudo (Phalacrocorax auritus) tuvieron los descensos más pronunciados de nidos activos respecto al resto de las especies estudiadas (USGS 93-4014, 1993). En un trabajo realizado en los Valles: del Yaqui, de Mexicali y de Culiacán se reportaron concentraciones de 0.009 a 26 µg/g (peso húmedo) de 4,4’-DDE en organismos completos de ocho especies de aves colectadas en las tres regiones; los niveles de este contaminante fueron significativamente mayores en las especies predadoras tope, respecto a las granívoras (Mora, 1997).
En el presente trabajo se estudiaron las concentraciones de los COPs en huevos de Espátula Rosada (Platalea ajaja), Garcita Dedos Dorados (Egretta thula), Garzón Gris (Ardea herodias), Garza Rojiza (Egretta rufescens), y Pedrete Corona Clara (Nyctanasa violacea) y su relación con el dragado a la LT.
Materiales y Métodos
Colecta de muestras
El muestreo se realizó en el estero Chilicochi (27°04’40.01’’N, 110°00’06.66’’O), ubicado en la parte interna de la isla Huivulai. Esta isla forma parte del sistema lagunar de El Tóbari, en la zona costera del VY en el sur de Sonora, y es parte de la Reserva de la Biósfera Islas del Golfo de California (CONANP, 1996) (Figura 2). El Chilicochi es una zona con vegetación espesa formada principalmente por tres especies de mangle (blanco Laguncularia racemosa, negro Avicennia germinans y rojo Rhizophora mang
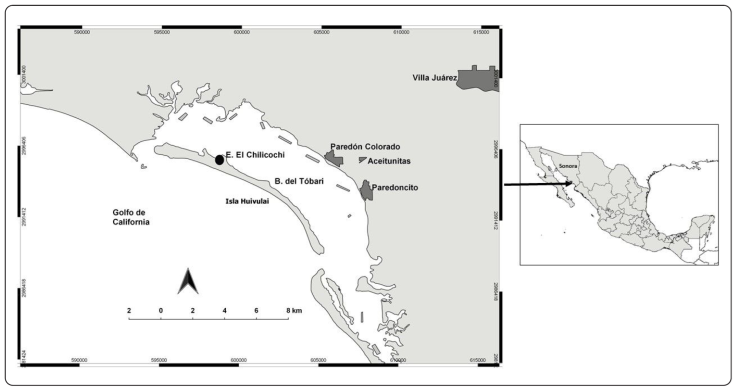
Figura 2 Sitio de colecta de huevos de aves en el estero Chilicochi ubicado en la Isla Huivulai, al sur del estado de Sonora, México (Coordenadas en UTM).
Se tramitaron los permisos de colecta SGPA/DGSV/03944/IO y SGPA/DGVS/04826/II ante la Dirección General de Vida Silvestre. Los huevos se colectaron de forma manual, primero al observar a la especie a la que correspondía el nido, y en cuanto el adulto lo dejaba, se inspeccionaba para verificar que hubiera huevos disponibles, posteriormente se tomó con cuidado un huevo por nido. En total se colectaron 30 huevos durante el periodo de 3 años de muestreo (Figura 3). Una vez colectados, se colocaron en un porta-huevos de plástico y en hieleras a 4 °C hasta su arribo al laboratorio en donde se mantuvieron en refrigeración previo a su análisis (Aguilera-Márquez, Leyva-García & García-Hernández, 2014).
En el laboratorio, los huevos colectados se lavaron con agua destilada y se secaron con servilletas de papel. Se midió la longitud y ancho del huevo en centímetros, estos datos fueron utilizados para calcular el Índice de Tamaño (IT) con la siguiente ecuación (Van der Pol, Anderson, Jodice & Stuckey, 2012; Anderson & Hickey, 1970):
El Volumen (V) se calculó mediante la fórmula reportada por Hoyt (1979):
donde L es la longitud (cm) y B el ancho (cm). De manera adicional, se midió el grosor del cascarón utilizando un vernier Mitutoyo® (Kawasaki, Japón), y se tomó el peso total (PT) en gramos del huevo completo y del cascarón. El peso del contenido (en g, clara y yema) se obtuvo de la diferencia del PT menos el peso del cascarón. El contenido se secó en un horno a 40 °C por 48 h o hasta sequedad. El cascarón y el contenido del huevo se homogenizaron por separado, utilizando un mortero de cerámica (Aguilera-Márquez, Leyva-García & García-Hernández, 2014).
Métodos analíticos
La extracción de los plaguicidas se llevó a cabo en un horno de microondas modelo MARSx marca CEM Corporation (Mathews NC, E.U.A.). Se pesaron 0.2 g del contenido de un huevo al que se agregaron 20 mL de una mezcla de diclorometano: hexano (1:1) (Daley, Leadley & Drouillard, 2009), esta preparación se introdujo en el horno de microondas programado a una temperatura de 100 °C y una presión de 100 psi durante 25 min, terminado el proceso la sustancia se dejó a temperatura ambiente para poder filtrarla en un filtro de fibra de vidrio (Whatman GF/F). El filtrado se llevó a sequedad a una temperatura no mayor a 60 °C y en baño María, con flujo de nitrógeno, mismo que se reconstituyó con 1 mL de hexano y se purificó en un cartucho con 1 g de sílica, alúmina, florisil y sulfato de sodio (Zhang et al., 2007). En el siguiente paso se eluyó con 10 mL utilizando una serie de solventes de acuerdo al método 3620C de la USEPA (USEPA, 2014). El extracto purificado se secó y se aforó a 1 mL con isooctano (2,2’,4-trimetilpentano). En el caso del cascarón se siguió el mismo proceso de extracción, aunque en la purificación solo se utilizó florisil y una mezcla diferente en la elución (hexano: acetona en proporción 1:1 v/v). Todos los solventes utilizados fueron grado HPLC.
Se cuantificaron el α-hexacloruro de benceno (BHC), γ-BHC, β-BHC, δ-BHC, heptacloro, heptacloro epóxido, aldrín, dieldrín, endrín, endrín aldehído, endosulfán i, endosulfán ii, endosulfán sulfato, 4,4’-DDD, 4,4’-DDE y 4,4’-DDT, usando cromatografía de gases con un detector de captura de electrones Varian Modelo CP 3800 (Santa Clara, CA, E.U.A), y con base en el método 8081A de la USEPA (USEPA, 1996). La cuantificación de los analitos se realizó a partir de curvas de calibración a cuatro puntos, y tres repeticiones por punto, en el intervalo de 0.00625 a 0.035 µg/g.
Para el control de calidad del análisis se añadió el decaclorobifenil a cada una de las muestras previo a la extracción como estándar subrogado, además de blancos y muestras fortificadas. Los porcentajes de recuperación se encontraron en el intervalo de 88-130 y un promedio de 108. El límite de cuantificación fue de 0.00625 µg/g para todos los analitos. Las concentraciones de COPs por contenido de huevo se transformaron de peso seco a peso húmedo considerando un 83 % de humedad, valor reportado por Frank et al. (2001) en los huevos de aves de colonia.
La validación del método se efectuó a partir de los ensayos de recuperación de las muestras fortificadas y blancos de las muestras de huevo comercial a distintas concentraciones. Se detectaron y cuantificaron 16 plaguicidas organoclorados y el decaclorobifenil, a partir de soluciones estándar y de curvas de calibración.
Análisis estadísticos
Las medidas morfométricas y las concentraciones de 4,4’-DDE en el cascarón y en el contenido de cada huevo no presentaron una distribución normal (Shapiro-Wilk test), por lo que se utilizaron pruebas no paramétricas con un nivel de significancia de 0.05. Para evaluar las diferencias morfológicas del huevo de cada especie entre los tres años de muestreo se utilizó la prueba de Kruskal-Wallis con chi-cuadrada y se reporta el valor-p. También se compararon las concentraciones de plaguicidas del contenido del huevo por especie entre los años de muestreo con la misma prueba no paramétrica y se realizaron regresiones lineares entre la concentración de plaguicidas, el grosor del cascarón y el índice de tamaño, por especie y por año de muestreo. Se utilizó el software John´s Macintosh Project (JMP) versión 8 (Sall & Lehman, 1996).
Resultados
Los valores medios de peso total, longitud, ancho, grosor, índice de tamaño y volumen, de los huevos de las 5 especies analizadas se enlistan en el Cuadro I. Se observa que para Espátula Rosada los valores de longitud y ancho del huevo variaron entre 65.33-66.30 mm y 42.67-43.00 mm, respectivamente. En el índice de tamaño y volumen no se observaron diferencias significativas (p>0.05) durante los años del estudio, con intervalos entre 27.87-28.36 mm2 y 60.65-62.17 mm3, respectivamente, pero sí hubo diferencias significativas en el PT y el grosor del cascarón (valor-p = 0.0439 y 0.0324 respectivamente), sin embargo, fue el año previo al dragado, de la laguna, en el que los valores son significativamente más altos. La longitud y el ancho del huevo de Garcita Dedos Dorados con intervalos entre 38.18-43.00 mm y 32.2-34 mm, respectivamente; en los valores del peso total, y el índice de tamaño y volumen sin diferencias significativas (p>0.05), contrario a que el cascarón presentó un mayor grosor en el año 2010 (valor-p = 0.0319). En Garzón Gris los valores fueron de 57.42-63.5 mm y 42.85-46.00 mm para la longitud y el ancho de huevo, respectivamente; sin diferencias significativas (p>0.05) en el peso total, el grosor del cascarón, el índice de tamaño y el volumen en los años de muestreo. De la Garza Rojiza los datos son de los años 2010 y 2011, con valores para la longitud y el ancho y de 47.67-52.00 mm y 36.00-36.57 mm, respectivamente; sin diferencias significativas en el peso total, grosor del cascarón, el índice de tamaño y el volumen en los años de muestreo. Únicamente se logró colectar un huevo de Pedrete Corona Clara en 2011, por lo que no se pudieron hacer comparaciones entre los años.
Cuadro I Resumen de las medidas morfológicas de los huevos de Espátula Rosada (PLAAJA), Garcita Dedos Dorados (EGRTHU), Garzón Gris (ARDHER), Garza Rojiza (EGRRUF) y Pedrete Corona Clara (NYCVIO), (Pyle & DeSante, 2012) (media ± Desv. Std.)
| Código/especie | año de colecta | peso total (gr) | longitud (mm) | ancho (mm) | grosor del cascarón (mm) | índice de tamaño (cm2) | volumen (cm3) |
|---|---|---|---|---|---|---|---|
| PLAAJA | 2010 | 71.65* | 66.3 | 42.68 | 0.86* | 28.20 | 61.36 |
| (n=2) | ±1.36 | ±5.59 | ±3.29 | ±0.06 | ±0.20 | ±4.29 | |
| 2011 | 55.51 | 65.33 | 42.67 | 0.60 | 27.87 | 60.65 | |
| (n=3) | ±1.79 | ±1.16 | ±0.58 | ±0.00 | ±0.45 | ±1.45 | |
| 2012 | 61.69 | 66.00 | 43.00 | 0.60 | 28.36 | 62.17 | |
| (n=3) | ±3.67 | ±3.46 | ±1.00 | ±0.00 | ±0.96 | ±1.58 | |
| EGRTHU | 2010 | 22.7 | 38.18 | 32.58 | 0.38 | 12.42 | 20.62 |
| (n=2) | ±2.25 | ±2.65 | ±1.03 | ±0.02 | ±0.47 | ±0.14 | |
| 2011 | 19.73 | 43.00 | 32.20 | 0.20 | 13.85 | 22.74 | |
| (n=5) | ±2.24 | ±1.23 | ±0.45 | ±0.00 | ±0.44 | ±0.90 | |
| 2012 | 17.27 | 43.00 | 34.00 | 0.10 | 14.62 | 25.35 | |
| (n=1) | |||||||
| ARDHER | 2010 | 56.88 | 57.42 | 42.85 | 0.57 | 24.64 | 54.09 |
| (n=3) | ±9.89 | ±2.55 | ±2.907 | ±0.191 | ±2.56 | ±8.93 | |
| 2011 | 60.05 | 63.5 | 46.00 | 0.50 | 29.21 | 68.53 | |
| (n=2) | ±2.82 | ±0.71 | ±0.00 | ±0.00 | ±0.33 | ±0.76 | |
| 2012 | 62.98 | 62.75 | 44.25 | 0.44 | 27.77 | 62.71 | |
| (n=4) | ±4.42 | ±0.96 | ±1.50 | ±0.048 | ±0.96 | ±4.21 | |
| EGRRUF | 2010 | 35.15 | 47.67 | 36.57 | 0.42 | 17.43 | 32.52 |
| (n=3) | ±4.14 | ±5.51 | ±0.16 | ±0.13 | ±2.07 | ±3.98 | |
| 2011 | 32.79 | 52.00 | 36.00 | 0.30 | 18.72 | 34.37 | |
| (n=1) | |||||||
| NYCVIO | 2011 | 28.72 | 50.00 | 36.00 | 0.30 | 18.00 | 33.05 |
| (n=1) |
* indica diferencias significativas entre los años de colecta (chi-cuadrada < 0.05, Tukey Kramer).
En el Cuadro II se muestran las concentraciones de COPs en las 5 especies analizadas durante los 3 años de muestreo. El metabolito 4,4’-DDE fue detectado en el contenido de los huevos en todas las muestras, con concentraciones entre 0.17 y 17.86 µg/g peso húmedo (mediana = 2.17 µg/g). Los valores máximos de β-BHC, heptacloro epóxido, 4,4’-DDD y 4,4’-DDT de 0.09, 0.02, 0.08 y 0.08 µg/g, respectivamente; y los mínimos de 0.04, 0.004, 0.04 y 0.03 µg/g peso húmedo, respectivamente. El α- BHC se determinó en una muestra, con un valor de 0.04 µg/g. Por otro lado, γ-BHC, δ-BHC, heptacloro, aldrín, dieldrín, endrín, endrín aldheído, endosulfán i, endosulfan ii y endosulfán sulfato no se detectaron.
Cuadro II Mediana (± Desv. Std.) de la concentración de plaguicidas organoclorados (µg/g peso húmedo) en el contenido de los huevos de Espátula Rosada (PLAAJA), Garcita Dedos Dorados (EGRTHU), Garzón Gris (ARDHER), Garza Rojiza (EGRRUF) y Pedrete Corona Clara (NYCVIO).
| Especie | PLAAJA | EGRTHU | ARDHER | EGRRUF | NYCVIO | |||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Año | 2010 (n=2) | 2011 (n=3) | 2012 (n=3) | 2010 (n=2) | 2011 (n=5) | 2012 (n=1) | 2010 (n=3) | 2011 (n=2) | 2012 (n=4) | 2010 (n=3) | 2011 (n=1) | 2011 (n=1) |
| OCPs (µg/g) | ||||||||||||
| α-BHC | ND | ND | ND | ND | ND | ND | ND | ND | ND | 0.0375 | ND | ND |
| γ-BHC | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND |
| β-BHC | ND | 0.05 | ND | 0.09 | ND | ND | 0.05 | 0.05 | ND | ND | ND | ND |
| δ-BHC | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND |
| heptacloro | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND |
| heptacloro | ND | ND | ND | ND | ND | 0.004 | 0.02 | 0.01 | 0.004 | ND | ND | ND |
| epóxido | (± 0.007) | |||||||||||
| aldrín | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND |
| dieldrín | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND |
| endrín | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND |
| endrín aldehído | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND |
| endosulfán i | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND |
| endosulfán ii | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND |
| endosulfán sulfato | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND | ND |
| 4,4’-DDD | 0.08 | 0.05 | ND | ND | ND | ND | 0.04 | 0.06 | ND | ND | ND | ND |
| (± 0.01) | ||||||||||||
| 4,4’-DDE | 4.82 | 6.68 | 1.59 | 1.06 | 1.76 | 3.41 | 10.32 | 6.94 | 2.54 | 0.74 | 5.49 | 2.31 |
| (± 3.86) | (± 3.56) | (± 0.12) | (± 0.72) | (± 0.91) | (± 7.33) | (± 4.03) | (± 2.55) | (±0.08) | ||||
| 4,4’-DDT | 0.03 | 0.05 | ND | ND | ND | ND | 0.08 | ND | ND | ND | ND | ND |
Las concentraciones de 4,4’-DDE en los cascarones de las aves variaron: en Garzón Gris con el intervalo 0.81-17.86 µg/g, en Espátula rosada con 0.69-7.81 µg/g, en la Garcita Dedos Dorados entre los valores 0.17-2.74 µg/g y en la Garza Rojiza de 0.69-6.32 µg/g. Se encontró una correlación negativa entre la concentración de 4,4’-DDE y el grosor del cascarón (R2=0.35) en la Garcita Dedos Dorados (Figura 4).
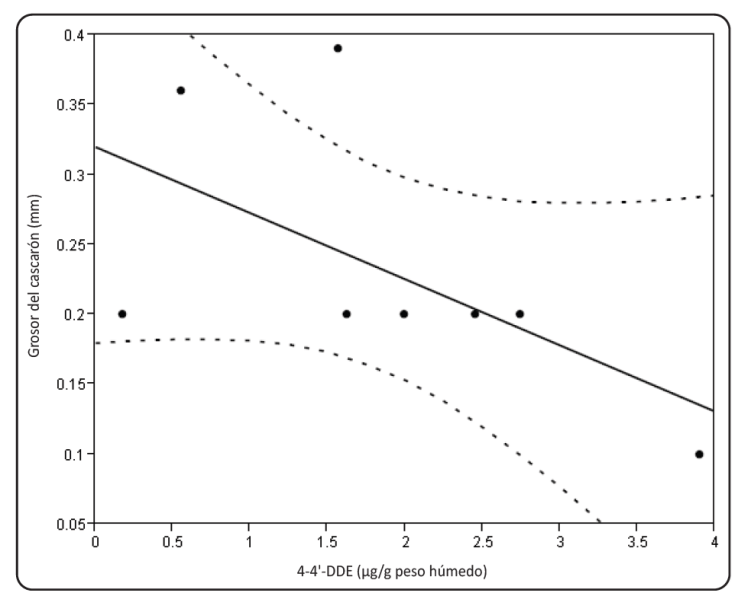
Figura 4 Correlación entre el grosor del cascarón (mm) y la concentración de 4,4’-DDE (µg/g peso húmedo) en huevos de Garcita Dedos Dorados. Grosor del cascarón (mm) = 0.32 - 0.047*4,4’-DDE (µg/g peso húmedo), R2 = 0.35.
Debido a que, del total de especies de estudio, solo se lograron recolectar los huevos de 3 especies: Garzón Gris, Espátula Rosada y Garcita Dedos Dorados en los 3 años consecutivos, porque en las otras dos especies hubo discontinuidad; el 4,4’-DDE fue el organoclorado presente en el contenido de los huevos del total de las muestras y al compararse las concentraciones de este compuesto en las especies citadas no se observaron diferencias significativas (valor-p = 0.0743), probablemente por el número reducido de muestras. No obstante, se vio una disminución de la concentración de 4,4’-DDE en el muestreo de los años recientes (Figura 5).
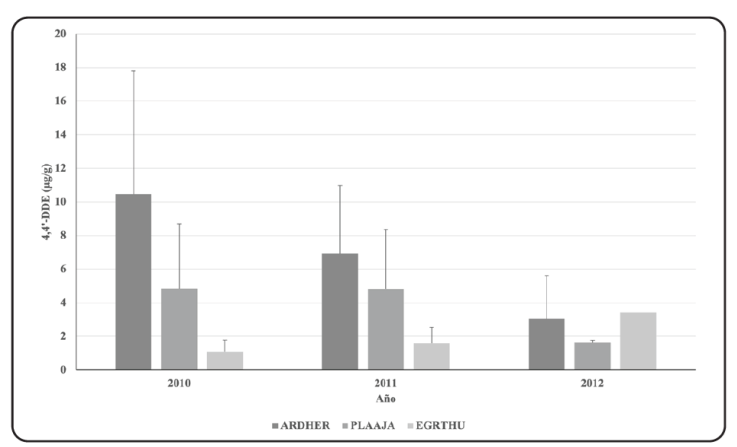
Figura 5 Concentraciones de 4,4’-DDE en contenido de huevo de tres especies de aves muestreadas del año 2010 a 2012 en el estero Chilicochi, Laguna El Tóbari, Sonora, México.
Los resultados del análisis al cascarón (Cuadro III) en las muestras del año 2010 sólo se llevaron a cabo en dos especies: Garza Rojiza y Garzón Gris en las que se encontró: β-BHC, heptacloro, endrín aldheído y 4,4’-DDE, este último en las 2 especies estudiadas, con mediana de 2.54 y 1.23 µg/g, respectivamente. Con diferencias en la distribución del 4,4’-DDE entre el cascarón y el contenido del huevo. La concentración de 4,4’-DDE en la Garza Rojiza fue más alta en el cascarón que en el contenido, a diferencia de los datos en el Garzón Gris con un mayor contenido en el huevo que en el cascarón.
Cuadro III Mediana (± Desv. Std.) de la concentración de plaguicidas organoclorados (µg/g peso seco) en el cascarón de los huevos de Garcita Dedos Dorados (EGRTHU) y de Garzón Gris (ARDHER) en el año 2010.
| Especie | EGRRUF | ARDHER | ||
|---|---|---|---|---|
| Matriz |
|
|
|
|
| OCPs (µg/g) | ||||
| α-BHC | ND | 0.04 | ND | ND |
| β-BHC | 1.95 | ND | ND | 0.05 |
| heptacloro | 0.06 | ND | ND | ND |
| heptacloro epóxido | ND | ND | ND | 0.02(±0.01) |
| endrín aldehído | ND | ND | 0.02 | ND |
| 4,4’-DDD | ND | ND | ND | 0.04 |
| 4,4’-DDE | 2.54(±1.67) | 0.76(±0.08) | 1.23(±1.24) | 10.46(±7.33) |
| 4,4’-DDT | ND | ND | ND | 0.08 |
Discusión
El monitoreo de los huevos en las aves de colonia en un sitio impactado por frecuente drenado agrícola, nos proporcionó información sobre las concentraciones de COPs, así como de la condición del huevo. En el caso del peso total y el grosor del cascarón de la Garcita Dedos Dorados, los valores más altos correspondieron con el año previo al dragado. Es posible que por lo mismo en el año 2011 disminuyera el alimento y se alterara la masa total del huevo, aunque no parece haberles afectado a otras especies, tal vez porque se alimentan solo en la zona lacustre de presas más pequeñas como peces, crustáceos, moluscos, semillas e insectos. A diferencia de las garzas que se alimentan principalmente de peces, insectos y crustáceos tanto en el mismo sitio como en el estuario (Oliveira-Brito & Bugoni, 2015).
En cuanto a los residuos de los plaguicidas organoclorados, la razón DDT/DDE en las muestras dio por resultado valores < 1 en todos los casos, lo que indica un uso histórico de este compuesto (Cantú-Soto et al., 2011). Como ejemplos de su aplicación, y un paréntesis en el tema que nos ocupa, el algodón fue el principal cultivo en Sonora de 1965 a 1975 (Grijalva-Díaz, 2014) donde se aplicó el DDT de manera intensiva para el control de las plagas, e igual sucedió en Mexicali en 1973 para el mismo cultivo reportándose niveles de hasta 17 kg/ha de este compuesto (García-Hernández, 2019). Es por ello que los residuos de este plaguicida y sus metabolitos continúan presentes en los suelos agrícolas de Sonora (Leal-Soto et al., 2014; Macías-Zamora et al., 2011).
También en estudios previos y realizados desde el norte del Golfo de California hasta el sur de México, en colonias de Bobo Café (Sula leucogaster) se encontró 4,4’-DDE en más del 99% de las muestras (Mellink, Riojas-López & Luévano-Esparza, 2009) y en Pelícano Café (Pelecanus occidentalis) del Golfo de California (Van der Pol et al., 2012). En lo que respecta al tema de las aves marinas, Mellink et al. (2009), no encontraron alteraciones en el grosor del cascarón entre los huevos de las colonias, posiblemente porque las concentraciones de 4,4’-DDE no excedieron el 0.05 µg/g de peso húmedo. Sin embargo, estudios realizados en los huevos de aves del sistema lagunar Altata-Ensenada del Pabellón en Sinaloa, se reportaron concentraciones de 4,4’- DDE de 0.25 µg/g (peso húmedo) en las garzas (Egretta sp.) (Carvalho et al., 2002). Los estudios reportan las mayores concentraciones de este compuesto en aves que anidan en sitios localizados, adyacentes, a los valles agrícolas intensivos y extensivos, como el Valle del Yaqui con una extensión de 227,000 ha y el Valle de Culiacán con 212,000 ha (Pedroza-González & Hinojosa-Cuéllar, 2014).
En el presente estudio se encontró una correlación negativa entre la concentración de 4,4’-DDE y el grosor del cascarón, únicamente en la Garcita Dedos Dorados. De acuerdo con Fasola et al. (1998), existe una ligera influencia en el éxito reproductivo del Garzón Gris en los huevos con niveles máximos (peso húmedo) de 26 µg/g de 4,4’-DDE y 13 µg/g de BPC’s, por lo que estos autores indican que para que se relacione la disminución del grosor del cascarón con la concentración de 4,4’-DDE, los valores deben alcanzar los 24 µg/g, para esta especie. En Ibis Cara Blanca (Plegadis chihi) que es una especie de tamaño similar al de la Garcita Dedos Dorados, las concentraciones de 4,4’-DDE > 4 µg/g de peso húmedo presentaron una disminución del 16.2% en el grosor del cascarón y una reducción del 30% de volantones, comparados con nidos con menores concentraciones (Henny & Herron, 1989). Tomando en cuenta el valor de 4 µg/g de peso húmedo de 4,4’-DDE como el valor límite de referencia para posibles efectos reproductivos en las aves de colonia, se observa que para Garzón Gris, un 55% de las muestras, excedieron este valor, para la Espátula rosada un 37%, para la Garza rojiza un 25%, para la Garcita Dedos Dorados un 12% y 0% para el Pedrete Corona Clara. Sin embargo, a pesar de que las concentraciones en la Garcita Dedos Dorados estuvieron en su mayoría por debajo del límite de referencia, fue la única especie con un probable efecto del 4,4’-DDE en el grosor del cascarón (Figura 4), por lo que es probable que esta especie sea más sensible que las otras. Sin embargo, es necesario un mayor esfuerzo de muestreo para poder evidenciar posibles diferencias entre las especies.
Los resultados indican que no existe una relación entre el índice de tamaño y la concentración de 4,4’-DDE. Vander Pol et al. (2012) compararon el índice de tamaño del huevo de Pelícano café en dos sitios de anidación (Carolina del Sur y Golfo de California), y no encontraron diferencias significativas (p>0.05). Sin embargo, sí las hubo en las proporciones de los metabolitos del DDT en los dos sitios, con una más alta en el Golfo de California, lo que indica un uso más reciente del plaguicida en esta región.
La variación observada en las concentraciones de 4,4’-DDE a lo largo de los tres años y que fue menor en los años recientes de muestreo, podría estar relacionado a una menor disponibilidad de alimento posterior al dragado y a una probable perturbación física en el ecosistema (Oliveira-Brito & Bugoni, 2015; Baker & Sepulveda, 2009) y por lo tanto menor acumulación del contaminante en las aves vía red trófica. Con excepción de la Garcita Dedos Dorados, que sí acumuló mayores concentraciones, en 2012, posterior al año de dragado.
Asimismo, las diferencias en las concentraciones de plaguicidas es probable que sea por los hábitos alimenticios de cada especie. Por ejemplo, el Garzón Gris habita en aguas dulces como saladas y se alimenta en los pastizales y en los campos de cultivo de reptiles, mamíferos pequeños, insectos, anfibios y peces (Krebs, 1974; Custer & Galli, 2002); contrariamente la Garza Rojiza está restringida a los humedales costeros poco profundos y su alimentación consiste de peces de aguas someras eurihalinas (Koczur, Kent, Ballard, Meyer & Green, 2018).
El dragado en la Laguna el Tóbari se realizó con el fin de mejorar las condiciones hidrodinámicas del sistema lagunar, ya que éstas fueron afectadas por un proceso de azolvamiento debido al continuo vertimiento de aguas residuales agrícolas, urbanas y acuícolas, y a la disminución de las corrientes por el pedraplén que comunicaba a la costa con la isla Huivulai (Arreola-Lizárraga, 2013). Las aguas residuales contienen diferentes contaminantes, muchos de los cuales se ligan rápidamente con la materia particulada presente en la columna de agua, para finalmente sedimentarse en el fondo marino. La perturbación o resuspensión del sedimento libera a los contaminantes a la columna de agua circundante y así se vuelven biológicamente disponibles (Knott, Aulbury, Brown & Johnston, 2009). Un estudio realizado por Hedge, Knott & Johnston (2009) reportó el efecto del dragado en la concentración de metales en los ostiones, en los que se observó un marcado incremento de nivel, comparado con los estuarios de referencia sin dragado. Sin embargo, no se observó un claro aumento de las concentraciones de los plaguicidas en la biota. La acumulación de metales y metaloides en los organismos acuáticos depende, no solamente de las propiedades fisicoquímicas de los elementos, sino también de los organismos y de las estrategias biológicas que han desarrollado de desintoxicación o para reducir la exposición a altas concentraciones de estos elementos en los tejidos de las especies. En cambio, los compuestos organoclorados son de naturaleza altamente hidrofóbica, por lo que tienden a asociarse a partículas suspendidas en el cuerpo de agua, o con los lípidos de la biota, y su acumulación se da en respuesta a procesos fisicoquímicos muy específicos. El coeficiente de partición entre los organoclorados y los lípidos es considerado el mecanismo de ingesta más importante (Mackay, Celsie, Powell & Parnis, 2018). Los grandes vertebrados y mamíferos marinos incorporan a los compuestos organoclorados directamente desde su dieta y no por la ingesta directa de agua (Phillips, 1995; Knott et al., 2009). Las rutas de excreción de los compuestos organoclorados también difieren entre estos grupos, siendo la partición la forma predominante en especies pequeñas a diferencia de la reproducción y el metabolismo que son las rutas de excreción más importantes en los mamíferos marinos y en las aves (Phillips, 1995, Knott et al., 2009).
Conclusiones
Este estudio confirmó la presencia de plaguicidas organoclorados en los huevos de diversas especies de aves en una laguna costera adyacente a la zona agrícola del Valle del Yaqui. Las concentraciones de 4,4’-DDE de hasta 17.86 µg/g en el Garzón Gris, indican una mayor bioacumulación en las aves de hábitos piscívoros. Un 55% de muestras de esta especie excedieron el límite de 4 µg/g de 4,4’-DDE determinado para Ibis Cara Blanca, un ave de colonia. En la Garcita Dedos Dorados se observó una correlación negativa entre las concentraciones de 4,4’-DDE y el grosor del cascarón, indicando posible afectación en esta especie. El proceso del dragado de la laguna no reflejó incrementos en las concentraciones de estos compuestos; por el contrario, se observaron disminuciones en los niveles, lo que se puede deber a una escasez temporal de alimento por la perturbación física de los sedimentos y, por lo tanto, una menor concentración de contaminantes.











 nueva página del texto (beta)
nueva página del texto (beta)