Introducción
Los nematodos agalladores Meloidogyne spp. son de los patógenos del suelo más importantes que limitan la productividad de los cultivos (Brito et al., 2008). Muchas de las especies están ampliamente distribuidas a nivel mundial en donde ocasionan pérdidas severas a los rendimientos y a la calidad de las cosechas (Hunt y Handoo, 2009; Karssen et al., 2013; Subbotin et al., 2021; Desaeger, 2022; Wesemael et al., 2024); algunas de estas especies se encuentran en las diferentes regiones agrícolas de nuestro país, ocasionando mermas importantes a los rendimientos y a veces pérdidas totales al afectarse la calidad de las cosechas, esto último hace que pierdan su valor comercial (Medina-Canales et al., 2011; Medina-Canales et al., 2012; Medina-Molina et al., 2018; Cid del Prado-Vera et al., 2018; Cristóbal-Alejo et al., 2018). En México, la zona agrícola conocida como el Valle de Tepeaca, en el estado de Puebla, una importante zona productora de hortalizas para el mercado nacional, destaca por la producción de zanahoria (Daucus carota L.), cilantro (Coriandrum sativum L.), betabel (Beta vulgaris L.), calabaza (Cucurbita pepo L.), brocoli (Brassica oleracea var. italica L.), lechuga (Lactuca sativa L.), col (Brassica oleracea var. capitata L.), coliflor (Brassica oleracea var. botrytis L.), entre otros (SIAP, 2020); en donde están presentes varias especies del nematodo agallador Meloidogyne como: M. chitwoodi (Montes-Belmont, 2000), M. incognita (Cid del Prado Vera et al., 2001), M. arenaria y M. hapla (Medina-Canales et al., 2011; Cid del Prado-Vera et al., 2018) y otras más atacando a éstas y a otras hortalizas. Autores como Medina-Canales et al. (2011, 2012) y Medina-Molina et al. (2018) han encontrado en la zona alta incidencia por estos nematodos en variedades comerciales de zanahoria y betabel; es frecuente que las pérdidas sean totales debido a que algunas de las cosechas al estar deformadas o con presencia de agallas prominentes pierdan su valor comercial. Hoy en día la identificación de las especies es de vital importancia, para contar con un diagnóstico preciso y oportuno y con ello poder diseñar programas de manejo para cada especie del nematodo y cultivo. La literatura actual hace referencia que para la identificación precisa de las especies de nematodos agalladores Meloidogyne es recomendable recurrir a métodos bioquímicos, moleculares y morfológicos entre los que debe de haber complementariedad (Carta et al.,2005; Powers & Ramírez-Suárez, 2012; Karssen et al., 2013; Wesemael et al., 2024). Los métodos bioquímicos, donde destacan los “fenotipos isoenzimáticos” de esterasa (EST) y malato deshidrogenasa (MDH), son muy valiosos para la identificación de las especies más importantes de Meloidogyne, son una herramienta estable, sensible, rápida, confiable y económica (Brito et al., 2010; Karssen et al., 2013; Subbotin et al., 2021, Wesemael et al., 2024). Esta herramienta es útil para estudios extensivos, en donde se busca evaluar la distribución de las especies, búsqueda de especies atípicas, permite detectar mezcla de especies en los cultivos (Souza, 2008). Esta prueba puede ser confirmatoria y complementaria a los datos morfológicos en especial con el patrón perineal de hembras (Hunt & Handoo, 2012). En el caso de los métodos moleculares es indispensable elegir correctamente los marcadores moleculares a utilizar, ya que con algunos de éstos no es posible distinguir especies emparentadas cercanamente (Carta et al., 2005; Adams et al., 2007; Karssen et al., 2013; Wesemael et al., 2024); además de que requieren de equipo costoso y reactivos caros importados, lo que los hace poco atractivos y prácticos. Por su parte, la morfología sigue siendo de gran valor en la identificación de las especies de nematodos agalladores dentro de éstos destaca en particular el patrón perineal de hembras, una de las herramientas más frecuentemente utilizadas. Este patrón describe la morfología de la región posterior de las hembras adultas en donde se localizan la zona vulva-ano (perineo), la terminación de la cauda, los fasmidios, las líneas laterales rodeadas por estrías cuticulares, este conjunto de caracteres son especie-específicos y por lo tanto de gran utilidad para la identificación de las especies (Hunt & Handoo, 2012; Karssen et al., 2013; Rosas-Hernández et al., 2024).
El objetivo del presente trabajo fue: Identificar las especies de Meloidogyne asociadas a hortalizas de la zona agrícola el Valle de Tepeaca, Puebla, utilizando la prueba de fenotipos isoenzimáticos de EST y MDH y complementar la identificación mediante la técnica morfológica de los patrones perineales de hembras adultas.
Materiales y métodos
Recolecta de material
Durante 2018-2019 se realizaron seis muestreos de suelo y raíces de diversas hortalizas en el municipio de Acatzingo, Puebla (18º 55º 30” y 19º 06’ 18” Latitud Norte y 97º 48’ 18” y 97º 59’ 18” longitud oeste); dichos muestreos se programaron de tal forma que coincidieran con la madurez de los cultivos, pues durante este período las agallas producidas por los nematodos son más visibles, favoreciendo así el reconocimiento de plantas infectadas (Brito et al., 2008). El muestreo se realizó de manera aleatoria en dos campos de zanahoria, uno de calabaza, uno de cilantro y uno de betabel. Estos campos fueron previamente muestreados y se detectó la presencia de este nematodo provocando poco crecimiento de plantas, agallas y deformaciones en las raíces (Medina-Canales et al., 2011; Medina-Molina et al., 2018).
La superficie muestreada en cada campo fue de aproximadamente una hectárea y en cada uno se recolectaron diez submuestras, las cuales constaron de 200 g de suelo y 100 g de raíces (Shurtleff & Averre, 2000). Cada muestra compuesta de cada cultivo se colocó en una bolsa de polietileno debidamente etiquetada con los datos de campo, las que se trasladaron al Laboratorio de Nematología Agrícola, del Departamento de Parasitología de la Escuela Nacional de Ciencias Biológicas del Instituto Politécnico Nacional, en donde fueron procesadas (De la Jara-Alcocer et al., 1994; Shurtleff & Averre, 2000).
Separación de raíces con agallas
Las raíces con agallas de cada muestra se separaron y lavaron con cuidado para eliminar el suelo adherido. Con ayuda de un estereomicroscopio y agujas de disección se extrajeron 40 hembras de 40 agallas (con sus respectivas masas de huevos) de cada campo muestreado, para determinar los fenotipos isoenzimáticos, analizar los patrones perineales y descartar mezcla de poblaciones (Brito et al., 2008; Medina-Canales et al., 2014; Da Cunha et al., 2021).
Determinación de fenotipos isoenzimáticos
Extracción y electroforesis de proteínas
Para determinar el fenotipo EST, cada hembra recolectada (en total se trabajaron con 40 hembras de cada campo muestreado de manera independiente) se colocó en un portaobjetos con 20 µL del regulador de extracción (20 g de sacarosa o glicerol, 2 mL de tritón X-100, 100 mL agua bidestilada), se lisó con ayuda de una punta de jeringa de insulina, se retiró la cutícula para posteriormente obtener el patrón perineal; tanto el regulador como el contenido de la hembra se colocaron en un tubo Eppendorff. Los tubos se centrifugaron a 13,000 rpm durante 2 minutos y se guardaron a -20°C hasta su uso. Para determinar el fenotipo MDH, el procesamiento de las hembras fue similar, variando únicamente el regulador de extracción (20 g de sacarosa o glicerol, 0.1 g de TRIS, 0.1 g de ascorbato, 0.1 g cisteína, 100 mL de agua bidestilada, pH 8.0) (Esbenshade & Triantaphyllou, 1985; Carneiro et al., 2024).
La electroforesis se realizó en geles de poliacrilamida, los cuales estuvieron formados por un gel separador con una concentración de acrilamida 12.5% y un gel concentrador al 18%. El gel se montó en una cámara de electroforesis vertical (EC® EU) y se colocó el regulador de corrimiento (TRIS 6 g, Glicina 28 g, Agua 1L, pH 8.3, Dilución 1:9) (Esbenshade & Triantaphyllou, 1985; Carneiro et al., 2024).
A los extractos de proteínas obtenidas previamente, se les colocaron 5 µL de azul de bromofenol 0.02% y la mezcla se colocó en los pozos del gel de poliacrilamida; el gel se dejó correr durante 30 minutos a 80 volts y después 70 minutos a 250 volts; se lavó con agua bidestilada y se realizó una tinción a 37°C durante 1 hora con la solución para teñir a la isoenzima de interés. Para los fenotipos isoenzimáticos EST se utilizaron 100 mL de regulador fosfatos, 30 mg de EDTA, 60 mg de fastblue RR y 40 mg de α-naftilacetato diluidos en 2 mL acetona; para el caso de los fenotipos isoenzimáticos MDH se utilizaron 10 mL de sol. A (10.6 g Na2CO3 + 13.4 g malato), 15 mL de sol. B (6.06 g TRIS, pH = 7.1), 50 mg de NAD, 30 mg de NBT, 50 mL de agua y 2 mg de PMS diluido en 26 mL de agua bidestilada (Esbenshade & Triantaphyllou, 1985; Carneiro et al., 2024).
Determinación del fenotipo isoenzimático
A partir del número de bandas y la movilidad electroforética se calculó la movilidad relativa (Rm) (Rm = distancia de migración de la banda proteica / la longitud de corrida total del gel x 100). Este índice es diferente entre especies de Meloidogyne, ya que a cada una le corresponde uno en específico.
Caracterización de patrones perineales
La cutícula obtenida anteriormente de 10 hembras de cada campo muestreado se colocó en un portaobjetos con una gota de ácido láctico al 45 %, se cortó ecuatorialmente con ayuda de una aguja de insulina. Después se hicieron los cortes de ajuste para tener el patrón perineal en forma de cuadrado. Cada patrón perineal se limpió cuidadosamente, posteriormente se transfirió a una gota de glicerina en un portaobjetos limpio, en donde se acomodó y se colocó un cubreobjetos, las preparaciones se etiquetaron con lo que quedaron listas para describir las características de los patrones de cada población (Hunt & Handoo 2012; Karssen et al., 2013).
Resultados
La Tabla 1 indica los cultivos muestreados, las localidades georreferenciadas, los patrones isoenzimáticos encontrados y las especies de Meloidogyne identificadas.
Tabla 1 Fenotipos isoenzimáticos y especies de Meloidogyne encontradas en diferentes cultivos de hortalizas, así como su localidad de origen dentro del Valle de Tepeaca, Puebla.Table 1. Isozyme phenotypes and species of Meloidogyne identify in different vegetable crops, as well as their locality of origin within the Tepeaca Valley, Puebla.
| Planta Hospedante | Ubicación geográfica | Localidad Municipio | Fenotipo enzimático | Especies | |
|---|---|---|---|---|---|
| EST | MDH | ||||
| Zanahoria (Daucus carota L.) | N 18º 58´ 549” O 97º 47´ 878” 1900 msnm | El Cristo, Acatzingo | A1, A2a, A3 | N1, N1e | M. arenaria |
| Calabacita (Cucurbita pepo L.) | N 18º 58´ 534” O 97º 47´ 855” 1900 msnm | El Cristo, Acatzingo | S1 | N1a | M. chitwodii |
| Cilantro (Coriandrum sativum L.) | N 18º 96´ 792” O 97º 79´ 017” 2138 msnm | Santa María Actipa, Acatzingo | G1 | N1a | Meloidogyne sp.1 |
| G1-VF1 | N1 | Meloidogyne sp.2 | |||
| Betabel (Beta vulgaris L.) | N 18º 87´ 583” O 97º 79´ 796” 2170 msnm | Santa María Actipa, Acatzingo | S1 | N1a | M. chitwoodi |
| H1 | H2 | M. hapla | |||
| J2a | N1 | M. javanica | |||
| Zanahoria (Daucus carota L.) | N 18º 97´ 429” O 97º 79´ 848” 2170 msnm | Santa María Actipa, Acatzingo | H1 | N2a | M. hapla |
| I1 | M. incognita | ||||
| VSI-SI | N1d | M. enterolobii | |||
Determinación de fenotipos isoenzimáticos y morfología del patrón perineal
Fenotipos de esterasa (EST)
Se encontraron once fenotipos de EST y 18 bandas importantes de actividad enzimática para las especies de Meloidogyne (Fig. 1) asociadas a zanahoria, cilantro, betabel y calabaza; además, se revisaron los patrones perineales, los cuales permitieron complementar la identificación con los fenotipos isoenzimáticos encontrados (Fig. 2). También se encontraron seis fenotipos de MDH y ocho bandas importantes de actividad enzimática (Fig. 1).
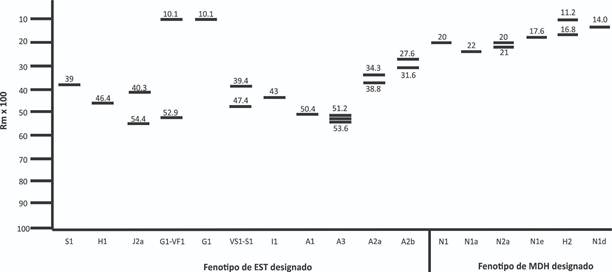
Figura 1 Representación esquemática de los fenotipos isoenzimáticos de EST y de MDH observados en Meloidogyne spp. provenientes de cultivos agrícolas el Valle de Tepeaca, Puebla.: S1 = M. chitwoodi; H1 = M. hapla; J2a = M. javanica; G1-VF1 = Meloidogyne sp. 1; G1 = Meloidogyne sp. 2, VS1-SI = M. enterolobii, I1 = M. incognita, A1, A3, A2a, A2b = M. arenaria. Fenotipos isoenzimáticos de MDH observados en Meloidogyne spp. N1= M. javanica, M. arenaria, Meloidogyne sp.2; N1a = M. chitwoodi, Meloidogyne sp.1; N2a = M. incognita; N1e = M. arenaria; H2 = M. hapla; N1d = No pudo asociarse a alguna especie.

Figura 2 Zimograma de los fenotipos isoenzimáticos de EST de Meloidogyne spp. provenientes de cultivos agrícolas el Valle de Tepeaca, Puebla: A y B) Fenotipos de M. arenaria, C) Fenotipo VS1-S1 de M. enterolobii, D) Fenotipo H1 de M. hapla, E) Fenotipo I1 de M. incognita, F) Fenotipo S1 de M. chitwodii, G) Fenotipo G1-VF1 de Meloidogyne sp. 2 y G1 de Meloidogyne sp. 1.
Los fenotipos correspondientes a M. arenaria fueron el A1 (Rm: 50.5), A3 (Rm: 51.2, 52.4, 53.6) y dos fenotipos atípicos designados como A2a (Rm: 34.3, 38.8) y A2b (Rm: 27.6, 31.6); todos se asociaron al cultivo de zanahoria (Tabla 1) (Figs. 1, 2A-B). El patrón perineal respectivo, fue redondeado con arco dorsal bajo, con hombreras en los costados formadas por ondulaciones pronunciadas de las estrías dorsales, cerca de las líneas laterales (Fig. 3A, B).
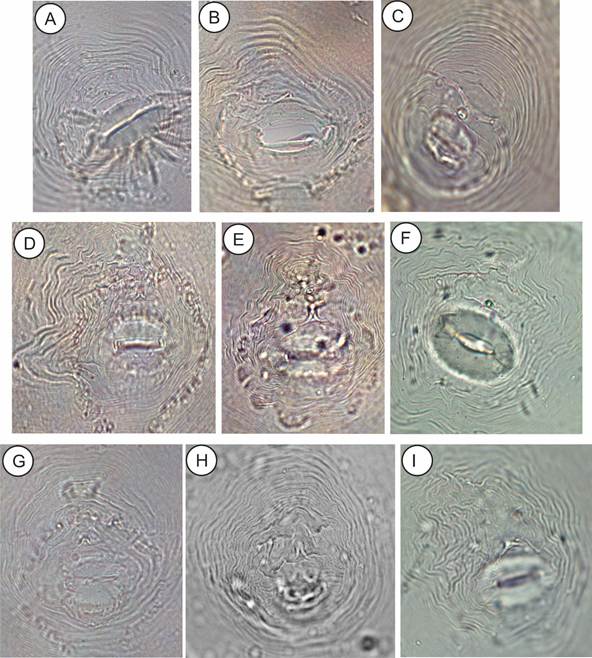
Figura 3 Patrón perineal de hembras de Meloidogyne spp. provenientes de cultivos agrícolas el Valle de Tepeaca, Puebla: A y B) patrón perineal de M. arenaria, C) Patrón perineal de M. enterolobii, D) Patrón perineal de M. hapla, E) Patrón perineal de M. incognita, F) Patrón perineal de M. chitwodii, G) patrón perineal de M. javanica, H) Patrón perineal de Meloidogyne sp. 1, I) Patrón perineal de Meloidogyne sp. 2.
Meloidogyne chitwoodi presentó el fenotipo S1 (Rm: 38.2) y fue encontrado en los cultivos de calabaza y betabel (Tabla 1) (Figs. 1, 2 F). El patrón perineal se caracterizó por ser redondeado a ovalado con arco dorsal bajo, con estrías rotas cerca del área perineal, curvadas, retorcidas, líneas del campo lateral débilmente visibles (Fig. 3F).
El fenotipo I1 (Rm: 43) correspondió a M. incognita y se encontró asociado a zanahoria (Tabla 1) (Figs. 1, 2E). El patrón perineal característico de la especie presentó arco dorsal alto y cuadrado formado por estrías lisas a onduladas; algunas estrías se bifurcan cerca de las líneas laterales, aunque no claramente visibles (Fig. 3E).
Meloidogyne enterolobii presentó el fenotipo VSI-SI (=En2) (Rm: 39.4, 45.4) en zanahoria (Tabla 1) (Figs. 1, 2C); el patrón perineal fue de forma ovalada, con arco dorsal alto a veces redondeado a cuadrado, con estrías finas muy espaciadas, campo lateral ausente o con una sola línea en la unión de los arcos dorsal y ventral (Fig. 3C).
Meloidogyne hapla presentó el fenotipo H1 (Rm: 46.8) y se encontró asociado a betabel y zanahoria (Tabla 1) (Figs. 1, 2D); el patrón perineal correspondiente con arco dorsal bajo, redondeado a aplanado, con estrías onduladas que forman una o dos alas; las estrías lisas a onduladas se observaron puntuaciones arriba del ano (Fig. 3D).
El fenotipo J2a (Rm: 40.3, 54.4), (Figs. 1) correspondiente a Meloidogyne javanica asociado al cultivo de betabel (Tabla 1), presentó un patrón perineal con arco dorsal bajo, ligeramente redondeado a aplanado, el rasgo característico de este patrón son las líneas laterales muy visibles que lo dividen en regiones dorsal y ventral (Fig. 3G).
Dos especies no se pudieron identificar provenientes del cultivo de cilantro y se les asignaron los fenotipos G1 (Rm: 10.1) y G1-VF1 (Rm: 10.1, 52.9); ambas correspondieron a especies no identificadas y se denominaron Meloidogyne sp. 1 y Meloidogyne sp. (Figs. 1, 2G) 2 (Tabla 1), estas hembras presentaron patrones perineales atípicos con arco dorsal alto, estrías onduladas, sin líneas del campo lateral visibles (Fig. 3H, I).
Fenotipos de malato deshidrogenasa (MDH)
Entre todas las poblaciones de Meloidogyne se observaron seis fenotipos diferentes y ocho bandas importantes de actividad para MDH (Fig. 1). El fenotipo designado como N1 (Rm: 20) correspondió a M. javanica y M. arenaria; ésta última también presentó el fenotipo atípico designado como N1e (Rm: 17.6). El N1a (Rm: 21) se asoció a M. chitwoodi, el N2a (Rm: 20, 21) a M. incognita y el H2 (Rm: 11.2, 16.8) a M. hapla. Además, en uno de los campos de zanahoria se encontró el fenotipo N1d (Rm: 14), el cual no pudo asociarse a alguna especie (Fig. 1) (Tabla 1).
Discusión
En calabaza se encontró a M. chitwoodi, misma que presentó los fenotipos S1:N1a para EST y MDH, respectivamente; lo que coincide con lo reportado por Esbenshade & Triantaphyllou, (1985) respecto a la caracterización enzimática de esta especie. Este fenotipo no es especie-específico, ya que también lo presenta M. plantani (Esbenshade & Triantaphyllou, 1985), por lo que se recurrió a la observación del patrón perineal para confirmar la identificación, dicho patrón presentó arco dorsal bajo y cuadrado, con estrías onduladas y sin líneas del campo lateral, como lo mencionan (Hunt & Handoo 2009; Hunt & Handoo 2012; Karssen et al., 2013), ello aunado a los antecedentes de la presencia de M. chitwoodii parasitando zanahoria en la zona de estudio (Montes-Belmont, 2000). Esta especie se ha encontrado asociada a papa (Solanum tuberosum L.), zanahoria, jitomate (Solanum lycopersicum L.), betabel (Beta vulgaris L.), girasol (Helianthus annuus L.), avena (Avena sativa L.) (Ferris et al., 1993; Cid del Prado-Vera et al., 2018), pero no en calabaza lo que representa un nuevo registro en la zona.
En betabel se identificó a M. javanica, M. hapla y M. chitwoodi. El hecho de que M. javanica se haya encontrado mezclada con M. hapla y M. chitwoodi, coincide con lo observado por otros investigadores (Brito et al., 2008). El fenotipo EST determinado en este estudio para M. javanica es J2a (atípico), el cual solo ha sido reportado en soya (Glycine max L.) en Brasil (Da Cunha et al., 2003; Machado et al., 2022) y en tabaco (Nicotiana tabacum L.) en Florida (Brito et al., 2008); los fenotipos de EST que comúnmente se han asociado a esta especie son el J2 y J3 (Carneiro et al., 1996; Cofcewicz et al., 2005; Molinari et al., 2005; Brito et al., 2008; Brito et al., 2010; Quénéhervé et al., 2011). A pesar de que M. javanica está ampliamente distribuida y tiene una amplia gama de hospedantes (Hunt & Handoo, 2009), el cultivo de betabel no ha sido reportado en México como hospedante y por ello este es el primer registro. Respecto a M. hapla, esta presentó el fenotipo H1 especie-específico, tal como se ha reportado en trabajos previos (Esbenshade & Triantaphyllou, 1985;Carneiro et al., 1996; Carneiro et al., 2000; Molinari, 2001; Brito et al., 2008), a pesar de que este fenotipo es especie-especifico en algunas ocasiones es necesario corroborar el fenotipo de otra enzima como la MDH, ya que puede haber diferencias en las movilidades electroforéticas debidas a las variaciones de la técnica y condiciones del laboratorio (Carneiro et al., 1996).
En el presente trabajo los fenotipos H1 de M. hapla encontrado en betabel y el fenotipo I1 encontrados en M. incognita en zanahoria presentaron una movilidad electroforética similar; cuando los fenotipos de EST son muy similares es necesario analizar el fenotipo MDH. El fenotipo H2 de MDH en cultivo de betabel confirma que la especie asociada a este cultivo es M. hapla; dicho fenotipo ha sido reportado por Carneiro et al. (1996) en poblaciones provenientes de jitomate, lechuga (Lactuca sativa L.), café (Coffea arabica L.) y kiwi (Actinidia deliciosa Liang). Además, el patrón perineal presentó arco dorsal bajo, redondeado, con estrías que forman una o dos alas laterales y puntuaciones arriba del ano lo cual lo reporta (Wesemael et al., 2024) como característico de esta especie.
De los dos campos de zanahoria infestados con Meloidogyne, en el primero, localidad El Cristo, municipio de Acatzingo, Puebla, se encontraron las especies M. incognita, M. enterolobii y M. hapla. Meloidogyne incognita mostró el fenotipo I1 de EST el cual es especie especifico, este fenotipo es el más común para M. incognita y ha sido reportado en países como: Brasil, Estados Unidos, Paraguay, Colombia (Carneiro et al., 1996; Molinari, 2001; Da Cunha et al., 2003; Carneiro et al., 2004; Molinari et al., 2005; Brito et al., 2008; Brito et al., 2010; Riascos et al., 2019; Resquín-Romero et al., 2023), además se determinó el fenotipo N2a de MDH el cual es poco común, ya que solo ha sido reportado en Florida asociado a una ornamental no identificada (Brito et al., 2010). La forma del patrón perineal presentó arco dorsal alto y cuadrado formado por estrías lisas a ondulada tal cual se reportan para M. incognita (Wesemael et al., 2024). Por lo que se confirma la especie usando tanto los fenotipos de EST, MDH y la forma del patrón perineal. Meloidogyne incognita es la especie más distribuida a nivel mundial, ya sea en forma individual o en mezcla con otras poblaciones (Trudgill et al., 2000), como en este caso. Es importante conocer cuando hay mezcla de especies porque se ha observado, que si éstas se reproducen por partenogénesis y bajo condiciones favorables del medio ambiente es factible la hibridación, dando lugar a nuevos fenotipos de MDH (Van Der Beek & Karssen, 1997).
Por su parte M. enterolobii mostró el fenotipo de EST VS1-S1 (= M2, = En2), el que ha sido reportado anteriormente en Brasil y es especie especifico (Carneiro et al., 2000; Souza et al., 2022), China (Xu et al., 2004), Florida (Brito et al., 2004), Martinica (Quénéhervé et al., 2011) y en Portugal (Santos et al., 2019). En cuanto a la MDH se encontró el fenotipo N1a, coincidente con M. enterolobii (Carneiro et al., 2000; Brito et al., 2004; Quénéhervé et al., 2011). Con lo que respecta a la morfología del patrón perineal mostró arco dorsal redondeado, con estrías finas espaciadas y campo lateral ausente distintivo de esta especie (Wesemael et al., 2024); sin embargo, Brito et al. (2004), así como Perichi & Crozzoli, (2010) comentan que existe variabilidad en estos patrones, los que pueden ser confundidos con M. incognita. En este estudio M. enterolobii se encontró asociada a zanahoria, lo cual constituye un nuevo registro en el Estado de Puebla, pues esta especie ya había sido identificada en zanahoria en el estado de Veracruz (Salinas-Castro et al., 2022). Esta especie aparece en el panorama mundial como polífaga parasitando ornamentales, arvenses y una gran variedad de plantas de cultivo, entre ellas jitomate, pimiento (Capsicum annuum var. annuum L), perejil (Petroselinum crispum Mill.), papa, col (Brassica oleracea var. esculenta L.), calabaza, zanahoria, brócoli (Brassica oleracea var. botrytis L.), apio (Apium graveolens L.), Cereus hildmannianus (Cactaceae), Lampranthus sp. (Aizoaceae), Physalis peruviana (Solanaceae) y Callistemon sp. (Myrtaceae) (Wang et al., 2004; Rodríguez et al., 2007; Moens et al., 2009; Santos et al., 2019); además, se ha encontrado a M. enterolobii en poblaciones concomitantes, conviviendo con M. incognita, M. arenaria y M. javanica (Rodríguez et al., 2007; Santos et al., 2019; Cid del Prado-Vera et al., 2018; Carrillo-Fasio et al., 2020) tal y como se observó en este estudio. Es importante resaltar: Xu et al. (2004) determinaron que esta especie es conespecífica con M. mayaguensis debido a que los marcadores moleculares IGS (espaciador intergénico largo), COII (Citocromo oxidasa II) e rRNA (RNA ribosomal) son idénticos para ambas especies, al igual que el fenotipo de esterasa; además, existe gran similitud en la gama de hospedantes y la morfología. Por tal motivo, Brito et al. (2008) mencionan que ambos nombres son sinónimos; sin embargo, se prefiere referir como M. enterolobii debido a que esta especie fue descrita primero (Yang & Eisenback, 1983). Esta especie ha sido considerada una de las más importantes por su amplia distribución geográfica, se ha detectado su presencia en África, Estados Unidos, Sudamérica, Centroamérica y Europa (Moens et al., 2009), en México M. enterolobii fue identificada por primera vez en sandía (Citrullus lanatus var. sunsugar) en el estado de Veracruz (Ramírez-Suárez et al., 2014). Esta especie actualmente ha sido reportada en el estado de Sinaloa en tomate (Solanum lycopersicum L.), en papa (Cid del Prado-Vera et al., 2018; Carrillo-Fasio et al., 2020; Rosas-Hernández et al., 2024) y en Veracruz parasitando zanahoria (Salinas-Castro et al., 2022) en estos casos la identificación se realizó a nivel morfométrico y molecular.
En el campo de zanahoria de la localidad de Santa María Aticpa, municipio de Acatzingo se identificó a M. arenaria, con los fenotipos de EST A1, A2a, A2b y A3, lo cual concuerda con Esbenshade & Triantaphyllou, (1985) ya que esta especie es la que presenta mayor variabilidad intraespecífica y se le ha designado seis fenotipos (Murata et al., 2023; Carneiro et al., 2024). Los fenotipos de EST más comunes son A2 y A3 y han sido reportados en Brasil y Argentina (Carneiro et al., 1996; Carneiro et al., 2000; Da Cunha et al., 2003; García & Sánchez-Puerta, 2012). El fenotipo de EST A1 es poco común y solo ha sido reportado por Esbenshade & Triantaphyllou, (1985) y por Cofcewicz et al. (2005) en un cultivo de banana (Musa paradisiaca L.). Además, se observaron dos fenotipos atípicos designados en este estudio como A2a y A2b, estos han sido reportados en poblaciones de M. arenaria en Japón provenientes de plantas de jitomate, taro, berenjena y soya (Murata et al., 2023). Para MDH se determinó el fenotipo N1, el cual ha sido ampliamente reportado para M. arenaria (Esbenshade & Triantaphyllou, 1985; Carneiro et al., 1996; Carneiro et al., 2000; Molinari, 2001; Carneiro et al., 2004; Cofcewicz et al., 2005; Brito et al., 2008; Brito et al., 2010; Quénéhervé et al., 2011) y también se observó un fenotipo atípico designado como N1e. A estos resultados se suma la morfología del patrón perineal, el cual fue redondeado con arco dorsal bajo, con hombreras en los costados característicos de la especie M. arenaria (Wesemael et al., 2024).
En cilantro se determinó la presencia de dos especies de Meloidogyne que no pudieron ser identificadas por este método, la primera con un fenotipo de EST designado como G1-VF1, el cual no coincide con alguno que haya sido reportado hasta el momento. La segunda especie mostró el fenotipo de EST designado como G1 (en este trabajo) el cual es de migración lenta, según lo reportado por Blok & Powers, (2009), el único fenotipo de EST de migración lenta reportado hasta el momento es Mg1 y corresponde a M. graminis. Este fenotipo de EST ha sido reportado en Stenotaphrum secundatum (planta arvense) (Brito et al., 2010), sorgo (Sorghum vulgare Pers.) y maíz (Zea mays) (Karssen, 2002; Perichi et al., 2006) y pastos de campo de golf (Azevedo de Oliveira et al., 2018). El cilantro no se encuentra dentro del grupo de las gramíneas, no ha sido reportado como un hospedante de M. graminis y además la morfología del patrón perineal obtenido no es característico de M. graminis, por lo que es necesario confirmar la identificación de la especie con técnicas moleculares en conjunto con la caracterización morfológica de hembras, machos y juveniles (Blok & Powers, 2009).
En la zona hortícola del Valle de Tepeaca, de donde proceden las muestras, se sabe de la presencia de M. chitwoodi (Montes-Belmont, 2000), M. hapla, M. arenaria (Medina-Canales et al., 2011) y M. incognita (Cid del Prado Vera et al., 2001), identificadas por caracteres morfológicos y morfométricos. La presencia de M. chitwoodi en calabaza y M. javanica en betabel en la zona constituyen nuevos registros en el país, mientras que Meloidogyne enterolobii en zanahoria es el primer registro en la zona. Lo que hace necesario tomar medidas para evitar su dispersión. Estos informes reafirman la importancia que tienen las especies emergentes como M. enterolobii, la cual cuenta con una amplia gama de hospedantes y es capaz de parasitar cultivos importantes que poseen el gen que les confiere resistencia a otras especies de Meloidogyne (Moens et al., 2009). Es de suma importancia conocer la distribución de estos nematodos en toda la zona y para ello es necesario llevar a cabo el diagnóstico integral, el cual implicaría el análisis morfológico, morfométrico, molecular y enzimático mediante el uso de fenotipos isoenzimáticos. Este método de identificación es poco usado en el país, a pesar de que en Europa es parte del protocolo para la identificación de algunas especies de Meloidogyne propuesto por la EPPO (2016), por lo que es necesario incluir este método como parte de la taxonomía integrativa y crear bases de datos de los perfiles de EST y MDH de especies de Meloidogyne presentes en México.
La identificación precisa y rápida de las especies del género Meloidogyne es de gran utilidad debido a que estos nematodos son los causantes de las mayores pérdidas en los cultivos, por lo que conocer la (s) especies presentes en una zona agrícola determinada permite poder implementar las estrategias adecuadas para llevar a cabo las prácticas para el manejo integrado de estos patógenos para cada cultivo (Sikora et al., 2022).
Conclusiones
Se identificaron a partir de los fenotipos isoenzimáticos de esterasa (EST), malato deshidrogenasa (MDH) y la morfología del patrón perineal seis especies de Meloidogyne en hortalizas provenientes de cuatro cultivos y cinco localidades muestreadas en el Valle de Tepeaca, Puebla; siendo de mayor importancia el hallazgo de M. enterolobii, M. chitwoodi y M. javanica, ya que representan nuevos registros para la zona de estudio, por lo que deben tomarse las medidas necesarias para evitar su dispersión.
Se encontraron los fenotipos de esterasa G1 y G1-VF1 los que no pudieron asociarse a ninguna especie, por lo que es necesario complementar la identificación con métodos moleculares, lo cual nos confirma la importancia de usar varias herramientas complementarias entre sí para realizar un diagnóstico certero.
En México, es importante establecer nuevos protocolos de diagnóstico que permitan la identificación precisa de las especies de Meloidogyne; dónde deben considerarse la determinación de los fenotipos isoenzimáticos a partir de una sola hembra, ya que es un método sensible, reproducible y confiable. Esto representa todo un reto para las autoridades fitosanitarias de nuestro país, pero los resultados serán favorables para el correcto manejo de las especies.











 nueva página del texto (beta)
nueva página del texto (beta)



