Introducción
El género Ardisia pertenece a la familia Primulaceae e incluye cerca de 500 especies, distribuidas en zonas tropicales y subtropicales del mundo (Kobayashi & De Mejía, 2005). Algunas especies poseen un enorme valor farmacológico, alimentario y medicinal, derivado del amplio contenido de metabolitos secundarios, como polifenoles, saponinas, quinonas, isocoumarinas, triterpenos y alquilfenoles (De Mejía & Ramírez-Mares, 2011; Tian-Liang et al., 2024). Se han identificado compuestos con diversa actividad biológica, como bergenina y norbergenina con actividad antiviral, antiinflamatorio, anticancerígeno, antidiabético y antiarrítmico (Bajracharya, 2015; Jouwa Tameye et al., 2020; Mehta et al., 2022); el ácido gálico, ardisinone, embelina y quercitrina con propiedades anticancerígenas (Deng et al., 2010; Newell et al., 2010) y kaempferol con actividad antioxidante y antimicrobiana (Chatatikun & Chiabchalard, 2017).
En el Sur de México, Ardisia compressa Kunth, se encuentra distribuida en áreas boscosas, en traspatios y en cultivos de cafeto (Martínez-Blanco et al., 2019). Los estudios sobre la actividad insecticida y antifúngica de los extractos de A. compressa con aplicación en la agricultura son limitados; sin embargo, se tiene antecedentes que otras especies del género Ardisia tienen actividad contra fitoparásitos. Por ejemplo, los extractos acuosos de hoja de A. crenata, A. japonica, A. standleyana y A. crispa, producen alta mortalidad en ninfas y huevos de B. tabaci y Trialeurodes vaporanariorum (Neal et al., 1998). El extracto metanólico de A. crenata es eficaz como disuasivo alimentario contra ninfas de Schistocerca americana (Drury) y adultos de Diaprepes abbreviatus L. (Sandoval-Mojica & Capinera, 2011). Los extractos vegetales de A. solanacea producen alto porcentaje de inhibición de alimentación contra Spilosoma obliqua (Al-Abd et al., 2017; Anjum et al., 2019), así como propiedades antifúngicas contra Trichophyton rubrum, Aspergillus fumigatus, Rhizoctonia solani y Fusarium oxysporum (Pournami & Pratap, 2021). En un estudio reciente, el extracto acuoso de A. compressa mostró actividad in vitro contra el agente causante de la roya del cafeto, Hemileia vastatrix, inhibiendo el desarrollo total de las urediniosporas (García-Pérez et al., 2021).
Las plagas y enfermedades de los cultivos son una gran limitante en la producción agrícola en todo el mundo. En este contexto, la cepa F. oxysporum y la mosquita blanca B. tabaci (Gennadius 1889) son dos especies de mayor importancia en la agricultura. La cepa F. oxysporum, afecta importantes cultivos básicos produciendo marchitamiento en varias especies como chile habanero, pimentón, tomate, plátanos, (Pérez-Acevedo et al., 2017; Colak Ates et al., 2019; Hernández-Amasifuen et al., 2019; Martínez-Solórzano et al., 2020;). Por su parte, B. tabaci es una especie ampliamente dañina, distribuida extensamente en regiones tropicales y subtropicales, que provoca serios daños a especies cultivadas de las familias Fabáceas, Cucurbitáceas, Solanáceas, entre otras, cuyo daño principal es la transmisión de una amplia gama de virus fitopatógenos (Navas-Castillo et al., 2011; Malka et al., 2021). Los extractos de A. compresa podrían representar una opción para control de plagas y enfermedades en la agricultura. El objetivo del presente trabajo fue determinar el efecto tóxico/repelente sobre B. tabaci y antifúngico contra F. oxysporum de los extractos etanólicos (EEs) de las hojas de A. compressa y determinar el perfil cromatográfico de los extractos mediante GC-MS.
Materiales y métodos
Recolección de plantas y obtención de extractos
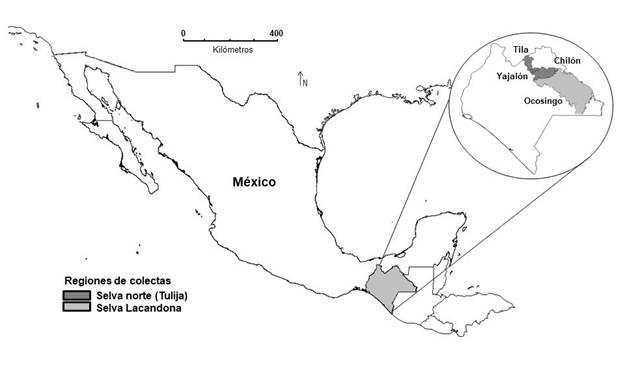
Las hojas de A. compressa se recolectaron de poblaciones silvestres/naturales en la zona Noreste del Estado de Chiapas, conocido como región Selva Lacandona y Selva Norte Tulijá, específicamente en los Municipios de Tila, Yajalón, Chilón y Ocosingo (Cuadro 1, Figura 1). Las hojas se deshidrataron a 45 °C por 10 días y se molieron con una licuadora (MAN mod. MLU-9090, México) hasta obtener polvo fino. Para la obtención de los extractos etanólicos (EEs) se siguió la metodología propuesta por Cruz-Estrada et al. (2013), con modificaciones. Se uso 50 g de material vegetal pulverizado y se agregó 500 mL de etanol (grado reactivo), se mantuvo en agitación constante durante 72 h a una temperatura de 25 ºC. Posteriormente se filtró en papel filtro Whatman no.1 para remover fragmentos del material vegetal. La muestra fue concentrada en un rotavapor (Yamato B0400.Yamato VR300, USA.) a presión con vacío constante. Los extractos crudos (material pastoso) obtenidos se mantuvieron en viales obscuros y almacenados en refrigeración a 4 °C hasta su uso.
Cuadro 1 Identificación de los extractos etanólicos obtenidos de hojas de A. compressa y ubicación de la localidad de recolecta de las poblaciones.Table 1. Ethanolic extracts identification obtained from leaves of A. compressa and location where the population was collected.
| Extracto | Localidad, Municipio | Altitud (msnm) |
Coordenadas |
|---|---|---|---|
| YRP | Río Pupiltillo, Yajalón | 500 | 17º 10' 14.00ʺ N, 92º 19' 49.00ʺ W |
| YBG | Banco de grava, Yajalón | 915 | 17º 10' 00.00ʺ N, 92º 19' 00.00ʺ W |
| CJC | Joybé carretera, Chilón | 972 | 17º 01' 07.00ʺ N, 92º 09' 19.66ʺ W |
| CJR | Joybé río, Chilón | 900 | 17° 01' 11.77ʺ N, 92° 09' 41.76ʺ W |
| CLC | Las Canchas, Chilón | 850 | 17° 00' 19.07ʺ N, 92º 06' 52.92ʺ W |
| CTia | Tiaquil , Chilón | 1141 | 17° 11' 99.00ʺ N, 92º 52' 58.61ʺ W |
| TCA | Coquijaz alto, Tila | 1800 | 17° 17' 05.40ʺ N, 92° 28' 46.20ʺ W |
| TCB | Coquijaz bajo, Tila | 1000 | 17° 12' 53.01ʺ N, 92° 22' 00.12ʺ W |
| TCC | Coquijaz centro, Tila | 1267 | 17º 17' 48.00ʺ N, 92º 25' 30.00ʺ W |
| OGV | Guadalupe Victoria, Ocosingo | 785 | 16° 59' 32.98ʺ N, 91° 55' 48.65ʺ W |
ID= identificador, msnm: metros sobre nivel del mar, YRP= Yajalón río Pupiltillo, YBG= Yajalón Banco de grava, CJC= Chilón Joybé carretera, CJR= Chilón Joybé río, CLC= Chilón Las Canchas, CTia= Chilón Tiaquil, TCA= Tila Coquijaz alto, TCB= Tila Coquijaz bajo, TCC= Tila Coquijaz centro, OGV= Ocosingo Guadalupe Victoria.
Bioensayo para evaluar el efecto tóxico sobre B. tabaco
Los ejemplares de B. tabaci Biotipo B se obtuvieron de una colonia establecida en 2022 (Herrera-Gorocica et al., 2023) en invernaderos del área de investigación hortícola del Instituto Tecnológico de Conkal, en Conkal, Yucatán (21º4’N, 89º31’W, 10). La colonia se ha mantenido en plantas de berenjena (Solanum melongena L.) establecidas en macetas de 10 L dentro del invernadero. Para los bioensayos, los extractos crudos se diluyeron en una solución de etanol y tween 80, a una relación de 1:1:1 (peso/volumen/volumen). Posteriormente esta mezcla fue diluida en agua destilada, para obtener la mezcla final de aplicación de EE al 0.2 % (peso/volumen), con una dilución final del disolvente (etanol y tween 80) de 0.5 % (volumen/volumen).
Plantas de tomate de 25 días de emergencia establecidas en macetas de 2 L, se ubicaron en la colonia de B. tabaci por dos semanas para lograr infestación. Las plantas infestadas fueron tratadas con los EEs, mediante la aplicación de las mezclas con atomizador manual, dirigiendo la aspersión al haz y envés de las hojas, hasta lograr punto de escurrimiento. Las evaluaciones de mortalidad de huevos y ninfas se realizaron a las 72 h después de la aplicación de los EEs. Para ello, se recolectó una hoja de cada planta tratada y se llevó al laboratorio para contabilizar los individuos muertos (huevos y ninfas) con ayuda de un microscopio estereoscopio (Motic, SMZ-161 SERIES), donde se observaron las hojas por el envés. Los huevos y ninfas necrosadas o con apariencia de desecación, se contabilizaron como individuos muertos (Herrera-Gorocica et al., 2023). Cada hoja representó una repetición. Se tuvieron 10 repeticiones por tratamiento. Se empleó un control negativo de etanol: tween 80 (1:1 volumen/volumen) diluido en agua a una concentración de 0.5% (volumen/volumen).
Todos los valores de mortalidad fueron corregidos por mortalidad natural utilizando la fórmula de Abbott (Abbott, 1925):
donde MC es la mortalidad corregida, Ts es el porcentaje de individuos sobrevivientes en el tratamiento (EEs) y Cs es el porcentaje de sobrevivientes en el control.
Bioensayo de repelencia y disuasión de la oviposición de B. tabaco
Plantas de tomate de 40 días de edad completamente sanas se trataron por el método de aspersión como se describió para el ensayo de actividad insecticida, siguiendo la metodología de Herrera-Gorocica et al. (2023). Después de la aplicación del tratamiento, las hojas se dejaron secar durante 30 min y se llevaron a un invernadero, donde las plantas tratadas con los EEs se colocaron en hileras alternas a una distancia de 40 cm de hileras de plantas de tomate infestadas con B. tabaci. La evaluación de repelencia y disuasión de la oviposición se realizó a los 2 y 5 días después de la aplicación de los EEs. Para tales efectos, se observaron dos hojas del tercio superior de cada planta para contar el número de adultos en el envés de las hojas. Estas hojas se cortaron y llevaron al laboratorio donde se observaron con un estereoscopio para determinar el número de huevos. El área foliar se calculó tomando una fotografía de la hoja y procesando con el software Image J. Una hoja representó una repetición. Se incluyeron 10 repeticiones para cada tratamiento.
El porcentaje de repelencia de adultos y disuasión de oviposición de B. tabaci se calculó mediante la fórmula:
Donde C y T correspondieron a los valores de número de individuos en el control y el tratamiento, respectivamente, por lo tanto, entre mayores sean los valores indican mayor repelencia (Akhtar et al., 2012).
Actividad in vitro de EEs de A. compressa contra F. oxysporum
Se empleó la cepa de F. oxysporum (GemBio acc. OM876888.1). Se cultivó en medio de cultivo PDA (Agar papa dextrosa, BD Bioxon). Para los bioensayos de inhibición de crecimiento micelial se siguió la metodología descrita por Carrillo-Morales et al. (2023), empleando concentraciones de 100 y 200 µg. mL-1 de cada EEs, mismos que se adicionaron al medio PDA aún en estado líquido (45 °C) y en proceso de solidificación. El medio PDA con EE se vertió en cajas Petri (1 cm x 10 cm). Las cajas Petri se conservaron en refrigeración hasta su uso. Posteriormente, un disco de 5 mm de diámetro con PDA con crecimiento micelial se colocó en el centro de las placas con PDA adicionadas con EEs y placas con PDA sin adición de EEs (control). Las cajas Petri se incubaron durante 96 h a 28 ºC y se midió el diámetro de la colonia fúngica con un vernier digital (INSIZE 1108-150). El ensayo se estableció por triplicado y se expresó en porcentaje de inhibición de crecimiento micelial comparado con el control, aplicando la fórmula:
Donde ICM es el porcentaje de inhibición de crecimiento micelial, Dt es el diámetro de la zona de crecimiento en las placas tratadas y Dc es el diámetro de la zona de crecimiento en la placa de control
Análisis del perfil cromatográfico de EEs de hojas de A. compressa por GC-MS
La identificación de los metabolitos secundarios de los EEs de A. compressa se realizó mediante la técnica de la cromatografía de gases acoplada a espectrometría de masas. Se empleó en un GC TRACE de la marca Thermo Scientific con un detector de masas con trampa de iones ITQ900 (Thermo Electron Corporation, Milán, Italia). El gas portador fue helio con un caudal de 1 mL/min. La columna utilizada fue TRACE-5MS (30 m, 0.25 µm de película y 0.25 mm de diámetro interno). El programa utilizado fue fullscan y se inició con una temperatura de 50 °C que se mantuvo durante 1 min., posteriormente, se aplicó una rampa de temperatura con incrementos de 7 °C/min hasta 300 °C. Los 300 °C se mantuvieron durante 5 min., la temperatura de la interfase fue de 280 °C y la temperatura de la masa fue de 200 °C.
Análisis de datos
Los datos fueron previamente transformados a función de coseno de raíz cuadrada para cumplir los supuestos de normalidad y homogeneidad de varianzas. Los datos transformados se analizaron mediante análisis de varianza (ANOVA) y comparación de medias con la prueba Tukey (P < 0.05) en el software estadístico Infostat versión 2018 para Windows (Di Rienzo et al., 2018). Para la discriminación de los extractos por su efecto biológico, se empleó la base de datos de compuestos mayoritarios y se analizó mediante análisis de mapas de calores y matriz de correlación de Pearson en el software RStudio para Windows versión 2023. 12.1+ 402.
Resultados
Efecto tóxico sobre estadíos inmaduros de B. tabaco
Los extractos etanólicos de A. compressa al 0.2% (p/v) mostraron efectos significativos (P < 0.05) en la mortalidad de huevos y ninfas de B. tabaci (Cuadro 2). En huevos, los extractos TCA y YRP causaron la mayor mortalidad, con valores de 98.1 y 99.1%, seguido de los extractos CTia, YBG y CLC que causaron entre 83.2 y 85.6% de mortalidad. El resto de los extractos etanólicos causaron entre 35.0 y 68.0% de mortalidad. En ninfas, los extractos TCA y CLC causaron mayor mortalidad, con valores de 94.7 y 97.4%, seguido de los extractos de TCB, YBG, YRP y TCC, con los valores de 83.9 a 93.9%. El resto de los extractos tuvieron efectos moderados a bajos, mismos que causaron mortalidad de ninfas entre 32.5 a 75.8% (Cuadro 2).
Cuadro 2 Efecto de los extractos etanólicos de A. compressa al 0.2% (p/v) sobre estadios inmaduros y adultos de B. tabaci a las 48 h posterior a la aplicación.Table 2. Effect of ethanolic extracts of A. compressa at 0.2% (w/v) on immature and adult stages of B. tabaci 48 h after application.
| Extractos | % Mortalidad | % Repelencia de adultos |
% Disuasión de oviposición |
|
|---|---|---|---|---|
| Huevos | Ninfas | |||
| CJC | 52.1 ± 12.0 bc | 50.6 ± 12.8 ab | 24.9 ± 7.1 ab | 28.2 ± 10.1 a |
| CJR | 46.2 ± 9.7 c | 32.5 ± 10.6 b | 11.0 ± 5.0 ab | 16.8 ± 7.7 a |
| CLC | 85.6 ± 3.8 ab | 94.7 ± 3.2 a | 28.9 ± 7.7 ab | 5.7 ± 4.2 a |
| CTia | 83.2 ± 3.9 ab | 75.8 ± 12.6 ab | 30.2 ± 9.9 ab | 10.4 ± 7.8 a |
| TCA | 98.1 ± 1.9 a | 97.4 ± 2.6 a | 38.3 ± 9.6 a | 22.0 ± 8.5 a |
| TCB | 67.9 ± 7.6 bc | 83.9 ± 10.1 a | 19.6 ± 7.9 ab | 8.9 ± 6.0 a |
| TCC | 55.6 ± 12.7 bc | 93.9 ± 2.8 a | 16,2 ± 4.9 ab | 25.7 ± 10.9 a |
| YRP | 99.1 ± 0.9 a | 91.5 ± 4.2 a | 19.2 ± 0.4 ab | 11.5 ± 6.6 a |
| YBG | 84.8 ± 4.5 ab | 85.5 ± 3.3 a | 1.1 ± 1.1 b | 10.8 ± 6.5 a |
| OGV | 34.9 ± 5.0 c | 49.2 ± 22.4 ab | 23.8 ± 10.2 ab | 17.5 ± 10.8 a |
| P < 0.01 | P < 0.01 | P < 0.01 | P = 0.29 | |
| F = 9.50 | F= 4.87 | F = 2.58 | F = 1.22 | |
| gl = 69 | gl = 49 | gl = 99 | gl = 99 | |
CJC= Chilón Joybé carretera, CJR= Chilón Joybé río, CLC= Chilón Las Canchas, CTia= Chilón Tiaquil, TCA= Tila Coquijaz alto, TCB= Tila Coquijaz bajo, TCC= Tila Coquijaz centro, YRP= Yajalón río Pupiltillo, YBG= Yajalón Banco de grava, OGV= Ocosingo Guadalupe Victoria. Medias con diferente literal en cada columna indican diferencia estadística significativa P < 0.05, Tukey ± error estándar
Repelencia en adultos y disuasión de la oviposición
Los extractos etanólicos de A. compressa causaron efectos significativos (P < 0.05) en la repelencia de adultos, pero no en la disuasión de oviposición (Cuadro 2). Para la repelencia de adultos, el extracto TCA tuvo mayor efecto (38.3 % repelencia), seguido de CTia (30.2 % repelencia). Para la disuasión de oviposición, los extractos CJC y TCC tuvieron mayor efecto (28.1 y 26.0% disuasión de oviposición), seguido del extracto TCA (22.0% disuasión de oviposición). El resto de los extractos causaron entre 5.7 a 16.8% disuasión de oviposición (Cuadro 2).
Inhibición de crecimiento micelial en F. oxysporum.
Los extractos etanólicos de A. compressa tuvieron efectos significativos (P < 0.05) en el crecimiento micelial de F. oxysporum. En ambas concentraciones, 100 y 200 µg.mL-1, el extracto CJC causó la mayor inhibición de crecimiento micelial (75.4 y 79.2%), seguido de los extractos TCB, TCC, YRP, YBG y OGV (48.4 a 55.3%). Los extractos CJR, CLC, CTia y TCA tuvieron muy bajos efectos (menor a 13.0%) en la inhibición de crecimiento micelial (Cuadro 3).
Cuadro 3 Porcentaje de inhibición del crecimiento micelial de F. oxysporum a las 96 h de exposición con Table 3. Percent inhibition of mycelial growth of F. oxysporum at 96 h of exposure with ethanolic extracts of leaves of A. compressa.
| Extracto | % Inhibición de crecimiento micelial | |
|---|---|---|
| (100 µg.mL-1) | (200 µg.mL-1) | |
| CJC | 75.41 ± 1.6 a | 79.17 ± 1.6 a |
| CJR | 9.42 ± 4.3 c | 11.51 ± 4.6 c |
| CLC | 12.46 ± 6.9 c | 5.35 ± 3.6 c |
| CTia | 3.50 ± 2.8 c | 10.76 ± 5.9 c |
| TCA | 3.45 ± 2.5 c | 5.45 ± 4.1 c |
| TCB | 51.83 ± 4.3 b | 51.63 ± 2.2 b |
| TCC | 51.64 ± 4.5 b | 53.50 ± 2.5 b |
| YRP | 49.62 ± 3.2 b | 55.33 ± 2.3 b |
| YBG | 48.35 ± 3.9 b | 54.55 ± 3.5 b |
| OGV | 52.42 ± 2.6 b | 53.57 ± 2.9 b |
| P≤ 0.0001 | P≤ 0.0001 | |
| F= 43.5 | F= 57.9 | |
| gl = 50 | gl = 50 | |
Medias con diferente literal en cada columna indican diferencia estadística significativa P < 0.05, test Tukey ± error estándar.
Perfil cromatográfico de los EEs de A. compressa por GC-MS
Los análisis por GC-MS de los EEs de A. compresa, obtenido de las diferentes localidades, se muestran en el Cuadro 4. En general, se identificaron un total de 36 constituyentes, entre los que destacan: seis ácidos carboxílicos, un alcano alifático, una cetona cíclica, un anhídrido, tres fenoles, nueve compuestos terpénicos (dos diterpenos, cuatro sesquiterpenos, tres triterpenos), diez ésteres de ácidos carboxílicos, una lactona, un ftalato y tres fitoesteroles. La abundancia de compuestos mayoritarios se determinó según el porcentaje relativo del compuesto en relación con las áreas totales de todos los compuestos presentes en el extracto (Cuadro 4).
Cuadro 4 Compuestos identificados por GC-MS en EE de hojas de A. compressa.Table 4. Compounds identified by GC-MS in EE of leaves of A. compressa.
| No. | Familia / Compuesto | TR(min) | FQ | PM | Extracto etanólico (% área) |
|---|---|---|---|---|---|
| Ácidos carboxílicos | |||||
| 1 | Ácido tetradecanoico. | 15.2 | C14H28O2 | 228.37 | TCA (1.8) |
| 2 | Ácido n-hexadecanoico. | 16.7 | C16H32O2 | 256.42 | CJC (11.55), CLC (11), TCA (14), OGV (21.3), YRP (22.8), YBG (23.5) |
| 3 | Ácido oleico. | 18.1 | C18H34O2 | 282.46 | YRP (7.7), YBG (9.5) |
| 4 | Ácido 9Z,12Z,15Z- octadecatrienoico. | 18.5 | C18H30O2 | 278.43 | CJC (10.5), CLC (4.5), TCA (13.4), OGV (13.3), CTia (21.3) |
| 5 | Ácido cis-10-nonadecenoico. | 20.4 | C19H36O2 | 296.49 | CTia (3.5), TCB (5.2) |
| 6 | Ácido octadecanoico. | 19.4 | C18H36O2 | 284.48 | CJC (2.9), CLC (2.2), TCA (2), TCB (14), CTia (2) |
| Alifático | |||||
| 7 | 3-etil-5-(2-etilbutil)- octadecano. | 22.1 | C26H54 | 366.71 | CJC (3.8) |
| Cetona cíclica | |||||
| 8 | 6-metilenbiciclo[3.2.0]hept-3-en-2-ona. | 8.6 | C8H8O | 120.15 | TCA (1.6) |
| Anhidridos | |||||
| 9 | Anhídrido cis-aconítico. | 6.7 | C6H4O5 | 156.09 | CLC (1.7) |
| Fenoles | |||||
| 10 | Trans 6-(p-tolil)-2-metil-2-heptenol. | 13.8 | C15H22O | 218.33 | CTia (1.9), YBG (6.7) |
| 11 | Catecol. | 8.6 | C6H6O2 | 110.11 | CJC (4.5), CLC (13.4), TCA (3.7), TCB (1.5) |
| 12 | 1,2,3-Bencenetriol. | 11 | C6H6O3 | 126.11 | CJC (3.7), CLC (12.9), TCA (5.3), TCB (1.9) |
| Diterpenos | |||||
| 13 | Neofitadieno. | 15.9 | C20H38 | 278.52 | CJC (1.7), TCB (1.6) |
| 14 | Fitol. | 17.8 | C20H40O | 296.53 | CJC (2.3), CLC (8.8), CTia (3.8), TCA (2.8), TCB (3.6), YRP (2.7), YBG (7.4), OGV (15.2) |
| Sesquiterpenos | |||||
| 15 | 8S, 13-Cedran-diol. | 14.7 | C15H26O2 | 238.37 | YRP (3.6) |
| 16 | 4,4,8-trimetilticiclo[6.3.1.0(1,5)] dodecano- 2,9- diol. | 15.6 | C15H26O2 | 238.37 | YRP (2.9) |
| 17 | Epóxido cis-Z-α-bisaboleno. | 14.9 | C15H24O | 220.35 | YRP (4.2) |
| 18 | 1-(1,5-dimethyl-4-hexenyl)-4- metil-benceno. | 11.2 | C15H22 | 202.33 | YBG (3.3) |
| Triterpenos | |||||
| 19 | Escualeno. | 24.6 | C30H50 | 410.72 | CJC (4.5), TCA (1.8), CLC (3.0) |
| 20 | α-Amirina. | 28.2 | C30H50O | 426.72 | CJC (6.8), TCA (6.7), TCB (6.8), CTia (5.4) |
| 21 | β-Amirina. | 28.5 | C30H50O | 426.7 | CJC (11.4), TCA (13.9), TCB (11) |
| Ésteres de ácidos carboxílicos | |||||
| 22 | Éster dimetílico del ácido [1,1':2',1''-terfenil]-3',4'-dicarboxílico, 5 ',6'-difenil. | 5.5 | C34H26O4 | 498.6 | CJR (1.8) |
| 23 | Éster metílico del ácido [1,1'-biciclopropil]-2-octanoico, 2'-hexil. | 18.3 | C21H38O2 | 322.5 | YRP (2.8) |
| 24 | Éster etílico del ácido octadecanoico. | 18.6 | C20H40O2 | 312.53 | OGV (2.2) |
| 25 | Éster etílico del ácido 9,12-octadecadienoico. | 18.7 | C20H36O2 | 308.5 | TCB (15.1), YBG (3.8) |
| 26 | Ester etílico del ácido hexadecanoico 2-hidroxi-1- (hidroximetil). | 22.5 | C19H38O4 | 330.5 | CJC (1.8), CTia (2.1) |
| 27 | Éster 2,3-dihidroxipropíl del ácido 9Z,12Z- octadecadienoico. | 23.3 | C21H38O4 | 354.5 | TCB (1.9) |
| 28 | Éster etílico 2-hidroxi-1-(hidroximetil) del ácido 9Z-octadecenoico. | 23.8 | C21H40O4 | 356.5 | CTia (4.4) |
| 29 | Éster etílico del ácido hexadecanoico. | 16.8 | C18H36O2 | 284.48 | CJC (2), YRP (7.5), YBG (11.6), OGV (8.4) |
| 30 | Éster etílico del ácido (E)-9-Octadecenoico. | 18.3 | C20H38O2 | 310.51 | YRP (4.3), YBG (7.2), OGV (8.5) |
| 31 | Compuesto x. | 5.4 | C34H44ClN5O2 | 590.2 | TCC (1.3) |
| Lactona | |||||
| 32 | (Z)-18-Octadec-9-enolida. | 18.8 | C18H32O2 | 280.45 | CJC (6.7) |
| Ftalato | |||||
| 33 | Ftalato de bis (2-etilhexil). | 21.5 | C24H38O4 | 390.6 | YRP (23.9), YBG (23.3), OGV (21.3) |
| Fitoesteroles | |||||
| 34 | γ-Tocoferol. | 25.7 | C28H48O2 | 416.68 | CJC (1.7) |
| 35 | Vitamina E. | 26.4 | C29H50O2 | 430.71 | CJC(2), TCA (2.2), TCB (1.7), CTia (2.2) |
| 36 | Estigmasterol. | 28.1 | C29H48O | 412.69 | CJC (1.8), CLC (8.7), TCA (2.8), TCB (1.8), CTia (1.5) |
TR= tiempo de retención, FQ= fórmula química, PM= peso molecular. Compuesto X= éster terc-butílico de [5-(5-Cloro-3,4-dimetil-1H-pirrol-2-ilmetilen)-,4-dimetil-5H-pirrol-2-il]-[5-(5-ciano-4, 4, 5-trimetil-4, 5-dihidro-3H-pirrol-2-ilmetileno)-4,4-dimetilpirrolidin-2-ilen]-ácido acético.
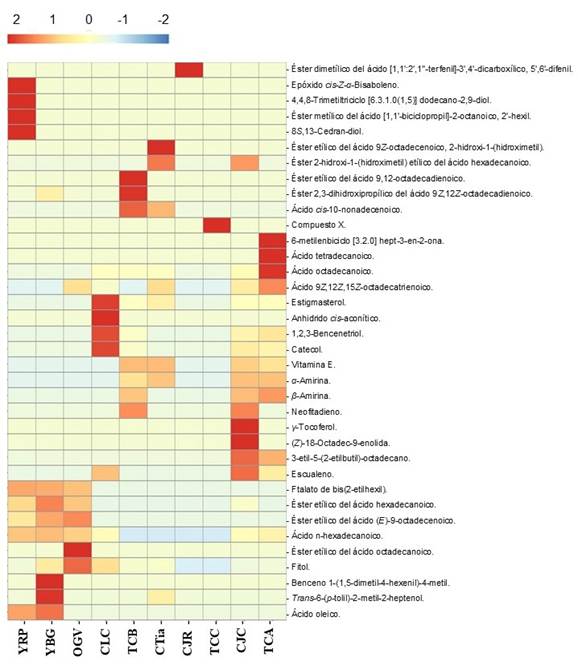
La distribución de 36 compuestos determinados por GC-MS varió entre extractos (Figura 2). El extracto YRP mostró mayor concentración de los compuestos epóxido de cis-Z-α-Bisaboleno; 8S,13-cedran diol; éster metílico del ácido [1,1'-biciclopropil]-2-octanoico, 2'-hexil y 4,4,8-trimetiltriciclo [6.3.1.0(1,5)] dodecano-2,9-diol. El extracto YBG tuvo altas concentraciones de trans-6-(p-tolil)-2-metil-2-heptenol; benceno 1-(1,5-dimetil-4-hexenil)-4-metil, seguido de ácido oleico y éster etílico del ácido hexadecanoico. El extracto OGV tuvo altas concentraciones de éster etílico del ácido octadecanoico seguido de fitol. El extracto CJC tuvo como compuestos mayoritarios a γ-Tocoferol y (Z)-18-Octadec-9-enolida, seguidos de escualeno y 3-etil-5-(2-etilbutil)-octadecano. Similarmente en el extracto TCA se encontró como compuestos mayoritarios el ácido tetradecanoico; 6-Metilenebicyclo [3.2.0] hept-3-en-2-ona; ácido octadecanoico, seguido del ácido 9Z,12Z,15Z-octadecatrienoico. El extracto CLC mostró como compuestos mayoritarios al estigmasterol y anhídrido cis-aconítico, seguidos de 1,2,3-bencenetriol y catecol. En el extracto CJR, el compuesto más abundante fue éster dimetílico del ácido [1,1':2',1''-terfenil]-3',4'-dicarboxilico, 5',6'-difenil. El extracto TCC tuvo como compuesto mayoritario al éster terc-butílico de [5-(5-Cloro-3,4-dimetil-1H-pirrol-2-ilmetilen)-,4-dimetil-5H-pirrol-2-il]-[5-(5-ciano-4,4,5-trimetil-4,5-dihidro-3H-pirrol-2-ilmetileno)- 4, 4-dimetilpirrolidin-2-ilen]-ácido acético. El extracto CTia tuvo como compuestos mayoritarios al éster etílico 2-hidroxi-1-(hidroximetil) del ácido 9Z-octadecenoico y éster etílico del ácido hexadecanoico 2-hidroxi-1-(hidroximetil). En el extracto TCB los compuestos mayoritarios fueron éster etílico del ácido 9,12-octadecadienoico; 2,3-dihidroxipropil éster del ácido 9Z,12Z-octadecadienoico y el ácido cis-10-nonadecenoico (Figura 2).
Compuesto X= éster terc-butílico de [5-(5-Cloro-3,4-dimetil-1H-pirrol-2-ilmetilen)- ,4-dimetil-5H-pirrol-2-il] - [5-(5-ciano-4,4, 5-trimetil-4,5-dihidro-3H-pirrol-2-ilmetileno)-4,4-dimetilpirrolidin-2-ilen]-ácido acético.
Figura 2 Mapa de calor del análisis de clúster jerárquico de metabolitos diferenciados por GC-MS en los EEs de A. compressa, los porcentajes relativos de las concentraciones con tres replicas se muestran en colores que van del rojo (alta concentración) al azul (baja concentración).
Análisis de correlación entre actividad biológica y perfil cromatográfico
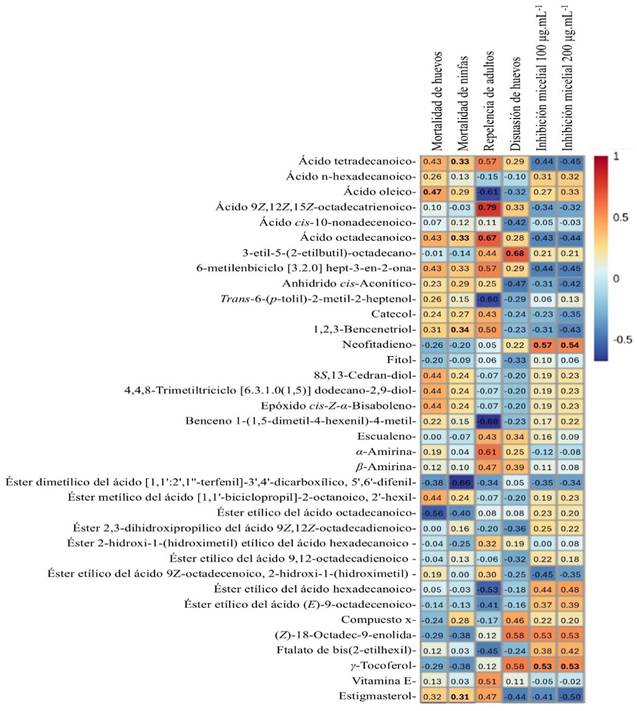
Se determinó la correlación entre la actividad biológica y la abundancia relativa de compuestos en los extractos (Figura 3), con variación de coloración azul a rojo, ubicando las correlaciones positivas como aquellas donde la mayor abundancia de los compuestos produjo mayor efecto. Para el caso de la mortalidad de B. tabaci, se observó que la mayor mortalidad de huevos y ninfas estuvo asociada a la alta abundancia de ácido oleico y 1,2,3-bencenetriol en los EEs, respectivamente. Se observó correlación positiva entre la repelencia de adultos y la abundancia del ácido 9Z-12Z-15Z-octadecanotrienoico y el ácido octadecanoico, en la disuasión de oviposición la correlación fue con el compuesto de 3-etil-5-(2-etilbutil)-octadecano. El mayor porcentaje de ICM en F. oxysporum se observó correlacionado con altas concentraciones del compuesto neofitadieno en los EEs.
Compuesto X= éster terc-butílico de [5-(5-Cloro-3,4-dimetil-1H-pirrol-2-ilmetilen)- ,4-dimetil-5H-pirrol-2-il] - [5-(5-ciano-4,4, 5-trimetil-4,5-dihidro-3H-pirrol-2-ilmetileno)-4,4-dimetilpirrolidin-2-ilen]-ácido acético.
Figure 3. Correlation heat map between the compounds of 10 ethanolic extracts of A. compressa leaves and the biological activity against B. tabaci and F. oxysporum, using Pearson's distance method and the value of the coefficient.
Figura 3 Mapa de calor de correlación entre los compuestos de 10 extractos etanólicos de hojas de A. compressa y la actividad biológica contra B. tabaci y F. oxysporum, con empleo del método de distancias de Pearson y el valor del coeficiente.
Discusión
En la actualidad el uso de derivados vegetales para manejo de plagas y fitopatógenos en la agricultura es un área que ha adquirido enorme relevancia, principalmente por la ventaja de este tipo de productos sobre los agroquímicos convencionales, que incluye una fácil degradación biológica y menor riesgo de resistencia en la plaga. En el presente estudio se observó que los extractos etanólicos (EEs) de hojas provenientes de diferentes poblaciones de A. compressa presentaron efectos tóxicos y repelentes sobre B. tabaci, y actividad antifúngica contra F. oxysporum.
De manera general la actividad de los EEs de TCA y YBG causaron alta mortalidad (> 95%) de huevos, mientras que los EEs de CLC, TCA, TCC y YRP ocasionaron alta mortalidad (> 90%) en ninfas de B. tabaci. Estos efectos son considerados altos, como se ha reportado en literatura con EEs al 0.2% de otras especies. Por ejemplo, los EEs de hojas de Eugenia winzerlingii causaron alrededor 90 a 100 % de mortalidad en huevos y ninfas de B. tabaci (Cruz-Estrada et al., 2013, 2019b). Con respecto al potencial de A. compressa como fuente de extracto para el manejo de plagas. Se considera que algunas poblaciones pueden ser consideradas de alta eficiencia para el control de B. tabaci. Otras especies de Ardisia, como A. crenata y A. japonica también han mostrado alta efectividad insecticida, se ha documentado efectos antialimentarios de los extractos de A. solanacea ((Anjum et al., 2019). Es importante mencionar que, si bien varios EEs de A. compressa causaron alta mortalidad en inmaduros de B. tabaci, su efecto en la repelencia de adultos (< 40%) y disuasión de oviposición (< 30%) fue muy bajo, lo cual indica que los metabolitos contenidos en los extractos tienen principalmente efectos tóxicos letales. Es probable que los EEs contengan metabolitos repelentes en concentraciones muy bajas, lo que pudo afectar su efectividad en la evaluación.
Los EEs de A. compressa (100 y 200 µg mL-1) también tuvieron efectos moderados (50-80 %) en la inhibición de crecimiento micelial de F. oxysporum. El EE más activo (CJC) causó entre 75-80% de inhibición de crecimiento micelial (ICM). En literatura sólo existe un reporte de evaluación antifúngica de extractos acuosos de A. compressa, que muestra inhibición de 83% de germinación de esporas de Hemilia vastatrix (García-Pérez et al., 2021). En otros estudios sobre evaluación de extractos orgánicos, en concentraciones de 100 y 200 µg mL-1, se ha observado alta efectividad en la inhibición de crecimiento micelial, como los extractos metanólicos de hojas y tallo de Vitex mollis contra F. verticillioides que produjeron valores hasta de 90% la ICM (Valencia-Botin et al., 2018). Así también el extracto hexánico de Syzygium aromaticum causó más del 90% de ICM en Fusarium spp. Los extractos etanólicos de Mosannona depressa(corteza de tallo y raíz), Parathesis cubana(raíz) y Piper neesianum (hojas) causaron 100% de ICM en F. equisetiy F. oxysporum (Cruz-Cerino et al., 2020). Tomando como base los resultados de estos estudios, se observa que los EEs de A. compressa tienen efectos moderados en F. oxysporum.
En el análisis GC-MS mostró que los grupos de compuestos más comunes fueron los ácidos grasos, fenoles, anhídridos, diterpenos, triterpenos, sesquiterpenos, ésteres de ácidos grasos, ftalatos y fitoesteroles. Esto concuerda con los análisis fitoquímicos previos de hojas de otras especies de Ardisia. Por ejemplo, Wong et al. (2021), aislaron compuestos fenólicos en el extracto hidro-etanol de A. elliptica al 50 y 70% (v/v). Yeong et al. (2014), reportaron una mezcla isomérica de α y β-amirina (triterpenos) y 2-metoxi-6-undecil-1,4-benzoquinona (quinona) del extracto hexánico de la raíz de A. crispa. Schindler et al. (2021), identificaron flavonoides (flavonoles and flavan-3-ol), catequina, epigalocatequina e isoquercetina de los extractos metanólicos de hojas de A. crenata. Ma et al. (2022), identificaron saponinas triterpenoides de extractos metanólicos de A. japonica. Syed et al. (2013), reportaron la presencia de alcaloides, taninos, flavonoides, saponinas, gomas y carbohidratos, esteroides, terpenoides del extracto etanólico de A. colorata (corteza y hojas). Derivado de estos estudios y los análisis del presente trabajo, es claro que el género Ardisia contiene metabolitos terpenoides, flavonoides, saponinas y esteroides.
En este estudio se determinó la correlación entre la actividad biológica y la presencia de ciertos metabolitos mayoritarios. Para el caso de B. tabaci, los efectos más altos se tuvieron al aplicar el extracto TCA, donde el análisis de GC-MS mostró la existencia de compuestos mayoritarios como el ácido tetradecanoico; 6-metileno biciclo [3.2.0] hept-3-en-2-ona; ácido octadecanoico; el ácido 9Z,12Z,15Z-octadecatrienoico; α-amirina; β-amirina; fitol; 1,2,3-benzenetriol; catecol; 3-etil-5-(2-etilbutil)-octadecano; escualeno, vitamina E y estigmasterol. Mientras que para la inhibición del crecimiento micelial de F. oxysporum el extracto que mostró mayor actividad fue CJC, que mostró como componentes mayoritarios a γ-tocoferol; α-amirina; β-amirina; (Z)-18-octadec-9-enólido; escualeno; 3-etil-5-(2-etilbutil)-octadecano; neofitadieno; 1,2,3-benzenetriol; ácido n-hexadecanoico; ácido 9Z,12Z,15Z-octadecatrienoico; ácido octadecanoico, ácido hexadecanoico; etíl éster del ácido hexadecanoico; etíl éster 2-hidroxi-1-(hidroximetil); catecol; fitol; vitamina E y estigmasterol.
Al analizar la presencia de metabolitos mayoritarios en los extractos y su relación con el nivel de actividad, en los mapas de calor se observó que la mortalidad de huevos se correlacionó con alta abundancia del ácido oleico. Se ha observado que el ácido oleico tiene propiedades insecticidas y funciona como protector de cultivos contra plagas, como se ha descrito en otros estudios. Por ejemplo, posee función protectora contra larvas de Spodoptera frugiperda (Ramos-López et al., 2012). Incluso, el ácido oleico y otros ácidos grasos son letales contra varias especies de insectos fitófagos. Se ha demostrado el efecto de los ácidos grasos contra insectos puede variar dependiendo de su estructura y longitud (Cruz Estrada et al., 2019a). En tanto, la mortalidad de ninfas fue correlacionada con la abundancia del compuesto 1,2,3-benzenetriol (pirogalol), dicho compuesto ha sido reportado con buena capacidad insecticida. Por su parte, la actividad de repelencia de adultos de B. tabaci, se asoció al contenido de ácidos grasos como el ácido 9Z-12Z-15Z-octadecanotrienoico y ácido octadecanoico; mientras que la disuasión de oviposición se correlacionó con el contenido de 3-etil-5-(2-etilbutil)- octadecano. Estos dos metabolitos no han sido reportados con efectos contra alguna especie de plaga. En general, se ha documentado que los compuestos alifáticos de cadenas largas y ácidos grasos poseen acción biológica debido a la capacidad de incorporarse a la membrana celular y generar mayor fragilidad para causar desintegración de la pared celular (Jangir et al., 2020). Con respecto a la actividad antifúngica, el análisis de mapa de calor mostró correlación positiva entre la actividad biológica y el contenido de neofitadieno y α-amirina y β-amirina. Estudios sobre la actividad antifúngica de compuestos naturales, han demostrado que el neofitadieno puede actuar en sinergia con otros compuestos, principalmente ácidos grasos para ejercer su efecto antifúngico (Dikhoba et al., 2019; Ramírez-López et al., 2023). También se sabe que los metabolitos triterpénicos (α-amirin y β-amirina) actúan como agentes antifúngicos contra varias especies de cepas filamentosas (Dikhoba et al., 2019). Diversas investigaciones señalan que estos compuestos poseen la habilidad de modificar la permeabilidad de la membrana, ocasionando liberación de cationes al citoplasma y originando degradación en la membrana celular en varias especies de hongos (Leite et al., 2014; J. H. Wong et al., 2019). En consecuencia, la inhibición de crecimiento fúngico podría ser el resultado de la acción sinérgica de las sustancias presentes en el extracto. Además, otros compuestos como el catecol y el fitol fueron identificados en el extracto CJC y de acuerdo con, Cruz Vázquez et al. (2019), el catecol tiene la capacidad de actuar como pro-oxidantes causando daños moleculares en el ADN y las proteínas. Asimismo, se ha informado que el constituyente fitoquímico fitol tiene actividad antifúngica, debido a la producción excesiva de especies reactivas de oxigeno que genera daño al ADN y desequilibrio en la membrana mitocondrial, lo que resulta en apoptosis celular (Agus, 2020).
Es importante notar que los compuestos encontrados en los EEs de A. compressa, sugieren que el amplio rango de metabolitos y su abundancia en A. compressa depende del sitio de procedencia del material vegetal, pues los factores ambientales contribuyen en la síntesis y acumulación de metabolitos secundarios en el follaje de las plantas (Vázquez-León et al., 2017; Gomes et al., 2019; Li et al., 2020; Ma et al., 2022). Varios de los grupos de metabolitos mencionados en la literatura, indican que esta especie posee alto potencial para el manejo de B. tabaci, principalmente por su efecto tóxico letal contra inmaduros.
Conclusiones
Los EEs de las hojas de A. compresa poseen importantes efectos contra B. tabaci, particularmente resalta su actividad tóxica letal contra estados inmaduros de esta especie plaga. La actividad antifúngica contra F. oxysporum, sin embargo, fue moderada. El análisis del perfil cromatográfico basado en GC-MS permitió la identificación de metabolitos potenciales en hojas de A. compresa y su correlación con la bioactividad, donde se destacaron los ácidos grasos y ésteres de ácidos grasos, como compuestos abundantes. La bioprospección de A. compresa como especie abundante del Sur de México enriquece el conocimiento de las fuentes de productos botánicos para el control de plagas en la agricultura.











 nueva página del texto (beta)
nueva página del texto (beta)