Introducción
Las neurociencias representan una disciplina intrínsecamente cuantitativa y multidisciplinaria, integra conocimientos provenientes de medicina, fisiología, física, matemáticas, química, fisicoquímica, farmacología, computación, electrónica e instrumentación, entre otros dominios. Esta amalgama de campos es esencial para abordar su complejidad inherente y maximizar su aplicabilidad traslacional, resaltando la necesidad de enfoques interdisciplinarios para la investigación (Hernández-Carrillo et al., 2018). El incremento exponencial en la producción científica, impulsado por avances tecnológicos, ha generado la demanda de una especialización cada vez más refinada en recursos humanos dentro del ámbito neurocientífico (Akil et al., 2016; Goldman & Fee, 2017). A nivel global, se proyecta un progreso continuado en esta disciplina durante los próximos cincuenta años, con implicaciones significativas en áreas como medicina, educación, consumo y sistema judicial (Altimus et al., 2020).
En el contexto mexicano, el robusto crecimiento de la neurociencia ha propiciado la adopción de técnicas de vanguardia en varios centros de investigación. Esta evolución ha generado nuevas exigencias en la formación de estudiantes para acceder a este campo científico y alcanzar resultados óptimos (Oprisan, 2022). En respuesta a este desafío, la Facultad de Medicina de la Universidad Nacional Autónoma de México (UNAM) creó la Licenciatura en Neurociencias en 2016 (García et al., 2019).
La formación en neurociencias abarca diversos perfiles. En el contexto de la investigación básica, se requiere el dominio de conceptos y técnicas especializadas, donde las prácticas de laboratorio desempeñan un papel crucial (Horrigan, 2018). Sin embargo, estas actividades experimentales conllevan considerables costos, incluyendo el uso de animales de experimentación, reactivos y equipamiento especializado. Ante este panorama, varios países exploran alternativas para la enseñanza de la medicina y las neurociencias, incluyendo el desarrollo de programas computacionales. Por ejemplo, en Europa, el proyecto European CompBioMed (https://www.compbiomed.eu/) sobresale por su potencial para reducir la dependencia de animales en la educación. En la India, actualmente se realiza el proyecto VirtualLab (Diwakar et al., 2014). En México, se han desarrollado simuladores específicamente orientados a la enseñanza en neurociencias y biofísica (Reyes-Monreal et al., 2022).
Los simuladores ofrecen grandes oportunidades para profesores y alumnos puesto que permiten reproducir experimentos reales (Av-Ron et al., 2008). Desde un enfoque educativo, los simuladores para las neurociencias se pueden clasificar en tres (Lorenz & Egelhaaf, 2008):
Enfoque de simulación científica. En este enfoque los simuladores son desarrollados con la participación de los alumnos. Durante su construcción se replica paso a paso el flujo del trabajo científico. Se trata de un desarrollo típico de la neurociencia computacional. Del lado de la investigación se encuentra: la hipótesis, el diseño, los experimentos, la evaluación, y se regresa a la hipótesis. Del lado del desarrollo de la simulación se encuentran: el modelo, la implementación, la simulación, la evaluación, y se regresa al modelo. Estos son procesos conjuntos destinados a pocos alumnos debido a que hacen experimentos y simuladores durante su formación. Los alumnos requieren una formación en neurociencias, y además una formación en computación y programación. El tipo de conocimiento adquirido es procedimental e intuitivo.
Enfoque de simulación precompilado. El aprendizaje se inicia con simuladores precompilados desarrollados previamente. Los alumnos exploran directamente una simulación y evalúan los datos obtenidos. Aquí se omite la parte del diseño y desarrollo del simulador. Está dirigido a alumnos sin una formación profunda en programación o en matemáticas aplicadas. Sin embargo, se requiere de un tiempo de aprendizaje para manejar el simulador que generalmente rebasa el límite de tiempo de un curso ordinario. En esta clasificación se encuentran simuladores que son verdaderos lenguajes de programación para las neurociencias, tal es el caso de GENESIS (Bower et al., 1995) y NEURON (Carnevale & Hines, 2006), entre otros. Estos simuladores son ampliamente valorados en la investigación científica más que en la enseñanza-aprendizaje.
Enfoque de simulación educativa. Se trata de unidades de simulación de aprendizaje que pueden ser autónomos o guiados. Cuentan con lecciones para introducir al alumno en el tema. Los simuladores fueron desarrollados previamente, y los alumnos no requieren conocimientos especializados de computación, programación o matemáticas. En los simuladores para escritorio basta con el manejo básico de ambientes como Windows, Linux, iOS, internet, etc. Estos simuladores abarcan un tema específico de las neurociencias. No se pretende, en ningún momento, cubrir toda la temática de las neurociencias o agotar el tema en particular. La selección del tema está asociado a la importancia neurocientífica y clínica que pueda tener.
El presente trabajo presenta un simulador con un enfoque de simulación educativa destinado a la enseñanza-aprendizaje de la recuperación de la desensibilización de neuronas de corteza displásica de pacientes con epilepsia refractaria.
Epilepsia por displasia cortical (CD)
Con el objetivo de interesar a los alumnos en la enseñanza-aprendizaje del proceso de recuperación de la desensibilización del receptor NMDA, se simularon los experimentos electrofisiológicos de neuronas de corteza displásica humana. La epilepsia es objeto de atención en la sociedad debido a la impresión que causan los episodios epilépticos en los observadores. Los niños afectados por epilepsia a menudo enfrentan la marginación en su vida cotidiana, lo que repercute en aspectos sociales, educativos y cognitivos. Entre el 10% y el 20% de estos niños presentan epilepsias que son refractarios al tratamiento convencional (Aneja & Jain, 2014). Dentro del espectro de la epilepsia infantil se incluye la epilepsia causada por displasia cortical (CD) focal (Mohsin et al., 2023). Esta condición se caracteriza por malformaciones en el desarrollo cortical debido a alteraciones en la migración celular, así como en la morfología y tamaño de las neuronas (Cepeda et al., 2003, 2006). Histológicamente, la corteza displásica exhibe células piramidales gigantes (citomegálicas), células inmaduras, células dismórficas y células en globo o balón (Crino, 2015).
La CD se subclasifica en varios tipos según la presencia de diferentes tipos de células: (1) Tipo I, difícil de detectar, asociada con anomalías en la arquitectura de la corteza cerebral; (2) Tipo II, subdividido en: Tipo IIa, caracterizado por neuronas dismórficas y citomegálicas, pero sin células en globo, y Tipo IIb, con la presencia de los tres tipos de células; y (3) Tipo III, con cuatro subtipos dependientes de cambios patológicos adyacentes (Crino, 2015; Mohsin et al., 2023). En casos de epilepsia gravemente incapacitante, la cirugía se recomienda para mejorar la calidad de vida del paciente al reducir o prevenir convulsiones. En niños, se sugiere realizar la cirugía a una edad temprana para mejorar aspectos cognitivos y conductuales (Herta & Dorfer, 2019). Los estudios citológicos, moleculares y electrofisiológicos en neuronas de corteza displásica extraídas durante la cirugía se han llevado a cabo gracias al consentimiento informado de los familiares. Además, los avances tecnológicos permiten una mejor selección de las células CD estudiadas, mediante el uso de videomicroscopía infrarroja y óptica Nomarski.
Las investigaciones electrofisiológicas en neuronas de pacientes con displasia cortical infantil pretenden identificar daños en estructuras celulares o moleculares (como receptores o canales iónicos) y proponer hipótesis sobre los mecanismos asociados a la epilepsia. Investigaciones relevantes en este campo incluyen las realizadas por Cepeda et al. (2003, 2006, 2007), así como las de André et al. (2004). Son poco frecuentes los estudios electrofisiológicos en neuronas de corteza displásica de humanos puesto que es difícil contar con pacientes con este padecimiento. Además, realizar este tipo de experimentos con propósitos educativos es incosteable y muy difícil. Una alternativa es el uso de simuladores (Gerstner et al., 2012), ya que son una herramienta excelente para los procesos de enseñanza-aprendizaje debido a que reproducen adecuadamente algunas de las funciones neuronales (Fan & Markram, 2019; McDougal et al., 2016).
El objetivo de este trabajo es desarrollar un simulador para la enseñanza-aprendizaje del proceso de recuperación de la desensibilización en neuronas de corteza displásica.
Materiales y métodos
Se ha concebido y desarrollado un simulador interactivo destinado al estudio de la recuperación de la desensibilización del receptor NMDA en neuronas de corteza displásica y no displásica. Los datos experimentales sobre las corrientes NMDA, fundamentales para la implementación del simulador, se extrajeron del estudio realizado por André et al. (2004). Los registros electrofisiológicos utilizados proceden de neuronas de humano obtenidas de tejido no displásico (aparentemente normal) y con displasia cortical.
El diseño del simulador implicó el ajuste de los datos experimentales con ecuaciones matemáticas utilizando el programa de cómputo Origin-Pro 6.0, mediante el algoritmo de Levenberg-Marquardt. Se mantuvo la terminología utilizada por Origin para las ecuaciones ajustadas, garantizando la coherencia en la nomenclatura y facilitando la utilización del simulador.
Simuladores de la recuperación de la desensibilización en NO-CD aparentemente normal, CD-aparentemente normal y CD-citomegálica
El receptor NMDA forma un canal iónico que se abre al unirse con glutamato o con su agonista N-metil-D-aspartato (NMDA), al mismo tiempo con glicina como coactivador. En una solución con una concentración de glicina fija, el receptor se activa con un estímulo de NMDA. El protocolo para el estudio de la recuperación de la desensibilización consiste en la aplicación de MNDA (100 µM) por dos segundos en dos ocasiones seguidas separadas por un intervalo de 0 ms a 1500 ms, con pasos de 250 ms. El primer estímulo provoca la desensibilización del receptor, y el segundo estímulo está destinado a generar la recuperación de la desensibilización.
El primer estímulo evoca una corriente NMDA que llega a un valor máximo denominado corriente pico (Ip), e inmediatamente esta corriente disminuye de manera exponencial hasta alcanzar un valor que se mantiene en el tiempo denominado corriente en estado estable (Iss). A esta disminución de la corriente se le llama desensibilización. Para este trabajo, los valores de corriente pico y de estado estacionario se miden en los registros experimentales y deben ser igualados en las simulaciones. Para el estudio del proceso de recuperación de la desensibilización se aplica un segundo estímulo de NMDA, separado del primero por un intervalo. Con este segundo estímulo, el valor pico de la corriente se va recuperando cada vez que se incrementa el intervalo entre los dos estímulos. Cada trazo de recuperación tiene su corriente pico (Ip) y su corriente en estado estable (Iss).
La corriente macroscópica NMDA se generó con la ecuación 1 (Reyes-Monreal et al., 2024):
donde INMDA es la corriente NMDA,
B(V, Mg2+) es la función de activación, [Mg2*] es la concentración externa de magnesio, V es el voltaje y 3.57 mM y 16.13 mV son parámetros de ajuste de datos de las curvas experimentales (Jahr & Stevens, 1990a, 1990b).
Para el segundo estímulo, se ajustaron los datos experimentales
donde RD es recuperación de la desensibilización, y0 y A1 son parámetros, tr es el tiempo de recuperación y τr es la constante de tiempo de recuperación.
Replicación de la desensibilización del receptor NMDA
Después de un estímulo con NMDA, la corriente evocada alcanza un máximo
Implementación del simulador
El simulador se desarrolló en HTML5 y JavaScript con el objetivo de ser ejecutado en el ambiente de internet en las versiones más recientes de los navegadores. Su interfaz incluye un título del simulador, un menú de navegación, una sección para la introducción de datos, botones para la ejecución de simulaciones, un osciloscopio y un apartado destinado a la presentación de material didáctico (Figura 1).
Resultados
Se desarrolló un simulador que reproduce el proceso de recuperación de la desensibilización en tres tipos de neuronas: neuronas no displásicas aparentemente normales (NO-CD), neuronas de la corteza cerebral displásica de apariencia normal (CD-aparentemente normales) y neuronas displásicas citomegálicas (CD-citomegálicas). La base de este simulador se encuentra en los experimentos realizados por André et al. (André et al., 2004), específicamente en la Figura 4 de dicho estudio. Todos los resultados generados en las simulaciones están comparados con los resultados experimentales de estos autores.
Fuente: Elaboración propia con base en el trabajo de André et al. (2004).
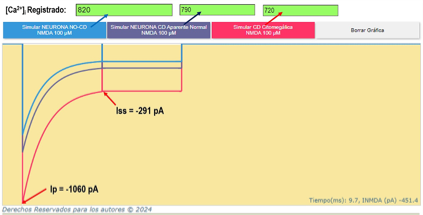
Figura 2 Simulaciones de corrientes NMDA ante un estímulo de NMDA. Cada tipo de neurona exhibe amplitudes pico de corriente NMDA y niveles de desensibilización distintos. La neurona citomegálica (trazo rojo) muestra una mayor amplitud de corriente, pero una menor desensibilización (34%), lo cual concuerda con la concentración de calcio interno calculada (720 nM). Las flechas indican la corriente pico (Ip) y la corriente en estado estable (Iss), representadas de manera equivalente en todos los trazos (azul claro para la neurona normal; azul oscuro para la neurona CD-aparentemente normal). El nivel de Iss se mantiene durante el registro. Las flechas en los botones de simulación señalan la concentración de calcio interno calculada en la simulación correspondiente.
Fuente: Elaboración propia con base en el trabajo de André et al. (2004).
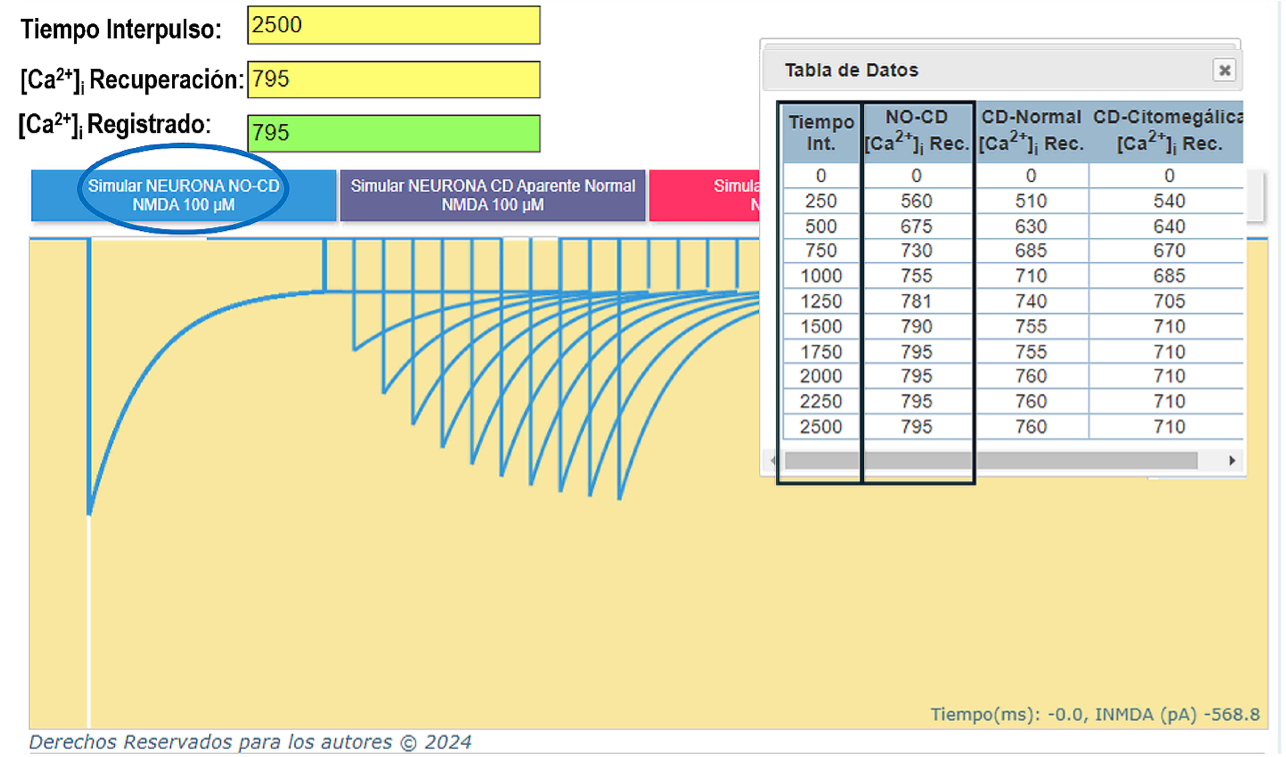
Figura 3 Simulación de la recuperación de desensibilización en neurona NO-CD. Se observa cómo el simulador reproduce los registros experimentales reportados. Las amplitudes máximas en cada trazo de recuperación aumentan de forma exponencial. La recuperación de la desensibilización es gradual y dependiente del tiempo interpulso y de la concentración de Ca2+ interno. Los trazos de recuperación nunca regresan a 0, se mantienen (Iss = -108 pA).
Fuente: Elaboración propia con base en el trabajo de André et al. (2004).
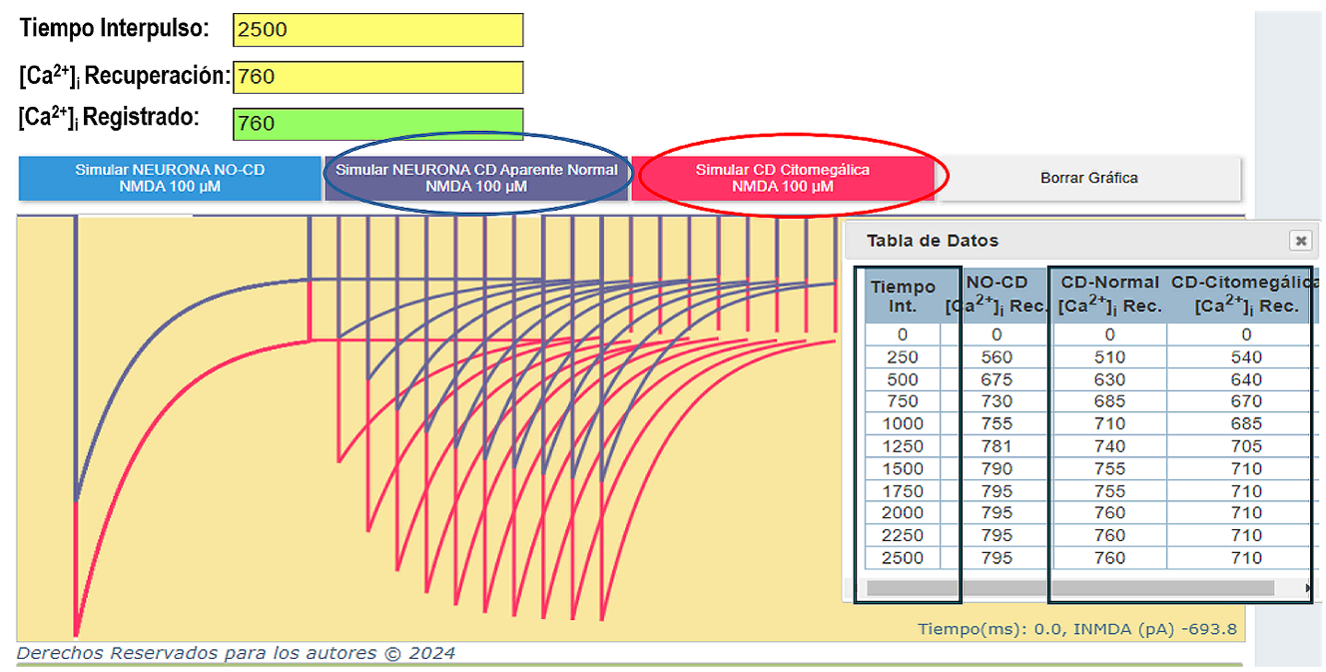
Figura 4 Simulaciones superpuestas de neuronas en tejido displásico. En azul se muestra el proceso de recuperación de la desensibilización en neuronas CD-aparentemente normales y en rojo se muestra el proceso de recuperación de la desensibilización en neuronas citomegálicas. La Tabla muestra las concentraciones de Ca2+ interno necesarias para cada caso. La recuperación de la desensibilización en las neuronas citomegálicas es más rápida. Los trazos de recuperación en ambas neuronas se mantienen. Iss = -153 pA y Iss = -291 pA, para la neurona CD-aparentemente normal y CD-citomegálicas, respectivamente.
La desensibilización se considera un proceso que previene los daños derivados de una concentración excesiva de calcio intracelular (Iacobucci & Popescu, 2017; Szydlowska & Tymianski, 2010). Según lo definido electrofisiológicamente, la desensibilización opera como una disminución gradual del pico de la corriente macroscópica NMDA (Vyklický, 1993). Se han identificado dos tipos de desensibilización: uno atribuido a la disminución en la afinidad de la glicina y otro relacionado con la dependencia de la concentración de calcio interno ([Ca2+]i) (Sibarov & Antonov, 2018).
La apertura del canal NMDA incrementa la concentración de calcio intracelular, lo que facilita su unión con calmodulina. El complejo calcio-calmodulina interactúa con el carbono terminal de la subunidad 1 del receptor NMDA (NMDAR1, también llamado NR1), modificando la estructura del canal y disminuyendo la corriente NMDA (Sibarov & Antonov, 2018). Con el primer estímulo, cada tipo de neurona simulada exhibe una amplitud de corriente NMDA diferente en respuesta al mismo estímulo (100 µM de NMDA).
La Figura 2 muestra tres simulaciones superpuestas correspondientes a un estímulo de NMDA aplicado a una neurona NO-CD aparentemente normal, una CD-aparentemente normal y una citomegálica (trazos azul claro, azul oscuro y rojo, respectivamente). La neurona citomegálica alcanza la mayor amplitud pico (~ -1060 pA), seguida de la CD-aparentemente normal (~ -680 pA) y la neurona NO-CD (~ -571 pA). A pesar de la mayor amplitud en las neuronas citomegálicas, los cálculos de concentración de calcio derivados de la ecuación 1 muestran una menor afluencia de calcio (720 nM, 790 nM y 820 nM, para las neuronas citomegálicas, CD-aparentemente normales y NO-CD, respectivamente). Estas concentraciones reflejan el grado de desensibilización alcanzado en cada tipo de neurona (en el mismo orden): 34%, 42.5% y 43%.
Estos resultados respaldan las conclusiones de André et al. (André et al., 2004) respecto a que la densidad o conductancia por unidad de área es menor en las neuronas citomegálicas. Este hallazgo sugiere que, a pesar de su mayor tamaño, las neuronas citomegálicas no presentan un mayor número de canales NMDA. Después de la desensibilización inducida por el primer estímulo, el registro permanece en el nivel de la corriente en estado estable (Iss), sin retornar a valores de 0 pA (Figura 2). Los valores en el estado estacionario fueron: Iss (pA) = -108, -153, -291, para las neuronas NO-CD, CD-aparentemente normales y CD-citomegálicas, respectivamente (Figura 2).
Proceso de recuperación de la desensibilización en neuronas NO-CD
El primer estímulo genera una corriente NMDA que desensibiliza. Con el segundo estímulo se produce la recuperación de la desensibilización. A medida que se incrementa el intervalo interpulso (incrementos de 250 ms), se produce una corriente Ip que aumenta gradualmente, y el receptor se va recuperando de la desensibilización para estar disponible nuevamente. Cada una de estas corrientes de recuperación presenta una Iss. Para que el simulador iguale los valores experimentales de la corriente en estado estable (Iss) de cada trazo de recuperación, se incrementó la concentración de [Ca2+]i. Las concentraciones de Ca2+ interno se recopilaron en una tabla que incluye los tiempos interpulso. Los valores de la tabla permiten al usuario ingresar rápidamente los datos correspondientes en las casillas amarillas para que el simulador reproduzca los trazos experimentales (Figura 3). Se puede observar que en la recuperación de la desensibilización, para que se alcance el estado estable en cada trazo, las concentraciones de calcio interno se fueron incrementando. En la neurona NO-CD normal, a partir del tiempo de 1750 ms, la concentración de [Ca2+]i se mantiene en 795 nM.
Recuperación de desensibilización en neuronas CD-aparentemente normales y CD-citomegálicas
Se llevó a cabo la simulación del proceso de recuperación en las neuronas CD-aparentemente normales y CD-citomegálicas. En la Figura 4 se presentan simulaciones superpuestas de estas dos clases de neuronas. Los trazos en azul corresponden a la neurona CD-aparentemente normal; los rojos corresponden a las CD-citomegálicas. Se destaca la amplitud de la corriente NMDA alcanzada en las neuronas citomegálicas, así como el rápido inicio del proceso de recuperación en comparación con las neuronas CD de apariencia normal. La corriente NMDA experimenta un rápido incremento hasta alcanzar un máximo de recuperación del 92.6% para las CD-aparentemente normales y del 96% para las citomegálicas; ambos tipos de neuronas logran recuperarse. Sin embargo, la velocidad de recuperación es mayor en las citomegálicas (0.15 pA/ms) en comparación con las de apariencia normal (0.12 pA/ms), lo que hace que las citomegálicas estén disponibles más rápidamente. En contraste, la cinética de recuperación entre las neuronas NO-CD y las CD-aparentemente normales es similar (Figura 5).
Fuente: Elaboración propia con base en el trabajo de André et al. (2004).
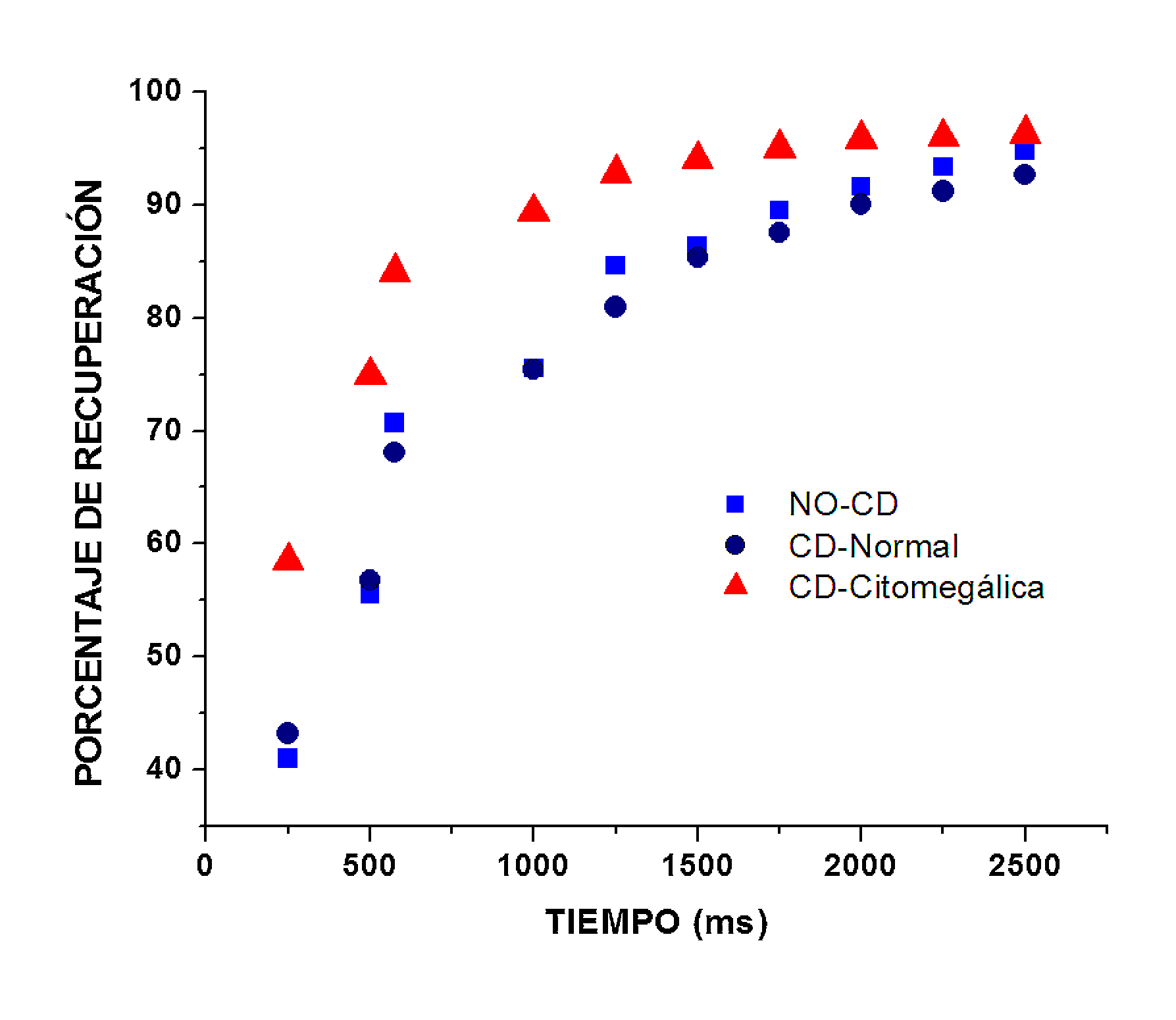
Figura 5 Porcentaje de recuperación como una función del intervalo interpulso. Los datos fueron calculados a partir de las simulaciones respectivas. Las neuronas citomegálicas (triángulos rojos) muestran una mayor recuperación inicial en comparación con las neuronas CD de apariencia normal (círculos azules) y las NO-CD (cuadrados azules). Esta representación gráfica, obtenida de las simulaciones, guarda similitud con la información experimental reportada por André et al. (2004).
Concentraciones de calcio interno
Para que el segundo estímulo reproduzca las corrientes experimentales, fue necesario incrementar la concentración de [Ca2+]i conforme se aumenta el intervalo interpulso. Este fenómeno ocurre en todos los tipos de neuronas simuladas. En las citomegálicas, la concentración de calcio interno fue menor en comparación con las otras neuronas (Figura 6). Esto sugiere que, a pesar de que las neuronas citomegálicas tienen un mayor tamaño comparadas con las otras neuronas de estudio, la densidad de canales en su membrana no aumentó, lo que coincide con las conclusiones de André et al. (2004).
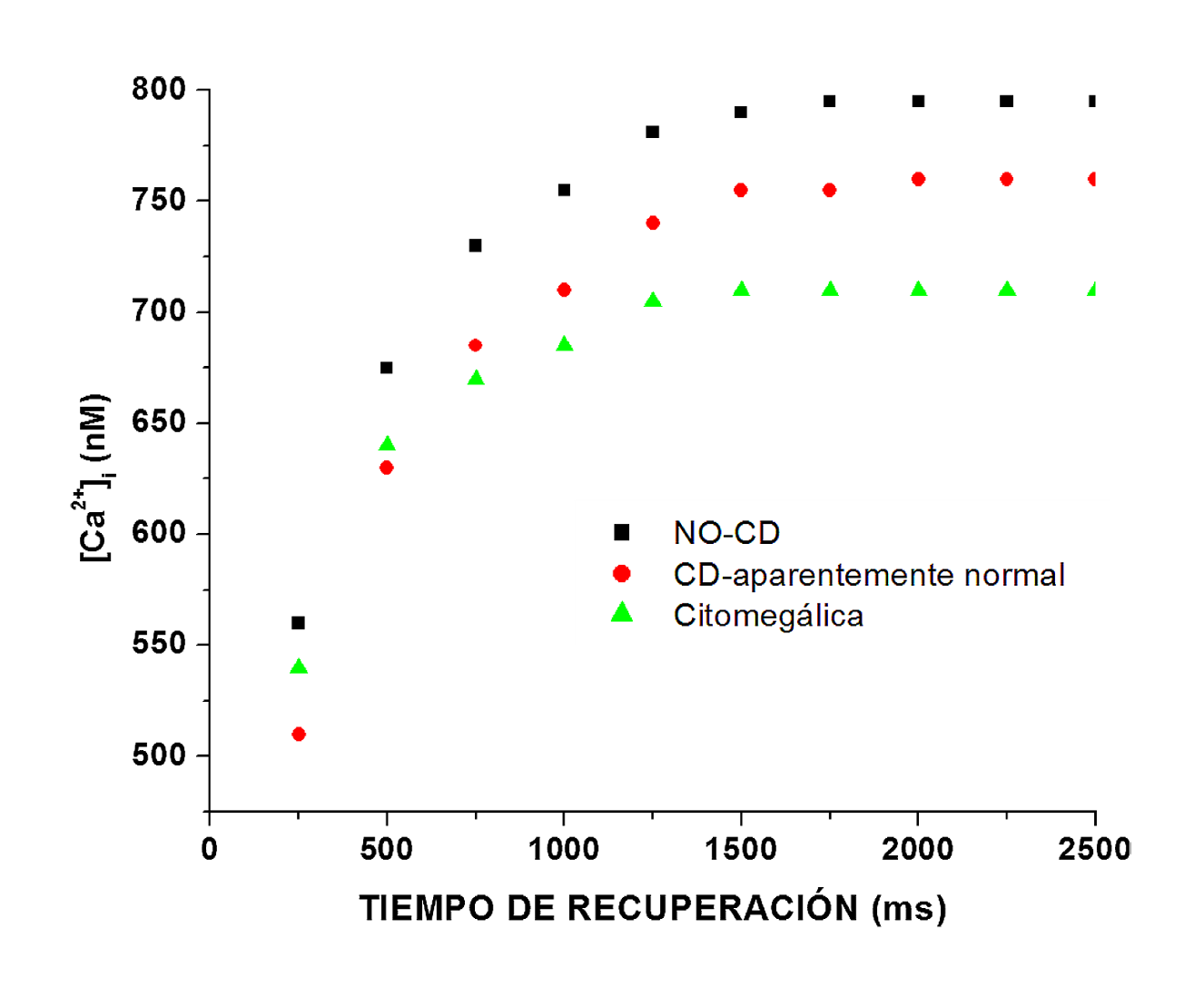
Fuente: Elaboración propia.
Figura 6 Concentración de Ca2+ interno necesario para reproducir la cinética de recuperación de la desensibilización en cada tipo de neurona simulada. Se observa que la concentración de Ca2+ interno concuerda con la amplitud de las corrientes. Una menor concentración de Ca2+ interno en las citomegálicas determina su menor nivel de desensibilización.
Lecciones
En el marco de un simulador con fines de enseñanza-aprendizaje, se integró un conjunto de lecciones que introduce al alumno en el tema. Está compuesto de cuatro lecciones que se pueden acceder en el orden que desee el usuario: Histología de la corteza cerebral normal y CD, Estructura del receptor NMDA, Electrofisiología básica del receptor NMDA y Condiciones experimentales para la recuperación de la desensibilización (Figura 7).
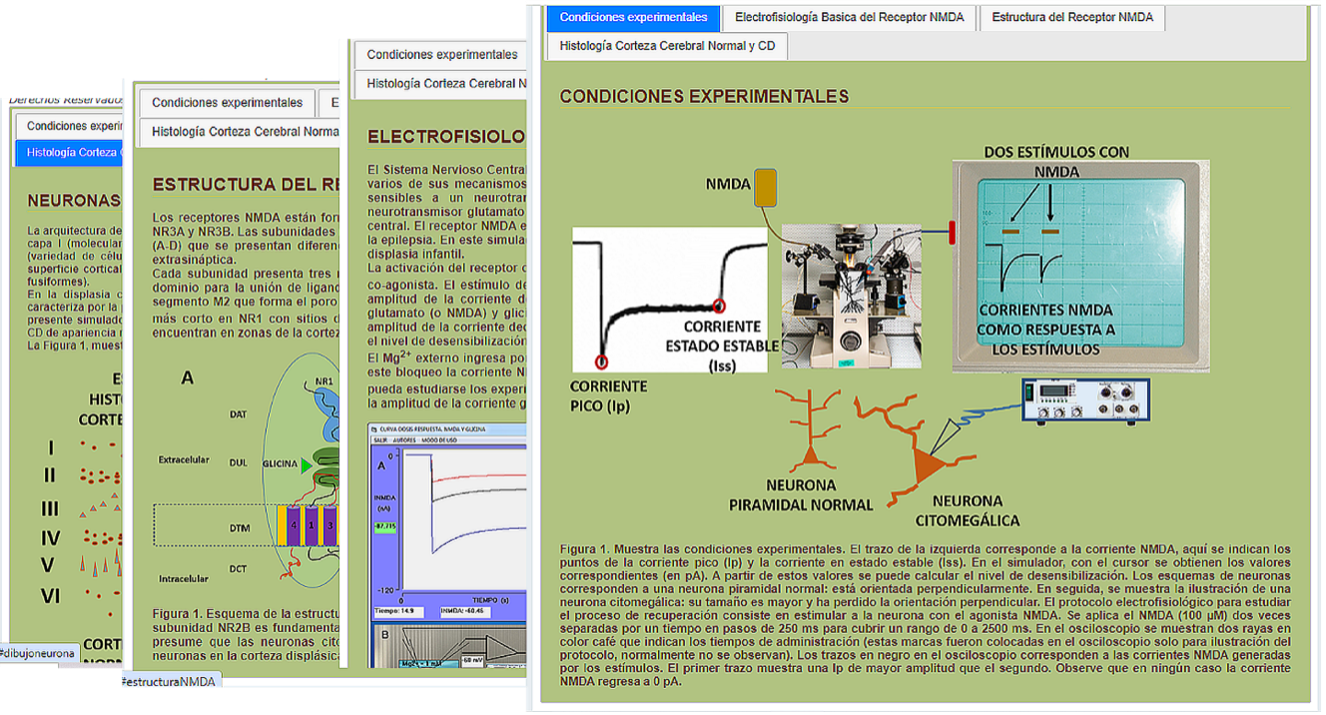
Fuente: Elaboración propia.
Figura 7 Lecciones sobrepuestas. Se muestran las cuatro lecciones sobrepuestas elaboradas para introducir al alumno en el tema. Cada lección orienta al alumno en el uso del simulador, las condiciones experimentales reales, la electrofisiología del receptor NMDA (esta lección presenta una liga a otro artículo relacionado con un simulador para este propósito) y las alteraciones en la migración de las neuronas durante el desarrollo en los pacientes con CD. Además, la figura muestra un esquema del receptor NMDA. Se puede acceder a las lecciones en el orden que desee el usuario.
Discusión
El receptor canal NMDA se activa mediante la estimulación simultánea de glicina y glutamato. En los simuladores, la concentración de glicina está predefinida por las condiciones experimentales de donde se obtuvieron los datos. La corriente NMDA corresponde a la suma de las corrientes entrantes de Na+ y Ca2+, así como de la corriente saliente de K+. Dado que se trata de un canal catiónico, no es posible distinguir el porcentaje de cada corriente iónica a partir de su registro.
Se ha reportado que la actividad sináptica excitatoria glutamatérgica normal y los potenciales de acción a ciertas frecuencias pueden producir un aumento de la concentración de Ca2+ interno que favorece la plasticidad neuronal (Inglebert & Debanne, 2021). Por el contrario, un aumento del glutamato en la sinapsis debido a diversas condiciones anómalas puede conducir a la excitotoxicidad (Guo et al., 2017). El proceso de desensibilización por calcio reduce la corriente NMDA y, en consecuencia, limita la entrada de calcio a través de este canal. La recuperación de la desensibilización vuelve a poner a disposición la neurona. En la corteza displásica existen neuronas anómalas que podrían estar asociadas a episodios convulsivos en los pacientes.
Diversos estudios revelan alteraciones en la migración neuronal, la orientación de las neuronas en la corteza cerebral y la estructura del receptor NMDA (Mohsin et al., 2023). Se presume que la estructura del receptor NMDA en las células citomegálicas está afectada. En las simulaciones, se reproducen los experimentos de recuperación de la desensibilización y sus porcentajes (André et al., 2004). El modelo matemático permitió estimar la concentración interna de Ca2+ en estos experimentos, complementando así los resultados experimentales. Con el primer estímulo se observó una menor concentración de Ca2+ interno en la neurona citomegálica y esto coincide con una densidad de corriente menor en estas neuronas y una menor desensibilización (34%). La función normal en una neurona implica la interacción del canal NMDA con otros canales, como el canal ácido -amino-3-hidroxi-5-metil-4-isoxazol-propiónico (AMPA) (Van Vugt et al., 2020). Por otro lado, las bombas PMCA (del inglés: plasma-membrane Ca2+ -ATPase) y SERCA (del inglés: Sarco Endoplasmic Reticulum Calcium Transporting ATPase) disminuyen la concentración de calcio interno al sacarlo de la célula y al ingresarlo al retículo endoplásmico, respectivamente (Berkefeld et al., 2010; Meldolesi, 2001).
El simulador presentado no considera el proceso de difusión de calcio ni una interacción explícita con moléculas quelantes o la interacción con otros canales. Está limitado a reproducir los registros electrofisiológicos macroscópicos, donde se define la recuperación de la desensibilización y se puede estimar el calcio interno, producto de esta corriente NMDA en las células displásicas y no displásicas.
Dentro de las ventajas de utilizar simuladores en la educación neurocientífica está una disminución en los costos de las prácticas de laboratorio. No es necesario el uso de animales, la compra de aparatos especializados y de reactivos. Estas características han motivado la integración curricular de simuladores en neurociencias (Lorenz & Egelhaaf, 2008). Con el desarrollo de este simulador se propone en los cursos de fisiología, neurociencias o biofísica integrar en su temario un canal dependiente de ligando con el objetivo de que los alumnos conozcan un canal diferente a los canales dependientes de voltaje. La enseñanza-aprendizaje del receptor NMDA estaría apoyado por simuladores que permitan introducir al alumno en las propiedades electrofisiológicas y biofísicas básicas del receptor NMDA (Reyes-Monreal et al., 2022), el estudio de la desensibilización (Reyes-Monreal et al., 2024) y el estudio de la recuperación de la desensibilización con el simulador presentado aquí.
Como un trabajo a futuro, se implementará un simulador para estudiar la participación del receptor NMDA en el dolor nociceptivo. Con el simulador presentado aquí, los alumnos de biología, medicina, biomedicina, biotecnología, neurociencias, fisiología y ramas afines tienen la oportunidad de realizar experimentos virtuales en células de tejido displásico, lo que sería imposible de realizar en un entorno real durante un curso de neurociencias o de biofísica.
Conclusiones
Se diseñó y desarrolló un simulador para el estudio de la recuperación de la desensibilización del receptor NMDA. Internamente, este simulador modela matemáticamente la relación del influjo de calcio a través del receptor, el incremento de calcio interno y el proceso de recuperación de la desensibilización. Reproduce los experimentos de recuperación de la desensibilización en neuronas NO-CD aparentemente normales, CD- aparentemente normales y CD-citomegálicas, tal como fueron reportados por André et al. (André et al., 2004). Estima la concentración de [Ca2+]i en todos los casos simulados y predice resultados que están de acuerdo con las conclusiones de estos autores. Este simulador se concibe como una herramienta de enseñanza guiada sobre el tema y debe considerarse como un recurso de apoyo didáctico. Se ejecuta en un ambiente de internet y su código estará disponible de manera abierta. Habiendo obtenido los derechos y publicado el producto final, el simulador será subido a internet en galeria.arpa.buap.mx/NMDA para ser usado por los interesados, siempre y cuando lo hagan sin fines de lucro.
Conflictos de interés
Los autores declaramos que no existe ningún conflicto de interés en esta investigación.











 nueva página del texto (beta)
nueva página del texto (beta)



