INTRODUCCIÓN
La constante generación de residuos peligrosos por las actividades propias de la industria petrolera y los derrames de hidrocarburos han ocasionado incidencias negativas en los ecosistemas, provocando escasez alimentaria y marginación, principalmente en poblaciones agrícolas expuestas a estos siniestros (Balseiro-Romero et al. 2018, Pérez-Muñoz et al. 2019). El daño ocasionado por los derrames de hidrocarburos depende del tipo de petróleo y su procedencia, siendo los productos livianos como la gasolina y el diésel más tóxicos que los crudos, ya que se evaporan a gran velocidad (Rivas-Trasancos et al. 2020). Estos combustibles contienen mezclas de diferentes moléculas químicas, clasificadas como hidrocarburos saturados, compuestos aromáticos, asfaltenos y resinas (Kim et al. 2013, Szewczyńska et al. 2017). En este sentido, la compleja estructura molecular de los hidrocarburos aromáticos policíclicos (HAP), les confiere alta resistencia al tratamiento, tornándose potencialmente bioacumulables (Mezzanotte et al. 2015, Khan et al. 2018. Debido a su hidrofobicidad, estos compuestos son difícilmente extraíbles del ambiente, por lo que se encuentran biodisponibles para los receptores ecológicos (Hunt et al. 2019). Por ello se ha demostrado que tienen consecuencias mutagénicas y carcinogénicas en organismos expuestos a sitios contaminados (Ukalska et al. 2018).
Esta problemática ha generado la búsqueda de alternativas viables que permitan remediar agroecosistemas contaminados sin frenar su producción (Alegbeleye et al. 2017), siendo la fitorremediación y la bioaumentación tecnologías biológicas sostenibles para la restauración de suelos agrícolas contaminados (Ventorino et al. 2019, Ławniczak et al. 2020), ya que la degradación de xenobióticos por acción radicular y su asociación con la microbiota de la rizósfera son los principales mecanismos en la eliminación de los HAP (Hussain et al. 2018, Hoang et al. 2021).
La bioaumentación permite la remoción de contaminantes mediante la inoculación de cepas microbianas con capacidad degradativa (Wu et al. 2020, Lipińska et al. 2021). La naturaleza de los suelos agrícolas exige la utilización de microorganismos que favorezcan la biodegradación del contaminante mientras promueven el crecimiento vegetal, disminuyendo el uso de agroquímicos costosos y dañinos para el ambiente (Prasad et al. 2017, Vejan et al. 2019). En este sentido, Azotobacter vinelandii es una bacteria diazótrofa cuya capacidad metabólica le permite degradar compuestos hidrocarbonados de origen petrogénico (Suryatmana et al. 2018, Chaudhary et al. 2019). Sin embargo, la viabilidad de microrganismos exógenos en sitios contaminados se compromete, por lo que se ha estudiado el uso de portadores o inmovilización, que mantienen su actividad, mejorando las tasas de degradación (Partovinia y Rasekh 2018).
Además, el uso de plantas ornamentales con valor comercial ha sido ampliamente estudiado en procesos de fitorremediación de suelos contaminados con hidrocarburos, debido a que su uso impide la asimilación del contaminante o sus metabolitos a la cadena trófica, disminuyendo las consecuencias a la salud y promoviendo la generación de recursos económicos durante el proceso de descontaminación de agroecosistemas (Liu et al. 2018). En este sentido, Tagetes erecta ha sido ampliamente cultivada por su uso decorativo en jardinería, así como en diversos eventos sociales y religiosos (Gopi et al. 2012, Tandel y Kumari 2021), destacando su importancia comercial y económica; además, esta especie vegetal tiene la capacidad de tolerar concentraciones de hasta 90 g/kg de hidrocarburos (Prematuri et al. 2019).
En este contexto, el objetivo de este trabajo fue evaluar el potencial de Tagetes erecta y Azotobacter vinelandii libre e inmovilizada, para la biorremediación de suelos agrícolas contaminados con diésel en condiciones de invernadero (ex situ), así como determinar la genotoxicidad y citotoxicidad de los suelos para generar alternativas sostenibles en la recuperación de suelos agrícolas impactados.
MATERIALES Y MÉTODOS
Muestreo
Se recolectaron 20 kg de suelo contaminado en una zona agrícola impactada por derrame de diésel en la región de Acatzingo, Puebla, México (18º 58’ 43.0” E, 97º 46’ 49.7” O). Las características físicas y químicas del suelo lo clasifican como arenoso, con pH de 7.47, 9.25 % de materia orgánica, 0.39 % de nitrógeno total, 20.32 mg/kg de fósforo, densidad aparente de 1.29 g/ml, conductividad eléctrica de 0.214 dS/m y capacidad de campo de 35 %.
Propagación del material vegetal
La propagación de Tagetes erecta se realizó en el invernadero de investigación del Centro de Innovación Tecnológica en Agricultura Protegida de la Universidad Popular Autónoma de Puebla (CITAP-UPAEP), en Atlixco, Puebla, México. Se sembraron 100 semillas de T. erecta en almácigos con turba como sustrato, humedecidos diariamente con solución nutritiva Steiner (1961) por 30 días. Posteriormente se procedió al trasplante.
Propagación e inmovilización de Azotobacter vinelandii
Para el proceso de bioaumentación se utilizó la cepa ATCC 12837 Azotobacter vinelandii la cual fue cultivada en el siguiente medio (g/L): 1 extracto de levadura; 5 D-manitol; 0.7 K2HPO4; 0.1 KH2PO4; 1 MgSO4 7H2O, ajustado a pH 7 ± 0.05. Para obtener la población bacteriana máxima se creció a 28 ºC durante 72 h a 200 rpm (Conde-Ávila et al. 2022). Posteriormente se realizó la mezcla de 2 ml del inóculo en una solución estéril de alginato de sodio a una concentración final de 2% (p/v), y se incubó a temperatura ambiente durante 1 h. Finalmente, para la obtención de las perlas de encapsulación, se adicionó por goteo una alícuota de la suspensión de alginato con A. vinelandii a una solución estéril de CaCl2 0.1 M (Reyes-Reyes et al. 2018).
Tratamientos del ensayo de biorremediación
El experimento se desarrolló en macetas plásticas de 1 kg de capacidad rellenas con 500 g de suelo contaminado con diésel, colocando 100 g de tezontle en el fondo del recipiente para evitar fugas. Los tratamientos empleados fueron; T0: microbiota autóctona, T1: Tagetes erecta, T2: Azotobacter vinelandii libre, T3: Tagetes erecta + Azotobacter vinelandii libre, T4: Azotobacter vinelandii inmovilizada, T5: Tagetes erecta + Azotobacter vinelandii inmovilizada, T6: Tagetes erecta + perlas de alginato, T7: perlas de alginato. Cada tratamiento constó de cinco repeticiones, utilizando un diseño de cuadrado latino. Por último, se realizó la inoculación de 108 UFC/ml de A. vinelandii para los tratamientos con la bacteria libre e inmovilizada, siete días antes del trasplante.
Ensayo de biorremediación
El experimento se llevó a cabo en las instalaciones del CITAP-UPAEP en condiciones de invernadero (humedad relativa de 39.3 ± 8.9 %, temperatura 31.4 ± 5.7 ºC), humedeciendo cada maceta con agua diariamente, procurando capacidad de campo. En los días 0 y 50 se determinó la concentración de diésel residual (mg/kg), así como la población microbiana viable (UFC/g) en cada unidad experimental.
Cuantificación de población bacteriana
La cuantificación de microorganismos heterótrofos cultivables en el suelo inicial y final de cada tratamiento se realizó por dilución seriada en condiciones estériles a partir de 1 g de suelo y 9 ml de solución salina 0.09 % y hasta la dilución 107, las cuales fueron sembradas por triplicado en agar nutritivo utilizando 0.2 ml de inóculo, e incubadas por 48 h a 28 ºC (Orozco et al. 2016). La determinación de unidades formadoras de colonia por gramo de suelo (UFC/g), se obtuvo mediante el conteo de UFC en placa, multiplicado por la dilución utilizada y dividido entre el volumen inoculado.
Cuantificación de diésel residual
La concentración de diésel se determinó para cada tratamiento, para lo cual se utilizaron 3 g de suelo mezclado con 3 g de sulfato de sodio anhidro, con una adición de 15 ml de diclorometano-acetona 1:1, utilizando baño ultrasónico por 45 min con intervalos de 10 min. Posteriormente, las muestras se transfirieron a tubos falcón de 15 ml para centrifugarse por 10 min a 2000 rpm (Mnif et al. 2015, Bolotnik et al. 2019). Por último, se recuperó el sobrenadante en tubos, se dejó evaporar el disolvente en campana de extracción hasta sequedad y se realizó el análisis gravimétrico de acuerdo con el método EPA 9071 B (USEPA 1998).
donde HTP es la concentración de hidrocarburos totales de petróleo, RB el peso (mg) del tubo con el extracto de hidrocarburos, RA el peso (mg) del tubo vacío a peso constante y P la cantidad de suelo utilizado (g).
Parámetros morfológicos de la planta
Se realizaron mediciones de altura de la planta (cm), longitud de raíz (cm), diámetro del peciolo (mm), peso húmedo (g) y peso seco (g) de la planta en cada unidad experimental. Posteriormente, se obtuvo el índice de calidad de Dickson (ICD), de acuerdo con Villalón-Mendoza (2016).
Análisis de citotoxicidad y genotoxicidad
La evaluación de citotoxicidad y genotoxicidad a los tratamientos se realizó utilizando Allium sativum como bioindicador, mediante la determinación del índice mitótico y el conteo de anormalidades nucleares y micronúcleos (Fiskesjö 1985). Los bulbos de A. sativum fueron expuestos durante siete días al suelo inicial y residual de cada tratamiento; posteriormente se realizaron cortes de 1-3 mm de la zona del meristema apical de las raíces, los cuales se fijaron con una solución 1:3 de ácido acético y etanol. Ulteriormente se realizó la hidrólisis de las muestras, colocándolas en una solución de ácido clorhídrico 1 N a 50 ºC durante 5 min. La tinción de raíces se realizó en un portaobjetos con orceína al 2 % durante 2 min. Finalmente se realizó el aplastado celular (squashing) de cada muestra con ayuda de un cubreobjetos. Los preparados citológicos se manejaron en simple ciego y se identificaron 1000 células meristemáticas para cada tratamiento. Las células se cuantificaron en cualquier fase de mitosis, al igual que las aberraciones cromosómicas, utilizando un microscopio óptico de fluorescencia Leica DM1000 LED. Por último, se calculó el índice mitótico (IM), y los resultados de anormalidades nucleares obtenidos se sometieron a prueba de χ2 para asociar la genotoxicidad presentada en células de Allium sativum.
Análisis estadístico
Para conocer las diferencias significativas entre tratamientos, las variables de respuesta fueron analizadas estadísticamente mediante la prueba T-student pareada, análisis de varianza (ANDEVA) de un factor y comparación de medias de Tukey, utilizando el programa estadístico Graphpad Prism 9 con un nivel de confianza del 95 %.
RESULTADOS Y DISCUSIÓN
Cuantificación de la población bacteriana
El conteo inicial de microorganismos en suelo antes de los tratamientos fue de 9.17 × 107 UFC/g (Cuadro I). Por otro lado, la prueba de T-student mostró un aumento estadísticamente significativo de UFC/g de suelo en la mayoría de los tratamientos (Fig. 1a). Asimismo, el crecimiento bacteriano en los tratamientos con Tagetes erecta sugiere que una fracción de la microbiota rizosférica logró utilizar el diésel como fuente de carbono o energía (Diaz et al. 2021). Resultados similares fueron obtenidos por Chuluun et al. (2014) con Perennial ryegrass (Lolium perenne L.), quienes observaron el aumento de microorganismos heterótrofos cultivables en todos los tratamientos con plantas en órdenes de 108 y 109 en un suelo contaminado de manera artificial con diésel a 50 g/kg, concluyendo que los exudados segregados por la planta pudieron servir como fuente de nutrientes y carbono para los microorganismos (Liu et al. 2014). Finalmente, el efecto de rizoestimulación pudo observarse en el tratamiento T3 (Tagetes erecta + Azotobacter vinelandii libre), cuya media de crecimiento bacteriano de 3.83 × 1010 UFC/g de suelo fue estadísticamente mayor a los otros tratamientos (p = 0.00) (Fig. 1b) debido a que plantas mejoran la porosidad del suelo y estimulan la actividad microbiana por medio de nutrientes y cosustratos exudados (Salim et al. 2020).
CUADRO I REMOCIÓN DE DIÉSEL Y MICROBIOTA EN EL ENSAYO DE BIORREMEDIACIÓN.
| Tratamiento | Diésel residual (mg/kg) | Remoción (%) | Microbiota (UFC/g) |
| Día 1 | |||
| Suelo contaminado inicial | 8 710.15 ± 1 032.90 | N/A | 9.17 × 107 ± 2.08 × 107 |
| Día 50 | |||
| T0 (microbiota autóctona) | 6 132.84 ± 255.13abc | 42.19 ± 5.92 | 4.83 × 108 ± 1.44 × 108 b |
| T1 (Tagetes erecta) | 6270.89 ± 1061.07abc | 41.63 ± 24.31 | 5.33 × 109 ± 2.02 × 109 b |
| T2 (Azotobacter vinelandii libre) | 7 121.06 ± 245.55abc | 25.86 ± 7.24 | 5.17 × 108 ± 1.26 × 108 b |
| T3 (Tagetes erecta + Azotobacter vinelandii libre) | 5 624.74 ± 24.63bc | 54.85 ± 0.68 | 3.83 × 1010 ± 1.15 × 1010 a |
| T4 (Azotobacter vinelandii inmovilizada) | 7 229.85 ± 543.22ab | 25.60 ± 11.91 | 3.67 × 108 ± 1.15 × 108 b |
| T5 (Tagetes erecta + Azotobacter vinelandii inmovilizada) | 5 595.91 ± 298.00c | 55.96 ± 8.54 | 8.00 × 108 ± 3.00 × 108 b |
| T6 (Tagetes erecta + perlas de alginato) | 6 327.34 ± 171.79abc | 31.92 ± 3.74 | 1.08 × 109 ± 1.76 × 108 b |
| T7 (perlas de alginato de sodio) | 7281.72 ± 239.99a | 24.05 ± 8.42 | 5.67 × 108 ± 1.04 × 108 b |
| Valor p | 0.00 | 0.00 | |
Medias que no comparten la misma letra son significativamente diferentes; nivel de significancia α = 0.05.
N/A: no aplica, UFC: unidades formadoras de colonias.
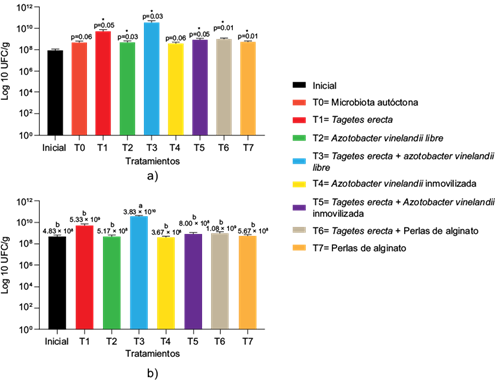
Fig. 1 Conteo de microorganismos heterótrofos en los distintos tratamientos. (a) Prueba T pareada respecto a la concentración de suelo inicial (*tratamientos estadísticamente significativos); (b) análisis de varianzas de una vía para comparar los diferentes tratamientos (p = 0.05). (UFC: unidades formadoras de colonias.)
Cuantificación del diésel residual
La concentración inicial de hidrocarburos fue de 8710.15 mg/kg. Rodríguez et al. (2012) concluyen que una concentración de 6270 mg/kg es considerada como el límite inferior de tolerancia de hidrocarburos para los microorganismos, por lo que pudo haber sido un factor limitante para la biodegradación de diésel; igualmente, el valor obtenido rebasa los 1200 mg/kg, límite máximo permitido de la fracción media en suelo agrícola de acuerdo con la NOM-138-SEMARNAT/SSA1-2012 (SSA 2013), lo cual incrementa la hidrofobicidad del suelo y afecta el crecimiento de las plantas y las actividades microbianas en suelo (Hewelke et al. 2018). Esto constituye un grave riesgo para la salud humana debido a su resistencia al tratamiento y a sus propiedades mutagénicas, teratogénicas y carcinogénicas (Rodríguez-Campos et al. 2019).
Por otro lado, la prueba de T pareada para concentración de diésel mostró diferencias significativas para el T0 (microbiota autóctona; p = 0.03), debido a que la microbiota autóctona estimulada por factores abióticos como la humedad, oxígeno y temperatura logra promover la degradación mediante el uso de hidrocarburos como fuente de energía (Silva-Castro et al. 2015). Igualmente, los tratamientos T1 (Tagetes erecta; p = 0.00), T3 (Tagetes erecta + Azotobacter vinelandii; p = 0.03), T5 (Tagetes erecta + Azotobacter vinelandii inmovilizada; p = 0.02) y T6 (Tagetes erecta + perlas de alginato; p = 0.04) fueron estadísticamente significativos respecto al suelo inicial (Fig. 1a), fenómeno atribuido al sistema denso de raíces de la especie Tagetes erecta. Ésta permite el desarrollo de microorganismos asociados y promueve la biodegradación (Rajkumari et al. 2021) que, al ser bioestimulada por A. vinelandii (la cual posee distintos mecanismos para la remoción de hidrocarburos, como fijación de nitrógeno esencial para el crecimiento de raíces), incrementa la presencia de exudados que contribuyen a la degradación (Suryatmana et al. 2019). Igualmente, A. vinelandii tiene la capacidad de producir biosurfactantes que reducen la tensión superficial de los hidrocarburos y favorecen la interacción de los microorganismos con el contaminante (Suryatmana et al. 2018). Por otro lado, se sabe que la presencia de enzimas oxidativas y cometabolismo con otras bacterias degradadoras conducen a la disminución de diésel en suelo (Onwurah y Nwuke 2004, Chaudhary et al. 2019).
En este sentido, la bioaumentación con bacterias exógenas en procesos de descontaminación suele ser relevante por su capacidad catalítica de compuestos hidrocarbonados (Laothamteep et al. 2022), lo cual se evidencia en el tratamiento T7 (perlas de alginato; Fig. 2a), en el cual no se empleó Azotobacter vinelandii y no presentó remoción significativa (p = 0.19). Por otra parte, el propio alginato pudo haber disminuido la degradación por ser una fuente alterna más accesible de carbono para los microorganismos (Goma-Tchimbakala et al. 2022). No obstante, los tratamientos T2 (Azotobacter vinelandii) y T4 (Azotobacter vinelandii inmovilizada) no presentaron diferencias estadísticamente significativas respecto al suelo inicial (p = 0.09 y p =0.08, respectivamente), lo cual pudiera estar relacionado con que la bacteria fue cultivada en un medio óptimo, impidiendo aclimatación al contaminante. Esto, sumado a los factores bióticos y abióticos que perjudicaron su crecimiento y, por tanto, el proceso de biodegradación (Innemanová et al. 2018).
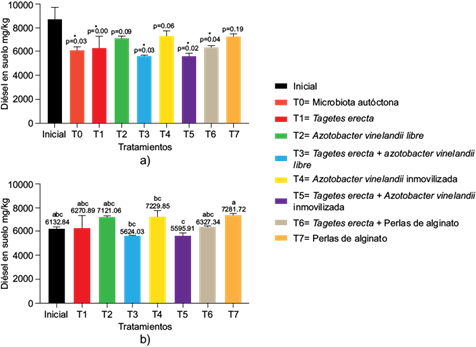
Fig. 2 Remoción de diésel en los diferentes tratamientos. (a) Prueba T pareada respecto a la concentración de suelo inicial (*tratamientos estadísticamente significativos); (b) análisis de varianza de una vía para comparar los diferentes tratamientos (p = 0.05).
Al realizar el ANDEVA de una vía (Fig. 2b) se observan diferencias estadísticas significativas entre las concentraciones de diésel residual en los tratamientos (Cuadro I); sin embargo, no se logra establecer un factor común que determine el tratamiento con mayor eficacia en la remoción de hidrocarburos, dado que los tratamientos comparten grupos estadísticos iguales. No obstante, se observa que los tratamientos T3 (Tagetes erecta + A. vinelandii) y T5 (Tagetes erecta + A.vinelandii inmovilizada) son estadísticamente diferentes al tratamiento T7 (perlas de alginato), que en la prueba t-Student resultó no ser significativo para la remoción de diésel respecto al suelo inicial. Esto acentúa la influencia de la planta en la mejora del proceso de biodegradación del contaminante, la cual se refleja en las tasas de remoción debido a que se promueve la aireación del suelo, esencial para los procesos aeróbicos de remoción de hidrocarburos (McIntosh et al. 2017). Además, cuando la rizorremediación es asistida por microorganismos provoca cambios en la microbiota autóctona, que favorecen la degradación (Pandey et al. 2021).
Parámetros morfológicos de Tagetes erecta
Los tratamientos T1 y T3 presentaron un ICD óptimo (0.9857 ± 0.3067 y 0.8907 ± 0.0568, respectivamente; Cuadro II) pese a la compactación, la escasa retención de humedad y la alta concentración de hidrocarburos en suelo; no obstante, estos factores pudieron haber disminuido el desarrollo y crecimiento morfológico vegetal adecuado en todos los tratamientos con planta (Hajabbasi 2016). Por otra parte, los tratamientos T5 y T6 (ICD= 1.4568 ± 0.6365 y 3.8809 ± 1.9705, respectivamente) mostraron que la presencia de alginato impacta negativamente la calidad de la planta, posiblemente porque obstaculiza la interacción de los exudados de la planta con los microorganismos (Pino et al. 2016).
CUADRO II PARÁMETROS MORFOLÓGICOS DE Tagetes erecta EN LOS DIFERENTES TRATAMIENTOS.
| Tratamiento | Longitud aérea (cm) | Longitud de raíz (cm) | Diámetro del peciolo (mm) | Peso húmedo total(g) | Peso seco total (g) | Peso seco aéreo (g) | Peso seco raíz (g) | ICD |
| T1 (Tagetes erecta) | 6.4000 ± 0.5568a | 4.7333± 1.2097a | 2.1000 ± 0.2000ab | 0.7957 ± 0.2065a | 0.1241 ± 0.0299a | 0.0581± 0.0085a | 0.0661± 0.0250a | 0.9857 ± 0.3067b |
| T2 (Tagetes ercta + Azotobacter vinelandii) | 6.3000± 2.8688a | 6.9000± 3.9230a | 2.3333± 0.3215a | 0.8406 ± 0.1332a | 0.1303± 0.0264a | 0.0596± 0.0139a | 0.0707± 0.0129a | 0.8907± 0.0568b |
| T5 (Tagetes erecta + Azotobacter vinelandii inmovilizada) | 4.8333 ± 1.3051a | 6.4667 ± 1.4844a | 2.0333 ± 0.9018ab | 0.7539 ± 0.4687ab | 0.1217 ± 0.0403a | 0.0676 ± 0.0268a | 0.0541 ± 0.0229ab | 1.4568 ± 0.6365a |
| T6 (Tagetes erecta + perlas de alginato) | 3.4333 ± 0.2082a | 2.3000 ± 0.2646a | 0.8667 ± 0.0577b | 0.1231 ± 0.0501b | 0.0557 ± 0.0186a | 0.0419 ± 0.0104a | 0.0138 ± 0.0102b | 3.8809 ± 1.9705a |
| Valor p | 0.15 | 0.11 | 0.02 | 0.03 | 0.04 | 0.34 | 0.02 | 0.02 |
Medias que no comparten la misma letra son significativamente diferentes, nivel de significancia α = 0.05.
ICD: índice de calidad de Dickson.
Análisis de citotoxicidad y genotoxicidad
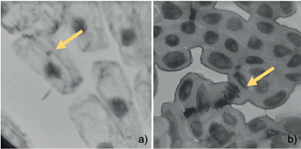
Los ensayos de toxicidad indicaron citotoxicidad con índices mitóticos ≤ 50 % (Cuadro III). Igualmente, se presentaron anormalidades nucleares y micronúcleos en todos los tratamientos (Fig. 3). Algunos estudios indican que las células de organismos expuestas a suelos contaminados con diésel presentan normalmente aberraciones cromosómicas a causa de la formación de puentes, rupturas y reordenamientos cromosomales que originan ADN excedente que se heterocromatiniza y posteriormente es expulsado del núcleo en forma de yemas y/o micronúcleos (Cruz et al. 2019, Alavi et al. 2022). Sin embargo, otros autores concluyen que la toxicidad no logra correlacionarse con la concentración de diésel en suelo, por lo que se infiere la influencia de otros factores (Leme y Marín-Morales 2008), tales como la formación de intermediarios de hidrocarburos aromáticos homocíclicos y heterocíclicos azufrado. Esto se debe a la degradación incompleta que ocurre en procesos de degradación bacteriana, los cuales suelen ser más tóxicos que sus precursores e impactan de manera importante en los sistemas biológicos (Mazzeo et al. 2018, Idowu et al. 2019).
CUADRO III PARÁMETROS CELULARES Y GENÉTICOS EN Allium sativum.
| Tratamientos | Índice mitótico con relación al testigo (%) | Anormalidades nucleares | Micronúcleos | χ2 |
| Testigo | 19 ± 0.6 | 2.33 ± 0.58 | 0.67 ± 0.58 | - |
| Suelo inicial | 9.33 ± 0.55** | 18.33 ± 1.16 | 4.33 ± 1.00 | 14.22* |
| T0 (microbiota autóctona) | 9.27 ± 0.85** | 15 ± 3.61 | 4.0 ± 1.53 | 10.86* |
| T1 (Tagetes erecta) | 9.60 ± 0.78 | 19.67 ± 7.77 | 3.67 ± 1.00 | 15.38* |
| T2 (Azotobacter vinelandii) | 12.10 ± 1.1 | 14 ± 5.20 | 3.0 ± 0.58 | 9.78* |
| T3 (Tagetes erecta + Azotobacter vinelandii) | 11.77 ± 1.08 | 17.67 ± 8.96 | 3.0 ± 2.08 | 13.09* |
| T4 (Azotobacter vinelandii inmovilizada) | 10 ± 0.92 | 17.33 ± 5.51 | 2.66 ± 1.73 | 10.86* |
| T5 (Tagetes erecta + Azotobacter vinelandii inmovilizada) | 9.60 ± 0.62 | 14.33 ± 3.51 | 2.67 ± 1.16 | 9.78* |
| T6 (Tagetes erecta + perlas de alginato) | 11.03 ± 1.10 | 12 ± 1.00 | 2.33 ± 0.58 | 7.68* |
| T7 (perlas de alginato de sodio) | 11.40 ± 1.04 | 17 ± 7.81 | 1.67 ± 1.16 | 13.09* |
** = Daño citotóxico (Índice mitótico ≤ 50 % del testigo)
* = Daño genotóxico (χ2= 3.84)
χ2 = Chi cuadrada
CONCLUSIÓN
Se ha demostrado que las técnicas de biorremediación como la fitorremediación y la bioaumentación en las que se utilizan Tagetes erecta y Azotobacter vinelandii, son de fácil aplicación y asequibles, tienen capacidad degradativa y enfatizan el papel de la rizoestimulación en el proceso de biodegradación.
Este estudio sugiere que el uso de matrices de inmovilización como el alginato de sodio en procesos de rizorremediación, no mejora de manera significativa las tasas de remoción de diésel en suelos agrícolas en condiciones de invernadero; por el contrario, afecta el crecimiento óptimo de la planta en ambientes de estrés. Sin embargo, el uso de microorganismos exógenos preadaptados al contaminante podría mejorar los procesos de bioaumentación y rizoestimulación.
La remoción significativa de hidrocarburos no garantiza la ausencia de toxicidad en el suelo, ya que el diésel residual ocasionó daño genotóxico y citotóxico en todos los tratamientos debido a las características mutagénicas, teratogénicas y carcinogénicas de estos xenobióticos. Se sugiere evaluar la toxicidad de suelos contaminados y biorremediados como estudio complementario en procesos de remoción biológica de contaminantes en suelos agrícolas.











 nueva página del texto (beta)
nueva página del texto (beta)