Introducción
Cuando la piedra caliza (CaCO3) es sometida a un proceso de calcinación se produce la cal viva u óxido de calcio (CaO) de acuerdo a Ec. (1) (Chávez-Guerrero et al., 2017; Sverak, 2004); el cual, si reacciona con un exceso de agua, genera la cal hidratada (cal apagada) o hidróxido de calcio (Ca(OH)2) de acuerdo a Ec. (2) (Zhao et al., 2018).
El equilibrio de solubilidad y su producto de solubilidad (Kps), en una disolución saturada de Ca(OH)2 está dado por la Ec. (3) y Ec. (4) respectivamente y el valor de su Kps está alrededor de 6.5 x 10-6 a 25 °C (IUPAC, 1992).
La Ec. (4) representa el Kps como producto de las concentraciones molares de los iones, que no predice el efecto que puede tener la fuerza iónica; en consecuencia, se debe modificar reemplazando las concentraciones molares por actividades. La actividad (a) de una especie A, se expresa como el producto de su concentración molar [A] y de su coeficiente de actividad (γA) de acuerdo a Ec. (5).
El coeficiente de actividad de un ion, es un valor adimensional que depende de la fuerza iónica de la solución (μ), de la carga y tamaño del ion. El γA se puede calcular de acuerdo a la ecuación extendida de Debye‐Hückel (Ec. (6)), para una temperatura de 25 °C y μ ≤ 0.1 M.
Donde zA es la carga del ion, αA es el diámetro efectivo del ion hidratado en nanómetros (0.6 para Ca2+ y 0.35 para OH-), 0.51 y 3.3 son constantes y μ es la fuerza iónica de la solución que se da, de acuerdo a Ec. (7) (Harvey, 2023).
Donde ci y zi son la concentración molar y carga del ión i-ésimo.
La solubilidad del Ca(OH)2 en agua decrece con el incremento de la temperatura (Yuan et al., 2010), por ejemplo a 20 °C y 100 °C son 1,66 g/L y 0,8 g/L, respectivamente (Zhao et al., 2018), así la concentración de la disolución saturada de hidróxido de calcio en agua pura a 25 °C, es de aproximadamente 0,02 M y su pH de 12,4 (Traynor et al., 2020).
Sørensen en 1909 introdujo el término valor de pH, para describir la concentración de iones de hidronio en mezclas acuosas (Chu et al., 2016) y lo definió como el logaritmo decimal negativo de la concentración molar de iones hidronio (H3O+). Sin embargo, es más satisfactorio definir el pH en términos de actividad de los iones hidrógeno de acuerdo a Ec. (8).
Siendo su rango habitual de 0 a 14; así, para una determinada solución; un valor de pH de 7, indica que es neutro y si el valor pH es mayor de 7 describe que la solución es básica y si el de valor de pH es menor a 7 indica que es ácida (Qin et al., 2015).
Los sensores de pH proporcionan una medida logarítmica de la concentración de iones de hidrógeno (Yoon et al., 2017). Cuando estos sensores miden el pH, lo hacen de manera indirecta; esto es, a través de la medida del potencial (E) que se genera cuando la membrana selectiva de iones del bulbo de vidrio, entra en contacto con un determinado analito, el cual posee una actividad de iones hidrógeno (H+) diferente al electrolito tampón interno (Traynor et al., 2020). Dicho de otra manera: cuando se calibra el electrodo usando las respectivas soluciones buffer, el medidor genera e incorpora una curva de calibración de pH vs mV, que lo utiliza para convertir los potenciales del analito, a pH; los cuales se muestran en la pantalla del medidor y así el potencial (E) de medición del electrodo sensor está determinado por la ecuación de Nernst, según Ec. (9) (Thermo Fisher Scientific, 2022).
Eo es el potencial estándar del electrodo de referencia interno con respecto al electrodo de hidrógeno, R es la constante de gas (8.314 JK-1 mol-1), T es la temperatura en grados Kelvin, F es la constante de Faraday (96485 °C mol-1) y log aH + es el pH.
A 25 °C, el E del electrodo en función del pH de la solución, se da de acuerdo a Ec. (10).
La ecuación 10, muestra que, el E cambiaría en 59,16 mV (negativo), por unidades de pH a temperatura ambiente (25 °C) (Zhang et al., 2019; Qin et al., 2015).
El uso de los sensores de pH, son eficaces en el control de procesos de diferentes industrias, como en la metalurgia, medicina, agricultura, alimentos, la bioingeniería, acuícolas, piscicultura, controles ambientales, industria del cemento, procesos de desinfección etc. (Chu et al., 2016).
El electrodo típico más utilizado para medir el pH, está provisto de: un bulbo de vidrio específico que contiene iones de litio o sodio, una solución interna que puede ser ácido clorhídrico 0.1 M o una solución tamponada de cloruro, un electrodo interno de Ag/AgCl (de referencia) y el cuerpo del electrodo de vidrio o plástico (Qin et al., 2015). Sin embargo, en el presente trabajo se utilizó un electrodo de pH de combinación (electrodo sensor y de referencia integrado en el mismo cuerpo), con sistema de referencia ROSS, que no contienen plata ni mercurio que puedan reaccionar con la muestra y tienen un rango de temperatura de 0 a100°C (Thermo Fisher Scientific, 2022).
Por otro lado, la conductividad eléctrica, es la capacidad de un material (Sólido, líquido o gaseoso) para conducir la corriente eléctrica. En soluciones, la conductividad, está determinada por la concentración total de iones; a mayor cantidad, su conductividad será más alta (Kaewthong y Wattanachant, 2018). Así la conductividad del agua altamente pura, a 25 °C es superior a 0,055 μS/cm (Asenbaum et al., 2011), la conductividad del agua potable suele estar entre 50‐500 μS/cm (Banna et al., 2014) y la conductividad del agua destilada y de mar están de 1‐10 y de 30000 a 50000 μS/cm respectivamente (Hach Company, 2021). En la mayoría de los casos, la temperatura incrementa la conductividad eléctrica; debido a que origina un mayor movimiento y colisiones de sus partículas (Kazemi et al., 2020; Duan et al., 2013).
El presente trabajo pretende validar la ecuación de Nernst y explorar el comportamiento de los valores pHe, E y de su conductividad, para poner en evidencia cómo son afectados por la baja solubilidad de las disoluciones de Ca(OH)2. Esta evidencia es de vital importancia en las industrias que utilizan el hidróxido de calcio como regulador del pH, ya que conduce a evitar, problemas y sobrecostos de tipo operativo. Este problema se toma como una oportunidad para resolverlo, empleando el aprendizaje basado en problemas (ABP) y resolver la pregunta: ¿Cómo se podría calcular la masa de Ca(OH)2 necesaria para tener un pH determinado en mezclas a nivel industrial?
Así el objetivo del presente trabajofuevalidar la ecuación de Nernst experimentalmente usando disoluciones de Ca(OH)2 y presentar una sugerencia didáctica que pretende resolver los gastos por el uso de exceso de Ca(OH)2 en la industria, estimando una relación matemática que permita hallar la masa de Ca(OH)2, que debe adicionar a una determinada cantidad de agua para alcanzar un pH requerido.
Material y métodos
Para caracterizar el Ca(OH)2, utilizado en el presente estudio; se realizó un ensayo XRD, con el difractómetro marca Rigaku, modelo Miniflex 600, con una longitud de onda de 0,154 nm y velocidad de barrido de 2°/min con un paso de medida 2θ de 0,02°. Se identificó, los grupos funcionales presentes en la muestra de Ca(OH)2, aplicando el análisis FTIR, con el espectrómetro ATR Thermo Nicolet IS50 FTIR. La morfología del Ca(OH), se determinó con el microscopio electrónico de barrido (SEM) TESCAN, modelo Vega 3 XMU, que utilizó un emisor de electrones LaB6 con un voltaje de aceleración de 20 kV; previamente las muestras fueron recubiertas con una película conductora de oro.
Los valores de pHe, con sus correspondientes E y temperatura, de cada muestra, fueron medido usando, el electrodo de combinación Thermo Scientific Orión 8157BNUMD con sistema ROSS ultra y la conductividad con el electrodo Thermo Scientific Orion Dura Probe 013005MD. Como dispositivo para visualizar los resultados, se usó, el multiparámetro Thermo Scientific, Orión Versa Star Pro y para todo ensayo se usó la sonda agitadora Thermo Scientific. Las muestras sólidas de Ca(OH)2, se pesaron en la Balanza analítica Mettler Toledo, Modelo AB 135‐S/FACT.
Se empleó el Ca(OH)2 grado analítico Aldrich Chemical (95%) y para calibrar el electrodo de pH se usó buffer Thermo Orion de pH 12,46, 10,01, 7 y 4,01. De similar manera, para calibrar el electrodo de conductividad se usó, estándares de conductividad Thermo Orion de 12,9 mS/cm y de 1413 μS/cm. Así, cuando se calibró el electrodo de pH, la pendiente de su recta, debía oscilar, de 92 a 102% (54,43 a 60,34 mV por unidad de pH) y entre cada ensayo, el electrodo de pH y de conductividad, fueron enjuagado con agua destilada y secadas suavemente, con una toallita sin pelusas, para evitar contaminación (Thermo Fisher Scientific, 2022). Para toda prueba se utilizó agua destilada cuyo valor de pH estuvo en el orden de 5,61 y de conductividad = 3,518 μS/cm a 27,5 °C ± 0,1 °C. Se usó fiolas volumétricas para preparar y homogenizar las respectivas muestras, con agitación intensa. Después de sedimentar, cada muestra fue filtrada, para su respectiva lectura.
Resultados y discusión
Caracterización del Ca(OH) 2
Según los resultados el patrón XRD (Figura 1), presenta una combinación de Ca(OH)2 (♦) y CaCO3 (●),debido a que presenta picos correspondiente a los planos (104) y (012) para el CaCO3 (Chávez-Guerrero et al., 2017; Praipipat et al., 2023) y los planos (001), (011), (110) y (111), para el Ca(OH)2 (Harish et al., 2022; Samanta et al., 2016; Song et al., 2022). Se hubiese esperado que el patrón de la muestra comercial en estudio coincidiera con la tarjeta JCPDS (N°.01-073-5492) (Khachani et al., 2014); sin embargo, no se dio debido a la formación de CaCO3 por la adsorción de CO2 del ambiente, por esta razón a cada peso de muestra se consideró el 95% de pureza del Ca(OH)2.
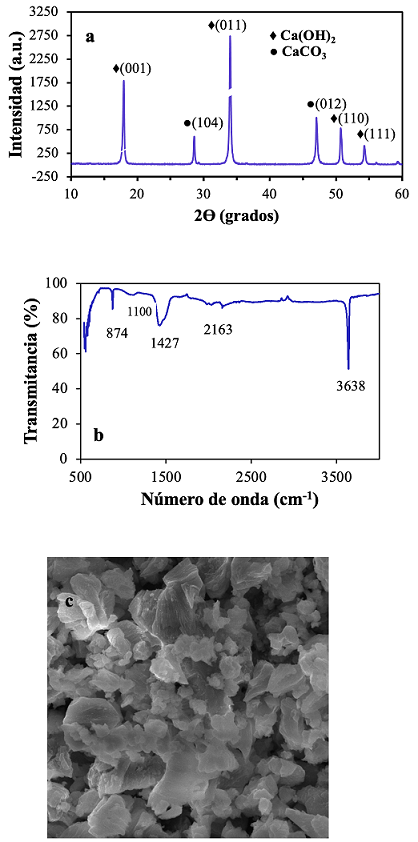
Figura 1 Caracterización del Ca(OH)2. (a) Patrón XRD. (b) Espectro FTIR. (c) Imagen morfológica SEM.
El espectro FTIR de la muestra Ca(OH)2 (Figura 1b), reveló que presenta una banda de estiramiento a 3638 cm-1, debido a la formación de grupos OH en Ca(OH)2 ( (Eletta et al., 2016; Khachani et al., 2014; Eisazadeh et al., 2012), los picos menores a 2163 cm-1, sugieren la adsorción de CO2 atmosférico (Samanta et al, 2016). Las bandas a 1427 cm-1, 1100 cm-1 y 874 cm-1, indican la formación de CO3 (grupos carbonatos) (Khachani et al., 2014). La imagen SEM (Figura 1c) del Ca(OH)2, muestra la presencia difusa de cristales hexagonales, junto a estructuras tipo romboedro, peñones y hojuelas.
Comportamiento de los valores de pHe frente a sus respectivos pH teórico
La Figura 2, evidencia que la curva formada por los valores de pHe, difiere del comportamiento lineal de los valores de pH teóricos (PHt) (R2=1), los cuales fueron calculados directamente, usando Ec. (8), tomando las mismas [OH-] de pHe. Se nota que los valores de pHe forman dos zonas bien definidas, la primera: entre el rango de valores de pHe de 8,171 a 12,348, tiene un comportamiento de tendencia lineal (R2= 0,99) con pendiente positiva. La segunda zona: con valores de pHe desde 12,423 a 12,474, no incrementan significativamente, a pesar de la excesiva adición de Ca(OH)2, como se puede apreciar, tienden a formar una línea horizontal paralela al eje de la [OH]; esto se explicaría porque se ha excedido el límite de solubilidad del Ca(OH)2 (Traynor et al., 2020), de tal manera que la adición en exceso del Ca(OH)2 , ha generado una mayor fuerza iónica de la solución (Fig 3) y como consecuencia la actividad de los iones OH-, no varían significativamente. Otra explicación, es debido al error alcalino en las mediciones de pH alto, cuyo efecto hace que la lectura de pHe sea más baja que el pHe real de la disolución, como consecuencia de altas [OH-], que sustituyen a los iones de hidrógenos alrededor del bulbo sensor del electrodo.
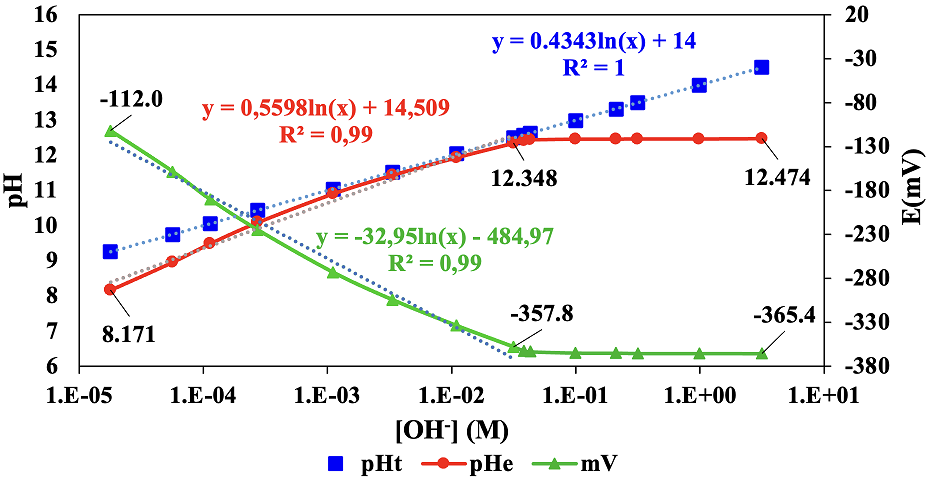
Figura 2 Comparaciones de los valores de pHt, pHe y E; en soluciones con determinadas concentraciones de [OH-], medidas a 27,5 °C ± 0,1 °C.
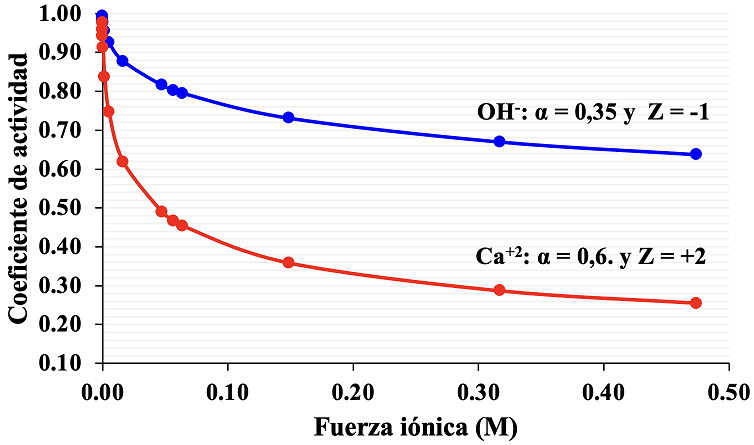
Figura 3 Variación de los coeficiente de actividad con la fuerza iónica, en las muestras de disoluciones de Ca(OH)2.
De acuerdo a la Figura 3, se puede observar que conforme aumenta la fuerza iónica en las disoluciones de Ca(OH)2, el coeficiente de actividad disminuye y así cuando μ tiende a cero, γ se aproxima a la unidad.
Evaluaciones de los potenciales y conductividad con respecto a los valores de pHe de las disoluciones de Ca(OH)2
De acuerdo a la Figura 2, la curva formada por los valores de E (mV), forma una imagen inversa, a la curva formada por los valores de pHe y ambas, presentan 2 secciones bien definidas: la primera sección comprendida desde -112,0 mV a -357,8 mV, presenta un comportamiento de tendencia lineal (R2=0,99) con pendiente negativa y la segunda sección que va desde -362,2 mV a -365,4 mV, tiende a ser paralela al eje de [OH] y así, su comportamiento es similar, a la segunda zona de la curva de valores de pHe, es decir que ante cualquier adición de Ca(OH)2; los valores en mV no incrementaron significativamente, tienden a mantenerse constantes, explicado por la baja solubilidad del Ca(OH)2 (Traynor et al., 2020) y a la mayor fuerza iónica (alta carga de atmósfera iónica) que modifica la capacidad de los iones para tomar parte de las reacciones.
De acuerdo a la Figura 4, la curva de las conductividades de las soluciones de Ca(OH)2, presenta tres zonas bien definidas, la primera con una leve pendiente entre los valores de 32,33 μS/cm y 63,11 μS/cm, debido a las bajas concentraciones de Ca(OH)2 en las muestras ensayadas (Kaewthong y Wattanachant , 2018). La segunda zona, entre 232,7 μS/cm y 6824 μS/cm, presenta un crecimiento brusco de su pendiente, con respecto a la primera sección, que va acorde con los incrementos de las [OH-] (Liu et al., 2019) [25], y la tercera sección que va desde 7192 μS/cm hasta 7548 μS/cm, tiende a mantenerse paralela al eje de [OH], así, cualquier adición de Ca(OH)2, no incrementa significativamente los valores de las conductividades, debido a la alta atmósfera iónica que modifica la conductividad de los iones de Ca+2 y OH-. Esta última sección guarda similar comportamiento con las segundas secciones de las curvas formadas por los valores de pHe y de mV frente a la [OH-].
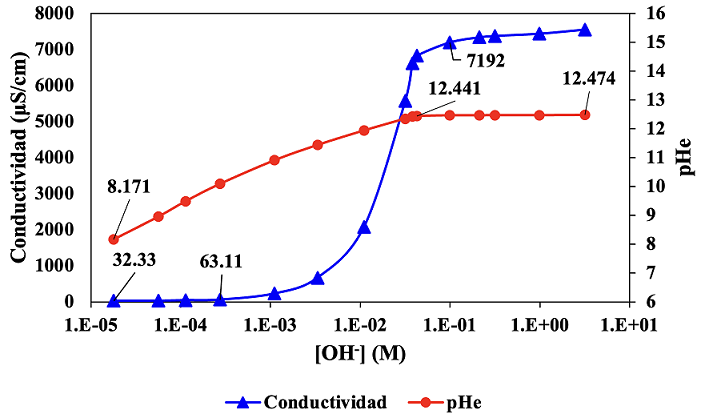
Figura 4 Variación de la conductividad y de los valores de pHe a determinadas concentraciones de [OH-], medidos a 27,5 °C ± 0,1 °C.
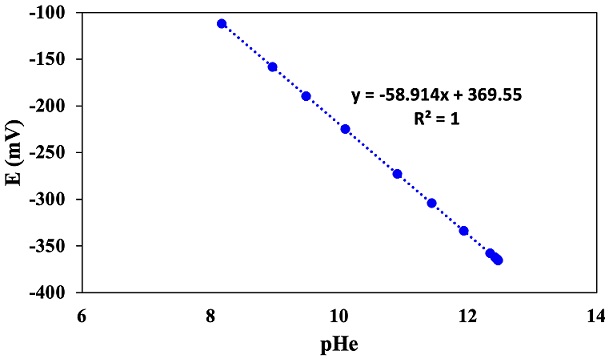
La Figura 5, muestra la recta (R2= 1), resultante de la gráfica semi logarítmica: pHe, frente a sus correspondientes E (mV), que se generaron al medir las respectivas muestras con determinadas concentraciones de Ca(OH)2. Su ecuación ajustada en función del pH (E = 369,55 - 58,914 pH) muestra una pendiente de 58,914, que es equivalente al factor de Nernst, con temperatura de ensayo de 27,5 °C ± 0,1 °C y es una pendiente que equivale a 99,58% de la pendiente teórica de la ecuación de Nernst (Ec.6) (Zhang et al., 2019). La pendiente resultante nos indica que, por cada unidad de pHe, le corresponde un cambio de 58,914 mV (Qin et al., 2015; Yoon et al., 2017).
Sugerencia didáctica que estima la masa de Ca(OH)2, para alcanzar el pH requerido
La autoionización del agua con su constante de equilibrio (producto iónico), se da de acuerdo a Ec. 11 y Ec. 12 respectivamente.
De acuerdo a Ec. 8, se tiene
Sin embargo, la fuerza iónica del agua pura (µ), es muy pequeña, por lo tanto:
De Ec. 8 y por definición de logaritmo se tiene:
Reemplazando Ec. (13) en Ec. (12) y despejando se tiene:
Por relación estequiométrica de Ec. (3): Ca(OH)2(s) ⇌ Ca2+ + 2OH- (ac)
Con la masa molar del hidróxido de calcio = 74.09 g/mol de Ca(OH)2, se deduce la constante (37.045).
Luego, la masa de hidróxido de calcio (g), en función del volumen de agua (L) y de pH, será:
El Ca(OH)2 se produce con un grado de pureza, por lo tanto, la Ec. (15) sería afectado por un factor de adición de (F), para compensar las impurezas del Ca(OH)2 industrial, y así, la ecuación completa sería:
Donde: W = Masa de Ca(OH)2, 37,045 = constante, pH = Valor esperado de pH; V = volumen de agua (L), F = Factor de adición de Ca(OH)2. Cuando el porcentaje de pureza del Ca(OH)2 es 90%, le corresponde un F de 1,1.
La Ec. (16), contribuye de manera directa, a realizar el cálculo teórico, de la masa de Ca(OH)2, para el ajuste del pH, en operaciones industriales de pequeña o gran escala, así como en controles ambientales; evitando sobrecostos y problemas de tipo operativos, reduciendo la generación de polvos y formación de sedimentos y de carbonatos en tuberías y reactores.
Conclusiones
Se validó experimentalmente la ecuación de Nernst, empleando muestras de disoluciones de Ca(OH)2 y su factor encontrado fue de 58,914, sugiere que es una pendiente que equivale al 99,58% de pendiente teórica de la ecuación de Nernst, que corresponde a un cambio de 58,914 mV/unidad de pHe.
Se brinda una sugerencia didáctica que permite encontrar la masa de Ca(OH)2 necesario, que se debe adicionar a un determinado volumen de agua, para alcanzar un pH requerido. Se pretende resolver el problema de gasto, por uso de exceso de hidróxido de calcio en la industria.
Los resultados de los ensayos experimentales, evidencian que el comportamiento de los valores de pHe, E y de su conductividad de las disoluciones, se ven afectados por la baja solubilidad del Ca(OH)2, por el error alcalino en las mediciones de las muestras con altos valores de pH y a la alta carga de atmósfera iónica.











 nueva página del texto (beta)
nueva página del texto (beta)