Introducción
Los organismos marinos bentónicos suelen encontrarse sobre distintas superficies en la zona litoral, y pueden ser sésiles o móviles (Underwood, 1979, 1981; Arias et al., 2006), haciéndolos dependientes de las condiciones ambientales (Fernández et al., 2014; Vassallo et al., 2014; Gaspar et al., 2017) y de las características particulares del sustrato. En el litoral, las rocas funcionan como el sitio principal de adhesión para muchos de esos organismos, la mayoría sésiles, como invertebrados y macroalgas (Fernández y Jiménez, 2006; Kokabi et al., 2016). Por otro lado, los organismos epizoicos utilizan a otros seres vivos como sustrato, en el que algunas especies aumentan sus oportunidades de asentamiento y supervivencia a través de la epibiosis (Sebens, 1991; Olabarria, 2000; Wahl, 2008, 2009).
Los epibiontes marinos se encuentran en diferentes grupos taxonómicos: briozoos, poríferos, hidroides, percebes, poliquetos, moluscos y algas (Wahl, 2008; Connelly y Turner, 2009; Harder, 2009). Por su parte, en los basibiontes (organismos que son sustrato) se incluyen animales como las ascidias, briozoos, corales, poríferos, moluscos y vertebrados, también en seres autótrofos, como pastos marinos y macroalgas (Connelly y Turner, 2009). Uno de los grupos animales con más especies basibiontes registradas son los moluscos con concha: bivalvos y gasterópodos (Wahl, 2008; Connelly y Turner, 2009).
Existen estudios que evalúan las relaciones entre organismos epibiontes y basibiontes, como macroalgas con crustáceos, corales vivos y moluscos (Mejía-Niño y Garzón-Ferreira, 2003; Lutaenko y Levenets, 2015; Jover et al., 2021). La mayoría de esos estudios son de carácter florístico y se han enfocado en inventariar las especies de epibiontes en diferentes sustratos vivos (Barrios et al., 2003; Connelly y Turner, 2009; Lutaenko y Levenets, 2015; Alfonso-Sánchez et al., 2020; Cabrera Guerrero y Jover Capote, 2022).
Los estudios relacionados con algas epizoicas, en México, son escasos, particularmente los que se enfocan en macroalgas; la mayor parte de ellos se han desarrollado en el Pacífico tropical mexicano (PTM) (Hernández-Vázquez y Valadez-González, 1998; Álvarez-Cerrillo et al., 2017; Quiroz-González et al., 2020; Aguilar-Estrada et al., 2022). En el caso del Atlántico mexicano los trabajos son escasos, destacando el de Sentíes et al. (1999), quienes registraron 37 taxones de macroalgas creciendo en caparazones de tortugas marinas.
Debido a su naturaleza geológica, el Atlántico mexicano (Golfo de México y Caribe mexicano) presenta costas mixtas entre zonas rocosas y playas arenosas (de la Lanza Espino et al., 2013). Dicha condición limita la existencia de sustratos líticos, por ello organismos bentónicos como los moluscos son utilizados a manera de sustrato por macroalgas u otros animales (Creed, 2000; López-Victoria et al., 2004; Lara-Lara et al., 2008; Connelly y Turner, 2009; Osorno-Arango y Sanjuan, 2009; Wahl, 2009; Levenets et al., 2010; Cabrera Guerrero y Jover Capote, 2019, 2022).
El conocimiento ficológico del Golfo de México y Caribe mexicano puede considerarse amplio; sin embargo, la mayoría de los estudios han estado orientados a conocer la flora adherida a las superficies rocosas dejando de lado a los sustratos vivos y en algunos casos, cuando estos son considerados, solo son una referencia circunstancial (Mateo-Cid et al., 2013; Acosta-Calderón et al., 2016; Quiroz-González et al., 2017, 2018; Landa-Cansigno et al., 2019; Mateo-Cid et al., 2024). Por lo tanto, los objetivos del presente trabajo fueron determinar la riqueza de especies y composición de macroalgas epizoicas para el Atlántico mexicano (Golfo de México y Caribe mexicano) a partir de los epibiontes documentados en el caracol Stramonita rustica (Lamarck, 1822) y mediante una búsqueda exhaustiva de literatura ficológica publicada para toda la región.
Materiales y Métodos
Revisión bibliográfica
Se llevó a cabo una búsqueda de literatura ficológica especializada desde 1992 hasta 2024, de tipo integradora (Guirao Goris, 2015), a partir del buscador de Google Académico (Google Scholar, 2024), empleando las siguientes palabras clave: algas epizoicas, epibiosis, epizoico, ficoflora y macroalgas, principalmente. Se tomaron en cuenta, entre otros, los siguientes criterios de exclusión: localidad de estudio, tipo de sustrato y tipo de basibionte.
A partir de las publicaciones consultadas, se obtuvo información para conformar un apéndice con el nombre científico de las macroalgas (epibionte), sustrato (basibionte), estado de la República Mexicana (Atlántico mexicano) donde se han registrado y la referencia bibliográfica correspondiente.
Área de estudio
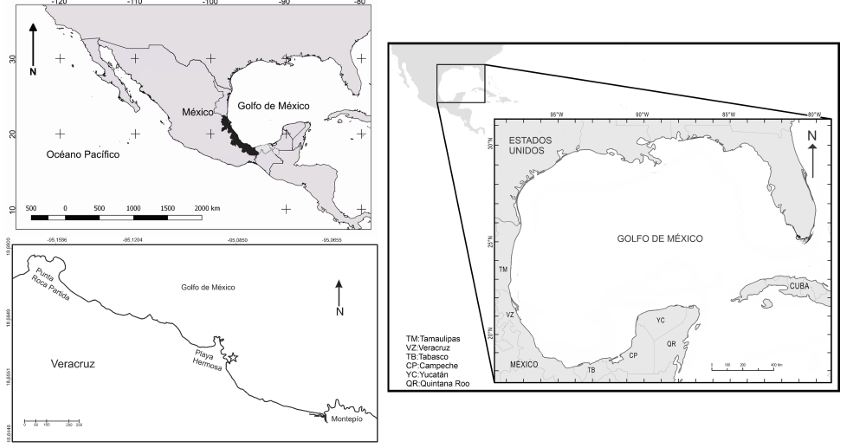
El sitio de recolección de los moluscos se ubica en las coordenadas geográficas 18°39'51''N y 95°7'48''O, en la localidad Playa Hermosa, Veracruz, México (Fig. 1). La playa se caracteriza por presentar una pendiente pronunciada y un derrame de lava solidificada (macizo expuesto) paralelo a la línea de costa, donde se forman pozas intermareales (García-López et al., 2017). En relación con el régimen de vientos y lluvias, presenta una estacionalidad climática que se caracteriza por tres periodos diferentes: secas, de febrero a mayo; lluvias, de junio a octubre, y frentes fríos anticiclónicos (nortes) de octubre a febrero, los cuales pueden sobreponerse relativamente (Day et al., 2005). Las mareas son diurnas con una amplitud media de 0.26 m (Sanvicente-Añorve et al., 2018).
Revisión de ejemplares
Los gasterópodos se capturaron en mayo de 2018 de forma manual con ayuda de una espátula (Truper ET-2FX, Truper®, Ciudad de México, México). Se colocaron en bolsas con agua de mar para ser transportados al Laboratorio de Protistas y Algas de la Facultad de Ciencias, de la Universidad Nacional Autónoma de México (UNAM). En el laboratorio, los ejemplares se preservaron en una solución de alcohol etílico al 70%. La identificación taxonómica se realizó con ayuda de literatura malacológica especializada para el Océano Atlántico (Abbott, 1974; García-Cubas y Reguero, 2004), utilizando los caracteres morfológicos de la concha (conquiliológicos), mismos que fueron observados en un microscopio estereoscópico (Nikon CLEDS, Nikon Corporation, Tokio, Japón). Los ejemplares identificados fueron depositados en la colección “Invertebrados Asociados a Macroalgas” del laboratorio de Ficología (Biodiversidad Marina) de la Facultad de Ciencias de la Universidad Nacional Autónoma de México.
Identificación de algas
Se tomaron los talos de macroalgas epibiontes de Stramonita rustica desde la base utilizando pinzas de relojero (STAINLEES-STEEL Factory, Ciudad de México, México). La identificación de las macroalgas a nivel específico se llevó a cabo mediante la observación de las características morfológicas de talos y cortes transversales realizados a mano alzada con navaja de doble filo (Gillete, The Gillete Company, Massachussets, Estados Unidos de América) en un microscopio estereoscópico (Nikon CLEDS, Nikon Corporation, Tokio, Japón). Posteriormente, los cortes y talos fueron montados con gelatina-glicerinada para elaborar preparaciones semipermanentes, que se analizaron en un microscopio óptico (OLYMPUS-CX23, Olympus corporation, Tokio, Japón). Para identificar taxonómicamente a las algas se utilizó la siguiente literatura ficológica especializada: Taylor (1960), Littler et al. (1989), Littler y Littler (2000); León-Álvarez et al. (2007; 2017), León-Álvarez y Núñez-Reséndiz (2012), Quiroz-González et al. (2017; 2018) y Pérez-Jiménez et al. (2020).
Después de revisar los ejemplares muestreados, se elaboró una lista de algas epizoicas encontradas sobre Stramonita rustica y de registros bibliográficos en distintos invertebrados, la cual se actualizó y arregló sistemáticamente a partir de la propuesta de AlgaeBase (Guiry y Guiry, 2024). Así mismo, se describieron los grupos morfofuncionales a los que pertenece cada especie de alga registrada, siguiendo la clasificación de Steneck y Dethier (1994), en el que se utiliza la siguiente terminología: filamento, folioso, foliosas corticadas, filamento corticado, coriáceas, calcáreas articuladas y costras. Se proporciona información referente a la estructura de fijación al sustrato observada para cada especie de macroalga registradas sobre S. rustica, así como para las que provienen de fuentes bibliográficas.
Resultados
Inventario de algas epizoicas en el Atlántico mexicano
En total hay 117 especies de algas epizoicas para el Atlántico mexicano, producto de la integración de los registros de las que crecen sobre las conchas de Stramonita rustica y de la revisión bibliográfica (Apéndice). Las especies registradas están distribuidas en 72 géneros, 40 familias, 21 órdenes y 3 divisiones. En Rhodophyta se documentaron 59 especies, 39 géneros y19 familias; para Chlorophyta 42 especies, 23 géneros y 15 familias; mientras que en Heterokontophyta-Phaeophyceae hubo16 especies, 10 géneros y 6 familias.
Como resultado de la revisión bibliográfica, se obtuvieron 61 publicaciones que reportan macroalgas de las costas del Atlántico mexicano (Veracruz, Tabasco, Campeche, Yucatán y Quintana Roo). Del total de publicaciones, 14 se referían a registros de macroalgas epizoicas (Mendoza-González y Mateo-Cid, 1992, 2000; Sentíes et al., 1999; Garduño-Solórzano et al., 2005; Cetz-Navarro et al., 2008; Mateo-Cid et al., 2013; Quiroz-González et al., 2017, 2018, 2021, 2024; Bastida-Zavala et al., 2000; Pérez-Jiménez et al., 2020; De la Cruz-Francisco et al., 2020).
En las fuentes bibliográficas se registraron 75 especies de macroalgas, creciendo sobre Stramonita rustica hubo 26 especies exclusivas y 16 compartidas entre los datos de la literatura y los obtenidos del molusco. Los principales géneros de algas fueron Ulva L. con seis especies, Cladophora Kützing y Chaetomorpha Kützing con cinco, Caulerpa J.V. Lamouroux, Ceramium Roth y Polysiphonia Greville con cuatro taxones cada uno (Apéndice). A nivel familia, Rhodomelaceae (16), Cladophoraceae (11) y Ceramiaceae (8) presentaron la mayor riqueza de especies. Los órdenes mejor representados en número de taxones fueron Ceramiales (32), Cladophorales (15) y Bryopsidales (15).
Macroalgas epizoicas de Stramonita rustica
Se registraron 42 especies de algas pertenecientes a 32 géneros, 22 familias y 13 órdenes de tres divisiones creciendo sobre la concha de S. rustica (Fig. 2). En cuanto al número de taxones por división, la mayor cantidad se encontró en Rhodophyta con 23, seguida de Chlorophyta (10) y Heterokontophyta-Phaeophyceae (9). Como parte de este listado, recientemente se describió Gelidium rodrigueziaeQuiroz-González & Ponce-Márquez (Quiroz-González et al., 2024), mientras que Siphonocladus rigidus M.A. Howe representa un registro nuevo para la ficoflora del estado de Veracruz (Fig. 3A, B).
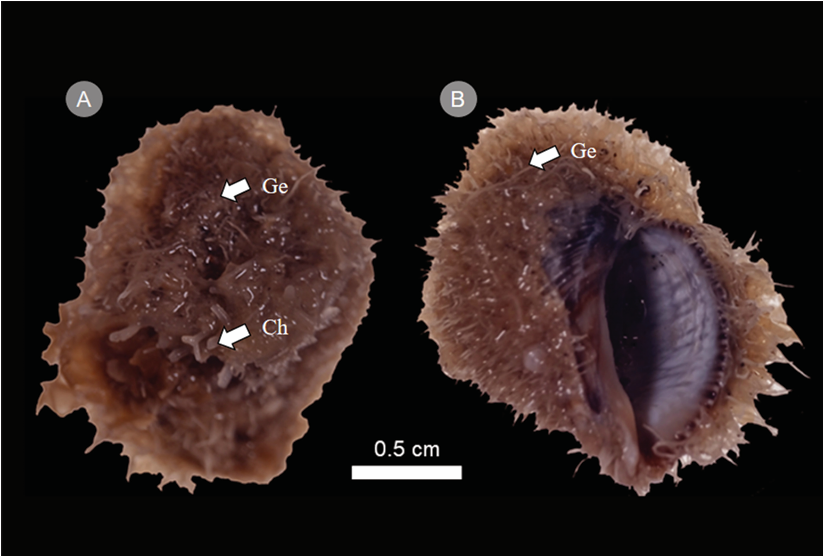
Figura 2: Stramonita rustica (Lamarck, 1822) cubiertas por algas epizoicas. A. vista dorsal, Ge (Gelidium J.V. Lamouroux), Ch (Chondria C. Agardh); B. vista ventral, Ge (Gelidium).
Riqueza de algas epizoicas por estado
En el apéndice se presentan las 26 localidades del Atlántico mexicano con reportes de macroalgas epizoicas. Tamaulipas fue el único estado en el que no se encontraron registros, mientras que en Yucatán únicamente se documentó una especie (Apéndice). Veracruz presentó el mayor número de algas epizoicas con 43 especies, seguido de Quintana Roo (36 spp.), Tabasco (12 spp.) y Campeche (2 spp.). Veinte especies fueron registradas en más de un estado y cuatro de ellas carecían de información referente a la localidad donde se encontraron. Ulva lactuca L. y U. rigida C. Agardh estuvieron presentes en 11 localidades (Apéndice).
Grupos morfofuncionales y estructuras de fijación
El grupo morfofuncional más frecuente fue el de los filamentos con 64 especies, seguido de los filamentos corticados (25 spp.) (Apéndice). Los rizoides dominaron el modo de adhesión al basibionte con 85 taxones y los discos basales con 25 (Apéndice). Cabe destacar que seis especies (Agissea simulans (Weber Bosse) Pestana, Lyra, Cassano & J.M.C. Nunes; Litophyllum sp.; Peyssonnelia Decaisne sp.; P. armorica (P. Crouan & H. Crouan) Weber Bosse; Pneophyllum fragile Kützing y Spongites yendoi (Foslie) Y.M. Chamberlain) segregan sustancias cementantes para la fijación al sustrato (costras) o presentan células basales de fijación.
Tipos de basibiontes
En la literatura consultada se registraron cinco grupos de basibiontes animales: tortugas marinas, crustáceos cirrípedos (balanos), corales pétreos, poríferos (esponjas) y moluscos; de estos últimos no se precisa si se trata de gasterópodos o bivalvos. Los basibiontes con la mayor riqueza de algas fueron los moluscos con 72 taxones, producto de la suma de los datos de Stramonita rustica, Crassostrea virginica (Gmelin, 1791) y los que se indicaron en este grupo (aunque no se especificó el taxón).
Las tortugas marinas en general, incluyendo Caretta caretta (Linnaeus, 1758) y Chelonia mydas (Linnaeus, 1758), ocuparon el segundo lugar en orden de importancia con 28 especies de algas epizoicas. En coral vivo se documentaron 14 taxones, cuatro en esponjas y uno en balanos. Por otra parte, cuatro especies (Centroceras clavulatum (C. Agardh) Montagne, Gelidium pusillum (Stackhouse) Le Jolis, Halimeda opuntia (L.) J.V. Lamouroux y Parviphycus trinitatensis (W.R. Taylor) M.J. Wynne) se documentaron creciendo en más de dos basibiontes, mientras que Gelidium americanum (W.R. Taylor) Santelices, G. pusillum y Pterocladiella calloglossoides (M. Howe) Santelices fueron registradas en tres epibiontes distintos (bivalvos, esponjas y gasterópodos). Por último, H. opuntia se documentó en cuatro basibiontes (Apéndice).
Descripción de un nuevo registro para Veracruz
Siphonocladus rigidus M. Howe. Phycological studies - I. New Chlorophyceae from Florida and the Bahamas. Bulletin of the Torrey Botanical Club 32: 241-252. 1905.
TIPO: ESTADOS UNIDOS DE AMÉRICA. Florida, Key West, s.f., M. Howe 1597 (holotipo: NY887544!) (Fig. 3 A, B).
Talos formando agregados, color verde pálido hasta 1.5 mm de alto. Talos erectos 200-480 µm de diámetro, uniseriados con escasa ramificación irregular o nula, células más largas que anchas.
Hábitat: creciendo sobre la concha de Stramonita rustica en la zona intermareal rocosa.
Ejemplar examinado: MÉXICO. Veracruz, municipio San Andrés Tuxtla, Playa Hermosa, 18.X.2018, L. Aguilar 908 (FCME).
Discusión
Los 117 taxones documentados en este estudio representan 15.5% de las 754 especies de algas que se han registrado para el Atlántico mexicano (Pedroche y Sentíes, 2020). Las algas epizoicas de la División Rhodophyta tuvieron el mayor número de especies (59 spp.), seguidas de Chlorophyta (42 spp.) y la menor cantidad corresponde a Heterokontophyta-Phaeophyceae (16 spp.). La proporción entre estos tres grupos algales coincidió con los registros previos en inventarios florísticos realizados en distintas localidades a lo largo de la costa del Golfo de México y Mar Caribe (Pedroche y Sentíes, 2020).
Las familias Cladophoraceae, Ceramiaceae y Rhodomelaceae fueron las que estuvieron mejor representadas en este estudio creciendo sobre sustratos animales. Esto coincidió con reportes previos de otros autores (Mateo-Cid et al., 1996, 2024; Quiroz-González et al., 2020), ya que poseen el mayor número de especies en inventarios ficoflorísticos. En estudios anteriores, los miembros de Ceramiaceae y Rhodomelaceae fueron registrados como epibiontes dominantes sobre diferentes sustratos; entre ellos, corales, macroalgas, pastos marinos y moluscos (Barrios et al., 2003; Mateo-Cid et al., 2013; Nava-Olvera et al., 2017; García-Redondo et al., 2019; Alfonso-Sánchez et al., 2020; Jover et al., 2021; Levenets et al., 2021), lo que explica que también sean abundantes en el presente estudio.
El estado con mayor diversidad de especies de algas en el Atlántico mexicano es Veracruz (De la Cruz-Francisco et al., 2020; Mateo-Cid et al., 2024). El presente trabajo adiciona un nuevo registro: Siphonocladus rigidus. Esta especie se ha documentado frecuentemente en la península de Yucatán, principalmente en localidades de Quintana Roo, como Puerto Morelos y Sian’Kaan, y en el Arrecife Alacranes en Yucatán (Huerta, 1961; Huerta et al., 1987; Aguilar-Rosas et al., 1989, 1992; Aguilar-Rosas, 1990). La ampliación de su intervalo de distribución puede relacionarse con la falta de muestreos en el sur de Veracruz, o a que son individuos de tallas pequeñas, por lo que pudieron pasar inadvertidos en trabajos anteriores. Además, se encontró Gelidium rodrigueziae, especie recientemente descrita con base en caracteres morfológicos y moleculares (Quiroz-González et al., 2024). Cabe mencionar que sus talos fueron abundantes en Stramonita rustica. Adicionalmente se registró en Tabasco creciendo en sustratos rocosos (Quiroz-González et al., 2024).
Quintana Roo es una región costera con gran diversidad de algas en México y el mundo (Cetz-Navarro et al., 2008). En el presente trabajo se reportan 34% de las especies de algas que posee este estado, y 4.9% con respecto a las que fueron documentadas previamente en el Atlántico mexicano (Pedroche y Sentíes, 2003; 2020).
Quiroz-González et al. (2020) y Levenets et al. (2021) han mencionado la importancia de realizar estudios en sustratos diferentes a las rocas como una estrategia para incrementar el conocimiento de la diversidad ficológica en distintas partes del mundo.
En cuanto a grupos morfofuncionales, la predominancia de los filamentos como epibiontes ha sido registrada por Quiroz-González et al. (2020) y Aguilar-Estrada et al. (2022), quienes señalaron que 43% de las algas epizoicas en el Pacífico tropical mexicano pertenecen precisamente a este, seguido de los filamentos corticados con 26%. La presencia mayoritaria de filamentos indica asociaciones algales constituidas principalmente por taxones anuales y oportunistas de rápido desarrollo, complementados por especies perennes, con sucesión tardía y desarrollo lento como son los filamentos corticados (Littler y Littler, 1980; Steneck y Dethier, 1994). Por otra parte, la presencia de filamentos en abundancia se ha relacionado con ambientes impactados por contaminación o con altos niveles de sedimentación, lo que podría dar cuenta de la situación de conservación ambiental en la que se encuentran las playas donde se registraron estas algas (Balata et al., 2011; López et al., 2017).
Respecto a las estructuras de fijación, predominan los rizoides con 79% de las especies seguidos de los discos de fijación con 18%. Esto también fue observado en otros estudios como el de Quiroz-González et al. (2020), donde estas mismas fueron las más frecuentes en algas que se desarrollan sobre las conchas del molusco Chiton articulatus G.B. Sowerby I, 1832. Por su parte, Cabrera Guerrero y Jover Capote (2022) encontraron una proporción de 58% para los rizoides y 33% para los discos de fijación sobre caparazones de distintas especies de crustáceos. Además, señalaron que los rizoides exhiben una serie de propiedades adaptativas, que incluyen crecimiento apical, ramificación frecuente, respuestas a los estímulos y plasticidad morfológica, que permiten a las algas aumentar el área de contacto superficie-sustrato y formar una fuerte unión.
Algunas de las especies de algas registradas en el presente trabajo han sido reconocidas previamente como epizoicas en otras regiones del Atlántico. Por ejemplo, Barrios et al. (2003) encontraron 11 taxones en común con este estudio para arrecifes de coral en Mochima, Venezuela, mientras que Mejía-Niño y Garzón-Ferreira (2003) coincidieron con cuatro taxones creciendo en corales en el Caribe colombiano. Por su parte, Alfonso-Sánchez et al. (2020) registraron 28 especies de algas en común creciendo en octocorales vivos de La Habana, Cuba. En este mismo país, Cabrera Guerrero y Jover Capote (2022) documentaron nueve especies de macroalgas epizoicas en crustáceos comunes con las encontradas en esta investigación. La similitud entre los taxones registrados en esos trabajos y el presente estudio puede deberse a las características propias de estas algas para colonizar fácilmente sustratos animales, como son talos simples y ciclos de vida cortos (Quiroz-González et al., 2020).
El valor que tienen los sustratos animales para las algas, particularmente el de los moluscos, ha sido estudiado por diferentes autores (McCook, 1996; Barrios et al., 2003; Gómez-Cubillos et al., 2019; Alfonso-Sánchez et al., 2020). Además, la presencia de algas epizoicas en todos los individuos revisados de Stramonita rustica indica que estos moluscos son excelentes basibiontes. Una de las características que podría favorecer esto es la morfología y en particular la escultura de la concha presente en la familia Muricidae, que está conformada por varias espinas y nodulaciones (Keen, 1971; Abbott, 1974). Esto se ha observado en otros géneros de moluscos bivalvos como Chama L. 1758 y Spondylus L. 1758, donde las ornamentaciones y espinas de la concha juegan un papel muy importante al inducir el asentamiento de epibiontes (Vance, 1978; Feifarek, 1987). Además de la porosidad de la superficie del periostraco, el cual favorece el establecimiento, adhesión y germinación de esporas de numerosas macroalgas (Pariona y Gil-Kodaka, 2011).
Las conchas son sustratos importantes para la unión de epibiontes, brindan refugio contra la depredación, el estrés físico o fisiológico y controlan el transporte de solutos y partículas en el ambiente béntico (Gutiérrez et al., 2003). Los estudios de epibiosis algal, particularmente aquellos donde los moluscos juegan el papel de basibiontes, deben seguirse desarrollando ya que estos invertebrados se consideran ingenieros de los ecosistemas y su ausencia o disminución en la disponibilidad de sus conchas podrían tener consecuencias importantes sobre los organismos que las utilizan como sustrato (Wahl, 2009).
Son pocos los estudios en los que se analizan datos referentes a la asociación entre algas y moluscos en otras partes del mundo. No obstante, existen algunas coincidencias con respecto a géneros y especies que también se documentaron en este estudio. Connelly y Turner (2009) trabajaron con el quitón Ceratozona squalida (C.B. Adams, 1845) en Florida, en el cual presentaron seis macroalgas en común. Martins et al. (2014) trabajaron con el gasterópodo Patella aspera (Röding, 1798) en las Azores, y registraron cuatro especies que también se reportaron en la presente investigación. Levenets et al. (2021) registraron dos taxones que coinciden con este trabajo. Si bien a nivel específico no se comparten muchas especies entre investigaciones previas y la presente, debido a las diferencias que existen entre distintas ecorregiones biogeográficas, a nivel genérico la representatividad es mayor. Por ejemplo, Polysiphonia Greville, Melanothamnus Bornet & Falkenberg, Ceramium Roth y Gelidium J. V. Lamouroux son géneros comunes en los estudios realizados hasta el momento, a pesar de sus diferencias biogeográficas. Así, a pesar de tratarse de sitios distantes se comparten taxones de macroalgas que suelen colonizar fácilmente sustratos vivos como los animales y que en muchas ocasiones tienen estrategias ecológicas que promueven su desarrollo sobre este tipo de sustratos (Aguilar-Estrada et al., 2022).
Conclusiones
Los resultados de este trabajo muestran que la riqueza ficológica de especies presente en sustratos animales es alta, particularmente en los moluscos. Además, contribuye al conocimiento de ficoflora registrada en Veracruz y el Atlántico mexicano con un enfoque complementario al resto de los inventarios florísticos que en su mayoría se concentran en sustratos rocosos. Con la información de algas epizoicas disponible hasta el momento, será posible generar estudios futuros que permitan resolver preguntas en torno a la ecología y biogeografía de estos organismos, así como la creación de programas de conservación y planes de manejo que contribuyan al mantenimiento de los recursos naturales, debido a que las algas epibiontes representan un elemento importante como estructuradoras de las comunidades marinas.











 nueva página del texto (beta)
nueva página del texto (beta)