Introducción
La degradación progresiva del medio ambiente, ocasionada por los efectos negativos de los productos químicos sintéticos y el cambio climático, pone en peligro la productividad de las plantas (Antoszewski, Mierek y Dąbrowska, 2022; Torres-Rodriguez, Reyes, Adame, Llerena y Hernandez, 2024a). La base de la producción agrícola sostenible es el funcionamiento saludable del ecosistema del suelo (Pinto et al., 2024).
La diversidad de microorganismos (bacterias, protozoos, algas, nematodos y hongos) mejora la calidad del suelo al mantener la productividad biológica (Silva et al., 2023; Xin, 2024). Los microorganismos en el suelo interactúan para formar una red trófica, la cual refleja el estado, la funcionalidad y la calidad del suelo (Pinto et al., 2024).
Los microorganismos son una herramienta importante en la agricultura para prevenir pérdidas en los cultivos debido a infecciones por fitopatógenos y para aumentar la producción de alimentos a nivel mundial. Estos disminuyen la necesidad de pesticidas y fertilizantes químicos, ofreciendo una opción sostenible y respetuosa con el medio ambiente (Guzmán-Guzmán et al., 2023).
El género de Trichoderma son hongos cosmopolitas con más de 375 especies descritas en la actualidad (Ahedo-Quero, Aquino, Ortiz y García, 2024). Las especies de Trichoderma desempeñan funciones cruciales en los agroecosistemas al actuar como biofertilizante, degradar la materia orgánica, control de fitopatógenos y participar en interacciones multitróficas junto con los insectos (Ismaiel, Lakshman, Jambhulkar y Roberts, 2024; Wang et al., 2024). Por lo tanto, las investigaciones se han orientado en estudiar y utilizar las propiedades de las especies de Trichoderma para su aplicación en la agricultura, la industria y la biorremediación ambiental (Ahedo-Quero et al., 2024).
Las bacterias presentes en el suelo desempeñan una función crucial en los ciclos biogeoquímicos (Meng et al., 2022). Además, son esenciales en la descomposición de la materia orgánica y la formación de humus, contribuyendo así a la fertilidad del suelo (Raza et al., 2023). Las bacterias del suelo de vida libre, conocidas comúnmente como rizobacterias promotoras del crecimiento de las plantas (PGPR), son beneficiosas para el desarrollo vegetal ya que tienen la capacidad de colonizar las raíces y promover el crecimiento de las plantas (Kálmán, Nagy, Berényi, Kiss y Posta, 2024). Algunas bacterias simbióticas, como las rizobios, establecen relaciones beneficiosas con las raíces de las plantas, facilitando la fijación biológica del nitrógeno (Sepp et al., 2023). Además, son importantes como agentes de control biológico de diferentes fitopatógenos (Torres-Rodriguez et al., 2022a; Benaissa, 2024).
Las especies de Pseudomonas spp. contribuyen significativamente a la calidad del suelo (Angelina, Papatheodorou, Demirtzoglou y Monokrousos, 2020; Medeiros et al., 2020). Estas bacterias se encuentran en la rizosfera, la región del suelo influenciada por las raíces de las plantas. Las especies de Pseudomonas spp. promueven el crecimiento y desarrollo de las plantas y protegen contra los fitopatógenos transmitidos por el suelo (He, Pantigoso, Wu y Vivanco, 2019). Además, producen compuestos antimicrobianos y enzimas, que les permiten inhibir el crecimiento de microorganismos fitopatógenos. Se ha demostrado que Pseudomonas spp. presentan potencial como agente de control biológico contra diversos fitopatógenos de plantas, incluido el género Phytophthora (Zohara, Akanda, Paul, Rahman y Islam, 2016).
En el suelo también, se encuentran diversos fitopatógenos que pueden infectar a las plantas cuando las condiciones ambientales son favorables, como los fitopatógenos Phytophthora spp., Fusarium spp. Rizoctonia spp., entre otros (Chen, Modi y Picot, 2023; Nikitin et al., 2023). Phytophthora es un fitopatógeno hemibiotrófico capaz de infectar una amplia gama de huéspedes (McCarthy y Fitzpatrick, 2017; Perrine-Walker, 2020).
A nivel mundial, la pudrición negra de la vaina, causada por especies de Phytophthora, es la enfermedad más grave del cacao. Esta enfermedad provoca pérdidas significativas de vainas, que pueden alcanzar hasta el 30%, y la mortalidad del 10% de los árboles cada año (Guest, 2007; Acebo-Guerrero, Hernández, Heydrich, El Jaziri y Hernández, 2012).
Muchas especies del género Fusarium son responsables de causar enfermedades en las plantas que provocan elevadas pérdidas económicas (Nikitin et al., 2023). Las especies de F. graminearum y F. oxysporum se encuentran entre los cinco fitopatógenos que más daño ocasionan en las plantas, junto con el carbón, la roya y la podredumbre parda y gris (Sharma y Marques, 2018). Incluso con la llegada de nuevos fungicidas sintéticos, estos hongos tienen un alto potencial de adaptación para infectar plantas agrícolas (Rampersad, 2020). Los principales síntomas de la fusariosis vegetal son el marchitamiento y la pudrición de raíces y semillas (Nikitin et al., 2023). F. oxysporum es el fitopatógeno más importante del género Fusarium en términos de agricultura y economía (Ploetz, 2006). Se conocen más de 150 formas especiales de F. oxysporum, cada uno con un conjunto de huéspedes específicos. F. oxysporum provoca marchitez en muchos cultivos, como la soja, el plátano, el algodón, el tomate, entre otros (Sun et al., 2023; Rodríguez-Yzquierdo et al., 2023; Abdelraheem, Zhu, Stetina y Zhang, 2024; Maqsood et al., 2024).
Por lo tanto, resulta fundamental poder identificar los microorganismos benéficos y fitopatógenos presentes en el suelo y en cultivo de interés agrícola, con el objetivo de implementar medidas de manejo adecuadas y efectivas. Este trabajo se centra en la caracterización morfológica y molecular de microorganismos presentes en el suelo agrícola, como especies de Trichoderma spp. y Pseudomonas spp., y su actividad antifúngica in vitro contra Fusarium oxysporum y Phytophthora palmivora, promoviendo estrategias agrícolas sostenibles.
Materiales y Métodos
Obtención de Muestra de Suelo para Microorganismos Benéficos
Se colectaron muestras de suelos asociados con cultivos de musáceas en el cantón Mocache ubicado a 01° 06’ 24” S, 79° 29’ 70” O a una altitud de 75 m de altitud. Las muestras de suelo se recolectaron utilizando una barrena de 10 cm de diámetro. La porción central de los 2 cm superiores de las muestras se extrajo con una cuchara estéril. Las muestras se colocaron en fundas de polietileno estériles y se transportaron al laboratorio de Microbiología de la Universidad Técnica Estatal de Quevedo.
Aislamiento de Microorganismo Benéficos: Pseudomonas spp. y Trichoderma spp.
Se tomó 1 g de muestra de suelo y se suspendió en 9 mL de agua estéril. Luego, se realizaron diluciones en serie hasta alcanzar una concentración de 10-6. De cada dilución intermedia, se añadió 1 mL a 15 mL de medios de cultivo King B (peptona 10 g L-1, sulfato de magnesio 1.5 g L-1 y fosfato de potasio dibásico 1.5 g L-1 y Agar 15 g L-1) para Pseudomonas spp y agar papa dextrosa (PDA, Difco 39 g L-1) para Trichoderma spp. Después de 48 h de incubación a 28 °C se seleccionaron los aislamientos de cada género en base a la morfología de las colonias y observaciones microscópicas. Posteriormente cada aislamiento fue purificado y almacenado en glicerol al 20% a -40 grados centígrados.
Identificación Morfológica de Pseudomonas spp. y Trichoderma spp.
Los aislados bacterianos fueron cultivados en King B a 28 °C durante 48 horas. Se identificaron basándose en las siguientes características morfológicas: color del micelio, forma, borde y elevación de las colonias, utilizando un microscopio estereoscopio (Olympus modelo S2) (Sousa, Machado, Nicolau y Pereira, 2013). Se determinó la producción de catalasa, mediante un frotis de cada cepa bacteriana en un portaobjetos de vidrio. Se añadió una gota de peróxido de hidrógeno (H2O2) y se observó la formación de burbujas, lo cual indica un resultado positivo. Para la prueba de oxidasa, se realizó un frotis de cada cepa bacteriana en un portaobjetos de vidrio. Se preparó el kit de “Oxidase Test Stick” en un microtubo con agua destilada. Luego, se añadieron 10 μL de la preparación a cada muestra y se observó la aparición de un color azul-púrpura para determinar si la oxidasa era positiva. Basándose en el cambio de color, las bacterias se distinguieron como oxidasa positiva (azul-púrpura) u oxidasa negativa (sin cambio de color). Además, se realizó la tinción de Gram siguiendo el protocolo estándar (Mahima, Amridha y Senan, 2020), utilizando cristal violeta, yodo de Lugol, alcohol acetona y safranina.
Para los aislamientos de Trichoderma spp., se cultivaron en placas de agar dextrosa papa (PDA) a 25 °C durante 7 días. Se realizaron observaciones regulares de la colonia bajo un microscopio óptico (Boeco, Germany) y se registraron características como el color y la forma de la colonia, la textura y la dispersión, el tamaño de los conidios y la formación de clamidosporas y conidióforos, siguiendo los criterios de Asis et al. (2021).
Aislamiento de Fitopatógenos del Suelo Fusarium spp. y Phytophthora spp.
Se recolectaron raíces de plantas de tomate que mostraban síntomas de fusariosis. El muestreo fue dirigido en un transecto en banda, seleccionando raíces de plantas que exhibían marchitez, ahorcamiento del tallo y amarillamiento de hojas. Para el aislamiento de Phytophthora spp. se tomaron muestras de frutos de cacao que mostraban síntomas de infección por Phytophthora spp. (lesiones firmes de color marrón/negro en las vainas) (Torres-Rodriguez, Reyes, Quiñones y Hernández, 2022b).
Las muestras se depositaron en fundas de plástico estériles, luego se colocaron en un contenedor y fueron trasladadas al laboratorio de Microbiología de la Universidad Técnica Estatal de Quevedo para su procesamiento. Las raíces y vainas sintomáticos de Fusarium spp. y Phytophthora spp respectivamente, se procesaron cortando piezas (5 mm) de los márgenes de las lesiones que comprenden tejido sano y necrótico, desinfectando la superficie sumergiéndolas en etanol al 70% durante 20 s y secando al aire en papel de filtro esterilizado en autoclave. A continuación, se sembraron en placas Petri que contenían medio agar papa dextrosa (PDA, Difco 39 g L-1) y medio V8 (jugo de verduras V8 un 20%, agar 20 g L-1 y agua destilada 1 L), se incubaron a 28 °C por 7 días. Las colonias resultantes se purificaron en medios PDA y V8 y posteriormente se almacenaron en tubos inclinados a 4 grados centígrados.
Identificación Morfológica de Fusarium spp. y Phytophthora spp.
Se identificaron macroscópicamente los aislamientos de Fusarium spp. evaluando el color de la colonia, tipo de micelio y la categoría de esporulación. Las características microscópicas, como macroconidios, microconidios y clamidosporas, se determinaron utilizando un microscopio Olympus con un aumento de 40×. La identificación se llevó a cabo siguiendo las claves taxonómicas descritas por Summerell, Salleh y Leslie (2003). La identificación de Phytophthora spp. se llevó a cabo evaluando la morfología de la colonia en placas de V8 incubadas a 25 °C durante 5 días. Se determinó la morfología de la colonia, como la forma, textura y color de las colonias y la categoría de esporulación. Las características de las estructuras como, la forma de los esporangios, las clamidosporas, los pedicelos, las papilas y el esporangióforo, utilizando un microscopio Olympus a un aumento de 40× (Drenth y Sendall, 2001).
Identificación Molecular de Pseudomonas spp.
El ADN se extrajo siguiendo la metodología modificada de Ochoa, Hernández, Latisnere, de la-Luz y Larralde (2007). La amplificación por PCR de la secuencia del gen 16S ARNr de los aislados BMOJ1 y BMOJ2 se llevó a cabo utilizando los cebadores 27f (5′-AGAGTTTGATCCTGGCTCAG-3′) y 1492r (5′-GGTTACCTTGTTACGACTT-3′). Las amplificaciones se realizaron en un termociclador con un periodo de desnaturalización a 95 °C durante.5 min seguido de 30 ciclos a 95 °C durante 1 min, 55 °C durante 30 s y 72 °C durante 90 s. Finalmente, una etapa de elongación a 72 °C durante 10 min. Las secuencias obtenidas se emplearon para realizar una búsqueda de homología de las secuencias 16S mediante el uso de BlastN, comparándolas con las secuencias disponibles en las bases de datos del NCBI.
Identificación Molecular de los Hongos (Fusarium spp., Phytophthora spp. y Trichoderma spp.)
Se realizó la identificación de los fitopatógenos (Fusarium spp. y Phytophthora spp.) (FMJ1 y PMJ1). La extracción de ADN de Fusarium spp., Phytophthora spp. y Trichoderma spp. se realizó de acuerdo con la metodología modificada de Ochoa et al., (2007). La región ITS1-5.8S-ITS2 del rDNA se amplificó utilizando los cebadores ITS1 (5’ TCCGTAGGTGAACCCTGCGG 3’) e ITS4 (5’ TCCTCCGCTTATTGATATGC 3’). Las reacciones de amplificación para Fusarium spp. incluyeron un período de desnaturalización inicial de 3 minutos a 95 °C, seguido de 30 ciclos que consistieron en una desnaturalización a 95 °C durante 1 minuto, una alineación a 50 °C durante 30 segundos y una extensión a 72 °C durante 1 minuto, concluyendo con una extensión final a 72 °C durante 10 minutos. El programa de PCR para Phytophthora spp. inició con una desnaturalización a 98 °C durante 30 s, seguido de 35 ciclos a 98 °C durante 10 s, 54 °C durante 20 s y 72 °C durante 35 s y un paso de extensión final a 72 ºC durante 10 min. El programa de PCR para Trichoderma spp. inició con una desnaturalización a 95 °C durante 4 min, seguida de 35 ciclos a 95 °C durante 1 min, 58 °C durante 1 min y 72 °C durante 2 min y una extensión final a 72 °C durante 10 min. Las secuencias amplificadas se compararon con la base de datos GenBank del NCBI mediante el alineamiento local de secuencias nucleotídicas utilizando el programa BLAST.
Análisis Filogenético
El análisis filogenético se realizó utilizando el programa MEGA 12 (Molecular Evolutionary Genetic Analysis) (Kumar, Stecher, Knyaz y Tamura, 2018). Para la construcción del árbol filogenético, se empleó la secuencia ITS obtenida de Genewiz y secuencias de otras especies disponibles en el NCBI. Las secuencias fueron seleccionadas a través de una búsqueda de secuencias nucleotídicas homólogas a la secuencia ITS obtenida.
Las secuencias se alinearon utilizando MUSCLE (Edgar, 2004) por medio del programa Gblocks (Talavera y Castresana, 2007) dentro de la plataforma Phylogeny.fr (Dereeper et al., 2008). Se excluyeron los segmentos que tenían posiciones variables o gaps, eligiendo los bloques conservados a partir del alineamiento múltiple. Con las secuencias curadas se determinó el modelo de evolución de ADN de mejor ajuste con el programa MEGA 7.0.21 (Kumar et al., 2018). El análisis filogenético de Fusarium spp. y Phytophthora spp. se realizó mediante el método de máxima parsimonia (MP), utilizando el modelo Kimura-2 parameter (Tamura, Stecher y Kumar, 2021) y distribución Gama. El análisis filogenético de Trichoderma spp. se realizó por el método de unión de vecinos (NJ), usando el modelo Jukes-Cantor (Tamura, Stecher y Kumar, 2021) y distribución Gama. Para Pseudomonas spp. se utilizó el método de unión de vecinos (NJ), usando el modelo Hasegawa-Kishino-Yano (Tamura, Stecher y Kumar, 2021) y distribución Gama. Para todos los análisis filogenéticos se utilizó 10 000 repeticiones (bootstrap).
Actividad Antifúngica in vitro de Pseudomonas spp. y Trichoderma spp. contra Fusarium spp. y Phytophthora spp.
La actividad antifúngica in vitro se determinó en placas de Petri mediante el método de cultivo dual. Un disco de 5 mm de cada aislado de Pseudomonas spp. o Trichoderma spp. se colocó a 10 mm del borde de las placas Petri con medio PDA. En el centro de cada placa, se ubicó un disco de 5 mm de Fusarium sp. o Phytophthora sp. procedente de un cultivo de 5 días en PDA y V8, respectivamente.
Un grupo de placas Petri se inoculó únicamente con Fusarium sp. y Phytophthora sp. (control).
Las placas se incubaron a 28 °C durante 7 días. El porcentaje de inhibición del crecimiento radial (PICR, %) del hongo se determinó utilizando la fórmula: PICR: [(R1-R2)/R1]×100% donde R1 es el crecimiento radial del hongo en la placa de control y R2 es el crecimiento del hongo en dirección hacia los microorganismos benéficos (Azadeh, Sariah y Wong, 2010). Se realizaron cinco repeticiones por tratamiento y el experimento se repitió dos veces.
Análisis Estadístico
Para la actividad antifúngica in vitro se determinó la normalidad de los datos mediante la prueba de Shapiro-Wilk y la homogeneidad de las varianzas mediante la prueba de Bartlett. Los datos se analizaron mediante análisis de varianza unidireccional (ANOVA) utilizando el software STATISTICA 10.0 (StatSoft, 2011) y se utilizó la prueba de comparación múltiple de media de Tukey (P < 0.05).
Resultados y Discusión
El aislamiento BMOJ1 (P. aeruginosa) presentó colonias de color blanco con una morfología irregular, elevación plana y borde ondulado. BMOJ2 (P. fluorescens) presentó colonias de color verde amarillo, con una morfología irregular, elevación convexa y borde lobulado (Cuadro 1). En cuanto a la tinción de Gram, ambos aislados fueron Gram negativos, lo que indica la presencia de una pared celular compuesta principalmente por una delgada capa de peptidoglicano y una membrana externa rica en lipopolisacáridos. Las pruebas bioquímicas revelaron que ambos aislados fueron positivos para las enzimas catalasa, los cuales presentaron una reacción abundante. Respecto a la oxidasa los aislados presentaron una reacción moderada (+) (Cuadro 1).
Table 1: Morphological and biochemical characteristics of Pseudomonas spp.
| Aislado | Zona | Color | Colonia | Elevación | Forma de borde | Tinción Gram | Catalasa | Oxidasa |
| BMOJ1 | Mocache | Verde azulado | Irregular | Plana | Ondulada | Negativa | ++ | + |
| BMOJ2 | Mocache | Verde amarillento | Irregular | Convexa | Lobulado | Negativa | ++ | + |
Reacción abundante = ++; Reacción moderada =+.
Abundant reaction = ++; Moderate reaction = +.
Las diferencias en la morfología de las colonias pueden estar relacionadas con variaciones en la composición de la membrana celular (Tavares et al., 2020; De Benedetti, Fisher y Mobashery, 2021). Manasa, Reddy, Triveni y Manasa (2017), reportaron a Pseudomonas con coloraciones verde-amarillentas y con pigmentación verde-claro hasta blanco apagado sin pigmentación, además de mostrar una variedad de formas y elevaciones. También, Soesanto, Mugiastuti y Rahayuniati (2011) reportaron aislamiento de Pseudomonas que presentaba color amarillo verdoso, elevación convexa y circular, resultados en correspondencia a este trabajo.
La acción principal que llevan a cabo las células bajo estrés oxidativo es la eliminación de agentes oxidantes (Romsang, Dubbs y Mongkolsuk, 2016). La desintoxicación de especies reactivas de oxígeno se realiza mediante enzimas especializadas, como la catalasa, el superóxido dismutasa, la peroxidasa, que catalizan la conversión de estas especies en sustancias menos tóxicas. Son enzimas esenciales para la supervivencia de las bacterias bajo estrés oxidativo (Da Cruz-Nizer et al., 2021). La presencia de catalasa sugiere que ambas bacterias pueden descomponer especies reactivas de oxígeno, protegiéndose así del estrés oxidativo. La actividad oxidasa indica la presencia de citocromo c oxidasa, implicada en la cadena de transporte de electrones y la producción de energía (Kadenbach, Ramzan, Wen y Vogt, 2010; Brischigliaro y Zeviani, 2021). Estos resultados muestran la diversidad fenotípica entre los aislados bacterianos de la misma región. Las diferencias en las características morfológicas y bioquímicas pueden influir en su adaptación al entorno.
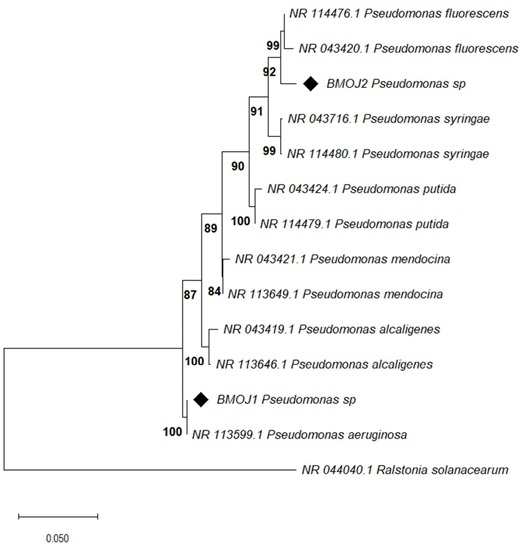
En la Figura 1 se presenta el árbol filogenético de los aislamientos de basados en las secuencias de ARNr 16S, se utilizó Ralstonia solanacearum (NR_044040.1) como grupo externo (outgroup) para enraizar el árbol filogenético. Las secuencias identificadas como BMOJ1 y BMOJ2, indicadas por diamantes negros en el árbol, mostraron relaciones taxonómicas dentro del género Pseudomonas. La secuencia BMOJ1 se agrupa con P. aeruginosa formando un clado con un valor de soporte bootstrap del 100%. Este agrupamiento sugiere que BMOJ1 está estrechamente relacionada con estas especies. La secuencia BMOJ2 se agrupa con P. fluorescens (NR_043420.1 y NR_114476.1). Este resultado sugiere que BMOJ2 está estrechamente relacionada con P. fluorescens, la cual es una especie reconocida como agente de control biológico y promotora del crecimiento de las plantas. Hernández-Montiel et al. (2020) evaluaron variables morfométricas, rendimiento y otras variables en plantas de pimiento morrón variedad ‘California Wonder y reportan que los resultados indicaron que las bacterias incrementaron todos las variables morfométricas y de productividad y que, el uso de Pseudomonas putida como un bio-fertilizante puede ser importante en la producción de especies hortícolas como el pimiento morrón.
La identificación molecular de las especies es muy importante en la agricultura y el control biológico, ya que permite una gestión precisa y eficiente de los cultivos y fitopatógenos. Mediante técnicas de secuenciación de ADN, se puede identificar tanto a los fitopatógenos como a los agentes de control biológico, facilitando la implementación de estrategias de control biológico efectivas y sostenibles (Gerace et al., 2022; Torres-Rodriguez et al., 2024b).
El Cuadro 2 presenta las características morfológicas de dos aislados de Trichoderma spp.: TC191 y TCUE16. El aislado TC191 mostró un color verde con una textura algodonosa, mientras que TCUE16 presentó un color verde olivo con una textura granular. Estas diferencias en color y textura son indicativas de la variabilidad fenotípica dentro del género Trichoderma y pueden reflejar diferencias en las condiciones de crecimiento o en la composición genética de los aislados (Martínez, Infante y Peteira, 2015).
Table 2: Morphological characteristics of Trichoderma spp.
| Cepa | CC | Textura | FC | Dispersión | TC | FCS | FCF |
| µm | |||||||
| TC191 | Verde | Algodonosa | Redonda con discos concéntricos | Sin dispersión | 2.7 | No | Ramificado |
| TCUE16 | Verde olivo | Granular | Filamentosa | Pequeñas colonias alrededor de la placa | 3.4 | No | Ramificado |
CC = color de la colonia; FC = forma de la colonia; TC = tamaño de conidios; FCS = formación de clamidosporas; FCF = forma de los conidióforos.
CC = colony color; FC = colony shape; TC = conidia size; FCS = chlamydospore formation; FCF = shape of the conidiophores.
La forma de la colonia de TC191 fue redonda con discos concéntricos, mientras que TCUE16 presentó forma filamentosa. El aislado TC191 no mostró dispersión, lo que podría implicar una menor capacidad de propagación en el entorno. En contraste, TCUE16 formó pequeñas colonias alrededor de la placa, indicando una capacidad dispersiva mayor. La alta capacidad de dispersión de Trichoderma spp. es crucial para el biocontrol, ya que mejora su eficacia en el control de fitopatógenos. La capacidad de dispersión le permite a Trichoderma spp. colonizar rápidamente grandes áreas y competir eficazmente contra fitopatógenos, facilitando la reducción de enfermedades en plantas y disminuyendo la dependencia de pesticidas químicos (Manzar et al., 2022; Guzmán-Guzmán et al., 2023). El tamaño de los conidios fue de 2.7 µm en TC191 y de 3.4 µm en TCUE16. Ambos aislamientos presentaron conidióforos ramificados, una característica típica de especies de Trichoderma, que facilita la producción de esporas y la colonización del sustrato (Mukhopadhyay y Kumar, 2020; Cao et al., 2023).
La capacidad de Trichoderma spp. para crecer rápidamente y adaptarse a diversos sustratos ha facilitado su aislamiento en una variedad de suelos en todo el mundo (Al-Ani, 2018; Bononi, Chiaramonte, Pansa, Moitinho y Melo, 2020). Se ha demostrado en suelos asociados a los cultivos de musáceas la presencia de especies de Trichoderma (Correa-Delgado, Brito, Jaizme y Laich, 2024). Asis et al. (2021) reportaron resultados similares en especies de T. harzianum a las obtenidas en este trabajo, como micelio de color amarillento a verde, tamaño de conidios entre 1.0 y 3.0 μm y conidióforos ramificados. También, Silva et al. (2022), reportaron que especies de Trichoderma presentaban coloración color verde oscuro y la formación de conidios ovoides con un tamaño promedio de 3.60 µm. Sebumpan et al. (2022) reportaron la formación de anillos concéntricos y una textura que varió desde algodonosa a granular en especies de Trichoderma asperellum.
La comparación de toda la región ITS (ITS1, 5.8S rDNA e ITS4) de los aislados de Trichoderma spp. TCUE16 y TC191 con las previamente depositadas en el GenBank reveló que la similitud genética más cercana (99.61 y 100%) de la secuencia ITS generada era con Trichoderma atroviride y Trichoderma harzianum, respectivamente.
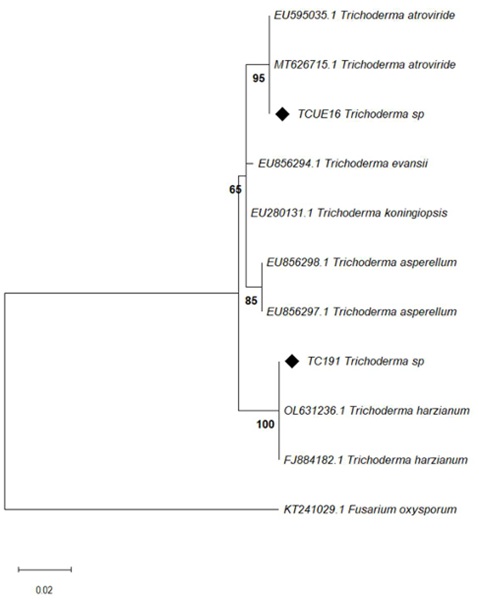
Las secuencias de Trichoderma spp. (indicada por un diamante negro) se analiza en dos posiciones diferentes dentro del árbol filogenético, representando a los aislados TCUE16 y TC191. La secuencia de TCUE16 se agrupa con Trichoderma atroviride (EU595035.1 y MT626715.1) con un soporte bootstrap del 95%. Este alto valor de bootstrap indica una fuerte relación evolutiva entre TCUE16 y Trichoderma atroviride, sugiriendo que comparten un ancestro común reciente. Trichoderma atroviride, es un agente de control biológico, que presenta capacidad de antagonismo contra diversos fitopatógenos (Liu et al., 2023) (Figura 2).
La secuencia de TC191 se agrupa en un clado con T. harzianum (OL631236.1 y FJ884182.1) con un soporte bootstrap del 100%. Este valor alto de bootstrap proporciona evidencia de una relación evolutiva muy cercana entre TC191 y T. harzianum. T. harzianum es otra especie reconocida por su eficacia en el control de fitopatógenos y su uso extensivo en prácticas agrícolas (Swathy, Nisha y Vivekanandhan, 2024) (Figura 2). En la actualidad las secuencias ITS son una opción para la identificación de aislados de Trichoderma a nivel de especie (Almaghasla, El-Ganainy y Ismail, 2023; Chan et al., 2023).
En la caracterización de Fusarium spp., se observaron diferencias en el tipo de micelio, el color de la colonia y la esporulación entre los distintos aislados, lo que sugiere variabilidad fenotípica. El aislado FMJ1 mostró una esporulación abundante (+++), con un micelio aéreo abundante y flocoso. Este tipo de crecimiento sugiere una cepa altamente virulenta y con capacidad de dispersión significativa, debido a la densidad y la estructura del micelio (Wang et al., 2021; Ajmal, Hussain, Ali, Chen y Lin, 2022; Yang et al., 2024). El aislado FMJ3, por otro lado, presentó una esporulación moderada (+) y un micelio algodonoso blanquecino con un centro café claro. Los aislados FMJ5 y FMJ6 presentaron una esporulación buena (++) y un micelio aéreo disperso (Cuadro 3). La variabilidad observada en los aislamientos de Fusarium spp. es consistente con la literatura, que indica una alta diversidad morfológica dentro de este género (Summerell et al., 2003). Estas diferencias fenotípicas son importantes para entender el comportamiento de las cepas y su posible impacto en los cultivos afectados.
Table 3: Macroscopic characterization of Fusarium spp.
| Aislado | Color de la colonia | Esporulación | Tipo de micelio |
| FMJ1 | Rosa | +++ | Micelio aéreo abundante y flocoso, color blanquecino y centro rosado |
| FMJ3 | Crema | + | Micelio aéreo escaso algodonoso, blanquecino y centro café claro |
| FMJ5 | Amarillo pálido | ++ | Micelio aéreo disperso y flocoso, color crema |
| FMJ6 | Amarillo pálido | ++ | Micelio aéreo disperso, color blanquecino |
Categoría de esporulación: abundante +++; bueno = ++; moderado = +.
Sporulation category: abundant +++; good = ++; moderate = +.
Las cuatro cepas evidenciaron características propias de especies de Fusarium, la coloración del micelio puede variar entre tonos de amarillo, crema, rosa, entre otros (Summerell et al., 2003; Vignesh, Rajamohan, Balabaskar y Anandan, 2021). Esta variabilidad en el color puede deberse a factores genéticos que regulan la producción de pigmentos y a factores ambientales como la temperatura, la luz, la disponibilidad de nutrientes y el pH del medio de cultivo (Rahman et al., 2021; Nikitin et al., 2023). Estos resultados son semejantes a los reportados por Chopada, Singh y Chandulal (2015) en su investigación, donde los aislados produjeron un crecimiento moderado, algodonoso, con pigmentación blanca, amarilla, rosa claro, rosa oscuro, naranja y púrpura anaranjada. Un micelio abundante podría indicar un mayor crecimiento del hongo y su capacidad para colonizar el tejido vegetal (Summerell et al., 2003; Yang et al., 2024).
El análisis de las estructuras microscópicas de los aislamientos de Fusarium spp. reveló diferencias en la morfología de macroconidias, microconidias y clamidosporas (Cuadro 4). Las macroconidias presentaron diferencias en cuanto a su forma y número de septos. El aislamiento FMJ1 mostró macroconidias semicurvas con 4-5 septos, mientras que FMJ2 y FMJ4 presentaron macroconidias rectas con 3 y 4-5 septos, respectivamente. Por otro lado, FMJ3 exhibió macroconidias curveadas con 3-4 septos.
Table 4: Characteristics of the microscopic structures of Fusarium spp.
| Aislado | Macroconidia | Clamidosporas | |||||
| Forma | Septo | Célula apical | Célula basal | Forma | Septo | ||
| FMJ1 | Semicurva | 4-5 | Romo | Forma de pie | Fusiforme | 0-1 | Pareada, pared lisa |
| FMJ2 | Recta | 3 | Romo | Forma de pie | Reniforme | 0 | Pareada, pared lisa |
| FMJ3 | Curveada | 3-4 | Papilado | Forma de pie | Fusiforme | 0-1 | Pareada, pared lisa |
| FMJ4 | Recta | 4-5 | Romo | Forma de pie | Fusiforme | 0-1 | Pareada, pared lisa |
En cuanto a las células apicales y basales de las macroconidias, todos los aislamientos, excepto FMJ3, mostraron una célula apical romo. Todas las células basales de los aislamientos presentaron forma de pie, lo que es característico de Fusarium spp. Las microconidias también mostraron variaciones significativas. FMJ1 y FMJ3 presentaron microconidias fusiformes, mientras que FMJ2 mostró microconidias reniformes. Las clamidosporas en todos los aislamientos fueron observadas en pares y con paredes lisas (Cuadro 4).
Los estudios morfológicos, ayudan en la clasificación taxonómica y la identificación de especies de Fusarium (Harish et al., 2023). Los macroconidios presentaron de tres a cinco septos con forma curva, semicurva y recta, resultados similares a los reportados por Tilahun, Abate, Tilahun y Taye (2024). Nawade, Talaviya, Vyas, Jadeja y Golakiya (2017) observó que las microconidias eran pequeñas, de una a dos células con forma oval a reniforme y oval a oblonga con ligera curvatura, resultados en correspondencia a este trabajo. La presencia de clamidosporas formando grupos o individuales, es una característica común de especies de Fusarium (Garibaldi, Gilardi, Ortu y Gullino, 2016).
Ramesha y Naik (2017) reportaron diferencias morfológicas en cuanto a la forma de las micro y macroconidias, así como variación en el número de septos en cada cepa, resultados en correspondencia a los de este trabajo. Las diferencias morfológicas de los aislados en la forma y el número de septos de las macroconidias, también fueron reportados por Harish et al. (2023).
Las clamidosporas de Fusarium son cruciales para la supervivencia del hongo en condiciones ambientales adversas. Estas esporas permiten que el hongo permanezca viable en el suelo incluso sin un huésped. Cuando las condiciones mejoran, las clamidosporas actúan como inóculos principales, iniciando infecciones en las plantas (Hou, Hsu, Wang, Lai y Chen, 2020; Bahadur, 2021). Por tanto, las enfermedades por Fusarium spp. se encuentran entre las más difíciles de controlar.
Las diferencias morfológicas en los aislamientos de Fusarium, especialmente en la forma y el número de septos de macroconidias y microconidias, son características fundamentales que influyen en su identificación.
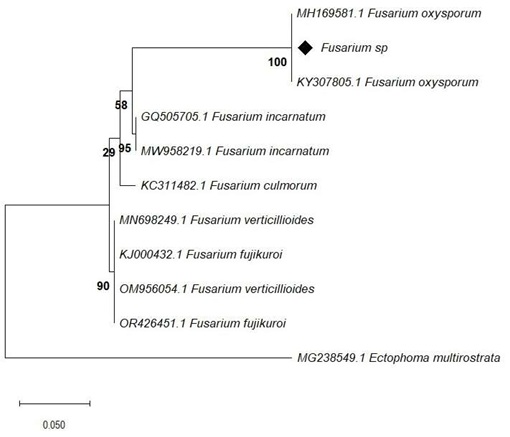
La comparación de toda la región ITS (ITS1, 5.8S rDNA e ITS4) del aislado de Fusarium sp. con las previamente depositadas en el GenBank mostró una cobertura del 100% con una identidad del 100% con F. oxysporum (MH169581.1). La secuencia de Fusarium sp. (indicada por un diamante negro) se agrupa en un clado con F. oxysporum, específicamente con las secuencias MH169581.1 y KY307805.1. Este clado tiene un soporte bootstrap del 100%, lo que proporciona una fuerte evidencia de que estas secuencias comparten un ancestro común reciente. La alta confiabilidad de este clado sugiere que la secuencia de Fusarium sp. está estrechamente relacionada con F. oxysporum (Figura 3).
La identificación a nivel de especie tiene implicaciones importantes para el manejo y control de especies de Fusarium en contextos agrícolas y medioambientales (Torres-Rodriguez et al., 2024a); Ekwomadu y Mwanza, 2023). La combinación de métodos morfológicos y moleculares son importantes, para lograr una identificación precisa de las especies de Fusarium (Singha, Kakoty, Unni, Das y Kalita, 2016). Además, Fusarium puede permanecer en el suelo por décadas, incluso sin la presencia de una planta huésped, por lo tanto, es necesario la identificación precisa para la toma de medidas (Bell et al., 2019).
Se observaron cuatro aislados distintos de Phytophthora spp., denominados PMJ1, PMJ2, PMJ3 y PMJ4. El aislado PMJ1 mostró una forma estriada y un color blanquecino, con una esporulación abundante (+++). En comparación, los aislados PMJ2 y PMJ4 presentaron una forma sumergida y radiada, también con un color blanquecino, pero con una esporulación limitada (+). El aislado PMJ3 exhibió forma estriada y un color blanquecino, con una esporulación moderada (++) (Cuadro 5).
Table 5: Morphological characteristics of Phytophthora spp isolates.
| Aislado | Forma | Color | Textura | Esporulación |
| PMJ1 | Estriada | Blanquecina | Esponjosa | +++ |
| PMJ2 | Sumergida y radiada | Blanquecina | Laxa | + |
| PMJ3 | Estriada | Blanquecina | Esponjosa | ++ |
| PMJ4 | Sumergida y radiada | Blanquecina | Laxa | + |
Categoría de esporulación: abundante = +++; moderado = ++; limitado = +.
Sporulation category: abundant = +++; moderate = ++; limited = +.
El análisis morfológico de los aislados de Phytophthora spp. mostraron diferencias en las características de forma y esporulación, demostrando la complejidad de este grupo de fitopatógenos. Castillo y González (2015) han observado características morfológicas similares a las obtenidas en este trabajo, los autores reportaron colonias en formas de anillos concéntricos y arrosetadas. Se ha demostrado que las colonias de algunas especies de Phytophthora presentan patrones concéntricos y arrosetados con un color blanquecino (Abad et al., 2023a y 2023b). Otro estudio sobre P. palmivora también describe colonias con crecimiento micelial blanco, lo que coincide con nuestros resultados (Decloquement et al., 2021). Los aislados con esporulación abundante, podrían presentar mayor potencial de dispersión.
Todos los aislados presentaron esporangios de forma ovoide. Los aislados PMJ1, PMJ2 y PMJ4 exhibieron esporangios papilados (P), mientras que el aislado PMJ3 mostró esporangios semipapilados (SP). En cuanto al pedicelo, todos los aislados tuvieron pedicelos cortos, y los esporangióforos fueron del tipo simple simpodial (SS). Los aislados PMJ1 y PMJ3 mostraron una abundante presencia de clamidosporas terminales (CT) e intercaladas (Cli), mientras que PMJ2 presentó una limitada presencia de clamidosporas (CT y Cli). PMJ4 solo presentó clamidosporas terminales (CT) y en una cantidad limitada (Cuadro 6).
Table 6: Characteristics of the reproductive structures of Phytophthora spp. isolates.
| Aislado | Esporangio | Clamidosporas | |||||
| Forma | Papila | Pedicelo | Esporangióforo | Forma | Presencia | ||
| PMJ1 | Ovoide | P | Corto | SS | CT, Cli | Abundante | |
| PMJ2 | Ovoide | P | Corto | SS | CT, Cli | Limitada | |
| PMJ3 | Ovoide | SP | Corto | SS | CT, Cli | Abundante | |
| PMJ4 | Ovoide | P | Corto | SS | CT | Limitado | |
SP = semipapilado; P = papilado; SS = simple simpodial; Cli = clamidospora intercalar; CT = clamidospora terminal.
SP = semipapillary; P = papillary; SS = simple sympodial; Cli = intercalary chlamydospora; CT = terminal chlamydospore.
Todos los aislados mostraron la presencia de esporangios y clamidosporas, resultados que concuerdan en la investigación realizada por Alsultan et al. (2022). Los esporangios, presentaron forma ovoide con pedicelos cortos, resultados similares a los obtenidos por Van-Tran, Ha, Vvedensky y Han (2023). En el presente estudio se detectó esporangióforos simples simpódicos en todos los aislados, similares a los resultados de Kuswinanti, Patandjengi y Hardina (2023). Karyath-Palliyath et al. (2021) indicó en su investigación la presencia de clamidosporas intercalares y clamidosporas terminales, concordando con los resultados obtenidos en este trabajo.
Las diferencias en la presencia de clamidosporas podrían estar asociadas a la capacidad de supervivencia y dispersión de los aislados en condiciones ambientales adversas (Judelson y Blanco, 2005). Los aislados con abundantes clamidosporas, como PMJ1 y PMJ3, podrían mantenerse por un mayor tiempo en el suelo e infestar nuevas plantas hospederas. La diversidad morfológica de los aislados de Phytophthora spp., puede influir en su comportamiento patogénico y en las estrategias de manejo necesarias para controlar las enfermedades que causan.
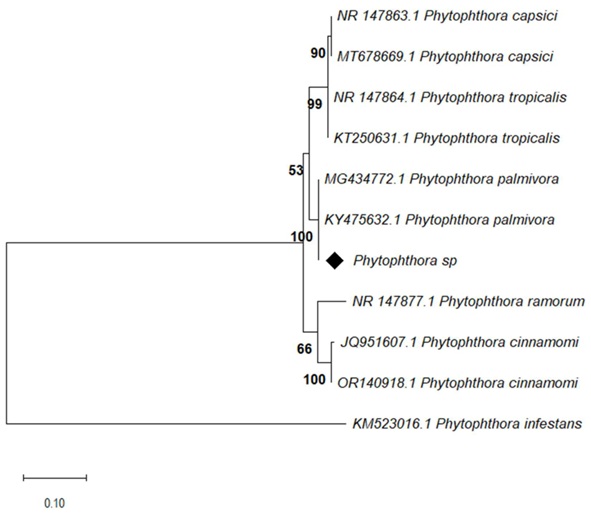
El análisis de identificación molecular reveló que el aislamiento PMJ1, se identificó como Phytophthora palmivora, el cual mostró una cobertura del 100% con una identidad del 100% en la secuencia registrada en la base de datos NCBI/GenBank bajo el número de acceso MG434772.1. La secuencia de Phytophthora sp. (indicada por un diamante negro) se agrupa en un clado con P. palmivora (MG434772.1 y KY475632.1), con un soporte bootstrap del 100%. Este alto valor de bootstrap indica una fuerte evidencia de que estas secuencias comparten un ancestro común reciente, sugiriendo que Phytophthora sp. está estrechamente relacionada con P. palmivora (Figura 4).
La correcta identificación de los fitopatógenos no solo es vital para vincular el conocimiento sobre una especie, como su biología, rango de huéspedes, distribución y riesgo potencial (Bhunjun, Philips, Jayawardena, Promputtha y Hyde, 2021), también es importante para desarrollar estrategias específicas de manejo. En nuestra investigación, esta identificación permite seleccionar y evaluar microorganismos antagonistas de manera efectiva, optimizando las medidas de control biológico y mejorando la sostenibilidad agrícola.
Un estudio realizado por Abdul-Haq, Shahzad, Lodhi y Rajput (2024) utilizó la secuenciación de ITS1-5.8S-ITS2 para identificar especies de Phytophthora. Otro estudio de Seddaiu y Linaldeddu (2020) utilizó la secuenciación ITS1-5.8S-ITS2 para caracterizar molecularmente aislamientos de Phytophthora spp., resultados similares a los obtenidos en esta investigación. También, El-Hasan, Ngatia, Link y Voegele (2022) utilizaron la secuenciación ITS1-5.8S-ITS2 para identificación y caracterización de P. infestans. En el estudio actual, existió una alta relación entre el análisis filogenético de los aislados y sus correspondientes coincidencias BLAST más cercanas, como lo demuestra el alto soporte de arranque en los nodos terminales.
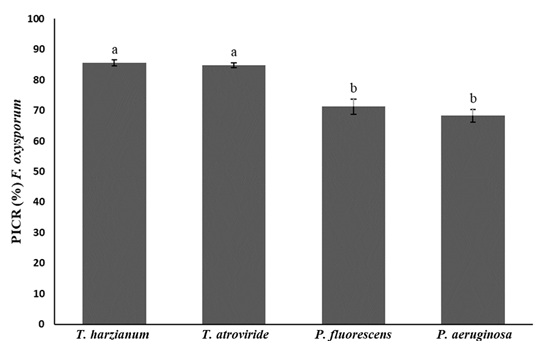
La Figura 5 muestra la inhibición de crecimiento micelial (PICR) de F. oxysporum en presencia de diferentes agentes de control biológico: T. harzianum, T. atroviride, P. fluorescens y P. aeruginosa. Los resultados indicaron que T. harzianum y T. atroviride presentan una alta eficacia en la inhibición de F. oxysporum, con porcentajes de superiores del 80%, significativamente mayores en comparación con P. fluorescens y P. aeruginosa (Figura 5).
Las pruebas de antagonismo revelan tanto la capacidad como la variabilidad genética del antagonista y del fitopatógeno para resistir la interacción antagonista. Estos ensayos facilitan una selección inicial para su evaluación en condiciones de campo, permitiendo determinar su eficacia como agentes de control biológico (Carmona-Hernandez et al., 2019).
Las estrategias actuales de control de Fusarium spp. a menudo no tienen éxito debido al desarrollo de resistencia química y a la falta de cultivares de plantas resistentes a las enfermedades (Goncharov, Glebova y Tiunov, 2020). Las cepas de T. viride y T. harzianum mostraron eficacia antagonista contra los fitopatógenos fusariales causantes de la pudrición del tallo del maíz. La cepa T. harzianum suprimió el crecimiento micelial de F. proliferatum y F. verticillioides en un 68.38 y 60.64%, mientras que la cepa T. viride lo hizo en un 80.17 y 70.46%, respectivamente (Yassin, Mostafa, Al-Askar, Sayed y Rady, 2021a). Sin embargo, nuestros resultados fueron superiores, logrando inhibir el crecimiento micelial de F. oxysporum en más del (80%).
Un estudio demostró que T. harzianum presentó actividad antagonista contra F. oxysporum en un 72.77% mediante mecanismos tanto mecánicos como enzimáticos (Chen et al., 2021). Otro estudio informó que T. harzianum inhibió el crecimiento de diferentes especies de Fusarium hasta en un 84.4%, resultados en correspondencia con nuestro trabajo (Yassin, Mostafa y Al-Askar, 2021b).
Los mecanismos de actividad antagonista de Trichoderma spp. incluyen antibiosis, micoparasitismo, resistencia inducida y exclusión de nichos (Wells, 2023). La antibiosis implica la producción de varios compuestos antimicrobianos que funcionan como inhibidores del crecimiento de fitopatógenos (Ali-Nusaibah y Musa, 2019; Kubheka y Ziena, 2022). Durante el proceso de micoparasitismo, las paredes celulares de los fitopatógenos son degradadas por enzimas producidas por especies de Trichoderma (Manzar et al., 2022; Yao et al., 2023). Además, existe competencia entre Trichoderma spp. y fitopatógenos en busca de sitios de infección y nutrientes, lo que se conoce como exclusión de nichos (Oszust, Cybulska y Frąc, 2020; Dutta et al., 2023).
Riera et al. (2023), encontraron que P. fluorescens inhibió significativamente el crecimiento de F. oxysporum, demostrando una fuerte actividad antagonista. También, en otro estudio P. fluorescens inhibió el crecimiento micelial de F. oxysporum f. sp. cumini en un 82.51%, resultados similares a esta investigación (Rathore, Vakharia y Rathore, 2020). Los principales mecanismos de actividad antifúngica de Pseudomonas spp. son la producción de metabolitos bioactivos, como lipopéptidos, sideróforos, policétidos y compuestos volátiles (Caulier et al., 2018).
Las especies de Phytophthora producen diferentes tipos de esporas (oosporas, clamidosporas y zoosporas), pero no pueden sintetizar esteroles, que son el objetivo de muchos fungicidas (Gaulin, Bottin y Dumas, 2010). Como resultado, los fitopatógenos Phytophthora son difíciles de controlar utilizando la mayoría de los fungicidas disponibles actualmente. Además, las especies de Phytophthora pueden superar los agentes de control químico y la resistencia a las plantas hospedantes mediante la flexibilidad genética (Bae et al., 2016).
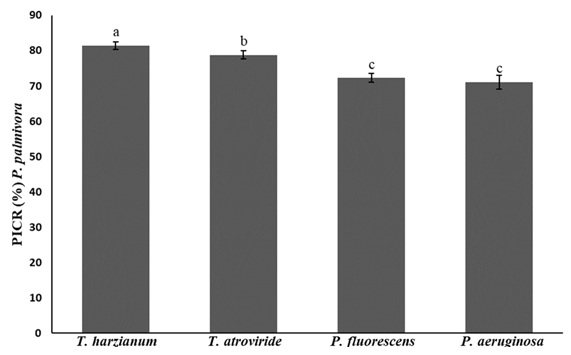
En la evaluación del porcentaje de inhibición del crecimiento radial (PICR) de Phytophthora palmivora, se observaron diferencias significativas entre los tratamientos evaluados (P < 0.05). T. harzianum mostró el mayor porcentaje de inhibición con un 82%, con diferencias significativas con el resto de los tratamientos. P. fluorescens y P. aeruginosa no presentaron diferencias significativas entre ellos (Figura 6).
Se ha demostrado que la aplicación de microorganismo como Trichoderma spp. y Pseudomonas spp como método de control biológico puede ayudar a reducir el uso de pesticidas y fertilizantes químicos en la agricultura (Nishioka, Suga y Shimizu, 2022; Martinez, Ribera, Schwarze y De-France, 2023).
Caulier et al. (2018) demostraron que cepas de Pseudomonas spp. mostraron una fuerte actividad inhibidora (≥ 70%) contra P. infestans, resultados similares a nuestro trabajo. Zohara et al. (2016) demostraron que Pseudomonas spp. inhibió el crecimiento de P. capsici, mediante la inducción de ramificación excesiva, hinchazón y daño celular.
También, se ha demostrado que P. putida reduce la incidencia del marchitamiento por Fusarium en lino, rábano y pepino, mediante la competencia por los iones de hierro entre el fitopatógeno y los sideróforos producidos por P. putida (Orr y Nelson, 2018; Nishioka et al., 2022).
Nuestros resultados son similares a los reportados por Bae et al. (2016), los autores demostraron la capacidad antifúngica de Trichoderma contra Phytophthora sp., además, Trichoderma sp. provocó cambios morfológicos significativos en las hifas de Phytophthora sp, como hinchazón, nudos, aplanamiento, arrugamiento, estallido y necrosis. También, Santos et al. (2023) demostraron la actividad antifúngica de cepas de T. aggressivum, T. longibrachiatum y T. saturnisporum contra P. capsici y P. parasitica obteniendo valores de inhibición de 82 y 88%, respectivamente.
Conclusiones
La identificación molecular y morfológica confirmó la presencia de microorganismos del suelo asociados a musáceas de especies de P. aeruginosa, P. fluorescens, T. harzianum y T. atroviride, todos con altos valores de soporte bootstrap. Los aislados de Trichoderma spp. (T. harzianum y T. atroviride) y Pseudomonas spp. (P. fluorescens y P. aeruginosa) presentaron una alta inhibición del crecimiento micelial de los fitopatógenos F. oxysporum y P. palmivora. T. harzianum y T. atroviride mostraron porcentajes de inhibición alrededor del 80%, superiores a los de P. fluorescens y P. aeruginosa. Estos resultados subrayan el potencial de estos microorganismos como posibles agentes de control biológico en la agricultura, ofreciendo una alternativa efectiva y sostenible a los fungicidas químicos sintéticos.











 nueva página del texto (beta)
nueva página del texto (beta)