Antecedentes
“El hombre que confundió a su mujer con un sombrero”1 es un reconocido cuento del neurólogo y escritor británico Oliver Sacks, homónimo de la obra que publicó en 1985. Relata la historia de un músico y maestro distinguido, quien empieza a presentar “ciertos errores” y “extraños problemas” al no distinguir el rostro de personas a su alrededor. El músico, quien parecía que “abordaba su entorno con los oídos pero no con los ojos”, lograba distinguir cada estructura de manera individual, sin embargo, no las integraba como un todo, esto es, no identificaba el rostro que construían ni sus expresiones, llegando a confundir rostros conocidos, como el de su esposa, con objetos inanimados, como su sombrero. Tampoco era capaz de reconocerse a sí mismo en una foto o en el espejo, e identificaba su entorno con el tacto, el olor, el sonido, pero no con la vista. Parecía que el déficit visual también comprometía su imaginación y su memoria visual. No obstante, sacando provecho de su gran talento musical, había logrado suplir su déficit con melodías y patrones para realizar sus actividades diarias, como alimentarse o vestirse.
MÉTODOS
Se realizó una revisión narrativa de la agnosia visual y sus bases neuroanatómicas en libros de neuroanatomía y revistas científicas de neurociencias, con énfasis en la vía visual, integración cortical, conexiones subcorticales y vascularización relevante. Para mejorar su compresión, la información se complementó con modelos anatómicos de disecciones cerebrales como material didáctico.
RESULTADOS AGNOSIA VISUAL
La agnosia es la pérdida de la capacidad para identificar objetos por medio de uno o más sentidos (vista, gusto, audición, olfato o tacto), objetos que previamente han sido identificados, reconocidos y almacenados en la memoria perceptiva. Esta condición no corresponde a una alteración en las vías aferentes de las modalidades sensoriales ni de atención, memoria o lenguaje.2 En general, la agnosia visual es la más frecuente y comprendida,2,3 esto podría relacionarse con que la visión es la modalidad sensorial más desarrollada en el humano4 y de la que es más dependiente, pues proporciona una experiencia directa del mundo y retroalimentación para relacionarse con él.5
La agnosia visual corresponde a un trastorno perceptivo secundario a una lesión en el parénquima cerebral que afecta el reconocimiento visual o la interpretación de objetos a pesar de que la vía visual, la campimetría, la agudeza visual y la percepción de colores se encuentren íntegras.3 Los objetos o escenarios visualizados pueden ser completamente indescifrables o carecer de significado ya que no es posible analizar las primitivas visuales como líneas, curvas, colores o formas.6 Sin embargo, la identificación de esos mismos objetos a través de otros sentidos se encuentra conservada. Al igual que otras agnosias, se clasifica en dos tipos según el mecanismo de procesamiento comprometido: puede tratarse de una agnosia visual aperceptiva, en la que no se identifican o discriminan las formas de los objetos y que en casos severos puede simular una amaurosis,4 o asociativa, en la cual, aunque se identifique el objeto, este no puede ser interpretado, comprendido ni vinculado con experiencias previas.2
Prosopagnosia
Constituye un tipo de agnosia visual caracterizado por la incapacidad para reconocer rostros, incluso de personas familiares o famosas, así como una limitación para identificar expresiones como alegría o miedo.7 En ocasiones, es posible reconocer rasgos no faciales como el color del cabello, la forma de caminar o la vestimenta, que ayudan en la identificación de un personaje.8 La habilidad para reconocer rostros y expresiones trasciende género, edad, cultura y raza, siendo esencial para la interacción social y la empatía, característica de los seres humanos.
Epidemiología
Menos de 1% de pacientes con trastornos neurológicos presentan agnosias puras, siendo la más frecuente la agnosia visual.9 La prosopagnosia aislada es poco frecuente, sin embargo, se describen casos de prosopagnosia congénita que afectan hasta 2.5% de la población general,10 y que incluso pueden estar asociados con otras alteraciones, como heminegligencia, acromatopsia o agnosia visual general.3,4
Etiología
Las agnosias son el resultado de diferentes tipos de lesiones de la corteza cerebral en áreas de asociación o procesamiento sensorial, principalmente la corteza parietal posterior y occipitotemporal.2 El tiempo de instauración de la enfermedad deriva del tipo de lesión, la asociación con otros déficits neurológicos y los hallazgos paraclínicos. Los casos de agnosia visual aguda se relacionan con infarto de la arteria cerebral posterior (ACP),11,12 infecciones o traumatismo craneoencefálico,13 en cambio, las alteraciones graduales, suelen asociarse con tumores, intoxicaciones por monóxido de carbono o demencias, como enfermedad de Alzheimer o demencia frontotemporal,14 e incluso se han descrito casos de prosopagnosia hereditaria secundaria a alteraciones en la corteza occipitotemporal.10,15
Fisiopatología
Anatómicamente la lesión de una agnosia visual no se localizará en la corteza visual primaria sino en la corteza visual asociativa o en sus conexiones, incluyendo áreas de los lóbulos occipital, parietal y temporal.4 En el caso de la prosopagnosia, se han descrito lesiones bilaterales en la corteza, principalmente en las circunvoluciones fusiforme (área 37 de Brodmann) y parahipocampal o, con menor frecuencia, unilateral del hemisferio dominante.16,17 Asimismo, se describen con poca frecuencia el giro lingual7 y la porción anterior del lóbulo temporal derecho.3,13 Estas zonas podrían verse afectadas por cualquiera de las etiologías descritas anteriormente. Bases neuroanatómicas
Vía visual
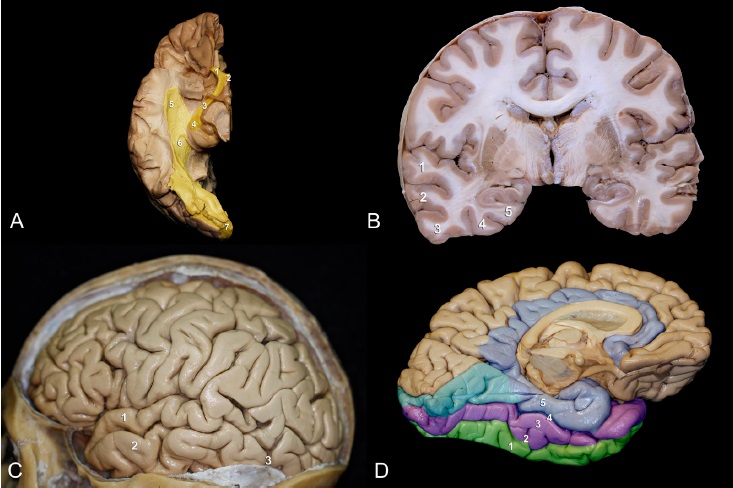
La visión es un sistema amplio y complejo que involucra múltiples estructuras, conexiones y funciones cognitivas y las convierte en un proceso consiente. Este sistema suele mantenerse íntegro en las agnosias visuales. El proceso inicia a partir la captación de una imagen por las células fotorreceptoras de la retina, luego se codifica el estímulo visual y los axones viajan de las células ganglionares que forman los nervios ópticos, los cuales cruzan la información captada en la retina visual a nivel del quiasma óptico, siguiendo por los tractos ópticos hasta hacer sinapsis en los cuerpos geniculados laterales del tálamo, y continúan por las radiaciones geniculocalcarinas superiores e inferiores hasta la cisura calcarina del lóbulo occipital, que corresponde a la corteza visual primaria18,19 (Figura 1A).
Corteza visual de asociación
Una vez la imagen está formada en la corteza visual primaria, deberá pasar a la corteza de asociación correspondiente para poder ser reconocida e interpretada de forma consciente, en esta área será comparada con imágenes previamente almacenadas en la memoria.4
Se describen dos vías principales de procesamiento: una vía ventral, que permite percibir un objeto, reconocerlo y relacionarlo con un significado, conectando áreas visuales primarias con la corteza temporal inferior, y una vía dorsal, que permite ubicar espacialmente el objeto y relacionarse corporalmente con él mediante la conexión con el surco intraparietal de la corteza parietal posterior5,20 En particular, la prosopagnosia suele incluirse dentro de los síndromes perceptivos o de la vía visual ventral.4
Corteza occipitotemporal
Las superficies basales de los lóbulos temporales y occipitales se continúan entre sí sin una clara división anatómica y además comparten varias funciones, por lo que se denominan como una unidad: la corteza occipitotemporal.
El lóbulo temporal se sitúa por debajo de la cisura lateral o de Silvio, clásicamente dividido en cinco circunvoluciones o giros (nombrados de T1 a T5) y cuatro surcos (t1 a t4)21(Figura 1B).
A su vez, la superficie lateral está compuesta por los giros temporales superior (T1), medio (T2) e inferior (T3), divididos por los surcos temporales superior (t1) e inferior (t2), que se disponen paralelamente a la cisura lateral o de Silvio. T3 se continúa hacia posterior con el giro occipital inferior sin una demarcación clara. En relación al borde inferior del hemisferio cerebral, entre los lóbulos temporal y occipital ubicamos la región de la muesca preoccipital (Figura 1C).
La superficie inferior o basal del lóbulo temporal tiene forma cóncava en dirección anteroposterior, de manera que se continua con la superficie basal del lóbulo occipital y reposa sobre el suelo de la fosa craneal media y el tentorio.21,22 Está compuesta de lateral a medial por la parte ventral del giro occipitotemporal lateral (T3), el giro temporooccipital medial o fusiforme (T4) y el giro parahipocampal (T5), separados por el surco occipitotemporal (t3) y el surco colateral (t4) respectivamente (Figura 1D).
Esta región del temporal inferior en el humano está especializada en el procesamiento y reconocimiento visual de los objetos y la discriminación de partes del cuerpo y rostros,23,24 además de estar asociado con la integración sensorial y memoria.25,26El giro parahipocampal y la porción anterior del surco colateral forman parte del sistema límbico relacionado con la memoria.21
Según estudios funcionales de resonancia magnética, la circunvolución fusiforme es la de mayor actividad en la mayoría de los individuos cuando se exponen a un estímulo visual tipo rostro, en comparación a objetos de otras categorías.27 Por este motivo, el giro fusiforme tiene un papel fundamental en la fisiopatología de la prosopagnosia. Este giro fue descrito por primera vez en 1854 por Emil Huschke,28 quien acuñó el término “fusiforme” por su forma de huso, siendo más ancho en el medio que en los extremos. En su extremo posterior alcanza a fusionarse con el giro temporal inferior, el giro lingual y la rama posterior del cuneo. Funcionalmente se han descrito tres porciones relacionadas con patrones de conexión: la porción medial parece estar involucrada en el procesamiento visual de bajo nivel, la porción lateral corresponde al nivel alto tipo categorización y la porción anterior a un procesamiento visual-semántico. Lesiones bilaterales del giro lingual, giro parahipocampal y giro fusiforme, o de su irrigación por la ACP, se relacionan con prosopagnosia.24
El lóbulo occipital, por su parte, se ubica posterior al surco parietooccipital, por encima del tentorio. De todos los lóbulos cerebrales, el occipital suele tener surcos menos definidos y con mayor variación anatómica.21
En la superficie superolateral se describen tres circunvoluciones con disposición transversal que convergen posteriormente en el polo occipital. Estas circunvoluciones occipitales se denominan superior (O1), media (O2) e inferior (O3), y se encuentran separadas entre sí por el surco occipital superior, que es la continuación del surco intraparietal y el surco occipital inferior.
En la superficie medial hay una mejor definición de los surcos, que abarcan las circunvoluciones cuneal (o cuneus) y lingual (o temporooccipital medial), separadas por la fisura calcarina. Esta última inicia sobre el esplenio del cuerpo calloso, limitando la circunvolución del cíngulo con la del parahipocampo. Esta área corresponde a la corteza visual primaria19 (Figura 2).
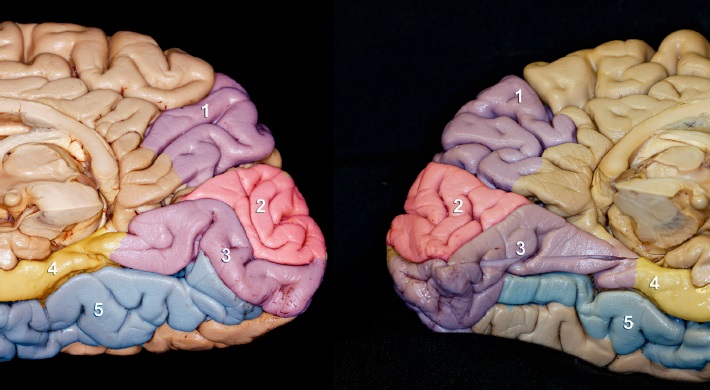
Figura 2 Cara medial de hemisferio derecho e izquierdo, lóbulos occipital y temporal: 1) precuneo, 2) cuneo, 3) giro lingual, 4) giro parahipocampal, 5) giro occipitotemporal medial
El lóbulo occipital se conecta mediante pliegues con los lóbulos parietal y temporal. El primer pliegue parietooccipital conecta con las circunvoluciones parietal y occipital superior, el segundo pliegue es una extensión posterior del giro angular que converge con la circunvolución occipital media, y en ocasiones con la superior. Mientras que el primer pliegue temporooccipital conecta la circunvolución temporal media con la occipital inferior, el segundo pliegue une la circunvolución temporal inferior con la occipital inferior.21,29 Estas conexiones de sustancia blanca son esenciales para entender las redes neuronales que permiten las funciones cognitivas de asociación e integración de modalidades sensoriales (Figura 3).
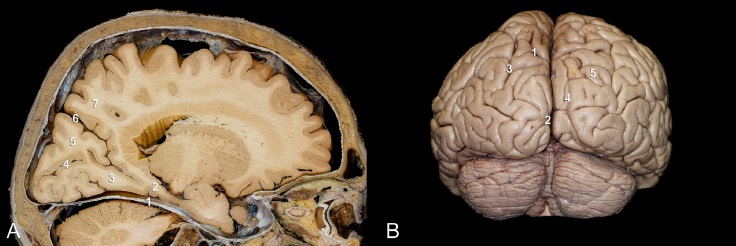
Figura 3 A. Corte parasagital: 1) tentorio, 2) giro parahipocampal, 3) giro fusiforme, 4) surco calcarino, 5) cuneo, 6) surco parieto-occipital, 7) precuneo. B. Cara posterior lóbulo occipital: 1) cisura parieto-occipital, 2) cisura calcarina, 3) surco intraparietal, 4) surco lunatum, 5) lóbulo parietal superior.
Irrigación de la corteza occipitotemporal
El lóbulo temporal tiene una irrigación mixta entre la circulación cerebral anterior (ACA), por la arteria carótida interna, y la posterior, por el sistema vertebrobasilar.30 La porción insular de la arteria cerebral media se encarga de irrigar a la porción anterolateral de la corteza temporal por medio de ramas temporales superiores anterior, media y posterior, y está asociada a ramas de la arteria coroidea anterior hacia el extremo anterior de la circunvolución parahipocampal, el uncus, la amígdala y el asta temporal del ventrículo lateral. La porción inferoposterior está irrigada en su mayoría por ramas de la ACP, al igual que el lóbulo occipital.
En 2012, Martinaud et al.11 analizaron 31 pacientes con antecedente de infarto de la ACP, en 23 de ellos encontraron defectos de campos visuales, 20 presentaron agnosias visuales de diferentes tipos, y diez de ellos mostraron dificultad en el reconocimiento de rostros, lo cual podía estar asociado o no al reconocimiento de objetos de otras categorías, especialmente cuando el territorio afectado correspondía a las circunvoluciones fusiformes y parahipocampal.
Este estudio sugiere que las agnosias visuales posteriores a infartos de la ACP son más frecuentes de lo que se cree.
Anatomía de la arteria cerebral posterior
La ACP surge en la bifurcación de la arteria basilar a nivel de la cisterna interpeduncular. Esta bifurcación puede ubicarse entre los cuerpos mamilares y la unión pontomesencefálica (Figura 4A). La ACP se relaciona en su origen con los nervios de los músculos extraoculares: oculomotor (III) y troclear (IV), posteriormente rodea el tronco encefálico por las cisternas crural y ambiens hasta llegar a la cisterna cuadrigeminal. Irriga no solo la parte posterior de los hemisferios cerebrales, sino también porciones del tálamo, mesencéfalo, plexos coroideos de la porción occipital de los ventrículos laterales y del tercer ventrículo.22
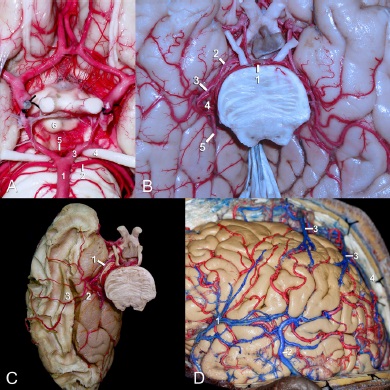
Figura 4 A. Arteria cerebral posterior: 1) arteria basilar, 2) arteria cerebelosa superior, 3) segmento P1 de la ACP, 4) nervio craneal oculomotor, 5) arteria talamoperforantes posteriores, 6) cuerpos mamilares. B. Cara ventral del lóbulo temporal y occipital y su relación con la arteria cerebral posterior: 1) arteria basilar, 2) segmento P2a, 3) segmento P2p, 4) segmento P3, 5) segmento P4. C. Disección de la región temporo-occipital por método Klingler e inyección vascular cerebral con látex. Irrigación de sustancia blanca y sustancia gris de la cara ventral de la región temporo-occipital: 1) arteria cerebral posterior, 2) giro parahipocampal, 3) fascículo longitudinal inferior. D: 1) vena cerebral media superficial, 2) vena anastómotica menor (Labbé), 3) venas corticales ascendentes, 4) seno sagital superior.
El trayecto de la ACP se divide en cuatro segmentos22 con sus respectivas ramas (Figura 4.B, C):
P1 o segmento precomunicante: desde la bifurcación basilar hasta la unión con la arteria comunicante posterior (AcomP). Tiene una longitud promedio de 7 mm. Ramas:
P2 o segmento postcomunicante: comienza en la AcomP, trascurre por las cisternas crural y ambiens y termina lateral al borde posterior del mesencéfalo. Se divide en dos subsegmentos, cada uno de 25 mm de largo aproximadamente:
-
P3 o segmento cuadrigémino: desde el borde posterior de la superficie lateral del mesencéfalo y la cisterna ambiens, trascurriendo por la parte lateral de la cisterna cuadrigeminal hasta terminar en el límite anterior de la fisura calcarina. Tiene una longitud media de 2 cm. Ramas terminales:
Arteria calcarina: trascurre por la fisura calcarina hasta el polo occipital, da ramas en abanico dirigidas hacia la circunvolución lingual y la porción inferior del cuneus. Irriga la corteza visual primaria.
Arteria parietooccipital: trascurre por la fisura parietooccipital para irrigar la región parasagital posterior, cuneus, precuneos, circunvolución occipital lateral y porción de los lóbulos parietal paracentral y superior.
P4: comienza en el extremo anterior de la cisura calcarina dando ramas corticales:
Arteria esplénica: para el esplenio del cuerpo calloso. Se anastomosa con ramas de la arteria pericallosa de la ACA.
Arterias temporales inferiores:
Anterior: irriga la superficie anteroinferior del lóbulo temporal hacia el polo temporal.
Media (infrecuente): irriga la superficie inferomedial del lóbulo temporal.
Posterior: oblicuamente hacia el polo occipital y circunvolución lingual.
Común (infrecuente): rama única alterna que irriga la mayor parte de la superficie inferior de los lóbulos temporal y occipital.
Drenaje venoso de la corteza occipitotemporal
La cara lateral del lóbulo temporal es drenada por las venas cerebrales medias superficial y profunda hacia el seno esfenoparietal o seno cavernoso, y por la vena anastomótica menor o de Labbé hacia el seno transverso. El drenaje de la cara lateral de la corteza parietooccipital se da mediante las venas corticales ascendentes hacia el seno sagital superior, mientras que el de la cara ventral de la región temporooccipital se produce a través de la vena basal de Rosenthal hacia la vena cerebral magna o de Galeno, y por las venas temporales hacia el tentorio24 (Figura 4D).
Abordaje clínico y diagnóstico
Las agnosias en fases iniciales podrían pasar desapercibidas o ser confundidas con otros trastornos neurológicos. Por lo general, son los cuidadores o familiares quienes reconocen que hay alguna alteración en el paciente, mientras este ignora su déficit. En ocasiones, la agnosia puede ser tan severa que puede limitar el funcionamiento del paciente, impidiéndole completar actividades de la vida diaria o relacionarse con su entorno.2
Es clave una anamnesis completa y un examen neurológico minucioso que evalúe la capacidad de reconocer y nombrar objetos previamente conocidos por medio de los sentidos. Las evaluaciones a profundidad sobre percepción, asociación, memoria y cognición suelen ser realizadas por neuropsicólogos. También deben descartarse déficit primarios de las modalidades sensoriales, afasia, demencia o delirium.31
Cuando el trastorno es de tipo asociativo, el paciente podrá dibujar o copiar objetos que identifique, así como reconocer si dos objetos son similares en el “juego de parejas”.4 En las prosopagnosia deben emplearse fotografías de familiares, amigos, personas famosas o incluso del paciente mismo, así como probar la identificación de expresiones faciales durante una escena cinematográfica o en una revista.
Algunas pruebas para evaluar la prosopagnosia, son el Warrington Recognition Memory Test32 de 1984 y el Benton Facial Recognition Test33 de 1983, además del Cambridge Face Memory Test (CFMT) de 2004 (Figura 5). Este último se basa en los puntos más fuertes de las dos pruebas anteriores y tiene un mejor desempeño diagnóstico.34 El CFMT evalúa la identificación de rostros sin objetos o características externas que faciliten su reconocimiento, como ropa o peinado. Un resultado positivo corresponde a la incapacidad para reconocer correctamente al menos un 50% de ellos.2
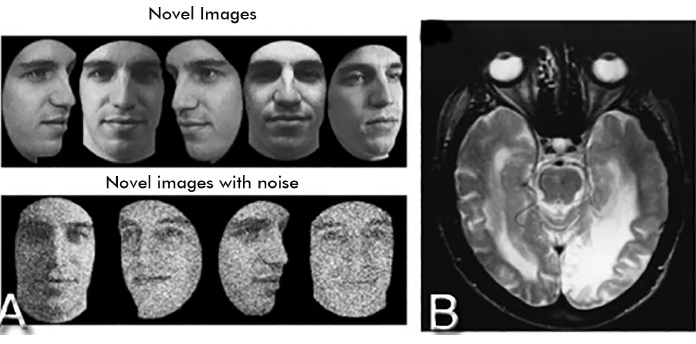
Figura 5 A. Cambridge Face Memory Test.34 B. Corte axial de resonancia cerebral simple ponderada en T2 en paciente con prosopagnosia por infartos de la ACP, principalmente en áreas de los giros fusiforme y lingual.12
Estos hallazgos deberán complementarse con estudios diagnósticos imagenológicos que descarten lesiones vasculares, inflamatorias o tumorales 2 y permitan plantear posibilidades de tratamiento médico-quirúrgico. En tomografías y resonancias simples pueden encontrarse infartos de territorios de la ACP, mientras que en estudios funcionales de resonancia magnética con imágenes de tensor de difusión, tractografías por emisión de positrones (PET), se pueden evidenciar cambios en la actividad funcional de personas con prosopagnosia,35 no solo en áreas específicas de corteza cerebral sino también en áreas de conexión y sustancia blanca.35,36
El giro fusiforme es la región de mayor actividad cuando un individuo visualiza un rostro,27,37 en comparación con la visualización de otros objetos. Además, se han descrito conexiones entre el giro fusiforme y áreas posteriores del giro lingual y giros temporales inferior y medio involucrados en el procesamiento e interpretación de información visual compleja,38 con conexiones paralelas a la red auditiva del giro temporal superior e ínsula posterior,27 por lo que el sistema de percepción humano está capacitado para captar señales sensoriales combinadas. Al respecto, las señales audiovisuales sincrónicas activan más al giro fusiforme que las asincrónicas.
Por otro lado, la función de “familiaridad”, relacionada con datos bibliográficos y respuestas afectivas asociadas a recuerdos, se ha localizado en regiones temporales anteriores y mediales con el polo temporal derecho.35,39 A su vez, la interpretación de la expresión facial involucra conexiones con neuronas del surco temporal superior,40 además de redes fuera de la corteza occipitotemporal que permiten el procesamiento emocional, principalmente amígdala, ínsula y cuerpo estriado.35
Conclusiones
Esta revisión sobre la prosopagnosia refleja la importancia de la neuroanatomía en la aplicación clínica, así como en el estudio y abordaje interdisciplinario de los trastornos neurológicos. Identificar adecuadamente los déficits cognitivos y sus alteraciones anatómicas permitirá brindar manejos médicoquirúrgicos específicos y rehabilitación integral que mejoren la calidad de vida de los pacientes y de sus cuidadores.
Fuentes de financiamiento
Este estudio no recibió financiamiento de ninguna entidad comercial, académica o gubernamental.