Introducción
A lo largo de la historia, el ser humano ha tratado de mimetizar la naturaleza con el objetivo de desarrollar la miniaturización de procesos más eficientes y de entender con mayor precisión los procesos naturales. En los últimos treinta años el desarrollo de máquinas moleculares artificiales análogas a las máquinas moleculares biológicas ha aumentado de manera drástica (Balzani et al., 2000).
Las máquinas moleculares biológicas son usadas para el transporte de material a la célula, para potenciar el movimiento de los organismos, sintetizar proteínas y separar las cadenas de ADN (Erbas-Cakmak et al., 2015; Mayer et al., 2009), por mencionar algunas funciones. Sin embargo, el uso de estos arreglos resulta difícil debido a su alta inestabilidad ex vivo y a las limitantes que representan las condiciones que éstas requieren (Browne y Feringa, 2006; Schnepp, 2013).
Las máquinas moleculares artificiales se presentan como una alternativa inspirada en sus análogos macroscópicos (Kassem et al., 2017; Zhang, 2020). El estudio de sus aplicaciones va desde la mimetización de tejidos musculares (Chen et al., 2017) y almacenamiento de energía solar (Kandinska et al., 2019) hasta la medición de la viscosidad de sistemas a partir del movimiento mecánico obtenido (Kuimova, 2008), por lo cual se han vuelto tendencia en años recientes, pues se aprovechan sus propiedades y versatilidad.
En este sentido, el artículo pretende otorgar un panorama de los rotores moleculares basados en hemitioíndigo (HTI) impulsados por luz, que son reportados en la bibliografía a partir del análisis de sus variedades, rutas sintéticas, mecanismos de fotoisomerización y sus propiedades físicas, químicas y fotocrómicas.
1. Máquinas moleculares
Credi et al. (2014a) indica que una máquina molecular se puede definir como el ensamblaje de un número discreto de componentes moleculares diseñados para llevar a cabo movimientos mecánicos (salida) en respuesta a determinados estímulos (entrada). Para que un arreglo molecular sea definido como máquina molecular debe cumplir con los siguientes requisitos (Sauvage y Gaspard, 2010; Feringa y Browne, 2011; Astumian, 2016): a) debe ser capaz de superar las fluctuaciones térmicas o movimiento browniano; b) debe poder realizar un trabajo en respuesta al estímulo externo aplicado; c) debe tener un alto grado de movimiento relativo controlado y continuo de la máquina al ser expuesta al estímulo (Balzani et al., 2003).
Los estímulos externos utilizados para que las máquinas moleculares ejecuten las tareas o los movimientos mecánicos son variados e incluyen el uso de luz (Pianowski, 2019; García-López et al., 2019), energía química (Baroncini et al., 2018), obtenida por diversas reacciones como las de óxido-reducción (Baroncini et al., 2019), o la formación de enlaces covalentes reversibles (Kassem et al., 2017), el control del movimiento por procesos electroquímicos (Credi et al., 2014b) y variaciones de pH (Kassem et al., 2017) y temperatura en el medio, donde los procesos fotoquímicos son los más atractivos debido a su alto carácter sustentable (Pianowski, 2019; Groppi et al., 2019).
Los motores biológicos en su mayoría utilizan la energía química de eventos de formación o rotura de enlaces como ATP, hidrólisis o gradientes de concentración para impulsar su operación (Schnepp, 2013); sin embargo, el uso de energía química en máquinas moleculares artificiales resulta poco viable, pues es necesario añadir reactantes nuevos (que fungen como “combustible” del motor), los cuales generan residuos químicos que al acumularse afectan y limitan la operación del motor (Erbas-Cakmak et al., 2015).
Dadas las limitaciones del uso de energía química, se ha propuesto el uso de fotones. A diferencia de la energía química, el uso de luz como estímulo tiene como ventaja que el sistema químico puede ser controlado por la longitud de onda y por la intensidad de luz usada (Ceroni et al., 2014). Como consecuencia, el uso de luz como fuerza impulsora de máquinas moleculares ha ganado popularidad muy rápido al ser un mecanismo no invasivo para alcanzar estados biestables (Feringa y Browne, 2011).
A diferencia de sus análogos macroscópicos, el movimiento de las máquinas moleculares se ve regido por diferentes leyes y principios, donde fuerzas como la gravedad son irrelevantes, mientras que el movimiento browniano y las fuerzas viscosas ganan relevancia (Astumian, 2016). Para diseñar máquinas moleculares es indispensable considerar el tipo de arreglo molecular, el estímulo que se va a utilizar y como se proveerá de éste, la polaridad del solvente y las características del medio, así como la influencia de los grupos funcionales presentes y el trabajo que se desea obtener; en este sentido, el reto principal es controlar el movimiento del arreglo (Feringa y Browne, 2011; Credi et al., 2014b).
1. 1. Clasificación de las máquinas moleculares artificiales
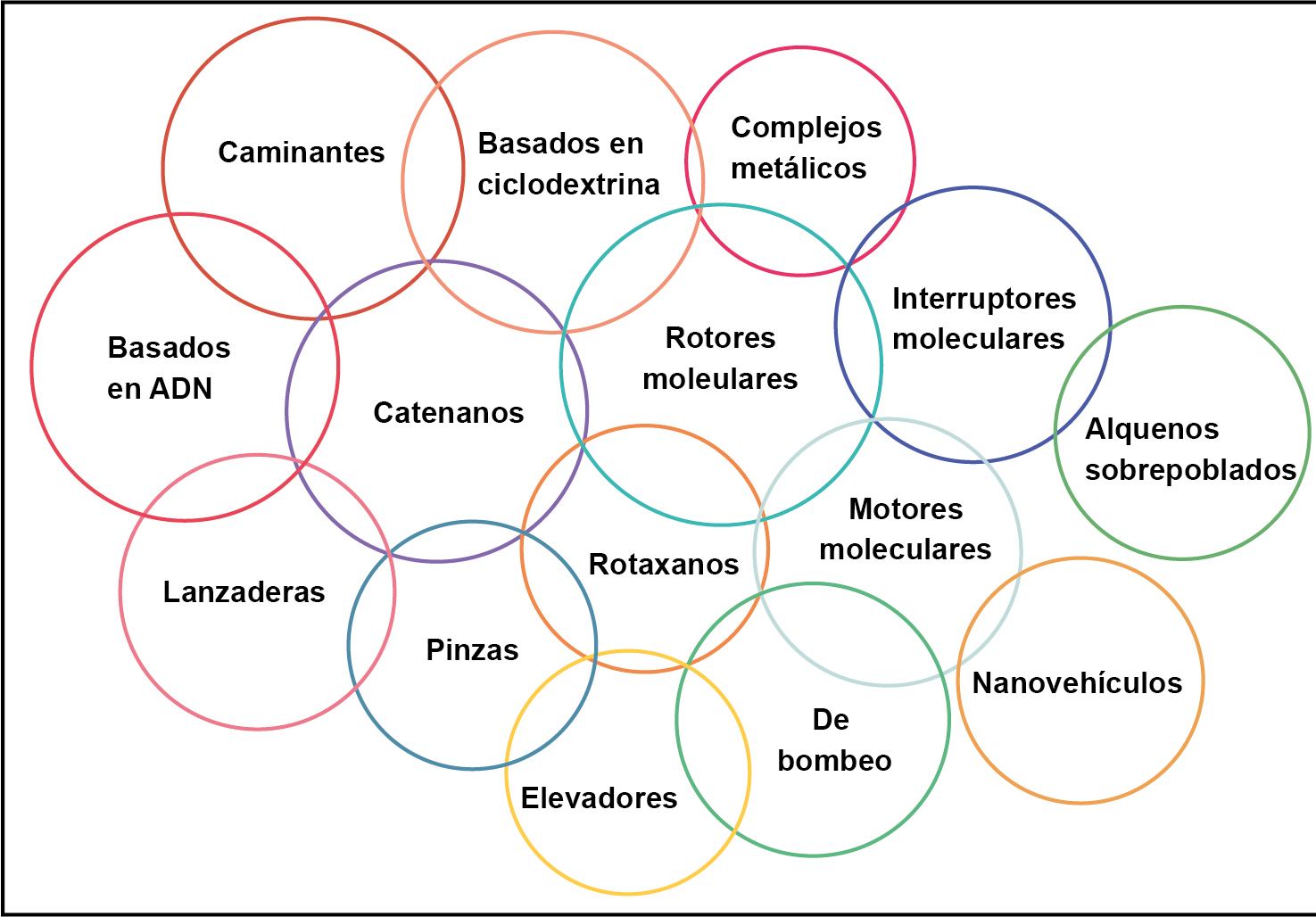
Debido a su versatilidad, clasificar las máquinas moleculares se vuelve una tarea compleja. Un determinado tipo de máquina molecular cumple a su vez con funciones o características de otro grupo, sin ser necesariamente excluyentes. La figura 1 muestra una clasificación de las máquinas moleculares más comunes y su intersección con las demás. Por ejemplo, un rotor molecular, dependiendo de su estructura, función y tipo de movimiento, puede ser una nanomáquina basada en ciclodextrina que, además de cumplir con la función de un rotor molecular, posee características de un rotaxano o catenano (Hashidzume et al., 2014), el cual a su vez puede entrar en la categoría de interruptor, lanzadera o motor.
Los primeros precedentes de máquinas moleculares artificiales datan de 1983, cuando Jean-Pierre Sauvage vinculó dos moléculas en forma de anillo para formar una cadena llamada catenano. Posteriormente, en 1991, Fraser Stoddart desarrolló un rotaxano, que es un macrociclo atravesado por una molécula en forma de mancuerna; estos arreglos tienen potenciales aplicaciones como soporte en síntesis de macromoléculas (De Bo et al., 2014). Stoddart también demostró que el anillo o macrociclo era capaz de moverse a lo largo del eje de la mancuerna (Balzani et al., 2003).
En 1999 se consiguió el desarrollo de un rotor molecular de giro unidireccional continuo y con este tipo de motores moleculares se logró hacer girar un cilindro de vidrio con un tamaño 10 000 veces más grande que el propio motor (Koumura et al., 1999; Koumura et al., 2002).
Si bien los arreglos topológicos o de enlace mecánico como los rotaxanos y catenanos han sido explorados por sus aplicaciones como la catálisis asistida o transporte de fármacos (Heard y Goldup, 2020), los arreglos moleculares basados en enlaces isomerizables resultan atractivos en respuesta a la posibilidad de producir cambios configuracionales mediante procesos fotoquímicos, además de ofrecer un alto control del movimiento del arreglo y la posibilidad de inducir estos mismos cambios en estructuras de importancia biológica como los péptidos, antibióticos y estructuras de ADN (Cameron y Eisler, 2018).
Los motores moleculares son aquellos arreglos cuya característica principal es el control direccional del movimiento que realizan, además pueden ser tanto intramoleculares como supramoleculares e influyen en el sistema como una función de trayectoria, es decir, cuando los componentes del motor molecular regresan a su posición original cualquier trabajo que se haya realizado no es deshecho (Kottas et al., 2005). Los motores moleculares ofrecen un amplio rango de aplicación en medicina, ciencia de materiales y desarrollo de tecnologías informáticas (Feringa, 2017). Para la activación en un nivel nanométrico, los motores moleculares operan en números de Reynolds bajos; de esta forma, su dinámica es dominada por movimientos térmicos aleatorios y fuerzas viscosas (Astumian, 2016).
Por otro lado, cuando los componentes de un interruptor molecular regresan a su posición original se deshace cualquier trabajo hecho y libera energía en el sistema (Kottas et al., 2005), lo que significa que los interruptores no sean utilizados repetitiva y progresivamente para un trabajo.
2. Rotores moleculares basados en hemitioíndigos
Los rotores moleculares son arreglos moleculares diseñados con el objetivo de imitar a sus análogos macroscópicos. Constan de dos partes que pueden rotar con facilidad en relación con el uno del otro al ser expuestos de manera continua al estímulo externo (Balzani et al., 2000); es común nombrar a la parte con mayor momento de inercia como (estacionario) estator y a la parte con el menor momento de inercia como el rotador (Kottas et al., 2005). El movimiento de un rotor molecular debe ser continuo y de 360º (Browne y Feringa, 2006).
Dentro de los rotores moleculares existe una subclasificación que los define como motores o interruptores moleculares, donde su principal diferencia reside en su rotación, pues mientras el interruptor no puede ser usado para los trabajos progresivos (Kottas et al., 2005), el motor molecular sí y al regresar a su estado inicial el trabajo realizado no se pierde (Kassem et al., 2017). En la actualidad se han identificado cuatro generaciones de rotores moleculares en función al tipo de rotación y a las características de sus componentes que abarcan un amplio rango de tamaños (desde 10 nm hasta 5 μm) y estructuras (García-López et al., 2019).
Los rotores moleculares basados en la molécula hemitioíndigo pertenecen a la segunda generación de rotores moleculares (Wiedbrauk y Dube, 2015). Esta generación de rotores se caracteriza por sus dos mitades diferentes una de la otra, creadas para ser isomerizadas con luz UV (Koumura et al., 2002); sin embargo, el uso de este tipo de luz resulta problemático para ciertas aplicaciones biológicas, por lo que se han propuesto rotores moleculares cuya isomerización se realice al irradiar al sistema con luz visible (Petermayer y Dube, 2018).
La molécula hemitioíndigo (HTI) consiste en un fragmento tioíndigo (estator), conectado a un fragmento estilbeno (rotador) mediante un doble enlace central (Wiedbrauk y Dube, 2015). Son moléculas quirales que tienen dos posibles configuraciones geométricas diferentes E y Z, que pueden ser isomeradas al irradiar con luz visible la molécula, lo que le otorga una gran ventaja frente a otros arreglos moleculares que requieren de luz UV o más cercano al infrarrojo y, al igual que los rotores reportados por Feringa (2017), su rotación es alrededor del enlace C = C (Nie et al., 2019).
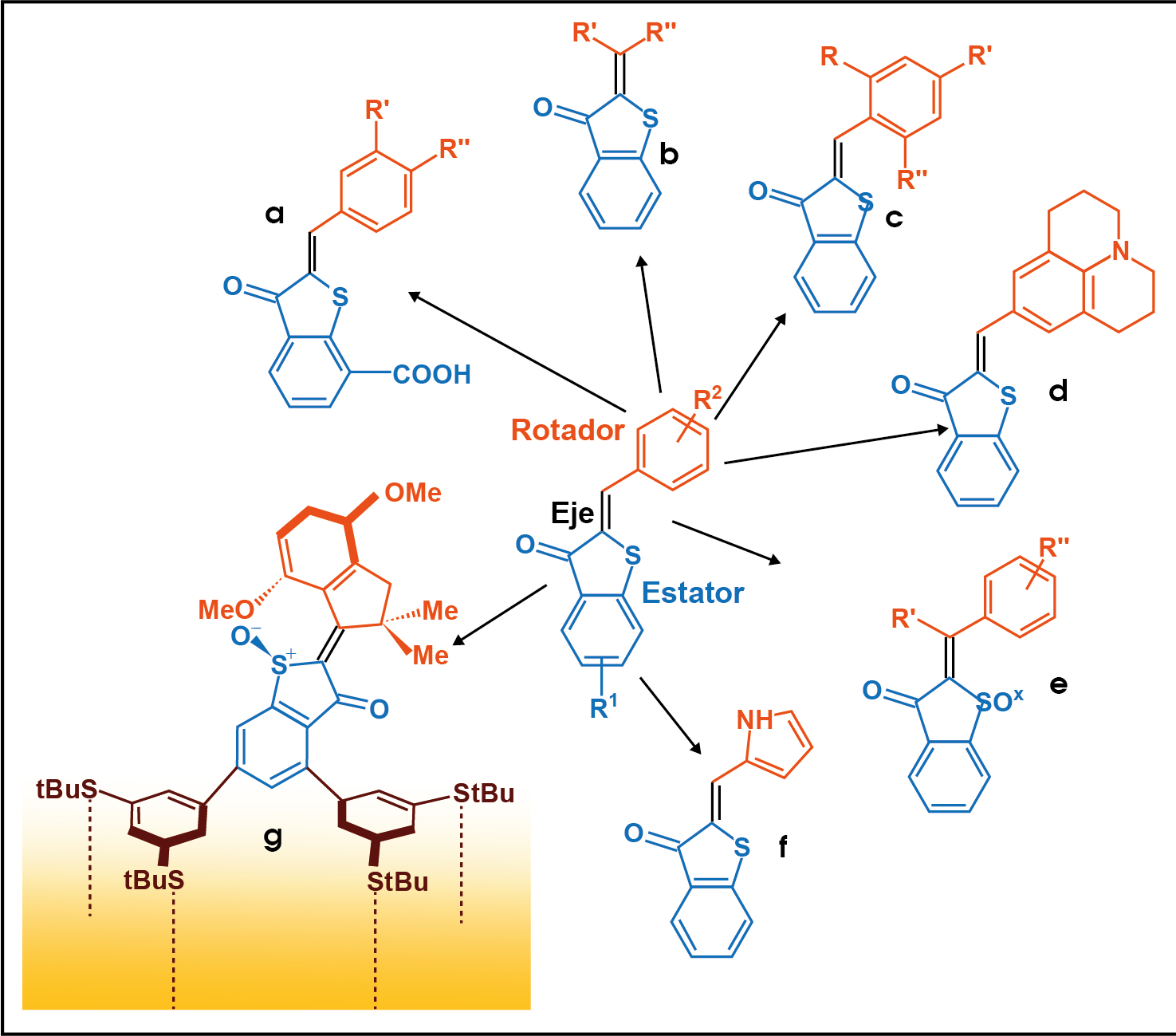
A partir de la estructura general de la molécula HTI se han propuesto diversos rotores moleculares que se adaptan a diferentes aplicaciones por sus características individuales, donde los diferentes sustituyentes son el principal distintivo entre variantes (Figura 2).
Entre los rotores moleculares basados en HTI, reportados para diversas aplicaciones, se encuentran los unidos a péptidos inhibidores y derivados de aminoácidos en posiciones meta y para (2a) también denominados cromopéptidos, donde se demostró que la presencia de los péptidos no afecta los procesos de fotoisomerización del HTI (Regner et al., 2012; Eggers et al., 2001). Las estructuras de HTI ω-aminoácido con tioesteres (pHTI) protegidos por Boc (Kitzig et al., 2016), así como los sistemas simétricos y no simétricos de bis-hemitioíndigo se presentan como grandes candidatos para aplicaciones celulares (Hoffmann et al., 2019a).
Además, se destacan los rotores HTI con cuatro sustituyentes diferentes (2b) en el eje del rotor (Gerwien et al., 2017) con sus respectivos métodos de síntesis: los rotores hemitioíndigos torcidos (twisted) (2c, 2d), por sus particulares movimientos de rotación respecto al doble enlace y entorno al enlace sencillo (Wiedbrauk et al., 2016), y los fotointerruptores moleculares derivados de sulfóxidos y sulfonas (Köttner et al., 2020) de HTI (2e), los cuales presentan cambios significantes en el fotocromismo de la molécula.
Otra variación de HTI son los que proponen Zweig y Newhouse en 2017 (2f), en donde el fragmento estilbeno es reemplazado por un rotador de arilpirrol (Zweig y Newhouse, 2017). Derivado de este trabajo, se reportó un grupo de moléculas que permitió estudiar los efectos de la extensión π del pirrol con diversos sustituyentes (Zweig et al., 2019). La primera aplicación celular de estos rotores fue como antimitótico (para inhibir la mitosis), controlado por luz exclusivamente (Sailer et al., 2021). Hoffmann et al. (2019b), (2g) reporta el primer rotor basado en HTI con una base de tioéter que admite el acoplamiento en superficies metálicas.
3. Síntesis de HTI
En general, cuando se sintetizan rotores moleculares unidireccionales es deseable obtener un solo enantiómero porque mientras cada molécula individual va en una rotación unidireccional, en una mezcla racémica el promedio de dirección del movimiento de las moléculas se ve afectado considerablemente, lo que dificulta tener control sobre el movimiento del rotor (Cnossen et al., 2014; Kassem, 2017).
Dentro de las metodologías reportadas para la síntesis de los HTI destacan las que se presentan en la Figura 3. En 2015, Guentner et al . reportaron una ruta sintética de tres pasos con precursores de fácil acceso; los rotores con cuatro sustituyentes diferentes en el doble enlace se pueden obtener a partir de HTI clorados (3a, 3b), que son fáciles de sustituir a través de reacciones de sustitución nucleofílica (como reacciones de Suzuki, Sonogashira o de acoplamiento cruzado Stille) dependiendo del sustituyente que se va a introducir y su carácter electrónico y estérico (Gerwien et al., 2017).
En 2017 se propuso una ruta de síntesis (3c) en donde es posible introducir más grupos funcionales con facilidad (Kink et al., 2017), y una ruta que permite introducir sustituyentes con considerablemente mayor impedimento estérico en el fragmento del rotor (Huber et al., 2017). Se tiene registro de una ruta sintética mediada por yodo (3e).
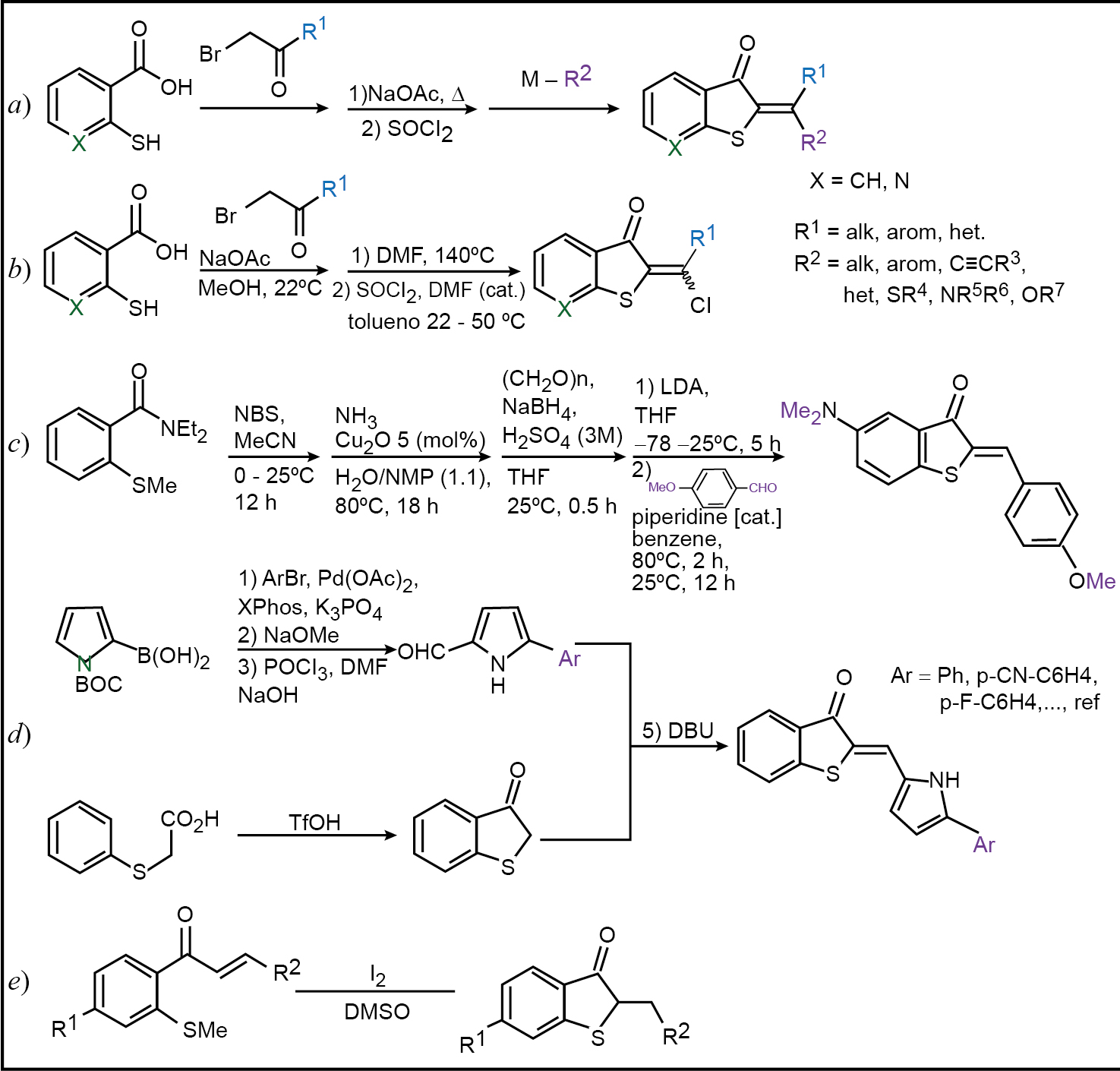
Fuente: elaboración propia. Nota: reportadas en los últimos 10 años.
FIGURA 3 Rutas sintéticas para obtener HTI *
Además, la síntesis de los compuestos derivados de hemitioíndigo con un rotador de arilpirrol (3d) reportada en el trabajo de Zweig et al. (2019), se da por un ensamblaje convergente que ayuda a obtener los fotointerruptores con rendimientos moderados (Zweig y Newhouse, 2017). Para la síntesis de péptidos que contienen rotores basados en HTI, destacan en fase sólida con grupos protectores (Kitzig et al., 2016) y la síntesis de cromopéptidos haciendo uso del auxiliar TMB (Kitzig y Rück-Braun, 2017).
4. Mecanismo de fotoisomerización de HTI
El proceso de fotoisomerización ha sido considerado por años como un proceso extremadamente rápido y, a menudo, involucra pasos intermedios inducidos por fluctuaciones térmicas que hacen posible obtener el movimiento unidireccional deseado (Liu, 2001), y ha sido estudiado haciendo uso de diversos métodos espectroscópicos, entre ellos los experimentos de sonda de bombeo UV/Vis, usada para identificar los procesos ultrarrápidos de fotoisomerización en ambas direcciones.
Si bien se han reportado varios estímulos externos para modificar la configuración espacial de un rotor molecular como el potencial electroquímico inducido o el cambio de carga (Balzani et al., 2000), la conmutación por luz surge a partir de la intención de mimetizar el comportamiento de los sistemas naturales, cuya configuración espacial se da a partir de la absorción de luz (García-López et al., 2019; Cameron y Eisler, 2018).
El proceso de fotoisomerización se refiere a la transformación de un compuesto de una forma isomérica a otra, inducida por la irradiación de luz (Ceroni et al., 2014). Por décadas, se aceptó la idea de que el mecanismo de la reacción de estos procesos se regía únicamente por procesos demandantes de volumen OBF (one-bond-flip por sus siglas en inglés), que consiste en el giro de una mitad de la molécula por rotación alrededor de un doble enlace: C = C, C = N, N = N, etc. (Liu, 2001).
En 1985 se propuso un mecanismo alterno llamado hula-twist (HT), cuyo objetivo principal fue esclarecer los procesos que no cumplían con las características del OBF. El hula-twist involucra la isomerización del doble enlace y del enlace sencillo en la molécula de manera simultánea y se considera un proceso de conservación de volumen debido a que solo una unidad C-H gira en el plano de la molécula mientras el resto de la molécula se mantiene respecto al plano general de la misma (Liu et al., 2006; Ramamurthy, 2012).
En ocasiones, los procesos mencionados resultan en los mismos productos; sin embargo, no todas las moléculas presentan el mecanismo de fotoisomerización HT. En solución, los procesos OBF son favorecidos gracias a sus condiciones sin confinar, mientras que bajo reacciones de confinamiento el HT es el favorecido (Ramamurthy, 2012). Es común identificar estos procesos en la fotoisomerización de HTI, dónde se favorece el HT en estructuras cristalinas de los isómeros, fácilmente separables e induce un movimiento más controlado (Gerwien et al., 2018a).
Algunas características del HT son las siguientes: a) sólo compuestos con un hidrógeno vinílico central pueden ser isomerizados bajo este mecanismo, b) a pesar de cumplir el primer requisito, los sustituyentes en cada mitad de la molécula son decisivos, c) se debe considerar la simetría de la molécula para determinar si los productos se definan selectivamente y d) por lo general los productos son confórmeros altamente energéticos (Ramamurthy, 2012).
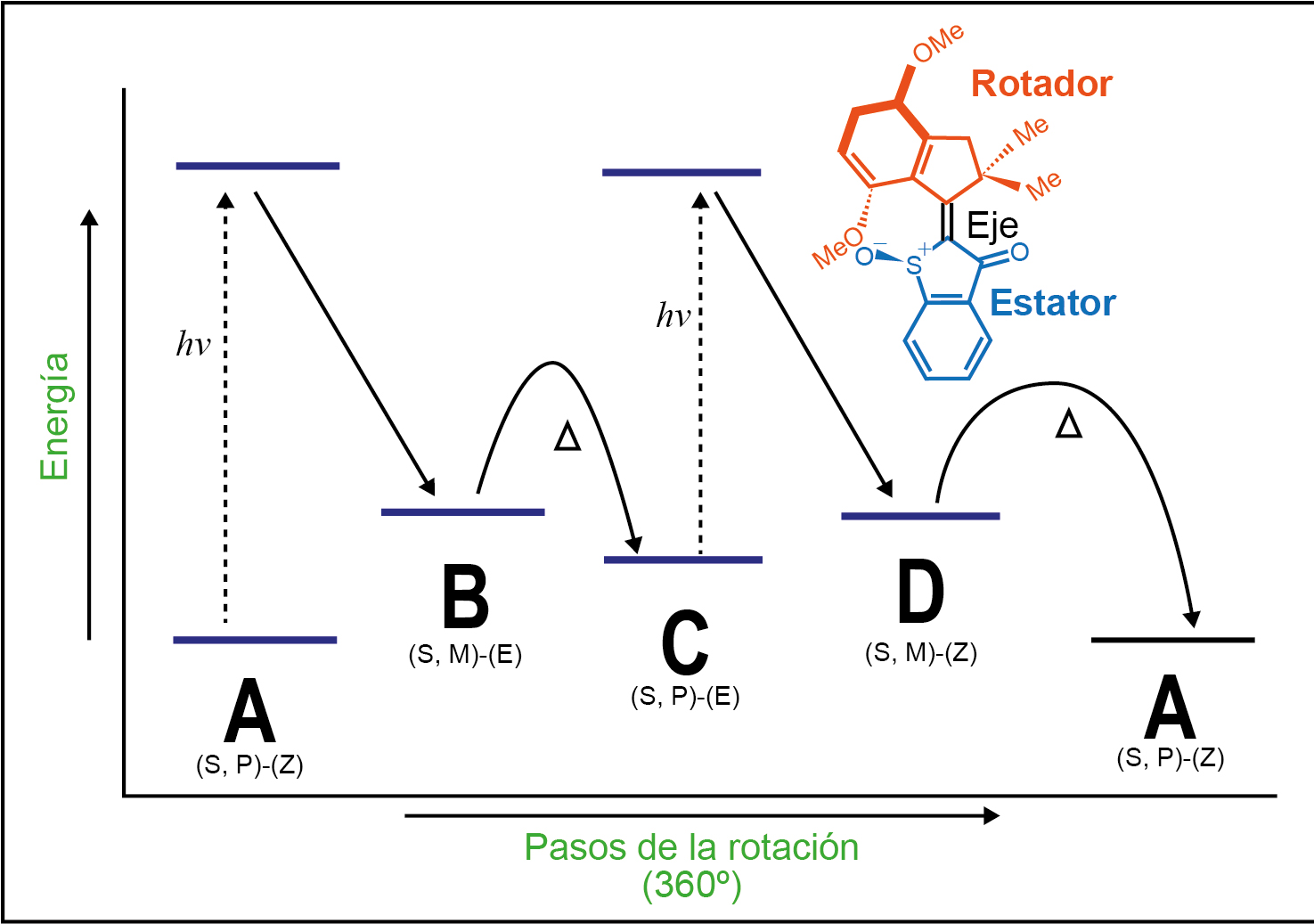
De manera general, se han determinado cuatro estados energéticos estables y metaestables de manera experimental con diferentes configuraciones conformacionales, de los cuales el isómero C es el más estable termodinámicamente hablando, seguido por A, como se observa en la Figura 4, donde también se aprecia la barrera energética de la inversión helicoidal térmica (THI por sus siglas en inglés) que conduce a la conversión del isómero B a C, así como la conversión de D a A a temperatura ambiente (adaptación de Wilcken et al., 2018). El paso limitante en el mecanismo de fotoisomerización para obtener la rotación unidireccional de 360° es la inversión helicoidal térmica (Huber et al., 2017) de D a A, cuya barrera energética ha sido calculada en 5.54 kcal mol-1 (Wilcken et al., 2018).
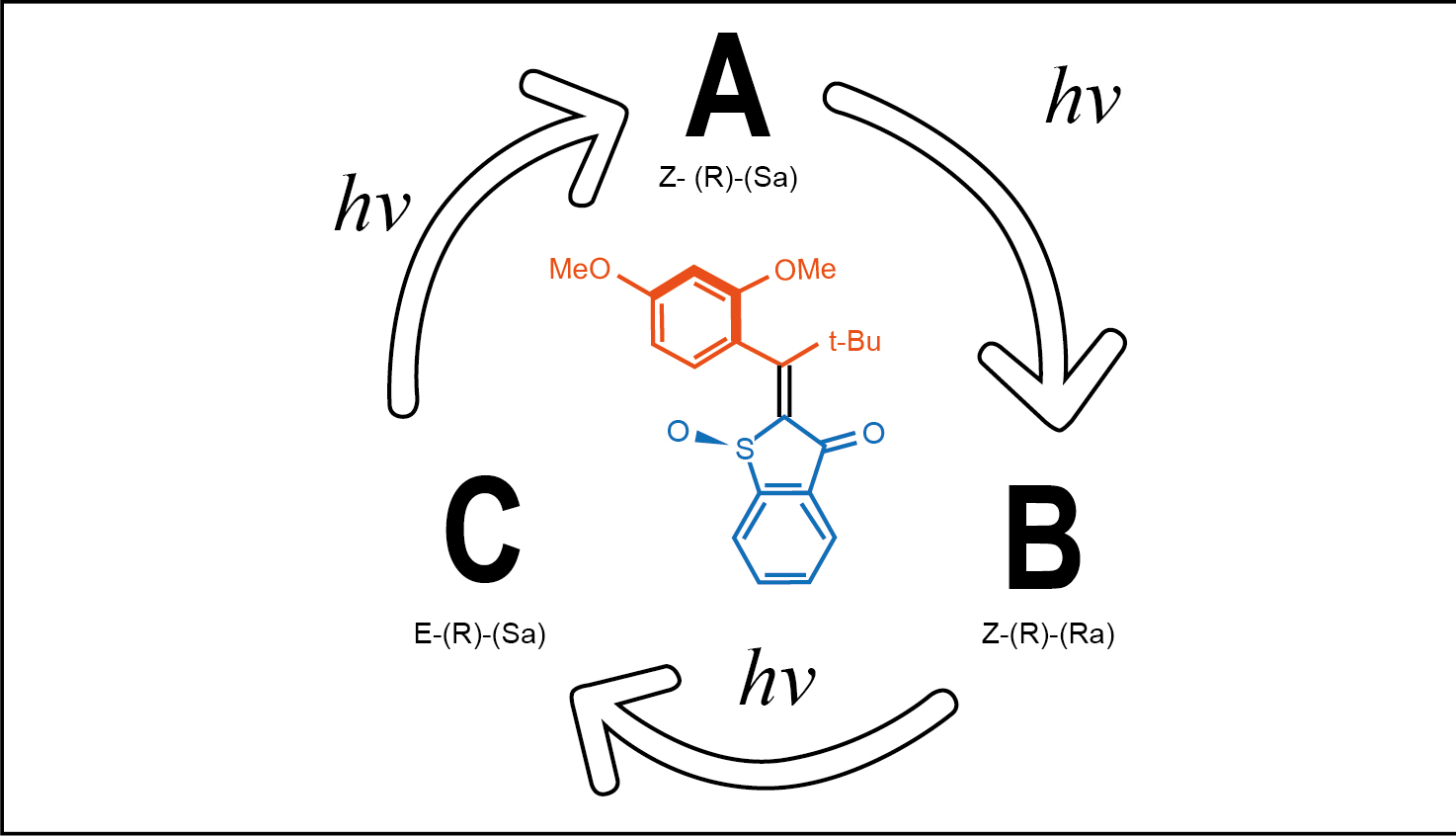
El trabajo de Gerwien et al. (2018a) reportó cuatro isómeros con una alta estabilidad; con esto, fue posible identificar los procesos fotoquímicos individuales en condiciones ambiente y sin la interferencia de procesos térmicos (Figura 4). A partir de estas observaciones, fue posible favorecer un ciclo ABC (Figura 5) inducido por fotones para un nuevo motor molecular cuya unidireccionalidad es alcanzada en solo tres pasos, que involucra tres isómeros resultantes de tres procesos diferentes: rotación de enlace sencillo, hula-twist e isomerización del doble enlace (SBR, HT y DBI). Para favorecer el paso del isómero B a C, se propuso un hula-twist bajo condiciones de temperatura de -50 °C (Gerwien et al., 2018b).
Los isómeros involucrados son térmicamente estables, lo que posibilita aislarlos y caracterizarlos. También fue reportada una ruta de isomerización en forma de “ocho”, que se apoya de procesos HT, SBR y DBI, lo cual permite la interconversión eficiente de los diaestereoisómeros de manera repetitiva y direccionada (Gerwien et al., 2019).
Fuente: adaptado de Wilcken et al., 2018.
FIGURA 4 Perfil energético simplificado de la rotación unidireccional del isómero S del motor
Fuente: adaptado de Gerwien et al., 2018a.
FIGURA 5 Ruta de interconversión de motor mediante tres fotorreacciones consecutivas sin involucrar los procesos térmicos
4. 1. Propiedades fotoquímicas y fotofísicas de HTI
En los rotores hemitioíndigos la parte cromófora se localiza en el centro de la molécula, justo en el doble enlace (Petermayer y Dube, 2018). Se les considera como excelentes propuestas para aplicaciones biológicas, ya que se trata de moléculas fotocromáticas sensibles a luz de baja energía (400-670 nm). Derivado de esto, se han reportado diversos rotores moleculares basados en HTI impulsados exclusivamente por luz visible no destructiva con perspectiva a aplicaciones farmacológicas (Wiedbrauk, 2015).
Otra característica clave de estos compuestos es tener un alto control del movimiento de rotación a causa de la diferencia de longitud de onda que absorbe cada isómero, donde la absorbancia de ambos isómeros se sobrepone en el área del azul-verde (Cordes et al., 2008). La introducción de sustituyentes en ambos fragmentos puede cambiar la absorbancia en cada isómero, lo cual garantiza procesos altamente selectivos y con rendimientos considerables (Wiedbrauk, 2015).
En el Cuadro 1 se aprecian diferentes longitudes de onda reportada para rotores HTI en los últimos diez años, tanto en el isómero E como Z, que dependen sobre todo de los sustituyentes que se tengan en los fragmentos de la molécula y de la polaridad del solvente. El producto del inciso b), Cuadro 1, presenta una absorción en el desplazamiento rojo; con esto, es posible manipular la longitud de onda deseada al introducir grupos funciones en los fragmentos del rotor (Kink et al., 2017).
Cuadro 1 Longitud de onda máxima en isómeros E y Z de diferentes rotores HTI
| Compuesto | λmáx E | λmáx Z | Solvente |
| a) | 490 nm | 440 nm | CH3Cl |
| b) | 625 nm | 500 nm | Tolueno |
| c) | 444-480 nm | 400-433 nm | CH2Cl2 |
| Compuesto | λmáx E | λmáx Z | Solvente |
| d) | 503 nm | 459 nm | CH2Cl2 |
| f) | 530 nm | 385 nm | CH2Cl2 |
| g) | 532 nm | 500 nm | Ciclohexano, CH2Cl2, DMSO |
Fuente: elaboración propia.
La estabilidad de los isómeros Z (estable) y E (metaestable) se ve influenciada por la adición de grupos sustituyentes en los fragmentos estilbeno y tioindigo, cuya influencia en el mecanismo de fotoisomerización se ve reflejada en cambios en la longitud de onda necesaria para inducir el proceso y en el solvatocromismo del sistema; se ha observado que los efectos de los sustituyentes en la dinámica de reacción compensan las deformaciones estructurales con rápidas redistribuciones de carga (Nenov et al., 2010). La presencia de sustituyentes en el fragmento estilbeno, a su vez, implica cambios en la velocidad de reacción en el paso limitante de la isomerización (Cordes et al., 2008).
Considerando la polaridad de la molécula reportada por Kitzig et al. (2017), los grupos que donan y retiran electrones tienen un efecto inverso en la velocidad de fotoisomerización, dependiendo de la parte de la molécula HTI en la que están unidos (Kitzig et al., 2016). Al introducir grupos sustituyentes de donadores al fragmento estilbeno se pudo aumentar la velocidad de fotoisomerización de fotointerruptores; sin embargo, con la introducción de grupos donadores demasiado fuertes (como NH2 o NMe2) el efecto fue un decremento en la velocidad del proceso (Maerz et al., 2014). Además, se ha reportado que al incrementar el impedimento estérico y reducir la densidad de electrones del sustituyente se modifica la dinámica de los estados excitados en el mecanismo de fotoisomerización (Wilcken et al., 2020).
Las estructuras de HTI ω-aminoácido con tioesteres (pHTI) protegidos por Boc (Kitzig et al., 2016), así como los sistemas simétricos y no simétricos de bis-hemitioíndigo, se presentan como grandes candidatos para aplicaciones celulares, cuya geometría varía de plana a torcida dependiendo de los sustituyentes en ambos fragmentos de tioíndigo (Hoffmann, 2019b).
Los experimentos en solventes polares y no polares (Cuadro 1) han sido estudiados desde 2010 y han demostrado las fotorreacciones Z→E y E→Z del HTI. Nenov et. al. reportaron en 2010 la isomerización de HTI sin sustituyentes en ciclohexano, que depende de la polaridad del disolvente (Cuadro 1, inciso g); la rotación de un solo enlace completo (en DMSO) o de doble enlace (en ciclohexano) puede ser inducida por la luz visible (Wiedbrauk et al., 2017).
5. Aplicaciones de rotores moleculares basados en HTI
Como se ha mencionado, en particular estos rotores moleculares resultan ventajosos debido a su sensibilidad a luz visible, lo que los incluye en la categoría de procesos sostenibles y de bajo costo y los hace ideales para aplicaciones farmacológicas y biológicas. Lejos de limitarse a estos campos de aplicación, los derivados de HTI tienen potencial tanto como interruptores como motores en reconocimiento molecular (Cameron y Eisler, 2018; Aprahamian, 2020).
En virtud de sus propiedades biológicas y su fácil isomerización al ser irradiados con luz visible, en la última década los HTI han destacado en el desarrollo de cromopéptidos para inducir cambios conformacionales y fotomodulación, inhibición de enzimas y reconocimiento molecular (Kink et al., 2017; Kitzig et al., 2016; Nie et al., 2019). Se han aplicado en materiales de membranas bicapa, como máquinas supramoleculares y encapsulación de compuestos activos (Wiedbrauk y Dube, 2015).
Cabe resaltar la aplicación reportada por Sailer et. al. (2021), donde, al aplicarse la estructura del inciso d), Cuadro 1, se logró el desarrollo de reactivos fotofarmacéuticos para un control in situ de microtúbulos celulares (citoesqueleto), los cuales son un objetivo primordial para llevar a cabo ensayos moleculares de modulación en alta definición que aseguran un proceso con precisión a una sola célula. A diferencia de otras alternativas, los fotofármacos no requieren de ingeniería genética, por lo que son adaptables entre modelos biológicos (Sailer et al., 2021).
Además, estos interruptores moleculares se han usado en operaciones combinacionales y lógicas secuenciales que fungen como sistemas integradores y estructuras de entrada-salida; debido a la emisión de fluorescencia intermitente, se abre la posibilidad de aplicarlos como un dispositivo de construcción fotónico o incluso para el monitoreo online de la operación de rotores moleculares (Kink et al., 2017). El motor desarrollado por Gerwien et. al. en 2019 muestra en ciclohexano fluorescencia amarilla en los isómeros A y B, mientras que los isómeros C y D no emiten (Gerwien et al., 2019).
En 2020 se reportó el uso de HTI para el fotocontrol de antimicóticos por microtubos denominados HOTubs y HITubs (Sailer et al., 2020). De la misma forma, su uso como farmacóforo es atractivo como resultado del fotocontrol obtenido en largos lapsos in situ (Jia et al., 2018).
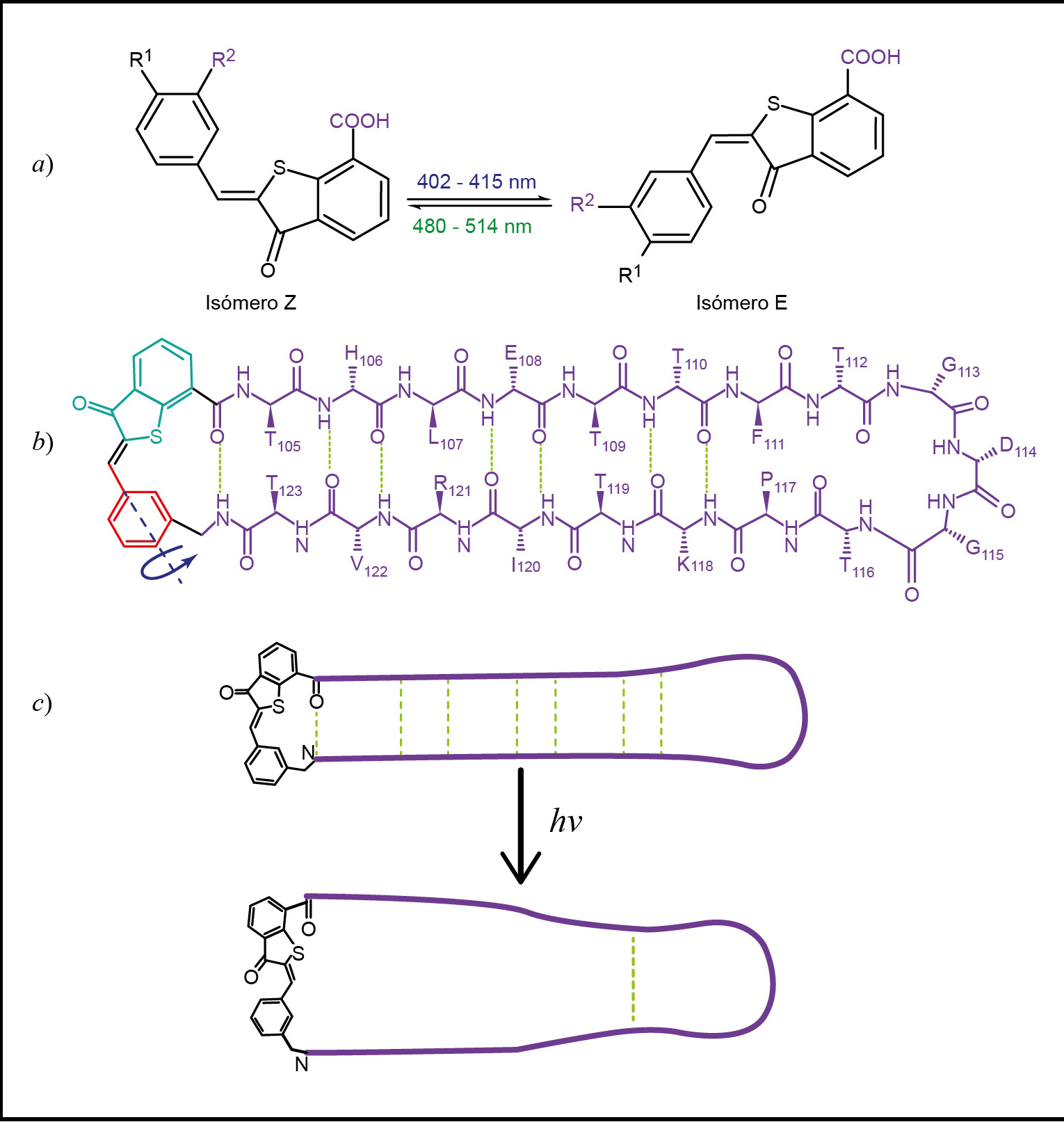
La Figura 6 muestra los siguientes procesos del rotor HTI: a) esquema general del proceso de fotoisomerización del rotor HTI, b) rotor molecular HTI enlazado a β-péptido tipo horquilla, c) proceso de isomerización del rotor HTI enlazado a β-péptido tipo horquilla.
En los rotores HTI con péptidos en posiciones meta y para, se han estudiado sus efectos en el proceso de fotoisomeración del HTI y el comportamiento de la estructura del péptido mediante métodos espectroscópicos ultrarrápidos. Bajo irradiación de luz (a) se demostró que la incorporación de un HTI a la estructura de péptidos no cambió significativamente el rendimiento del proceso de fotoisomerización.
Uno de los estudios en estas estructuras de mayor relevancia ha sido en péptido con estructura estable tipo horquilla β (b), donde, después de irradiar con luz el rotor molecular en configuración Z, se pudo establecer el proceso de rotación y la ruptura de los puentes de hidrógeno en una escala de tiempo de 2-3 ns al alcanzar el equilibro en el isómero E (c) (Regner et al., 2012).
Prospectiva
Los rotores moleculares tienen un amplio campo de aplicación que van desde las médicas y farmacológicas hasta la innovación de materiales inteligentes y sistemas lógicos.
Los rotores basados en hemitioíndigos, al ser manipulados de manera óptima con luz visible, obtienen un carácter sostenible mayor frente a varias de las estructuras propuestas y se prevé un amplio uso de estas moléculas en tratamientos fotofarmacológicos o de imagenología. Aunque no se limita a esto, su desarrollo se ha enfocado en su mayoría en estudios recientes en sus propiedades al interactuar con péptidos, lo que guiará a un desarrollo acelerado para la modificación de dichas estructuras.
Además, se espera que sus futuras aplicaciones contribuyan en sobremanera en el entendimiento de procesos fotoquímicos y químicos en el almacenamiento de energía, en la realización de trabajos a escala mayor y como soporte de reacciones químicas.
Conclusiones
Los rotores HTI han sido relevantes en el estudio de los procesos de fotoisomerización, fenómeno de especial interés cuando se incluyen a la estructura los péptidos. Por lo tanto, es determinante para predecir las características que requiere el medio, promover una mayor estabilidad térmica y tiempos de vida media mayores.
La polaridad del solvente también gana importancia en este tipo de rotores, ya que, al ser fácilmente incluidos en estructuras de péptidos, son excelente candidatos para el transporte de fármacos; de este modo, el solvente es decisivo para determinar su farmacodinámica y la posibilidad de explotar sus propiedades fluorescentes.
Por último, estos rotores moleculares han sido utilizados en sistemas supramoleculares host-guest con el objetivo de alcanzar un control fotoquímico alto, además de que sus principales aplicaciones consisten en transporte de fármacos y la configuración de cadenas grandes de péptidos con la ruptura de fuerzas intramoleculares (puentes de hidrógeno) que posibilitan manipular sistemas biológicos con alta precisión.