Introducción
Las plantaciones de cacao (Theobroma cacao) constituyen un agroecosistema de gran relevancia cultural, económica y ambiental en el sureste de México (Garay-Peralta et al. 2024). El estado de Tabasco ocupa el primer lugar en producción de cacao, con 34 260 ha cultivadas de las que dependen aproximadamente 31 139 familias (Vázquez-Vidal y López-Rodríguez 2021, SIAP-SAGARPA 2023). Del mismo modo, este agroecosistema ha incrementado su importancia ecológica, ya que se establece bajo la sombra de un dosel diversificado y estratificado semejante al de las selvas tropicales (Torres-de-la-Cruz y Ortiz-García 2019). Esta característica ha favorecido la conectividad en paisajes altamente fragmentados, dado que Tabasco es una de las entidades federativas más afectadas por la deforestación en México (Ochoa-Gaona et al. 2019). Actualmente, el estado ha perdido el 90% de su cobertura vegetal natural, y la selva alta perennifolia representa alrededor del 5% de su superficie (Cámara-Cabrales et al. 2019, Ochoa-Gaona et al. 2019). En este contexto, el agroecosistema cacao se presenta como una alternativa estratégica para la conservación de la fauna silvestre en la región (Torres-de-la-Cruz y Ortiz-García 2019).
Uno de los grupos de vertebrados mejor adaptados a las plantaciones de cacao son las aves (Ocampo-Ariza et al. 2023). En México se han realizado estudios de avifauna asociada a este agroecosistema en los estados de Veracruz (Estrada et al. 1997), Chiapas (Rangel-Salazar et al. 2013) y Tabasco. En este último se registraron 144 especies de aves diurnas y nocturnas distribuidas en 35 familias y 13 ordenes (Arriaga-Weiss 1985, Greenberg et al. 2000, Ibarra et al. 2001, Trejo-Pérez 2007). Esto representa el 30% de las aves que actualmente se distribuyen en la entidad (Arriaga-Weiss et al. 2019). Este número es comparable con la cantidad de especies reportadas en algunos remanentes de selva alta perennifolia en Tabasco, como el Parque Estatal de la Sierra (125 especies) y el Complejo Ecológico de Agua Selva (140 especies) (Arriaga-Weiss et al. 2008, Sánchez-Soto 2022). A pesar de su relevancia ecológica el agroecosistema cacao enfrenta presiones económicas para permanecer, debido principalmente a las pérdidas por enfermedades como la moniliasis ocasionada por el hongo Moniliophthora roreri o la mancha negra por Phytophtora capsici (Torres-de-la-Cruz et al. 2023). Esto ha llevado a los productores de cacao a reducir los árboles de sombra o a homogenizar las parcelas con clones resistentes, disminuyendo la diversidad vegetal (Chávez-García 2024). En ocasiones los dueños abandonan sus parcelas o las derriban para establecer monocultivos (Torres-de-la-Cruz y Ortiz-García 2019). Esta pérdida de diversidad florística o el abandono de las plantaciones puede incidir de forma nociva en la riqueza de aves que utilizan este agroecosistema para subsistir (Greenberg et al. 2000, Ibarra et al. 2001, Torres-de-la-Cruz y Ortiz-García 2019).
Una forma de evaluar el efecto de las actividades humanas sobre la avifauna es mediante el estudio de la ecología trófica (Herpin et al. 2025), la cual analiza las relaciones entre las aves y los recursos alimenticios disponibles (García 2016). Para ello, se documentan los gremios tróficos, se identifican las presas o fuentes de alimento y se evalúa su disponibilidad en el ecosistema (Romero-Díaz et al. 2022). Un gremio trófico se define como un conjunto de especies, taxonómicamente relacionadas o no, que se benefician de un mismo tipo de recurso y lo obtienen de manera similar (López-Muñoz et al. 2022). Mientras que una interacción trófica es una relación biológica que ocurre cuando un organismo se alimenta de otro para obtener energía (Zhang et al. 2018). En el caso particular de las interacciones ave-planta, estas ocurren cuando las aves consumen órganos vegetales de diversas especies (García 2016). Dichas interacciones pueden ser mutualista o antagonista (Avalos et al. 2023).
A pesar del conocimiento que se tiene sobre la avifauna asociada al agroecosistema cacao en Tabasco, existe un vacío de información sobre las interacciones tróficas ave-planta, ya que no se tienen registros sobre los árboles frutales, maderables u ornamentales de las que se alimentan los diferentes grupos de aves (Ibarra et al. 2001, Trejo-Pérez 2007). El único trabajo que hace alusión a la ingesta de un recurso vegetal, es el realizado por Arriaga-Weiss (1985), en donde menciona cuatro especies de aves que se alimentan de la mazorca de cacao: Melanerpes aurifrons, Amazona albifrons, Eupsittula nana y Momotus lessoni. Las primeras dos especies fueron registradas mediante observaciones directas y las otras dos por medio entrevistas (Arriaga-Weiss 1985). Pese a esto, se desconoce la mayoría de las plantas que forman parte de la dieta habitual de los grupos de aves en este agroecosistema (Trejo-Pérez 2007). Conocer las plantas utilizadas como recurso alimenticio para las aves en estas plantaciones puede proporcionar información valiosa para atraer especies de interés: polinizadoras o dispersoras de semillas (Greenberg et al. 2000, Van-der Wal et al. 2012). Del mismo modo, puede ser un incentivo para generar negocios alternativos como el aviturismo y ofrecer beneficios económicos directos al productor, mientras se conserva el agroecosistema, como se ha realizado con el mono aullador (Alouatta palliata) (Valenzuela-Córdova et al. 2015). Por lo anterior, el objetivo de este trabajo fue caracterizar la riqueza de aves y las interacciones tróficas ave-planta en el agroecosistema cacao en Tabasco, mediante revisión de literatura y la obtención de datos en campo. Esto permitirá tener una base de datos actualizada, con aspectos alimenticios que sentarán las bases para elaborar programas de conservación de aves en el agroecosistema.
Materiales y métodos
Área de estudio
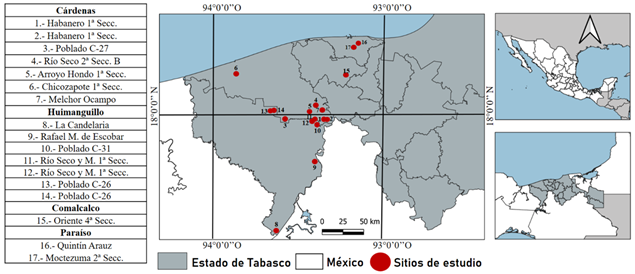
El estudio se llevó a cabo en 17 plantaciones de cacao de la subregión Chontalpa (Figura 1, Tabla 1), que es la principal zona productora de cacao en Tabasco (SIAP-SAGARPA 2023). Esta subregión se ubica en la parte occidental del Estado, y es parte de la subprovincia fisiográfica denominada Llanuras y Pantanos Tabasqueños, la cual presenta clima cálido húmedo con abundantes lluvias en verano, una variación isotermal de entre 26 y 28 °C y una precipitación pluvial que va de 2000 a 2500 mm anuales (INEGI 2017). La mayoría de las plantaciones visitadas se ubican en esta subprovincia, y solo una de ellas se localiza en la subprovincia fisiográfica denominada Sierras del Norte de Chiapas, en el ejido La Candelaria, municipio de Huimanguillo, la cual presenta clima cálido húmedo con lluvias todo el año, variación isotermal de 22 a 24 °C y variación pluvial de 3000 a 3500 mm anuales (INEGI 2017) (Figura 1, Tabla 1).
Tabla 1 Características principales de los sitios de estudio en el estado de Tabasco, México
| Plantación | Localidad | Coordenadas | Superficie | Árboles de sombra | Matriz de Vegetación |
|---|---|---|---|---|---|
| Municipio de Cárdenas | |||||
| 1 | Habanero 1aS. | 17°57’40’’N, 93°20’23’’O | 0.45 h | Cedro, Frutipan | Cultivo-Cítricos |
| 2 | Habanero 1aS. | 17°58’13’’N, 93°19’52’’O | 0.075 h | Moté, Amate | Cultivo-Cítricos |
| 3 | Poblado C-27 | 17°59’05’’N, 93°35’31’’O | 2 h | Melina, Moté | Acahual |
| 4 | Río Seco 2a S. B | 18°04’16’’N, 93°23’12’’O | 0.15 h | Moté, Apompo | Acahual |
| 5 | Arroyo Hondo 1aS. | 18°0’50’’N, 93°25’59’’O | 0.5 h | Ceiba, Almendro | Acahual |
| 6 | Chicozapote 1aS. | 18°12’39’’N, 93°51’2’’O | 3 ha | Apompo, Mango | Humedales y Potreros |
| 7 | Melchor Ocampo | 18°01’59’’N, 93°21’19’’O | 4 ha | Cocoite, Apompo | Cultivo-Banano |
| Municipio de Huimanguillo | |||||
| 8 | La Candelaria | 17°19’19’’N, 93°36’28’’O | 6 ha | Caoba, Tatuán | Selva Alta Perennifolia |
| 9 | Rafael M. de Escobar | 17°43’19’’N, 93°22’59’’O | 0.75 ha | Palo mulato, Amate | Cultivo-Maíz |
| 10 | Poblado C-31 | 17°57’20’’N, 93°23’15’’O | 0.10 ha | Melina, Teca | Potreros |
| 11 | Río Seco y M. 1aS | 17°58’38’’N, 93°23’12’’O | 0.92 ha | Moté, Cedro | Acahual y Urbanización |
| 12 | Río Seco y M. 1aS | 17°58’31’’N, 93°23’10’’O | 1 ha | Ceiba, Frutipan | Acahual y Urbanización |
| 13 | Poblado C-26 | 18°01’54’’N, 93°39’56’’O | 0.40 ha | Melina, Moté | Cultivo-Maíz |
| 14 | Poblado C-26 | 18°02’20’’N, 93°39’23’’O | 0.05 ha | Cedro | Potrero |
| Municipio de Comalcalco | |||||
| 15 | Oriente 4aS. | 18°13’21’’N, 93°13’25’’O | 6 ha | Melina, Teca | Acahual |
| Municipio de Paraíso | |||||
| 16 | Quintín Arauz | 18°22'16"N, 93°12'42"O | 8 ha | Caoba, Frutipan | Acahual y Humedal |
| 17 | Moctezuma 2aS. | 18°21’07"N, 93°12´52"O | 50 ha | Moté, Amate | Acahual y Humedal |
Para generar un inventario actualizado de aves asociadas al agroecosistema cacao en Tabasco se consultaron los artículos de Arriaga-Weiss (1985), Greenberg et al. (2000), Ibarra et al. (2001) y Trejo-Pérez (2007), generando una base de datos con 144 especies de aves pertenecientes a 35 familias y 13 órdenes. Los nombres científicos fueron actualizados siguiendo la AOS (Chesser et al. 2023) y los nombres comunes de la propuesta de Berlanga et al. (2019). Los taxones que ya no resultaron válidos para Tabasco fueron excluidos de la base de datos (Chablé-Santos et al. 2005, Arriaga-Weiss et al. 2019, Chesser et al. 2023). Adicionalmente, se agregó al listado el estatus residencial de las especies siguiendo el trabajo de Chablé-Santos et al. (2005); los gremios tróficos y las preferencias de ambientes siguiendo a Howell y Webb (1996) y Van-der Wal et al. (2012); y las categorías de la NOM-059 (SEMARNAT 2010).
El inventario actualizado se completó con 29 recorridos diurnos (9:00 - 12:00 h) y 12 nocturnos (22:00 - 01:00 h) en 17 plantaciones de cacao, durante el periodo que va de abril del 2023 a abril del 2024. Para los registros de aves diurnas se utilizó el método de transectos en franja, en el que se registran todas las especies de aves detectadas de manera visual y auditiva, dentro del ancho y longitud del transecto, mientras se camina de forma unidireccional en la franja, sin detenerse, retroceder o mirar hacia atrás (Seber 2002). Para ello, se establecieron de dos a cuatro transectos por plantación, con un ancho de 15 a 20 m dependiendo la dificultad de visualización. La longitud de cada transecto varió entre 200 y 1 000 m continuos, dependiendo la superficie de cada cacaotal, tratando de abarcar la mayor extensión posible para incluir los microhábitats disponibles en cada elemento (Selém-Salas et al. 2011). Los avistamientos fueron realizados por una sola persona en cada transecto a una velocidad de 1.0 km/h, para minimizar el efecto de observador (Arriaga-Weiss et al. 2008, Selém-Salas et al. 2011). Los avistamientos se realizaron con binoculares Brunton Eterna 12x45, una cámara Canon EOS T7 55mm-300mm y una cámara Nikon Coolpix P610 con zoom óptico de 60X. Durante los recorridos también se registraron las interacciones tróficas: ave-planta. Se identificaron las especies de ave, las especies de plantas y el órgano vegetal consumido por el ave. Las aves se identificaron siguiendo a Howell y Webb (1995). Las plantas se identificaron con las guías de Maldonado-Mares et al. (2007) y Magaña-Alejandro (2010). Las plantas que no pudieron ser identificadas en campo fueron colectadas y se llevaron para su determinación al Laboratorio de Sistemática Vegetal del Colegio de Postgraduados, Campus Tabasco.
Los recorridos nocturnos se llevaron a cabo en las cinco plantaciones con mayor superficie. En cada parcela se establecieron transectos de 500 m de longitud y 10 m de ancho en donde se colocaron estaciones de llamado cada 100 m. En cada estación se empleó el método de la provocación auditiva que consiste en emitir vocalizaciones pregrabadas de las especies nocturnas en la región (Rodríguez-Hernández et al. 2022). Los llamados se realizaron con una bocina Select Sound de 2000 watts con un alcance radial de 25 m. La duración de cada llamado varió de 5 a 15 min con periodos de espera de 5 min. Las grabaciones se obtuvieron de la base de datos de Xeno-Canto (2023). El esfuerzo de muestreo total (recorridos diurnos y nocturnos) por plantación fue de: 30 h/hombre para la plantación 8 (La Candelaria); 24 h/hombre para la plantación 17 (Moctezuma 2aS.); 12h/hombre para la plantación 11 y 12 (Río Seco y Montaña 1a Secc.); y 9 h/hombre para la plantación 3 (Poblado C-27). Las demás plantaciones tuvieron un esfuerzo de 3 h hombre-1.
Con la información obtenida de la revisión bibliográfica y los recorridos de campo se generó un inventario actualizado de aves asociadas al agroecosistema cacao en Tabasco, que consistió en los siguientes apartados: a) nombre de la especie, b) preferencia de hábitat, c) gremio trófico, d) estatus residencial y e) categoría de riesgo en México. Los datos se analizaron con herramientas de estadística descriptiva. Del mismo modo, los registros de interacciones tróficas se ordenaron en una matriz que relaciona las especies de aves con las especies de plantas consumidas.
Resultados
Actualización de inventario
Durante los recorridos de campo se registraron 107 especies de aves pertenecientes a 18 órdenes y 34 familias, de las cuales 22 son nuevos registros para el agroecosistema cacao en Tabasco. Con esta información el inventario se actualiza a 165 especies, pertenecientes a 40 familias y 19 órdenes. De estas especies, 120 fueron residentes y 45 migratorias; además, 13 estuvieron sujetas a protección especial, seis amenazadas y dos en peligro de extinción. Las familias con el mayor número de especies registradas son Parulidae, Tyrannidae y Trochilidae, con 25, 17 y 13 especies respectivamente.
Preferencias de hábitat
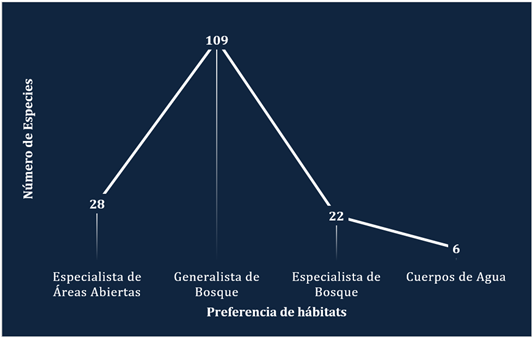
El mayor número de especies de aves son de la categoría: generalista de bosque (GB) (109 especies) (Figura 2). Estas especies requieren áreas boscosas para subsistir, pero son capaces de tolerar condiciones de perturbación en el hábitat. En segundo lugar, se encuentran las especies que son especialistas de áreas abiertas (EAA) (28 especies). Estas aves se benefician de los claros y los bordes del cacaotal, así como otros microhábitats abiertos o semiabiertos en el agroecosistema. Asimismo, identificamos 22 especies de aves especialistas de bosque (EB), estas, fueron más escasas porque suelen ser más sensibles a la fragmentación del hábitat. Finalmente se registraron seis especies asociadas a cuerpos de agua (CA) (Figura 2). Estas especies dependen de grandes extensiones de agua o de humedales circundantes a las plantaciones de cacao.
Gremios tróficos
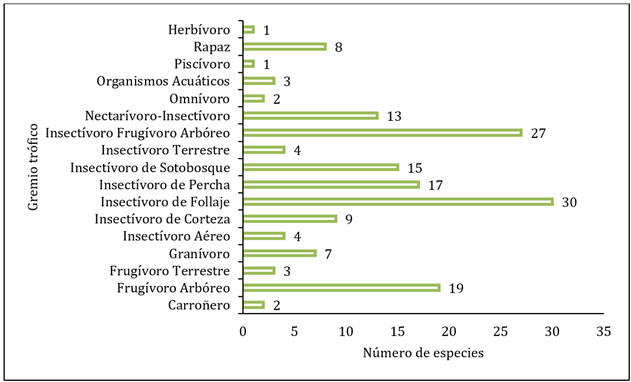
El gremio trófico predominante es el de los insectívoros de follaje (30 especies.) (Figura 3). Estas especies forrajean entre las hojas de cacao y árboles de sombra en busca de artrópodos. Generalmente son especies migratorias de talla pequeña que pertenecen a las familias Parulidae, Vireonidae y Polioptilidae con algunas excepciones. El siguiente gremio es el de los insectívoros-frugívoros arbóreos (27 especies). Estas especies forrajean entre las ramas de los árboles en busca de insectos, pero son capaces de alimentarse de hojas, frutos y néctar, dependiendo la disponibilidad de recursos. Por lo general son especies de talla mediana que pertenecen a las familias Icteridae, Thraupidae y Cardinalidae. En tercer lugar, se encuentra el gremio frugívoro arbóreo (19 especies). Estas son especies con picos fuertes de las familias Psitacidae, Trogonidae y Cracidae.
Riqueza específica
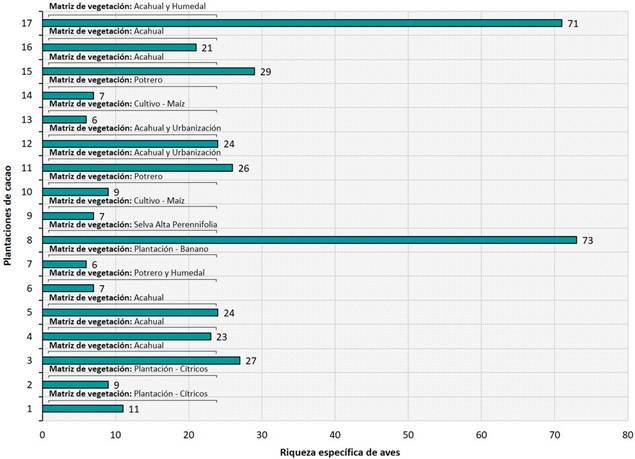
La riqueza específica varió en función de la matriz circundante de vegetación en la que se encuentran las parcelas y la superficie de cada una (Figura 4, Tabla 1). La plantación con un mayor número de especies fue la plantación 8 que se encuentra rodeada de selva alta perennifolia y tiene una superficie de 6 ha. En esta plantación se registraron la mayoría de las especies de aves sujetas a protección especial, amenazadas y en peligro de extinción. Se destaca la presencia del loro corona azul (Amazona farinosa) registrado el 25 de abril de 2024 a las 9:07 h. La segunda plantación con un mayor número de especies fue la 17 que tiene una superficie de 50 ha y se encuentra rodeada de acahuales y humedales. La mayoría de las especies asociadas a cuerpos de agua se encontraron en esta plantación. Se destaca la presencia de la garza tigre (Tigrisoma mexicanum) que se registró anidando en un árbol de ceiba (Ceiba petandra) el 28 de febrero de 2024. Las demás plantaciones rodeadas de acahuales tuvieron un número similar de especies registradas (entre 21 y 29 especies), superando a las plantaciones rodeadas de potreros, cultivos anuales o cítricos (entre 6 y 11).
Interacciones tróficas: ave-planta
Se cuantificaron 70 interacciones tróficas entre 31 especies de aves y 22 especies de plantas. Los recursos vegetales más consumidos fueron frutos (44), seguidos de néctar (26). Las especies de plantas que más recursos alimenticios proporcionaron a las aves fueron el amate (Ficus sp.) para 15 especies de aves, y el gallito (Erythrina fusca), para 12 especies. El carpintero chejé (Melanerpes aurifrons), el perico pecho sucio (Eupsittula nana) y el tordo cantor (Dives dives) fueron las aves que se alimentaron de más especies de plantas, con cinco especies cada una (Figura 5).
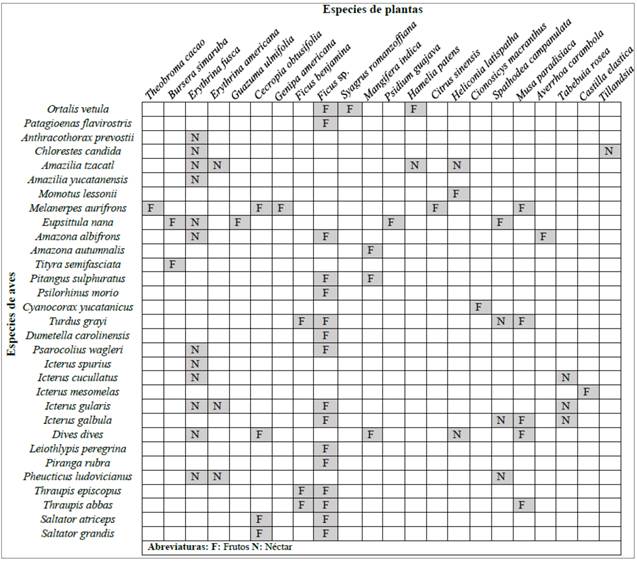
Figura 5 Matriz de interacciones tróficas ave-planta en el agroecosistema cacao en Tabasco. F: Frutos. N: Néctar.
Los ítems alimentarios que no habían sido registrados en la dieta de las aves fueron: los frutos del coralillo (Hamelia patens) y la palmera pindó (Syagrus romanzoffiana) en la dieta de la chachalaca oriental (Ortalis vetula). El fruto del ave del paraíso (Heliconia latispatha) para el momoto corona negra (Momotus lessonii). La sandía de pea (Cionosicys macranthus) para la chara yucateca (Cyanocorax yucatanicus). La jagua (Genipa americana) y el guarumo (Cecropia obtusifolia) para el carpintero chejé. El fruto del árbol de caucho (Castilla elástica) para la calandria cola amarilla (Icterus mesomelas). El tulipán de la India (Spathodea campanulata) para el mirlo café (Turdus grayi). El colorín (Erythrina americana) para el picogordo degollado (Pheucticus ludovicianus). La flor del gallito (Erythrina fusca) para todas las especies que indica la matriz, exceptuando la calandria de Baltimore (Icterus galbula) y el colibrí garganta negra (Anthracothorax prevostii), de las cuales ya existían registros previos. Para el género Ficus en la dieta del chipe peregrino (Leiothlypis peregrina) y la oropéndola cabeza castaña (Psarocolius wagleri). Resultando en un total de 21 nuevos registros en la dieta de aves neotropicales (Figura 6).

Figura 6 Representación de algunas interacciones tróficas ave-planta en el agroecosistema cacao en Tabasco, México: A) Dives dives, B) Icterus gularis, C) Amazona albifrons y D) Eupsittula nana; alimentándose de Erythrina fusca; E) Momotus lessonii ingestando fruto de Heliconia latispatha y F) Amazona autumnalis alimentándose de Mangifera indica.
Discusión
El inventario actualizado de aves asociadas al agroecosistema cacao en Tabasco (165 especies) es superior al número de especies documentadas en otros agroecosistemas de la entidad, como monocultivos forestales (148 especies); sistemas silvopastoriles (154 especies); y huertos familiares (70 especies) (González-Valdivia et al. 2014, Sánchez-Soto 2018, Cadenas-Madrigal et al. 2023). Del mismo modo, esta cifra es mayor al número de especies registradas en las plantaciones de cacao en Chiapas, en donde se han documentado alrededor de 150 especies (Rangel-Salazar et al. 2013). Esto resalta la importancia del agroecosistema cacao en la entidad, sobre todo en las áreas fragmentadas en donde no quedan remanentes de vegetación original (Ochoa-Gaona et al. 2019).
En cuanto a las preferencias de hábitat, la categoría GB (generalista de bosques) obtuvo un mayor número de especies registradas (109 especies), seguida de la categoría (EAA) especialista de áreas abiertas (28 especies). Esto coincide con Van-der Wal et al. (2012), quienes encontraron resultados similares en 38 sistemas agroforestales evaluados en Tabasco, no obstante, el número de especies EB (especialistas de bosques) es contrastante, ya que en su estudio sólo reportaron una especie de esta categoría, mientras que en este trabajo se identificaron 22 especies. Es posible que la diferencia radique en que los sistemas agroforestales estudiados por Van-der Wal et al. (2012) se encontraban a más de 2 km de los fragmentos de bosque natural más cercanos, mientras que, para este trabajo se evaluó una plantación rodeada de selva alta perennifolia en las laderas del Cerro Mono Pelón en Huimanguillo (plantación 8) en donde se registraron seis especies de esta categoría: Tinamus major, Penelope purpurascens, Crax rubra, Trogon caligatus, Amazona farinosa y Habia rubica. Esto coincide con Reitsma et al. (2001) quienes indican que la cantidad de especies EB disminuye a medida que la distancia de los bosques naturales incrementa, por lo que sugieren que las plantaciones de cacao proporcionan hábitats para un número considerable de especies, pero no pueden sustituir a los bosques naturales en la conservación de las aves.
La riqueza de especies identificadas en campo parece responder favorablemente a la calidad de matriz circundante en cada parcela, incluso más que la superficie de la plantación. Por ejemplo, la plantación 8 con 6 ha de superficie y matriz de selva alta perennifolia, presentó un mayor número de especies (73 especies) en comparación con la plantación 17 constituida por 50 ha y una matriz de vegetación secundaria y humedales (71 especies). Asimismo, las plantaciones que presentaron un número menor de especies son las que se encuentran rodeadas de monocultivos o potreros. Esto, coincide con Ibarra et al. (2001) y Trejo-Pérez (2007), quienes mencionan que la riqueza de aves en el agroecosistema cacao incrementa en función de la heterogeneidad del paisaje. Es importante destacar que el esfuerzo de muestreo fue variable en cada parcela, por lo que se recomienda realizar un estudio sistemático y además comparar otros factores como la composición y estructura vegetal; el manejo agrícola y cobertura arbórea en cada plantación.
Los gremios tróficos estuvieron predominados por aves insectívoras (106 especies), probablemente porque el cacao es uno de los cultivos con mayor número de insectos asociados a nivel mundial (Pereira-Jordão et al. 2024). El gremio trófico predominante fue el de insectívoros de follaje con 30 especies, de las cuales la mayoría son migratorias. Esto coincide con Greenberg et al. (2000), quienes registraron un 57% de especies migratorias, principalmente de la familia Parulidae. Algunas especies de esta familia como Cardellina pusilla y Mniotilta varia han sido observadas alimentándose de insectos plaga en otros agroecosistemas (Romero-Díaz et al. 2022). En Panamá, se ha documentado que las aves insectívoras reducen la densidad de artrópodos defoliadores de hojas de cacao en un 46% (Van-Bael et al. 2007), y en Perú son consideradas agentes de control biológico en la producción de cacao (Ocampo-Ariza et al. 2023).
En este estudio se observaron especies catalogadas como insectívoras estrictas alimentándose de numerosos recursos vegetales, tal es el caso de M. aurifrons que se alimentó de cinco frutos y se encuentra clasificada en el gremio insectívoro de corteza (Arriaga-Weiss et al. 2008, Van-Der Wal et al. 2012, Cadenas-Madrigal et al. 2023). Esto, podría explicarse con la teoría del forrajeo óptimo, la cual describe que las especies seleccionan su alimento en función del mayor aporte nutricional con el menor gasto de energía (Romero-Díaz et al. 2022). Es posible que las plantas, al ser organismos sésiles, sean una fuente de alimento fácil de obtener en temporadas de floración y fructificación, comparado con la captura de insectos. Esto ya se ha reportado para M. aurifrons que durante la temporada de secas se alimenta de mucílago de cacao maduro para obtener líquido de las mazorcas (Arriaga-Weiss 1985). Esta especie también perfora los frutos de naranja dulce (Citrus sinensis) para obtener jugo ante la insuficiencia de recursos (Guzmán-Canul y Sánchez-Soto 2024). El aprovechamiento de las plantas como segunda fuente de alimento es común para el gremio trófico insectívoro-frugívoro arbóreo, pero no para los gremios de especies clasificadas como insectívoras estrictas, como es el caso del gremio insectívoro de corteza, por lo que se sugiere hacer una revisión y de ser pertinente, una reclasificación, para las especies que se alimentan de un mayor número de plantas, como es el caso de M. aurifrons que con los registros del presente trabajo se incrementa a 23 el número de especies vegetales identificadas en su dieta: cacao, naranja dulce, mandarina (Citrus reticulata), papaya (Carica papaya), banano (Musa paradisiaca), maíz (Zea mays), chirimoya (Annona reticulata), saramuyo (Annona squamosa), nance (Byrsonima crassifolia), tamarindo (Tamarindus indica), mango (Mangifera indica), pitahaya (Selenicereus undatus), cedrillo (Trichilia cuneata), smukut (Miconia trinervia), zarzaparrilla (Smilax bona-nox), guarumo (Cecropia obtusifolia), cinco hojas (Oreopanax echinops), palo brujo (Sapium oligoneuron), cucharo (Rapanea myricoides), coronos (Xylosma chlorantha), falsa anona (Cymbopetalum mayanum), algodoncillo (Hampea appendiculata) y jagua (Genipa americana) (Wheelwright et al. 1984, Arriaga-Weiss 1985, Foster 2007, Sánchez-Soto 2018, Guzmán-Canul y Sánchez-Soto 2024, Billerman et al. 2025).
El conocimiento de las interacciones tróficas ave-planta en el agroecosistema cacao, puede servir para atraer o repeler especies de interés, por ejemplo, para el caso de M. aurifrons cuya percepción se considera perjudicial (Greenberg et al. 2000), se pueden enriquecer las plantaciones con árboles frutales para disminuir los daños en el fruto de cacao. Por otro lado, para atraer especies de interés ecológico (polinizadores o dispersoras de semillas) se pueden establecer especies nativas que incrementen estos servicios ambientales, como se ha realizado con jardines para polinizadores en otros ambientes antrópicos (Del Coro-Arizmendi et al. 2020).
Una de las interacciones tróficas más importantes identificadas en este estudio fue el de las aves con la especie arbórea E. fusca, cuya técnica de forrajeo varió en cada especie de ave. Algunas estrategias resultaron ineficaces para la polinización, pero otras fueron compatibles con el transporte de polen, ya que preservaban la integridad de las flores (Parrini y Raposo 2010). La familia Psittacidae desprendía los pétalos carnosos y los desechaba hasta llegar a la base de la flor en donde se encontraban los nectarios, en ocasiones removía toda la flor durante el proceso, pero en otras, quedaban inflorescencias sujetas al árbol y eran aprovechadas por aves de talla menor, como los colibríes y los ictéridos, que introducían su cabeza directamente al eje principal, llegando a la base de los estambres donde podían sorber el néctar. Esto coincide con Russo (1981) quien menciona que las aves son los principales polinizadores para el género Erythrina, debido a la morfología de la flor y a su abundante flujo de néctar. Estas características limitan la actividad polinizadora de los insectos, ya que los grupos que pueden acceder al néctar encuentran abundante alimento en una sola flor, sin tener necesidad de desplazarse a otras flores. Por el contrario, los colibríes requieren altas concentraciones de carbohidratos al día y los psitácidos tienen tallas superiores por lo que necesitan un mayor aporte nutricional (Howell y Webb 1995). Asimismo, Parrini y Raposo (2010) reportaron 20 especies de aves alimentándose de E. fusca de los cuales destacan a la familia Icteridae y Trochiliade por presentar conductas no destructivas durante su alimentación, lo que las convierte en polinizadoras potenciales.
La familia Psittacidae es uno de los grupos más importantes en el agroecosistema cacao debido a que todas las especies registradas en este trabajo se encuentran en alguna categoría de riesgo por la NOM-059 (SEMARNAT 2010). E. nana fue una de las tres especies de aves que se alimentó de un mayor número de plantas sin ocasionar daños al agroecosistema. Esta especie es una de las que más ha sido perjudicada por el tráfico ilegal en México (Cantú et al. 2007). Una forma de disminuir esta problemática, es promoviendo la cultura de observación de aves, que ha incrementado su auge en las últimas décadas y que podría traer beneficios económicos adicionales a los productores de cacao (Carvajal-Alfaro y Oviedo 2022). Los psitácidos son uno de los grupos con mayor potencial para difundir esta actividad en el agroecosistema, debido a su valor estético, sus vocalizaciones y su estrecho vínculo con la cultura mexicana (Cantú et al. 2007). En este trabajo se registraron tres especies de esta familia Psittacidae alimentándose de plantas y una que no se observó forrajeando, A. farinosa, pero se observó perchando en los árboles de sombra por alrededor de una hora, por lo que podría utilizar el agroecosistema como un sitio de descanso.
La mayoría de las plantas registradas en la matriz de interacciones fueron especies nativas (68%), superando a las introducidas (32%). Esto refuerza la importancia de la flora nativa para la conservación de la biodiversidad (Hernández-Ascención et al. 2025). Por otro lado, las especies introducidas registradas en este trabajo son especies que se cultivan en México desde hace más de un siglo para la producción agroalimentaria y se han adaptado a las condiciones ambientales de Tabasco, por lo que se han naturalizado, es decir, sus poblaciones son estables en las condiciones locales (Maldonado-Mares y Maldonado-Sánchez, 2019). Tal es el caso de la naranja dulce, mango, banano y la carambola; con excepción de la palmera pindó y el laurel de la India, que son especies ornamentales. Esto, parece indicar la capacidad de algunas aves para adaptarse a los recursos disponible en el medio (Medina-Madrid et al. 2021). Es importante destacar que un número considerable de aves y plantas que coexisten en el agroecosistema cacao y de los que se tienen registros de interacciones en otros sistemas agrícolas, no fueron observadas en este trabajo, por ejemplo, las especies del género Euphonia que habitualmente se alimentan de frutos en los huertos familiares (Sánchez-Soto 2018), no se registraron en este trabajo. Por lo que incrementar este tipo de estudios y replicarlos en otros agroecosistemas podría contribuir al conocimiento de las interacciones tróficas ave-planta, y sentaría las bases para establecer estrategias de manejo hábitat y conservación de las aves en Tabasco.
Conclusiones
El inventario actualizado de aves asociadas al agroecosistema cacao en Tabasco se incrementó en un 15% con 22 nuevos registros, esto lo posiciona como el sistema agrícola tropical con una mayor riqueza avifaunística registrada en la entidad, asemejándose a algunos ecosistemas naturales. Además, se identificaron 70 interacciones tróficas: ave-planta, de los cuales 21 fueron nuevos registros en la dieta de aves neotropicales. Esta información contribuye al conocimiento de la historia natural de las aves y las plantas que coexisten en el agroecosistema cacao, y puede servir para enriquecer las plantaciones con el fin de atraer especies de aves polinizadoras, dispersoras de semillas o de interés turístico, para generar un valor agregado a la producción.