Introducción
El uso de diodos emisores de luz (LED) en la agricultura ha experimentado un crecimiento significativo en los últimos años, proporcionando una forma nueva e innovadora de cultivar debido a su eficiencia energética, durabilidad y flexibilidad en la composición espectral (Bantis et al. 2018). La luz es una forma de radiación electromagnética que incluye diferentes longitudes de onda (perceptibles e imperceptibles). El espectro de luz visible para el ojo humano está en un rango aproximado de 380 a 700 nm. Esta luz es crucial para las plantas ya que coincide con la radiación fotosintéticamente activa (PAR 400-700 nm) (Dou y Niu 2020). Las plantas se adaptan al monitorear las señales de la luz ambiental, lo que les permite regular las vías de señalización con precisión. Los cambios en el ambiente de la luz se sincronizan con otras señales ambientales, como la temperatura, estrés biótico y fluctuaciones estacionales, mientras que las vías de señalización de la luz se relacionan con otras vías que regulan la fisiología y el desarrollo de las plantas (Paik y Huq 2019). Las plantas perciben la luz como fuente de energía para la fotosíntesis y como una señal que puede provocar diversas respuestas fisiológicas (Paponov et al. 2020). Las estructuras a través de las cuales se perciben las señales de la luz ambiental son los cloroplastos y los fotorreceptores (Roeber et al. 2021). Los cloroplastos contienen dos tipos de pigmentos llamados clorofilas y carotenoides, que absorben la luz para el proceso de la fotosíntesis. Las clorofilas, son los pigmentos que predominan en las plantas y absorben la luz roja y azul, mientras que, los carotenoides son pigmentos accesorios y absorben fuertemente la luz azul, permitiendo que el cloroplasto coseche mayor cantidad de energía (Yamori 2019). Por otra parte, la función de la luz como una señal interactúa en la fisiología de la planta como el crecimiento, periodo de floración e impacta en las características morfogenéticas como altura y forma (Fukuda 2019).
Los fotorreceptores son cromoproteínas que absorben longitudes de onda especificas (250 a 750 nm) y las traducen en señales que controlan los procesos biológicos, son fundamentales para controlar la fotomorfogénesis (Oka y Yamamoto 2019). Hay dos categorías de fotorreceptores en las plantas: las clorofilas (a, b y total) y carotenoides que cosechan luz para la fotosíntesis y los receptores fotosensibles fitocromos, criptocromos, fototropinas, que regulan las respuestas de luz no fotosintéticas (Dou y Niu 2020). Las plantas superiores utilizan fitocromos (PHY) que absorben luz roja lejana/roja, fotorreceptores especializados en luz azul/UV-A, incluidos criptocromo (CRY), fototropina (PHOT) y otros, y el locus 8 de resistencia UV (UVR8) que absorbe UV-B (Oka y Yamamoto 2019). Pero aún no se ha encontrado un fotorreceptor específico para la radiación UV-C, ya que esta, es bloqueada por la capa de ozono, pero se cree que las fototropinas y UVR8, son los fotorreceptores encargados de percibir esta radiación (Badmus et al. 2022). El estímulo lumínico puede alterar la concentración de fitohormonas y provocar modificaciones morfogenéticas, además de que las señales de los fotorreceptores pueden gestionar la expresión génica y producir efectos sincrónicos en metabolitos y fitohormonas en el fenotipo de la planta (Fukuda 2019). Actualmente se ha demostrado que la suplementación de luz puede mejorar el crecimiento y rendimiento de las plantas. Al respecto, Liang et al. (2021) encontraron que la iluminación con longitudes de onda roja (663 nm) y azul (454 nm) aumentó el crecimiento de plántulas de tomate y pepino, además de inducir mayor producción de biomasa; por lo que sugieren que estos efectos dependen de la calidad y cantidad de luz que se da a las plantas. Por otra parte, la luz también puede afectar la calidad nutricional y sensorial de las frutas y verduras, que está determinada por una variedad de factores, como el color, el sabor, la textura y la composición de nutrientes (Hasan et al. 2017). Particularmente, el incremento en el contenido de nutrientes y compuestos bioactivos es benéfico para la salud humana debido al valor nutritivo y sus propiedades antioxidantes (Coelho et al. 2023).
La iluminación suplementaria, puede afectar la pigmentación de los tomates, e inducir la síntesis de licopeno, principal pigmento carotenoide de estos frutos, y uno de los antioxidantes más potentes que se conocen (Dannehl et al. 2021). Se ha reportado que la iluminación con LEDs en longitudes de onda roja (660 nm) y azul (430 nm) incrementa el contenido de licopeno en frutos de tomate en 18% (Dannehl et al. 2021). La adición de luz roja + rojo lejano (600-800 nm) a través de LEDs mejoró los parámetros de la calidad del fruto del tomate, como los sólidos solubles totales (SST), la acidez titulable (AT), el pH, y características sensoriales, como aroma, dulzura, acidez y textura (Kim et al. 2020). Además, se ha reportado que la iluminación debajo del dosel con tratamientos de combinación de luz roja (666 nm) y azul (462 nm) en plantas de tomate incrementa el rendimiento (24%), y acelera la maduración de frutos (Paucek et al. 2020). Algunos autores proponen que el uso de LEDs para aplicar combinaciones de luz en longitud de onda específicas, por ejemplo, 87.5% rojo (660 nm) y 12.5% azul (440 - 460 nm), pueden aumentar el rendimiento en pepino, al aumentar la producción de clorofilas en las hojas y el intercambio gaseoso en la planta (Gajc-wolska et al. 2021).
La iluminación LED ha mostrado efectos diferentes en varios cultivos, etapas fenológicas, y calidad postcosecha. Por ejemplo, en plántulas de sandía (Citrullus lanatus) al aplicar una combinación de luz 12% roja (661 nm), 83% azul (450 nm) y 5% rojo lejano (725 nm), durante la aclimatación, promovió el crecimiento, floración y precocidad (Bantis et al. 2022). En el cultivo de la fresa (Fragaria × ananassa) la adición de luz roja (665 nm) y azul (455 nm) a través de LEDs en período fuera de temporada mejoró los parámetros agronómicos en las bayas (peso de fruto, solidos solubles totales y rendimiento), al igual que el crecimiento vegetativo (área foliar y número de coronas) (Stuemky y Uchanski 2020). En la planta de salvia roja (Salvia miltiorrhiza) promovió el crecimiento y producción de compuestos fenólicos con la aplicación de luz en proporción 30% rojo (635 nm) y 70% azul (460 nm) (Zhang et al. 2020). En coles de bruselas (Brassica oleracea) después de cosecharse se mantuvieron bajo tratamientos de luz azul (458-467 nm) y blanco (450/525-558 nm) a través de LEDs, obteniendo menor respiración, manteniéndose visualmente más verdes y con mayor cantidad de clorofilas en comparación al control (Hasperué et al. 2016). Este estudio tiene como objetivo evaluar el efecto de la iluminación suplementaria con LEDs en tres longitudes de onda específicas (azul, rojo y rojo lejano) sobre el crecimiento, la síntesis de fitoquímicos y la calidad del fruto en cultivos de tomate y pepino. Mejorar la calidad nutricional y el rendimiento de los cultivos es fundamental para la salud humana y la sostenibilidad agrícola. Los hallazgos de este estudio podrían ofrecer directrices precisas para la aplicación de tecnologías LED en la producción agrícola, optimizando tanto la eficiencia del cultivo como la calidad de los productos. Por lo tanto, se busca proporcionar una base científica para implementar esta tecnología en la agricultura moderna, mejorando la fisiología de las plantas, la síntesis de compuestos nutricionales y sensoriales de los frutos.
Materiales y métodos
Se estableció un cultivo de tomate con semillas de la variedad Cid F1 (Harris Moran, Davis, CA, USA), de tipo saladette y crecimiento indeterminado, trasplantadas en bolsas de polietileno negro de 10 L. Paralelamente, se cultivó pepino con semillas de la variedad Centauro F1 (Fitó, ESP), sembradas de forma directa en bolsas de polietileno negro de 10 L. Ambos cultivos se realizaron en una mezcla de sustrato de perlita y peat moss en proporción 1:1, y se nutrieron con solución Steiner (Steiner 1961). El pH se ajustó a 6.5 con ácido sulfúrico cada vez que se preparó la solución nutritiva. La conductividad eléctrica (CE) de la solución fue de 1.9 a 2.5 mS cm−1 durante todo el desarrollo del cultivo. Las plantas se distribuyeron en hileras de cinco macetas, con dos filas por tratamiento y una distancia de 30 cm entre plantas. Cada tratamiento incluyó 10 plantas, de las cuales cuatro se utilizaron como bordes para evitar la contaminación lumínica, resultando en seis plantas por tratamiento. Cada maceta representó una repetición. El invernadero donde se establecieron los cultivos es de tipo túnel, con cubierta de polietileno, y ventilación lateral. La radiación fotosintéticamente activa en los picos máximos fue de 1 400 µmol m−2 s−1, temperatura mínima de 15 °C y máxima de 35 °C, y humedad relativa de 40-85%. El cultivo de tomate se desarrolló durante 120 días y el de pepino durante 90 días, ambos manejados a un solo tallo.
Aplicación de tratamientos de iluminación
El área del invernadero se dividió en secciones para evitar la contaminación lumínica entre tratamientos. La iluminación se aplicó con lámparas LED (modelo LILZBAL-S100WFRBPBC, Sola Basic, Ciudad de México, México) de 2.2 m de largo y 25 W de potencia. Las lámparas se instalaron a 30 cm por encima del dosel de las plantas y para tres tratamientos en la base del tallo, para irradiar de abajo hacia arriba. Se implementaron seis tratamientos de iluminación: Luz azul con una lámpara sobre el dosel (B1). Luz azul con dos lámparas, dosel y base de planta (B2). Luz roja con una lámpara sobre el dosel (R1). Luz roja con dos lámparas, dosel y base de planta (R2). Luz roja lejana con una lámpara sobre el dosel (FR1). Luz roja lejana con dos lámparas, dosel y base de planta (FR2). Control sin luz suplementaria (T0). Las longitudes de onda específicas para cada tipo de luz fueron: luz azul (455 nm), luz roja (660 nm) y luz roja lejana (730 nm). La radiación suplementaria se aplicó durante el desarrollo del cultivo, durante 5 horas diarias de las 19:00 a las 24:00 horas.
Análisis de parámetros agronómicos
Durante el desarrollo del cultivo se cuantificó el número y el peso de frutos cosechados para obtener el rendimiento de frutos por planta. Al final del cultivo se determinó la altura de la planta, número de hojas, número de racimos y/o frutos según el cultivo, y se cuantificó la biomasa seca después de tener las plantas en horno de secado (DRYING OVEN/INCUBATOR, 9065) a 90 °C por 72 horas.
Recolección de hojas y frutos para análisis
A los 70 días después del establecimiento de los cultivos, se tomaron muestras de la hoja más joven y completamente desarrollada. Las muestras se colectaron en hielo y se almacenaron a una temperatura de −20 °C. Se sometieron a liofilización (Freeze dryer, ECO-FD10PT), y se maceraron para obtener un polvo fino para los análisis posteriores.
También se colectaron muestras de frutos a los 70 días después del trasplante y/o siembra según el cultivo. Los frutos de tomate fueron colectados del tercer racimo y en grado de madurez rojo completo, y de pepino fueron el cuarto fruto en el desarrollo de cada planta y en grado de madurez comercial. Las muestras se colectaron en hielo y se almacenaron a temperatura de −20 °C. Posteriormente, se liofilizaron (Freeze dryer, ECO-FD10PT) y maceraron hasta obtener un polvo fino.
Análisis bioquímicos
Los contenidos de clorofilas A y B (mg 100 g−1 PS) y β-caroteno (mg 100 g−1 PS) se determinaron según el método de Nagata y Yamashita (1992). La muestra liofilizada (10 mg) se mezcló con 2 mL de hexano:acetona (3:2). Posteriormente las muestras fueron sometidas a un baño de ultrasonidos durante 5 minutos, en un ultrasonicador (Ultrasonic cleaner BK-2000). Luego se centrifugaron a 15 000 ×g durante 10 minutos a 4°C. Se eliminó el sobrenadante y se leyó la absorbancia a 645 y 663 nm en un espectrofotómetro UV-Vis (Espectrofotómetro Unico, Modelo UV2150, Dayton, NJ, EE. UU.).
Los valores obtenidos se utilizaron en las ecuaciones para calcular el contenido de clorofila. Para el β-caroteno, se midieron las absorbancias a 453, 505, 645 y 663 nm y los valores obtenidos se utilizaron en la ecuación de β-caroteno.
La vitamina C (mg 100 g−1 DW) se determinó mediante espectrofotometría como se describe en Hung y Yen (2002). Se extrajeron 10 mg de tejido liofilizado con 1 mL de ácido metafosfórico (HPO3) al 1% y se filtraron con papel de filtro Whatman No. 1. Para la cuantificación, se tomaron 200 μL de extracto y se mezclaron con 1800 μL de 2,6 diclorofenol indofenol (100 mM), midiendo la absorbancia a 515 nm en un espectrofotómetro UV-Vis (Espectrofotómetro Unico, Modelo UV2150, Dayton, NJ, EE. UU.).
El contenido de flavonoides se determinó según Arvouet-Grand et al. (1994) . Para la extracción se colocaron 20 mg de tejido liofilizado en un tubo de ensayo al que se le agregaron 2 mL de metanol grado reactivo y este se homogeneizó durante 30 segundos. La mezcla se filtró usando papel Whatman No. 1. Para la cuantificación, se agregaron a un tubo de ensayo 1 mL del extracto y 1 mL de solución metanólica de tricloruro de aluminio (AlCl3) al 2% y se dejó reposar durante 20 minutos en oscuridad. La lectura se tomó a longitud de onda de 415 nm en un espectrofotómetro UV-Vis (Espectrofotómetro Unico, Modelo UV2150, Dayton, Nueva Jersey, EE. UU.). Los resultados se expresan en mg EQ de quercetina por 100 gramos de PS.
El contenido de fenoles totales se obtuvo según Yu y Dahlgren (2000). En total, se extrajeron 100 mg de tejido liofilizado con 1 mL de una solución agua:acetona (1:1) y la mezcla se homogeneizó durante 30 segundos. Los tubos de muestra se centrifugaron a 17 500 ×g durante 10 minutos a 4 °C. En total, se colocaron en un tubo de ensayo 18 μL del sobrenadante, 70 μL del reactivo de Folin-Ciocalteu y 175 μL de carbonato de sodio (Na2CO3) al 20% y se agregaron 1 750 μL de agua destilada. Las muestras se colocaron en un baño de agua a 45 °C durante 30 minutos. Finalmente, la lectura se tomó a una longitud de onda de 750 nm en el espectrofotómetro UV-Vis (Unico Spectrophotometer, Model UV2150, Dayton, NJ, USA). Los fenoles totales se expresaron en mg EQ de ácido gálico por gramo de PS.
Análisis de calidad de fruto
A los 71 días después del trasplante (ddt) y/o siembra según el cultivo, se tomaron frutos de tomate del tercer racimo y el cuarto fruto de pepino en los que se evaluaron los parámetros de calidad. La firmeza se determinó utilizando un penetrómetro (Wagner Force Dial FDK 2). El contenido de solidos solubles totales (°Brix) se determinó con un refractómetro (Atago, 1-425-637-2107). Mientras que el pH y conductividad eléctrica (CE) con un potenciómetro (Ohaus, STARTER3100m).
Análisis estadístico
El experimento se estableció bajo un diseño completamente al azar, y se consideraron seis repeticiones por tratamiento. Se realizó un análisis de varianza y prueba de medias de diferencia mínima significativa de Fisher (LSD, α = 0.05) mediante el software InfoStat (v2019) (Casanoves et al. 2012).
Resultados
Cultivo de tomate
La aplicación de luz suplementaria con LEDs aumentó el crecimiento de las plantas de tomate encontrando diferencias significativas en altura (Figura 1A). Los tratamientos B2 y B1 indujeron un incremento de 5.7 y 4%, en comparación al testigo (T0). El número de frutos no mostró diferencias entre tratamientos (Figura 1B). Pero se observó menor peso de frutos en los tratamientos R2, FR1 y FR2 de 16.5, 18 y 14.3% con respecto al T0 (Figura 1C). El número de racimos disminuyó en R2 en 12.2% con relación al T0 (Figura 1D). En el número de hojas, hubo una reducción en los tratamientos R1 y R2 de 5.8% con respecto al T0 (Figura 1E). La biomasa seca disminuyó en los tratamientos B1, B2, R1, R2 y FR1, en 17.3, 17.9, 15.8, 15.4, y 17.1% en comparación al T0 (Figura 1F).
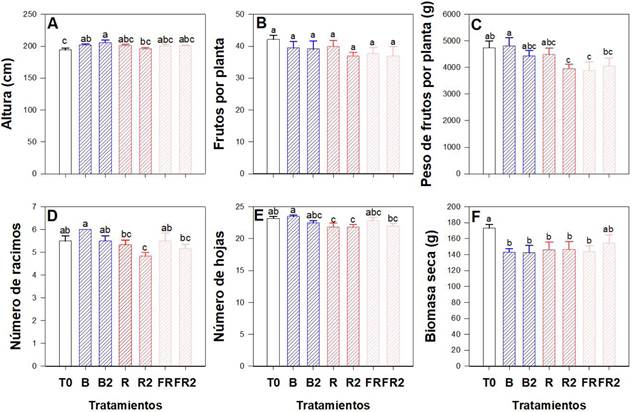
Figura 1 Efecto de la iluminación LED suplementaria en el crecimiento y fructificación de las plantas de tomate. (A) Altura; (B) Frutos por planta; (C) Peso de frutos por planta; (D) Número de racimos; (E) Número de hojas; (F) Biomasa seca; T0: control; B1: LED azul, dosel; B2: LED azul, dosel y base de planta; R1: LED rojo, dosel; R2: LED rojo, dosel y base de planta; FR1: LED rojo lejano, dosel; FR2: LED rojo lejano, dosel y base de planta. Letras diferentes indican diferencias significativas entre tratamientos según LSD Fisher (α = 0.05). n = 6 ± error estándar.
El contenido de pigmentos fotosintéticos en hojas de tomate mostró diferencias entre tratamientos, ya que B1, B2 y FR2 indujeron aumentos en la clorofila a, b y total, en clorofila a fue del 29.1, 20.7 y 19.5%, en clorofila b del 26.9, 19.2 y 15.4%, y en clorofila total del 28.6, 20.4 y 18.4%, en relación con el T0 (Figura 2A). En contraste, el licopeno disminuyó en los tratamientos R1, R2, FR1 y FR2, en 27.8, 23.8, 40.5 y 56.2% con respecto al T0 (Figura 2B). El contenido de β-caroteno incrementó en los tratamientos FR2, B1, R1, B2, R2 y FR1 en 40.1, 36.5, 32.2, 31.9, 30.2 y 23.9% en comparación al T0 (Figura 2C). En contraste, el contenido de vitamina C mostró una reducción en los tratamientos B2, R1 y R2 de 13, 17.5 y 43.3% con relación al T0 (Figura 2D). Hubo un incremento de flavonoides en el tratamiento B2 de 22.8% con relación al T0 (Figura 2E). Por otra parte, la mayor cantidad de fenoles se obtuvo con FR1 el cual promovió un aumento de 59.7%, seguido de B1, R1 y B2 con 51.6, 50.7 y 45.3%, en comparación al T0 (Figura 2F).
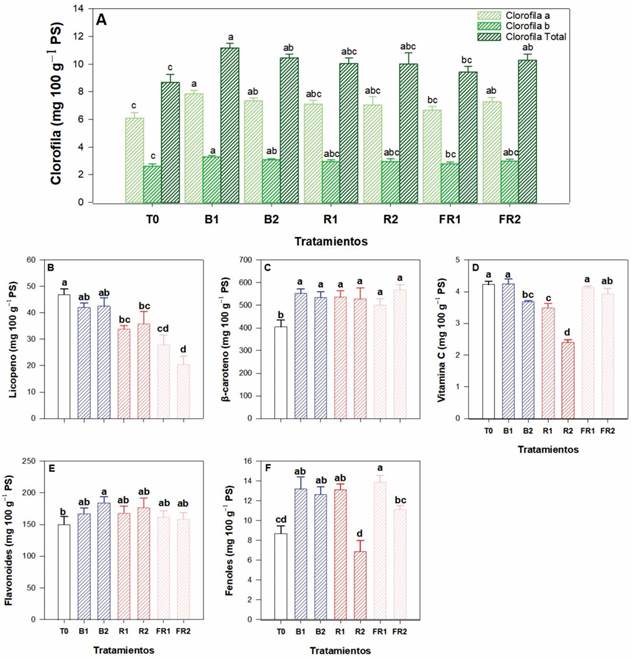
Figura 2 Efecto de la iluminación LED suplementaria en el contenido de clorofilas y compuestos antioxidantes en hojas de tomate. (A) Pigmentos fotosintéticos: clorofila a; clorofila b; clorofila total: suma de clorofila a + clorofila b; (B) Licopeno; (C) β-caroteno; (D) Vitamina C; (E) Flavonoides; (F) Fenoles; T0: control; B1: LED azul, dosel; B2: LED azul, dosel y base de planta; R1: LED rojo, dosel; R2: LED rojo, dosel y base de planta; FR1: LED rojo lejano, dosel; FR2: LED rojo lejano, dosel y base de planta. Letras diferentes indican diferencias significativas entre tratamientos según LSD Fisher (α = 0.05). n = 6 ± error estándar.
El contenido de licopeno en frutos de tomate se modificó con la aplicación de luz suplementaria mediante LEDs, la concentración se redujo en FR1 en un 23.3%, en comparación al T0 (Figura 3A). En contraste, el mayor contenido de β-caroteno, fue promovido por los tratamientos FR2 y R1, con 127.5 y 106.9%, con relación al T0 (Figura 3B). En vitamina C, se observó una reducción en los tratamientos, FR1, FR2, R2 y B1 de 10.6, 10.9, 11. 2 y 12.2% en comparación al T0 (Figura 3C). También se observó una reducción en el contenido de flavonoides en los tratamientos B2 y FR1 de 15.7 y 16.3%, en comparación al T0 (Figura 3D). En contraste la concentración de fenoles en fruto no mostró diferencias entre tratamientos (Figura 3E).
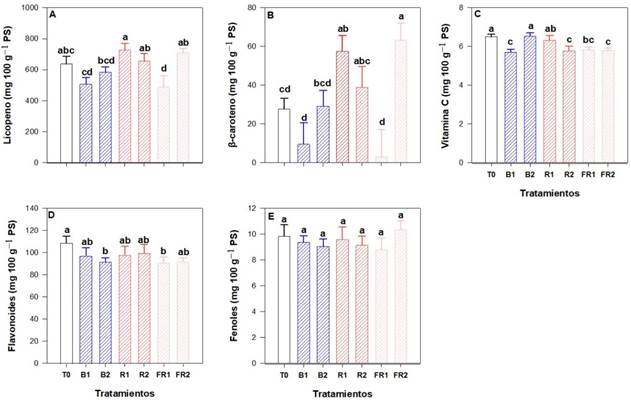
Figura 3 Efecto de la iluminación LED suplementaria en el contenido de compuestos antioxidantes de frutos de tomate. (A) Licopeno; (B) β-caroteno; (C) Vitamina C; (D) Flavonoides; (E) Fenoles; T0: control; B1: LED azul, dosel; B2: LED azul, dosel y base de planta; R1: LED rojo, dosel; R2: LED rojo, dosel y base de planta; FR1: LED rojo lejano, dosel; FR2: LED rojo lejano, dosel y base de planta. Letras diferentes indican diferencias significativas entre tratamientos según LSD Fisher (α = 0.05). n = 6 ± error estándar.
La iluminación de luz suplementaria con LEDs modificó el contenido de sólidos solubles totales en el fruto del tomate, disminuyendo en R1 en 9.7%, con relación al T0. Por otro lado, la iluminación suplementaria no modificó la firmeza del fruto del tomate. Sin embargo, hubo una reducción de la conductividad eléctrica en frutos de tomate en los tratamientos B2, R1 y FR de 15, 17.2 y 18.1%, en comparación al T0. El pH del fruto de tomate incrementó 3.1% en el tratamiento FR2, sin embargo, en los tratamientos B2, FR1 hubo una reducción de 2.5 y 2.7% con relación al T0 (Tabla 1).
Tabla 1 Efecto de la iluminación LED suplementaria sobre los parámetros físico-químicos de frutos de tomate.
| Tratamientos | TSS (°Brix) | Firmeza (kg cm−2) | CE (mS cm−1) | pH |
|---|---|---|---|---|
| T0 | 5.17a ± 0.17 | 16.77a ± 0.59 | 3.2ª ± 0.18 | 5.13b ± 0.03 |
| B1 | 4.83ab ± 0.17 | 18.77a ± 0.80 | 2.9ab ± 0.11 | 5.06bc ± 0.03 |
| B2 | 5.00ab ± 0.01 | 18.88a ± 1.17 | 2.72b ± 0.12 | 5.0cd ± 0.02 |
| R1 | 4.67b ± 0.21 | 18.05a ± 0.69 | 2.65b ± 0.07 | 5.07bc ± 0.01 |
| R2 | 5.00ab ± 0.01 | 17.62a ± 0.90 | 2.78ab ± 0.21 | 4.96d ± 0.02 |
| FR1 | 5.00ab ± 0.01 | 18.20a ± 1.42 | 2.62b ± 0.15 | 4.99cd ± 0.02 |
| FR2 | 5.00ab ± 0.01 | 16.43a ± 1.29 | 2.96ab ± 0.24 | 5.29ª ± 0.07 |
| Valor-p | NS | NS | NS | 0.0001 |
T0: control; B1: LED azul, dosel; B2: LED azul, dosel y base de planta; R1: LED rojo, dosel; R2: LED rojo, dosel y base de planta; FR1: LED rojo lejano, dosel; FR2: LED rojo lejano, dosel y base de planta. Letras diferentes indican diferencias significativas entre tratamientos según LSD Fisher (α = 0.05). n = 6 ± error estándar.
Cultivo de pepino
La aplicación de luz suplementaria con LEDs no afectó la altura de las plantas de pepino (Figura 4A). Sin embargo, el número de frutos disminuyó en todos los tratamientos en comparación con T0, hasta un 37.3% en FR2 (Figura 4B). El peso de los frutos también se redujo en los tratamientos, con disminuciones de hasta un 36.6% en FR2 (Figura 4C). El número de hojas fue menor en los tratamientos R1, R2, FR1 y FR2, con la mayor reducción del 15% en FR2 (Figura 4D). La biomasa fresca disminuyó en los tratamientos B1, FR1 y FR2 hasta un 14% (Figura 4E). La biomasa seca fue menor en FR1, con una reducción del 23.6% en comparación con T0 (Figura 4F). En general, el tratamiento control (T0) mostró mejores resultados en todas las variables morfológicas.
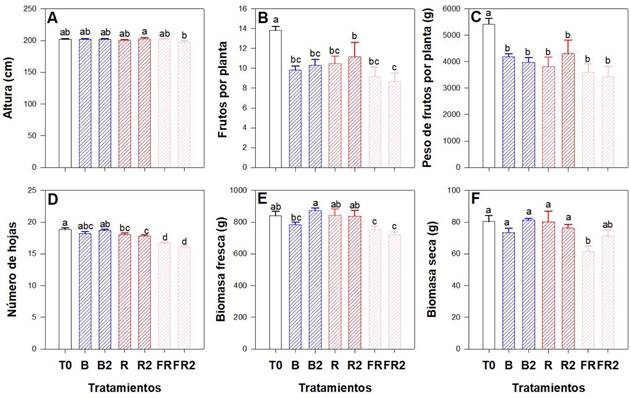
Figura 4 Efecto de la iluminación LED en el crecimiento de las plantas de pepino. (A) Altura; (B) Número de frutos; (C) Peso de frutos; (D) Número de hojas; (E) Biomasa fresca; (F) Biomasa seca; T0: control; B1: LED azul, dosel; B2: LED azul, dosel y base de planta; R1: LED rojo, dosel; R2: LED rojo, dosel y base de planta; FR1: LED rojo lejano, dosel; FR2: LED rojo lejano, dosel y base de planta. Letras diferentes indican diferencias significativas entre tratamientos según LSD Fisher (α = 0.05). n = 6 ± error estándar.
La aplicación de luz suplementaria con LEDs modificó el contenido de pigmentos fotosintéticos en pepino, no obstante, con T0 se obtuvo la mayor concentración en la clorofila a, b y total (Figura 5A). En contraste, se indujo el contenido de licopeno en los tratamientos R2 y B1, con 207.4, y 166.7%, en comparación al T0 (Figura 5B). Sin embargo, hubo una reducción de β-caroteno en todos los tratamientos, siendo R2 hasta un 34.7% menor con respecto al T0 (Figura 5C). El tratamiento R1 disminuyó en 4.6% el contenido de vitamina C (Figura 5D). También hubo una reducción en los flavonoides en el tratamiento R2 de 19.9% con respecto al T0 (Figura 5E). En contraste, hubo una reducción del contenido de fenoles en todos los tratamientos con respecto a T0 (Figura 5F).
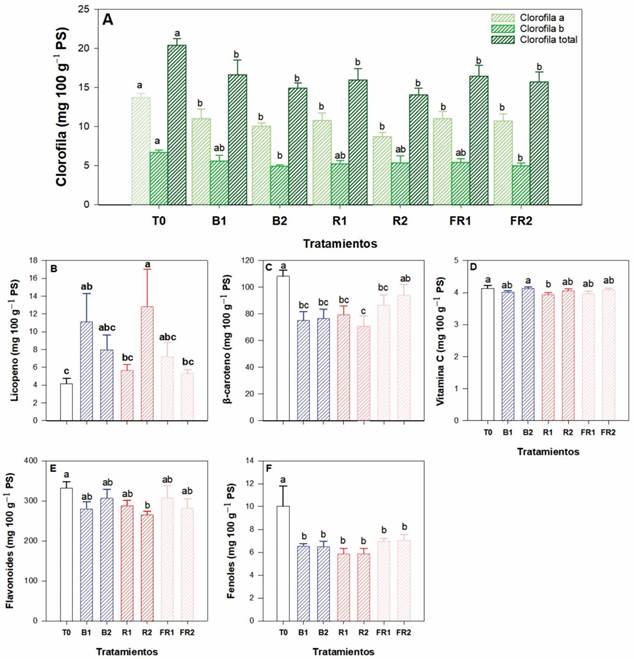
Figura 5 Efecto de la iluminación LED suplementaria en el contenido de clorofilas y compuestos antioxidantes de hojas de pepino. (A) Pigmentos fotosintéticos: clorofila a; clorofila b; clorofila total: suma de clorofila a + clorofila b; (B) Licopeno; (C) β-caroteno; (D) Vitamina C; (E) Flavonoides (F) Fenoles; T0: control; B1: LED azul, dosel; B2: LED azul, dosel y base de planta; R1: LED rojo, dosel; R2: LED rojo, dosel y base de planta; FR1: LED rojo lejano, dosel; FR2: LED rojo lejano, dosel y base de planta. Letras diferentes indican diferencias significativas entre tratamientos según LSD Fisher (α = 0.05). n = 6 ± error estándar.
La aplicación de luz a suplementaria mediante LEDs modificó el contenido de licopeno en frutos de pepino, incrementando este compuesto en los tratamientos R1 seguido de R2, FR1, FR2, B2 y B1 con 175.5, 175.3, 157.6, 133.6, 105.9 y 83.2%, con relación al T0 (Figura 6A). En contraste, el contenido de vitamina C aumentó en el tratamiento FR en 33.8%, con relación al T0 (Figura 6B). La concentración de fenoles no se modificó entre tratamientos (Figura 6C). En contraste, el contenido de flavonoides incrementó en FR1 seguido de R1, en 34.7 y 27.1% con relación al T0 (Figura 6D).
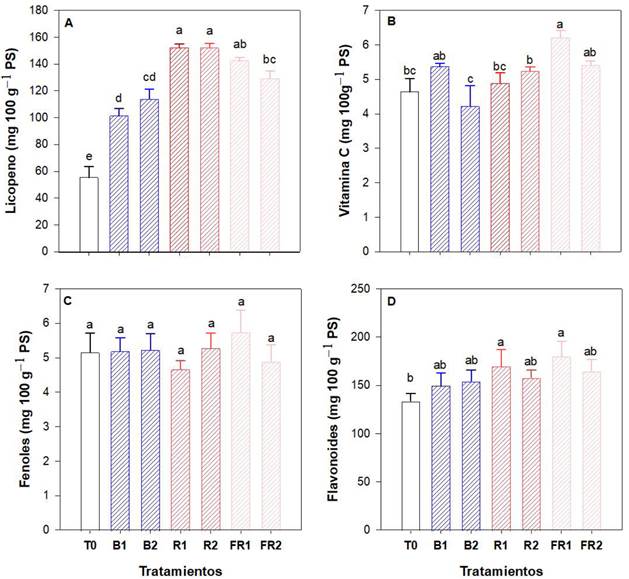
Figura 6 Efecto de la iluminación LED suplementaria compuestos antioxidantes en frutos de pepino. (A) Licopeno; (B) Vitamina C; (C) Fenoles; (D) Flavonoides; T0: control; B1: LED azul, dosel; B2: LED azul, dosel y base de planta; R1: LED rojo, dosel; R2: LED rojo, dosel y base de planta; FR1: LED rojo lejano, dosel; FR2: LED rojo lejano, dosel y base de planta. Letras diferentes indican diferencias significativas entre tratamientos según LSD Fisher (α = 0.05). n = 6 ± error estándar.
La iluminación de luz suplementaria con LEDs modificó la firmeza del fruto de pepino, el tratamiento R1 indujo la mayor firmeza y B1 la menor, sin embargo, no fueron diferentes al T0. Para el contenido de sólidos solubles totales no hubo diferencias en el pepino. Sin embargo, hubo una reducción de la conductividad eléctrica en frutos de pepino, los tratamientos R1 y FR2 la incrementaron en 19.1 y 17.4%, en relación con el T0, respectivamente. En contraste se observó una reducción del pH en todos los tratamientos en comparación al T0 (Tabla 2).
Tabla 2 Efecto de la iluminación LED suplementaria sobre los parámetros físico-químicos de frutos de pepino.
| Tratamientos | TSS (°Brix) | Firmeza (kg cm−2) | CE (mS cm−1) | pH |
|---|---|---|---|---|
| T0 | 2.33a ± 0.21 | 16.98ab ± 1.72 | 3.04c ± 0.11 | 5.76ª ± 0.15 |
| B1 | 2.17a ± 0.17 | 15.55b ± 0.96 | 2.97c ± 0.11 | 5.22b ± 0.03 |
| B2 | 2.17a ± 0.17 | 16.93ab ± 0.87 | 3.17bc ± 0.18 | 5.21b ± 0.05 |
| R1 | 2.00a ± 0.01 | 19.67a ± 0.67 | 3.62ª ± 0.09 | 5.13b ± 0.05 |
| R2 | 2.33a ± 0.21 | 17.88ab ± 0.58 | 3.33abc ± 0.12 | 5.14b ± 0.03 |
| FR1 | 2.50a ± 0.22 | 18.32ab ± 1.67 | 3.29abc ± 0.20 | 5.11b ± 0.04 |
| FR2 | 2.33a ± 0.21 | 18.55ab ± 1.24 | 3.57ab ± 0.23 | 5.04b ± 0.07 |
| Valor-p | NS | NS | 0.0405 | 0.0001 |
T0: control; B1: LED azul, dosel; B2: LED azul, dosel y base de planta; R1: LED rojo, dosel; R2: LED rojo, dosel y base de planta; FR1: LED rojo lejano, dosel; FR2: LED rojo lejano, dosel y base de planta. Letras diferentes indican diferencias significativas entre tratamientos según LSD Fisher (α = 0.05). n = 6 ± error estándar.
Discusión
La luz tiene varios efectos en las plantas, no solo como origen de energía para la fotosíntesis, también actúa como señalizador que induce efectos morfológicos y fisiológicos en el crecimiento y desarrollo, al activar diferentes respuestas a los cambios en las condiciones de luz natural (Paponov et al. 2020). Esto fue observado en los resultados obtenidos en este trabajo, ya que, con la suplementación de luz en diferentes longitudes de onda se indujeron cambios en altura de la planta, peso de los frutos por planta, números de racimos por planta, número de hojas por planta y biomasa seca (Figuras 1 y 4). Se ha reportado que diversas alteraciones morfológicas inducidas por el impacto de tratamientos complementarios con luz roja lejana (712 nm) sobre el crecimiento de las plántulas vegetales modificaron la longitud del hipocótilo de plántulas de solanáceas (tomate y pimiento rojo) y cucurbitáceas (pepino, calabaza y sandía) (Hwang et al. 2020). Aquí se observaron respuestas diferentes entre las longitudes de onda empleadas azul, rojo y rojo lejano; siendo más marcado el efecto en el tomate, donde la luz azul suplementaria indujo respuestas positivas, mientras que la luz roja indujo efectos negativos en la mayoría de las variables y la luz rojo lejano disminuyó el peso de frutos por planta y la biomasa seca (Figura 1). La mayor altura de las plantas en el cultivo de tomate se obtuvo con el tratamiento B2 (Figura 1A). En un trabajo en el que se iluminó debajo del dosel con tratamientos de combinación de luz roja (666 nm) y azul (462 nm) en plantas de tomate se encontró mayor rendimiento (24%) y se aceleró la maduración de los frutos (Paucek et al. 2020). Por otra parte, en cultivos ornamentales también varían los efectos de las LEDs. La rosa en miniatura en maceta (Rosa hybrida) Aga, suplementada con LED rojo (R 660 nm); azul (A 450 nm); blanca fria (B 5000 Kelvin) y rojo lejano (RL 730 nm), las plantas cultivadas bajo ambas luces RAB fueron las más altas, y tuvieron la mayor longitud de brote total, independientemente de R:RL. En contraste, no se encontraron beneficios en el crecimiento y la morfología en el cultivo del pepino con diferentes proporciones de flujo de fotones con luz azul (455 nm) y roja (661 nm) (Hernández y Kubota 2014). Sin embargo, en las plantas de tomate bajo los tratamientos de luz roja, se observó un menor número de hojas y de racimos, esto puede deberse a que la radiación roja promueve la elongación del tallo, lo que confirma este estudio. Esto demuestra que las funciones de la planta inducidas por el espectro dependen de cada tipo de especie (Zou et al. 2020). Por otro lado, los resultados obtenidos con rojo lejano suplementado a las plantas de pepino demostraron que es más sensible que el tomate bajo este tipo de radiación ya que hubo una reducción del número de hojas, frutos, biomasa fresca y seca. Al respecto, se ha reportado que el pepino es más susceptible a los cambios en la proporción de luz roja (663 nm) y azul (454 nm), que el tomate (Liang et al. 2021). Esto sucede porque la radiación rojo lejano es percibida por el fotorreceptor del fitocromo B (PHYB). Durante una intensidad de luz roja alta, PHYB se activa e inhibe las respuestas de crecimiento de las plantas, mientras que bajo una luz rojo lejano alta, PHYB se desactiva y conduce a respuestas del síndrome de evitación de la sombra (SAS), alargando los entrenudos y aumentando la altura de la planta (Meijer et al. 2022). Por otra parte, tanto las luces azules como las rojas pueden promover la apertura de los estomas y están mediadas por estos fotorreceptores de luz PHOTS, CRYS y PHYS (Huché-Thélier et al. 2016). Esto conduce a tasas de respiración más altas, lo que a su vez afecta el metabolismo general de los frutos (Hasperué et al. 2016). Esto puede explicar la pérdida de peso en los frutos de pepino observada en este estudio.
La luz modifica varias rutas bioquímicas durante el crecimiento y desarrollo de las plantas y los resultados difieren de la especie, tipo de célula, tejido y órgano de la planta (Jarerat et al. 2022). Las especies reactivas de oxígeno (ROS) son sintetizadas durante la fotosíntesis y la respiración mitocondrial. Donde una intensidad de luz alta, produce una tasa fotosintética mayor y a su vez, una producción más alta de ROS (Ntagkas et al. 2020). Los fitocromos se encargan de la biosíntesis de fitoquímicos y de las respuestas fisiológicas de las plantas mientras que los criptocromos se encargan de los procesos como apertura estomática, producción de biomasa, síntesis de antocianinas, carotenoides y clorofilas (Al-Murad et al. 2021). El contenido de pigmentos fotosintéticos se modificó de manera positiva en el tomate bajo todos los tratamientos de radiación suplementaria azul, rojo y rojo lejano (Figura 3A). Una mayor síntesis de pigmentos podría conducir a mayor absorción de luz, la eliminación de ROS, y en consecuencia, un mejor crecimiento de las plantas (Johkan et al. 2010). En contraste hubo una reducción del contenido de pigmentos en pepino, lo que puede estar ligado a los espectros específicos de radiación solar que pueden dañar los fotosistemas, particularmente el PSII, y causar la fotoinhibición. Además de que la reducción del contenido de pigmentos es uno de los mecanismos que reducen el aporte en exceso de luz a los cloroplastos, lo que a la vez disminuye los efectos de la fotoinhibición (Pashkovskiy et al. 2021).
El contenido de vitamina C, fue variable bajo los tratamientos evaluados, tanto en hojas como en frutos, se ha reportado que la luz azul es más eficiente para la biosíntesis de vitamina C en comparación con la roja. Al respecto, Ntagkas et al. (2019) encontraron que la luz azul mejora los niveles de ASA en frutos de tomate, lo que sugiere que la variabilidad de vitamina C se deba al tiempo de exposición de la luz. En los flavonoides hubo una tendencia positiva en la producción de este compuesto en frutos de pepino (Figura 6D), los cuales son importantes para la fotoprotección y su biosíntesis incrementa con la adición de luz azul y rojo, y se puede reducir con rojo lejano (Lazzarin et al. 2021). Tal vez esto se deba a que el pepino es más sensible a las longitudes de onda que el tomate, ya que el contenido de compuestos fenólicos, en hojas de pepino disminuyeron y en el caso de los frutos se conservaron en niveles adecuados, esto se debe a que los compuestos de flavonoides son todos antioxidantes y los compuestos fenólicos no todos los son (Tungmunnithum et al. 2018). Por otro lado, se ha demostrado que la luz azul y roja incrementan la producción de fenilpropanoides como antocianinas, flavonoides y compuestos fenólicos al modificar las transcripciones de los genes que regulan estos compuestos (Alrifai et al. 2019). En este sentido, Taulavuori et al. (2015) observaron que la biosíntesis de fenoles y flavonoides se incrementaron en lechuga roja suplementada con una composición de LED (120 W) con luz azul, 410 nm (5%), 430 nm (18%), 450 nm (48%) y 460 nm (29%), mientras que la luz azul y roja 720 nm (1.8%), 660 nm (50%), 630 nm (30%), 450 nm (11%), 430 nm (3.6%), 410 nm (0.9%) y 3500 K (2.7%) (luz blanca neutra), regulaban su producción en albahaca (Ocimum basilicum). Los carotenoides incrementaron en hojas y frutos de tomate (Figura 3C y 4B). Estos funcionan como fotosensibilizadores y juegan un papel importante como reguladores de ROS (Polívka y Frank 2010). Se ha comprobado que las proporciones bajas de luz rojo/rojo lejano inhiben la expresión de PSY, que es la enzima encargada de la velocidad de la ruta de los carotenoides, mientras que altas proporciones de luz rojo/rojo lejano, resultan en mayor expresión de PSY y por lo tanto inducen mayor contenido de estos compuestos (Xie et al. 2019). Esto indica que la suplementación durante cinco horas al día mejora los parámetros de estos compuestos, incrementando la calidad nutracéutica para los consumidores. En este sentido, se ha reportado que el gen S1PSY1 está estrechamente involucrado en la biosíntesis de licopeno en frutos de tomate tratados con luz roja (657 nm) y azul (457 nm) (Li et al. 2021). El receptor de la luz roja (PHY) y el de la luz azul (CRY) muestran una respuesta similar en ambas longitudes de onda. Sucede lo mismo para los genes HY5 y PIFs, lo cual sugiere que la luz azul y roja comparten mecanismos similares al inducir la activación de HY5 y PIF, y por consecuencia aumentan el contenido de licopeno en los frutos (Xie et al. 2019).
La calidad de los frutos varió entre el tomate y pepino (Tabla 1 y 2). Estos cambios metabólicos pueden atribuirse a la activación de diferentes vías, como las implicadas en la síntesis de aminoácidos y azucares, sin embargo, las vías metabólicas específicas que se activan pueden depender de factores como el tipo de irradiación LED utilizada y la duración de la exposición (Ngcobo y Bertling 2021). Además, los procesos de maduración y los mecanismos moleculares subyacentes son diferentes entre frutas climatéricas y no climatéricas. Los LED, dependiendo de la longitud de onda específica, pueden tener diferentes impactos en los procesos moleculares en frutas climatéricas y no climatéricas (Hasan et al. 2017). La luz rojo lejano (700-800 nm) estimula la partición de la masa seca de las frutas principalmente al aumentar la descarga de fotosintatos en la fruta a través de la regulación positiva simultánea del transporte y el metabolismo del azúcar (Ji et al. 2020). La luz azul (400-500 nm) puede facilitar la pérdida de humedad, al estimular la conductancia estomática y la transpiración. Por otro lado, la luz roja (600-700 nm) ayuda a retener la humedad en los tejidos de frutas y verduras (Hasan et al. 2017). Por su parte, Nadalini et al. (2017) encontraron que la luz azul (436 nm) y roja (666 nm) no modificaron las características principales de la calidad de fruto de la fresa (contenido de azúcares totales, acidez y consistencia de la pulpa), mientas que el color y la producción de antocianinas si se modificó. Además, se ha reportado que el momento de la aplicación también modificó las características de la calidad de los frutos de tomate, la suplementación con luz matutina mejoró la calidad nutricional de los frutos, mientras que la suplementación con luz vespertina mejoró su sabor (Wang et al. 2022). Sin embargo, no siempre la iluminación ha mejorado la calidad de los frutos, ya que se ha reportado que con diferentes tratamientos de iluminación LED roja (638 nm) y azul (450 nm) no se modificó la firmeza en frutos de tomate, al no encontrar ninguna vía de la lignina relacionada con la iluminación LED (Ntagkas et al. 2020).
Conclusiones
La iluminación suplementaria con LEDs puede mejorar ciertos aspectos del crecimiento y la composición química de las plantas y frutos de tomate y pepino, pero también puede tener efectos negativos. Los resultados indican que la suplementación LED influye en el crecimiento y la morfología de las plantas, aunque las respuestas varían según la intensidad de la luz y la especie vegetal. Es fundamental seleccionar las intensidades de luz azul, roja y roja lejana adecuadas para cada especie y aplicar la iluminación suplementaria LED de manera precisa para lograr los resultados deseados. Este estudio, permite identificar criterios claros en cuanto a la iluminación a través de LEDs como longitud de onda, sitio de iluminación, intensidad y tiempo de iluminación, que deben ser considerados para inducir respuestas positivas en los cultivos de tomate y pepino.
















