Introducción
La familia Asparagacea prolifera en zonas áridas y semiáridas que van desde el sur de Estados Unidos de América hasta Oaxaca, México. Dentro de esta se encuentra el género Dasylirion del cual se reconocen 24 especies, todas presentes en México y la mayoría identificadas como endémicas (Reyes-Valdés et al. 2012, Rodríguez-Trejo et al. 2019a, CONABIO 2023). Es mayormente reconocida por su valor económico, debido a que en el norte de México (Durango, Chihuahua y Coahuila) se destila para producir una bebida alcohólica con denominación de origen llamada sotol, que proviene del nombre común de la planta (IMPI 2002). En la Mixteca oaxaqueña esta planta de crecimiento silvestre se conoce como cucharilla, destacándose por la utilidad de sus hojas para la elaboración de arcos florales (Haeckel 2008, Reyes-Valdés et al. 2019) y de cucharas artesanales para las festividades religiosas, lo que promueve la tradición y conservación de costumbres en las localidades. Además, se reconocen usos de sus raíces, hojas, tallos e inflorescencias como medicina, forraje, alimento, ornato y uso del bagazo como biocombustible (SADER 2015, Hernández-Quintero et al. 2015, Duarte y Martínez 2019, PROFEPA 2020, González-Chávez et al. 2022). Actualmente productores de la Mixteca Oaxaqueña obtienen un destilado con excelente olor y sabor, conocido localmente como “mezcal de cucharilla”. Al respecto Palacios-Romero et al (2019) mencionan que, en el estado de Oaxaca se busca su aprovechamiento como bebida alcohólica.
La reproducción de esta planta es principalmente por semillas (Penfield 2017), situación de gran importancia para la sucesión, regeneración y dispersión de las especies (Bidwell 1979, Trejo et al. 2024), por lo que los factores externos en donde crecen juegan un papel fundamental para su propagación. Las semillas son el principal órgano reproductivo con tejido de reserva en estado de reposo, que al pasar por un proceso de imbibición se reactiva el metabolismo y el proceso fisiológico, dando paso a la germinación (Lambers et al. 2008, Doria 2010, Shalini et al. 2024), en el cual, el embrión debe tener la capacidad de pasar por el endospermo hasta salir por la cubierta de la semilla y generar la nueva planta (Rajjou et al. 2012, Bai et al. 2017). La germinación y el vigor son las características más importantes relacionadas con la calidad fisiológica de las semillas (Morales-Santos et al. 2017).
Una vez que las semillas se dispersan y llegan al suelo, el proceso de germinación se retrasa mediante la propiedad conocida como latencia de las semillas (Penfield 2017). En el caso de Dasylirion, sus frutos secos indehiscentes dificultan su germinación (3-22%), haciendo que la remoción del fruto sea indispensable para lograr la germinación mayor de 90% (Rodríguez-Trejo et al. 2019a). Esta especie tiene resistencia a altas temperaturas e incluso tolerancia a incendios intensos, sobre todo en plantas adultas (Rodríguez-Trejo et al. 2019b). Además, las características del área natural de proliferación impulsan a la planta y semillas a adaptaciones para sobrevivir. Por lo tanto, ciertos factores ambientales, a menudo la luz y la temperatura, pueden interrumpir la latencia de diferentes especies (Santiago et al. 2017). En la mayoría de las especies silvestres de Lupinus elegansyLupinus rotundiflorus de ecosistemas forestales, el calor es el factor importante para romper la latencia física, ya que reduce la impermeabilidad y de esta manera estimula la germinación (Valbuena y Vera 2002, Zuloaga-Aguilar et al. 2011, Ya-Fei et al. 2022).
La situación de las poblaciones silvestres de especies del género Dasylirion es preocupante, debido a que tres de ellas (D. acrotrichum (Schiede) Zucc., D. longissimum Lem. y D. quadrangulatum S. Watson) ya se encuentran incluidas en la NOM-059 (SEMARNAT 2010) en la categoría de amenazadas, y una sujeta a protección especial (D. palaciosii Rzed). De modo que la extracción de plantas de poblaciones silvestres, sin regulación y sin el manejo adecuado puede ocasionar la extinción local de la especie a corto plazo. Por lo anterior, en este estudio se evaluó el potencial germinativo de Dasylirion spp. recolectadas en tres sitios de la Mixteca Oaxaqueña, como respuesta a diferentes regímenes térmicos aplicados en los frutos, en condiciones de laboratorio, dando pautas para su conocimiento, manejo y conservación.
Materiales y métodos
Sitios de recolección de semillas
El material vegetal se recolectó en tres localidades de la Mixteca Oaxaqueña: a) Asunción Nochixtlán (Nx), que se ubica en las coordenadas 17° 27′ 26″ N y 97° 43′ 30″ O a 2 080 m. El clima es semiseco templado, con temperatura media anual de 17 °C y precipitación anual de 440 mm, predominan los suelos vertisol y luvisol. b) San Andrés Lagunas (SA), ubicado en las coordenadas 17° 34′ 21″ N y 97° 31′ 17″ O a 2 299 m. El clima es templado subhúmedo, con temperatura media anual de 16 °C y precipitación anual de 774 m, con suelo vertisol. c) San Jerónimo Tamazulapam (SJ), ubicado en las coordenadas 17° 38′ 06″ N y 97° 32′ 37″ O a 2 230 m. En el sitio predomina el clima templado subhúmedo, con temperatura media anual de 17 °C y precipitación anual de 900 mm, predominando el tipo de suelo vertisol (INEGI 2004, SIATL 2023).
La recolección de Nochixtlán se realizó en agosto del 2021, en San Andrés Lagunas y San Jerónimo en julio y agosto del 2022, respectivamente. Se seleccionaron escapos florales femeninos de plantas de sotol visiblemente sanas y vigorosas. La población de plantas en estos sitios se encuentra en laderas con pendiente pronunciada. Se seleccionaron al azar plantas de sotol visiblemente sanas y vigorosas con presencia de escapos florales femeninos por sitio y por progenitor, al momento de la colecta se mantuvieron separados en bolsas de papel previamente enumeradas con aireación constante y bajo sombra.
Calidad de semillas
Las semillas se extrajeron manualmente a los 21 días y se determinó su calidad de acuerdo con las Reglas Internacionales para el Análisis de Semillas (ISTA 2019), cada sitio de recolección se consideró un tratamiento.
La determinación del peso (g) de 1000 semillas (P1000) se realizó con balanza analítica (Sartorius, modelo CP224, Goettingen, Germany), en 10 grupos de 100 semillas. Con el peso obtenido de cada grupo de semillas se estimó el número de semillas por kg-1. Se aplicó la siguiente fórmula:
Posteriormente, a estos grupos de semillas se les retiró las impurezas manualmente y nuevamente se pesaron, de esta forma se determinó la pureza de las semillas y se aplicó la siguiente fórmula:
Las semillas con tamaño de 3.5 a 4.0 mm de longitud y 3.0 a 4.0 mm de ancho, esferoidales, trigonales, de textura lisa y de color café dorado, fueron consideradas puras; se consideró como impurezas aquellas semillas demasiado pequeñas, perforadas por insectos, con manchas producidas por hongos, negras, plegadas, además de la presencia de objetos como piedras, basuras o ramillas.
La viabilidad se determinó en cuatro grupos de 25 semillas, las cuales se colocaron en tubos Eppendorf™ y se les agregó 2.0 mL de solución 2,3, 5-trifenil-tetrazolio al 1%. Se envolvieron con papel aluminio para limitar la exposición de la luz, y se dejaron en reposo por 24 h a temperatura ambiente. Las semillas se observaron interna y externamente con un microscopio estereoscópio (ZEIZZ, STEMI 305, Jena, Germany). Solo se consideraron como viables aquellas que presentaron tinción roja y se descartaron las de tinción tenue y sin tinción.
El contenido de humedad se obtuvo en cuatro grupos de 25 semillas, estas se colocaron en cajas Petri y se introdujeron en una estufa de secado a 40 °C por 72 h, donde alcanzaron el peso constante. Las semillas se pesaron al inicio y al final de este proceso y se aplicó la siguiente fórmula:
Germinación
Con la finalidad de deshidratar los frutos y extraer las semillas, se les aplicó calor artificial por tiempos determinados, aplicando posibles temperaturas que no afectaran la germinación. El estudio se realizó mediante un diseño completamente al azar, enmarcado en una factorial 3x3x3, esto es, tres sitios: San Jerónimo, San Andrés y Nochixtlán; tres temperaturas-tiempo: 40 °C por 35 min, 58 °C por 4 min y 25 °C por 21 días (testigo); y tres métodos de aplicación de calor artificial: 1) calor con estufa de secado, que consistió en colocar los frutos en cajas Petri (100×20 mm de diámetro y altura) y se introdujeron en una estufa de secado (Felisa®, modelo FE-291, Jalisco, México); 2) calor con arena de río, se agregó 1.5 cm de espesor de arena en un recipiente de barro y se colocó sobre una estufa con quemador de gas (mabe®, modelo Em7641bai, México). Cuando la temperatura se estabilizó y homogenizó en la arena de acuerdo con las temperaturas y tiempos establecidos, se colocaron los frutos sobre el sustrato. Se midió la temperatura con un termómetro (SETA, ASTMS65CZ, Surrey, Inglaterra). Posteriormente, se separaron los frutos de la arena y se almacenaron en recipientes de plástico con tapa; 3) sin aplicación de calor artificial, los frutos se colocaron sobre papel absorbente y se mantuvieron bajo sombra. Para la extracción de las semillas se les aplicó abrasión manual y se guardaron en tubos Eppendorf™ hasta su siembra.
La siembra se realizó en cajas petri (90×15 mm de diámetro y altura), con algodón humectado de agua destilada y 3 g L-1 de fungicida (Carboxamida). Se introdujeron en una cámara de germinación (BIOTRONETTE MARK III ®, modelo 846, Melrose Park, IL, USA) a 25 °C, con fotoperíodo de 12 h luz y 12 h oscuridad. Se consideró como semilla germinada la aparición de la radícula visible (ISTA 2019), este dato se registró diariamente a la misma hora. La unidad experimental se conformó de 20 semillas con cinco repeticiones.
Indicadores de vigor de las semillas
Los indicadores de vigor se obtuvieron a partir del número de semillas germinadas acumuladas. Los días a germinación (DAG) se determinaron contando los días desde la siembra hasta la primera semilla germinada (Czabator 1962). El periodo de energía (PE) se refiere cuando el número de semillas que germinaron por día alcanzaron su máxima (FAO 1983). La velocidad de germinación (VG) se determinó mediante la fórmula de Nakagawa (1999), donde: VG = número de semillas germinadas por día, Ni = número de días acumulados desde el inicio del ensayo de germinación, y Gi = número acumulado de semillas germinadas en el día i-ésimo. El valor G es una media aritmética de los Ni ponderada por los Gi, por lo tanto, las unidades de esta velocidad se indica en días.
Además, se calculó el índice de Velocidad de Germinación (IVG) (Maguire 1962), el cual se expresó como número de semillas germinadas por día; donde Xi = número de semillas germinadas por día; Ni = número de días después de la siembra; n = número de conteos, donde, i =1,2,3,…,n conteos.
Por último, se obtuvo la potencia germinativa (PG). Se cuantificó el número de semillas que germinaron (Sg) con relación al número total de semillas sembradas (Czabator 1962).
Análisis estadístico
Con base a los supuestos de normalidad (Shapiro-Wilk) y homogeneidad de varianzas (Bartlett) (α = 0.05), las variables DAG, IVG, VG y PG se transformaron con
Resultados
Calidad de semilla
El peso de las 1000 semillas osciló entre 1.82 g y 5.28 g, valores inversamente relacionados con el número de semillas kg-1, esto es, cuanto mayor fue el peso, menor fue el número de semillas kg-1 (Tabla 1). Las semillas limpias o puras presentaron color café claro, superficie lisa y consistencia firme; las semillas con impurezas fueron de color negro, plegadas o rugosas, incompletas, dañadas y perforadas por insectos. El valor de impurezas que se encontraron en San Andrés (SA) fue el más alto (65 %) de las tres localidades, presentó mayormente semillas con ataques de insectos y plegadas de color negro. El análisis con tetrazolio mostró un intervalo del 45 % entre el valor mayor (70 %) y menor (25 %) de viabilidad. Las semillas procedentes de San Jerónimo (SJ) presentaron el valor más alto de semillas viables. Todas las muestras obtuvieron valores bajos de humedad, con intervalos de variación de 4 % hasta 10 %.
Tabla 1 Indicadores físicos de semillas de Dasylirion spp. procedentes de la Mixteca oaxaqueña.
| Sitio | Peso de 1000 semillas (g) | Número de semillas kg-1 | Pureza (%) | Viabilidad (%) | Humedad (%) |
|---|---|---|---|---|---|
| San Andrés | 1.82 ± 0.01 | 549 450 ± 42 985 | 35 ± 1.5 | 25 ± 3.5 | 7 ± 2.8 |
| San Jerónimo | 5.28 ± 0.01 | 189 393 ± 5 551 | 88 ± 2.7 | 70 ± 5.0 | 10 ± 1.5 |
| Nochixtlán | 3.52 ± 0.00 | 284 090 ± 69.06 | 50 ± 3.0 | 45 ± 4.1 | 4 ± 0.9 |
Medias ± error estándar
Indicadores de vigor
Durante el proceso germinativo, los análisis de varianza mostraron que las fuentes de variación, aplicadas sobre las semillas no influyeron significativamente (P > 0.05) en el comportamiento de los días a germinación, periodo de energía, velocidad germinativa e índice de velocidad de germinación. Se encontraron diferencias altamente significativas (P ≤ 0.01) en la potencia germinativa de acuerdo con la temperatura, el método de aplicación de calor, las interacciones sitio-temperatura y sitio-temperatura-método de aplicación de calor.
Los indicadores de vigor de San Andrés fueron significativamente (Duncan, P ≤ 0.05) más bajos que San Jerónimo y Nochixtlán (Tabla 2), lo que es atribuido al bajo peso de las semillas, menor pureza, viabilidad y humedad, en otras palabras, a la baja calidad de la semilla. Las semillas procedentes de San Jerónimo expresaron los mayores índices de vigor. Las diferentes temperaturas-tiempo no influyeron significativamente en los indicadores de vigor evaluados. Sin embargo, la tendencia observada en el nivel 25 °C-21 días (testigo) fue que los índices de vigor se alcanzan en menores días. En general, los índices de vigor se beneficiaron cuando se aplicó calor artificial a los frutos, y específicamente estimularon de forma significativa (Duncan, P ≤ 0.05) los días a germinación (DAG), esto es, sin calor artificial esta variable fue significativamente menor. Se observaron menor número de días para alcanzar la misma potencia germinativa.
Tabla 2 Indicadores de vigor en semillas de Dasylirion spp. en función de los factores sitio de recolección, temperatura- tiempo y método de secado.
| Factores | Días a germinación | Periodo de energía (días) | Velocidad de germinación (días) | Índice de velocidad de germinación | Potencia germinativa (sg/ss) |
|---|---|---|---|---|---|
| Sitio | |||||
| San Andrés | 3.24 ± 4.2 b | 4.40 ± 6.2 b | 4.52 ± 5.3 b | 0.60 ± 1.0 c | 0.05 ± .06 c |
| San Jerónimo | 5.04 ± 0.9 a | 14.04 ± 2.7 a | 11.0 ± 1.8 a | 11.63 ± 4.2 a | 0.85 ± 0.1 a |
| Nochixtlán | 5.52 ± 3.2 a | 12.20 ± 6.3 a | 9.56 ± 4.3 a | 3.20 ± 3.0 b | 0.17 ± .09 b |
| Temperatura-tiempo | |||||
| 25 °C-21 días | 5.73 ± 3.5 a | 11.93 ± 7.7 a | 9.84 ± 5.9 a | 4.90 ± 6.4 a | 0.35 ± 0.3 a |
| 40 °C-35 min | 4.53 ± 3.3 a | 9.33 ± 6.6 a | 7.39 ± 4.7 a | 5.11 ± 6.0 a | 0.35 ± 0.3 a |
| 58 °C-4 min | 4.10 ± 2.8 a | 10.80 ± 6.0 a | 8.63 ± 4.5 a | 4.90 ± 5.1 a | 0.35 ± 0.3 a |
| Método de secado | |||||
| Sin calor artificial | 5.73 ± 3.5 a | 11.93 ± 7.7 a | 9.84 ± 5.9 a | 4.90 ± 6.4 a | 0.35 ± 0.3 a |
| Calor_estufa | 4.86 ± 4.1 b | 8.93 ± 6.1 a | 7.55 ± 5.0 a | 4.45 ± 5.9 a | 0.35 ± 0.4 a |
| Calor_arena | 3.76 ± 1.4 b | 11.20 ± 6.4 a | 8.47 ± 4.2 a | 5.56 ± 5.1 a | 0.36 ± 0.3 a |
Letras distintas en la misma columna y dentro de cada factor representan diferencias significativas (Duncan, P ≤ 0.05). sg/ss = semillas germinadas entre semillas sembradas. Media ± desviación estándar.
Respuesta del régimen térmico en la germinación de semillas
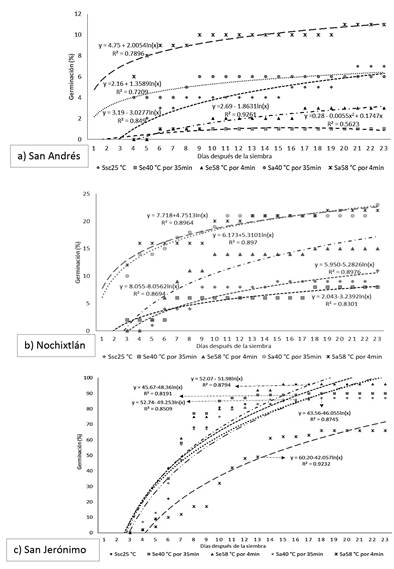
La germinación de las semillas se observó hasta los 30 días. En San Andrés (Figura 1a) la germinación con aplicación de calor apenas fue del 10 % con un mínimo del 1 %. Los modelos logarítmicos alcanzaron un coeficiente de determinación (R2) superior al 70 % y solo un modelo polinómico alcanzó un R2 del 56 %. En Nochixtlán (Figura 1b) se alcanzó una germinación del 6 al 21 %. Los modelos que mejor explicaron la germinación fueron logarítmicos con R2 superior al 80%. En San Jerónimo (Figura 1c) se obtuvo entre el 70 y el 95 % de germinación, y se alcanzó entre los 14 y 15 días después de la siembra. La aplicación de calor facilitó considerablemente la extracción de semillas debido a la deshidratación y rompimiento del pericarpio del fruto.
Discusión
La variación en la cantidad de semillas (unidades kg-1) registrada entre los diferentes sitios obedece a la estrategia reproductiva de la planta silvestre, lo cual beneficia su dispersión y capacidad adaptativa para su propagación natural (Rubio-de Casas et al. 2017, Leslie et al. 2017, Benavides-Mendoza et al. 2023). En tanto que Rodríguez-Trejo et al. (2019a) encontraron en el Valle de Tehuacán-Cuicatlán, en Dasylirion lucidum Rose, un menor número por kg (141 615 semillas), mayor peso en 1 000 semillas (7.08 g) y mayor viabilidad (74%) respecto a los valores encontrados en el presente estudio. Esta diversidad quizás está influenciada por su polinización libre y cruzada de las especies, lo cual puede generar una diversidad morfológica de las poblaciones (Reyes-Valdés et al. 2012, Trejo et al. 2024) además, de que puede estar delimitada por las condiciones climáticas y tipo de suelo donde se desarrollan (Villanueva-Castillo et al. 2021). Las semillas plegadas y de color negro encontradas, podrían estar relacionadas con un estrés ambiental, debido a que una estrategia clave para que la mayoría de las semillas sobrevivan el mayor tiempo posible, es alcanzar un estado desecado para reducir su actividad metabólica, lo que necesariamente conduce al estrés oxidativo y, por lo tanto, a la senescencia (Kranner et al. 2010, Nagel et al. 2015, Pastrana-Ignes et al. 2023).
El peso y la densidad de las semillas están asociados con mayor endospermo y embriones más grandes y maduros, ya que debe tener la energía necesaria para lograr la ruptura del endocarpio; el vigor está relacionado con la calidad fisiológica de las semillas, que a su vez depende de su genética, madurez, condición ambiental durante su crecimiento, deterioro, envejecimiento y sanidad (Morales-Santos et al. 2017, ISTA 2019, Lin et al. 2022). Por lo tanto, una semilla de calidad competente garantiza buenos rendimientos, como lo mostraron las semillas de San Jerónimo, que proyectaron los indicadores más altos en calidad física (peso, pureza y humedad), mayor viabilidad y potencial germinativo, lo cual beneficiara el establecimiento de plántulas a futuro.
Los resultados de la baja calidad y germinación en la muestra de San Andrés, pueden ser ocasionados por las condiciones ambientales estresantes, baja precipitación, diferentes características de los suelos en donde crecen, e incluso una deficiente polinización, aspectos que suelen variar fuertemente entre microrregiones y que es característico de la Mixteca Oaxaqueña. Lo anterior causa la disminución en el número y tamaño de las semillas, y por lo tanto la reducción del vigor, afectan directamente a la planta madre durante el desarrollo de la semilla (He et al. 2014, Renard et al. 2021, CONAGUA 2023). Los indicadores de vigor significativamente bajos podrían estar relacionadas con la reducción del peso de las semillas, debido a que, en los procesos metabólicos de la germinación, se da el crecimiento y la diferenciación de células del embrión, de esta manera agotan sus reservas del endospermo, es decir, un buen contenido de reservas promueve una exitosa germinación y emergencia (Bidwell 1979, Celis-Velázquez et al. 2010, Basu y Groot 2023, Sripathy y Groot 2023).
La temperatura ambiental es un factor importante para la germinación, su influencia dependerá de la especie y del tipo de latencia, debido a diferentes adaptaciones ecofisiológicas en donde se han desarrollado (Rojas-Aréchiga et al. 1998). La aplicación de calor moderado o un choque térmico, es un factor eficiente para eliminar la latencia de la cubierta, esto se debe a que reduce la impermeabilidad y estimula la germinación, especialmente cuando es física (Vázquez-Yanes y Orozco-Segovia 1982, Zuloaga-Aguilar et al. 2011, Ren y Bai 2017, Ya-Fei et al. 2022). En el caso de las semillas de Dasylirion recolectadas en San Jerónimo, alcanzaron el 96% de germinación al aplicar calor de 58 °C durante 4 minutos en la estufa de secado. Por su parte, Rodríguez-Trejo et al. (2019a) obtuvieron el 94.3% de germinación solo con remoción del fruto manual a los 14 días. Los embriones y el endospermo presentan respuestas distintas ante elevadas temperaturas, y la germinación de las semillas se inhibe cuando se someten a períodos prolongados con temperaturas superiores a las óptimas, esto va a depender también de la especie (Yan et al. 2014). Posiblemente fue lo que disminuyó el 30% de la germinación en la muestra de San Jerónimo con el método de aplicación en arena, a una temperatura de 58 °C por 4 min.
Las plantas de Dasylirion han desarrollado adaptaciones como respuesta a ambientes hostiles y versátiles, e incluso tolerancia al fuego en incendios forestales (Rodríguez-Trejo et al. 2019b). Ciertas poblaciones de la familia Asparagaceae, presentan variaciones morfológicas y de floración, lo que va a depender de su distribución geográfica e influencia antrópica (Jimenez-Torres et al. 2021, Eshel et al. 2022). Es así, que la encapsulación de la semilla en paredes de frutos (pericarpio), tiene funciones protectoras y de dispersión en muchas familias de plantas (Huss y Gierlinger 2021). Esta característica está relacionada con la latencia física que presentan las semillas (Juárez-Morales et al. 2023), por lo que esta especie puede responder al ambiente semiárido donde habitan, de manera que la cubierta flexible y dura de los frutos sirve como protección. Lo anterior puede estar relacionado con que las temperaturas aplicadas, no influyeron significativamente en los indicadores de vigor evaluados, e incluso en la aceleración de la germinación. La temperatura juega un papel importante, tanto en la regulación de la latencia como de la germinación, debido a que las semillas detectan cambios en su entorno y ajustan rápidamente su estado de latencia en respuesta, ya que son altamente sensibles a las señales ambientales (luz, temperatura, entre otros) (Footitt et al. 2014, Nautiyal et al. 2023).
Finalmente, las semillas obtienen la vida útil durante la maduración y está influenciada por su estructura, su genética y el ambiente, de esta manera se considera semillas ortodoxas cuando son viables con un contenido de humedad del 5 al 10% (FAO 2019, Ranganathan y Groot 2023). Esto es, mientras las semillas tengan procesos metabólicos lentos, mediante un proceso de control del contenido de agua y oxígeno, se mantendrán latentes lo suficiente para un crecimiento exitoso posterior (Lambers et al. 2008, Pastrana-Ignes et al. 2023). Este tipo de semillas están relacionadas a ambientes áridos cálidos erosivos, donde las semillas pueden permanecer secas gracias a los intervalos irregulares de lluvias (Probert et al. 2009, Pellizzaro et al. 2020). Además, las semillas silvestres tienen la capacidad para sobrevivir y germinar en condiciones ambientales adversas (Morales-Santos et al. 2017, Huss y Gierlinger 2021). Por lo que se infiere que las semillas de Nochixtlán después de un año de resguardo expuestas a la temperatura ambiente pudieran sobrevivir con un contenido de humedad del 4 %, de esta forma, las semillas parecen tener un comportamiento de almacenamiento ortodoxo.
Conclusiones
Las semillas de Dasylirion recolectadas en San Andrés, San Jerónimo y Nochixtlán presentaron variación intraespecífica. Las semillas de San Jerónimo mostraron mayor calidad con base en el peso de 1 000 semillas (5.28 g), pureza (88 %), viabilidad (70 %) y contenido de humedad (10 %), lo cual se reflejó en los índices de vigor, debido a que superaron significativamente en velocidad germinativa, índice de velocidad de germinación y porcentaje germinativo a las semillas provenientes de San Andrés y Nochixtlán. Las semillas con los indicadores de calidad física más altos (peso, pureza y humedad) garantizaron mejor rendimiento y por tanto mayor vigor, lo que se reflejó en una germinación significativa. El tratamiento pregerminativo de aplicación de calor en la estufa a 58 °C por 4 minutos, alcanzó 96% de germinación en 15 días en las semillas de San Jerónimo. Además, dicho tratamiento modificó la estructura física y la resistencia mecánica del fruto, se deshidrató la cubierta de la semilla y se rompió la latencia física.