La familia Bromeliaceae es una de las más ricas en especies del Neotrópico con cerca de 3,800 especies distribuidas en 82 géneros (Gouda et al. 2023), la mitad de los cuales incluyen especies epífitas (Zotz 2013, Givnish et al. 2014). Esta familia ha pasado por una de las radiaciones adaptativas más notables en las angiospermas, en parte debido a la diversidad de estrategias reproductivas que presenta (Benzing 2000, Givnish et al. 2014); la mayoría de las especies muestran flores bisexuales y el sistema reproductivo predominante es la autofecundación o un sistema mixto entre ésta y la fecundación cruzada (Matallana et al. 2010, Zanella et al. 2012, Cascante-Marín & Núñez-Hidalgo 2023). No obstante, el número de especies en las cuales se ha documentado su sistema reproductivo (152 especies) es bajo considerando la riqueza total de esta familia (Cascante-Marín & Núñez-Hidalgo 2023).
Las flores de las bromelias son polinizadas por insectos (abejas, mariposas diurnas y polillas nocturnas) (Benzing 2000, Krömer et al. 2006, Kamke et al. 2011), colibríes (Martinelli 1994, Kessler & Krömer 2000, Kessler et al. 2020), aves paseriformes (Hornung-Leoni et al. 2013) y murciélagos (Aguilar-Rodríguez et al. 2019). Sin embargo, la mayoría de las especies no cuentan con observaciones de sus polinizadores, limitándose a inferencias sobre síndromes de polinización (Faegri & van der Pijl 1979, Fenster et al. 2004).
Se estima que por lo menos la mitad de las especies de bromelias podrían ser polinizadas por colibríes (Benzing 2000, Canela & Sazima 2005, Kessler et al. 2020). Por ejemplo, en cadenas montañosas de los Andes o en la Mata Atlántica de Brasil, 40-85 % de las especies de bromelias son polinizadas principal o exclusivamente por colibríes (Kessler & Krömer 2000, Krömer et al. 2006, de Queiroz & Varassin 2007). Estas aves, transportan una mayor carga polínica y a mayores distancias que los insectos (Krauss et al. 2017). Además, su comportamiento de forrajeo en rutas de alimentación (traplining), favorece la polinización cruzada y un mayor flujo de polen entre poblaciones (Serrano-Serrano et al. 2017).
Aunque se espera que los rasgos del síndrome de polinización reflejen la adaptación de las flores a los polinizadores primarios, éstos no excluyen a los polinizadores secundarios (menos efectivos espacio-temporalmente por sus características, comportamiento y/o abundancia) y tampoco a los visitantes antagonistas (p. ej., florívoros, ladrones de polen y de néctar) (McCall & Irwin 2006, Ashworth et al. 2015). En algunas familias de plantas como Bromeliaceae, los polinizadores secundarios pueden asegurar su reproducción cuando los polinizadores primarios disminuyen o están ausentes (Schmid et al. 2011, Aguilar-Rodríguez et al. 2016, Jaeger et al. 2023). Por otro lado, los antagonistas influyen directa e indirectamente en la adecuación (fitness) de las plantas, por medio del consumo de tejidos florales, lo que tiene un impacto negativo en la atracción de polinizadores (p. ej., afectando la producción de frutos y semillas) (Hargreaves et al. 2009, Moreira et al. 2019). Por lo tanto, la selección fenotípica ejercida por antagonistas y polinizadores secundarios puede ayudar a explicar los rasgos reproductivos florales que no coinciden con el polinizador primario, así como revelar cuáles rasgos modulan estas interacciones entre especies (Stebbins 1970, Fenster et al. 2004, Strauss & Irwin 2004, Rosas-Guerrero et al. 2014, Ashworth et al. 2015).
Tillandsia limbata Schldl. presenta características florales que no se relacionan con la polinización por colibríes, como son los pétalos blancos y una antesis nocturna. Debido a ello, Gardner (1986) sugirió que esta especie podría ser polinizada por polillas, sin embargo, hasta la fecha esto no se ha confirmado. Esta especie es relativamente común en bosques tropicales y vegetación derivada de estos en México, por lo que diversos estudios taxonómicos y listados florísticos la incluyen en sus registros (p. ej., Espejo-Serna et al. 2005, Krömer & Acebey 2007, Pinzón et al. 2019). Sin embargo, hasta donde tenemos conocimiento no se ha estudiado su sistema de polinización, lo que permitiría mejorar la comprensión de los aspectos ecológicos y evolutivos que han propiciado los diversos patrones reproductivos en Bromeliaceae. El presente trabajo caracteriza la biología floral y el sistema reproductivo de T. limbata, para determinar cuáles son sus polinizadores efectivos, si estos son consistentes con lo predicho por su síndrome floral y cómo contribuyen en la reproducción de esta bromelia endémica de México.
Materiales y métodos
Sitio de estudio. El estudio se realizó en la comunidad de Tres de Mayo, municipio de Catemaco, ubicado dentro de la Reserva de la Biósfera Los Tuxtlas, al sureste del estado de Veracruz, México (18 ° 32’ 17.8" N, 95 ° 3’ 48.4" O; Figura 1). El sitio tiene una altitud de 90 m snm, presenta una temperatura máxima de 27.3 °C y una mínima de 21.5 °C, y una precipitación promedio anual de 1,500 a 3,000 mm. La temporada con mayor temperatura y mayores precipitaciones va de junio a febrero, y la seca, con menores precipitaciones y mayor temperatura, va de marzo a mayo (Soto & Gama 1997). Esta región representa el límite boreal de distribución de la selva alta perennifolia en el continente americano; sin embargo, cerca del 80 % de la extensión original de este tipo de vegetación desapareció en la década de 1990 (Dirzo & García 1992). Actualmente, se observa una matriz de pastizales, con elementos de vegetación secundaria (acahuales) y cultivos, entre los que destacan las plantaciones de maíz y cítricos, así como remanentes de selva alta perennifolia (Guevara et al. 2004).
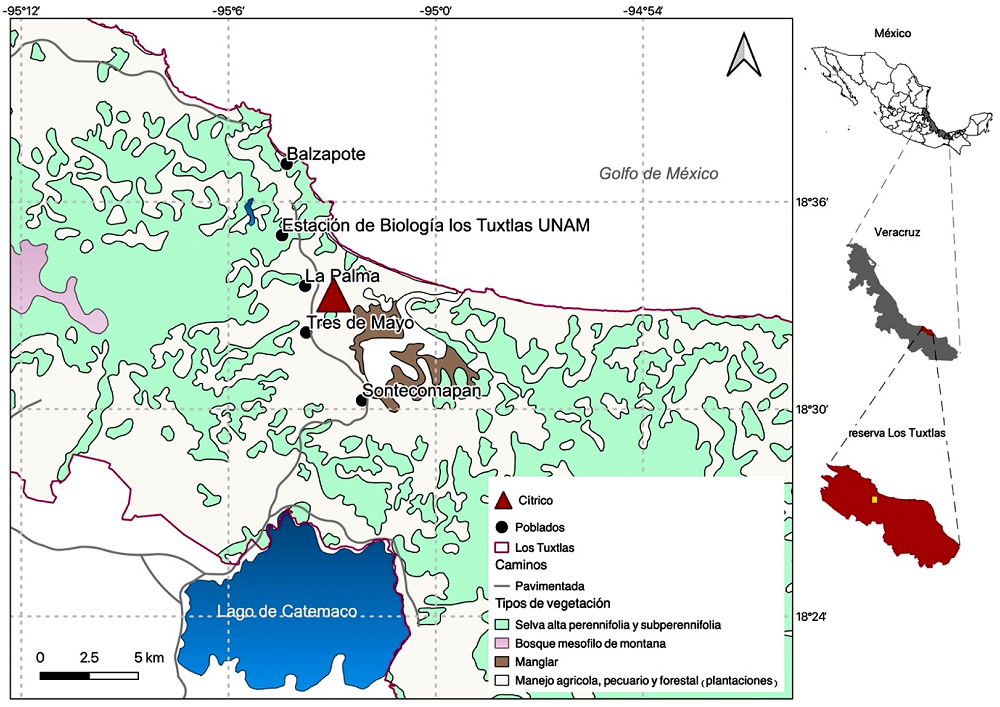
Figura 1 Ubicación del área de estudio (triángulo rojo), dentro del polígono de la Reserva de la Biósfera Los Tuxtlas, Veracruz, México. Se muestran con puntos negros las localidades cercanas a la parcela de estudio ubicada en la localidad Tres de Mayo.
El trabajo de campo se realizó entre abril y octubre del 2021 en una parcela de 6,730 m2, la cual presenta un cultivo de cítricos (Citrus sinensis (L.) Osbeck., C. aurantifolia (Christm.) Swingle, C. latifolia Tanaka ex Q. Jiménez), con 20 años de abandono y con árboles remanentes de vegetación primaria. Los árboles de cítricos son de baja altura y presentan un gran número de individuos adultos de T. limbata en sus ramas, lo que permitió una gran disponibilidad de plantas para realizar las observaciones y experimentos que se describen posteriormente.
Especie de estudio. Tillandsia limbata es una especie epífita endémica de México, que se distribuye en los estados de Chiapas, Hidalgo, Oaxaca, Puebla, Querétaro, San Luis Potosí y Veracruz (Espejo-Serna et al. 2017, Espejo-Serna & López-Ferrari 2018). Habita principalmente en bosque caducifolio, bosque de encino, cafetal, manglar, matorral, selva alta perennifolia, selva baja, selva mediana y selva mediana subperennifolia, a una altitud entre 0-1,200 m (Espejo-Serna et al. 2005, Krömer et al. 2020). Presenta inflorescencias terminales, erectas, compuestas, dos veces divididas, con hasta 15 espigas, el eje floral es de color magenta a rosado, cilíndrico, robusto, de 35-70 cm de largo, 3-15 mm de diámetro, cubierto parcialmente por las vainas de las brácteas. Las flores son sésiles, presentan una corola tubular blanquecina-verdosa, dísticas, erectas, 5-16 por espiga, actinomorfas a ligeramente zigomorfas, geniculadas a curvadas (Espejo-Serna et al. 2005) (Figura 2).

Figura 2 Lado izquierdo, vista general de una planta de Tillandsia limbata, la barra blanca equivale a 50 cm de longitud. Lado derecho, detalle de una inflorescencia y una flor en antesis, la barra blanca equivale a 5 cm de longitud.
Fenología floral. El seguimiento de la dinámica de floración se realizó en 20 individuos seleccionados al azar en el campo de cítricos, registrando en cada uno el número de flores abiertas cada día durante toda la floración. De acuerdo con Dafni (1992), se identificó: el inicio de la floración (hasta que el 25 % de las flores están abiertas), el pico de floración (> 50 % o más de flores abiertas) y el término de la floración (< 10 % abiertas). Posteriormente, se calculó el número de flores promedio por inflorescencia y la duración total de la floración. En estas mismas plantas se seleccionaron algunas flores (n = 20) para observar su tiempo de vida, registrando las siguientes etapas: 1) Pre-antesis: cuando el botón emerge de la bráctea floral y comienza a crecer; 2) Antesis: lapso que incluye la apertura de la corola, la dehiscencia de las anteras y la receptividad del estigma; 3) Senescencia: momento en el que ocurre la marchitez de los pétalos, así como la pérdida de turgencia de los estambres y el pistilo (Dafni 1992, Cascante-Marín et al. 2005).
El registro de las fases florales se realizó utilizando dos cámaras digitales (modelos D800 y D7100, Nikon Corporation, Tokio, Japón), equipadas con lentes para macrofotografía (modelos atx-i 100 mm, Tokina Corporation, Tokio, Japón y micro Nikkor 55 mm, Nikon Corporation, Tokio, Japón). Las cámaras se colocaron en trípodes delante de las inflorescencias, enfocando los botones florales a 30 cm de distancia de estos. Se programó la toma de fotografías en intervalos de cinco minutos, iniciando desde la condición de botón hasta la marchitez de la flor. Las series fotográficas obtenidas fueron analizadas mediante la técnica cinematográfica de cámara rápida (time-lapse), utilizando los programas Adobe Lightroom Classic 2019, LR Timelapse 5 y DaVinci Resolve (versión 17.2). Esto permitió observar detalladamente, y en poco tiempo (cerca de un minuto), las diferentes etapas de la antesis (Material suplementario 1 y 2).
Para estimar el tiempo de receptibilidad del estigma, se colectaron estigmas vírgenes (n = 21 plantas mantenidas en el vivero) desde el inicio de la antesis y por intervalos de cuatro horas hasta cumplir 24 horas (tiempo de vida de las flores). Los estigmas se sumergieron individualmente en peróxido de hidrógeno (H2O2) al 3 %. La efervescencia, producto de una alta reacción enzimática, fue indicativo de receptividad (Dafni 1992, Dafni & Motta 1998). Durante la colecta de los estigmas, se observó la presencia de exudado, lo que también fue indicativo de receptividad, pues favorece la hidratación y germinación del polen (Dafni 1992, Martén-Rodríguez & Fenster 2008).
Sistema reproductivo. Para determinar el sistema reproductivo de T. limbata se aplicaron los siguientes tratamientos de polinización manual (sensuKearns & Inouye 1993) en 20 individuos (40 flores por tratamiento, dos flores por individuo). Las plantas fueron medidas, etiquetadas y mantenidas en un vivero portátil instalado dentro de la parcela de estudio. Las flores se cubrieron con tela semipermeable antes y después de las manipulaciones para evitar la llegada de polen no deseado. Los tratamientos de polinización aplicados fueron: 1) Apomixis, con ayuda de pinzas de disección se removieron las anteras indehiscentes de la flor tratada antes de las primeras horas de la antesis; 2) Autopolinización espontánea, se embolsó la espiga completa desde la condición de botón sin realizar manipulación de las flores; 3) Autogamia, se removieron las anteras dehiscentes de la flor tratada y se frotaron en el estigma de la flor a la que pertenecían las anteras; 4) Geitonogamia, se emasculó la flor tratada y se polinizó con las anteras dehiscentes de otra flor del mismo individuo; 5) Xenogamia, se frotaron las anteras dehiscentes provenientes de tres individuos diferentes en el estigma de la flor tratada, la cual fue previamente emasculada; 6) Control (polinización natural), las flores estuvieron expuestas todo el tiempo a los visitantes florales.
La presencia de frutos se registró y cuantificó cuatro meses después de aplicar los tratamientos, y para cada tratamiento se calculó el porcentaje de fructificación (fruit set). Los frutos se colectaron en bolsas de papel individuales, se pesaron y se registró el número de semillas por fruto (seed set). Para determinar si T. limbata es autocompatible, se obtuvo el Índice de Incompatibilidad Autógama (ISI por sus siglas en inglés); calculado como el cociente del número de semillas promedio por fruto del tratamiento de autogamia entre el número de semillas promedio por fruto del tratamiento de xenogamia; donde valores ≥ 1 indican que la planta es autocompatible, valores < 1 pero ≥ 0.3 indican que la autocompatibilidad es incompleta y valores ≤ 0.3 indican autoincompatibilidad (Zapata & Kalin 1978, Ramírez & Brito 1990). También se calculó el Índice de Autopolinización Autógama (IAS por sus siglas en inglés) calculado como el cociente del número promedio de semillas por fruto del tratamiento de autopolinización espontánea entre el número promedio de semillas por fruto del tratamiento de autogamia multiplicado por 100 (Martén-Rodríguez & Fenster 2008); donde valores ≥ 1 indican autogamia, valores > 0 pero < 1 indican autogamia parcial y valores = 0 se obtienen en plantas que presentan mecanismos eficaces para prevenir la autogamia (Zapata & Kalin 1978, Wendt et al. 2002, Kamke et al. 2011). Para determinar si existe limitación de polen en la población, se calculó el Índice de Limitación de Polen (PLI por sus siglas en inglés) utilizando la siguiente razón matemática: 1-(número promedio de semillas del tratamiento control entre el número promedio de semillas del tratamiento de xenogamia (Larson & Barret 2000, Becker et al. 2011). Para este índice, valores negativos indican que la población no presenta limitación de polen (Becker et al. 2011).
Análisis de néctar. La tasa de producción y concentración de azúcares en el néctar se midió en 40 flores vírgenes (flores sin tratamientos experimentales y aisladas de los polinizadores) elegidas al azar entre los 20 individuos mantenidos en vivero (dos flores por individuo). El néctar se extrajo con ayuda de tubos microcapilares de 5 μl, en intervalos de dos horas, desde el inicio de la antesis hasta que la producción descendió a cero, un poco antes de la senescencia de las flores. Cuando el néctar no llenó el microcapilar se midió la altura alcanzada por el líquido con un vernier, y posteriormente se calculó el volumen obtenido mediante una regla de tres. El volumen total de néctar por flor se calculó como la suma de los valores horarios (Tschapka & Helversen 2007). Para cada una de las muestras de néctar se registró la concentración de azúcares (°Brix, 1 g azúcares / 100 g de solución), mediante el uso de un refractómetro manual (Mod. HRT32, rango: 0-32 % Brix, precisión: 0.2 % Brix; A. Krüss Optronic, Hamburg, Germany).
Visitantes florales. Se realizaron observaciones focales en los árboles que presentaban mayor número de individuos de T. limbata en sus ramas, de la siguiente manera: 1) Observaciones diurnas directas (n = 20 inflorescencias): se instaló un escondite portátil a seis metros de distancia del árbol hospedero, desde el cual se observaron hasta cinco individuos en floración cuando se encontraban de manera contigua. Las observaciones se realizaron en un horario de 07:00 a 13:30 h y de 16:30 a 18:00 h, durante 18 días, acumulando un total de 120 horas de muestreo. En cada periodo de observación se cuantificó el número de flores disponibles; 2) Observaciones diurnas indirectas: se realizaron registros en flores individuales de inflorescencias aisladas (n = 24 flores) utilizando el equipo fotográfico descrito anteriormente (ver sección de fenología floral). Las cámaras se colocaron en trípodes enfrente de la inflorescencia, enfocando las flores a 60 cm de distancia. Las grabaciones y toma de fotografías se realizaron de manera automatizada mediante la técnica de foto-trampeo, utilizando sensores de movimiento (pir motion sensor v2, Camtraptions, Willersey, United Kingdom) (Material suplementario 3). El registro se realizó en los periodos de mayor actividad de forrajeo de los visitantes, de 07:00 a 09:00 h y de 11:00 a 13:00 h durante ocho días, para un esfuerzo total de muestreo de 236 minutos (ca. 4 horas) de grabación de video y 840 fotografías. Las series fotográficas y videograbaciones fueron procesadas con ayuda de los programas Adobe Lightroom Classic 2019, LR Timelapse 5 y DaVinci Resolve (versión 17.2); 3) Observaciones nocturnas directas, se realizaron registros focales en inflorescencias aisladas (n = 4 inflorescencias). El observador se colocó a cuatro metros frente a la inflorescencia, iluminándola con lámparas de luz roja. Los registros se realizaron en un horario de 20:00 a 00:00 h, para un esfuerzo total de muestreo de 16 horas; 4) Observaciones nocturnas indirectas: se realizaron registros en flores individuales de inflorescencias aisladas (n = 9 flores) mediante la técnica de fototrampeo descrita anteriormente, en un horario de 00:00 a 04:00 h durante cuatro días, para un esfuerzo total de muestreo de 16 horas.
Tanto las grabaciones como las fotografías permitieron registrar a todos los visitantes florales, así como evaluar la conducta de forrajeo, los recursos florales obtenidos e identificar si las visitas fueron legítimas (sensuIrwin et al. 2010, Freitas 2018). Todos los visitantes fueron colectados e identificados por un especialista.
Efectividad de polinizadores. Para determinar la efectividad de los polinizadores se realizaron los siguientes tratamientos de polinización controlada: 1) Exclusión de abejas (n = 40 flores de 20 plantas): se emascularon las flores al inicio de la antesis para eliminar el polen (principal recompensa buscada por las abejas). De esta forma las flores no fueron atractivas para este grupo de insectos, siendo solo visitadas por los libadores de néctar (colibríes); 2) Exclusión de colibríes (n = 28 flores de 20 plantas): observaciones previas en el área de estudio mostraron que los colibríes no toleran la presencia humana a corta distancia, por lo que un observador se colocó dos metros frente a las inflorescencias provocando que los colibríes no visitaran las flores. Por su parte, las abejas continuaron recolectando el polen disponible en un lapso aproximado de tres horas. Posteriormente, las flores fueron embolsadas para evitar las visitas de los colibríes; 3) Control (n = 40 flores de 20 plantas): las flores no se manipularon y quedaron expuestas a todos los polinizadores.
Análisis estadísticos. Para evaluar si el tratamiento de polinización influyó en el número de frutos producidos, se construyó una tabla de contingencia entre los tratamientos con la variable binomial de producción de frutos (sí/no). Para analizar si los datos obtenidos en los experimentos de polinización responden a una distribución normal, se aplicó la prueba de Shapiro-Wilk. Para determinar si los tratamientos de polinización controlada influyeron en el número de semillas, en el caso de los tratamientos para evaluar el sistema reproductivo se empleó un análisis de covarianza (eliminando el potencial efecto del tamaño de la planta) y un análisis de varianza para los tratamientos de exclusión. Por otro lado, se realizó una correlación de Pearson para determinar la relación entre el volumen y la concentración de azúcares del néctar con las visitas de los polinizadores. Todos los análisis estadísticos se realizaron con el software jamovi v. 2.5 (JAMOVI 2024).
Resultados
Fenología floral. El desarrollo y crecimiento de las inflorescencias de T. limbata comenzó en la última semana de abril y las últimas en la tercera semana de junio, registrando un periodo de floración de sesenta días, con un pico durante el mes de mayo (Figura 3).
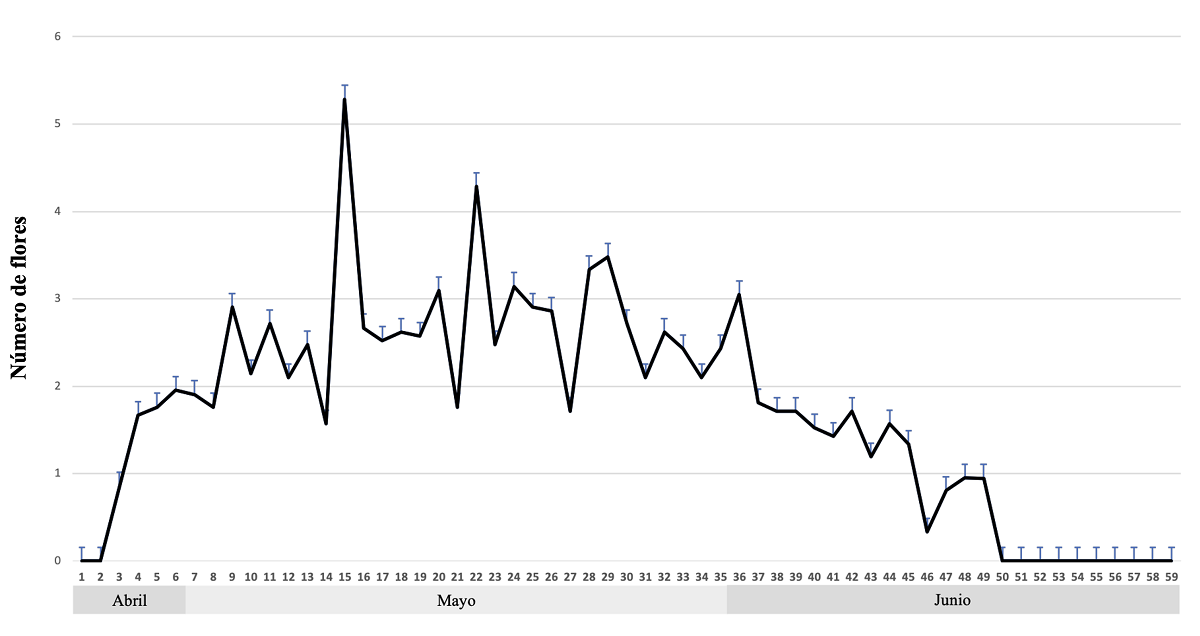
Figura 3 Dinámica de floración de Tillandsia limbata. Cada punto equivale a la media de producción de flores por día durante el ciclo reproductivo de 20 individuos, las barras azules indican la desviación estándar entre las plantas.
El promedio de la floración de un individuo fue de 41.52 días (± 4.16, DE; rango: 35-47 días, n = 20 individuos), durante el cual se produjeron 2.6 flores diarias (± 1.95, rango: 0-14 flores, n = 20 inflorescencias) y un total de 103 flores por inflorescencia (± 41.75). Se registraron un total de 2,278 flores en los 20 individuos observados. Estos, presentaron cuatro morfotipos florales, caracterizados por presentar diferencias notables en la longitud estilar y el tiempo de maduración de las anteras: 11 individuos hercógamos (n = 1,237 flores); seis individuos homógamos (n = 688 flores); dos individuos hercógamos-protóginos (n = 237 flores) y un individuo homógamo-protógino (n = 116 flores) (Figura 4).

Figura 4 Morfotipos florales registrados en individuos de T. limbata: A. Flores hercógamas (se presenta una separación espacial entre los órganos reproductivos, situándose el estigma por encima de las anteras). B. Flores homógamas (las anteras y el estigma se encuentran posicionados al mismo nivel). C. Flores hercógamas con protogina (además de la separación espacial entre los órganos reproductivos, se presenta una separación en el tiempo de maduración; mientras que el estigma se encuentra maduro (receptivo), las anteras no lo están (indehiscentes)). D. Flores homógamas con protoginia (anteras indehiscentes y estigma receptivo posicionados al mismo nivel espacial).
La dirección de apertura de las flores dentro de la inflorescencia fue centrífuga; es decir, las flores comenzaron a abrir en el eje de la inflorescencia y la antesis fue avanzado hacia la periferia, mientras que la floración en las espigas fue acrópeta, ya que el desarrollo de las flores comenzó en la base y se extendió hacia el ápice (Figura 2).
La pre-antesis inicia por la mañana, cerca de las 10:00 h, con el alargamiento del botón floral y continúa hasta el día siguiente cuando ocurre la antesis, la cual comienza con la separación de los pétalos alrededor de las 05:00 h (rango: 03:50-08:00 h, n = 122 flores), momento en que también inicia la receptividad del estigma (n = 21 flores). La corola se cierra por la noche alrededor de las 21:00 h (16 horas después del inicio de la antesis) y la senescencia (marchitamiento) de la flor se presenta 24 horas después de la antesis. El estigma se mantuvo receptivo desde el inicio de la antesis, hasta las 24 horas después; sin embargo, la mayor actividad enzimática y formación de exudado estigmático, se observó entre las cuatro y las 16 horas posteriores a la antesis.
Sistema reproductivo. En los tratamientos de polinización controlada la mayor producción de frutos se registró en el tratamiento de xenogamia, con 100 % de fructificación (χ2 = 161, gl = 5, P < 0.001), mientras que para la autogamia y geitonogamia fue de 12.5 y 10 %, respectivamente. Por su parte, en el tratamiento control se registró 65 % de fructificación, mientras que los tratamientos de autopolinización espontánea y apomixis no desarrollaron frutos (Tabla 1).
Tabla 1 Frutos y semillas desarrollas en los tratamientos de polinización controlada en vivero aplicados a las flores de Tillandsia limbata.
| Tratamiento | Flores (#) | Frutos (#) | Fructificación (%) | Semillas/fruto (media ± D.E.) |
|---|---|---|---|---|
| Xenogamia | 40 | 40 | 100 a | 322 ± 15 a |
| Control | 40 | 26 | 65 b | 198 ± 13 b |
| Autogamia | 40 | 5 | 12.5 c | 22 ± 12 c |
| Geitonogamia | 40 | 4 | 10 c | 6 ± 12 c |
| Autopolinización espontánea | 40 | 0 | 0 | 0 |
| Apomixis | 40 | 0 | 0 | 0 |
Número de semillas promedio por fruto (± Desviación Estándar). Letras distintas en las columnas indican diferencias significativas en cuanto al porcentaje de fructificación (χ2 = 161, gl = 5, P < 0.001) y producción de semillas (F = 95, gl = 5, P < 0.001).
Respecto a la producción de semillas por fruto se registraron diferencias entre tratamientos (F = 95, P < 0.001), siendo la xenogamia el que mayor producción de semillas tuvo con un promedio de 322 (± 15.1, DE), seguido del tratamiento control que registró en promedio 198 (± 13). Los tratamientos de autogamia y geitonogamia mostraron una producción promedio por debajo de 25 (± 12) semillas por fruto, no existiendo diferencias significativas entre ambos (Tabla 1).
El índice de Incompatibilidad Autógama muestra que T. limbata presenta autoincompatibilidad (ISI = 0.06), con una alta capacidad de reproducción sexual cruzada. El índice de Autopolinización Autógama (IAS = 0) indica que la planta cuenta con mecanismos eficaces para evitar la autogamia. El Índice de Limitación de Polen, usando tanto el número de frutos como el número de semillas como variable, mostró un valor positivo (PLI = 0.3 y 0.4, respectivamente), lo que indica que existe limitación de polen en la población.
Análisis de néctar. El volumen de néctar de las flores de T. limbata en promedio por día fue de 20.6 ± 9.5 μl (± DE, rango: 3.6 a 53.2 μl), y la concentración promedio de azúcares disueltos fue de 13.5 ± 9.0 °Brix (rango: 0.0 a 29.0 °Brix). La producción de néctar se mantuvo por 20 horas, a 1.03 μl/h. El volumen (μl) promedio más alto de néctar se presentó por la tarde, a las 13:00 h (3.17 ± 2.63), y la producción descendió acercándose a cero en la madrugada, después de la 01:00 h (0.45 ± 3.90). Al igual que el volumen, la concentración de azúcares disueltos en el néctar fue mayor a las 13:00 h (19.94 ± 2.63 °Brix) y descendió a cero después de la 01:00 h (1.85 ± 4.37 °Brix) (Figura 5). El análisis de correlación de Pearson determinó una relación positiva entre el número de visitas de los colibríes con la concentración de azúcares en el néctar (r 2 = 0.51, P < 0.001) y el volumen de producción de néctar (r 2 = 0.75, P < 0.001) (Figura 6).
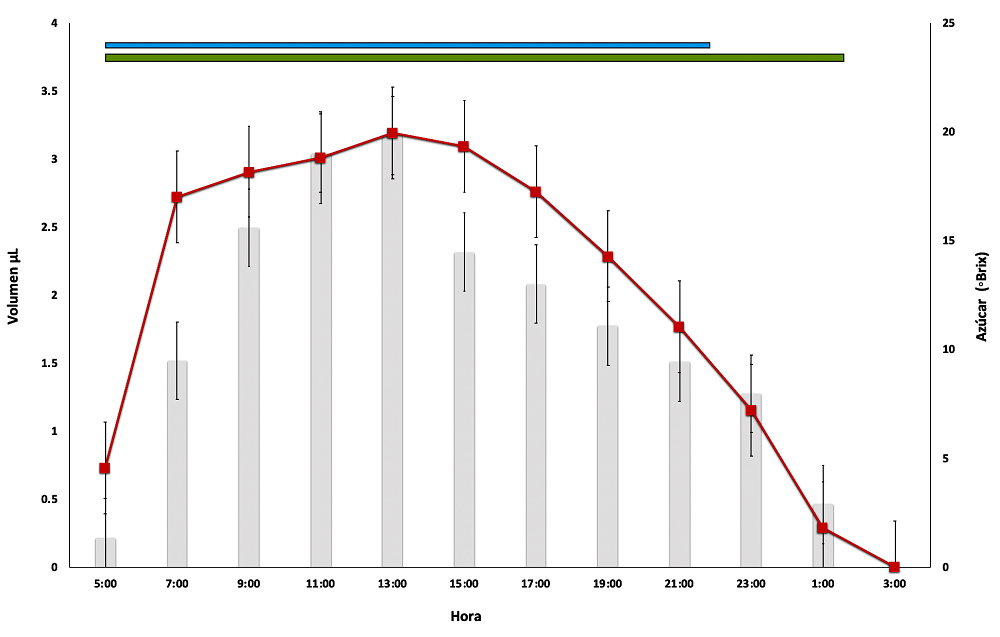
Figura 5 Volumen (en μl, barras grises) y concentración de azúcares (en °Brix, línea roja) del néctar, registrado en las flores de Tillandsia limbata a lo largo del tiempo de vida de las flores. Las líneas negras representan la desviación estándar. La barra verde indica el período en que el estigma se mantiene receptivo. La barra azul muestra el tiempo en que la corola permanece abierta.
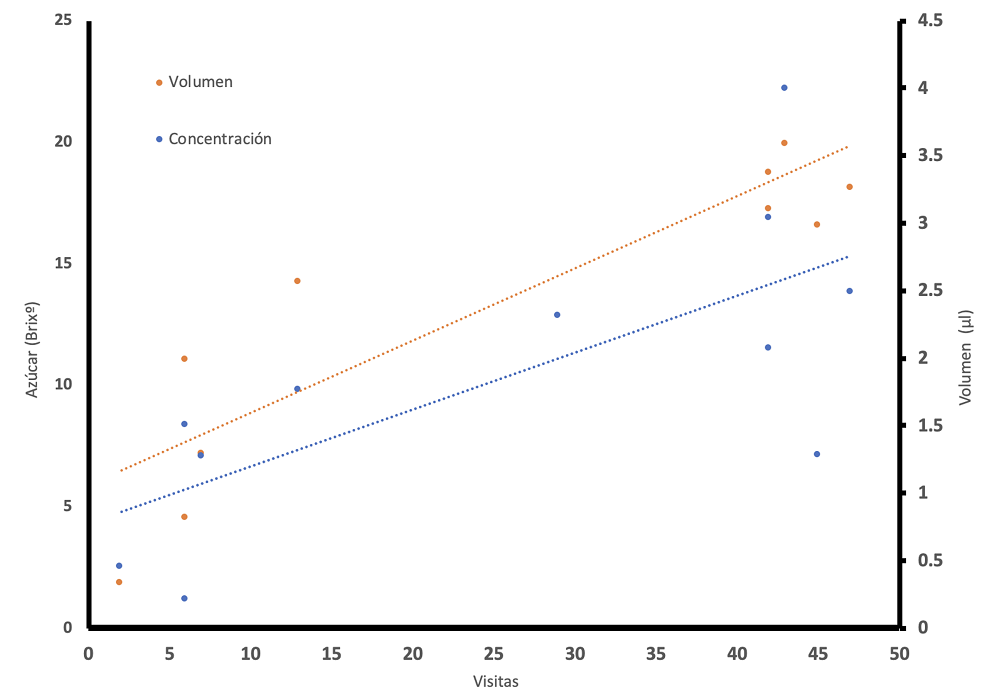
Figura 6 Relación positiva entre la producción y concentración de azúcares del néctar y las visitas de los colibríes. La línea naranja muestra la correlación entre la concentración de azúcares (ºBrix) en el néctar y las visitas de los colibríes (y = 0.0422x + 0.7761, r2 = 0.517). La línea azul muestra la correlación entre la producción de néctar (volumen) y las visitas de los colibríes (y = 0.2972x + 5.922 9, r 2 = 0.7568).
Visitantes florales. Observaciones diurnas: Se registraron ocho visitantes florales diurnos (Apéndice 1). La abeja Trigona fulviventris Guérin-Méneville 1845 (Meliponini, Apidae) presentó el mayor número de visitas a las flores (36 %). Las primeras abejas arribaron a las inflorescencias cerca del amanecer (06:45 h), individualmente o en grupos de hasta ocho, realizando repetidas visitas a una misma flor y manteniéndose en una inflorescencia durante 46.4 ± 15.8 segundos (± DE), tiempo en que visitaron un promedio de 4.7 ± 1.4 flores (Figura 9). Algunos individuos con ayuda de sus partes bucales rompieron el ápice de botones florales en pre-antesis (28 botones presentaron marcas de consumo), logrando de esta manera acceder a sus anteras, las cuáles se encontraban aún indehiscentes, por lo que fueron masticadas para robar su polen. De la misma manera robaron el polen de anteras indehiscentes de flores protóginas (las anteras de 47 flores fueron masticadas) (Figura 7). Por la tarde, entre las 17:00 h y las 18:30 h, momento en que el polen se encontraba agotado en la mayoría de los individuos de T. limbata, se observaron abejas masticando los pétalos de sus flores (22 flores presentaron marcas de consumo), así como también realizando perforaciones en la base de las corolas y en los botones florales (14 corolas y seis botones presentaron perforaciones) (Figura 7).

Figura 7 Comportamiento de forrajeo de la abeja Trigona fulviventris en las flores de Tillandsia limbata. A. Perforación en el ápice de botón en pre-antesis. B. Robo de polen en anteras de flor homógama con protoginia. C. Robo de polen en flor hercógama. D. Perforación en la base de la corola para el robo de néctar. E. Consumo de pétalos. F. Perforación en botón floral.
El segundo visitante más frecuente fue el colibrí Anthracothorax prevostii Lesson 1832, con 33 % de las visitas. Los machos de esta especie en su estadio juvenil, así como las hembras fueron los más frecuentes. Otras especies de colibríes que se registraron fueron Amazilia yucatanensis Cabot 1845, A. tzacatl De la Llave 1833, Chlorestes candida Bourcier & Mulsant 1846, Heliomaster longirostris Audebert & Vieillot 1801 y Phaethornis striigularis Gould 1854, todos ellos con porcentajes menores de visita (Figura 8; Apéndice 1).

Figura 8 Polinizadores de Tillandsia limbata registrados durante las observaciones diurnas. A. Trigona fulviventris. B. Anthracothorax prevostii (macho inmaduro). C. Amazilia yucatanensis. D. Amazilia tzacatl. E. Heliomaster longirostris. F. Phaethornis striigularis.
Todas las especies de colibríes establecieron rutas de forrajeo (traplining) visitando flores e inflorescencias en una misma secuencia y en repetidas ocasiones a lo largo del día. Ninguna especie estableció territorios de alimentación y no se registraron comportamientos agonísticos intraespecíficos o interespecíficos.
Las visitas de los colibríes a las inflorescencias fueron breves, en promedio 27.9 ± 30.8 segundos (± DE), durante este tiempo visitaron un promedio de 6.7 ± 4.4 flores (Figura 9). Cuando en una misma flor coincidían ambos grupos de polinizadores, las abejas atacaron a los colibríes, volando directamente hacia ellos, logrando de esta manera desplazarlos de las inflorescencias (se observaron 29 desplazamientos, todos registrados en las primeras horas de la mañana).
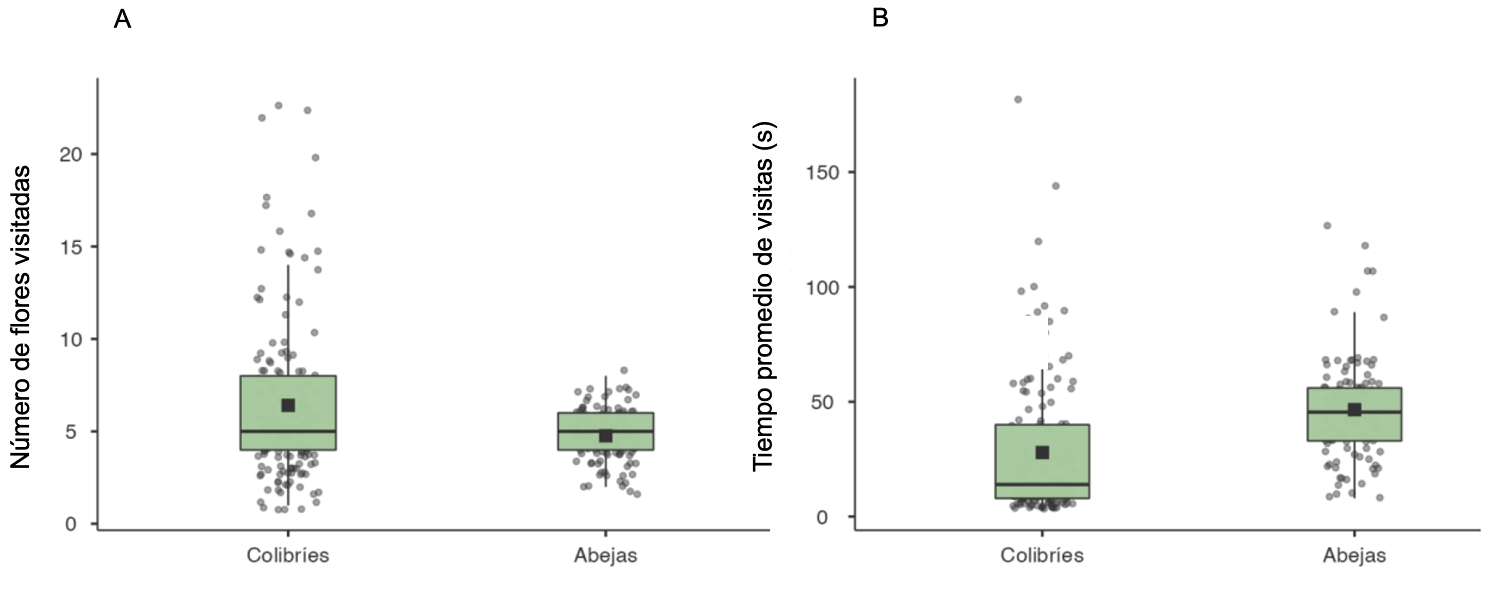
Figura 9 A. Número de flores visitadas por colibríes y abejas, y B. Tiempo promedio de duración de las visitas (en segundos) efectuadas por colibríes y abejas. Los puntos corresponden a cada una de las observaciones, los cuadros negros a la media, y las cajas y alambres al cuartil 1, 2 y 3.
Observaciones nocturnas: Se registró la visita de dos especies de blátidos, Periplaneta americana Linnaeus 1758 y la morfoespecie-1 (Blattidae), las cuales consumieron partes florales, principalmente pétalos y anteras de las flores senescentes. Ambas especies, presentaron el porcentaje más bajo de flores visitadas con apenas 0.19 y 0.13 %, respectivamente (Tabla 2).
Tabla 2 Frutos y semillas desarrolladas en los tratamientos de polinización de Tillandsia limbata efectuados en campo para determinar la efectividad de los polinizadores. Número de semillas promedio por fruto (± Desviación Estándar).
| Tratamiento | Flores (#) | Frutos (#) | Fructificación (%) | Semillas/fruto (media ± DE) |
|---|---|---|---|---|
| Control | 40 | 26 | 65 a | 198 ± 157 a |
| Exclusión de abejas | 40 | 25 | 62.5 a | 177 ± 146 a |
| Exclusión de colibríes | 28 | 3 | 10.7 b | 24 ± 71 b |
Letras distintas en las columnas indican diferencias significativas en cuanto al porcentaje de fructificación (χ2 = 24, gl = 2, P < 0.001) y producción de semillas (F = 28, gl = 2, P < 0.001).
Efectividad de polinizadores. El tratamiento de exclusión de abejas registró un porcentaje de fructificación de 62.5 %, valor cercano al control que tuvo 65 %. En cambio, la exclusión de colibríes registró apenas 10.7 % de producción de frutos (χ2 = 24, gl = 2, P < 0.001). Por otro lado, la producción de semillas promedio por fruto entre los tratamientos de exclusión de abejas y control, fueron similares (177 ± 146 y 198 ± 157 semillas, respectivamente; ± DE), mientras que en el tratamiento de exclusión de colibríes la producción de semillas fue significativamente menor, con apenas 28 (± 24) semillas por fruto (F = 28, gl = 2, P < 0.001) (Tabla 2).
Discusión
Fenología de floración. Según la clasificación de Newstrom et al. (1994), el patrón de floración a nivel poblacional de T. limbata en el sitio de estudio es anual, con un solo periodo de floración en el año. De acuerdo con la clasificación de Gentry (1974), el tipo de fenología de floración a nivel individual fue constante (steady state), con un promedio de 2.6 flores diarias en un periodo de 42 días. Ambos patrones de floración han sido reportados para otras especies epífitas del género Tillandsia, y en general son los más comunes en bromelias que son polinizadas por colibríes (Canela & Sazima 2003, Santana & Machado 2010, Kessler et al. 2020). Una temporada de floración prolongada con individuos produciendo pocas flores por día, como sucede en T. limbata, favorece el flujo de polen entre la población, ya que el polinizador debe visitar una gran cantidad de flores para satisfacer sus necesidades energéticas (Feinsinger & Colwell 1978, Canela & Sazima 2005). Este tipo de floración impulsa a los polinizadores a establecer rutas o circuitos de forrajeo (traplining), lo que implica la visita secuenciada a las mismas bromelias (epífitas) a lo largo de diferentes localidades de alimentación (Ohashi & Thomson 2009). Lo anterior coincide con lo observado en T. limbata, donde todas las especies de colibríes visitaron las flores en secuencias repetibles a lo largo del día. Una floración constante puede alimentar la población de un polinizador específico y especialista durante un periodo de tiempo prolongado (Yumoto 1987). Este parece ser el caso del colibrí A. prevostii que fue la especie más constante, efectiva y la única que estuvo presente durante toda la etapa de floración de T. limbata.
Algunos autores relacionan el pico de floración con el periodo reproductivo de los polinizadores (Newstrom et al. 1994, Bhat & Murali 2001, da Cruz et al. 2006), pudiendo establecerse una interdependencia entre ambos (Yamamura et al. 2007). Esto parece estar ocurriendo con el colibrí A. prevostii, ya que gran parte de su temporada reproductiva (Juárez et al. 2022) coincidió con el pico de floración de T. limbata, lo que podría explicar el mayor número de visitas florales registrado, siendo además individuos hembras y juveniles los más frecuentes y constantes.
En la zona de estudio el clima es cálido-húmedo, con una temporada seca, de menores precipitaciones y mayor temperatura que va de marzo a mayo (Soto & Gama 1997). Esta temporada coincide con el periodo de floración de T. limbata. Se ha reportado que una mayor actividad de floración durante la estación seca es común en bromelias epífitas de hábitats tropicales que son polinizadas por colibríes (Toledo 1975, Ramírez-Morillo et al. 2008, Orozco-Ibarrola et al. 2015, Sheldon & Nadkarni 2015). Lo anterior puede ser una estrategia para disminuir el riesgo de florivoría, ya que en la temporada seca los florívoros (como larvas de lepidópteros o himenópteros) son menos abundantes (Lieberman & Lieberman 1984), los cuales producen daños a los tejidos meristemáticos y órganos reproductivos reduciendo sustancialmente su fecundidad (García-Franco & Rico-Gray 1991, Pierce & Gottsberger 2001, Winkler et al. 2005, Yamamura et al. 2007, Cascante-Marín et al. 2009).
También podría ser un mecanismo para maximizar el servicio de polinización, ya que en la época seca disminuyen los recursos en el ambiente y la oferta de recompensas florales en las bromelias puede atraer a más visitantes (Janzen 1967, Talavera et al. 2001). Por otro lado, durante la temporada de lluvias la actividad de los polinizadores se ve afectada por condiciones ambientales desfavorables como la entrada de huracanes y tormentas tropicales, las cuales además pueden llegar a dañar las inflorescencias (Téllez-Baños, datos sin publicar; Díaz-Infante et al. 2020).
Sistema reproductivo. Tillandsia limbata es una especie autoincompatible, característica poco extendida en las bromelias del género Tillandsia, en donde hasta ahora predominan los sistemas de autocompatibilidad (Ramírez-Morillo et al. 2008, Matallana et al. 2010, Zanella et al. 2012, Orozco-Ibarrola et al. 2015, Ramírez-Rosas et al. 2020, Cascante-Marín & Núñez-Hidalgo 2023). La diferencia entre la fructificación del tratamiento de xenogamia (100 %) y el de autopolinización espontánea (0 %) demuestra que esta bromelia en condiciones naturales requiere de vectores para la transferencia de polen. Esta condición se ha reportado en pocas especies dentro del género, por ejemplo: T. achyrostachys É.Morren, T. caput-medusae É.Morren, T. hubertiana Matuda y T. streptophylla Scheidw (Ramírez-Morillo et al. 2009, Orozco-Ibarrola et al. 2015). El hecho de que el tratamiento de autopolinización espontánea no desarrollara frutos, y la limitada producción de estos en los tratamientos de autogamia y geitonogamia, suponen que las estrategias que presenta la planta como son la hercogamia, la protoginia y su sistema de autoincompatibilidad son muy eficaces para prevenir la autopolinización. Esta combinación de estrategias no se ha reportado en alguna otra especie del género Tillandsia, sin embargo, la hercogamia y la protoginia están presentes en algunas especies autocompatibles (Ramírez-Morillo et al. 2008, Orozco-Ibarrola et al. 2015).
Limitación de polen. La diferencia en el porcentaje de fructificación y producción de frutos entre el tratamiento de xenogamia (100 %) y la polinización natural (65 %), indican limitación de polen en la población; es decir, que en condiciones naturales no llegó la suficiente carga polínica al estigma de las flores de T. limbata o que el polen depositado fue de mala calidad (mezcla de polen proveniente de diferentes especies o de una polinización geitonógama). Atribuimos esta limitación de polen a la interacción antagónica y el comportamiento agonístico mostrado por la abeja T. fulviventris: 1) Robo de polen durante las primeras horas de la mañana, por lo que cuando los colibríes tuvieron su mayor actividad de forrajeo (cerca de las 11:00 h), las anteras contenían poco polen para ser transportado y depositado en los estigmas (Paton 1993, do Carmo et al. 2004, Hargreaves et al. 2009). Se ha demostrado que el consumo de polen puede reducir gravemente la producción de semillas (Bertness & Shumway 1992, Hargreaves et al. 2009); 2) Su conducta agresiva hacia los colibríes, obligó a estos a modificar su comportamiento de búsqueda de alimento, reduciendo su frecuencia de visitas; 3) Su polinización geitonógama, ya que en especies autoincompatibles el polen propio obstruye los estigmas, e interfiere con el crecimiento del tubo polínico xenógamo reduciendo la producción de semillas (Snow et al. 1996); 4) Los daños causados a botones y flores disminuyen la funcionalidad de la flor, su atractivo y además puede causar el aborto de los frutos (McCall 2008).
Lo anterior sugiere que estas abejas presentan una doble interacción con esta bromelia; por un lado, se desempeñan como mutualistas con su polinización secundaria, y por el otro, como antagonistas con su robo de polen, el de néctar y la florivoría. Además, su comportamiento agonístico hacia los polinizadores primarios, los colibríes, afecta negativamente el éxito reproductivo de esta planta. Hasta donde sabemos, esta dualidad en la interacción de un visitante floral no se ha reportado en otra especie del género Tillandsia. En bromelias ornitófilas distribuidas en la Mata Atlántica de Brasil se ha observado el robo de polen y la florivoría por parte de abejas del género Trigona (Canela & Sazima 2005). Por ejemplo, en la especie terrestre Bromelia antiacantha Bertol., estas abejas roban polen y también el néctar, lo que afecta las visitas de los colibríes y de otras especies de abejas por la reducción de recursos (Canela & Sazima 2005); sin embargo, no se comprobó un efecto negativo en el éxito reproductivo.
Síndrome de polinización. Gardner (1986) sugirió para T. limbata una polinización por polillas nocturnas, sin embargo, a pesar de que la antesis se extiende hasta el anochecer, los siguientes factores limitan la polinización nocturna: 1) La corola cierra alrededor de las 21:00 h, impidiendo el acceso a la recompensa; 2) El volumen de néctar y la concentración de azúcares decrece significativamente al anochecer; 3) No hay polen disponible en las anteras ya que este se libera por las mañanas. Aunque en el área de estudio existen polillas nectarívoras que podrían visitar esta bromelia (Raguso & Llorente-Bousquets 1991), tendrían poco o nulo efecto en la producción de semillas por la limitación de polen en las flores. No obstante, durante múltiples horas de observación nocturna no se registró la visita de ningún lepidóptero.
Los resultados indican que T. limbata es polinizada por visitantes diurnos, particularmente colibríes y abejas. La cercanía de la zona de estudio con el fragmento de selva conservada de la Estación de Biología Tropical Los Tuxtlas de la Universidad Nacional Autónoma de México (ca. 3 km), podría estar favoreciendo la alta diversidad de colibríes que visitan las flores de T. limbata. En otras especies de Tillandsia se han reportado de una a tres especies de colibríes como polinizadores (Toledo 1975, García-Franco & Rico-Gray 1991, Aguilar-Rodríguez et al. 2016), y excepcionalmente siete especies de colibríes en diversos sitios de Brasil (Kessler et al. 2020).
Polinizadores efectivos. Los colibríes registraron el mayor número de visitas legítimas a las flores, ya que propiciaron una alta producción de frutos y semillas. Lo anterior demuestra que son los principales polinizadores de esta bromelia. En otras especies del género Tillandsia se ha registrado que este grupo de aves también parecen ser sus principales polinizadores (Gardner 1986, Sáyago et al. 2018, Missagia et al. 2023).
Los colibríes establecieron circuitos de alimentación (traplining) como estrategia de forrajeo, lo que estaría favoreciendo la polinización cruzada, el transporte de polen a largas distancias y el intercambio genético entre los individuos de la población de T. limbata. El hecho de que no establecieran territorios de alimentación puede deberse a que la oferta floral y el volumen de néctar proporcionado por las flores de esta bromelia son bajos, y no superaron los costos energéticos que implicaría la defensa de un territorio de alimentación (Feinsinger & Chapling 1975). Posiblemente por eso no se registraron comportamientos agonísticos intraespecíficos e interespecíficos entre las aves. Sin embargo, en otros estudios sobre bromelias epífitas donde la oferta floral y de néctar fue abundante se registró que ocurrieron interacciones antagónicas (Faria & Araújo 2010, Piacentini & Varassin 2007, Santana & Machado 2010, Silva et al. 2022).
Las abejas Trigona presentaron baja eficiencia como polinizadoras, con una mínima producción de frutos y semillas, actuando principalmente como ladrones de polen. En los individuos con flores hercógamas (donde se presenta una separación espacial entre los órganos reproductivos, situándose el estigma por encima de las anteras), no llegaron a depositar polen en los estigmas. Por el contrario, en individuos con flores homógamas (donde las anteras y el estigma estaban posicionados al mismo nivel), las abejas sí depositaron polen en los estigmas, aunque la mayoría de este provenía de la misma flor que estaba siendo polinizada (Material suplementario 3). En el caso de las flores con protoginia, donde las anteras se encontraban cerradas (inmaduras), éstas fueron mordidas por las abejas para recolectar su polen y aunque en ocasiones fue depositado en los estigmas, no representó ninguna contribución a la reproducción, debido a la autoincompatibilidad de la planta y a la inviabilidad del polen a causa de su inmadurez. Aunque la eficiencia polinizadora de las abejas Trigona fue baja, éstas podrían asegurar la reproducción de esta bromelia en caso de una disminución o ausencia de los polinizadores primarios. Se ha reportado que algunos polinizadores secundarios, actúan como ladrones de polen cuando otros visitantes proporcionan un servicio de polinización más eficiente, pero pueden servir como polinizadores primarios cuando son los únicos visitantes de una planta (Thomson & Thomson 1992).
Néctar. El volumen y la concentración de azúcares disueltos en el néctar de T. limbata se encuentran entre los más bajos reportados para bromelias polinizadas por colibríes (Bernardello et al. 1991, Stiles & Freeman 1993, Krömer et al. 2008, Orozco-Ibarrola et al. 2015). Sin embargo, se ha demostrado en plantas epífitas que las visitas de los colibríes se pueden mantener con bajas cantidades de néctar por flor si hay suficientes plantas disponibles en el área (Ackerman et al. 1994). Además, una menor concentración de azúcar significa un néctar más diluido, lo que favorece su absorción (Sick 1997), y en consecuencia estas aves gastan menos energía en vuelo suspendido mientras se alimentan (Feinsinger & Colwell 1978).
El patrón temporal de mayor producción y concentración del néctar durante la mañana, es común en flores que son polinizadas por colibríes, ya que es cuando estos tienen mayor actividad de forrajeo (Baker 1975, Freeman et al. 1984, Bernardello et al. 1991, Stiles & Freeman 1993, Krömer et al. 2008). Sin embargo, T. limbata recibió más visitas de las abejas en las mañanas (ca. 07:00-10:00 h), mientras que, por la tarde, los colibríes realizaron mayor número de visitas (ca. 11:00 - 13:00 h).
Los resultados demuestran que T. limbata es una especie autoincompatible con una alta capacidad de reproducción por xenogamia, su sistema de polinización está especializado hacia los colibríes, siendo estos sus polinizadores efectivos. Por otro lado, la abeja T. fulviventris resultó ser un polinizador secundario bastante ineficiente debido a que por su comportamiento de forrajeo efectúa mayormente una polinización geitonógama. Además, su conducta de florivoría, el robo de polen y néctar, junto con su conducta agresiva hacia otros polinizadores, limitó la transferencia de polen entre individuos de esta bromelia, afectando negativamente su éxito reproductivo.
Material suplementario
El material suplementario de este trabajo puede ser consultado aquí: https://doi.org/10.17129/botsci.3582.
















