Introducción
La disfunción sexual se define como la ausencia o alteración de una o varias fases de la respuesta sexual (deseo, excitación, orgasmo y resolución).1 Este trastorno impacta negativamente el equilibrio biopsicoemocional de los pacientes que la padecen y por tanto generando estrés, ansiedad o angustia. No cabe duda del impacto negativo que trasciende los estereotipos sociales, de hecho, esta condición está enmarcada de manera errónea en la falsa sensación de perdida de masculinidad.2
Dentro de las disfunciones sexuales masculinas, la disfunción eréctil y la eyaculación precoz son las más prevalentes,3 siendo de interés para esta revisión la primera. Esta patología en particular afecta aproximadamente a 100 millones de hombres en todo el mundo,4 y debido a la relación con múltiples comorbilidades, se espera que para el año 2025, al menos 332 millones de hombres tendrán algún tipo de disfunción eréctil.5 Las investigaciones en este campo han identificado varios mecanismos moleculares implicados en el desarrollo de esta enfermedad, incluidos el óxido nítrico, guanosina monofosfato cíclica (cGMP)/proteína quinasa G (PKG), especies reactivas de oxígeno, el sistema renina angiotensina y ciertas citoquinas proinflamatorias como el TNF-a.6 Además, se han descrito factores que juegan un papel determinante en el desarrollo de disfunción eréctil, sin embargo, los más comunes son los de tipo orgánico, psicológico, estructurales e infecciosos. Dentro de los factores infecciosos relacionados con el desarrollo e instauración de disfunción eréctil se encuentran las secuelas vasculares inducidas por infecciones virales producidas por el virus del dengue, virus de la inmunodeficiencia humana (VIH), SARS-CoV-2, virus linfotrópico humano de células tipo 1 (HTVL1), hepatitis y herpes, los cuales afectan significativamente a la personas en la actualidad. De ahí que el objetivo de esta revisión es describir la asociación entre disfunción eréctil e infecciones virales y sus posibles mecanismos fisiopatológicos.
Erección y disfunción eréctil
La respuesta eréctil en los hombres supone una serie de fases que incluyen; latente, tumescente, erección completa, erección rígida y detumescencia, en estas participan varios factores de tipo nerviosos, vasculares y psicógenos, cuya finalidad es aumentar el flujo de sangre hacia el cuerpo cavernosos. Una vez se consigue aumentar el riego sanguíneo hacia el cuerpo cavernoso, los espacios sinusoidales se expanden, dando como resultado la erección.6 La erección o flacidez del pene está determinada por mecanismos que favorecen ya sea a la contracción o relajación de la musculatura lisa, la cual es regulada por una combinación de control adrenérgico (noradrenalina), control miogénico intrínseco y factores de contracción derivados del endotelio como lo son las prostaglandinas y endotelinas.6
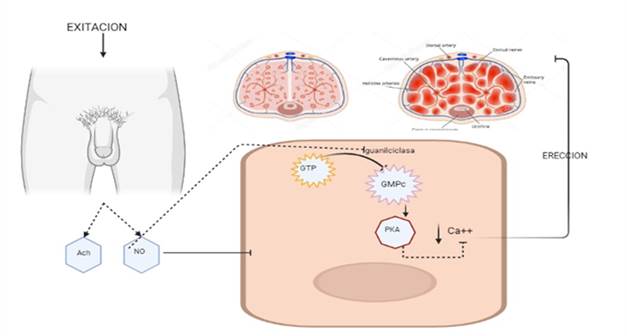
Tras la excitación sexual, se estimula la liberación de acetilcolina de las fibras nerviosas colinérgicas parasimpáticas, así como óxido nítrico (NO) de las fibras nerviosas no colinérgicas, este último, es un potente vasodilatador local en las células endoteliales del pene. Una vez en el pene, el NO aumenta la producción endógena de monofosfato de guanosina cíclico a partir de trifosfato de guanosina por la activación de la guanilciclasa presente en las células del musculo liso del cuerpo cavernoso. El monofosfato de guanosina cíclico activa a la proteína quinasa dependiente de monofosfato de guanosina y conlleva a una disminución de los niveles de calcio intracelular y a la relajación del musculo liso vascular.6,7 Todo lo anterior garantiza la erección del miembro masculino,7 como se muestra en la Figura 1.
No obstante, este proceso se ve afectado por: a) desregulación del NO)/guanosina monofosfato cíclica (cGMP)/proteína quinasa G (PKG) (los niveles intracelulares de cGMP juegan un papel importante en la erección masculina, se ha demostrado que su disminución favorece la disfunción en la erección, debido posiblemente a la conversión de cGMP en 5-guanosina monofosfato por la fosfodiesterasa tipo 5, la cual aumenta en condiciones que privan o disminuyen la producción endógena de óxido nítrico); b) Inhibición de las 5-fosfodiesterasas (PDE-5), enzimas que inactivan la adenosina monofosfato cíclico (AMPc) y el GMPc, los cuales actúan como segundos mensajeros para la producción de NO; c) el estímulo persistente y crónico de la fosfodiesterasa tipo 5 que disminuye los niveles de GMPc en el cuerpo cavernoso, conllevando a niveles persistentes de calcio intracelular, menos relajación de la musculatura lisa del cuerpo cavernoso y finalmente menor flujo sanguíneo en el tejido eréctil; y d) daño endotelial, y la capacidad de relajación y contráctil del cuerpo cavernosos, como ocurre en enfermedades como la hipertensión, la diabetes, la obesidad.8,9,10 Todo lo anterior conduce a fenómeno opuesto conocido como disfunción eréctil.
Anteriormente, se creía que la disfunción eréctil se debía a un problema psicógeno, pero actualmente la evidencia ha mostrado que más del 80% de los casos se debe a un problema orgánico.8 Tanto así que en la actualidad las causas de disfunción eréctil se pueden clasificar como disfunción eréctil de causas endocrinas y no endocrinas.11 Dentro de las causas no endocrinas se encuentran las secuelas vasculares inducidas por infecciones del virus de la inmunodeficiencia humana (VIH), virus linfotrópico humano de células T tipo 1 (VHTL1), herpes simple, herpes zóster (HVS,HVZ), virus de la hepatitis B y C , virus SARS-CoV2, Tabla 1.
Tabla 1 Causas de disfunción eréctil
| Endocrinas | No endocrinas |
|---|---|
| *Hipogonadismo | * Vasculogénica (+ común): dislipidemias, hipertensión, ateroesclerosis, fumar. |
| *Diabetes mellitus | *Neurogénicas: lesión médula espinal, esclerosis múltiple, lesiones sacras S2-S4. |
| * Obesidad | *Iatrogénicas: cirugía pélvica radical, fractura pélvica, lesión nervio cavernosos, lesión arteria pudenda accesoria. |
| *Síndrome metabólico | *Infecciones; virales: SARS-CoV2, VIH, hepatitis, HTLV1, herpes simple, zóster. |
| *Hipo - hipertiroidismo. | *Fármacos: drogas recreativas, tiazídicos, bloqueadores B, espironolactona, antidepresivos tricíclicos, benzodiacepinas, fenitoína, opiáceos. |
| *Traumatismos: de pelvis, de médula espinal. |
Tomado de: Yafi FA, Jenkins L, Albersen M, et al. Disfuncion erectil. Imprimadores Nat Rev Dis . 2016;2:16003. Publicado el 4 de febrero de 2016. doi:10.1038/nrdp.2016.3.8
Disfunción eréctil e infecciones virales
A continuación, se describe el efecto documentado de las secuelas vasculares inducidas por infecciones virales en la disfunción eréctil.
Infección por SARS-CoV-2
La infección por SARS-CoV-2 y disfunción eréctil se relacionan por los mismos mecanismos fisiopatológicos que conectan a la infección por SARS-CoV2 y el daño endotelial sistémico, así cuando una persona se expone al virus y este ingresa al cuerpo, la proteína S se ancla a la enzima convertidora de angiotensina 2 (ECA2), la cual convierte la angiotensina I en angiotensina II mediante una serie de procesos activados por el sistema renina-angiotensina-aldosterona (RAAS). La ECA2 se encuentra en células epiteliales respiratorias, células alveolares, cavidad oral, riñón, testículo, hígado, intestino, cerebro y en el endotelio vascular, de ahí que sea un blanco para el SARS-CoV-2.12,13 La unión del virus con la ECA2 es facilitada por la proteasa transmembrana serina 2 (TMPRSS2), esta permite el acoplamiento y el paso del virus al endotelio capilar.14
Una vez en el endotelio vascular se activan citoquinas inflamatorias como TNF-α, IL-6 e IL-1β, las cuales producen un proceso de hiperinflamacion sistémica, y favorecen la inmunogénesis de la disfunción eréctil. A su vez, se ha demostrado que el estrés oxidativo inducido por la respuesta hiperinflamatoria puede conllevar a suprimir el eje hipotalámico-pituitario-testicular (HPT), y por ende a una disminución de la hormona luteinizante (LH), hormona estimulante del folículo (FSH) y niveles de testosterona.14,15,16
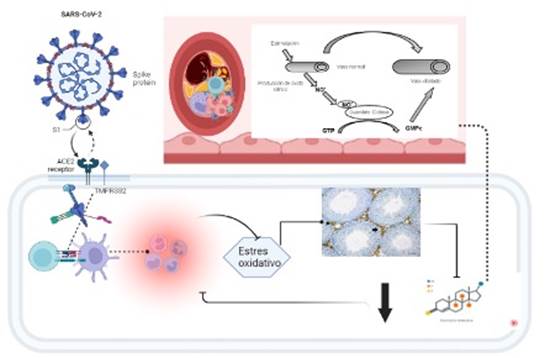
En pacientes infectados por este virus, el estado hiperinflamatorio y el daño endotelial, producen cambios tromboembólicos en la luz vascular, asociados con formación de imnunotrombosis; eventos que a nivel de la vasculatura de los cuerpos cavernosos pueden alterar el flujo de sangre, y conducir a obstrucción e impedir el riego sanguíneo.14 Por otra parte, los estudios histopatológicos en pacientes que padecieron COVID-19 muestran una expresión endotelial disminuida de la enzima óxido nítrico sintasa en los cuerpos cavernosos, que se ve favorecida por los bajos niveles de testosterona lo cual podría favorecer a una mayor disfunción endotelial y atenuación de la vasodilatación del tejido cavernoso ligado al endotelio y atrofia de las células del músculo liso vascular.14,15,17 Los mecanismos mediante el cual la infección por SARS-CoV2 produce disfunción eréctil se muestran en la Figura 2.
La evidencia muestra que la infección por COVID-19 afecta la respuesta eréctil, al punto de producir disfunción, inclusive el número de pacientes diagnosticados con esta patología durante la pandemia por COVID-19 se incrementó. Adicionalmente, se ha evidenciado que la infección induce en pacientes disfunción endotelial, hipogonadismo subclínico y deterioro de la hemodinámica pulmonar; factores de riesgos atribuibles al desarrollo y aparición de disfunción eréctil.17
Por otro lado, se ha encontrado que pacientes con COVID-19 tienen niveles más bajos de testosterona y menor aporte de oxido en las células endoteliales, lo que se traduce en un decaimiento de la respuesta eréctil.18
Un paso obligado para que se dé la infección por SARS-CoV2 es la unión al receptor ECA2 mediado por la proteasa transmembrana serina 2, que escinde el receptor y facilita la entrada del virus, como se mencionó anteriormente.19 Por tanto, la expresión de ECA2 juega un papel importante en la infectividad del virus. La expresión de ECA2 en el tejido del pene se relaciona con la edad, a tal punto que se han informado expresiones más altas en pacientes entre 20-30 años y menor expresión en mayores de 60 años. Supone esto que los pacientes jóvenes tienen mayor riesgo de sufrir daño testicular posterior a la infección por SARS-CoV2.20
La afectación testicular induce hipogonadismo de inicio tardío o temprano, con la consecuente disminución de hormonas fundamentales en la erección como la testosterona. Se ha observado que el estado hiperinflamatorio de la infección por SARS-COV2 se caracteriza por citoquinas que también están asociadas con el empeoramiento de la disfunción sexual masculina, incluidos TNF-α, IL-6 e IL-1β; respuesta hiperinflamatoria que puede empeorarse debido a los bajos niveles de testosterona encontrada en los pacientes con SARS-CoV2, lo cual aumenta el daño endotelial y genera una menor respuesta eréctil.20,21 La afectación testicular y su consecuente alteración en la testosterona ha sido reportada en varios estudios, como se muestra a en la Tabla 2.
Tabla 2 Reportes de la implicación de infección por SARS-CoV-2 y testículos
| Autores | Conclusión |
|---|---|
| Ferran García et al.15 | Uno de los fenómenos más notables es la infiltración leucocitaria, que podría disminuir la producción de testosterona por alteración en las células de Leydig; con su consecuente daño a la barrera hematotesticular, de lo cual, las citoquinas inflamatorias, podrían activar la respuesta autoinmune y producir el desarrollo de autoanticuerpos. |
| Kharbach et al.21 | Se ha sugerido un posible tropismo del SARS-CoV-2 en los tejidos testiculares. Un estudio realizado en 81 pacientes en edad reproductiva con infección por SARS-CoV-2 y 100 hombres sanos mostro niveles bajos de testosterona, hormona luteinizante y niveles de hormonas estimulantes del folículo en 81 pacientes con infección por SARS-CoV-2, lo cual sugiere un potencial hipogonadismo. |
| Yang et al.22 | Se realizó examen post mortem en 12 pacientes con COVID-19, utilizando la técnica (RT-PCR) para detectar el virus a nivel testicular. Los testículos de pacientes con COVID-19 mostraron una lesión tubular seminífero significativa, células de Leydig reducidas e inflamación linfocítica leve. Las células de Sertoli se vieron afectadas predominantemente y mostraron hinchazón, vacuolación y rarefacción citoplasma, y desprendimiento de las membranas basales tubulares. |
| La Marca et al.23 | Varios estudios han descrito la relación entre los miembros de la familia SARS-CoV y la orquitis, inclusive sin que se detecte el SARS-CoV en el tejido testicular. La unión del virus al receptor ECA2 puede producir inflamación del tejido. En relación al SARS-CoV-2 se cree que induce una vasculitis sistémica, lo cual puede ser otra posible causa del daño testicular. |
| Abobaker et al.24 | Existe una posibilidad de que la infección por SARS-CoV-2 pueda cuásar daño testicular. Este daño puede ser causado por la invasión viral directa a través de la unión del virus SARS-COV2 a los receptores ACE2 o secundaria a una respuesta inmunológica e inflamatoria. |
| Younis et al.25 | La evidencia muestra que los pacientes con COVID-19 grave podrían tener un síndrome de tormentas de citoquinas, este síndrome hiperinflamatorio, el cual se acompaña de fiebre sostenida, hipercitocinemia lo cual puede impactar negativamente la salud reproductiva masculina. |
| Rastrelli et al.26 | Al analizar a 31 pacientes positivos para SARS-CoV-2, los investigadores encontraron que algunos pacientes desarrollaban hipogonadismo. En este mismo estudio, los niveles de testosterona total o libre, actuaron como predictores de mal pronóstico, al aumentar morbilidad y un mayor riesgo de requerimiento de unidad de cuidados intensivos. |
Herpes y disfunción eréctil
La infección por el virus del herpes simple (HSV), constituye una infección de trasmisión sexual, con una prevalencia estimada de 53.9% para HSV tipo I y 15.7% para HSV tipo II.27) Generalmente producen infección oral y anogenital, pero, además, aunque en menor medida pueden presentarse casos de mieloradiculitis sacra, en la cual por el neurotropismo que tiene el HSV por los ganglios de la raíz dorsal sacra, conlleva desmielinización axonal, conduciendo a una disminución en el estímulo nervioso al tejido del pene y por tanto a disfunción eréctil.28
Por su parte la varicela zóster es una enfermedad neuropática dermatomal, cuya afectación sobre el dermatoma sacro es un fenómeno raro, que suele causar retención urinaria, disfunción de la vejiga, y rara vez disfunción eréctil, cuyo curso se presenta de forma transitoria.29
Se ha llegado a considerar que la inflamación causada por patógenos ya sea virales o bacterianos desempeña un papel importante en el proceso de ateroesclerosis por acumulación de lípidos, que en el caso de infecciones por HSV puede provocar oclusión de las arterias cavernosas por acumulación de placas ateroescleróticas.30 Por otra parte, las infecciones por HSV pueden afectar la relajación del musculo liso ya sea por mecanismos dependientes o no del endotelio; y se ha observado que los leucotrienos, bradicinina, especies reactivas de oxígeno y el TNF-α, pueden afectar la función vascular y participar en la aparición de disfunción eréctil en pacientes con infección por HSV.30 Otros estudios han asociado a la variante herpes zóster con disfunción eréctil por un mecanismos distinto al del HSV.31,32
Hepatitis
La prevalencia de disfunción eréctil en pacientes con enfermedad hepática crónica oscila entre el 14% y 78%.33 La inflamación, el estrés oxidativo y la elevación de reactantes de fase aguda como la proteína C reactiva se relacionan con el desarrollo de disfunción eréctil mediante el daño endotelial que esta infección produce, la cual genera una disminución de óxido nítrico en las células endoteliales, dificultando la capacidad vasodilatadora y eréctil.33 Se ha reportado una prevalencia de disfunción eréctil de 8.6 % y el 41.2 % para aquellos con virus de la hepatitis C y virus de la hepatitis B, respectivamente. En pacientes cirróticos y alcohólicos, la disfunción eréctil se puede atribuir al efecto toxico del etanol en las gónadas, suponiendo un mayor riesgo de desarrollar disfunción eréctil.34,35
Linfotrópico humano de células tipo 1 (HTLV-1)
Es poco el conocimiento que se tiene en relación con el compromiso de la función sexual en pacientes infectados por el virus linfotrópico humano de células tipo 1 (HTLV-1), no obstante, la disfunción eréctil ocurre en más del 50% de los pacientes con esta infección, que se ve agravada o potenciado por el grado de afectación neurológica que pueda llegar a presentar el paciente.36
El mecanismo fisiopatológico por el cual el virus HTLV-1 produce disfunción eréctil no es muy claro pero se cree que guarda relación con los mecanismos propuestos en otras entidades como lo es la esclerosis múltiple. En condiciones normales la inervación del pene proviene del sistema autónomo FS (T11 - L2) y FP (S2-S4) así como también inervación somática, que se encarga de llevar la inervación a los músculos isquiocavernosos y bulbocavernosos. En aquellos pacientes con infección por el virus HTLV-1, se ha atribuido como causa de disfunción eréctil, al compromiso degenerativo de los nervios espinales S2-S4.37
Mielitis transversa posdengue
El dengue es producido por cuatro serotipos de los cuales, el 2 y 3 se destacan por causar complicaciones a nivel neurológico. Aunque estos deterioros son muy raros, pueden causar daño a nivel de la columna vertebral por invasión directa del virus, desencadenando así una serie de inmunorreaciones que conlleva a la aparición mielitis transversa (afectación del segmento T1-T10 de la médula espinal torácica).38 La principal manifestación de esta enfermedad es el deterioro de los miembros inferiores seguido de síntomas como la disfunción eréctil y miccional.38
Virus de la inmunodeficiencia humana (VIH)
En pacientes infectados por el VIH, la prevalencia de disfunción eréctil oscila ampliamente entre el 7% y el 74%.39 Existen cuatro factores relacionados con la aparición de esta patología: a) trastornos mentales, b) farmacológicos, c) trastornos hormonales y d) otros trastornos mórbidos.40 Se ha descrito en la literatura la posible producción de hipogonadismo como uno de los trastornos endocrinos más frecuentes en pacientes positivos para VIH, inclusive se considera como la causa de disfunción eréctil más frecuente antes del tratamiento antirretroviral.41 Además de esto, se ha encontrado hiperprolactinemia en algunos pacientes VIH positivos, que es un agente causal de la disminución de la liberación de gonadotropinas.41 Por otra parte, antirretrovirales como el indinavir y la nevirapina se han asociado con el deterioro de la erección en estos pacientes.41,42,43
Virus del papiloma humano (VPH)
A esta familia pertenecen pequeños virus de doble cadena de ADN que infectan el epitelio cutáneo y las mucosas. La evidencia a la fecha sugiere que los pacientes del sexo masculino con presencia de verrugas genitales tienen una tasa más alta de disfunción eréctil.44 La aparición de esta patología puede presentarse por varios mecanismos, incluidos la inflamación sostenida que puede progresar a ateroesclerosis la cual tiene un papel importante en su patogenia,45 y el desarrollo de vasculitis granulomatosos necrosante que puede alterar la arquitectura vascular.46,47,48
Conclusión
La disfunción eréctil constituye un problema de salud multifactorial que afecta e interfiere en la calidad de vida de las personas que la padece. Anteriormente se pensaba que su aparición era el resultado de un desorden orgánico, hoy en día se sabe pueden existir otras causas involucradas como las secuelas vasculares inducidas por las infecciones virales, hecho que se evidenció en la pandemia por la COVID-19, donde los pacientes afectados posterior a la infección desarrollaban disfunción eréctil como una complicación de esta enfermedad. Otras infecciones virales como las producidas por el virus de la hepatitis B y C, herpes simple y zóster, virus linfotrópico humano, VIH e infección por dengue tambien se han relacionado con el desarrollo de esta patología, cada una por mecanismos directos o indirectos al tejido endotelial de los cuerpos cavernosos o por afectación nerviosa.