Introducción
La neuropatía diabética es la complicación neurológica más común en pacientes con diabetes, se calcula que 16% de los diabéticos presentan esta patología. De todas las neuropatías en el paciente diabético, 75% corresponden a la categoría de distal symmetric polyneuropathy o DSPN (Tabla 1).1-3 Los axones de neuronas sensitivas de la raíz dorsal reciben señales de la piel y articulaciones; son 20,000 veces más largos que sus cuerpos celulares y la mayoría de estos axones no están mielinizados, por lo que son más susceptibles a sufrir daños en comparación con los axones motores que envían señales a los músculos.4 Esta patología se diagnostica por método de exclusión, ya que existen diversas causas de neuropatía no diabética que se pueden generar en pacientes diabéticos.5
Tabla 1: Clasificación de los diferentes tipos de neuropatía en el paciente diabético.
| Neuropatía difusa | DSPN | Neuropatía principalmente de fibras pequeñas | |
| Neuropatía principalmente de fibras grandes | |||
| Mixta (más común) | |||
| Autonómica | Cardiovascular | Taquicardia en reposo, hipotensión ortostática, muerte súbita | |
| Gastrointestinal | Gastroparesia diabética, enteropatía diabética, hipomotilidad colónica | ||
| Urogenital | Cistopatía diabética, disfunción eréctil, disfunción sexual femenina | ||
| Disfunción sudomotora | Hipohidrosis distal/anhidrosis, sudoración gustativa | ||
| Inconsciencia de hipoglucemia | |||
| Función anormal de la pupila | |||
| Mononeuropatía | Nervio craneal o periférico aislado | ||
| Mononeuritis múltiple | |||
| Radiculopatías | Neuropatía radiculoplexa | ||
| Radiculopatía torácica | |||
DSPN = distal symmetric polyneuropathy. Adaptada de: Pop-Busui R et al.5
Es necesario establecer los términos polineuropatía y neuropatía periférica. La polineuropatía es un proceso homogéneo que abarca la afección de diversos nervios periféricos, principalmente los nervios distales. Por otra parte, la neuropatía periférica puede referirse a cualquier trastorno del sistema nervioso periférico, incluidas radiculopatías y mononeuropatías.6
Clasificación
Es de reciente conocimiento que la DSPN, en especial el subtipo de neuropatía dolorosa de fibras pequeñas, se presenta en 10-30% de los pacientes con intolerancia a la glucosa, también conocido como prediabetes, o con síndrome metabólico.5 De los factores de riesgo más importantes para la generación de neuropatía diabética, se contempla la duración y severidad de la hiperglucemia, así como ciertas comorbilidades, por ejemplo, síndrome metabólico.4
Hay un involucro de los sistemas nerviosos autonómico y periférico, que conlleva una pérdida gradual de la integridad de las fibras nerviosas, que generan síntomas que inician de manera distal y simétrica en extremidades inferiores. Como hay pérdida de la sensibilidad, aumenta el riesgo de formación de úlceras y amputaciones.1,4 Para pacientes con neuropatía y/o angiopatía diabética, el aumento de la presión plantar y factores sistémicos como alteración de la cicatrización celular de heridas conlleva lesiones en el pie de forma crónica, lo cual puede generar una mayor complicación, como pie diabético.7
Dentro de la clínica, uno de los principales síntomas es el dolor, que es referido como quemante o apuñalante, éste se puede llegar a resolver o puede empeorar hasta llevar al paciente a tener dificultad para caminar.1 Los pacientes diabéticos son más propensos a padecer problemas del sueño y desorden del estado de ánimo, lo que puede influenciar en la percepción del dolor.2
Fisiopatología
Dentro de la clasificación, la afección a las fibras pequeñas es más común por su vulnerabilidad desde estadios tempranos de la enfermedad. A pesar de que la fisiopatología completa aún es desconocida, se han establecido diferentes modelos para explicar sus mecanismos de manera más completa y encontrar nuevas estrategias terapéuticas.8
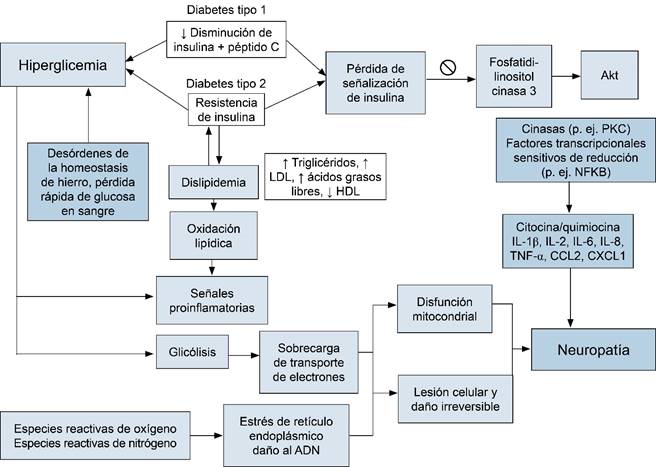
Es importante mencionar ciertos procesos metabólicos que se ven alterados y propician el desarrollo de la neuropatía, como la acumulación de metabolitos tóxicos en los estados hiperglucémico, en el cual la glucosa se acumula en células nerviosas, lo que genera la formación de sorbitol, el cual se asocia a daño celular.9 Otro mecanismo estudiado dentro de la fisiopatología es la presencia de polimorfismos en el gen AKR1B1, que producen un aumento de riesgo para la neuropatía diabética. La vía metabólica más estudiada es la del sorbitol, ya que se ha observado que este aminoácido se encuentra elevado en diabéticos, lo que ocasiona la acumulación de desoxiesfingolípidos, los cuales generan disminución del crecimiento axonal (Figura 1).9
Inflamación
Se ha demostrado en diferentes estudios que hay una respuesta inflamatoria aumentada con infiltración leve y proliferación de macrófagos y células T, así como concentraciones elevadas de citoquinas solubles en el nervio ciático, siendo la afectación principalmente en las fibras nerviosas intraepidérmicas pequeñas. Todo este proceso se ve igualmente asociado con la pérdida de la mielinización de las fibras y daño axonal. En un estudio clínico prospectivo realizado por Herder y colaborador, se encontró una elevación de los biomarcadores de inflamación que daban inicio y progresión a la neuropatía, así como un aumento de genes inflamatorios en los macrófagos del ganglio de la raíz dorsal, lo que contribuye en la hipersensibilidad al dolor.8
Estos procesos inflamatorios resultan de la formación de productos finales de glicación avanzada y la disfunción mitocondrial, lo que conlleva estrés oxidativo y daño al ADN con necrosis celular o inflamación por citocinas como TNF-α e IL-6.9
Papel neuropatogénico del hierro
Diferentes estudios han propuesto que niveles elevados de ferritina sérica y bajos niveles de transferrina se asocian con mayor riesgo de diabetes tipo 2. Se ha propuesto que una deficiencia de hierro se relaciona con la patogénesis de neuropatías periféricas; no obstante, el exceso de hierro ejerce efectos tóxicos y se involucra en la patogénesis de enfermedades neurodegenerativas. Un estudio experimental demostró que una dieta baja en hierro tiene un fuerte efecto en el desarrollo de neuropatía diabética, así como una reducción de las velocidades de conducción sensorial en el nervio ciático.8
Tratamiento
Es importante resaltar que el método número uno para el manejo de la neuropatía es la prevención, buscando el control de la glucosa y las modificaciones en el estilo de vida.5 Un estudio realizado en Utah menciona una regeneración de fibras nerviosas con un régimen alimenticio bajo en calorías y grasas junto con ejercicio aeróbico y de resistencia. Para el manejo del dolor, considerar pregabalina o duloxetina como tratamiento inicial, en el caso de síntomas como entumecimiento se recomienda el uso de terapia física en lugar de analgésicos.1,5 De acuerdo con la evidencia, se recomienda como primera línea de tratamiento el uso de duloxetina, seguido de la pregabalina como segunda línea y el tapentadol como tercera línea.
A pesar de la eficacia de los antidepresivos tricíclicos (amitriptilina) y la venlafaxina, aún no han sido aprobados por la FDA. Otra opción es la capsaicina tópica, pero generalmente no se tolera bien.1,2,5,10 Por último, el uso de opioides también es una opción terapéutica, sin embargo, no se recomiendan de primera línea por el alto riesgo de adicción.2,5 Otros medicamentos como nabilona y ginkgo biloba también podrían funcionar sobre el dolor. La amitriptilina es el medicamento más comúnmente usado en la terapia intratecal, a pesar de sus diversos efectos adversos. En cuanto a la pregabalina, tiene mejor efecto si se junta con N-acetilcisteína.2,10
La Guía Norteamericana de Neurología estudió los gabapentinoides, inhibidores de la recaptura de serotonina, antidepresivos tricíclicos, bloqueadores del canal de calcio y los agentes de doble mecanismo opioide/inhibidores de la recaptura de serotonina y noradrenalina, de los cuales resaltan que tienen poco beneficio sobre el dolor a diferencia del uso de placebo.2
Ácido α-lipóico
El ensayo ALADIN II, multicéntrico, aleatorizado y doble ciego, demostró que el uso de ácido α-lipóico genera una mejora en la puntuación del deterioro de la neuropatía (NIS).11
En el metaanálisis de Ziegler D y colegas, se evaluaron los ensayos clínicos ALADIN I, ALADIN II, SYDNEY y NATHAN I, en el que se observó una mejoría en la puntuación total de síntomas con el uso de ácido α-lipóico.12
Gabapentina
En un estudio realizado por Andrew Moore y su equipo, que buscaba valorar el uso de gabapentina en 5,914 pacientes, se observó que el uso de 1,200 mg/día generó una reducción del dolor en 50% comparado con el placebo.13
Pregabalina
Es el medicamento más estudiado para DSPN, con una mejora en el dolor de 30-50%.5 En el metaanálisis de Snedecor S y colaboradores de 58 pacientes, se demostró que el uso de 300 mg/día es una terapia efectiva para la mejoría de los pacientes en la escala analógica visual de 100 puntos.12 El uso de pregabalina ha demostrado una buena tolerancia y reducción de 50% del dolor comparado con placebo, convirtiéndolo en un tratamiento de segunda línea factible.14
Duloxetina
Amitriptilina
Tapentadol
En un estudio, cuyo objetivo era valorar la efectividad de tapentadol contra el uso de placebo, se administraron dosis de 100-250 mg de tapentadol dos veces al día, observando una reducción en la intensidad del dolor en el grupo tratado con tapentadol, comparado con el placebo.13 En la actualidad, es considerado tratamiento de tercera línea, al demostrar reducción en la intensidad del dolor comparado con placebo.14
Capsaicina a.
Es un analgésico tópico que ha demostrado reducción en la intensidad del dolor neuropático, diversos estudios han demostrado no inferioridad de la capsaicina al 8% comparado con pregabalina y duloxetina con mayor tolerancia a efectos adversos.14
Vitamina D
En un ensayo prospectivo aleatorizado, en el que se analizaron 67 pacientes con diabetes tipo 2 con la intención de evaluar el efecto de dosis altas (grupo I con 5,000 UI a la semana) y bajas (grupo II con 40,000 UI a la semana) de vitamina D en la microcirculación y en las escalas de neuropatía, se observó que en el grupo II, posterior a 24 semanas de tratamiento, hubo disminución en la intensidad del dolor evaluada por escala visual análoga (EVA). Sin embargo, se concluyó en el ensayo que el efecto de la vitamina D se debe mayormente a la mejora de parámetros metabólicos en los pacientes y no una acción directa de este fármaco (Tabla 2).15
Tabla 2: Principales fármacos empleados en el manejo de la neuropatía diabética.
| Grupo | Medicamento | Mecanismo de acción | Dosis | Recomendaciones | Reacciones adversas |
|---|---|---|---|---|---|
| Anticonvulsivantes | Pregabalina | Inhibe el voltaje del ligando de la subunidad alfa 2-delta del canal de calcio | Inicial 50 mg/día Rango de 300 mg/día |
Reducción de la intensidad del dolor neuropático. Segunda línea de tratamiento | Mareo, somnolencia, visión borrosa, vértigo, insomnio |
| Gabapentina | Inhibe el voltaje del ligando de la subunidad alfa 2-delta del canal de calcio | Inicial 300 mg/día Rango de 1,800-3,600 mg/día |
Reducción de la intensidad del dolor neuropático | Ataxia, nistagmo, amnesia, depresión, mareo | |
| Antidepresivos (ISRSN) | Duloxetina | Inhibidor selectivo de la recaptura de serotonina y noradrenalina | Inicial 60 mg/día Rango de 120 mg/día |
Reducción de la intensidad del dolor neuropático. Primera línea de tratamiento | Trastorno depresivo mayor, náusea, sequedad de boca |
| Venlafaxina | Inhibidor selectivo de la recaptura de serotonina y noradrenalina | Inicial 75 mg/día Rango de 75-225 mg/día |
Sin evidencia de efectividad | Náusea, cefalea, insomnio, somnolencia, vértigo, sequedad de boca | |
| Amitriptilina | Inhibidor selectivo de la recaptura de serotonina y noradrenalina | Inicial 10-25 mg/día Rango de 100 mg/día |
Sin efectividad en la reducción de dolor | Fatiga, somnolencia, mareo, sequedad bucal, taquicardia | |
| Opioides | Tapentadol | Agonista del receptor opioide μ e inhibidor de la recaptura de norepinefrina | Inicial 100 mg/día Rango de 100-250 mg/día |
Reducción de la intensidad del dolor neuropático. Tercera línea de tratamiento | Náusea, vértigo, vómito, somnolencia, cefalea |
| Tramadol | Agonista puro no selectivo de receptores opioides mu, delta y kappa | Inicial 200 mg/día Rango de 400 mg/día |
Sin evidencia de efectividad | Mareo, náuseas, cefalea, vómito, diaforesis | |
| Tópicos | Capsaicina | Agonista de TRPV1 | 1-4 aplicaciones de parche al 8% por 30 minutos | Reducción de intensidad de dolor neuropático | Sensación de quemazón o ardor cutáneo en zona de aplicación |
TRPV1 = receptor de potencial transitorio, un canal catiónico capaz de activarse por calor, pH ácido, voltaje y por diferentes sustancias químicas.
Tratamiento no farmacológico
Neuromodulación: dispositivos implantables y no implantables que liberan agentes eléctricos, químicos o de otro tipo que tienen el objetivo de suprimir la actividad del sistema nervioso. Hay tres tipos de neuromodulación: estimulación nerviosa eléctrica transcutánea, terapia de dolor intratecal y estimulación de médula espinal.
Dentro de la estimulación de médula espinal, se divide en convencional, explosiva y delta frecuencia.
Estimulación del ganglio de la raíz dorsal (GRD).
Estimulación nerviosa eléctrica transcutánea: terapia no invasiva, no costosa y fácil de utilizar. Se conforma de adhesivos con electrodos que liberan estimulación eléctrica de tipos de frecuencia, alta (< 50 Hz) y baja (< 10 Hz) o más.
Terapia de dolor intratecal: muestra mejoría en la habilidad de caminar.5
Conclusiones
Se recomienda explicar a los pacientes que el uso de terapia en neuropatía diabética tiene el fin de reducir las molestias y el dolor, pero no necesariamente quitarlo. Hoy en día, el manejo terapéutico de la neuropatía diabética debe personalizarse de acuerdo al grado y tipo de molestias que presente el paciente, sin poder establecer un abordaje terapéutico único. Se recomienda como fármaco de primera línea el uso de duloxetina debido a su efectividad y tolerabilidad, continuado por la pregabalina como segunda línea y el tapentadol como tercera línea de tratamiento, debido al alto riesgo de adicción de los opioides. Es importante contemplar las nuevas opciones no farmacológicas para el tratamiento de la neuropatía como complemento al manejo inicial y dar énfasis a las modificaciones del estilo de vida.
Si bien iniciamos con la pregunta “¿fantasía o realidad?”, se puede concluir que el tratamiento de la neuropatía diabética sigue siendo una fantasía debido a las diversas consideraciones que se involucran para la decisión terapéutica, desde individualizar cada caso y aún no tener claras evidencias de una mejoría con el inicio de los distintos fármacos. Tras la realización de esta revisión podemos mencionar que no existe en la actualidad una recomendación completamente fundamentada de cómo iniciar el abordaje terapéutico de los pacientes, recordando que, si bien los fármacos indicados ayudan con la mejoría de los síntomas, no hay tratamiento para detener la progresión de la enfermedad y nos debemos fundamentar en las medidas de control metabólico para retrasar el desarrollo de la neuropatía.
Finalmente, si bien el uso de duloxetina como fármaco de primera línea es la recomendación actual, no podemos asegurar que ésta sea efectiva en todos los pacientes, lo que conlleva a la necesidad de un cambio terapéutico de acuerdo con la severidad de síntomas y la tolerabilidad al medicamento, motivo por el cual no hay un fármaco mejor que otro, sino pacientes que responden mejor.