Introducción
Las macroalgas marinas bentónicas son uno de los grupos más representativos dentro de los ecosistemas marinos costeros e insulares (Dreckmann, 1998; Pedroche y Sentíes, 2020). En México, su estudio se ha incrementado considerablemente en la última década, sobre todo en temas florísticos, taxonómicos y sistemáticos (García-García et al., 2020, 2021; Núñez-Resendiz et al., 2017; Pedroche y Sentíes, 2020). Sin embargo, este conocimiento se ha sesgado hacia ambientes marinos continentales, siendo pocos los trabajos enfocados en el estudio de la diversidad macroalgal insular (Carranza-Ramírez et al., 2023; González-Solis et al., 2018; Ortegón-Aznar y Aguilar-Perera, 2014; Robledo et al., 2003). La importancia de estudiar la biota de ambientes insulares radica en que sus procesos ecológicos y dinámicas evolutivas son muy particulares debido a su aislamiento, tamaño y origen, siendo los ecosistemas con mayor riqueza de especies en el mundo, muchas de ellas endémicas o provenientes de distintas regiones biogeográficas, cuyas poblaciones son altamente vulnerables (INEGI, 2015; Whittaker y Fernández-Palacios, 2007).
La zona de transición biótica del Atlántico mexicano abarca toda la región marítima del estado de Yucatán y se denomina así por ser el punto de encuentro entre las biotas marinas del golfo de México y el mar Caribe, esto hace que potencialmente sus ambientes insulares sean de los más biodiversos del país (Vilchis et al., 2018). En cuanto a macroalgas se refiere, resulta paradójico que a pesar de ser una de las zonas de mayor riqueza específica (García-García et al., 2020; Tapia-Silva et al., 2015; Vilchis et al., 2018), tan solo se tenga conocimiento ficoflorístico de 2 de los 80 elementos insulares (islas, arrecifes y cayos) registrados por el INEGI (2015) para el área, los cuales son Arrecife Alacranes y Cayo Arenas. Lo anterior es evidencia de los vacíos de información que existen sobre la diversidad de macroalgas en estos ecosistemas ubicados en una región biogeográficamente compleja (Tapia-Silva et al., 2015; Vilchis et al., 2018).
En consecuencia, el objetivo de este trabajo fue contribuir al conocimiento de las macroalgas marinas bentónicas de ambientes insulares, presentando la composición taxonómica de 3 arrecifes de la zona de transición biótica del Atlántico mexicano, cuya ficoflora hasta el momento se desconoce.
Materiales y métodos
Los arrecifes explorados fueron Bajos de Diez, Madagascar y Serpientes, los cuales pertenecen al Sistema Arrecifal Sisal, Yucatán (Fig. 1). Todos ellos son someros y presentan un fondo mayormente carbonatado (Zarco-Perelló et al., 2013). Están ubicados al noroeste de la península de Yucatán entre las coordenadas 21°20’ N, 90°14’ O y 21°14’ N, 89°50’ O (Winfield et al., 2020).
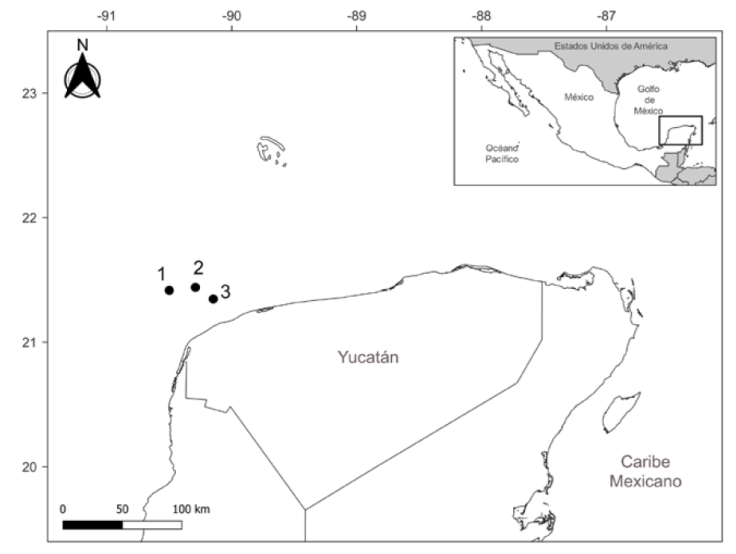
Figura 1 Ubicación geográfica de los arrecifes de Sisal estudiados en este trabajo. 1, Serpientes; 2, Madagascar; 3, Bajos de Diez.
Bajos de Diez es el más cercano a la costa (23 km), tiene el área más grande (0.67 km2) y profundidades de 2 a 10 m, predominan las llanuras arenosas y varios arrecifes segregados. Madagascar es una sola estructura arrecifal (0.21 km2) que se encuentra a 40 km de la costa, con profundidades de 4 a 13 m. Serpientes, el más pequeño de todos (0.17 km2), se ubica a 54 km del continente con profundidades de 7 a 13 m y cuenta con 2 unidades de arrecife separadas por 2.5 km (Zarco-Perello y Simões 2017; Zarco-Perelló et al., 2013).
Se realizaron en total 6 buceos SCUBA en diversos sitios de los arrecifes de Sisal durante los años 2007 (arrecife Madagascar), 2012 a 2019 (Bajos de Diez) y 2017 (Serpientes) para la recolecta de macroalgas marinas bentónicas (Tabla 1). Es importante resaltar que el esfuerzo de muestreo fue más intensivo en Bajos de Diez, con un mayor número de recolectas (Tabla 1). Los especímenes fueron recolectados a mano, desprendiéndolos del sustrato rocoso con ayuda de una espátula y colocados en bolsas herméticas con agua de mar. Cada ejemplar fue identificado mediante observaciones morfológicas macro y microscópicas, siguiendo las obras de Dawes y Mathieson (2008), Littler y Littler (2000), Taylor (1960) y Wynne (2022). La nomenclatura fue verificada en la base de datos Algaebase (Guiry y Guiry, 2024). Las muestras se preservaron individualmente en húmedo con formalina al 4%, posteriormente fueron depositadas en el Herbario Alfredo Barrera Marín de la Universidad Autónoma de Yucatán (UADY).
Tabla 1 Coordenadas y fechas de muestreo de cada estructura arrecifal estudiada de Sisal.
| Estructura arrecifal | Estación | Coordenadas | Fecha/ estacionalidad | |
|---|---|---|---|---|
| Bajos de Diez | B.D.1 | 21°21’12.6” N | 90°09’27.5” O | Diciembre 2012 (secas), 2013, abril 2017 y julio 2019 (lluvias) |
| B.D.2 | 21°21’6.32” N | 90°09’23.4” O | ||
| B.D.3 | 21°20’59.53” N | 90°09’21.7” O | ||
| B.D.4 | 21°50’52.2” N | 90°08’56.4” O | ||
| Madagascar | MAD1 | 21°26’26.1” N | 90°16’55.2” O | Agosto y septiembre 2007 (lluvias) |
| MAD2 | 21°26’19.2” N | 90°16’56.5” O | ||
| MAD3 | 21°26’19.2” N | 90°16’42.3” O | ||
| MAD4 | 21°26’29.6” N | 90°17’36.1” O | ||
| Serpientes | SER1 | 21°26’05.2” N | 90°27’23.1” O | Julio 2017 (lluvias) |
| SER2 | 21°26’21.7” N | 90°28’22.5” O |
La diversidad taxonómica para cada arrecife se obtuvo contabilizando el número de familias, géneros y especies presentes en ellos. Además, se calculó la frecuencia relativa (fi) de cada especie en los 10 sitios de muestreo (4 en Bajos de Diez, 4 en Madagascar y 2 en Serpientes), con la finalidad de conocer cuáles eran las más frecuentes en los 3 arrecifes estudiados (Tabla 1).
La similitud florística entre las 3 estructuras arrecifales estudiadas se evaluó realizando una matriz de presencia-ausencia de las especies en cada sitio, la cual fue sometida a un análisis de agrupamiento bajo el índice de Jaccard (IJ) y el algoritmo por ligamiento promedio no ponderado (UPGMA, por sus siglas en inglés) en el programa PAST v4.7b (Hammer et al., 2001). El análisis resumió los resultados en un fenograma.
Resultados
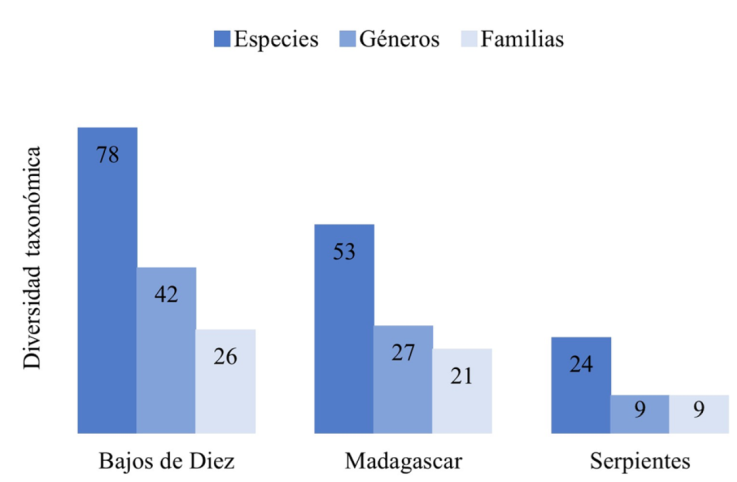
Se presenta un listado de 119 especies de macroalgas marinas bentónicas para los 3 arrecifes estudiados, las cuales se distribuyen en 32 familias y 59 géneros (Tabla 2): 41 especies pertenecen a Chlorophyta (algas verdes), 51 a Rhodophyta (algas rojas) y 24 a Ochrophyta (Phaeophyceae, algas pardas). Nueve especies corresponden a nuevos registros para Yucatán (Tabla 2), señalados con un asterisco, 2 son algas verdes (Udotea abbottiorum D.S. Littler et Littler, Microdictyon marinum (Bory) P.C. Silva), 2 algas pardas (Padina perindusiata Thivy, Sargassum platycarpum Montagne) y 5 algas rojas (Dictyurus occidentalis J. Agardh, Gracilaria cuneata Areschoug, Corynomorpha clavata (Harvey) J. Agardh, Platoma gelatinosum (M. Howe) C.W. Schneider, McDevit, G.W. Saunders et C.E. Lane, Ceratodictyon variabile (J. Agardh) R.E. Norris), algunas de estas se muestran en la Figura 2. Las familias mejor representadas por su número de especies fueron: Caulerpaceae (11), Dictyotaceae (18), Halimedaceae (17) y Rhodomelaceae (13). La estructura arrecifal que presentó mayor diversidad taxonómica fue Bajos de Diez, seguida de Madagascar y por último Serpientes (Fig. 3). Las divisiones predominantes en los 3 arrecifes fueron Chlorophyta y Rhodophyta (Fig. 4).
Tabla 2 Listado de macroalgas marinas bentónicas de los arrecifes de Sisal, Yucatán, México. * Registros nuevos para Yucatán.
| Especie | Bajos de Diez | Madagascar | Serpientes |
|---|---|---|---|
| Ochrophyta | |||
| Dictyotaceae | |||
| Canistrocarpus cervicornis (Kützing) De Paula y De Clerck | X | X | |
| Canistrocarpus crispatus (J.V. Lamouroux) De Paula et De Clerck | X | X | |
| Dictyopteris delicatula J.V. Lamouroux | X | X | X |
| Dictyopteris jamaicensis W.R. Taylor | X | ||
| Dictyopteris justii J.V. Lamouroux | X | ||
| Dictyopteris plagiogramma (Montagne) Vickers X95 | X | ||
| Dictyopteris polypodioides (De Candolle) J.V. Lamouroux | X | X | |
| Dictyota ciliolata Sonder ex Kützing | X | ||
| Dictyota dichotoma (Hudson) J.V. Lamouroux | X | X | |
| Dictyota mertensii (C. Martius) Kützing | X | ||
| Dictyota pinnatifida Kützing | X | ||
| Dictyota pulchella Hörning et Schnetter | X | ||
| Lobophora variegata (J.V. Lamouroux) Womersley ex E.C. Oliveira | X | X | |
| Padina boergesenii Allender et Kraft | X | ||
| Padina pavonica (Linnaeus) Thivy | X | ||
| Padina perindusiata Thivy * | X | ||
| Padina sanctae-crucis Børgesen | X | X | |
| Spatoglossum schroederi (C. Agardh) Kützing | X | ||
| Sphacelariaceae | |||
| Sphacelaria rigidula Kützing | X | ||
| Chordariaceae | |||
| Cladosiphon occidentalis Kylin | X | ||
| Nemacystus howei (W.R.Taylor) Kylin | X | ||
| Scytosiphonaceae | |||
| Colpomenia sinuosa (Mertens ex Roth) Derbès et Solier | X | X | |
| Sargassaceae | |||
| Sargassum furcatum Kützing | X | ||
| Sargassum hystrix J. Agardh | X | ||
| Sargassum platycarpum Montagne * | X | ||
| Sargassum pteropleuron Grunow | X | ||
| Sargassum sp. C. Agardh | X | ||
| Sporochnaceae | |||
| Sporochnus pedunculatus (Hudson) C. Agardh | X | ||
| Rhodophyta | |||
| Corallinaceae | |||
| Jania capillacea Harvey | X | ||
| Jania cubensis Montagne ex Kützing | X | ||
| Jania pedunculata J.V. Lamouroux | X | ||
| Jania pumilla J.V. Lamouroux | X | ||
| Lithophyllaceae | |||
| Amphiroa fragilissima (Linnaeus) J.V. Lamouroux | X | X | |
| Amphiroa tribulus (J. Ellis et Solander) J.V. Lamouroux | X | ||
| Bonnemaisoniaceae | |||
| Asparagopsis taxiformis (Delile) Trevisan | X | X | X |
| Callithamniaceae | |||
| Spyridia filamentosa (Wulfen) Harvey | X | X | |
| Ceramiaceae | |||
| Centroceras micracanthum Kützing | X | ||
| Ceramium cimbricum H.E. Petersen | X | X | |
| Ceramium cruciatum Collins et Hervey | X | X | |
| Ceramium nitens (C. Agardh) J. Agardh | X | ||
| Ceramium virgatum Roth | X | ||
| Gayliella flaccida (Harvey ex Kützing) T.O. Cho et L.J. McIvor | X | ||
| Delesseriaceae | |||
| Dictyurus occidentalis J. Agardh * | X | X | |
| Heterosiphonia gibbesii (Harvey) Falkenberg | X | ||
| Rhodomelaceae | |||
| Acanthophora spicifera (M. Vahl) Børgesen | X | ||
| Alsidium seaforthii (Turner) Kützing | X | ||
| Alsidium triquetrum (S.G. Gmelin) Trevisan | X | ||
| Bostrychia tenella (J.V. Lamouroux) J. Agardh | X | ||
| Chondria sp. | X | ||
| Digenea mexicana G.H. Boo et D. Robledo | X | ||
| Laurencia intricata J.V. Lamouroux | X | ||
| Melanothamnus sphaerocarpus (Børgesen) Díaz-Tapia et Maggs | X | ||
| Osmundaria obtusiloba (C. Agardh) R.E. Norris | X | ||
| Polysiphonia binneyi Harvey | X | ||
| Polysiphonia sp. | X | ||
| Wilsonosifonia howei (Hollenberg) D. Bustamante, Won et TOCho | X | ||
| Yuzurua poiteaui (J.V. Lamouroux) Martin-Lescanne | X | ||
| Wrangeliaceae | |||
| Ptilothamnion speluncarum (Collins et Hervey) D.L. Ballantine et M.J. Wynne | X | ||
| Gelidiaceae | |||
| Gelidium americanum (W.R. Taylor) Santelices | X | ||
| Caulacanthaceae | |||
| Catenella caespitosa (Withering) L.M. Irvine | X | ||
| Cystocloniaceae | |||
| Hypnea spinella (C. Agardh) Kützing | X | X | |
| Solieriaceae | |||
| Agardhiella subulata (C. Agardh) Kraft et M.J. Wynne | X | X | |
| Eucheumatopsis isiformis (C. Agardh) Núñez-Resendiz, Dreckmann et Sentíes | X | ||
| Solieria filiformis (Kützing) Gabrielson | X | ||
| Gracilariaceae | |||
| Gracilaria cuneata Areschoug * | X | ||
| Gracilaria cervicornis (Turner) J. Agardh | X | ||
| Gracilaria domingensis (Kützing) Sonder ex Dickie | X | ||
| Gracilaria sp. | X | ||
| Gracilaria tikvahiae McLachlan | X | ||
| Halymeniaceae | |||
| Corynomorpha clavata (Harvey) J. Agardh * | X | ||
| Halymenia elongata C. Agardh | X | ||
| Halymenia pseudofloresii Collins et M.Howe | X | X | |
| Halymenia floridana J. Agardh | X | ||
| Schizymeniaceae | |||
| Platoma gelatinosum (M. Howe) C.W. Schneider, McDevit, G.W. | X | ||
| Saunders et C.E. Lane * | |||
| Champiaceae | |||
| Coelothrix sp. | X | ||
| Lomentariaceae | |||
| Ceratodictyon intricatum (C. Agardh) R.E. Norris | X | ||
| Ceratodictyon planicaule (W.R. Taylor) M.J. Wynne | X | ||
| Ceratodictyon variabile (J. Agardh) R.E. Norris * | X | ||
| Chlorophyta | |||
| Derbesiaceae | |||
| Derbesia marina (Lyngbye) Solier | X | ||
| Codiaceae | |||
| Codium isthmocladum Vickers | X | X | |
| Dichotomosiphonaceae | |||
| Avrainvillea sp. | X | ||
| Caulerpaceae | |||
| Caulerpa ambigua Okamura | X | X | |
| Caulerpa ashmeadii Harvey | X | X | |
| Caulerpa brachypus Harvey | X | ||
| Caulerpa chemnitzia (Esper) J.V. Lamouroux | X | ||
| Caulerpa cupressoides (Vahl) C. Agardh | X | ||
| Caulerpa microphysa (Weber Bosse) Feldmann | X | ||
| Caulerpa prolifera (Forsskål) J.V. Lamouroux | X | ||
| Caulerpa racemosa (Forsskål) J. Agardh | X | X | |
| Caulerpa racemosa var. macrophysa (Sonder ex Kützing) W.R. Taylor | X | ||
| Caulerpa verticillata J. Agardh | X | X | X |
| Caulerpa webbiana Montagne | X | X | |
| Halimedaceae | |||
| Boodleopsis pusilla (Collins) W.R. Taylor, A.B. Joly et Bernatowicz | X | ||
| Halimeda discoidea Decaisne | X | X | |
| Halimeda incrassata (J. Ellis) J. V. Lamouroux | X | X | X |
| Halimeda monile (J. Ellis et Solander) J. V. Lamouroux | X | ||
| Halimeda opuntia (Linnaeus) J.V. Lamouroux | X | ||
| Halimeda scabra M. Howe | X | X | |
| Halimeda sp. | X | X | |
| Halimeda tuna (J. Ellis et Solander) J.V. Lamouroux | X | ||
| Penicillus capitatus Lamarck | X | X | |
| Penicillus dumetosus (J.V. Lamouroux) Blainvillea | X | X | X |
| Rhipocephalus phoenix (J. Ellis et Solander) Kützing | X | X | |
| Udotea abbottiorum D.S. Littler et Littler * | X | ||
| Udotea caribaea D.S. Littler et Littler | X | X | |
| Udotea conglutinata (J. Ellis et Solander) J.V. Lamouroux | X | ||
| Udotea cyathiformis Decaisne | X | X | |
| Udotea dixonii D.S. Littler et Littler | X | ||
| Udotea unistratea D.S. Littler et Littler | X | ||
| Anadyomenaceae | |||
| Microdictyon marinum (Bory) P.C. Silva* | X | ||
| Boodleaceae | |||
| Cladophoropsis macromeres W.R. Taylor | X | ||
| Cladophoropsis membranacea (Hofman Bang ex C. Agardh) Børgesen | X | ||
| Cladophoraceae | |||
| Chaetomorpha sp. | X | ||
| Chaetomorpha gracilis Kützing | X | ||
| Cladophora intertexta Collins | X | ||
| Cladophora laetevirens (Dillwyn) Kützing | X | X | |
| Cladophora prolifera (Roth) Küitzing * | X | X | |
| Rhizoclonium riparium (Roth) Harvey | X | ||
| Polyphysaceae | |||
| Acetabularia crenulata J.V. Lamouroux | X |

Figura 2 Fotografías de 6 de las macroalgas que integran el listado presentado, 5 de ellas corresponden a los nuevos registros. A, Platoma gelatinosum; B, Udotea abbottiorum; C, Cladophora prolifera; D, Microdictyon marinum; E, Dictyota dichotoma; F, Corynomorpha clavata.
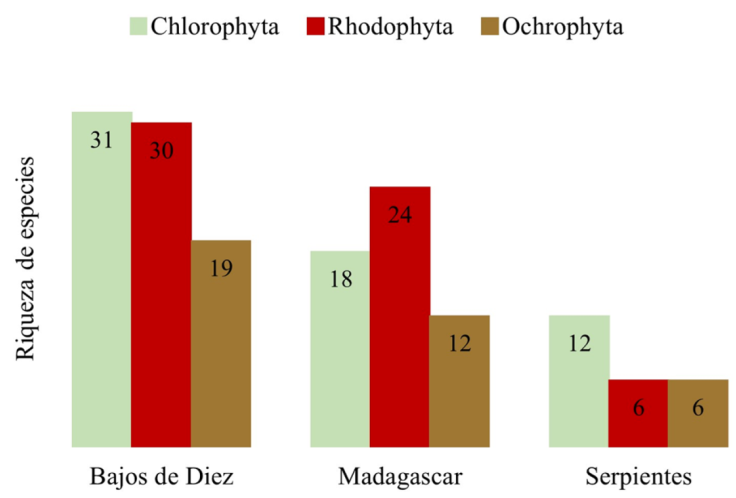
Figura 4 Predominancia de las divisiones algales en 3 arrecifes de Sisal. Las cifras en cada barra corresponden al número de especies por cada división.
Las especies que fueron registradas en los 3 arrecifes fueron 5: Caulerpa verticillata J. Agardh, Halimeda incrassata (J. Ellis) J. V. Lamouroux, Penicillus dumetosus (J. V. Lamouroux) Blainvillea, Dictyopteris delicatula J.V. Lamouroux y Asparagopsis taxiformis (Delile) Trevisan. En cuanto a la frecuencia relativa (fi , material suplementario: S1), Asparagopsis taxiformis fue la especie más frecuente en las 3 estructuras arrecifales (fi = 80%), seguida de Codium isthmocladum, Halimeda incrassata, Halimeda sp., Dictyopteris delicatula, Dictyota sp., Hypnea spinella y Dictyurus occidentalis (fi = 60%). La mayor parte de las especies (82) se presentaron una sola vez, 49 en Bajos de Diez, 26 en Madagascar y 7 en Serpientes.
El fenograma resultado del análisis de agrupamiento, muestra de manera general 2 grupos con una similitud florística de aproximadamente 7% (Fig. 5); el primer grupo integra a los arrecifes de Bajos de Diez y Serpientes, similares en su composición florística de especies en aproximadamente 15% y el segundo grupo, solo formado por las estaciones muestreadas en arrecife Madagascar. Los porcentajes de similitud revelan que la composición florística de los arrecifes explorados, en realidad, son disímiles entre sí.
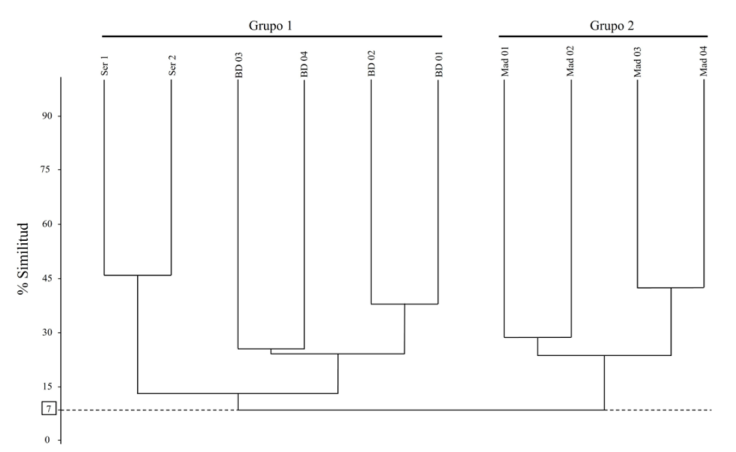
Figura 5 Fenograma resultante del análisis de agrupamiento. Los nombres en cada rama terminal son las abreviaciones empleadas para nombrar y numerar las estaciones muestreadas en cada arrecife. BD: Bajos de Diez; Mad: Madagascar; Ser: Serpientes. La línea punteada señala el porcentaje de similitud entre los 2 grupos principales formados en el fenograma.
Discusión
De acuerdo con los resultados, las algas rojas son el grupo taxonómico con mayor número de especies, su predominancia en ambientes insulares, costeros y lagunares tropicales es algo común, y ya reportado por varios autores para las costas de Yucatán (Dreckmann, 1998; Ortegón-Aznar y León-Tejera, 2022; Pedroche y Sentíes, 2020). A nivel de familia, los datos también son coincidentes con lo que existe en la literatura para la zona (Dreckmann, 1998; García-García et al., 2022; Mendoza-González et al., 2016; Ortega et al., 2001; Ortegón-Aznar y León-Tejera, 2022; Pedroche y Sentíes, 2020; Vilchis et al., 2018) y específicamente para ambientes insulares (González-Solis et al., 2018); Caulerpaceae, Halimedaceae, Dictyotaceae y Rhodomelaceae son las familias con mayor riqueza específica. En cuanto a las macroalgas que habitan los arrecifes, en Bajos de Diez y Serpientes se registraron más clorofitas, mientras que en Madagascar rodofitas. La predominancia de las algas verdes en los 2 primeros arrecifes probablemente puede estar correlacionado con el tipo de sustrato presente en ellos, ya que sus estructuras coralinas y rocosas segregadas promueven la existencia de fondos carbonatados y grandes llanuras arenosas, que son donde las algas verdes encuentran mejores condiciones para su desarrollo y distribución. En consecuencia, esto también explicaría el hecho de que Caulerpaceae y Halimedaceae son las familias con más representantes en estos arrecifes, al establecerse las especies de la primera preferentemente en suelos arcillo-arenosos, y en carbonatados las de la segunda, al ser fijadoras de calcio en su pared celular (Garduño-Solórzano et al., 2005).
La similitud florística entre los 3 arrecifes se encuentra por debajo de 15%, lo cual es bajo si se considera que forman parte del mismo sistema arrecifal y que la similitud entre localidades aumenta con la cercanía entre ellas (Nekola y White, 1999). Sin embargo, la ubicación geográfica e historia geológica tan compleja de la península de Yucatán ha dado lugar a una gran heterogeneidad de hábitats, lo que promueve una elevada riqueza de especies, muchas veces adaptadas a microambientes específicos y conlleva, a su vez, a diferencias notables en la composición biológica de localidades cercanas entre sí, además, es importante considerar que esta parte del territorio nacional es una zona de convergencia biótica, derivada también de su historia geológica (Vilchis et al., 2018). Ahora bien, haciendo una comparación florística, de manera general, entre los arrecifes analizados en este estudio y los ya explorados, es posible saber que de las 119 especies reportadas aquí, 9 son exclusivas del Sistema Arrecifal de Sisal, mientras que el resto ya se ha registrado en Arrecife Alacranes y Cayo Arenas.
Los nuevos registros que se incorporan a la ficoflora de Yucatán ya han sido reportados antes para el Atlántico. Cladophora prolifera y Ceratodictyon variabile son especies pantropicales presentes tanto en el Pacífico como en el Atlántico mexicano. Corynomorpha clavata, Dictyurus occidentalis, Gracilaria cuneata, Microdictyon marinum, Padina perindusiata y Udotea abbottiorum son macroalgas con afinidad a las aguas tropicales del mar Caribe, algunas llegando a introducirse en la región sur del golfo de México. De estas especies resaltan los casos de C. clavata y G. cuneata, la primera solo había sido reportada para el litoral de Campeche y Quintana Roo, lo que significa que este nuevo registro es también el primero para ambientes insulares mexicanos y Yucatán; G. cuneata , hasta antes de este trabajo solo formaba parte de la flora insular de Quintana Roo, ahora se sabe que extiende su área de distribución hasta arrecifes de Sisal. Por último, la presencia de Platoma gelatinosum en Yucatán refuerza el único reporte que hay en México, un ejemplar colectado en la costa de Campeche por Huerta-Múzquiz y Garza-Barrientos (1966), producto de una recolecta en arribazón y, por ende, su ubicación puntual no era conocida. Las diferentes afinidades biogeográficas que muestran los nuevos registros podrían estar evidenciando que los elementos insulares del Sistema Arrecifal Sisal son un mosaico compuesto de especies de diferente origen biótico, lo que sustentaría lo propuesto por Vilchis et al. (2018); sin embargo, sería importante realizar un estudio más detallado sobre el tema, considerando la distribución de todas las especies presentes en estos arrecifes.
Asparagopsis taxiformis fue la especie con mayor frecuencia relativa (material suplementario: S1), presente en 8 de las 10 estaciones, en listados florísticos previos no había sido reportada para el área de estudio; sin embargo, Ortegón-Aznar et al. (2008) señalaron que era una especie abundante en arrecife Madagascar. En general, A. taxiformis, así como las otras 7 especies con alta frecuencia relativa, son macroalgas que se encuentran típicamente en ambientes arrecifales, además de que algunas han sido consideradas como invasoras (Littler y Littler, 2000). Como ya se había mencionado con anterioridad, en la zona de transición biótica del Atlántico mexicano el conocimiento ficoflorístico que se tiene de ambientes insulares es escaso, centrado principalmente en Arrecife Alacranes y sus alrededores, y aunque la información se encuentre dispersa en artículos, catálogos, colecciones de herbario, monografías y proyectos de instituciones públicas, se sabe de manera general que de las 386 especies de macroalgas reportadas para la región, aproximadamente 243 se distribuyen en ambientes insulares (Ortegón-Aznar y León-Tejera, 2022); este número representa casi el doble de las 119 registradas en este trabajo, lo cual resulta coherente si se toma en cuenta que el área de los arrecifes de Sisal es considerablemente menor (~ 1 km2) a la de Arrecife Alacranes (~ 326 km2); evidenciando la relación especies-área, cuya premisa es que, a mayor tamaño de área de una isla, mayor será el número de especies que pueda albergar (MacArthur y Wilson, 1967). Dicha relación también se cumple entre los 3 arrecifes de Sisal: Bajos de Diez (78 spp. / 0.67 km2), Madagascar (53 spp. / 0.21 km2) y Serpientes (24 spp. / 0.17 km2); sin embargo, se debe considerar que el esfuerzo de muestreo no fue el mismo para los 3 arrecifes. En este sentido, también es importante resaltar que, aunque hasta antes de este trabajo solo se conocía la ficoflora insular de Arrecife Alacranes y sus alrededores, Yucatán ocupaba y sigue ocupando uno de los primeros lugares en la lista de los ambientes insulares más diversos del Atlántico mexicano, superado tan solo por Quintana Roo (García-García et al., 2020; González-Solis et al., 2018; Tapia-Silva et al., 2015; Vilchis et al., 2018). Los arrecifes contiguos del estado de Campeche, aunque en número son más los que se han estudiado, su diversidad máxima registrada es de 12 especies (González-Solis et al., 2018).
En la ficología, la publicación de los listados y composición florística sigue siendo muy relevante, sobre todo en un país como México, donde las exploraciones han sido discontinuas y sesgadas hacia ambientes costeros continentales, y donde existe una gran cantidad de elementos insulares aún sin explorar (Ortegón-Aznar y Aguilar-Perera, 2014; Robledo et al., 2003), así como especies reportadas una sola vez y en un solo sitio. La importancia de trabajos como el que se presenta aquí, no solo radica en proveer información fundamental para el conocimiento de la riqueza de especies y diversidad de estos ambientes, sino también que representan los datos primarios para otro tipo de trabajos de índole biológico como los taxonómicos, sistemáticos, biogeográficos y ecológicos, que en un futuro proporcionarán criterios para la protección y conservación de estos ecosistemas, cuyas poblaciones naturales son altamente vulnerables a las actividades antropogénicas principalmente relacionadas con el turismo, desastres naturales, cambios climáticos globales y a la introducción de especies exóticas, razones primordiales del deterioro de la biodiversidad, desaparición de especies, deterioro de hábitats, contaminación y sobreexplotación de especies comerciales o económicamente importantes.