Introducción
Las bronquiectasias (BQ) son anomalías permanentes, caracterizadas por dilatación de los bronquios. Los pacientes con BQ experimentan tos crónica, producción de esputo, disnea, fatiga y exacerbaciones recurrentes, junto con otros síntomas, como malestar general, dolor torácico, hemoptisis y pérdida de peso. Fisiopatológicamente, la dilatación bronquial conduce a alteración de la depuración mucociliar y una alteración en la eliminación de bacterias y moco, facilitando el atrapamiento de partículas y microorganismos que entran en las vías respiratorias. Lo anterior genera focos infecciosos persistentes, inflamación y lesión en otras zonas de la vía respiratoria1.
Las BQ pueden desarrollarse como resultado de enfermedades infecciosas, inflamatorias, alérgicas, genéticas y degenerativas, y, por tanto, es la vía común donde convergen múltiples procesos fisiopatológicos1,2. Las BQ tienen un impacto sanitario significativo, se estima que hasta el 78% de los pacientes que acuden a urgencias experimentan agudización de los síntomas, lo que resulta en una estancia hospitalaria de más de 10 días, más prolongada que con otras enfermedades respiratorias como el asma3.
Epidemiología
Las BQ pueden afectar a personas de todas las edades, pero la incidencia aumenta con la edad. En los niños, las BQ tienen mayor prevalencia en regiones con infecciones respiratorias frecuentes, y suelen tener un retraso hasta de 14.8 años en el diagnóstico desde la aparición de los síntomas iniciales, haciendo que los pacientes accedan de forma tardía a un tratamiento adecuado4.
En pediatría no hay un claro predominio de sexo y se asocia principalmente a infecciones1,5. El tabaquismo no se ha demostrado como un factor asociado al desarrollo de BQ6. La susceptibilidad al desarrollo de BQ puede variar según la localización geográfica y la etnia; sin embargo, hay una mayor carga de enfermedad en países con alta incidencia de infecciones graves recurrentes y tuberculosis7. La fibrosis quística (FQ) es la causa más frecuente de BQ en países occidentales, mientras que en Asia pueden tener mayor protagonismo las causas infecciosas y la discinesia ciliar primaria7,8. Se han descrito múltiples causas, Brower et al. reportan la evaluación de 989 pacientes y además de las ya mencionadas incluyen errores innatos de la inmunidad como deficiencia de inmunoglobulina (Ig) G, subclases de IgG, IgA, síndrome hiper-IgE, deficiencia de células T, candidiasis mucocutánea, enfermedad granulomatosa crónica y inmunodeficiencia grave combinada. Además, se ha asociado a malformaciones congénitas como fístula traqueoesofágica y enfermedad pulmonar quística entre otras9.
Fisiopatología
La fisiopatología de las BQ involucra diversos mecanismos heterogéneos y complejos, los cuales varían según la causa subyacente y los factores genéticos y epigenéticos relacionados. En esencia, el epitelio respiratorio cumple una función clave como barrera física para resistir la lesión, por medio de uniones celulares estrechas y la participación de factores funcionales como la producción de mucina, la motilidad ciliar, la síntesis de péptidos antimicrobianos y el transporte de iones. Estos mecanismos trabajan en conjunto para proteger las vías respiratorias1.
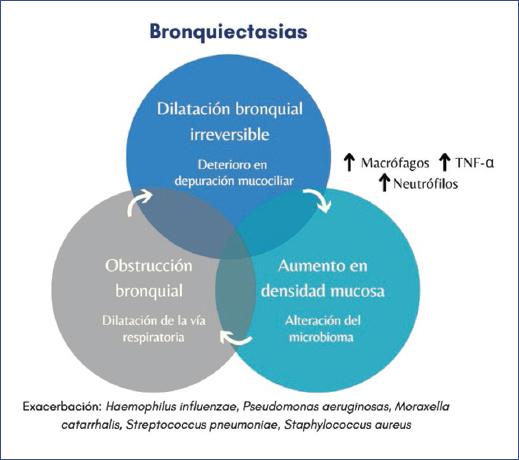
En la fase inicial ocurre una lesión que causa dilatación bronquial y posteriormente el deterioro de la función mucociliar. El aumento de la densidad mucosa, la presencia persistente de microorganismos y una inefectividad del sistema inmunitario para su depuración con desregulación local favorecen la progresión de la enfermedad1,2. Con el avance de la microbiología molecular se ha logrado optimizar el aislamiento de microorganismos en exacerbaciones, las principales bacterias son Haemophilus influenzae, Pseudomonas aeruginosa, Moraxella catarrhalis, Streptococcus pneumoniae y Staphylococcus aureus. Las asociadas a mayor gravedad son P. aeruginosa y H. influenzae. La carga bacteriana se relaciona con el riesgo de exacerbaciones10. Los hongos, virus y micobacterias no tuberculosas (NTM) también pueden tener un papel importante en las exacerbaciones agudas10.
Estos patógenos pueden evadir la respuesta inmunitaria mediante múltiples mecanismos, como la formación de biopelícula y cambios genéticos que confieren resistencia antimicrobiana6. Algunos microorganismos tienen mecanismos adicionales: H. influenzae puede invadir el epitelio de las vías respiratorias y sobrevivir intracelularmente con desregulación inmunitaria secundaria; P. aeruginosa utiliza la IgG del hospedero para bloquear la activación del complemento1,11.
En los pacientes con BQ hay una mayor densidad de macrófagos en esputo. Los macrófagos producen factor de necrosis tumoral alfa (TNF-α), que atrae a los neutrófilos, que son las células predominantes en el esputo, lavado broncoalveolar y en biopsias de pacientes con BQ. Las células epiteliales también participan en la quimiotaxis de neutrófilos mediante la liberación de sustancias proinflamatorias que aumentan la adhesión leucocitaria y la migración transepitelial. Los neutrófilos liberan enzimas que causan lesión en las células epiteliales, reducen la motilidad ciliar, promueven la hiperplasia glandular y el aumento en la secreción de moco. A pesar de encontrarse aumento de los neutrófilos, estos pueden tener una menor actividad fagocítica y microbicida12. La infección persistente perpetúa la inflamación local en los pacientes con BQ (Fig. 1)13.
La fisiopatología de las BQ varía según la causa. En errores innatos de la inmunidad (EII) humoral podemos encontrar deficiencias selectivas de isotipos de Ig, deficiencia de subclases de IgG y síndromes de inmunodeficiencias combinadas, entre otras9,14. La alteración en la producción de Ig predispone a infecciones recurrentes por gérmenes encapsulados y a daño bronquial secundario15,16. Las alteraciones anatómicas o funcionales de la vía respiratoria pueden provocar BQ por depuración deficiente de las vías respiratorias, exceso de secreciones e infección recurrente17. El atrapamiento de moco causa obstrucción y dilatación de las vías respiratorias, un ambiente propicio para la infección12,17.
Manifestaciones clínicas
Los pacientes con BQ se caracterizan por la producción abundante de moco, tos crónica productiva con secreción mucopurulenta de esputo. Tienen infecciones respiratorias recurrentes, esputo fétido, hemoptisis, hipocratismo digital, retraso del crecimiento y deformidad de la pared torácica18. La presencia de bronquitis bacteriana recurrente (más de tres episodios por año) y la necesidad de antibióticos endovenosos pueden ser indicadores de BQ19.
Diagnóstico
El diagnóstico de BQ requiere un alto índice de sospecha y el diagnóstico precoz permite mejorar los desenlaces clínicos, iniciar la terapia temprana y evitar la progresión de la enfermedad20,21.
La aproximación imagenológica inicial se realiza mediante una radiografía de tórax, algunos signos característicos incluyen la visualización de las paredes bronquiales «en carrilera», opacidades tubulares periféricas ramificadas y el signo del «dedo de guante» en casos de dilatación bronquial proximal grave. El diagnóstico objetivo de las BQ se realiza mediante tomografía axial computarizada de alta resolución (TACAR) pulmonar, considerada el método de referencia. Este tipo de tomografía permite un examen más detallado de todo el pulmón, mejorando así la sensibilidad en la detección de BQ. En la TACAR se evalúa el diámetro luminal interno del bronquio en relación con el diámetro externo del vaso sanguíneo adyacente. Una relación bronco: arterial ≥ 1 en adultos y ≥ 0.8 en niños se considera patológica y sugiere la presencia de BQ22,23. El bronquio dilatado adyacente a su rama arterial de menor calibre confiere la apariencia del característico «signo del anillo de sello»24. Algunos signos radiológicos adicionales incluyen la ausencia de estrechamiento de los bronquios y la presencia de bronquios visibles a menos de 1 cm de distancia de la pleura. Puede haber condiciones como el asma y vivir en alturas que aumentan el diámetro intraluminal del bronquiolo y generar falsos positivos, por lo que es fundamental la correlación clínica1,25.
Las BQ se clasifican en tres grupos principales según su morfología macroscópica: cilíndricas, varicosas y quísticas. Sin embargo, esta clasificación tiene poca utilidad diagnóstica debido a que los diferentes tipos suelen coexistir y pueden estar asociados a más de una enfermedad24. El conocimiento de los diferentes tipos de BQ y sus asociaciones con diversas enfermedades es fundamental para establecer un diagnóstico oportuno y un tratamiento adecuado para mejorar la calidad de vida de los pacientes25,26 (Tabla 1 y Fig. 2).
Tabla 1 Principales causas de bronquiectasias en niños
| Enfermedades congénitas o genéticas | Obstrucción endobronquial | Otras causas |
|---|---|---|
| – Fibrosis quística – Discinesia ciliar primaria – Errores innatos de la inmunidad – Deficiencia de alfa-1 antitripsina – Síndrome de Williams-Campbell – Síndrome de Marfan – Malformaciones congénitas del tracto respiratorio (atresia, estenosis, secuestro, quistes, hendiduras, fístulas) – Malacia de las vías respiratorias |
– Infecciones graves (tuberculosis, Staphylococcus spp., gramnegativos – Bronquiolitis obliterante postinfecciosa (virus) – Aspergilosis broncopulmonar alérgica – Cuerpo extraño |
– Aspiración crónica – Alteración en el mecanismo de la tos (enfermedades neuromusculares) – Compresión extrínseca de vías respiratorias (vascular, linfática, tumoral) |
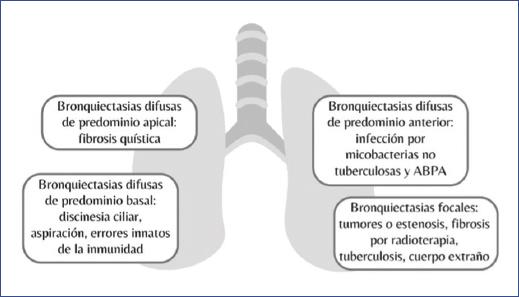
Figura 2 Distribución de las bronquiectasias según su causa. ABPA: aspergilosis broncopulmonar alérgica.
Es importante tener en cuenta que el estudio de las BQ focales requiere una evaluación específica para determinar la causa subyacente. Algunos signos radiológicos característicos incluyen el «dedo de guante» en la radiografía de tórax, que describe la apariencia de BQ focales, y la presencia de broncoceles en casos de retención de secreciones y dilatación importante del bronquio afectado26,27.
El estudio se completa con la tomografía de tórax, los hallazgos en esta pueden ayudar a estadificar la gravedad del compromiso, para ello se han usado las varias escalas. La escala de Reiff modificada evalúa el número de lóbulos afectados (incluida la língula como un lóbulo independiente) y el grado de dilatación (tubular = 1, varicosa = 2 y quística = 3). La puntuación máxima es 18 y la mínima 128. El score FACED consta de cinco variables, incluyendo valores espirométricos, colonización por P. aeruginosa, extensión radiológica y disnea; es efectivo para predecir mortalidad, exacerbaciones y hospitalizaciones29,30. El Bronchiectasis Severity Index (BSI) también se ha validado para predecir mortalidad y exacerbaciones30,31, y para la población pediátrica se modificó al Paediatric Bronchiectasis Severity Index (PBSI)32.
Evaluación inicial
En el caso de un paciente con BQ se deben realizar historia clínica completa y estudios de extensión para evaluar la causa subyacente y determinar la gravedad de la enfermedad (Tabla 2).
Tabla 2 Estudios de evaluación inicial en pacientes con bronquiectasias
| Evaluación mínima |
| Hemograma completo |
| Inmunoglobulinas G, A, M y E |
| Iontoforesis - electrolitos en sudor |
| Cultivo de secreciones de las vías respiratorias |
| Espirometría (generalmente en mayores de 6 años) |
Dada la amplia variedad diagnóstica se debe ser muy cuidadoso en la historia clínica, se debe buscar siempre la causa porque aunque muchos casos se asocian a infección pulmonar previa o son idiopáticos, se pueden encontrar causas tratables como EII, aspiración recurrente o aspergilosis broncopulmonar alérgica33, y resaltamos también que según la región geográfica se debe sospechar tuberculosis o infección por virus de inmunodeficiencia humana (VIH). Para descartar infección/enfermedad por tuberculosis se sugiere realización de prueba de tuberculina, baciloscopias en esputo inducido o jugo gástrico y cultivo. En el caso de sospecha de VIH, será necesaria la toma de serología23.
En todos los pacientes con BQ se debe descartar FQ mediante iontoforesis y de acuerdo con los signos y síntomas considerar estudio genético. Para el abordaje inmunológico se recomienda evaluar la inmunidad humoral, ya que son los defectos predominantes de anticuerpos los EII más frecuentes y los que más se asocian con BQ. Tienen mayor riesgo de BQ cuando hay síntomas pulmonares crónicos y diagnóstico tardío34. Se debe sospechar EII principalmente en pacientes con infecciones sinopulmonares recurrentes; en algunos casos puede haber autoinmunidad, linfoproliferación, alergia o malignidad asociada. Se debe realizar hemograma y medición cuantitativa de Ig G, A, M y E como estudios iniciales. De ser normales las Ig iniciales, se debe considerar realizar estudios más avanzados de defectos específicos de anticuerpos como lo son la respuesta vacunal a antígenos proteicos, polisacáridos y subclases de IgG.
En pacientes con diagnóstico establecido de deficiencia de anticuerpos y BQ la terapia sustitutiva con Ig es fundamental para prevenir nuevas infecciones pulmonares y progresión de las BQ. Se deben mantener niveles de IgG en el umbral fisiológico para la edad del paciente, idealmente > 800 mg/dl siempre y cuando no estén presentando infecciones recurrentes34. Sugerimos además que en todos los pacientes con diagnóstico reciente de defecto de anticuerpos o con antecedente de infecciones respiratorias bajas recurrentes se realice una TACAR al diagnóstico para abordaje de BQ. El seguimiento en estos pacientes se debe realizar sistemáticamente con síntomas y pruebas de función pulmonar, limitando la realización de imágenes a cada 3-5 años o antes en caso de deterioro clínico o deterioro de la función pulmonar por el mayor riesgo de malignidad en esta población.
En casos con sospecha de discinesia ciliar primaria (p. ej., en pacientes con dificultad respiratoria neonatal, rinosinusitis crónica o situs inversus) se puede evaluar la motilidad y ultraestructura ciliar mediante microscopía electrónica, sin embargo se sugiere la realización de panel genético para diagnóstico molecular35.
En algunos niños con predisposición anatómica o factores funcionales que puedan predisponer a broncoaspiración se debe evaluar la deglución, en el caso de que se sospeche reflujo gastroesofágico se recomienda realizar pH-metría36.
La espirometría es útil para evaluar la gravedad de la enfermedad pulmonar30, determinar el grado de obstrucción pulmonar y evaluar la respuesta broncodilatadora, lo cual puede ayudar a diferenciar del asma. Cuando el compromiso es grave puede haber un patrón obstructivo con disminución del volumen espiratorio forzado en el primer segundo con una capacidad vital forzada normal37,38 sin respuesta al broncodilatador. Sin embargo, es importante tener en cuenta que la espirometría puede no detectar daños estructurales tempranos en las BQ37. Algunos pacientes asmáticos pueden desarrollar BQ, particularmente en asma grave de difícil control, lo cual puede empeorar la función pulmonar. Se deben considerar en pacientes asmáticos con enfermedad grave, tos húmeda persistente, esputo purulento, exacerbaciones frecuentes y falta de respuesta al tratamiento39.
Se recomienda realizar cultivo de secreciones respiratorias cada 6 meses, pero pueden ser más frecuentes en pacientes de mayor gravedad o microorganismos resistentes. En caso de exacerbación y deterioro clínico, se debe tomar nueva muestra para dirigir la terapia antibiótica. En pacientes que no pueden expectorar se podría considerar la realización de lavado broncoalveolar. Aunque es infrecuente, la aspergilosis broncopulmonar alérgica puede ser una causa de exacerbación de los síntomas en pacientes con BQ; por lo tanto, ante un deterioro pulmonar sostenido o falta de respuesta al tratamiento médico se sugiere tomar IgE específica para Aspergillus o la realización de pruebas cutáneas para descartarla.
Tratamiento
Los principales objetivos del tratamiento de niños/adolescentes y adultos con BQ son:
- Preservar la función pulmonar y detener la progresión de la enfermedad.
- Optimizar el bienestar y la calidad de vida del paciente y su familia.
- Minimizar la frecuencia y gravedad de las exacerbaciones respiratorias.
- Prevenir complicaciones.
- Optimizar el crecimiento pulmonar.
- Si es posible, revertir la lesión pulmonar estructural21.
Los pilares del tratamiento son los cambios en el estilo de vida (dejar de fumar, realizar ejercicio regularmente y mantener un buen estado nutricional), la vacunación, la realización de terapia respiratoria y el uso temprano de antibióticos en las exacerbaciones25,40,41. En niños, el tabaquismo pasivo o humo de segunda mano se ha relacionado con disfunción de la vía aérea pequeña, lo que podría influir en la fisiopatología de las BQ42. En los pacientes con BQ se sugiere la aplicación anual de vacuna contra la influenza y tener un esquema vacunal completo para neumococo que incluya la aplicación 23 serotipos de S. pneumoniae.
El tratamiento de las BQ tiene como eje fundamental mejorar los mecanismos fisiopatológicos que perpetúan su aparición (Tabla 3). El fortalecimiento de la barrera mucociliar permite disminuir la inflamación y la proliferación bacteriana, y esto se logra mediante las técnicas de limpieza de las vías respiratorias25,41.
Tabla 3 Recomendaciones para el manejo y seguimiento de pacientes con bronquiectasias
| Intervención | Estrategia |
|---|---|
| Inmunización | Calendario regular de vacunación que incluye: difteria, tos ferina, tétanos; sarampión; neumococo conjugado Vacunación contra Haemophilus influenzae tipo b Vacuna anual contra la influenza Vacuna anual contra COVID-19 Vacuna cada 5 años contra neumococo |
| Control ambiental | Evitar el tabaquismo materno y doméstico Minimizar la exposición a la contaminación interior y exterior Prevenir el tabaquismo en adolescentes |
| Actividad física | Los niños y jóvenes de 5 a 17 años mínimo 60 minutos diarios en actividades físicas de intensidad moderada a vigorosa Participación en un programa de rehabilitación pulmonar de 8 semanas |
| Concentraciones de vitamina D | Valores inferiores a 25 ng/ml, recomendamos inicio de suplencia con 200 UI/kg día por 3 meses |
| Técnicas de limpieza de vías respiratorias | Terapia individualizada (revisada 2 veces al año por terapeutas respiratorios expertos en pediatría) Sesiones de limpieza mucociliar duración entre 10 y 30 minutos, dos veces al día (considerar aumento del número de sesiones durante exacerbaciones) |
| Agentes mucolíticos | Previa administración de salbutamol inhalador 400 μg/dosis única N-acetilcisteína Solución salina hipertónica al 3 y 7% |
| Antibioticoterapia empírica en exacerbaciones | – Pacientes sin colonización demostrada por Pseudomonas ⟶ amoxicilina clavulánico/ampicilina sulbactam – Paciente colonizados crónicamente por Pseudomonas ⟶ piperacilina tazobactam, cefepima |
| Terapia de erradicación contra Pseudomonas aeruginosa | – Cultivo de rutina positivo: • Ciprofloxacino oral por 14 días • Tobramicina inhalada por 4 a 12 semanas • Colistina inhalada por 4 a 12 semanas – Cultivo positivo durante exacerbación: • Piperacilina tazobactam • Ceftazidima/cefepima |
| Azitromicina | Pacientes con más de 1 exacerbación hospitalaria o 3 exacerbaciones ambulatorias en el último año Azitromicina 5 mg/kg/dosis (máximo 250 mg) con administración 3 días a la semana durante un periodo de 3 a 6 meses |
- Técnicas de limpieza de vías respiratorias. La terapeuta respiratoria debe enseñar técnicas de higiene bronquial. La técnica dependerá de la edad, comprensión y colaboración del niño35.
No existe una técnica de higiene bronquial perfecta, su elección dependerá de la preferencia del paciente y de la etapa de desarrollo y las capacidades cognitivas del paciente o su cuidador. Se recomienda la terapia individualizada impartida y revisada al menos dos veces al año por fisioterapeutas torácicos capacitados en pediatría20,21. Se recomienda realizar sesiones de limpieza mucociliar que duren entre 10 y 30 minutos, dos veces al día, así como evaluar el drenaje postural según la tolerancia del niño y la ubicación de las BQ. Durante los periodos de exacerbación se debe aumentar la frecuencia de la terapia respiratoria hasta que supere la agudización.
No existen estudios que comparen la efectividad de las técnicas de higiene respiratoria entre sí, a continuación se nombrarán algunas de las más conocidas:
El ciclo activo de técnicas de respiración.
Drenaje autógeno.
Espiración lenta y total con glotis abierta en decúbito lateral.
Dispositivos de presión espiratoria positiva.
Máscara de presión espiratoria positiva.
Dispositivos de presión espiratoria positiva oscilante.
Presión espiratoria positiva oscilante con Flutter, Acapella, Aerobika, REVITIVE, RC-Cornet o lung flute.
Dispositivos de percusión: percutor acústico Vibralung, Frequencer, Dymedso.
Terapia con oscilación de alta frecuencia sobre la pared torácica.
- Actividad física. El ejercicio físico, al igual que la participación en un programa de rehabilitación pulmonar de 8 semanas, podría disminuir la frecuencia de exacerbaciones y mejorar la calidad de vida de los pacientes43.
- Agentes mucolíticos. Las guías internacionales para las BQ no recomiendan uso de ADNasa recombinante en adultos o niños que no tienen FQ20,21,23. La solución salina hipertónica al 3% y concentraciones mayores (hasta 7%) se podría recomendar para humidificar las secreciones previo a realizar la terapia respiratoria con higiene bronquial, sobre todo en pacientes con secreciones viscosas y en quienes se evidencian placas de moco43. También se ha descrito el uso de N-acetilcisteína y manitol en pacientes adultos44,45.
- Terapia antibiótica. En pacientes con BQ y exacerbaciones agudas se recomienda tratamiento sistémico durante 14 días, dirigido según cultivos previos del paciente. En aquellos capaces de expectorar sugerimos que se recolecten muestras de esputo espontáneo o inducido al menos cada 6 meses como medio para identificar nuevos patógenos, específicamente P. aeruginosa, y para ayudar a guiar la terapia antibiótica empírica inicial para exacerbaciones futuras26. La infección bronquial crónica por Pseudomonas se asocia a mayor gravedad clínica, mayor número de exacerbaciones, menor calidad de vida y peor pronóstico46.
Para tratamiento empírico de exacerbación en pacientes NO colonizados por Pseudomonas se sugiere el inicio de amoxicilina/clavulanato a dosis de 90 mg/kg/día por 14 días23; en caso de manejo endovenoso se recomienda ampicilina/sulbactam a dosis de 200 mg/kg/día en 4 dosis.
En caso de primer aislamiento de P. aeruginosa se recomienda realizar terapia de erradicación26. En pacientes asintomáticos se sugiere ciprofloxacino a dosis de 40 mg/kg/día en 2 dosis (máximo 750 mg dosis) por dos semanas con antibiótico inhalado (tobramicina 300 mg cada 12 horas) durante 4-12 semanas. Si al finalizar el tratamiento oral el paciente continúa con cultivo positivo para Pseudomonas, o si el paciente está sintomático se debe considerar, además de la tobramicina inhalada, la administración de antibiótico intravenoso, dentro de lo cual se sugiere como primera línea la administración de piperacilina-tazobactam a dosis de 300-400 mg/kg/día en 4 dosis (máximo 16 g día) o cefepima 150 mg/kg/día en 3 dosis (máximo 6 g/día) por 10-14 días. Se podría adicionar amikacina según gravedad o criterio clínico, también se describe el uso de tobramicina IV en donde tengan disponibilidad; en caso de adicionar el tratamiento es por 10-14 días.
Uso de terapia crónica con macrólidos: la terapia prolongada con macrólidos puede suprimir el crecimiento bacteriano, reducir la inflamación de la vía aérea con menor frecuencia de exacerbaciones, menos síntomas y mejoría de función pulmonar y calidad de vida47. En pacientes con BQ y exacerbaciones recurrentes (más de una exacerbación hospitalaria o tres exacerbaciones ambulatorias en el último año) se sugiere el uso de azitromicina 5 mg/kg/dosis (máximo 250 mg) con administración 3 días a la semana durante un periodo de 3 a 6 meses, con reevaluación periódica para determinar si continúa ofreciendo un beneficio clínico. Se recomienda estudio de esputo previo para descartar infección por NTM23,25,40.
- Esteroides inhalados: no se recomienda la administración sistemática de esteroides inhalados en pacientes con BQ sin asma, ya que no existe evidencia de mejoría de la función pulmonar o menor número de exacerbaciones, y puede asociarse a aumento de la densidad bacteriana23,25.
- Vitamina D: la deficiencia de vitamina D es frecuente en pacientes con BQ y se puede asociar con marcadores de gravedad de la enfermedad pulmonar48. Se sugiere evaluar los niveles de vitamina D en pacientes con BQ y suplementar en caso de estar deficientes.
- Manejo quirúrgico: se debe evaluar manejo con cirugía de tórax en pacientes con las siguientes condiciones43:
•Síntomas persistentes a pesar de recibir tratamiento médico integral durante todo un año.
•Exacerbaciones graves o frecuentes e interfieren con su calidad de vida.
•Hemoptisis de difícil manejo, masiva o recurrente.
•Presencia de un lóbulo/segmento localizado gravemente dañado que puede ser una fuente de sepsis y que puede llevar a la extensión de daño pulmonar.
Conclusiones
El manejo de las BQ no relacionadas con la FQ requiere un enfoque multidisciplinario y personalizado. Las BQ pueden tener múltiples causas, es fundamental aclarar el diagnóstico específico dada la oportunidad de tratar la enfermedad de base en varias condiciones como aspergilosis broncopulmonar alérgica, infección por micobacterias y EII.
La tos crónica húmeda y las infecciones recurrentes son manifestaciones frecuentes, la sospecha diagnóstica es fundamental para el diagnóstico temprano. Los estudios iniciales para el paciente con BQ incluyen hemograma, Ig séricas, iontoforesis, TACAR y pruebas de función pulmonar. Durante el seguimiento de estos pacientes es fundamental la vigilancia microbiológica con cultivos de esputo al menos dos veces al año y se debe hacer seguimiento de la función pulmonar e individualizar nuevas imágenes según la evolución.
Los pilares de tratamiento son la educación del paciente, las técnicas de limpieza de las vías respiratorias y antibioticoterapia ante exacerbaciones o colonización por Pseudomonas; se necesita más investigación para establecer pautas de tratamiento adicionales y más efectivas. Cada paciente debe ser evaluado individualmente y por un equipo multidisciplinario para determinar el enfoque terapéutico más adecuado para su caso particular.