Introducción
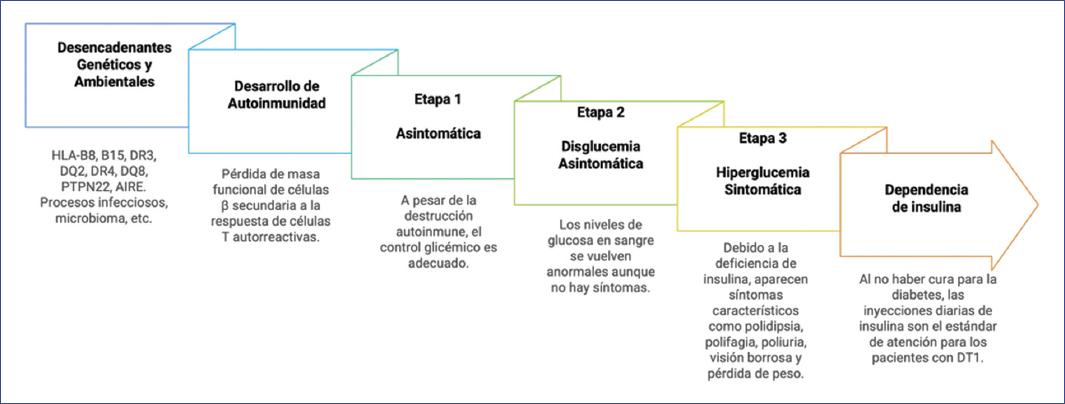
La diabetes tipo 1 (DT1) es una enfermedad crónica autoinmunitaria1 con desencadenantes genéticos y ambientales caracterizada por la pérdida inmunomediada de la masa de células beta pancreáticas, lo que ocasiona un estado de hiperglucemia, la presentación sintomática de la enfermedad y la dependencia de terapia insulínica de por vida. El trastorno es una enfermedad que comienza antes de sus manifestaciones clínicas2.
En su etapa temprana (etapa 1), la DT1 suele ser asintomática, aunque el desarrollo de autoinmunidad suele detectarse en etapas precoces de la vida con autoanticuerpos circulantes dirigidos a la insulina u otras proteínas, como GAD65 asociada al insulinoma 2 (IA2) o transportador de zinc 8 (ZnT8)3. Cuando una gran parte de la masa de células beta se ha vuelto disfuncional o se ha perdido se produce una disglucemia asintomática (etapa 2), y más tarde aparecen síntomas de hiperglucemia (etapa 3) debido a la secreción insuficiente o ausente de insulina. La mayoría de las personas con DT1 en etapa 1 progresarán a etapa 3, aproximadamente el 35% de ellos en los siguientes 5 años, el 70% en 10 años y > 95% a los 15 años4,5 (Fig. 1).
Epidemiología
La prevalencia mundial de la DT1 es del 5-15%, siendo la forma más común de diabetes en niños menores de 15 años; más de 500,000 niños viven con este padecimiento en todo el mundo1. En la actualidad se reporta un aumento constante del 2-5% anual, aproximadamente 90,000 niños diagnosticados con DT1, con una variación significativa de este diagnóstico por regiones6. Los países escandinavos tienen mayor incidencia, seguidos por el Reino Unido, Norteamérica y Australia, asociándose esta alta incidencia principalmente a la «hipótesis de la higiene», que puede explicar el aumento de los casos en los países desarrollados. En México, los datos obtenidos del anuario de morbilidad de 2017 de la Dirección General de Epidemiología reportaron una tasa de incidencia de casos nuevos de 5.45/100,000, mostrando un marcado incremento en la incidencia de 1993 a 20177. Respecto al componente genético, se sabe que los genotipos HLA-DR/DQ varían entre países; en México, el mayor riesgo de desarrollar la enfermedad se asocia a los genotipos HLA-DR3 y DR4, mientras que el haplotipo más fuertemente protector es el DRB1*1402, de origen nativo americano. Se ha reportado que los portadores de DQB1*0302 o DQ8/DQ2 presentan un mayor riesgo para el desarrollo de DT11,8,9.
La DT1 sigue siendo la enfermedad autoinmunitaria más frecuente en pacientes jóvenes, diagnosticada principalmente en niños y adolescentes, pero puede aparecer a cualquier edad. En los adultos, la DT1 de nueva aparición puede diagnosticarse erróneamente como diabetes tipo 210.
Existen factores genéticos desencadenantes de la DT1. Se han reconocido principalmente genes relacionados con la respuesta inmunitaria, sobre todo al complejo principal de histocompatibilidad (MHC), una región poligénica en el cromosoma 6p21.3 que incluye genes que codifican moléculas de antígenos leucocitarios humanos (HLA) de clase I (HLA-A, B y C) y de clase II (HLA-DR, DQ y DP). El papel que tiene su variación genética está relacionado con enfermedades autoinmunitarias en el punto de la presentación de antígenos, interfiriendo en el proceso de tolerancia central y periférica dentro del polimorfismo genético de HLA. Los principales factores de riesgo genéticos asociados son los alelos HLA-B8 y HLA-B15 en la clase I, y los alelos HLA de clase II HLA-DR3, HLA-DQ2, HLA-DR4 y HLA-DQ8 en la clase II. En contraste, los alelos HLA-DR2, HLA-DR5 y HLA-DR7 se han asociado a protección3. Además de los haplotipos HLA relacionados con la enfermedad, se han revelado más de 60 loci no HLA que contribuyen al riesgo de desarrollar DT111. La mayoría de los factores genéticos están relacionados con componentes del sistema inmunitario y solo un número limitado se asocia con la formación de autoanticuerpos dirigidos contra las células beta. El gen que codifica la tirosina fosfatasa linfoide (PTPN22) y el gen de la insulina (INS) parecen influir en el desarrollo de DT1 en el estadio 1. La tirosina cinasa 2 (TYK2), la IFIH1 (interferon induced with helicase C domain 1), la proteína adaptadora SH2B3, la catepsina H, la proteína AIRE (autoimmune regulator), la perforina 1 (PRF1) y el gen FUT2 son relevantes tanto en las células presentadoras de antígeno como en las células T, donde la variación en PTPN22 afecta la señalización del receptor de células T y su activación; también interfiere en la señalización de las células B. TYK2 y PRF1 están implicadas en la regulación de respuestas celulares tras la señalización de citocinas, y SH2B3 en la alteración de la función de células inmunitarias innatas alterando la señalización de citocinas. Las variantes proteicas que afectan a la célula beta son IFIH1, que modula respuestas intracelulares de RNA viral, la variación en TYK2, catepsina H y variaciones que alteran proteínas AIRE y FUT 2 que participan en la selección tímica y la respuesta a infecciones bacterianas o virales3,12.
Además de los factores genéticos, existen numerosos factores ambientales de componente perinatal, como la introducción de alimentos, las infecciones gestacionales y las enfermedades virales, la diversidad del microbioma, entre otros13.
El dato fisiopatológico principal de la DT1 es la pérdida de masa funcional de células beta en los islotes pancreáticos de Langerhans, secundaria a la presentación de autoantígenos por parte de las células presentadoras de antígeno (principalmente células dendríticas) a los linfocitos TCD4+, lo que induce la formación de linfocitos TCD4+ y CD8+ autorreactivos que provocan daño celular tras la activación de macrófagos por parte de las células Th1, la secreción de citocinas y quimiocinas que amplifican el estado inflamatorio y la secreción de gránulos citotóxicos (granzimas y perforinas), así como la secreción de citocinas y la inducción de apoptosis por vía de la expresión de Fas, aunado a una disminución de la actividad de los linfocitos reguladores, lo que favorece un ambiente inflamatorio crónico en los islotes. En la etapa 1 de la enfermedad también se encuentran autoanticuerpos contra antígenos de los islotes pancreáticos, como aquellos dirigidos contra la insulina, GAD65, IA-2, ZnT8, los anticuerpos de las células de los islotes no específicos, el pancreático duodenal 1 (PDX1), la cromogranina A (CgA), la proteína de choque térmico 60 (HSP60) y el antígeno de las células de los islotes 69 (ICA69)14. Sin embargo, se desconoce el punto de origen de estos anticuerpos como reflejo de la presentación de autoantígenos a las células T CD4+ y CD8+ específicas15.
La progresión de la enfermedad de la etapa 1 a la 2 se caracteriza por disglucemia detectada mediante una prueba de tolerancia a la glucosa oral, por la pérdida de la liberación de insulina de primera fase en una prueba de tolerancia a la glucosa intravenosa, o posiblemente por un aumento en los valores de hemoglobina glucosilada (HbA1c), aunque manteniéndose dentro de las cifras normales de referencia. Queda por esclarecer si la disglucemia se debe solo a la disminución de la masa de células beta o si también implica células beta disfuncionales16. Cabría pensar que el inicio clínico de la enfermedad ocurre después de un periodo prolongado de autoinmunidad dirigido contra las células beta, indicado por el infiltrado de linfocitos y células presentadoras de antígeno (CPA) hacia los islotes pancreáticos17.
Complicaciones
La diabetes que no se trata de manera adecuada puede provocar diversas complicaciones, muchas de ellas potencialmente mortales. Las complicaciones agudas incluyen hipoglucemia y cetoacidosis diabética, mientras que las complicaciones a largo plazo son enfermedad cardiovascular, nefropatía y retinopatía diabéticas18. Aunque la hiperglucemia se puede controlar mediante la administración de fármacos o insulina exógena, estos tratamientos no pueden proporcionar una regulación de la glucosa en sangre. Idealmente, un tratamiento viable para la DT1 restablecería tanto la producción de insulina como la regulación de la secreción por la glucosa.
En la actualidad no existe cura para la diabetes y las inyecciones diarias de insulina siguen siendo el estándar de atención para los pacientes con DT1, al ser la opción terapéutica indispensable para el control glucémico19. Sin embargo, conlleva una carga crónica y costosa de atención, y resulta en una disminución general de la expectativa de vida20.
Con poca frecuencia los pacientes con DT1 alcanzan los objetivos glucémicos y de tiempo en rango recomendados, y la hiperglucemia sigue siendo un factor de riesgo para complicaciones metabólicas a corto plazo y para complicaciones macro- y microvasculares a largo plazo1. Además, el uso de insulinoterapia requiere un control glucémico constante y un ajuste de dosis controlado para evitar el riesgo de hipoglucemia. El riesgo de mortalidad por cualquier causa es aproximadamente tres veces mayor para las personas con DT1 con respecto a la población general21, y se ha demostrado que la DT1 está relacionada con problemas cardiovasculares más que cualquier otra enfermedad, incluida la diabetes tipo 222.
En el momento actual, el uso generalizado de dispositivos de autocontrol para medir la glucosa y la HbA1c en sangre ha mejorado la aplicabilidad terapéutica de las preparaciones comerciales de insulina, lo que ha dado lugar a la generación de una gama de análogos de insulina. Dichas preparaciones dependen de sistemas de administración, entre los que se encuentran jeringas, bombas de infusión con sensores de glucosa, inyectores y plumas23. El uso de estos sistemas de administración tradicionales implica un procedimiento invasivo y el tratamiento no proporciona independencia de la insulina a largo plazo24. Con una larga duración de la DT1, la hipoglucemia asintomática se vuelve más común, siendo un factor limitante en el manejo glucémico de la DT1, causando morbilidad recurrente en la mayoría de las personas con DT1 y resultando fatal en algunas ocasiones25.
En consecuencia, se están realizando investigaciones para identificar medios alternativos de terapia de reemplazo de insulina. Si bien el progreso ha sido limitado, el perfil cambiante de una persona con DT1 sugiere que, más allá de asegurar una dosificación exacta de la insulina exógena, el tratamiento eficiente de la enfermedad debe basarse en intervenir de manera temprana, estimular o reprogramar la masa de células beta restante con la finalidad de preservar la secreción de insulina, y reducir el riesgo de complicaciones a largo plazo26.
Secreción de insulina preservada
Uno de los parámetros que más se han revisado para determinar el beneficio clínico de las diferentes inmunoterapias es el grado de secreción de insulina, a través de la medición del péptido C de manera basal o de una prueba de tolerancia a comidas mixtas. Los datos clínicos colectivos sugieren que incluso una secreción mínima de insulina residual proporciona un beneficio clínico a los individuos con DT1. No obstante, los beneficios específicos pueden requerir diferentes umbrales de secreción de insulina.
En el estudio Diabetes Control and Complications Trial (DCCT) se estratificó a un grupo de pacientes de terapia intensiva con insulina según su nivel de péptido C estimulado. Aquellos con un péptido C estimulado > 0.04 nmol/l (0.12 ng/ml) en el momento de ingreso al estudio mostraron un riesgo reducido de retinopatía y de nefropatía diabéticas. Sin embargo, solo aquellos participantes con un nivel de péptido C estimulado > 0.2 nmol/l (0.6 ng/ml) experimentaron una menor frecuencia de hipoglucemia grave4.
En otro análisis de datos del DCCT se encontró que cualquier incremento del péptido C por encima del punto de detección (0.03 nmol/l [0.09 ng/ml]) se asoció con una HbA1c más baja, un menor uso diario de insulina, menos episodios de hipoglucemia y un menor riesgo de retinopatía27.
En la búsqueda de blancos terapéuticos han emergido nuevos abordajes enfocados a la modulación del sistema inmunitario.
Terapias inmunológicas
El objetivo de la inmunoterapia en la enfermedad clínica temprana es preservar la secreción de insulina restante, lo que se asocia con una variabilidad glucémica reducida, un menor riesgo de complicaciones a largo plazo y menos riesgo de hipoglucemia.
La inmunoterapia no cura la DT1, pero numerosas terapias han demostrado el potencial de alterar la evolución natural de la enfermedad. Desde la década de 1980, se han probado docenas de terapias a corto plazo en la DT1 de nueva aparición4.
El aumento del número de casos de DT1 no se puede explicar únicamente por la predisposición genética. Se acepta que una interacción de la susceptibilidad genética y las influencias ambientales es la causa de la activación de las células inmunitarias autorreactivas. En consecuencia, la patogenia de la DT1 implica una interacción compleja de las células beta y los componentes de los sistemas inmunitarios innato y adaptativo.
Los esfuerzos recientes se han concentrado en intervenciones dirigidas a células o citocinas, tratamientos que han tenido éxito en otras enfermedades autoinmunitarias, como el lupus eritematoso sistémico, la artritis reumatoide y la esclerosis múltiple9.
En un intento de bloquear la destrucción inmunomediada de las células beta que ocurre en la DT1, se han probado varios agentes inmunomoduladores e inmunosupresores, solos o en combinación. La mayoría de los estudios se han realizado en pacientes al inicio de las manifestaciones clínicas de la enfermedad, momento en que ya se ha perdido la mayor parte de la masa de células beta, y el parámetro principal a determinar es la preservación de la función residual de dichas células.
Este enfoque ha tenido un éxito limitado a largo plazo, principalmente debido a los importantes efectos inmunosupresores secundarios que han impedido obtener resultados terapéuticos. Entre los abordajes más destacados están la inmunoterapia con anticuerpos humanizados dirigidos a linfocitos (cofactores de la respuesta antígeno-anticuerpo) y la terapia basada en el uso de citocinas o anticuerpos.
Terapias dirigidas a los linfocitos B
En las enfermedades autoinmunitarias se cree que los linfocitos B desempeñan un papel patogénico relevante al fungir como células presentadoras de antígenos que participan en la activación de los linfocitos T, que son los mediadores de la destrucción autoinmunitaria. Las terapias dirigidas a los linfocitos B han demostrado efectos beneficiosos en el ratón diabético no obeso (NOD), el modelo animal más ampliamente utilizado para el estudio de la DT128. Se propone que estos abordajes reducen la interacción de los linfocitos B y los linfocitos T, disminuyendo así la respuesta autorreactiva de estos últimos y preservando la función de las células beta en los pacientes con DT1 de aparición reciente.
Anti-CD20: rituximab
Pescovitz et al.28 realizaron un ensayo aleatorizado de fase 2 con rituximab (un anticuerpo monoclonal quimérico dirigido contra el marcador CD20 expresado en las células B), en el cual se asignaron aleatoriamente 87 sujetos (de 8 a 40 años) para recibir cuatro infusiones de rituximab o placebo en los días 1, 8, 15 y 22 del estudio. Se realizó un seguimiento cada 6 meses hasta los 30 meses posteriores. Este estudio comparó los niveles de péptido C y se halló un incremento en el grupo tratado con rituximab en comparación con el grupo que recibió placebo. El seguimiento de los sujetos se realizó con la medición de péptido C posterior a una prueba de tolerancia a comidas mixtas, y se observó que la tasa de caída del péptido C fue paralela a la caída observada en el grupo de control. Esto sugiere que el rituximab no alteró fundamentalmente la fisiopatología subyacente de la enfermedad. Sin embargo, el tratamiento temprano con rituximab sí retrasó (8.2 meses) la caída en el péptido C en comparación con el grupo de control, lo que resultó en una mayor preservación general de la función de las células beta en todos los puntos temporales. Aunque los niveles de péptido C y de HbA1c, y la dosis de insulina por kilogramo de peso, tendieron a ser más favorables en el grupo tratado con rituximab que en el grupo placebo, se encontró una disminución de este efecto en el seguimiento a 2 años. La caída paralela en los niveles de péptido C puede reflejar la reanudación de la destrucción en curso de las células beta mediada por el sistema inmunitario, aunque sin un verdadero marcador de la respuesta autoinmunitaria28,29. Respecto a la seguridad del anticuerpo, los efectos secundarios más frecuentes ocurren en el momento de la infusión, destacando la aparición de fiebre, escalofríos y eritema. Entre los efectos hematológicos, la linfocitopenia es el más importante. También cabe destacar la susceptibilidad a infecciones. Una indicación para suspenderlo es la reactivación de hepatitis B y el desarrollo de leucoencefalopatía multifocal progresiva debido al virus de John Cunnigham30. Igualmente, durante el estudio se encontró que los niveles de inmunoglobulina (Ig) M disminuyeron en el grupo de rituximab, un efecto que persistió al año. Aunque ningún paciente requirió tratamiento para hipogammaglobulinemia, resulta relevante en la valoración del riesgo/beneficio de la terapia29.
Se reconoce que el rituximab retrasa la caída del péptido C, pero no parece alterar fundamentalmente la fisiopatología subyacente de la enfermedad. Se siguen realizando estudios de terapias combinadas, con resultados prometedores. Por ejemplo, un ensayo clínico aleatorizado de fase 1/2, con seguimiento a 12 y 24 meses, en pacientes pediátricos con DT1 de reciente diagnóstico (etapa 1), exploró la eficacia y la seguridad del tratamiento combinado con células T reguladoras autólogas expandidas (CD4+ CD25highCD127) y rituximab29. Los pacientes fueron asignados a tres grupos: uno tratado solo con células T reguladoras (n = 13), otro tratado con células T reguladoras y rituximab (n = 12) y un grupo de control (n = 11). Los análisis de eficacia clave fueron los niveles de péptido C (prueba de tolerancia a comidas mixtas) y la proporción de pacientes en remisión a los 12 y 24 meses. En el grupo que recibió la terapia combinada se observaron más pacientes en remisión en los meses 3, 6, 9 y 21, en comparación con el grupo de control. Sin embargo, esa diferencia se perdió en los meses 18 y 24. En el grupo que solo recibió células T reguladoras no se encontraron diferencias significativas. Durante el estudio ocurrieron eventos adversos en el 80% de los pacientes, principalmente en el grupo de terapia combinada y en el grupo tratado con células T reguladoras; no obstante, ningún evento adverso condujo al retiro de la intervención ni a la muerte29. Por lo tanto, el uso de rituximab en combinación con otras terapias biológicas puede ser una opción que amplíe su eficacia.
La eficacia limitada del rituximab en el tratamiento de la DT1 podría estar asociada a ciertos perfiles de células T y B. En un estudio de 2 años de seguimiento, mediante citometría de flujo, se evaluaron 32 marcadores de células T y B de sangre periférica y se encontró una mayor expresión del receptor PD-1 en las células T, expresión que se correlacionó con un mayor nivel de péptido C y una dosis diaria reducida de insulina en los pacientes tratados con rituximab31. En otro estudio de expresión génica se identificaron las firmas transitorias de individuos tratados con rituximab, y se encontró reducida la expresión de algunos genes relacionados con las células B y un incremento relativo de los genes de células T a las 26 semanas posteriores al tratamiento, lo que predijo una progresión más rápida de la DT132. Este incremento relativo de las células T autorreactivas condicionaría una mayor destrucción autoinmunitaria de las células beta, con la consecuente pérdida de la capacidad de producción de péptido C.
Terapias dirigidas a los linfocitos T
Anti-CD3: teplizumab
El teplizumab es un anticuerpo monoclonal de IgG1 humanizado que se une con alta afinidad a la cadena épsilon de CD3. Los primeros estudios de su mecanismo de acción mostraron que el agonismo parcial del teplizumab condujo a efectos sobre las células T CD8+ relacionadas con la destrucción autoinmunitaria de las células beta pancreáticas33.
En 2002 se realizó un primer ensayo clínico aleatorizado de fase 2 que evaluó la seguridad, la tolerabilidad y la eficacia del teplizumab, administrado como un ciclo único de 12 o 14 días, en comparación con el estándar de atención en pacientes (n = 12) con DT1 de reciente diagnóstico, en estadio 3 de la enfermedad. El tratamiento con el anticuerpo monoclonal mantuvo o mejoró la producción de insulina después de 1 año en 9 de los 12 pacientes del grupo de tratamiento, mientras que solo 2 de los 12 controles tuvieron una respuesta sostenida con aparente seguridad. Los efectos adversos más notables fueron fiebre, anemia y exantema34.
Por otra parte, en el ensayo clínico de fase 2 abierto del grupo AbATE se evaluó el tratamiento con una dosis anual de teplizumab durante 2 años en pacientes con reciente diagnóstico de DT1. Se evalúo el estado clínico, inmunitario y metabólico de los pacientes después de un seguimiento promedio de 7 años (n = 43). Se determinaron los niveles de péptido C en respuesta a una prueba de tolerancia a comidas mixtas. Los pacientes respondedores tratados con el fármaco mejoraron significativamente y presentaron una menor pérdida de péptido C. Sin embargo, las mejoras en la respuesta del péptido C no se asociaron con niveles más bajos de HbA1cni con menos requerimientos diarios de insulina35,36.
En el ensayo aleatorizado de fase 3 Protége se probaron dos ciclos de 12 días de teplizumab o placebo, y se evaluaron la preservación de las células beta y la seguridad. Se valoraron los cambios en los niveles de péptido C a la semana 78. Participaron en el ensayo pacientes de ambos sexos, de 8 a 17 años de edad, con diagnóstico reciente de DT1 en etapa 3 (n = 318 pacientes). Este ensayo demostró beneficios con respecto a la preservación de la función de las células beta, con unos niveles de péptido C significativamente más altos en el grupo tratado con teplizumab en comparación con los pacientes que recibieron placebo37.
Para confirmar la consistencia de la preservación de las células beta, se han realizado diversos metaanálisis integrando los datos del péptido C. En un metaanálisis de cinco ensayos clínicos realizado por la American Diabetes Association se valoraron los cambios en los niveles de péptido C y el uso de insulina exógena. Se incluyeron los datos de 375 pacientes con diagnóstico de DT1 en etapa 3 tratados con teplizumab. Además, se realizó un análisis de seguridad con los datos de aproximadamente 1500 pacientes en 1 año de seguimiento38. Los resultados confirmaron la consistencia en la preservación de la función de las células beta, medida por el nivel de péptido C detectado. El perfil de seguridad del teplizumab mostró que los eventos adversos más comunes fueron linfocitopenia, erupción cutánea y dolor de cabeza; la mayoría ocurrieron durante y después de las primeras semanas de administración de teplizumab y generalmente se resolvieron sin intervención, lo que concuerda con el perfil de seguridad caracterizado por eventos adversos autolimitados en ensayos con uno o dos ciclos de tratamiento con teplizumab36.
Un metaanálisis realizado en 2024 incluyó ocho ensayos controlados aleatorizados con 1052 pacientes, de los cuales 754 recibieron teplizumab. Este tratamiento aumentó significativamente los niveles de péptido C a los 6, 12, 18 y 24 meses de seguimiento, reduciendo también de manera significativa los niveles de HbA1c y los requerimientos de insulina a los 6 y 12 meses39.
En noviembre de 2022, el teplizumab (Tzield, Provention Bio, Inc., Sanofi, Red Bank, NJ, USA) se convirtió en el primer fármaco aprobado para cambiar la progresión de la autoinmunidad en la DT1, al lograr retrasar la progresión de la enfermedad a estadio 3 en adultos y niños ≥ 8 años con enfermedad en estadio 234. Sin embargo, la disponibilidad del medicamento y la complejidad que conlleva la detección temprana de DT1 en la población requieren programa de detección eficaz que permita identificar a los individuos en riesgo, y educar a los proveedores de atención médica sobre las etapas de la DT1 y la población en riesgo.
Ig CTLA4: abatacept
También se ha explorado la inmunomodulación sin agotamiento con el bloqueo de CD80 y CD86 utilizando un anticuerpo acoplado a CTLA-4 (Ig-CTLA-4), el abatacept, el cual modula selectivamente una de estas dos vías, uniéndose a los receptores CD80 y CD86 de las células presentadoras de antígeno, bloqueando selectivamente la interacción de los receptores CD80/CD86 con CD28, e inhibiendo la activación y la proliferación de las células T, así como la respuesta de las células B. Es importante resaltar que existen otras señales coestimuladoras diferentes de CD80/86 que no se ven afectadas por Ig CTLA-4.
El uso de abatacept ya ha dado resultados en la normalización de mediadores inflamatorios en pacientes con artritis reumatoide40. En ratones NOD prediabéticos, el abatacept previno la diabetes autoinmunitaria cuando se administró antes del inicio de la hiperglucemia, pero los efectos dependieron del estadio de la enfermedad41.
Por otro lado, en un ensayo clínico controlado, aleatorizado y doble ciego, en el que se probó el abatacept con la hipótesis de que al bloquear la coestimulación y limitar el número de linfocitos autorreactivos se podría preservar la secreción de péptido C, se incluyeron 112 pacientes de entre 6 y 45 años con diagnóstico reciente de DT1 y niveles estimulados de péptido C ≥ 2.0 pmol/ml. Los pacientes fueron asignados aleatoriamente para recibir abatacept (10 mg/kg, máximo 1000 mg por dosis) o infusiones de placebo. Los resultados mostraron que los niveles de péptido C fueron un 59% mayores en los pacientes tratados con abatacept a los 2 años de seguimiento. Además, estos se mantuvieron en promedio 9.6 meses antes de decaer. No se encontraron diferencias entre los efectos adversos asociados a la infusión. A pesar de la administración continua de abatacept durante 24 meses, la disminución de la función de las células beta fue paralela a la observada con placebo después de 6 meses de tratamiento, por lo que se propone que la activación de los linfocitos T tiende a disminuir de manera natural con el tiempo, más allá del efecto del fármaco42.
En otro ensayo de fase 2 con abatacept, aleatorizado, controlado, con 112 participantes con anticuerpos positivos y tolerancia normal a la glucosa que recibieron infusiones mensuales de abatacept o placebo durante 12 meses, el grupo de abatacept mostró mayores niveles de péptido C en respuesta a una prueba de tolerancia a comidas mixtas, un incremento en el porcentaje de células T CD4+ vírgenes y una disminución de células T reguladoras y T foliculares PD1+ICOS+. A pesar de que el efecto sobre los subconjuntos de células T desapareció en los 12 meses posteriores al tratamiento, el hecho de que se preservara la secreción de insulina sugiere una modificación de la progresión de la enfermedad. No obstante, se requieren más estudios sobre el efecto del abatacept para evaluar su efecto inmunosupresor y su eficacia a largo plazo. Respecto a la seguridad del abatacept, en este estudio se notificaron cinco eventos adversos graves, así como un aumento de lesiones cutáneas y del tejido conectivo, en comparación con el grupo que recibió placebo43.
Globulina antitimocítica
Una de las terapias inmunológicas que ha demostrado potencial para preservar el péptido C en la etapa 3 es la globulina antitimocítica (ATG) a dosis baja (2.5 mg/kg). La ATG es una IgG policlonal contra múltiples antígenos de células T humanas (CD2, CD3, CD4, CD8, CD11, CD18 y CD25) y sus precursores, como los timocitos dobles negativos, que se utiliza principalmente en el rechazo de injerto agudo e hiperagudo.
En un ensayo de fase 2b aleatorizado, doble ciego, realizado en pacientes con DT1 en etapa 3 (n = 89), se formaron grupos al azar para recibir ATG sola o ATG con factor estimulador de colonias de granulocitos. Se observó que dosis bajas de ATG retardan la disminución del péptido C y reducen el porcentaje de HbA1c en personas con DT1 reciente. Sin embargo, la adición de factor estimulador de colonias de granulocitos no contribuyó a la conservación del péptido C lograda con ATG44.
En una serie de casos se evaluó la eficacia de la ATG en 6 pacientes con DT1 en etapa 2, con el objetivo de valorar la factibilidad de retrasar la progresión de la enfermedad a etapa 3. Tres de los pacientes permanecieron libres de diabetes después de 1 y 5 meses, y a los 3 y 4 años de seguimiento, mientras que los otros tres evolucionaron a la etapa 3 dentro de los primeros 2 meses posteriores a la terapia. Dieciocho meses después del tratamiento, incluso aquellos con progresión de la enfermedad mostraron una HbA1c casi normal (5.1-5.6%) y tenían bajos requerimientos de insulina (0.17-0.34 U/kg al día). Los niveles de péptido C aumentaron (1.3-1.4 ng/dl) en respuesta a una prueba de tolerancia a comidas mixtas45.
Son necesarios estudios adicionales para comprender mejor qué individuos tienen más probabilidades de responder a la terapia. Además, se debe evaluar el perfil de seguridad e inmunitario a largo plazo, aun cuando los efectos adversos fueron leves (cefalea, náuseas, vómito, etc.) tras la infusión.
Terapias dirigidas a las citocinas
Las citocinas desempeñan un papel relevante dentro de la DT1 favoreciendo o inhibiendo múltiples respuestas celulares entre las células beta pancreáticas y las células de la respuesta inmunitaria. Por ello, desde modelos animales hasta ensayos clínicos en humanos, se han probado como probables blancos terapéuticos en la enfermedad citocinas clásicas de la respuesta tanto antiinflamatoria (interleucina [IL] 2, IL-10, factor de crecimiento transformador beta) como proinflamatoria (IL-1, IL-6, factor de necrosis tumoral alfa [TNF-α]). Se conoce que la IL-1β induce disfunción y muerte de las células beta al favorecer la activación de Fas46.
En dos ensayos controlados aleatorizados doble ciego se aplicó el tratamiento con un anticuerpo monoclonal anti-IL-1 (canakinumab) en dosis mensuales de 2 mg/kg por 12 meses, y de un antagonista del receptor de IL-1 (anakinra) en dosis diarias de 100 mg durante 9 meses, para evaluar si había mejoría de la función de las células beta. Se incluyeron 70 pacientes con diagnóstico reciente de DT1. Dicho abordaje no logró cumplir con el resultado primario de protección funcional de las células beta. Sin embargo, un subanálisis mostró una función residual basal de células beta y una capacidad secretora de insulina 2.5 veces mayor en los pacientes tratados con anakinra y canakinumab. El canakinumab y el anakinra resultaron tratamientos de bajo riesgo, pero no efectivos como fármacos inmunomoduladores individuales en la DT1 de reciente aparición, debido a que los niveles de péptido C en los grupos de canakinumab y de placebo a los 12 meses fueron de 0.01 nmol/l, y en los grupos de anakinra y de placebo fueron de 0.02 nmol/l47.
Por otro lado, el TNF-α, que regula positivamente las moléculas MHC-I, favorece la presentación de autoantígenos a las células T CD8+ y acelera así la apoptosis de las células beta46. Con el objetivo de probar el etanercept, una proteína de fusión del receptor TNF-α que elimina al TNF-α de la circulación y bloquea su actividad, se realizó un estudio doble ciego, aleatorizado y controlado con placebo, de 24 semanas de duración, en 18 pacientes de 7 a 18 años de edad con diagnóstico reciente de DT1 (etapa 3). En el estudio se halló una disminución de la HbA1c en el grupo de pacientes tratados con etanercept en comparación con el grupo que recibió placebo48.
Más recientemente, para probar si el golimumab (un anticuerpo monoclonal humano anti-TNF-α) tiene eficacia para preservar las células beta, se realizó un estudio de fase 2a, doble ciego y controlado con placebo, en el que los pacientes con diagnóstico reciente de DT1 en etapa 3 recibieron golimumab durante 52 semanas. Los participantes tratados con golimumab tuvieron menos requerimientos de insulina y menores tasas de hipoglucemia, así como proporciones mayores de proinsulina/péptido C, en comparación con el grupo placebo49.
Otro de los abordajes probados es el bloqueo de la IL-21, citocina producida principalmente por los linfocitos T foliculares que ha sido estudiada por su papel como inductor de la progresión de la enfermedad y la producción de IL-6, lo que a su vez favorece la proliferación de células Th17 y el ataque por parte de las células CD8+46. El uso de anti-IL-21 en combinación con liraglutida (análogo del péptido-1 similar al glucagón) se ha probado como una nueva estrategia para modificar el curso de la enfermedad en la DT1 al retrasar el proceso inmunitario, preservando y mejorando la función residual de las células beta4.
En un ensayo clínico de fase 2 se evaluó la elegibilidad de 553 adultos, de los cuales 308 fueron asignados aleatoriamente para recibir los siguientes tratamientos: anti-IL-21 más liraglutida, anti-IL-21, liraglutida o placebo. Los resultados mostraron que los niveles de péptido C estimulados por una prueba de tolerancia a comidas mixtas, desde el valor inicial hasta la semana 54, fueron significativamente menores con el tratamiento combinado, pero no así en el grupo de pacientes tratados solo con anti-IL-21 o con liraglutida. A la semana 54 de seguimiento, los niveles de péptido C fueron mayores con todos los tratamientos activos en comparación con el placebo. Respecto a la seguridad, los eventos adversos más frecuentes fueron trastornos gastrointestinales. La tasa de eventos hipoglucémicos no difirió significativamente entre los grupos de tratamiento activo y de placebo50.
Otras terapias farmacológicas
En estudios previos, dentro de los diferentes enfoques inmunológicos para el tratamiento de la DT1, se consideró el uso de fármacos como el micofenolato de mofetilo, el cual se absorbe rápidamente después de su administración oral y se hidroliza a ácido micofenólico, que inhibe de manera selectiva y reversible a la inosina monofosfato deshidrogenasa, que a su vez inhibe la síntesis de novo de nucleótidos de guanosina sin incorporación al ADN, actuando como inmunosupresor de los linfocitos T y B que dependen de la síntesis de purinas para su proliferación. Por lo tanto, el micofenolato de mofetilo tiene potentes efectos citostáticos sobre los linfocitos y es eficaz en enfermedades autoinmunitarias como la psoriasis. En un estudio para determinar su efecto, ya sea solo o combinado con daclizumab (anticuerpo monoclonal humanizado dirigido contra IL-2), sobre la progresión de la destrucción de células beta en pacientes con DT1 de reciente diagnóstico (3 meses), se estudió la respuesta a una prueba de tolerancia a comidas mixtas en un grupo de 126 pacientes, de entre 8 y 45 años, con niveles de péptido C > 0.2 pmol. En el estudio se administró micofenolato de mofetilo o placebo diariamente a dosis de 600 mg/m2 dividida en 2-3 dosis diarias, durante 2 años, y daclizumab o placebo en infusión intravenosa el día 0 del estudio y 2 semanas después en una dosis de 1 mg/kg. Los grupos de pacientes tuvieron un seguimiento mínimo de 2 años, tras los cuales los valores de péptido C no se vieron afectados por el micofenolato de mofetilo solo ni en combinación con daclizumab. Por lo tanto, no hubo efecto en la preservación de la función de las células beta. Respecto a su seguridad, se informaron 28 (34%) eventos adversos graves en el grupo de pacientes tratados con micofenolato de mofetilo y daclizumab; entre ellos, destaca la presencia de neutropenia y leucocitopenia, así como 27 eventos de hipoglucemia51.
Terapias basadas en trasplante celular
Otra estrategia que ha sido evaluada en la búsqueda de mejores aplicaciones terapéuticas es el trasplante.
Alotrasplante de islotes
El trasplante de páncreas completo es una estrategia que ha mejorado con el paso de los años y proporciona un buen control glucémico; sin embargo, es un procedimiento invasivo. El trasplante de células de islotes surge como una solución prometedora que proporciona independencia de la insulina con normalización de la HbA1c y un riesgo quirúrgico mínimo52. Dentro de los tipos de trasplantes, el alotrasplante de islotes consiste en el aislamiento de los islotes mediante digestión enzimática y la infusión de estos en la vena porta (5000 islotes/kg de peso). El protocolo Edmonton es el primero exitoso y constituye el estándar actual en el trasplante de islotes. En un ensayo multicéntrico se realizó un estudio retrospectivo de 255 pacientes sometidos a trasplante de islotes. Durante un seguimiento promedio de 7.4 años, sobrevivieron 230 pacientes (90%). La supervivencia media del injerto fue de 5.9 años y se produjo un fallo del injerto en el 36% de los pacientes. El 70% de los receptores tuvieron una supervivencia mantenida del injerto. Estos tuvieron tasas significativamente más altas de independencia de insulina y mejoras mantenidas en el control glucémico, en comparación con aquellos con supervivencia no mantenida del injerto. Los análisis multivariados identificaron que el uso combinado de anakinra más etanercept está asociado con la supervivencia del injerto53,54.
Se ha demostrado que el alotrasplante de islotes aumenta la calidad de vida de los pacientes al mejorar el control glucémico, reducir la necesidad de suplementación externa con insulina y disminuir las complicaciones microvasculares. Sin embargo, también existen complicaciones por la cirugía mínimamente invasiva y los efectos secundarios de la inmunoterapia a largo plazo53.
Xenotrasplante de islotes
La dificultad para conseguir donadores de islotes ha llevado al planteamiento de nuevas estrategias, como el xenotrasplante de injertos de islotes porcinos. El principal desafío con este tipo de trasplante es la respuesta inmunitaria contra los xenoantígenos, como la galactosa-α1,3-galactosa (Gal) y el ácido N-glicolil neuramínico (Neu5Gc) específicos de las células endoteliales porcinas, además del riesgo de transmisión de retrovirus endógenos porcinos. No obstante, en estudios clínicos en primates no humanos, el xenotrasplante de injertos islotes porcinos logra mantener la normoglucemia en sujetos con diabetes inducida químicamente, y la supervivencia del injerto fue de casi 2 años55.
Trasplante de islotes derivados de células madre
El uso de células madre es una estrategia que ha cobrado fuerza en los últimos años. Entre las variantes utilizadas se encuentra el trasplante de células madre embrionarias (ESC, embryonic stem cells), que por sus capacidades pluripotenciales pueden producir células de cualquier linaje. El conocimiento de las señales del páncreas y de las células beta permite un mejor control de las señales que las ESC necesitan para diferenciarse en células beta productoras de insulina tras un proceso de diferenciación progresiva en el endodermo. El análisis de la transcriptómica del injerto de células beta derivadas de ESC en modelos murinos ha permitido optimizar los procesos de maduración, y mostrar la necesidad del microambiente pancreático para lograr una maduración adecuada56. Aunque ha habido grandes avances en estos aspectos técnicos, todavía existen problemas éticos respecto a la recolección de embriones humanos.
Células madre pluripotentes inducidas
El uso de células madre pluripotentes inducidas (iPSC, induced pluripotent stem cells) y de células madre adultas es de gran interés en la producción de células beta para la terapia de reemplazo de islotes. Las iPSC obtenidas a partir de células adultas expuestas a los denominados factores de Yamanaka (genes maestros Oct4, Sox2, Klf4 y c-Myc) tienen la capacidad para diferenciarse en células endodérmicas, mesodérmicas y ectodérmicas. A diferencia del uso de ESC, no existe el dilema ético de la necesidad de embriones, y además evitan el ataque autoinmunitario, lo que las hace útiles para el autotrasplante; no obstante, su uso enfrenta desafíos como la inestabilidad genética para la diferenciación y una menor eficacia que las ESC. La optimización del proceso de diferenciación de las células madre en células beta se basa en gran medida en la expresión de genes específicos de la célula beta y en su capacidad para responder a la glucosa. Sin embargo, esta respuesta sigue siendo inferior a la obtenida con el trasplante de islotes57.
Células madre mesenquimales
Otro tipo de células que ha originado interés para la generación de células beta son las células madre mesenquimales multipotentes (MSC, mesenchymal stem cells). Las MSC se pueden aislar de la médula ósea, el cordón umbilical y el tejido adiposo. Ofrecen la ventaja de superar el riesgo de rechazo inmunitario y no tienden a formar teratomas. Además, secretan muchos factores de crecimiento que ayudan a la supervivencia de las células circundantes. Se ha demostrado que tienen propiedades inmunomoduladoras a través de la supresión de la proliferación de células T mediante la inhibición del interferón gamma y del TNF-α, y la regulación positiva de la IL-10. Se ha experimentado con ellas tanto para producir células beta derivadas como para la inducción de cofactores junto a islotes derivados de iPSC. Las MSC muestran un impacto significativo en la terapia de reemplazo de células beta cuando se trasplantan junto con células beta, mejorando la supervivencia del injerto53.
Los efectos beneficiosos de las MSC en la DT1 se pueden atribuir a la IL-4 secretada y a la inducción de la maduración de células T naive hacia Th2. Además, las MSC pueden inhibir de manera directa e indirecta a través de diferentes vías, como la producción de IL-17 o la inducción de apoptosis de células beta mediada por Fas, o alterando la maduración y la activación de células presentadoras de antígeno, principalmente células dendríticas, mediante la secreción de prostaglandina E2, IL-6 y factor estimulante de colonias de macrófagos58,59.
En diferentes experimentos se han usado MSC cocultivadas con islotes de ratones o de humanos. En uno de ellos diseñaron MSC para expresar PD-L1 y CTLA-4 con el fin de mejorar aún más sus efectos inmunoprotectores. Las MSC ofrecieron un efecto protector local y mejoraron de manera significativa la viabilidad y la función de los islotes durante un máximo de 100 días cuando se trasplantaron conjuntamente en la cápsula renal de ratones diabéticos sin inmunosupresión, en comparación con las MSC de tipo salvaje. Las MSC rescataron los niveles de glucosa en sangre en ratones diabéticos y redujeron significativamente la presencia de células T efectoras en el sitio del trasplante, retrasando el rechazo del injerto60.
En una comparación de los resultados de los estudios clínicos disponibles, las terapias con MSC derivadas de tejido adiposo y de médula ósea son muy controvertidas, lo que sugiere que pueden ser menos efectivas que la terapia con MSC derivadas de cordón umbilical (gelatina de Warthon) en la DT1. En un estudio prospectivo, no aleatorizado, con 53 participantes, de los cuales 33 tenían diagnóstico de DT1 de inicio en la edad adulta y 20 de inicio en la juventud, se infundieron MSC de cordón umbilical de donantes sanos en dos ciclos separados por 3 meses. Después de 1 año de seguimiento, en el 40.7% de los sujetos del grupo tratado con MSC los niveles de péptido C fueron significativamente más altos que en el grupo de control. Tres sujetos del grupo tratado con MSC, y ninguno del grupo de control, lograron independencia de la insulina y se mantuvieron libres de insulina durante 3 a 12 meses. No hubo diferencia en los niveles de péptido C entre los grupos de pacientes con DT1 en cuanto a la edad de diagnóstico61.
Inmunización
Otro de los abordajes en auge es la inmunoterapia específica de antígeno, que consiste en la administración de autoantígenos por diferentes vías (insulina completa, proinsulina o péptidos relacionados con los islotes, como GAD65 o HSP60) con la finalidad de inducir tolerancia específica de las células T CD4+ y CD8+ para prevenir la activación de células T naive con potencial autorreactivo62,63.
Por sus características tolerogénicas, las vías preferentes para la administración son la oral y la intranasal. Los primeros estudios en modelos preclínicos sugieren que la insulina oral o nasal podría tener eficacia en la prevención de la diabetes autoinmunitaria, y hallazgos posteriores señalan que una mejor opción de antígeno podría ser la prohormona proinsulina, como un objetivo inmunogénico más temprano. Un análisis post hoc de un gran ensayo clínico, en el que se usaron 7.5 mg diarios de insulina oral en niños en riesgo de padecer la enfermedad, propone que la inmunización con insulina podría reducir la progresión de la enfermedad63. Los estudios también indican que podría ser necesaria la administración oral de dosis altas de insulina (67.5 mg) para inducir tolerancia inmunitaria. Los modelos preclínicos plantean que una dosificación frecuente o alta de antígeno podría funcionar eliminando las células T autoinmunitarias efectoras, mientras que una dosificación más baja y escalonada tendría un potencial mayor efecto sobre las vías reguladoras64.
Un ejemplo de estudio de prevención primaria es el ensayo clínico aleatorizado Pre-POINT, en el cual la administración de insulina oral (67.5 mg/día) condujo a una respuesta inmunitaria reguladora sin hipoglucemia en niños con alto riesgo de DT1, que no presentaban signos de autoinmunidad de los islotes, lo que indica una inducción exitosa de la tolerancia oral65.
Además, se han probado otras estrategias de administración de péptidos para favorecer las vías reguladoras. En un estudio se administró péptido de proinsulina por vía parenteral poco después del diagnóstico de DT1, y la retención de péptido C en los participantes tratados se asoció con la producción de IL-10 estimulada por proinsulina, con una mayor expresión de FOXP3 por Treg y unos niveles basales bajos de células T citotóxicas específicas62.
Para determinar si la proinsulina era la causante de la preservación del péptido C, se realizó un estudio en el que se aplicó por vía intramuscular un plásmido de ADN modificado que codifica para la proinsulina en un grupo de 80 pacientes con DT1 (etapa 3). Los resultados mostraron que los niveles de péptido C mejoraron con todas las dosis (0.3-6.0 mg) en relación con el grupo que recibió placebo, y no se reportaron eventos adversos66.
Con respecto a GAD65, este se ha aplicado en forma de conjugado con aluminio para inducir una contrarregulación del proceso autoinmunitario patológico, mediante la inducción de un perfil Th2, evitando la destrucción de las células beta. Sin embargo, aún no se ha logrado establecer su eficacia en la experimentación clínica67.
Otro de los autoantígenos objeto de estudio es DiaPep277, un péptido de 24 aminoácidos derivado de la proteína Hsp60. Un estudio clínico multinacional (DIA-AID 1) de fase 3, aleatorizado, equilibrado, doble ciego, controlado con placebo y de grupos paralelos, evalúo la seguridad y la eficacia de DiaPep277 en la preservación de la producción de insulina, en un grupo de 457 pacientes de entre 6 y45 años de edad con diagnóstico de DT1 en etapa 3. Se les administró DiaPep277 subcutáneo o placebo de manera trimestral por 2 años. El estudio concluyó que el péptido fue bien tolerado y de bajo riesgo, pero no mostró diferencias significativas en la preservación del péptido C en comparación con el grupo que recibió placebo68.
Los estudios en el campo de las terapias específicas de antígenos aún necesitan optimizar la dosificación y vincularse a biomarcadores que evalúen el tratamiento y su funcionalidad en las diferentes etapas de la enfermedad, con el fin de consolidar su potencial uso (Fig. 2). No obstante, los avances y la optimización de estos son considerables.
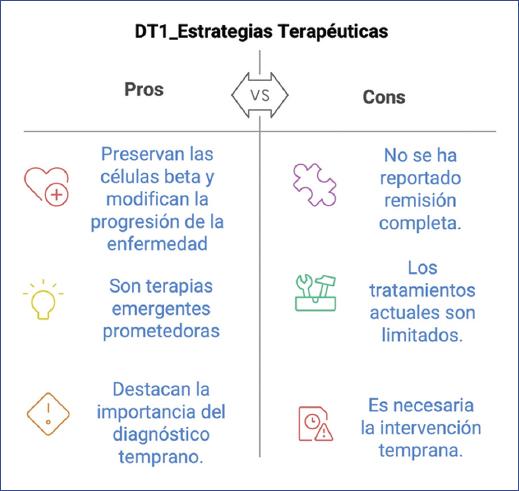
Figura 2 Descripción general de las ventajas y desventajas de las actuales estrategias terapéuticas para la diabetes tipo 1.
En la tabla 1 se hace una comparación de las terapias abordadas en esta revisión.
Tabla 1 Inmunoterapias en la diabetes tipo 1
| Tipo de terapia | Blanco terapéutico | Ventajas | Desventajas |
|---|---|---|---|
| Terapias dirigidas contra linfocitos o citocinas (anticuerpos dirigidos contra moléculas coestimuladoras y de activación celular con el objetivo de evitar la respuesta autorreactiva)29-50 | Rituximab (anti-CD20) | Preservación residual de la función de las células beta Disminución del requerimiento de insulina Potencial reducción de complicaciones a largo plazo | No modifica la fisiología subyacente Efectos adversos moderados |
| Rituximab + Treg | Induce remisión temporal de la enfermedad | Depende de los perfiles celulares de cada individuo | |
| Teplizumab (anti-CD3) | Mejora la producción de insulina y la preservación del péptido C | Efectos adversos leves No favorece los niveles de HbA1c ni los requerimientos de insulina | |
| Abatacept (Ig-CTLA-4) | Mejora los niveles de péptido C Modula temporalmente la proporción de células T (naive, reguladoras y foliculares) | Efectos adversos graves No mejora la función de las células beta | |
| Globulina timocítica (ATG) | Preserva el péptido C en pacientes de reciente diagnóstico y en estadio 3 Retrasa la progresión de la enfermedad de etapa 2 a 3 Normaliza los niveles de HbA1c Disminuye los requerimientos de insulina | Efectos adversos leves Se requieren estudios de eficacia y seguridad a largo plazo | |
| Canakinumab (anti-IL1) + anakinra (agonista de IL-2) | Favorece la capacidad secretora de insulina | No preserva la función de las células beta Efectos secundarios leves | |
| Etanercept (proteína de fusión de TNF-R) | Disminuye los niveles de HbA1c | Efectos secundarios leves | |
| Golimumab (anti-TNF-α) | Favorece menores requerimientos de insulina y preservación de péptido C | Efectos secundarios leves | |
| Anti-IL-21 + liraglutida (análogo de GLP-1) | Preserva la función residual de péptido C | Efectos secundarios leves | |
| Terapia farmacológica combinada (agentes inmunosupresores con el objetivo de reducir la respuesta autorreactiva)51 | Micofenolato de mofetilo + daziclumab (anti-IL-2) | Útil en otras enfermedades autoinmunitarias | No favorece la concentración de péptido C Efectos adversos graves |
| Terapias basadas en trasplante celular (pretende la repoblación con estirpes celulares funcionales)52-60 | Alotrasplante de islotes | Independencia insulínica Normalización de niveles de HbA1c Mejor control glucémico | Efectos adversos leves Riesgos asociados a la cirugía y a la inmunosupresión a largo plazo Costos elevados |
| Xenotrasplante | Favorece niveles de normoglucemia | Faltan estudios en humanos | |
| Islotes derivados de células madre | Eficacia experimental | Menor respuesta en comparación con trasplante de islotes Requiere optimización de los procesos de obtención celular | |
| Células madre mesenquimales | Disminuye la respuesta autorreactiva Mejora la viabilidad de las células beta en modelos murinos Mejora el nivel de péptido C | Los estudios en humanos han resultado controvertidos No se alcanza la independencia insulínica | |
| Inmunización de antígenos específicos (busca inducir tolerancia específica para prevenir la respuesta autorreactiva contra componentes pancreáticos)62-67 | Administración oral de GAD, HSP60, insulina | Potencial prevención en personas con alto riesgo para diabetes tipo 1 Terapias de bajo riesgo Favorece vías de regulación inmunitaria Preservación de péptido C | Falta de optimización de dosis y eficacia clínica para generar tolerancia en las diferentes etapas de la enfermedad |
GAD: glutamato descarboxilasa; GLP-1: péptido similar al glucagón tipo 1; HbA1c: hemoglobina glucosilada; HSP60: proteína de choque térmico 60; TNF-R: receptor del factor de necrosis tumoral; Treg: células T reguladoras.
Discusión
En la búsqueda de nuevas estrategias enfocadas en tratar la causa de la enfermedad, en lugar de solo controlar sus efectos, se han probado diversos blancos inmunoterapéuticos. Aun así, la DT1 sigue siendo una de las principales causas de retinopatía, insuficiencia renal y accidentes cerebrovasculares. En las últimas cuatro décadas, el número de casos de DT1 ha aumentado de forma constante. Aunque la reciente aparición de análogos de la insulina de acción rápida y prolongada ha mejorado la calidad de vida de los pacientes con DT1, todavía quedan muchos desafíos por resolver.
Es importante reconocer las limitaciones que han tenido los diversos ensayos comentados en esta revisión, ya que incluso con los avances en diversas terapias es necesario realizar estudios con mayor cantidad de pacientes y con seguimientos a largo plazo. Será interesante analizar estudios comparativos de diferentes inmunoterapias con la finalidad de comprobar su eficacia, seguridad y capacidad de preservación del péptido C a lo largo de varios años. En general, se observa un riesgo bajo con el uso de diversos anticuerpos dirigidos contra las células T o sus productos, como el teplizumab (anti-CD3) y el abatacept (Ig-CTLA-4), así como de anticuerpos dirigidos contra citocinas, como el golimumab (anti-TNF-α) y los anti-IL-21. Cabe resaltar la eficacia que ha mostrado el uso de anti-CD3 en las etapas 2 y 3 de la enfermedad, al modificar su curso clínico, favorecer una menor dosificación de insulina y disminuir los riesgos de hipoglucemia.
Respecto a las terapias de expansión celular, principalmente las MSC y el trasplante de células beta, parecen estrategias que pueden llegar a lograr la remisión de la enfermedad. También habría que destacar el hecho de que la mayoría de los estudios se han realizado en pacientes con diagnóstico reciente, por lo que las terapias mencionadas tendrían que explorarse para su potencial aplicación en un universo más amplio de pacientes con DT1.
Otro aspecto relevante es la aplicabilidad de estas terapias, pues considerando la relación costo-beneficio, por ahora, estos abordajes resultan costosos y no son ampliamente accesibles para todos los pacientes con DT1. Aunque las diferentes inmunoterapias basadas en anticuerpos han mostrado beneficios a corto plazo en la preservación de las células beta, los resultados han sido contradictorios a lo largo del tiempo. Esto, aunado a los efectos adversos, las limitaciones en el acceso, las pruebas solo en grupos específicos de pacientes y los costos de los tratamientos, en conjunto han constituido una barrera importante para su aplicación.
En un estudio de la relación costo-beneficio realizado en 2020, Mital y Nguyen69 reportaron que los ciclos de tratamiento con teplizumab llegan a tener un costo de más de 100,000 USD por paciente, y estiman que para resultar rentable la aplicabilidad a diferentes grupos de riesgo el costo debería ser menor de 19,600 USD anuales.
Se ha analizado también la relación costo-efectividad de otras inmunoterapias para la DT1 de nueva aparición, como ATG en dosis baja (2.5 mg/kg), ATG en dosis alta (6.5 mg/kg), abatacept, rituximab y teplizumab. De todos ellos, el tratamiento con ATG en dosis bajas reporta un ahorro de aproximadamente 10,270 USD, con un coste per cápita que varía desde 5000 hasta 7000 USD para la ATG de dosis baja. Por su parte, los regímenes completos de abatacept por 2 años tienen un costo de al menos 30,000 USD, y el rituximab en cuatro infusiones tendría un costo de 15,000 a 20,000 USD70. Entonces, la terapia con dosis bajas de ATG parece ser la que presenta una mejor relación costo-beneficio. No obstante, no se ha encontrado eficacia plena con ninguno de los tratamientos planteados.
En lo que respecta a las terapias basadas en trasplante celular, los costos tienden a ser aún más altos. El trasplante de islotes pancreáticos, que es uno de los más probados, se estima que cuesta alrededor de 13,872 USD, más los costos de su mantenimiento a lo largo de 20 años y el uso de inmunosupresores, alcanzando un costo estimado de 519,000 USD71. Una alternativa para evitar la administración de fármacos inmunosupresores sería el trasplante autólogo de iPSC humanas, pero esta terapia también genera unos altos costos derivados del bioproceso para obtener las células. Así mismo, el uso de células estromales y de islotes pancreáticos parece mejorar la calidad de vida de los pacientes, pero alcanzan costos de hasta 80,000 USD anuales72,73. Por lo tanto, este tipo de abordajes, aunque prometedores, requieren aún importantes avances en cuanto a adecuación y abatimiento de costos para mejorar su aplicabilidad y disponibilidad.
Conclusiones
Los diversos blancos inmunoterapéuticos han tenido resultados promisorios. Aunque por ahora se ha descartado la idea de una remisión total por parte de anticuerpos dirigidos a células o citocinas, sí se puede hablar de la eficacia que han mostrado estos tratamientos para preservar las células beta pancreáticas, cambiando significativamente la evolución de la enfermedad y modificando las estrategias terapéuticas convencionales.
Las terapias de reemplazo de células madre, las técnicas de expansión celular y un desarrollo reorientado de terapias combinadas de bajo riesgo, que sean bien toleradas, son las vías preventivas y terapéuticas emergentes más prometedoras. Al mismo tiempo, los esfuerzos para predecir o diagnosticar la DT1 lo antes posible son igualmente importantes, dado que incluso las mejores intervenciones deben introducirse lo antes posible para preservar o rescatar eficazmente a las células beta de la destrucción autoinmunitaria.
El abordaje inmunológico de la DT1 resulta prometedor en relación con sus pocos riesgos, aunque se debe continuar explorando y desarrollando vías de tolerancia inmunitaria. Se requiere más investigación para conocer cómo modular la respuesta inmunitaria y generar áreas de desarrollo de estas terapias.