Introducción
El estándar de referencia para el diagnóstico de enfermedad por coronavirus 2019 (COVID-19) es la reacción en cadena de la polimerasa transcriptasa inversa (RT-PCR), la cual detecta el virus mediante muestras de hisopado nasofaríngeo, esputo o lavado bronquial1,2. Sin embargo, debido a la alta demanda de pruebas de detección, se han desarrollado otros métodos de laboratorio que se conocen como pruebas de antígeno y anticuerpos, caracterizadas por sus resultados a corto plazo, como son los anticuerpos inmunoglobulina (Ig) M e IgG, entre otros que son igualmente utilizados en el análisis de los casos (IgA, IgE, IgD), los cuales cuentan con una menor sensibilidad y especificidad2,3.
El método de imagen utilizado para la detección y estadificación de la neumopatía secundaria a COVID-19 es la tomografía computarizada (TC), que aunque no se recomienda para detección sistemática, ha demostrado ser una herramienta rápida complementaria en el diagnóstico, especialmente en aquellos lugares donde las pruebas no están ampliamente disponibles4-6. La TC posee una alta sensibilidad (98%) basándose en el sistema de puntuación CO-RADS (COVID-19 Reporting and Data System), que proporciona un nivel de sospecha etiológica7,8; así como datos pronósticos de la enfermedad, determinados con base en características y medición del compromiso pulmonar, aparte de la valoración vascular en pacientes con riesgo de tromboembolia pulmonar agregada9,10.
Ante la saturación de los servicios de radiología, herramientas auxiliares como la inteligencia artificial (IA) han adquirido relevancia con software packages como el CT Pneumonia Analysis (Siemens Healthlineers), el cual se define como un sistema de procesamiento de imágenes que proporciona un análisis cualitativo y cuantitativo de imágenes DICOM provenientes de TC11-13. Este sistema se utiliza para asistir a radiólogos y médicos a la hora de evaluar y valorar patologías pulmonares, lo que hace de él una herramienta útil de apoyo al diagnóstico y medición de los hallazgos tomográficos pulmonares14, sobre todo en una enfermedad como la COVID-19, que tiene patrones muy similares a otras patologías, agilizando así el análisis y la obtención de resultados15-17. Las ventajas del software en cuanto a servicios con prevalencia elevada de esta enfermedad y alta carga de trabajo son: mayor objetividad, cuantificación tomográfica de la neumopatía, reducción significativa del tiempo de interpretación, mejor abordaje en la supervisión con índices pronósticos y el seguimiento con impacto en el manejo médico.
La IA representa una herramienta prometedora en el campo de la imagen clínica18, sin embargo se debe tener presente que al ser un programa computacional que se codifica con algoritmos, tiene errores de precisión diagnóstica. Esto se da principalmente debido a patologías de base del paciente que pueden terminar confundiendo al software, a artefactos de respiración, o simplemente a errores aleatorios del sistema.
El Instituto Nacional de Cardiología Ignacio Chávez ha enfrentado el compromiso de dar atención a pacientes con COVID-19, contando con un manejo multidisciplinario en el que la imagen médica ha sido clave; aun así, no hay datos fiables que demuestren el valor diagnóstico de las herramientas humanas y de software aplicables a nuestra experiencia local en comparación con la evaluación por el radiólogo. Realizamos un estudio de prueba diagnóstica para la evaluación de la probabilidad de neumopatía por COVID-19 obtenida mediante el software de IA, con el resultado de la evaluación cualitativa CO-RADS, comparando esto con el estándar de referencia RT-PCR para coronavirus 2 del síndrome respiratorio agudo grave (SARS-CoV-2), y entregando así la experiencia de nuestra institución; al implementarse de esta manera, además de documentar la certeza diagnóstica permite evaluar la reproducibilidad de la IA documentando sus potenciales factores que contribuyen a errores en el software, así como sus ventajas y desventajas.
Materiales y métodos
Se realizó un estudio observacional, comparativo y retrolectivo en pacientes adultos con sospecha de infección por SARS-CoV-2 ingresados en el Instituto Nacional de Cardiología Ignacio Chávez durante el periodo comprendido entre diciembre de 2020 y enero del 2021, tiempo durante el cual el instituto se encontraba en fase COVID (centro híbrido), donde su principal objetivo era la atención de pacientes con diagnóstico o sospecha de esta infección. A estos sujetos se les realizó TC de tórax como parte de su evaluación clínica. La privacidad de los pacientes fue asegurada mediante la anonimización de la información, teniendo como base los principios de la declaración de Helsinki para el tratamiento de los datos.
Población de estudio
Se incluyeron pacientes mayores de 18 años, registrados de forma consecutiva en nuestro sistema PACS-RIS, a quienes se les realizó una TC de tórax por sospecha clínica de COVID-19. Se tuvieron en cuenta datos de la historia clínica electrónica, incluyendo los registros de RT-PCR para SARS-CoV-2 para cada uno de los participantes, y se excluyó a aquellos a quienes no se les realizó esta prueba. Se registraron variables demográficas como la edad y el sexo, además de variables clínicas como comorbilidades y diagnósticos diferenciales.
Protocolo de TC de tórax
La TC de tórax se realizó en fase inspiratoria por medio de un tomógrafo Somaton Definition Flash de 256 cortes Somatom Definition Flash (Siemens, Alemania). Se emplearon en todas las adquisiciones CARE Dose 4D, pitch mayor de 0.8, colimación adecuada para tórax (FoV aproximado de 350 mm) y tiempo de rotación de 0.28 s. Además, el kilovoltaje (Kv) con límite máximo de 120 de acuerdo con corrección de atenuación en el eje Z, los miliamperios por segundo (mAs) de 120 a 150 y dosis de radiación desde 120 a 250 mGy*cm, con dosis promedio de 2 milisieverts (mSv). Las reconstrucciones se realizaron con corte de 1 mm utilizando un Kernel B50f (de alta frecuencia espacial), según las recomendaciones dadas por el proveedor del software.
Análisis de imágenes y resultados del software IA
Las reconstrucciones fueron visualizadas y analizadas en una estación dedicada (SYNGO VIA versión VA48A), mediante el sistema de IA (CT Pneumonia Analysis versión 2.0. Siemens Healthlineers, Erlangen, Alemania). Este es un software que toma como entrada una TC de tórax simple e identifica y fracciona en 3D los pulmones y los lóbulos antes de segmentar las anomalías. Posteriormente, genera dos medidas combinadas de la gravedad de la afectación de pulmón/lóbulo, cuantificando la extensión de la presencia de opacidades altas (vidrio despulido y consolidación), de las que ya se ha demostrado su relación con síntomas graves y peor pronóstico (asistencia ventilatoria y mortalidad). La primera medida de gravedad de la enfermedad es global, mientras que la segunda se refiere específicamente a lóbulos6-12. El algoritmo de IA fragmenta de forma automática ambos pulmones y sus lóbulos, y muestra los contornos resultantes como una superposición gráfica. Con base en la atenuación de los vóxeles y de acuerdo con umbrales preestablecidos, este cuenta volúmenes y porcentajes entregando el cálculo de las zonas de ocupación acinar, las cuales están representadas por aquellos con una densidad mayor de –200 U (high average volumen), mientras que el parénquima pulmonar normal tiene densidades de –750 a –950 UH12, un grosor de segmentación de 2 mm con un nivel de ventana de –600 y un ancho de ventana de 1,200. Es importante resaltar que los valores generales de la probabilidad de COVID-19, la puntuación de opacidad total y los valores de porcentaje de opacidad que se muestran junto al gráfico corresponden a la totalidad del pulmón11 (Fig. 1). Las tres variables analizadas en el presente estudio, el cual fue construido con base en cohortes de comprobación, son:
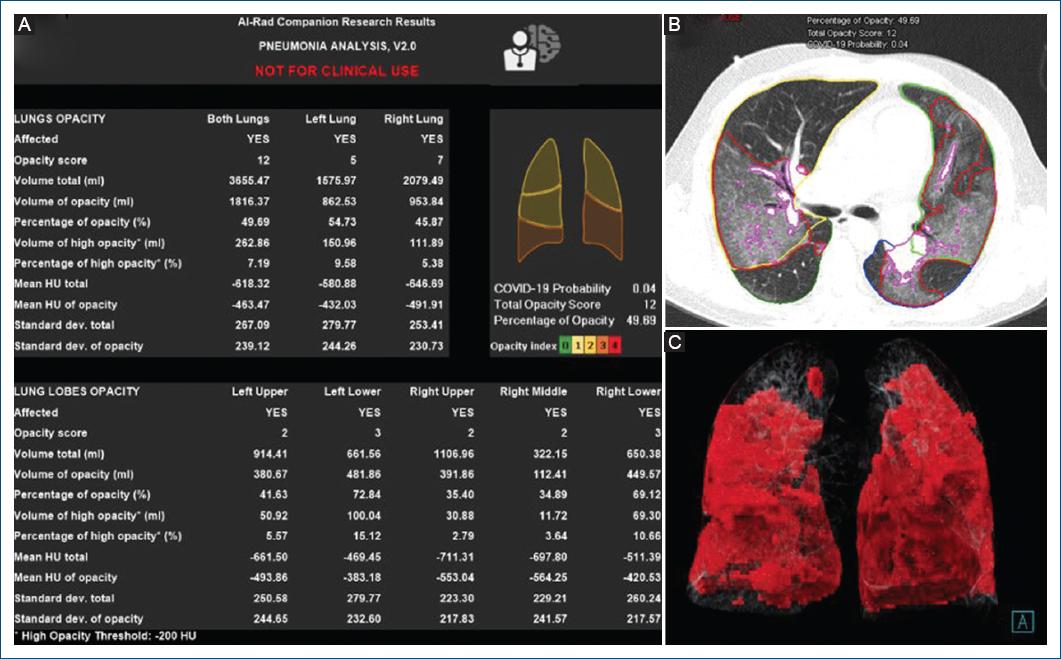
Figura 1 Ejemplo de los resultados arrojados por la inteligencia artificial. A: lista de los resultados de las mediciones que se muestran para cada lóbulo y pulmones. Los valores encasillados en las líneas blancas representan las constantes principales valoradas en este estudio. B: resultados de la segmentación y de la medición de la densidad pulmonar. C: imagen en volumen rendering de los pulmones y lesiones que se definieron en la configuración.
- Probabilidad de COVID-19: esta puntuación varía entre 0 y 1, y hace referencia a la probabilidad de que los hallazgos de la IA sean causados por COVID-19.
- Puntaje de opacidad total: su rango va de 0 a 20, representa la suma de los puntajes de opacidad de los cinco lóbulos pulmonares.
- Porcentaje de opacidad: este valor refiere el porcentaje de opacidad de todo el pulmón. El análisis tardó en promedio un minuto, y se registraron las tres variables previamente mencionadas.
Posteriormente se extrajeron los resultados de CO-RADS de las interpretaciones de radiólogos expertos en tomografía de tórax con más de cinco años de experiencia, quienes se basaron en la guía descrita por Prokop et al.7, con las siguientes definiciones:
- CO-RADS 0: cuando el resultado no encaja dentro de ninguna de las cinco categorías, debido a que las exploraciones son incompletas o de calidad insuficiente.
- CO-RADS 1: significa un nivel muy bajo de sospecha de afectación pulmonar por COVID-19, ya que los resultados de la TC son normales, o sus hallazgos son de origen inequívoco no infeccioso.
- CO-RADS 2: hace referencia a un bajo nivel de sospecha de afectación pulmonar por COVID-19 con base en hallazgos de TC en los pulmones típicos de origen infeccioso no COVID-19.
- CO-RADS 3: representa hallazgos indeterminados para la afectación pulmonar por COVID-19.
- CO-RADS 4: denota un alto nivel de sospecha de afectación pulmonar por COVID-19, determinando que los hallazgos de la TC son típicos de COVID-19. Sin embargo, también muestran cierta superposición con otras neumonías (virales).
- CO-RADS 5: nivel muy alto de sospecha de afectación pulmonar por COVID-19 por hallazgos típicos de TC.
- CO-RADS 6: indica resultado conocido de RT-PCR para SARS CoV-2 positivo. El índice de severidad por tomografía utilizado es el puntaje de severidad total (TSS, por sus siglas en inglés). En este los hallazgos encontrados se dividen por lóbulos y no por segmentos pulmonares, es un método visual cuantitativo que consiste en puntuar los porcentajes de cada uno de los cinco lóbulos implicados (lóbulo superior derecho, lóbulo medio, lóbulo inferior derecho, lóbulo superior izquierdo y lóbulo inferior izquierdo): 1 punto, < 5% de afectación; 2 puntos, 5-25% de afectación; 3 puntos, 26-49% de afectación; 4 puntos, 50-75% de afectación, y 5 puntos, > 75% de afectación. La puntuación total de la TC es la suma de las puntuaciones lobares individuales, y puede oscilar entre 0 (sin afectación) y 25 (afectación máxima), la cual se da cuando los cinco lóbulos muestran más del 75% de afectación.
RT-PCR para SARS-CoV-2
Finalmente, se cotejaron y se registraron en la base de datos los valores de IA, los reportes tomográficos realizados por los radiólogos y los resultados de RT-PCR para SARS-CoV-2. En nuestra institución se realiza la prueba RT-PCR para SARS-CoV-2 por medio de exudado del tracto respiratorio superior (nasofaringe), y consta de dos procesos automatizados: la extracción de ácidos nucleicos y la reacción de amplificación. El equipo que se utilizó es un Elite Ingenius serie 500. La tecnología es ELISA (ensayo por inmunoabsorción ligado a enzimas) y la determinación es del genoma viral SARS-CoV-2. El distribuidor de reactivos es Abalat y se encuentra autorizado por el InDRE (Instituto de Diagnóstico y Referencia Epidemiológico).
Análisis estadístico
Se computaron resultados estadísticos de tendencia central y de dispersión para las variables continuas, mientras que las variables categóricas se expresaron como porcentajes y frecuencias. Se tomó como significancia estadística una p < 0.05 (resultado clínicamente importante). Se obtuvo la información de precisión diagnóstica luego de comparar el estándar de referencia (RT-PCR) con el CO-RADS realizado por los observadores y la probabilidad de COVID-19 que arrojaron las imágenes de TC por medio del software de IA. Todo esto mediante un análisis basado en ROC (Receiver-Operating-Characteristic), con su respectiva área bajo la curva (AUC, por sus siglas en inglés) e intervalos de confianza del 95% (IC 95%). Los umbrales óptimos se obtuvieron utilizando el índice de Youden para describir la sensibilidad, la especificidad y los valores predictivos. El análisis se realizó en el software STATA SE versión 14.1.
Resultados
Se consideraron en primera instancia 280 sujetos potenciales con estudios de TC almacenados en el PACS realizados por sospecha de SARS-CoV-2 en el periodo ya expuesto, de los cuales se analizaron 192 pacientes elegibles que contaban prueba RT- PCR para SARS-CoV-2 (107 hombres y 85 mujeres). En la comparación CO-RADS vs. RT-PCR para SARS-CoV-2 se omitieron 72 pacientes por presentar CO-RADS 6, ya que esto significaba prueba conocida de RT-PCR positivo al momento de la evaluación de las imágenes de TC por parte de los radiólogos que determinaron el CO-RADS. La edad media de los 192 pacientes es de 50.39 años y la mediana de 49 años (± 15.61), con un mínimo de 18 años de edad y un máximo de 97 años (Tabla 1).
Tabla 1 Variables calculadas de la edad y las otorgadas por la inteligencia artificial junto con la frecuencia en porcentajes de las variables diagnósticos diferenciales con respecto al total de la muestra analizada, la cual fue de un total de 192 pacientes distribuidos de la siguiente manera: CO-RADS en categoría 1 alcanza 42 pacientes CO-RADS en categoría 2 alcanza 2 pacientes CO-RADS en categoría 3 alcanza 23 pacientes CO-RADS en categoría 4 alcanza 0 pacientes CO-RADS en categoría 5 alcanza 53 pacientes CO-RADS en categoría 6 alcanza 72 pacientes. CO-RADS 6 fue eliminado del análisis de resultados en la comparación CO-RADS vs. RT-PCR.
| Mediana (rango intercuartílico) | Rango mínimo- máximo | Diagnósticos diferenciales | Frecuencia n (porcentaje) | |
|---|---|---|---|---|
| Edad | (38-62) | 1-97 | Sobrecarga hídrica/edema | 20 (10.4%) |
| Probabilidad de COVID-19 | 1 (0.25-1) | 0-1 | Hipertensión pulmonar | 8 (4.1%) |
| Puntaje de opacidad total | 5 (1-10) | 0-20 | Neumopatía intersticial/enfisema | 10 (5.2%) |
| Porcentaje de opacidad total | 12 (1 –33) | 0-88 | Infección por otros agentes | 2 (1.04%) |
| Infarto pulmonar | 4 (2.08%) | |||
| Total | 44 (22.9%) | |||
| Total de pacientes | 192 (100%) |
CO-RADS: COVID-19 Reporting and Data System; RT-PCR: reacción en cadena de la polimerasa transcriptasa inversa.
Precisión diagnóstica de las variables tomográficas en relación con la RT-PCR para SARS-CoV-2
Se realizó la curva ROC entre la probabilidad de COVID-19 obtenida por la IA vs. la RT-PCR para SARS-CoV-2, encontrando un AUC de 0.774 (IC 95%: 0.69-0.81) con p = 0.0001, con sensibilidad del 65.3%, especificidad del 84.50%, área ROC de 0.75%, razón de verosimilitud positiva de 4.21 y negativa de 0.41, razón de momios diagnóstica de 10.26, valor predictivo negativo (VPN) del 58.8% y valor predictivo positivo (VPP) del 87.8% (Fig. 2). Gracias al índice de Youden se halló el punto de corte, siendo una probabilidad de 0.975 (IC 95%: 0.63-0.80) con sensibilidad y especificidad del 72 y 77%, respectivamente. Se dicotomizó esta variable respecto a dicho valor (> 0.97), obteniendo una sensibilidad, especificidad, VPP y VPN del 67.3, 76.10, 66 y 77.1%, respectivamente (Tabla 2).
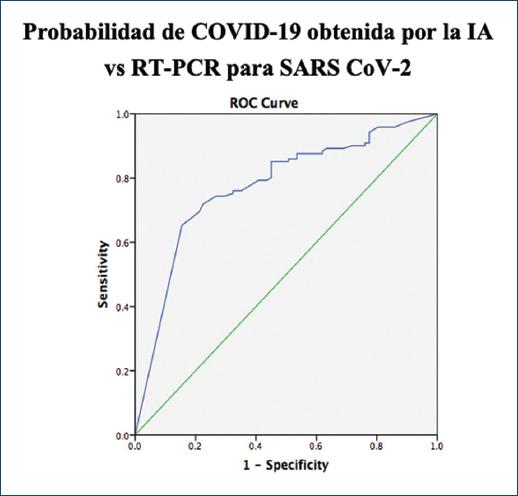
Figura 2 Gráfico de la curva que muestra la precisión diagnóstica de la probabilidad de COVID-19 determinada por el software vs. la RT-PCR para SARS-CoV-2 (línea azul: probabilidad de COVID-19 obtenida por IA). COVID-19: enfermedad, por, coronavirus, 2019; IA: inteligencia artificial; RT-PCR: reacción en cadena de la polimerasa transcriptasa inversa; SARS-CoV-2: coronavirus 2 del síndrome respiratorio agudo grave.
Tabla 2 Dicotomización de la probabilidad de COVID-19 en > 0.97
| Parámetro | > 0.97 95% - Intervalo de Confianza |
|---|---|
| Prevalencia | 40.80% (32.0-50.2%) |
| Sensibilidad | 67.30% (52.5-80.1%) |
| Especificidad | 76.10% (64.5-85.4%) |
| Área ROC | 0.72 (0.63-0.80) |
| Razón de verosimilitud (+) | 2.81 (1.78-4.45) |
| Radio de verosimilitud (-) | 0.43 (0.28-0.66) |
| Razón de momios diagnostica | 6.55 (2.94-14.62) |
| Valor predictivo positivo | 66.00% (51.2-78.8%) |
| Valor predictivo negativo | 77.10% (65.6-86.3%) |
ROC: Receiver-Operating-Characteristic; COVID-19: enfermedad por coronavirus 2019.
Se realizó la curva ROC entre CO-RADS vs. RT- PCR para SARS-CoV-2, obteniendo un AUC de 0.9 (IC 95%: 0.85-0.96), con sensibilidad del 91.80%, especificidad del 88.7%, VPP del 84.9 % y VPN del 94% (Tabla 3).
Tabla 3 Variables otorgadas en la comparación CO-RADS vs. RT-PCR para SARS-CoV-2, con un AUC 95%
| Parámetro | CO-RADS vs. RT- PCR para SARS CoV-2 95% - Intervalo de Confianza |
|---|---|
| Prevalencia | 40.80% (32.0-50.2%) |
| Sensibilidad | 91.80% (80.4-97.7%) |
| Especificidad | 88.70% (79.0-95.0%) |
| Área ROC | 0.9 (0.85-0.96) |
| Razón de verosimilitud (+) | 8.15 (4.22-15.74) |
| Radio de verosimilitud (-) | 0.09 (0.04-0.24) |
| Razón de momios diagnostica | 88.59 (25.80-301.20) |
| Valor predictivo positivo | 84.90% (72.4-93.3%) |
| Valor predictivo negativo | 94.00% (85.4-98.3%) |
AUC: área bajo la curva; CO-RADS: COVID-19 Reporting and Data System; ROC: Receiver-Operating-Characteristic; RT-PCR: reacción en cadena de la polimerasa transcriptasa inversa; SARS-CoV-2: coronavirus 2 del síndrome respiratorio agudo grave.
Discusión
Esta investigación se enfocó en evaluar la precisión diagnóstica de la variable de probabilidad de COVID-19 brindada por el software de IA diseñado por Siemens y la valoración hecha por el radiólogo (CO-RADS), comparadas con la RT-PCR en una institución de alta complejidad con población mexicana. La probabilidad de COVID-19 tuvo una precisión aceptable, con un buen VPP (87.80%), pero con un bajo VPN (58.80%). La variable CO-RADS vs. la RT-PCR para SARS CoV-2 obtuvo una mayor precisión con valores de sensibilidad y especificidad mucho más elevados, alcanzando el 91.80 y 88.7%, respectivamente.
La menor precisión del proceso automatizado de análisis se produjo debido a que existen constantes que pueden provocan el error en la IA, como aquellos escenarios en los que existen otros procesos infecciosos y no infecciosos diferentes del COVID-19 (p. ej., CO-RADS 1, 2 y 3), los cuales en nuestra institución son muy frecuentes, por las enfermedades de base y diagnósticos diferenciales de la población analizada, representadas por sobrecarga hídrica/edema agudo de pulmón, hipertensión pulmonar, neumopatía intersticial/enfisema, infección por otros agentes e infarto pulmonar (Tabla 1). Estas condiciones producen fallas en el análisis del software, y en estas circunstancias es que el radiólogo al tener la correlación clínica adecuada y el patrón de los hallazgos, sumado a su experiencia, pueden ser clave en el diagnóstico diferencial puede determinar si la neumopatía proviene o no del COVID-19.
El metaanálisis de Moezzi et al.19 demostró un rendimiento satisfactorio utilizando el algoritmo de IA para la identificación de COVID-19 por medio de TC asistida por IA frente a muestras sanas. Demostraron que la IA fue precisa en la afectación pulmonar durante el COVID-19, con una sensibilidad combinada de 0.90 (IC 95%: 0.90-0.91), una especificidad de 0.90 (IC 95%: 0.90-0.91) y un AUC de 0.96 (IC 95%: 0.91-0.98), lo que contrasta con nuestro estudio, pues este demostró una sensibilidad y especificidad de 0.65 y 0.84, respectivamente. Al igual que la investigación realizada por Mei20, donde indican el potencial valor de precisión diagnóstica de los sistemas de cuantificación tomográfica automática, con un 84.3% de sensibilidad y un 82.8% de especificidad. En comparación con nuestra investigación, su sensibilidad y especificidad fueron mayores, por lo tanto se debe realizar una correlación con la información clínica para tener un diagnóstico más apropiado, y lograr implementar algoritmos multivariados.
La variable de probabilidad COVID-19 otorgada por la IA nos permite salir de dudas frente a pacientes de los que no tengamos la certeza diagnóstica de COVID-19, pero debemos tener claro que el sistema no supera la lectura del radiólogo, sino que la complementa. Hay varias publicaciones sobre el apoyo de la IA con la severidad clínica, encontrándola acertada para el manejo de estos pacientes, y con adecuada comparación respecto a los pacientes de severidad elevada, con resultados cuantitativos reproducibles. En cuanto a la precisión diagnóstica, se ha validado en múltiples ocasiones el software, sin embargo actualmente ninguno ofrece la posibilidad de mejora para el sistema determinado por los diagnósticos diferenciales. Georgescu et al.18 encontraron que si bien hay propiedades dominantes que se pueden observar en la COVID-19, como la presencia de opacidades en vidrio despulido y distribución periférica y basal, estas características no se observan en todos los casos. Sin embargo, mencionaron que teniendo en cuenta que los resultados de RT-PCR para SARS-CoV-2 pueden tardar varias horas, el sistema se puede utilizar para la clasificación rápida de casos positivos, particularmente en entornos con recursos limitados donde la experiencia radiológica puede no estar disponible de inmediato. Además, demostraron un AUC de 0.90 con una sensibilidad del 86% y especificidad del 81%, siendo mucho mayor la sensibilidad que la adquirida en nuestro trabajo (65.3%), probablemente debido al tipo de pacientes que manejamos. Este sistema podría ayudar al radiólogo a priorizar la interpretación de TC en pacientes con COVID-19 mediante la detección de casos de menor probabilidad21.
En la investigación realizada por Machnicki et al.3 se demostró que la apariencia típica de la TC de tórax tiene una sensibilidad y especificidad del 73.5 y 82.8% en relación con la precisión diagnóstica del radiólogo con respecto a la RT-PCR para SARS-CoV-2, así como la sensibilidad y especificidad de la apariencia indeterminada es del 92 y 41%. Para la IA se vuelve un limitante los pacientes con una morfología atípica, los cuales cada vez son más frecuentes.
Este estudio tiene varias limitaciones: la muestra poblacional es pequeña, la investigación tiene un diseño retrolectivo y un 22.9% de los pacientes tienen enfermedades de base (sobrecarga hídrica/edema agudo de pulmón, hipertensión pulmonar, neumopatía intersticial/enfisema, infección por otros agentes e infarto pulmonar), lo que puede disminuir la especificidad de la IA.
Invitamos a seguir investigando sobre la cuantificación tomográfica automática en pacientes con COVID-19, en especial en aquellos que presentan comorbilidades que pueden ser un desafío para los sistemas de cómputo. En un futuro se requiere implementar algoritmos avanzados que permitan la mejoría de la especificidad en el diagnóstico de estos pacientes.
Conclusión
La comparación entre los resultados obtenidos por el CO-RADS e IA vs. el estándar de referencia en pacientes con sospecha de COVID-19 mostró mayor efectividad diagnóstica del primero. Sin embargo, la IA tiene impacto en la evaluación de estos pacientes, ya que puede apoyar la sospecha de infección viral por su alto VPP, además de que permite agilizar la valoración del radiólogo.















