Introducción
El género Bursera es un grupo de árboles y arbustos caducifolios representativos de bosques tropicales secos, con una distribución de 94 especies en México, de las cuales 80 son endémicas y 50 se localizan en cuenca del rio Balsas (Barrales-Alcalá y Bonfil 2024; Blancas-Vázquez et al., 2022).
En numerosas comunidades rurales de México y desde tiempos antiguos las especies del género Bursera han tenido importancia cultural, económico, ecológica, medicinal y religiosa (Blancas et al., 2022; Rio et al., 2022). Los árboles y arbustos sirven de cercas vivas para delimitar propiedades, de la corteza se pueden extraer resinas aromáticas (copales) y látex, la madera sirve para fabricar herramientas agrícolas, figuras religiosas, máscaras tradicionales y en algunos casos se puede usar como leña (Blancas-Vázquez et al., 2022; Rio et al., 2022).
Las resinas del género Bursera son sustancias que tiene una composición química rica en terpenos (mono, sesqui y tri-terpenos), y su función es proteger a las plantas de herbívoros y microrganismo patógenos (Blancas et al., 2022; Antúnez-Mojica et al., 2021). A la vez, presentan actividad antioxidante, antimicrobiana (bactericida y fungicida), desinfectante, antiviral, antiinflamatoria y anticancerígena (Blancas et al., 2022).
Una resina poco estudiada es la producida por la especie de Bursera fagaroides (Kunth) Engl., un grupo de árboles y arbustos diocos o hermafroditas que pueden alcanzar hasta diez metros de altura y se encuentran distribuidos en matorrales xerófilos, selvas tropicales caducifolias y bosques de encino de México (Blancas-Vázquez et al., 2022). Además, esta especie en la medicina tradicional se utiliza para tratar desordenes estomacales, inflamaciones, daños físicos, lesiones cutáneas e incluso algunos tipos de tumores y cáncer (Pérez-Mejía et al., 2024).
En la resina de B. fagaroides los metabolitos secundarios más estudiados son lignanos que presentan propiedades anticancerígenas (Antúnez-Mojica et al., 2021; Marcotullio et al., 2018). Sin embargo, aunque se sabe que el componente mayoritario de las resinas son terpenos (Blancas et al., 2022), las investigaciones de la identificación y actividad de otros metabolitos secundarios presentes en la resina de B. fagaroides son escasas (Barrales-Alcalá y Bonfil 2024; Blancas et al., 2022). Por lo que, el objetivo de esta investigación fue obtener extractos con disolventes de diferente polaridad de la resina de Bursera fagaroides recolectada en Puebla, con el propósito de identificar y cuantificar metabolitos secundarios por medio de técnicas colorimétricas, y evaluar su potencial antioxidante, para enriquecer el conocimiento fitoquímico que se tiene acerca de la resina que produce esta especie.
Materiales y métodos
Material vegetal
Por medio de un muestreo dirigido, en el municipio de “Huehuetlan El Grande”, Puebla, México, paralelos 18º 41' 06'' y 18º 53' 12'' de latitud norte y meridianos 98º 03' 18'' y 98º 15' 06'' de longitud oeste, en agosto de 2014 (verano), se seleccionaron cinco árboles adultos de Bursera fagaroides identificados por la Dra. Agustina Rosa Andrés Hernández investigadora de la Facultad de Biología de la Benemérita Universidad Autónoma de Puebla, al mismo tiempo, una muestra del espécimen fue herborizado y depositado en el herbario de la Universidad Autónoma de Guerrero (UAGC), número de registro 14874. Los árboles seleccionados tenían alturas superiores a los cinco metros y estaban en etapa de fructificación, a los cuales se realizó una recolecta de resina solidificada (color ámbar con tonalidades blanquecinas y oscuras) con un bisturí estéril sin tomar corteza del árbol.
Obtención de los extractos de la resina
Las muestras de resina solidificada recolectadas (5 en total) se molieron en mortero hasta obtener polvo. Se pesaron 3.410 g del polvo de resina por cada muestra y se procedió a realizar una extracción secuencial con hexano (J.T. Baker®), diclorometano (J.T. Baker®) y metanol (J.T. Baker®). Las muestras permanecieron 48 h con los disolventes y después se centrifugaron (45000 rpm, durante 10 min), para recuperar las soluciones. A las soluciones se les evaporaron los disolventes, en rota-evaporador (BUCHI, R-114) a presión reducida y temperatura (60 a 70 °C), para obtener los extractos. En total se obtuvieron 15 extractos, cinco de la extracción con hexano (hexánicos), cinco de la extracción con diclorometano (diclorometánicos) y cinco de la extracción con metanol (metanólicos) y el rendimiento promedio se expresó en miligramo sobre gramo de resina (mg g-1 de resina).
Identificación preliminar de metabolitos secundarios en los extractos de la resina
De los 15 extractos se tomó un miligramo y se disolvieron en un mililitro de los disolventes con los que se extrajeron, en tubos de ensayo. Se obtuvieron 15 soluciones a las que se les realizaron las técnicas descritas por Yadav y Agarwala (2011) y del Laboratorio de Fitoquímica Vegetal del Colegio de Postgraduados (CP) Campus Montecillo, para la identificación de seis metabolitos secundarios:
Fenoles. Se tomaron 100 µL de las soluciones, se depositaron en tubos de ensayo (15 en total) y se agregaron tres gotas de reactivo de Folin-Ciocalteau (Sigma-Aldrich®) a 50%. La mezcla de los tubos se agito (Vórtex, GENIE II MIXER) y la reacción positiva fue un cambio de color a tonalidad azul oscuro. El control positivo fue 100 µL de una solución de ácido gálico (MERCK®) de 1 mg mL-1 en etanol a 80% y el control negativo fueron solo los reactivos.
Flavonoides. En tubos de ensayo (15 en total) se depositaron 100 µL de las soluciones y se les agregaron un trozo de cinta de magnesio (Sigma-Aldrich®) de cinco milímetros y tres gotas de ácido clorhídrico (HCl, MEYER®) concentrado (prueba de Shinoda). La mezcla de los tubos se agito y la reacción positiva fue la presencia de un ligero color amarillo a rosa en solución efervescente. El control positivo fue 100 µL de una solución de quercetina (MERCK®) de 1 mg mL-1 en metanol a 80% y el control negativo fueron solo los reactivos.
Alcaloides. Se tomaron 100 µL de las soluciones, se depositaron en tubos de ensayo (15 en total) y se agregaron dos mililitros de HCl a uno por ciento. Luego los tubos de ensayo se agruparon en un vaso de precipitados y se metieron en un recipiente de metal con agua caliente (60 a 70 °C) por 20 min. Después, se sacó el vaso de precipitados del agua caliente y los tubos de ensayo se dejaron reposar a temperatura ambiente durante 20 min. Finalmente, en los tubos de ensayo se agregaron tres gotas de reactivo Dragendorff (Sigma-Aldrich®). La mezcla de los tubos se agito y la reacción positiva fue un cambio de color a tonalidad naranja. El control positivo fue 100 µL de una solución de polvo de hojas de Lupinus sp., de 10 mg mL-1 en metanol a 80% y el control negativo fueron solo los reactivos.
Saponinas. En tubos de ensayo (15 en total) se depositaron 100 µL de las soluciones y se agregaron 0.5 mL se solución AB (mezclar 1.5 mL de solución A y 1.5 mL de solución B) junto con 0.5 mL de carbonato de sodio (Na2CO3, MERCK®) 1 molar (prueba de Fehling). Luego los tubos de ensayo se agruparon en un vaso de precipitados y se metieron en un recipiente de metal con agua caliente (60 a 70 °C) durante 30 min. La mezcla de los tubos se agito y la reacción positiva fue un cambio de color a tonalidad rosa. Control positivo fue 100 µL de una solución de polvo de saponina de soya, de 10 mg mL-1 en agua destilada y el control negativo fueron solo los reactivos.
Preparación de solución A: 0.64 g de sulfato de cobre (CuSO4, MERCK®) en cinco mililitros de agua.
Preparación de solución B: 1.76 g de tartrato potasio-sodio (KNaC4H4O6·4H2O, MERCK®) y 0.77 g de hidróxido de sodio (NaOH, MERCK®) en cinco mililitros de agua.
Taninos. Se tomaron 100 µL de las soluciones, se depositaron en tubos de ensayo (15 en total) y agregaron tres gotas de cloruro férrico (FeCl3, Sigma-Aldrich®) a 5%. La mezcla de los tubos se agito y la reacción positiva fue un cambio de color a tonalidad azul violeta. El control positivo fue 100 µL de una solución de ácido tánico (MERCK®) de 1 mg mL-1 en metanol a 80% y el control negativo fueron solo los reactivos.
Terpenos. En tubos de ensayo (15 en total) se depositaron 100 µL de las soluciones y agregaron dos gotas de anhídrido acético (Ac2O, Sigma-Aldrich®) y dos gotas de ácido sulfúrico (H2SO4, MEYER®) concentrado (prueba de Liebermann-Burchard). La mezcla de los tubos se agito y la reacción positiva fue un cambio de color a tonalidad azul verdoso. El control positivo fue 100 µL de una solución de ácido masticadienónico (MERCK®) de 1 mg mL-1 en diclorometano a 80% y el control negativo solo los reactivos.
Cuantificación de terpenos totales en el extracto obtenido de la extracción con diclorometano
De los cinco extractos diclorometánicos se prepararon soluciones de 10 mg mL-1 en diclorometano a 80% y se siguió el método utilizado por el Laboratorio de Fitoquímica del CP, para cuantificar terpenos.
Por triplicado se realizó una curva estándar de ácido masticadienónico (0.1 mg mL-1 en diclorometano a 80%) con concentraciones de 0, 25, 75, 150 y 300 µL y se tomaron también por triplicado 10 µL de las soluciones de los extractos diclorometánicos, en tubos de ensayo. Luego a los tubos de ensayo se les adiciono diclorometano hasta completar 1000 µL, después se agregaron 25 µL de una solución Ac2O a 50% y 975 µL de H2SO4 a 2.5%. Los tubos de ensayo se dejaron reposar 45 min y después se les adiciono un mililitro de agua destilada. Las mezclas de los tubos se agitaron y se les hicieron lecturas a 610 nm en espectrofotómetro de luz ultravioleta-visible (GENESYSTM 5). Con las lecturas de la curva estándar (eje Y absorbancia y eje X concentración de molécula estándar) se realizaron los cálculos del contenido de terpenos totales a partir de las lecturas de los extractos diclorometánicos y el promedio de los resultados se expresó en miligramo de equivalentes de ácido masticadienónico sobre gramo de extracto diclorometánico (mg de EAM g-1 de ED).
Cuantificación de saponinas totales en el extracto obtenido de la extracción con diclorometano
De los cinco extractos diclorometánicos se prepararon soluciones de 10 mg mL-1 en agua destilada y se siguió el método utilizado por el Laboratorio de Fitoquímica del CP, para cuantificar saponinas.
Por triplicado se realizó una curva estándar de saponina de soya (un mg mL-1 en agua destilada) con concentraciones de 0, 20, 25, 50 y 100 µL y se tomaron también por triplicado 10 µL de las soluciones de los extractos diclorometánicos, en tubos de ensayo. Luego a los tubos de ensayo se les adiciono agua destilada hasta completar 1000 µL, después se agregaron 1000 µL de H2SO4 a 70% y 100 µL de Vainillina (Sigma-AldrichR) a 8%. Luego los tubos de ensayo se agruparon en un vaso de precipitados y se metieron en un recipiente de metal con agua caliente (60 a 70 °C) durante 20 min. Después, se sacó el vaso de precipitados del agua caliente y se pasó a otro reciente de metal con agua fría (-2 a -4 °C) durante 20 min. Finalmente, a los tubos de ensayo se le agregaron 900 µL de agua destilada. Las mezclas de los tubos se agitaron y se les hicieron lecturas a 544 nm en espectrofotómetro de luz ultravioleta-visible. Con las lecturas de la curva estándar se realizaron los cálculos del contenido de saponinas totales a partir de las lecturas de los extractos diclorometánicos y el promedio de los resultados se expresó en mg de equivalentes de saponina de soya sobre gramo de extracto diclorometánico (mg de ESY g-1 de ED).
Cuantificación de fenoles totales en el extracto obtenido de la extracción con metanol
De los cinco extractos metanólicos se prepararon soluciones de 10 mg mL-1 en etanol a 80% y se siguió el método descrito por Yadav y Agarwala (2011), para cuantificar fenoles.
Por triplicado se realizó una curva estándar de ácido gálico (0.1 mg mL-1 en etanol a 80%) con concentraciones de 0, 25, 75, 150 y 300 µL y se tomaron también por triplicado 10 µL de las soluciones de los extractos metanólicos, en tubos de ensayo. Luego a los tubos de ensayo se les adiciono agua destilada hasta completar 1000 µL, después se agregaron 25 µL de una solución de Folin-Ciocalteau a 50% y 975 µL de Na2CO3 a 2.5%. Los tubos de ensayo se dejaron reposar 45 min en oscuridad y después se les adiciono un mililitro de agua destilada. Las mezclas de los tubos se agitaron y se les hicieron lecturas a 765 nm en espectrofotómetro de luz ultravioleta-visible. Con las lecturas de la curva estándar se realizaron los cálculos del contenido de fenoles totales a partir de las lecturas de los extractos metanólicos y el promedio de los resultados se expresó en miligramo de equivalentes de ácido gálico sobre gramo de extracto metanólico (mg de EAG g-1 de EM).
Cuantificación de flavonoides totales en el extracto obtenido de la extracción con metanol
De los cinco extractos metanólicos se prepararon soluciones de 10 mg mL-1 en metanol a 80% y se siguió el método descrito por Yadav y Agarwala (2011), para cuantificar flavonoides.
Por triplicado se realizó una curva estándar de quercetina (0.1 mg mL-1 en metanol a 80%) con concentraciones de 0, 20, 25, 50 y 100 µL y se tomaron también por triplicado 10 µL de las soluciones de los extractos metanólicos, en tubos de ensayo. Luego a los tubos de ensayo se adiciono metanol a 80% hasta completar 800 µL, después se agregaron 100 µL de acetato de potasio (CH3CO2K) uno molar y 100 µL de cloruro de aluminio (AlCl3) a 10%. Los tubos de ensayo se dejaron reposar 30 min en oscuridad y después se les adicionaron dos mililitros de agua destilada. Las mezclas de los tubos se agitaron y se les hicieron lecturas a 420 nm en espectrofotómetro de luz ultravioleta-visible. Con las lecturas de la curva estándar se realizaron los cálculos del contenido de fenoles totales a partir de las lecturas de los extractos metanólicos y el promedio de los resultados se expresó en mg de equivalentes de quercetina sobre gramo de extracto de metanólico (mg de EQ g-1 de EM).
Análisis antioxidante por el método de 2, 2-difenil-1 picrilhidrazil (DPPH) de los extractos obtenidos de la extracción diclorometano y metanol
De los cinco extractos diclorometánicos y metanólicos se prepararon soluciones de 10 mg mL-1 en etanol a 80% y se siguió la metodología de Kuskoski et al., (2005) y del Laboratorio de Fitoquímica del CP, para evaluar la actividad antioxidante.
Por triplicado se realizó curvas patrón de Trolox (Sigma-Aldrich®, un miligramo sobre mililitro de metanol a 80%,) con concentraciones de 0, 25, 50, 100, 200 y 300 µL y se tomaron también por triplicado 10 µL de las soluciones de los extractos diclorometánicos y metanólicos, en tubos de ensayo. Luego a los tubos de ensayo se les adiciono etanol a 80% hasta completar 400 µL, después se agregaron 500 µL de metanol a 80% y un mililitro de DPPH (Sigma-Aldrich®, 7.5 mg en 50 mL de etanol a 80%). Las mezclas de los tubos de agitaron, se dejaron reposar 30 min en oscuridad y después se les hicieron lecturas a 517 nm en espectrofotómetro de luz ultravioleta-visible. Con las lecturas de la curva estándar se realizaron los cálculos de la actividad antioxidante a partir de las lecturas de los extractos diclorometánicos y metanólicos, y el promedio de los resultados se expresó en microgramos de equivalentes de Trolox sobre gramo de extracto diclorometánico y metanólico (µg de ET g-1 de ED y de EM) y en porcentaje de DPPH inhibido (% de DPPH inhibido). También como referencia se usaron 10 µL de una solución de ácido gálico de 0.1 mg mL-1 en etanol a 80%, la cual es una molécula con fuerte actividad antioxidante.
Análisis estadísticos
Estadística descriptiva se realizó de los datos del rendimiento de extractos y de la cuantificación de metabolitos secundarios y actividad antioxidante los extractos diclorometánicos y metanólicos. Además, se hizo comparación de medias de Student-Newman-Keuls (SNK, n=5, p ≥ 0.05) del contenido de metabolitos secundarios y de la actividad antioxidante de los extractos diclorometánicos y metanólicos. Todos los análisis se realizaron en el programa estadístico Sigma Plot versión 14.0 (Jandel Scientifc, Erkrath, Germany).
Resultados
Rendimiento de los extractos de la resina
De los cinco extractos hexánicos se obtuvo un rendimiento (promedio ± error estándar) de 1.58 ± 0.85 mg g-1 de resina, de los cinco extractos diclorometánicos se logró conseguir una productividad de 990.0 ± 16.5 mg g-1 de resina y de los cinco extractos metanólicos se consiguió un rendimiento de 42 ± 2.5 mg g-1 de resina. De manera que, la productividad máxima de los extractos se logró obtener a partir de la extracción con diclorometano.
Metabolitos secundarios identificados en los extractos de la resina
En los extractos hexánicos solo se identificaron terpenos (Tabla 1), mientras que en los extractos diclorometánicos se encontraron saponinas y terpenos (Tabla 1) y en los extractos metanólicos se descubrieron terpenos, saponinas, fenoles y flavonoides (Tabla 1). A la vez, en los extractos no se identificó la presencia de alcaloides y taninos (Tabla 1).
Tabla 1 Metabolitos secundarios identificados en los extractos de la resina.Table 1. Secondary metabolites identified in the resin extracts.
| Fitoquímica | Reacción | Control positivo | Extracto | Resultado |
|---|---|---|---|---|
| Fenoles | Folin-Ciocalteau | Ácido gálico | Hexano | - |
| Diclorometano | - | |||
| Metanol | + | |||
| Flavonoides | Prueba de Shinoda | Quercetina | Hexano | - |
| Diclorometano | - | |||
| Metanol | + | |||
| Alcaloides | Dragendorff | Lupinus sp. | Hexano | - |
| Diclorometano | - | |||
| Metanol | - | |||
| Saponinas | Prueba de Fehing | Saponina de soya | Hexano | - |
| Diclorometano | + | |||
| Metanol | + | |||
| Taninos | FeCl3 | Ácido tánico | Hexano | - |
| Diclorometano | - | |||
| Metanol | - | |||
| Terpenos | Prueba de Liebermann-Burchard | Ácido masticadenónico | Hexano | + |
| Diclorometano | + | |||
| Metanol | + |
Reacción positiva (+) y negativa (-) de las soluciones de los extractos obtenidos de la extracción con cada disolvente.
Positive (+) and negative (-) reaction of the solutions of the extracts obtained from the extraction with each solvent.
Contenido de saponinas y terpenos totales del extracto obtenido de la extracción con diclorometano
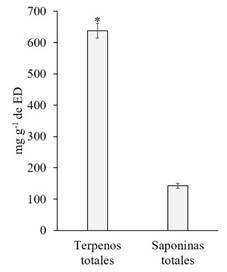
De los extractos diclorometánicos se obtuvo un contenido (promedio ± error estándar) de terpenos totales de 638.2 ± 23.6 mg de EAM g-1 de ED y el de saponinas fue de 142.5 ± 7.7 mg de ESY g-1 de ED. El contenido de terpenos totales fue mucho mayor que el de saponinas totales en los extractos diclorometánicos (Figura 1), mostrando diferencias estadísticas significativas (SNK, n=5, p < 0.001*).
Contenido de fenoles y flavonoides totales del extracto obtenido de la extracción con metanol
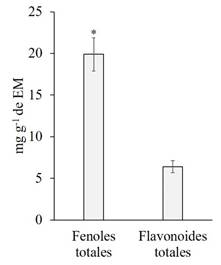
En los extractos metanólicos se obtuvo un contenido (promedio ± error estándar) de fenoles totales de 19.9 ± 2.0 mg de EAG g-1 de EM y el de flavonoides totales fue de 6.4 ± 0.7 mg de EQ g-1 de EM. El contenido de fenoles totales fue más alto que el de flavonoides totales en los extractos metanólicos (Figura 1), teniendo diferencias estadísticas significativas (SNK, n=5, p < 0.001*).
Actividad antioxidante de los extractos obtenidos de la extracción con diclorometano y metanol de la resina
Los extractos diclorometánicos y metanólicos no mostraron efectos antioxidantes. Con altas concentraciones de microgramos equivalentes de Trolox sobre gramo de resina generaron muy poca inhibición de DPPH, con respeto a la actividad antioxidante del ácido gálico (Tabla 2).
Tabla 2 Actividad antioxidante de los extractos diclorometanicos (ED) y metanolicos.Table 2. Antioxidant activity of dichloromethane (DE) and metabolic (ME) extracts.
| Extractos | µg de ET g-1 de extracto | % de DPPH inhibido |
|---|---|---|
| ED | 11400 ± 1207* | 23.95 ± 1.07* |
| EM | 6100 ± 1163* | 26.15 ± 1.95* |
| Ácido gálico | 34 ± 2.6 | 55.0 ± 2.5 |
Promedio ± error estándar de microgramos de equivalentes de Trolox sobre gramo de extracto (µg de ET g-1 de extracto) y porcentaje de DPPH inhibido (% de DPPH inhibido). Diferencias estadísticas significativas de los extractos diclorometanicos y metanolicos con respecto al ácido gálico (SNK, n=5, p < 0.001*).
Mean ± standard error of micrograms of Trolox equivalents per gram of extract (µg of ET g-1 of extract) and percentage of inhibited DPPH (% DPPH inhibited). Statistically significant differences were observed between the dichloromethane and methanol extracts with respect to gallic acid (SNK, n=5, p < 0.001*).
Discusión
Rendimiento de los extractos de la resina
Las resinas del género Bursera tiene una constitución aproximada de 87 a 95% de terpenos (Ferreira et al., 2019), lo que las vuelve altamente solubles en disolventes como etanol (Antúnez-Mojica et al., 2021) y diclorometano (Sánchez-Monroy et al 2021). Esto confirma por que el mayor rendimiento se obtuvo de los extractos diclorometánicos, y la productividad de los extractos hexánicos y metanólicos fue menor. Además, debido al escaso rendimiento de los extractos hexánicos, solo se utilizaron para identificar metabolitos secundarios.
Metabolitos secundarios identificados en los extractos de la resina
En las resinas de Bursera está constituida por mono y sequiterpenos (Blancas et al., 2022; Ferreira et al., 2019), triterpenos (Blancas et al., 2022; Sánchez-Monroy et al 2021), flavonoides (Blancas et al., 2022) y líganos (Antúnez-Mojica et al., 2021; Marcotullio et al., 2018). Lo que corrobora porque encontramos terpenos en los extractos hexánicos, diclorometánicos y metanólicos. Además, encontramos fenoles y flavonoides, pero solo en los extractos metanólicos, lo que es interesante porque los extractos hidroalcohólicos y metanólicos de hojas y tallos de especies del género Bursera son ricos en flavonoides (Sánchez-Monroy et al., 2020; Guevara-Fefer et al., 2017).
El contenido de fenoles en los extractos metanólicos es probable que se relacione con la presencia de lignanos, los cuales son polifenoles solubles en solventes orgánicos (Antúnez-Mojica et al., 2021; Marcotullio et al., 2018).
En las resinas de especies de género Bursera no se ha reportado la presencia de saponinas, sin embargo, en el extracto etanólico del tallo de B. fagaroide se registró la aparición de este tipo metabolitos secundarios en 1998 y en el extracto obtenido de la combinación de diclormetano-metanol y metanol-agua de especies del género Bursera se identificaron glucósidos asociados a flavonoides, esteroles y triterpenos (Columba-Palomares et al., 2018; Guevara-Fefer et al., 2017). Lo que puede explicar la presencia de saponinas en los extractos diclorometánicos y metanólicos.
En los extractos no se identificaron alcaloides y taninos, pero esto es de esperarse, debido a que no existen reportes de la presencia de este tipo de metabolitos secundarios en las resinas de especies del género Bursera (Blancas et al., 2022).
Contenido de saponinas y terpenos totales del extracto obtenido de la extracción con diclorometano
En los extractos diclorometánicos, por tener el mayor rendimiento, se evaluó el contenido de terpenos y saponinas. Como se mencionó antes los terpenos constituyen entre un 87 a 95% de los componentes de la resina (Ferreira et al., 2019). El rendimiento de terpenos del extracto fue de 63 a 66%, menor al reportado en la literatura. No obstante, los terpenos siguen siendo el componente mayoritario de los extractos diclorometánicos.
En el caso de las saponinas no hay investigaciones que respalden su contenido en especies del género Bursera (Blancas et al., 2022), sin embargo, en esta investigación constituyeron del 14 a 15% de los extractos diclorometánicos.
Contenido de fenoles y flavonoides totales del extracto obtenido de la extracción con metanol
En los extractos metanólicos se identificaron fenoles y flavonoides, por lo que, en ellos se realizó la cuantificación de estos metabolitos secundarios. Además, como en los extractos diclorometánicos se cuantificaron saponinas, no se analizó el contenido de este metabolito secundario en los extractos metanólicos.
En el extracto etanólico de hojas de B. microphylla se registró un contenido de fenoles del 24 a 25% (Vidal-Gutiérrez et al., 2020b), que si lo comparamos con la cantidad de fenoles presente en los extractos metanólicos de 1.9 a 2.1%, la presencia de estos metabolitos secundarios es poca. Lo mismo sucede en el caso de los flavonoides donde se encontró que los extractos etanólicos de tallos de especies del género Bursera tienen un contenido de flavonoides de 5 a 10% y el de hojas fue de 6 a 40%, si se compara con la cantidad de flavonoides de los extractos metanólicos de 0.6 a 0.7% (Sánchez-Monroy et al., 2020), también la presencia de estos metabolitos secundarios es baja. A la vez, B. fagaroide es la especie del género Bursera que contiene la menor cantidad de flavonoides en tallos y hojas (Sánchez-Monroy et al., 2020). Por lo que, es un dato relevante encontrar este tipo de metabolitos secundarios en el extracto metanólico de la resina.
Actividad antioxidante de los extractos obtenidos de la extracción con diclorometano y metanol de la resina
En la literatura se registró que los extractos metanolicos de la resina de B. hindsiana y B. microphylla, no presentaron actividad antioxidante por el método de DPPH (Vidal-Gutiérrez et al., 2020a). Por lo que, los extractos de la resina de B. fagaroides al tampoco tener propiedades antioxidantes se suman a los resultados antes mencionados. Sin embargo, hay que destacar que los extractos metanólicos de la resina de B. laxiflora tienen potencial antioxidante, inhiben el 50% de DPPH con 100 µg de ET g-1 de EM (Vidal-Gutiérrez et al., 2020a). A la vez, extractos hidroalcohólicos y etanólicos de hojas (Vidal-Gutiérrez et al., 2020b; Sánchez-Monroy et al., 2020; Guevara-Fefer et al., 2017), hidroalcohólicos de tallos (Sánchez-Monroy et al., 2020), etanólicos de frutos (Vidal-Gutiérrez et al., 2020b) y lignanos (Marcotullio et al., 2018) de especies del género Bursera presentan excelentes propiedades antioxidantes. Al igual que los extractos hidroalcohólicos de tallos y hojas de B. fagaroides que inhiben el 50% de DPPH con 15.41 y 5.72 µg mL-1 (Sánchez-Monroy et al., 2020).
Conclusiones
Los extractos de la resina de Bursera fagaroides son una fuente rica de terpenos, que pueden contener saponinas, fenoles y flavonoides en baja concentración, y no presentan propiedades antioxidantes por el método de 2,2-difenil-1 picrilhidrazil. De igual manera, se realizó el primer reporte de la presencia y cuantificación de ácidos fenólicos y saponinas en el extracto de diclorometano y metanol de la resina.
Esta investigación aporta un estudio general del análisis de los extractos de resina de Bursera fagaroides, para futuros experimentos se recomienda un análisis fitoquímico con técnicas de cromatografía liquida de alta resolución acoplada a espectrometría de masas, resonancia magnética nuclear de protón o análisis metabolómicos masivos para identificar o corroborar el tipo de terpenos, saponinas, fenoles y flavonoides presentes en los extractos de la resina.