Introducción
La familia Lamiaceae está ampliamente distribuida, sus especies poseen valor biotecnológico y potencial farmacológico. Dentro de los géneros incluidos en esta familia se encuentra Salvia, con 900 especies en la República Mexicana (Martínez-Gordillo et al., 2017), las cuales presentan gran diversidad en sus formas de crecimiento, producen abundantes y diversos metabolitos secundarios además de mostrar una morfología floral llamativa por su belleza, se consideran ornamentales (Ramírez-Zea et al., 2016). Algunas especies se desarrollan en zonas cuyas temperaturas diarias exceden los 33°C en verano, promoviendo estrés por calor, suelos poco apropiados para el cultivo, lo cual inhibe el crecimiento y altera el desarrollo de las plantas. En la actualidad no se conoce algún método útil para fenotipificar la susceptibilidad de estas plantas a las altas temperaturas y elevadas intensidades lumínicas, que permitan medir la tolerancia sostenible al calor y que sirva como base para evaluar el rendimiento y la adaptación de las plantas de Salvia en determinadas zonas de cultivo (Lin et al., 2021).
Aunque hay datos relacionados con el comportamiento del desarrollo de plantas del género Salvia bajo algunas condiciones, como el estrés hídrico (Bayat & Moghadam, 2019), salino y oxidante inducido con ozono (Lin et al., 2020); hay poca información sobre la morfología, fisiología y bioquímica de plantas de Salvia cultivadas bajo estrés por altas temperaturas y modificaciones en la intensidad lumínica (Lin et al., 2021).
Salvia elegans Vahl, es nativa de México y Centroamérica. Es una herbácea semileñosa, perenne, de 1 a 1.5m de altura. Es una especie que crece en climas templados entre los 2280 y 3100 msnm asociada a los bosques de pino, encino y mixto. Se desarrolla en suelos bien drenados y húmedos todo el año; preferentemente cubiertos por rocas ígneas con pH ácido (5-7), con diferentes texturas (arenosos o arcillosos), pedregosos y laderas de cerros. En la República Mexicana se puede encontrar en los estados de Sonora, Chihuahua, Durango, Michoacán, Hidalgo, Estado de México, Morelos, México D.F., Veracruz y Oaxaca (Argueta et al., 1994).
Es utilizada en la medicina tradicional mexicana en forma de cataplasma para tratar trastornos asociados a la inflamación como, por ejemplo, edemas, heridas y golpes (Argueta et al., 1994). Es endémica de nuestro país, donde está ampliamente distribuida (Martínez-Gordillo et al., 2017), lo cual promueve que la composición y concentración de sus metabolitos secundarios varíen según su hábitat (Ricciardi & Ricciardi, 2000). Con base en los reportes etnomédicos y farmacológicos mencionados más adelante, esta especie resulta de interés medicinal, por esta razón es indispensable que la composición de sus compuestos activos sea homogénea y para ello se requieren condiciones controladas de cultivo.
Al ser S. elegans una especie ampliamente distribuida, es muy probable que la composición y cantidad de principios activos (metabolitos secundarios) varíe de acuerdo con su hábitat (Ricciardi & Ricciardi, 2000). De aquí que su propagación bajo condiciones controladas, resulte ser una buena alternativa para asegurar la concentración constante y homogénea de sus principios activos.
Una opción es la propagación vegetativa o clonal, que consiste en generar nuevos individuos a partir de tejidos vegetales diferenciados (Gautam et al., 2021). Es utilizada cuando la probabilidad de germinación de las semillas es muy baja la cual, en el caso de las plantas medicinales y aromáticas, a veces es inferior al 50%. Lo anterior fue comprobado en esquejes de la especie S. officinalis L. que promovieron el enraizamiento por esqueje, aunque este proceso se vio favorecido significativamente por la aplicación de productos de enraizamiento Cytokin® y Radix® (Nicola et al., 2005). De hecho, se ha reportado que esta técnica de propagación favorece el enraizado de esquejes de S. uliginosa silvestre, comparada con esquejes de esta especie sometidos a 10, 20, 30, 40 ó 50 Gy de rayos gamma procedentes de una fuente de 60Co (Maynard & Ruter, 2024).
Se ha reportado que las especies del género Salvia, entre ellas S. elegans, S. officinalis o S. miltiorrhiza, tienen la capacidad de producir monoterpenos, sesquiterpenos, triterpenos, cumarinas, sacáridos y flavonoides en las partes aéreas, y en la raíz ácidos fenólicos y diterpenos (Karpiński, 2020); (Martínez-Hernández et al., 2021); (Martínez-Hernández et al., 2024).
Farmacológicamente, se ha demostrado desde el 2006 que el extracto hidroalcohólico de hojas de S. elegans a diferentes dosis en ratas a 3.12, 12.5, 25 y 50 mg/kg (Mora et al., 2006) y en ratones ICR a 125, 250, 500, 1000 y 2000 mg/kg (Herrera-Ruiz et al., 2006), ejerce efecto antidepresivo, ansiolítico y sedante. Posteriormente en el 2010, se mostró que el extracto hidroalcohólico de partes aéreas (flores, hojas y tallos) y dos fracciones obtenidas de este (butanólica, así como la fracción nombrada SeF8-22) contienen flavonoides y fenilpropanoides, además de poseer efecto antihipertensivo al actuar como inhibidor de la enzima convertidora de la angiotensina (ECA) (Jiménez-Ferrer et al., 2010). Para el 2020 se identificó que la mezcla de dos terpenos rosignol y agarospirol administrados a las dosis de 0.01, 0.1, 0.5, 1.0 y 2.0 mg/kg vía oral a ratones ICR, fueron capaces de provocar efecto antidepresivo, cuando los animales fueron expuestos a la prueba de Natación forzada (NF) (Martínez-Hernández et al., 2021). En un estudio químico-biodirigido se aislaron de esta especie, 17 compuestos que fueron evaluados en el ensayo in vitro de inhibición de la ECA, siendo los más activos el ácido rosmarínico, los flavonoides isosakuranetina-5-O-rutinósido y neoeriocitrina (Gutiérrez-Román et al., 2021). En el 2018 se registró que la decocción de partes aéreas (hojas, flores y tallo) de S. elegans, posee efecto antioxidante por actuar como “scavenger” de radicales libres como el DPPH•, NO• y O₂•⁻; además de mostrar la capacidad de reducir Fe3+ y evidenciaron un efecto inhibidor de las enzimas α-glucosidasa y xantina oxidasa (Pereira et al., 2018).
Recientemente, se publicó que el extracto hidroalcohólico de partes aéreas (100 mg/kg), la fracción de acetato de etilo SeFAc (50 mg/kg) y una sub-fracción nombrada SeF3 (10 mg/kg), pueden actuar sobre una parte de la fisiopatología asociada al síndrome metabólico en ratones que ingirieron una dieta hipercalórica. Por ejemplo, redujeron los niveles séricos de glucosa, triglicéridos y colesterol, el índice de adiposidad y la resistencia a la insulina. Además, actuó como inmunomodulador en diferentes órganos al disminuir citocinas inflamatorias, además de ejercer un efecto antidepresivo y disminuir los niveles de corticosterona en sangre. Asimismo, se reportó la presencia del ácido rosmarínico, ácido cafeico a través de gases masas, glicerol y algunos esteroles como el Stigmastano‐3,5‐dieno y acetato de campesterol (Martínez-Hernández et al., 2024).
Debido a que en los últimos años S. elegans ha sido reportada con efectos farmacológicos relevantes, la convierten en una especie con posibilidades de continuar con su estudio y de ser posible, llegar a la clínica, y generar la necesidad de realizar estudios sobre la obtención de material vegetal bajo condiciones controladas. En este sentido, el objetivo de este trabajo fue, por un lado, evaluar el crecimiento y el desarrollo foliar (densidad estomática, área y color) de esquejes de S. elegans, introducidos en sustratos sólidos químicamente activos, inertes y en solución nutritiva, cultivados bajo dos intensidades de luz diferentes y, además, evaluar el efecto antiinflamatorio del extracto hidroalcohólico de las partes aéreas y raíces de las plantas cosechadas.
Materiales y métodos
Material vegetal
Se colectaron las plantas silvestres de S. elegans en la localidad de Ozumba, Estado de México (19°2′21″ N, 98°47′37″ W) y posteriormente fueron adaptadas en el Laboratorio de Biotecnología del Centro de Desarrollo de Productos Bióticos del Instituto Politécnico Nacional (CEPROBI-IPN). A partir del material cultivado bajo diferentes condiciones de cultivo (partes aéreas y raíces), se prepararon extractos hidroalcohólicos en el Laboratorio de Química del Centro de Investigación Biomédica del Sur del Instituto Mexicano del Seguro Social (CIBIS-IMSS). Un ejemplar fue enviado al Herbario del IMSS (IMSSM), para ser identificado como IMSSM-14588, por la M.Sc. Abigail Aguilar Contreras.
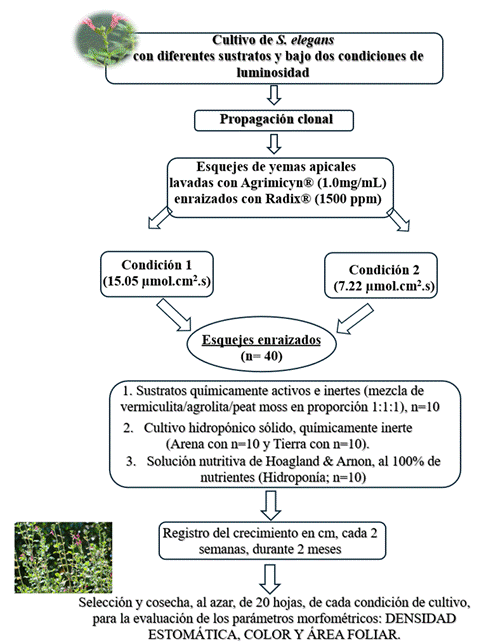
Cultivo de s. Elegans en diferentes sustratos bajo dos condiciones de luz
Con el objetivo de evaluar si el sustrato y la intensidad lumínica ejercen algún efecto sobre el crecimiento y/o el desarrollo foliar de S. elegans, se planteó el siguiente diseño experimental:
Inicialmente, se obtuvieron esquejes a partir de yemas apicales de una planta madre sana, se recortaron en segmentos de 10 cm de longitud y se eliminaron las hojas de la parte inferior de cada esqueje. Posteriormente, se lavaron con agua destilada y se sumergieron en una solución de Agrimicyn® (1 mg/ml) durante 1 min. Se estableció un lote experimental con 17 estacas, para promover el enraizado se removieron las hojas situadas cerca del corte inferior, cada estaca se impregnó con Radix® a una concentración de 1500 ppm y fueron introducidas en un orificio de 3 cm de profundidad (Maynard & Ruter, 2024).
Posteriormente, se eligieron al azar esquejes enraizados, para introducirlos en macetas para vivero de plástico (4 in), empleando sustratos sólidos químicamente activos e inertes de la siguiente manera: a) Mezcla de vermiculita/agrolita/peat moss; en proporción 1:1:1 (agrolita; n=10); b) Cultivos hidropónicos sólidos químicamente inertes, con arena (n=10) y con tierra (n=10) y otros en solución de Hoagland & Arnon (Hoagland & Arnon, 1950) al 100% de nutrientes (Hidroponía; n=10). Los sistemas de cultivo previamente mencionados (sólidos y solución nutritiva), se establecieron por triplicado y evaluaron bajo dos diferentes condiciones de cultivo entre los meses de septiembre y octubre del año 2006. Para tal efecto, el sistema de cultivo se reprodujo. La condición uno (C1), de alta intensidad lumínica registrada como cantidad de fotones por unidad de área y unidad de tiempo (15.08 µmol.cm2.seg-1), situada dentro de los invernaderos del Centro de Desarrollo de Productos Bióticos, en el municipio de Yautepec, Morelos (18°49'29.4"N 99°05'46.0"W), en un ambiente que registró promedios de humedad relativa (HR) de 26.0%, temperatura (T) mínima de 22.3ºC y máxima de 33.8ºC. La condición 2 (C2), de baja intensidad lumínica (7.22 µmol.cm2.seg-1), HR de 32.9%, T media mínima y máxima de 30.8 ºC y 39.4 ºC respectivamente, situada en el exterior, a un costado de los invernaderos y cubierta por una malla de sombra al 50 %. Durante ocho semanas, se mantuvo la humedad de los sustratos sólidos activos e inactivos, administrando 200 ml de agua cada dos días y se registró el crecimiento de la parte aérea de los especímenes (cm), cada dos semanas (Diagrama 1).
Evaluación del desarrollo foliar, a través de parámetros morfométricos
Para los parámetros morfométricos se cortaron, al azar, para cada experimento cuarenta hojas de las plantas de S. elegans cultivadas en cada condición lumínica y al azar se eligieron veinte de cada una (n=20). Los experimentos se efectuaron por triplicado. Para analizar los parámetros morfométricos relativos al área foliar y el color, se tomaron imágenes de las hojas empleando una cámara digital (Sony, MVC-CD500) y se almacenaron en formato jpg (color RGB, 24 bits; 640 x 480 píxeles).
Densidad estomática
La densidad estomática se midió utilizando 20 hojas, en la región adaxial y la abaxial se aplicó esmalte de uñas transparente de marca comercial Renova® en la parte media, se dejó secar por 5 min y posteriormente, con ayuda de una pinza de disección, se retiró la película de esmalte (Barrera & Mesa, 1992).
La película se estableció como una preparación fija, que fue observada en un microscopio óptico (Nikon, Eclipse i80) a 20X, con una cámara adaptada (Dage Mita, DC300) con la cual se obtuvieron imágenes de la región adaxial y abaxial de las hojas procesadas de ambas condiciones de cultivo. Las imágenes colectadas fueron procesadas usando el software MetaMorph (V.7.0). Para calcular densidad estomática, se siguió la metodología reportada por Barrera y Mesa (1992) en la cual establecen un área de muestra de 0,5 x 0, 4 mm, al considerar que 0,4 mm corresponde al ancho de la banda estomática, región donde se cuantifican las estomas y se sitúa en la zona central del envés de la hoja. Se realizaron tres mediciones por área de muestra para cada preparación y se registró el promedio (número de estomas/μm2).
Área foliar
Las imágenes en formato jpg, se procesaron utilizando el programa Corel Photo Paint (V11.5). Para transformarlas a escala de grises de 8 bits, se realizó un contraste y se imprimieron en una impresora digital a 600 dpi. El área foliar (cm2) se obtuvo colocando en un medidor de área foliar (marca LICOR modelo 3100) las impresiones de las hojas (Husin et al., 2012).
Color
Se empleó el software Image J (V.1.52) para la evaluar el color de las hojas en las imágenes digitales (RGB, 24 bits) capturadas previamente. Los valores digitales, fueron transformados a un sistema de notación descrito en la carta de colores Munsell para tejidos vegetales (Pérez et al., 2008) y la interpretación se realizó tomando en cuenta lo que sugiera el sistema CIE de colorimetría, según Schanda (Shanda J., 2007).
Los valores RGB se transformaron a unidades de luminosidad (L*), tono rojo-azul (a*) y tono verde-amarillo (b*) utilizando el software EasyRGB-PC (V.1.53). La diferencia de color (ΔE) entre ambas condiciones de intensidad luminosa se determinó según Schanda (Shanda J., 2007), con la ecuación:
Donde:
ΔE: diferencia de color entre las muestras foliares colectadas de C1 y C2.
ΔL*: Diferencia de luminosidad entre las muestras foliares colectadas de C1 y C2.
Δa*: Diferencia de tonalidad rojo-azul entre las muestras foliares colectadas de C1 y C2.
Δb*: Diferencia de tonalidad verde-amarillo entre las muestras foliares colectadas de C1 y C2.
Utilizando el programa Prism@, V1.10 (Quintanilla-Carvajal et al., 2015) se transformaron los datos RGB y L*a*b* a datos Munsell digitalizados, se reportaron como RGB y CIELab y se compararon con el croma (C, saturación), matiz (H) y valor (V, luminosidad u oscuridad) del sistema de notación Munsell (HV/C) según (Mathias-Rettig & Ah-Hen, 2014).
Extracto hidroalcohólico
Se obtuvieron extractos hidroalcohólicos de las partes aéreas (tallos, hojas y flores) y de raíces de S. elegans (C1 y C2); para ello, las muestras se secaron a temperatura ambiente en condiciones de oscuridad durante 2 semanas, posteriormente el material vegetal seco, se molió y maceró en una solución de etanol y agua (60:40) durante 24 h. Después, cada extracto se filtró con papel Whatman #1; el material sólido filtrado, se maceró, filtró y concentró en dos ocasiones más, las cuales se reunieron y se calcularon los porcentajes de rendimiento. Finalmente, se liofilizaron (Heto Drywinner Brand, Modelo DW3, USA) y mantuvieron en refrigeración (4ºC) hasta su posterior uso.
Cada extracto hidroalcohólico fue etiquetado como:
SeC1r: Raíces de plantas cultivadas en C1.
SeC1a: Partes aéreas de plantas cultivadas en C1.
SeC2r: Raíces de plantas cultivadas en C2.
SeC2a: Partes aéreas de plantas cultivadas en C2.
SeHa: Partes aéreas de plantas en solución hidropónica en C2.
Los esquejes cultivados en solución hidropónica en la condición 1, fueron descartados debido a que la producción de biomasa en dicho cultivo fue escasa para la obtención de extractos. Lo mismo ocurrió con las raíces de los esquejes cultivados en solución nutritiva de ambas condiciones.
Animales de experimentación
Ratones macho ICR (
Ensayo de Edema local inducido por un éster de forbol (actividad antiinflamatoria)
Cada extracto fue administrado (disuelto en acetona), en la oreja izquierda (OI) y en la oreja derecha (OD) se administró el vehículo (control con acetona) en un volumen total de 10 μL en la parte interna y en externa del pabellón auricular. Los ratones se dividieron en control negativo [(VEH; 2.5 μg/oreja de 12-O-Tetradecanoilforbol 13-acetato (TPA)], control positivo, con dexametasona (DEX, 1.0 mg/oreja), los tratamientos de S. elegans (SeC1r, SeC1a, SeC2r, SeC2a, SeHa) a 1.0 mg/oreja (Payá et al., 1993). Quince minutos posteriores a la aplicación de cada tratamiento, se colocó el TPA en la OI y 4 h después, los animales fueron sacrificados con una sobredosis de pentobarbital sódico (NOM-062-ZOO-1999). Se tomaron secciones circulares de 6 mm de diámetro tanto de las orejas tratadas (t; OI) como de las no tratadas (nt; OD), las cuales se pesaron para determinar la inflamación y el porcentaje de inhibición empleando la siguiente fórmula:
Donde: Δp = pt - pnt
∆pt= peso de la sección de la oreja tratada.
pnt= es el peso de la sección de la oreja no tratada.
Cromatografía en capa fina (CCF)
Se utilizaron placas de gel de sílice 60-F254, con 2 µL de cada extracto y se marcó la posición inicial del desplazamiento del solvente en la placa. La fase móvil utilizada fue cloroformo: metanol (9:1). Una vez transcurrida la cromatografía, las placas fueron observadas con una lámpara de luz UV a 254 nm de longitud de onda y con luz visible. Además, las placas fueron reveladas aplicando una disolución de sulfato cérico amoniacal disuelto en ácido sulfúrico concentrado, para obtener una solución final del revelador con valor de concentración de 2N, posteriormente se calentaron en una parrilla a 100 °C por 3 min, para visualizar la presencia de terpenos en color marrón (Carratù et al., 2010).
Otro sistema utilizado fue una solución metanólica de difenilboriloxietilamina (c) al 1% en una solución etanólica de polietilenglicol-4000 al 5%, para mostrar la presencia de flavonoides que pueden revelar en color amarillo hasta naranja (Carratù et al., 2010). Se capturaron imágenes de cada placa (antes y después de revelar) y se identificaron los diferentes compuestos con base en la migración de los estándares de referencia para terpenos: Ácido Oleanóico (AO), Ácido Ursólico (AU) y para flavonoides quercetina (Q). Finalmente, se midió el factor de retención (Rf), de los estándares y de los extractos analizados en la CCF. Los Rf se determinaron aplicando la ecuación:
Rf = distancia que recorre la muestra desde el punto de aplicación/distancia que recorre el solvente hasta el frente del eluyente.
Análisis estadístico
El análisis estadístico de los datos obtenidos durante las dos fases experimentales (crecimiento, densidad estomática, área foliar, color y pruebas biológicas) y para la prueba de inflamación, se realizó con ANOVA de una vía con una post-prueba de Bonferroni, con un valor de significancia de p<0.05, en el programa estadístico SPSS V.17. La medida de distribución normal de cada ensayo se hizo con Shapiro-wilk, con un valor de p > que 0.05, para considerarlo como distribución normal.
Resultados
Cultivo de S. elegans
En la Figura 1A, se muestran los resultados del crecimiento de esquejes de S. elegans cultivados en la condición C1 (barras grises), se puede observar que las plantas colocadas en solución nutritiva (Hidroponía), crecieron 66.3±4.15 cm, valor estadísticamente mayor al obtenido en los sustratos sólidos de Agrolita (vermiculita/agrolita/peat moss; 32.02±2.79 cm), de Arena (27.82±4.2 cm) y de Tierra (41.93±4.55 cm) (p <0.05). Con un crecimiento de las plantas de mayor a menor de la siguiente manera: hidroponía>tierra>agrolita>arena, no hubo diferencia entre arena y agrolita (p >0.05, Figura 1A).
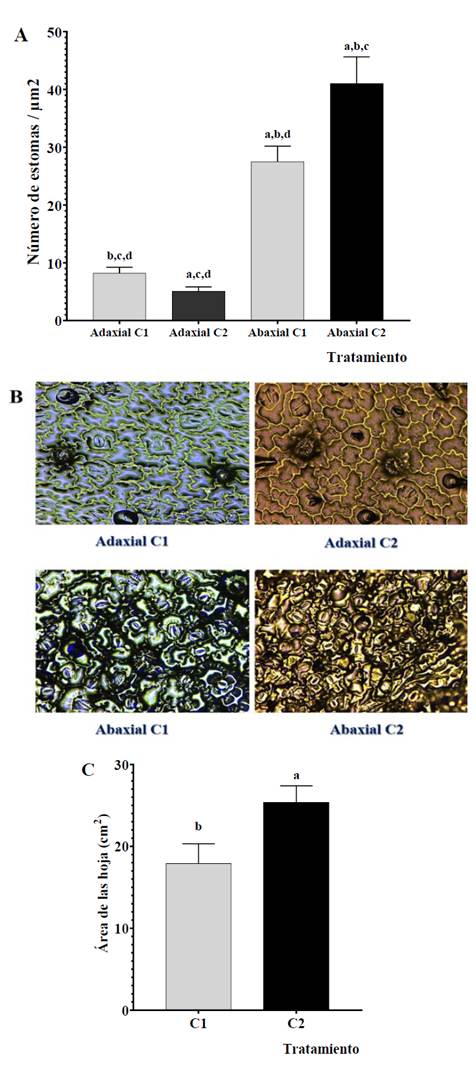
Figura 1 Crecimiento de los esquejes de S. elegans (cm) en diferentes tipos de sustratos y condiciones de luz C1 (A) o C2 (B). n= 10; ANOVA ± desviación estándar; post prueba de Bonferroni, p < 0,05. Los símbolos a, b, c y d, indican diferencias con el tratamiento con arena, con tierra, con hidroponía y con agrolita, respectivamente (n=10;
En la condición C2, se observó un crecimiento de 44.68±3.42 cm en el tratamiento con hidroponía, significativamente mayor al del grupo con arena (29.01±2.89) o con tierra (33.89±0.30) (p <0,05, Figura 1B). El cultivo en agrolita con un crecimiento de 36±5.5 cm, no induce cambios estadísticamente significativos cuando se compara con los grupos con hidroponía, o con tierra o con arena (p >0.05, Figura 1B).
Parámetros morfométricos y de color durante crecimiento y desarrollo foliar
Densidad estomática y área foliar
La densidad de estomas en las regiones adaxiales de las hojas provenientes de C1 (8.95

Figura 2 Densidad estomática (A) de plantas de S. elegans que crecen en diferentes condiciones de luz, C1 (□) y C2 (■). (B) microfotografías de los estomas en las regiones adaxiales y abaxiales; el área foliar C se representa como el tamaño del follaje en cm2. ANOVA post prueba Bonferroni; p< 0,05 (n=20;
Color
En la Tabla 1, se muestran los datos obtenidos del análisis por colorimetría realizado en hojas de S. elegans cultivadas bajo las condiciones C1 y C2.
Como sugiere el sistema CIE de colorimetría expuesto por Schanda (2007), para los valores de color normalizados con un iluminante D65 (luz diurna) y una posición del observador de 10º, se encontró que el color de las hojas entre ambas condiciones es ligeramente diferente, como se indica con un ΔE= 2.65.
Tabla 1 Resultados de colorimetría de hojas de S. elegans cultivadas en dos condiciones de luz (n= 40).Table 1. Colorimetric results of S. elegans leaves grown in two light conditions (n= 40)
| Condición de cultivo | R | G | B | L* | a* | b* |
|---|---|---|---|---|---|---|
| C1 | 47.87 | 78.13 | 27.48 | 29.79 | -21.46 | 26.39 |
| C2 | 56.18 | 82.60 | 31.21 | 32.07 | -20.26 | 27.01 |
ΔE (C1, C2) = 2.65
La diferencia antes mencionada también se observa en el diagrama de cromaticidad tomado del CIE (Figura 3), el cual sitúa los valores medios de ambas condiciones (Shanda J., 2007). De acuerdo con lo anterior, el tono dominante en el sistema RGB fue G, ya que las hojas eran verdes. Sin embargo, a pesar de que el análisis mostraba que ambas condiciones coincidieron en G, se observó que el dato correspondiente al color de hojas cultivadas en C2 mostró una mayor contribución en R y B en comparación con aquellas provenientes de C1 (Tabla 1) (Mathias-Rettig & Ah-Hen, 2014). La variabilidad instrumental de RGB y CIEL*a*b* fueron traducidas al sistema Munsell digitalizado (Jiménez-Aparicio & Gutiérrez, 2000); (Mathias-Rettig & Ah-Hen, 2014) y se observó que ambas muestras eran verde-amarillentas (5GY) y las diferencias se relacionaban con las contribuciones de V (luminosidad u oscuridad) y C (saturación). Por lo tanto, el color de las hojas cultivadas en C1 era menos claro, mientras que aquel de C2 tiene una mayor contribución del croma amarillo (Figura 3).
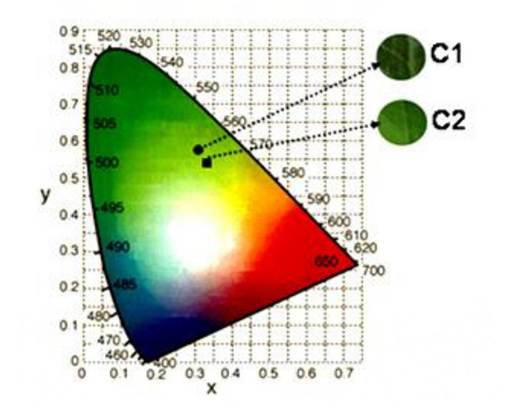
Figura. 3 CIE, diagrama de cromaticidad que muestra la diferencia de color de las hojas de plantas de S. elegans, cultivadas en las condiciones C1 y C2.
En este sentido, el color de las hojas de C1 presentaron mayor intensidad en el verde en comparación con las de C2, que fueron verde-amarillentas; este aspecto se destaca con el valor de L* (luminosidad), donde los valores que tienden a 100 corresponden al blanco y los cercanos a 0, al negro. El valor de C1 fue menor que C2 en términos de L* y su apariencia es más oscura. En la Figura 3, se muestran las diferencias, posicionando el color para ambas condiciones.
Edema local inducido por TPA
El TPA provocó un edema significativo en la oreja (control negativo VEH, Tabla 2), que fue significativamente disminuido en un 85.2% por la DEX (control positivo, *p <0.05). Todos los tratamientos experimentales fueron activos, y presentaron diferencias estadísticas significativas en comparación con el VEH (*p <0.05), con excepción de SeC2r (p >0.05). El tratamiento SeC1a indujo el mayor porcentaje de inhibición del edema (81.82%), por lo que fue seleccionado para una curva dosis-respuesta (0.25, 0.5, 2.0, 4.0 mg/oreja). En la Tabla 2, se observa que las dosis bajas no inducen cambios significativos respecto al grupo de control negativo VEH (p >0.05), pero las dosis altas disminuyen el edema por encima del 80%, valores significativamente menores al grupo VEH (*p <0.05). Los valores farmacodinámicos fueron Emáx= 68.49 % y DE50=2.42 mg/oreja.
Tabla 2 Efecto de la administración local del extracto hidroalcohólico de plantas de S. elegans cultivadas a diferentes condiciones, sobre la inflamación inducida con TPA en oreja de ratón.Table 2. Local administration effect of S. elegans hydroalcoholic extract from plants grown at different conditions on TPA-induced inflammation in mouse ear.
| Tratamiento | Dosis (mg/oreja) | Edema de oreja (mg) | Inhibición del edema (%) |
|---|---|---|---|
| VEH | 8.8 ±1.15 | --- | |
| DEX | 0.5 | 1.3 ±0.18* | 85.23 |
| SeHA | 1.0 | 2.46 ±0.75* | 72.05 |
| SeC1r | 2.28 ±0.41* | 74.09 | |
| SeC1a | 1.6 ±0.47* | 81.82 | |
| SeC2r | 6.36 ±0.86* | 27.73 | |
| SeC2a | 3.16 ±0.32* | 64.09 | |
| Curva dosis-respuesta | |||
| SeC1a | 0.25 | 8.8 ±1.15 | 7.77 |
| 0.5 | 6.44 ±1.07 | 18.18 | |
| 1.0 | 1.6 ±0.47* | 81.82 | |
| 2.0 | 0.93 ± 0.54* | 89.39 | |
| 4.0 | 0.4 ±0.38* | 95.45 | |
Grupo vehículo (VEH); dexametasona (DEX), Raíz C1 (SeC1r), Aérea C1 (SeC1a), Raíz C2 (SeC2r), Aérea C2 (SeC2a), extracto de cultivo hidropónico partes aéreas (SeHa). ANOVA post hoc Bonferroni, *p ≤ 0.05 (n=6;
Vehicle group (VEH); dexamethasone (DEX), C1 Root (SeC1r), C1 Aerial (SeC1a), C2 Root (SeC2r), C2 Aerial (SeC2a), hydroponic culture aerial parts extract (SeHa). ANOVA post hoc Bonferroni, *p ≤ 0.05 (n=6;
Perfil químico cualitativo
El análisis químico preliminar realizado con CCF, permitió analizar los extractos tipo hidroalcohólico provenientes de partes aéreas (SeC1a, SeC2a y SeHa) y raíces (SeC1r y SeC2r) de S. elegans cultivados en C1 y C2, así como del extracto hidroalcohólico de especímenes que crecieron de forma silvestre (SeS). Para ello, las muestras fueron comparadas contra estándares de terpenos, en este caso el ácido oleanóico (AO) y el ácido ursólico (AU) así como del flavonoide Quercetina (Q).
La detección de compuestos fue realizada al comparar los valores de Rf obtenidos de las bandas observadas de cada muestra, con aquellos registrados para cada estándar (Tabla 3).
Tabla 3 Análisis del rendimiento de extracción y del perfil químico cualitativo realizado a través de cromatografía en capa fina de los extractos hidroalcohólicos de partes aéreas y de raíces de plantas de S. elegans cultivadas en dos condiciones de luz y de plantas silvestres.Table 3. Extraction yield and qualitative chemical profile analysis performed by thin layer chromatography of hydroalcoholic extracts from aerial parts and roots of S. elegans plants grown under two light conditions and from wild plants.
| Extracto | Estándares (Rf) | Rendimiento (%R) | ||
|---|---|---|---|---|
| AO (0.34) | AU (0.32) | Q (0.72) | ||
| SeC1a | + | + | - | 20.55 |
| SeC2a | + | - | + | 6.78 |
| SeHa | - | - | - | 44.89 |
| SeC1r | - | - | - | 11.41 |
| SeC2r | - | - | - | 5.12 |
| SeS | + | + | - | 39.87 |
De acuerdo con la metodología empleada en el presente trabajo, el material vegetal cosechado de S. elegans C1 y C2, el rendimiento de algunos extractos fue menor al 20 % y sólo SeC1a, SeHa y el de la planta silvestre SeS, rebasan dicho valor (Tabla 3). De acuerdo con lo anterior, se decidió utilizarlos principalmente para las pruebas farmacológicas. Al término de la evaluación farmacológica, los residuos de cada extracto se emplearon para la identificación preliminar de compuestos presentes en ellos a través de CCF y evaluar las diferencias y semejanzas químicas entre estos.
Los tratamientos de S. elegans, al ser comparados con los estándares de los terpenos AU y AO y del flavonoide Q, empleando un sistema de elución de CHCl3: acetonitrilo: MeOH (1:2:1) y revelando con difenilborato de aminoetanol no se detectó alguna mancha amarillo-anaranjado que revelaría la presencia de flavonoides. Sin embargo, al revelar con Sulfato cérico, se logró detectar la banda que correspondía para Q en la muestra SeC2a. Por otro lado, la comparación de los extractos con actividad antiinflamatoria con los estándares AU y AO, en un sistema de elución CHCl3: Acetona (9:1) que fue revelado con sulfato cérico, se pudo confirmar que AU está presente en SeC1a y SeS; mientras que en el extracto SeC2a al parecer sólo tiene AO al ser analizado por esta técnica cualitativa (Tabla 3).
Discusión
A la fecha no se han reportado datos de un estudio sobre métodos de cultivo para obtener material vegetal estandarizado de S. elegans. En este trabajo se propone que esta especie medicinal puede lograr ser cultivada de una forma controlada en condiciones de hidroponía, ya que como se sabe es una excelente técnica de propagación, que proporciona un alto rendimiento de biomasa y de metabolitos secundarios con actividades farmacológicas (Dayani & Sabzalian, 2017), permite controlar el volumen de agua de riego y la eliminación de contaminantes, disminuyendo el impacto negativo al medio ambiente (Maggini et al., 2022). El cultivo bajo condiciones controladas, por ejemplo, de luz y temperatura, es una alternativa para producir plantas medicinales, asegurando la obtención constante y homogénea de sus principios activos debido a que la fotosíntesis y la acumulación de masa es constante (Aggarwal y Mathur, 2020). Observamos que, para esta planta mexicana, las condiciones de luz en cultivo hidropónico fueron determinantes para el mejor crecimiento y desarrollo. Se mostró que la superficie adaxial de las hojas de S. elegans cultivadas bajo altas intensidades de luz, desarrolló mayor densidad estomática, resultados similares se han reportado en tomate (Gay & Hurd, 1975), tabaco (Thomas et al., 2004) y Arabidopsis (Wang et al., 2007). Se ha observado que el movimiento, tamaño, distribución y densidad de las estomas son factores que determinan el intercambio de agua y CO2, por tanto, la fotosíntesis y la transpiración son indispensables para el crecimiento y desarrollo de las plantas. La intensidad de la luz ambiental es uno de los factores que afectan la densidad estomática (Lake et al., 2002). Así que, al controlar la intensidad de esta variable en el cultivo hidropónico de mirto rojo, como se indica en la literatura también se incide sobre la presencia de los estomas.
El área foliar se vio afectada por la intensidad de luz a la que fue sometida, con valores bajos se desarrollaron hojas más grandes. En la literatura se menciona que cuando las plantas crecen en intensidades de luz bajas, muestran tasas más altas de fotosíntesis, lo que se relaciona con la conductancia del CO2 dentro de la hoja, afectando el área foliar (Francisco-Nava et al., 2011).
Aunque los resultados obtenidos en Munsell pueden ser subjetivos, en el caso de los tejidos vegetales es útil, ya que se pueden intuir posibles deficiencias nutricionales como K, Fe, Cu o algunas enfermedades como la clorosis (Mendoza et al., 2006). El desarrollo de las plantas puede atribuirse a los niveles de luminosidad (C1 y C2), debido a que la variable fue modificada.
Se sabe que la luz afecta la concentración y presencia de pigmentos accesorios (Shanda J., 2007), por ello se esperaba que ambas condiciones presentaran diferencias en los valores del tri-estímulo (L*, a*, b*). El valor de a* indica la contribución del rojo (valores positivos) y del verde (valores negativos) al color total; C1 fue superior a C2. Mientras que b*, indica el componente amarillo (positivo) y azul (negativo); en ambos casos el componente se observó amarillo, el valor para C1 fue menor que en C2. Los resultados obtenidos coinciden con la literatura, debido a que la composición química de la planta se altera en función de la luminosidad aplicada al cultivo (Jiménez-Aparicio & Gutiérrez, 2000).
Para sobrevivir a las condiciones ambientales adversas, las plantas han desarrollado mecanismos útiles para defenderse y utilizar de manera óptima los recursos circundantes para su crecimiento y desarrollo (Camacho-Escobar, 2020). Según los resultados de la CCF, en el extracto SeC1a están presentes los triterpenos AU y AO. Estos compuestos se distribuyen ampliamente por todo el reino Plantae como parte del metabolismo secundario y se ha reportado que tienen actividades farmacológicas como la anticancerígena y antiinflamatoria (Gudoityte et al., 2021).
Se ha demostrado que al menos 88 especies de la familia Lamiaceae son capaces de sintetizar AU y AO (Kalaycıoğlu et al., 2018). Algunos ejemplos son S. officinalis (Rodrigues et al., 2021), S. microphylla (Aydoğmuş et al., 2006), S. hydrangea (Abdollahi-Ghehi et al., 2019) y S. glutinosa (Bajalan et al., 2016), cuyas propiedades farmacológicas han sido demostradas en diferentes modelos biológicos. El AO y su isómero AU, son potentes antiinflamatorios y eficaces en diferentes ensayos antiinflamatorios (González-Chávez et al., 2017). Se ha publicado que el AU ocasionalmente es capaz de inducir la liberación de mediadores proinflamatorios en células y tejidos normales, de modo que se le puede asignar un doble papel biológico (Ikeda et al., 2008). El AO es un compuesto principal de las plantas medicinales e igualmente induce una variedad de actividades biológicas, por ejemplo, como antioxidante, anticancerígeno (Gudoityte et al., 2021) e inhibe la síntesis de leucotrienos (mediadores inflamatorios) reduciendo la acción inflamatoria local de sustancias como TPA (González-Chávez et al., 2017); (Paje et al., 2022). Es probable entonces, que la acción antiinflamatoria del extracto SeC1a en la prueba de edema por TPA, se debiera a la presencia de esos ácidos terpénicos, sin descartar la participación de otros compuestos, como los flavonoides.
Los extractos SeC2a, SeHa y SeC1r redujeron significativamente el edema local en la oreja de ratón. SeC2a también contiene AO, aunque no reveló para AU, por lo que en este caso el efecto antiinflamatorio se puede atribuir, en parte, al contenido del primero. En SeHa y SeC1r, no fue posible detectar AU ni AO, se infiere que otros son los compuestos activos.
A la fecha, no existen datos de cultivos tecnológicos de la especie S. elegans, que muestren que la intensidad de luz en condiciones de hidroponía modifique el desarrollo de la planta. Aunque, existe un estudio con otra especie, S. yangii (B. T. Drew), en el que se evaluó la influencia de 3 diferentes intensidades lumínicas (70, 130 y 220 µmol.cm2.s-1), en cultivos in vitro y sobre el perfil metabólico de las plantas estudiadas. Encontrando que las condiciones de luz aplicadas al cultivo en su diseño experimental modifican la longitud y la masa de los brotes axilares, además de una variación en el perfil de metabolitos secundarios asociados a la intensidad luminosa aplicada (Kozłowska et al., 2022).
Conclusiones
Las condiciones lumínicas sobre las cuales se estableció el cultivo de S. elegans, permitieron determinar el impacto de este factor sobre las plantas, ya que se observó que incide de manera importante sobre su crecimiento y sobre los parámetros morfométricos asociados al desarrollo foliar, influyendo en la producción de metabolitos secundarios, lo cual le confiere la calidad como antiinflamatoria a dicha especie medicinal.
Recomendaciones. Se propone continuar con el establecimiento de técnicas que permitan la obtención del material vegetal en condiciones controladas, que conduzcan a mejorar la calidad de S. elegans, tanto en la abundancia, crecimiento del material vegetal y aumentar también la producción homogénea de metabolitos secundarios que puedan ser útiles farmacológicamente.