ANTECEDENTES
La diabetes gestacional es un padecimiento caracterizado por intolerancia a los carbohidratos, que resulta en hiperglucemia de gravedad variable, que se inicia y reconoce durante el embarazo. La American Diabetes Association (ADA) la define como una diabetes diagnosticada en el segundo o tercer trimestre del embarazo que no es claramente diabetes tipo 1 o tipo 2 preexistente. En la actualidad, la ADA reconoce que la definición facilitaba una estrategia uniforme para la detección y clasificación, pero con limitaciones porque muchos casos de diabetes mellitus gestacional representan hiperglucemia preexistente, que se detecta en el tamizaje rutinario durante el embarazo. Esta Asociación hace hincapié en la necesidad de identificarla antes de la concepción en mujeres con factores de riesgo o en poblaciones de alto riesgo.1
En la mayoría de los casos, la diabetes mellitus gestacional se origina debido a una intolerancia a la glucosa causada por disfunción de las células β pancreáticas, en un contexto de resistencia crónica a la insulina. Entre los principales factores de riesgo se encuentran el sobrepeso, la obesidad, la edad materna avanzada y los antecedentes familiares o personales de diabetes.2 La obesidad es un factor predisponente clave en la diabetes gestacional debido a su estrecha relación con la inflamación crónica y la resistencia a la insulina. Los adipocitos de mujeres embarazadas con obesidad secretan citocinas proinflamatorias, como el factor de necrosis tumoral alfa (TNF-α), interleucinas proinflamatorias y adipocinas, lo que contribuye a un estado inflamatorio persistente. Esa inflamación altera la sensibilidad a la insulina, promueve la acumulación de glucosa en sangre y la hiperglucemia, lo que incrementa el riesgo de diabetes gestacional. Además, la secreción de insulina y la regulación metabólica se afectan debido a la sobrecarga de lípidos y a la activación de vías inflamatorias que interfieren con la señalización de la insulina en órganos clave, como el hígado, los músculos y el tejido adiposo. En mujeres embarazadas con diabetes mellitus gestacional se ha observado una disminución en la expresión del sustrato del receptor de insulina-1 (IRS-1) en los músculos esqueléticos que reduce la captación de glucosa en un 25 a 30%. La disfunción de las células β pancreáticas y la disminución de la sensibilidad periférica a la insulina pueden generar hiperinsulinemia y alteraciones metabólicas que afectan a la madre y al feto.3
La vitamina D es liposoluble y tiene como función principal la regulación del metabolismo calcio-fósforo. Su receptor se encuentra en gran parte de las células nucleadas, lo que sugiere su participación en múltiples procesos metabólicos y fisiológicos.4 La vitamina D incluye dos formas principales: D3 (colecalciferol), de origen animal, y D2 (ergocalciferol) de origen en plantas y hongos. Ambas se metabolizan en el organismo para generar su forma activa, la 1,25-dihidroxivitamina D3 (calcitriol), que se une a su receptor intracelular.5 Se ha planteado la hipótesis de que la deficiencia de vitamina D podría estar asociada con un mayor riesgo de diabetes mellitus gestacional.
Durante el embarazo, las necesidades de vitamina D aumentan debido al rápido crecimiento fetal y las demandas metabólicas maternas. Esta vitamina juega un papel decisivo en la función de las células β pancreáticas y en la secreción normal de insulina. Su deficiencia se ha relacionado con alteraciones en las concentraciones de glucosa, insulina y sensibilidad a la insulina, quizá por su papel en la regulación de la función de las células β pancreáticas, mediante la activación del receptor de vitamina D, lo que mejora la secreción de insulina, modulación del calcio intracelular, esencial para la señalización de la insulina en los tejidos diana y reducción de la inflamación sistémica, factor clave en la resistencia a la insulina y el inicio de la diabetes mellitus.6
Derivado de lo anterior, esta revisión tiene como objetivo: evaluar la evidencia científica del efecto de la suplementación de vitamina D en las variables metabólicas de la diabetes mellitus gestacional.
METODOLOGÍA
Revisión sistemática de la evidencia científica del efecto de la suplementación con vitamina D a pacientes con diabetes mellitus gestacional. La revisión se apegó a los elementos de informe preferidos para revisiones sistemáticas y criterios de metanálisis PRISMA y estrategia PICO de Cochrane. Se utilizaron las bases de datos MEDLINE-PubMed, LILACS, Cochrane, Scielo, Springer Link. Los resultados principales fueron: concentraciones de glucosa en ayuno, hemoglobina glucosilada, resistencia a la insulina e insulina en ayuno. Como resultados secundarios se consideró el perfil lipídico: triglicéridos, colesterol total, colesterol HDL y LDL.
Los criterios de elegibilidad incluyeron: ensayos clínicos aleatorizados efectuados en mujeres con diabetes mellitus gestacional que recibieron suplementación con vitamina D comparada con placebo, sin restricción en la dosificación indicada. Se seleccionaron ensayos doble y triple ciego que evaluaran, al menos, una de las siguientes variables: glucosa en ayuno, hemoglobina glucosilada, resistencia a la insulina o insulina en ayuno. Se excluyeron los estudios que no evaluaron estas variables, los que indicaron la suplementación con otros compuestos adicionales a la vitamina D y los que tuvieran baja calidad metodológica, según las escalas PEDro y JADAD.
Métodos de búsqueda
Para lograr la fundamentación de esta investigación se efectuaron exploraciones en las bases de datos PubMed, LILACS, Cochrane, Scielo y Springer Link, según los tesauros “Vitamin D” or “Gestational diabetes mellitus” or “Pregnant women” or “Vitamin D supplementation”. La búsqueda se hizo solo de artículos escritos en español e inglés publicados de enero 2012 hasta agosto 2024.
Estrategia de búsqueda: la estrategia de búsqueda se desarrolló en función de la estrategia PICO. Cuadro 1
Cuadro 1 Estrategia de búsqueda PICO
| Término PICO | Términos de búsqueda | Estrategia de búsqueda |
|---|---|---|
| Población | Mujeres embarazadas de cualquier raza, edad, diabetes mellitus gestacional | Pregnant women any race, age Gestational diabetes mellitus |
| Intervención | Suplementación con vitamina D | Vitamin D supplementation Cholecalciferol Vitamin D3 |
| Resultado | Concentraciones de glucosa, hemoglobina glucosilada, resistencia a la insulina, insulina en ayuno | Glucose concentrations, glycated hemoglobin, insulin resistance, fasting insulin |
| Diseño del estudio | Ensayo clínico aleatorizado | Randomized clinical trial |
Selección de estudios: después de una búsqueda exhaustiva se hizo un concentrado de datos en la que se identificó cada estudio, por autor, en orden alfabético. Esto permitió eliminar duplicados. Posteriormente, se llevó a cabo una revisión por título y se filtró en función de las características.
Extracción y análisis de datos: se integró una base de datos para obtener toda la información relevante de los estudios elegidos, que se revisaron minuciosamente para extraer datos descriptivos: objetivo, población, diseño de estudio, intervención, duración de la intervención y resultados, para después ser evaluados.
Evaluación del riesgo de sesgo
La calidad global de los ensayos clínicos aleatorizados se midió con el sistema de puntuación de calidad de Oxford (escala JADAD) y la escala Physiotherapy Evidence Database (PEDro). El primer método permitió al evaluador asignar una puntuación de calidad en una escala que va de 0 a 7 puntos en su versión extendida, de manera que, a mayor puntuación es mejor la calidad metodológica del ensayo clínico aleatorizado evaluado. Así, se considera “riguroso” un ensayo con una ponderación de igual o mayor a 5 puntos, mientras que un ensayo clínico aleatorizado es de pobre calidad si su puntuación es inferior a 3 puntos. Por su parte, la escala PEDro permitió obtener ensayos clínicos aleatorizados de buena calidad mediante 11 ítems que los ubicó en alguna de las siguientes categorías: menos de 4 calidad pobre, 4 a 5 calidad justa, 6 a 8 calidad buena y 9 a 10 calidad excelente.
Consideraciones éticas: para esta revisión solo se seleccionaron los estudios que cumplieran con las normativas vigentes en el trato ético del paciente y que utilizaran consentimiento informado.
RESULTADOS
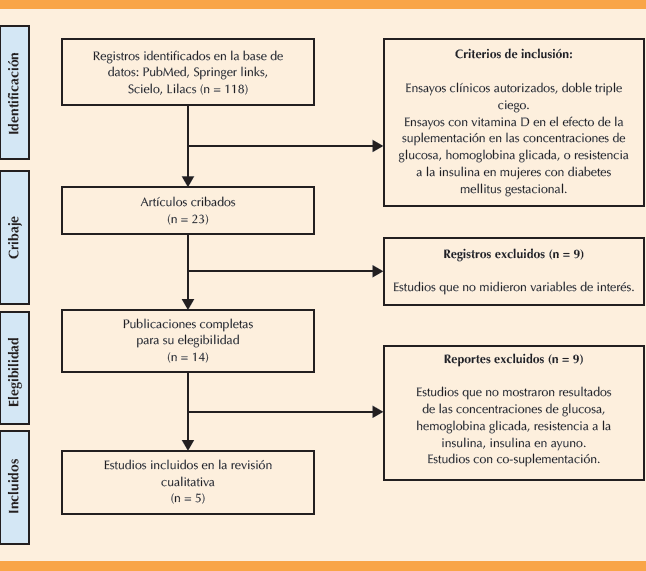
La búsqueda inicial arrojó 118 estudios pero después de la eliminación solo 23 resultaron útiles para revisar los criterios de inclusión y exclusión. Se excluyeron 9 que no midieron las variables de interés. Posteriormente, se evaluaron 14 según el resultado principal y las características de estrategia PICO, para verificar que se cumpliera con todo lo establecido. De los 14 solo 5 estudios cumplieron con los criterios preestablecidos para esta revisión. Figura 1
En el Cuadro 2 se enlistan los ensayos controlados aleatorizados incluidos y las características principales de los cinco estudios seleccionados. Los participantes en estos estudios fueron mujeres embarazadas de entre 18 y 40 años. En relación con el tipo de suplementación de vitamina D3, un estudio7 administró una dosis única de 300,000 UI mediante una inyección intramuscular. Tres estudios utilizaron cápsulas de vitamina D3. Yazdchi y colaboradores8 administraron 50,000 UI durante dos meses. Camarena y su grupo9 lo hicieron con 5000 UI diarias durante ocho semanas y Mirzaei-Azandaryani y coautores10 indicaron 4000 UI en un lapso de 18 semanas y, finalmente, un estudio Li y colaboradores11 experimentó con yogur enriquecido con 500 UI de vitamina D3 en un periodo de 16 semanas.
Cuadro 2 Características de la suplementación con Vitamina D de los estudios incluidos
| Estudio | Intervención (n) | Control (n) | Dosis suplementación | Duración de la intervención | Forma de administración (pastilla, yogur, etc.) |
|---|---|---|---|---|---|
| Mozaffari-Khosravi et al. (2012)7 | 24 | 21 | 300 000 UI vitamina D3 única dosis | 3 meses | Inyección intramuscular |
| Yazdchi et al. (2016)8 | 36 | 36 | 50,000 UI vitamina D3 1dosis/2 semanas | 2 meses | Cápsulas |
| Li et al. (2016)11 | 48 | 49 | 1000 UI vitamina D3/diario | 4 meses | Yogur |
| Camarena et al. (2022)9 | 27 | 27 | 5000 UI vitamina D3/diario | 2 meses | Pastillas |
| Mirzaei-Azandaryani et al. (2022)10 | 44 | 44 | 4000 UI vitamina D3/diaria | 4.5 meses | Pastillas |
Por lo que se refiere a la evaluación de la calidad metodológica, los cinco estudios seleccionados fueron objeto de diferentes evaluaciones. Para la primera se tomó en cuenta la escala PEDro donde dos de cinco artículos tuvieron 10 de 10 puntos: Li y Yazdchi y sus correspondientes colaboradores,11,8 con dos de cinco estudios obtuvieron puntuación de 8 de 10: Mirzaei-Azandaryani y Camarena10,9 con una calidad excelente y el último estudio seleccionado fue el de Mozaffari-Khosravi y coautores7 que obtuvo 7 de 10 con una calidad buena. También se utilizó la escala JADAD para la evaluación. Al analizar los estudios, el trabajo de Li y colaboradores11 obtuvo una puntuación de 6 de 7, mientras que 3 estudios obtuvieron 5 de 7: Yazdchi,8 Mirzaei-Azandaryani,10 Camarena9 y por último Mozaffari-Khosravi7 y los respectivos colaboradores de cada uno, que obtuvo 4 de 7 puntos. Todos los estudios utilizados para este análisis fueron de excelente y buena calidad. Cuadro 3
Cuadro 3 Evaluación del riesgo de sesgo, según las escalas PEDro y JADAD
| Escala PeDRO | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Ítem | 1 (no puntúa) | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | Puntaje total (máximo 10 puntos) |
| Mozaffari-Khosravi et al. (2012)7 | 1 | 1 | 0 | 1 | 0 | 0 | 1 | 1 | 1 | 1 | 1 | 7 |
| Li et al. (2016)11 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 10 |
| Yazdchi (2016)8 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 10 |
| Mirzaei-Azandaryani et al. (2022)10 | 1 | 1 | 1 | 0 | 1 | 1 | 0 | 1 | 1 | 1 | 1 | 8 |
| Camarena et al. (2022)9 | 1 | 1 | 1 | 1 | 1 | 0 | 0 | 1 | 1 | 1 | 1 | 8 |
| Escala JADAD | ||||||||||||
| Ítem | 1 | 2 | 3 | 4 | 5 | 6 | 7 | Puntaje | ||||
| Mozaffari-Khosravi et al. (2012)7 | 1 | 0 | 1 | 0 | 0 | 1 | 1 | 4 | ||||
| Li et al. (2016)11 | 1 | 1 | 1 | 1 | 1 | 0 | 1 | 6 | ||||
| Yazdchi (2016)8 | 1 | 1 | 0 | 1 | 1 | 0 | 1 | 5 | ||||
| Mirzaei-Azandaryani et al. (2022)10 | 1 | 1 | 0 | 1 | 1 | 0 | 1 | 5 | ||||
| Camarena et al. (2022)9 | 1 | 1 | 0 | 1 | 1 | 0 | 1 | 5 | ||||
RESULTADOS
Mozaffari-Khosravi y colaboradores7 en Irán evaluaron a 45 mujeres con diabetes mellitus gestacional entre las 24 y 28 semanas de gestación. Los participantes se asignaron a un grupo de intervención (n = 24) y a otro de control (n = 21). El primero recibió una suplementación de vitamina D3 mediante una inyección intramuscular de 300,000 UI durante tres meses, mientras que el grupo control no recibió la suplementación. Los autores midieron las concentraciones de vitamina D, de glucosa en ayuno, la hemoglobina glucosilada, la sensibilidad a la insulina y el índice HOMA-IR. Al finalizar el estudio, se observó un aumento significativo en las concentraciones de vitamina D en el grupo de intervención, que alcanzó valores de 62.10 nmol/L (55.47-71.70), en comparación con el grupo placebo, cuyos valores fueron de 24.10 nmol/L (21.70-48.60) (p < 0.001), las concentraciones de glucosa en ayuno en el grupo de intervención permanecieron estables (91.8 ± 17.3 mg/dL al inicio y 92.9 ± 10.6 mg/dL al final; p = 0.76), mientras que el grupo control experimentó un aumento significativo (98.3 ± 30.7 mg/dL a 104.7 ± 33.5 mg/dL; p = 0.05). La hemoglobina glucosilada se mantuvo sin cambios significativos en ambos grupos. El índice QUICKI mejoró ligeramente en el grupo de intervención (0.37 ± 0.23 a 0.38 ± 0.02; p = 0.09), mientras que en el grupo control disminuyó de manera muy importante (0.38 ± 0.29 a 0.36 ± 0.02; p = 0.008) y el índice HOMA-IR permaneció constante en el grupo de intervención, con una mediana de 0.6 al inicio y 0.5 al final (p = 0.7) en comparación con el grupo control que experimentó un aumento significativo, pasando de una mediana de 0.5 a 0.9 ( p = 0.01).
Yazdchi y coautores8 llevaron a cabo un estudio en Irán para evaluar el efecto de la suplementación con vitamina D3 en mujeres de entre 15 y 45 años con diabetes mellitus gestacional. La muestra incluyó 76 participantes, divididas en un grupo de intervención (n = 38) y un grupo control (n = 38). El grupo de intervención recibió cápsulas de 50,000 UI de vitamina D3 cada dos semanas durante dos meses. Se midieron las concentraciones de vitamina D, glucosa en ayuno, insulina, hemoglobina glucosilada y el índice HOMA-IR. Al finalizar el estudio, el grupo de intervención experimentó un aumento significativo en las concentraciones de vitamina D (30.40 ng/mL [24.70-37.94]) en comparación con el grupo placebo (8.42 ng/mL [6.98-15.10]; p = 0.01). Asimismo, la glucosa en ayuno fue menor en el grupo de intervención (92.08 ± 20.19 mg/dL) frente al grupo placebo (100 ± 17.75 mg/dL; p = 0.01). En cuanto a la hemoglobina glucosilada, el grupo de intervención mostró valores más bajos (5.17 ± 0.59%) en comparación con el grupo control (5.54 ± 0.65%; p = 0.02). No se observaron diferencias significativas en el índice HOMA-IR (grupo de intervención: 2.46 µIU/mL [1.22-3.57] en comparación con el grupo placebo: 2.21 µIU/mL [1.44-4.16]; p = 0.51) ni en las concentraciones de insulina en ayuno (grupo de intervención: 10.65 µIU/mL [6.22-13.57] comparado con el grupo placebo: 9.65 µIU/mL [6.07-15.92]; p = 0.23).
Li y coautores11 realizaron un estudio en China para evaluar el efecto de la suplementación con vitamina D3 en mujeres embarazadas de entre 24 y 28 años, con embarazo único y diagnóstico de diabetes mellitus gestacional al inicio del segundo trimestre. La muestra incluyó 148 participantes, divididas en un grupo de intervención (n = 97) y grupo placebo (n = 51). El grupo de intervención recibió 500 UI de vitamina D3 diariamente a través de un yogur de 100 g durante 16 semanas. Se evaluaron las concentraciones de vitamina D, glucosa en ayuno, insulina y el índice HOMA-IR. Al finalizar el estudio, el grupo de intervención tuvo un aumento significativo en las concentraciones de 25-hidroxivitamina D (29.5 ± 5.7 ng/mL) en comparación con el grupo placebo (15.9 ± 4.5 ng/mL; p = 0.02). Asimismo, la glucosa plasmática en ayuno fue menor en el grupo de intervención (87.6 ± 7.9 mg/dL) que en el de placebo (98.7 ± 8.1 mg/dL; p = 0.04). Las concentraciones de insulina en ayuno también fueron más bajas en el grupo de intervención (10.7 ± 5.3 µIU/mL) respecto del grupo placebo (16.7 ± 6.2 µIU/mL; p = 0.03) y el índice HOMA-IR fue significativamente menor en el grupo de intervención (1.6 ± 1.2 µIU/mL) en comparación con el grupo placebo (3.9 ± 2.7 µIU/mL; p = 0.01).
Camarena y coautores9 evaluaron el efecto de la suplementación con vitamina D en pacientes con diabetes mellitus gestacional de entre 18 y 35 años, con 24 a 28 semanas de embarazo. La muestra incluyó 54 participantes, divididas en un grupo de intervención (n = 27) y un grupo placebo (n = 27). El primero recibió 5000 UI de vitamina D por vía oral durante ocho semanas. Se midieron las concentraciones de vitamina D, hemoglobina glucosilada, glucosa en ayuno, insulina y el índice HOMA-IR. Al finalizar el estudio, el grupo de intervención mostró un aumento significativo en las concentraciones de vitamina D (32 ng/mL [25-37]) en comparación con el grupo placebo (26 ng/mL [17-29]; p = 0.006). Sin embargo, no se encontraron diferencias significativas en los demás indicadores: las concentraciones de hemoglobina glucosilada en el grupo de intervención fueron de 6.0% (5.5-6.4) y las del grupo placebo 6.1% (5.7-6.3) (p = 0.29). En cuanto a la glucosa en ayuno, el grupo de intervención tuvo un valor de 99 mg/dL (83-120) y el de placebo 87 mg/dL (80-104; p = 0.29). Las concentraciones de insulina en ayuno al finalizar el estudio fueron 14 µIU/mL (11-17) en el grupo de intervención y 13 µIU/mL (9.3-20) en el de placebo (p = 0.79). El índice HOMA-IR tampoco mostró diferencias significativas, con valores de 3.6 µIU/mL (2.7-4.7) en el grupo de intervención y 2.6 µIU/mL (1.8-4.8) en el de placebo (p = 0.55).
Mirzaei-Azandaryani y colaboradores10 emprendieron un estudio en mujeres embarazadas de entre 8 y 10 semanas de gestación para evaluar el efecto de la suplementación con vitamina D. La muestra incluyó 88 participantes, divididas en un grupo de intervención (n = 44) y un grupo placebo (n = 44). El primero recibió 4000 UI de vitamina D en comprimidos durante 18 semanas. Se cuantificaron las concentraciones de vitamina D, glucosa en ayuno, el índice HOMA-IR. Al finalizar el estudio se observó un aumento significativo en las concentraciones de vitamina D en el grupo de intervención (32.17 ± 13.20 ng/mL) en comparación con el grupo placebo (26.51 ± 9.99 ng/mL; p = 0.02). Sin embargo, no se encontraron diferencias significativas en los demás indicadores: la glucosa en ayuno fue de 81.97 ± 8.90 mg/dL en el grupo de intervención y 82.37 ± 8.46 mg/dL en el grupo placebo (p = 0.672). De manera similar, las concentraciones de insulina en ayuno fueron de 7.24 ± 5.11 mg/dL en el grupo de intervención y 8.55 ± 5.97 mg/dL en el grupo placebo (p = 0.672) y el índice HOMA-IR tampoco mostró diferencias significativas, con valores de 27.29 ± 26.63 en el grupo de intervención y 29.85 ± 23.9 en el grupo placebo (p = 0.637).
En el Cuadro 4 se exponen los resultados principales de los cinco estudios incluidos en la revisión.
Cuadro 4 Estudios clínicos aleatorizados que suplementaron vitamina D en mujeres con diabetes mellitus gestacional (continúa en la siguiente página)
| Autores | Población de estudio | Participantes | Interveción comparada con las controles | Resultados |
|---|---|---|---|---|
| Mozaffari-Khosravi et al. (2012)7 | Mujeres con diagnóstico de diabetes mellitus gestacional entre las 24 y 28 semanas de gestación. País: Irán | n = 45 mujeres Grupo de intervención: 24 años (media): 30.7 ± 6.2 Grupo control: 21 años (media): 29.5±4.0 | Grupo de intervención: Inyección intramuscular 300,000 UI de vitamina D3 Grupo control: No reportado Temporalidad: 3 meses | Mediana, (P25-P75) 25 hydroxivitamina D (nmol ⁄ L) Grupo de intervención: 62.10 (55.47-71.70) Grupo control: 24.10 (21.70-48.60 p = <0.001 Resultados principales: Media (DE) Concentraciones de glucosa en ayuno (mg/dL): Grupo de control: 104.7 ± 33.5 Grupo de intervención: 92.9 ± 10.6 p = 0.11 Hba1c (%) Grupo control: 5.20 ± 0.73 Grupo intervención: 5.48 ± 0.69 p = 0.1 Sensibilidad a la insulina (%S) Grupo intervención 169.68 ± 53.48 Grupo control 122.84 ± 41.15 p < 0.002 Mediana (P25-P75) HOMA-Ir Grupo de intervención: 0.5(0.4-0.8) Grupo control: 0.9 (0.7-1.0) p = 0.004 |
| Yazdchi et al. (2016)8 | Mujeres entre 15-45 años con diabetes mellitus gestacional entre 24 y 28 SG País: Irán | 76 mujeres Grupo de intervención: 38 Grupo Placebo: 38 n final para ambos grupos: 36 | Grupo de intervención: Cápsulas orales que contenían 50,000 UI de vitamina D3, una vez cada 2 semanas durante 2 meses Grupo placebo: placebos compuestos de aceite de parafina 1 cápsula, una vez cada 2 semanas | Media (IC95%) 25-hidroxivitamina D (ng⁄mL) 30.40 (24.70-37.94) Grupo control: 8.42 (6.98-15.10) p = 0.01 Resultados principales: Insulina (μIU/mL): Grupo intervención: 10.65 (6.22-13.57) Grupo control: 9.65 (6.07-15.92) p = 0.23 HOMA-IR: Grupo de intervención: 2.46 (1.22-3.57) Grupo control: 2.21 (1.44-4.16) p = 0.51 Media (DE) Glucosa (mg/dL): Grupo de intervención: 92.08 ± 20.19 Grupo control: 100 ± 17.75 p = 0.01 HbA1c (%): Grupo intervención: 5.17 ± 0.59 Grupo control: 5.54 ± 0.65 p = 0.02 Resultados secundarios: Media (DE) Colesterol total (mg/dL): Grupo intervención: 237.75 ± 121.48 Grupo control: 232.33 ± 96.60 p = 0.88 Triglicéridos (mg/dL): Grupo de intervención: 238.75 ± 121.48 Grupo control: 232.33 ± 96.60 p = 0.58 Colesterol LDL (mg/dL): Grupo intervención: 97 ± 44.54 Grupo control: 140.36 ± 39.53 p = 0.46 Colesterol HDL (mg/dL): Grupo intervención: 71.75 ± 19.94 Grupo control: 68.28 ± 15.53 p = 0.18 |
| Li et al. (2016)11 | con 24 a 28 semanas de gestación y edad de 24 a 32 años, con embarazo único y diagnóstico de diabetes gestacional al inicio del segundo trimestre. País: China | Intervención:48 Control: 49 | Grupo de intervención: 2 porciones de 100 g de yogur natural con 500 UI de vitamina D3 Temporalidad: 16 semanas | Media (DE) 25-hidroxivitamina D (ng/mL) Grupo de intervención: 29.5 ± 5.7 Grupo control: 15.9 ± 4.5 p = 0.02 Resultados principales: Glucosa en ayuno (mg/dL): Grupo de intervención: 87.6 ± 7.9 Grupo control: 98.7 ± 8.1 p = 0.04 Insulina en ayuno (μIU/mL): Grupo de intervención: 10.7 ± 5.3 Grupo control: 16.7 ± 6.2 p = 0.03 HOMA-IR: Grupo de intervención: 1.6 ± 1.2 Grupo control: 3.9 ± 2.7 p = 0.01 Resultados secundarios: Media (DE) Triglicéridos (mg/dL): Grupo de intervención: 161.8 ± 69.2 Grupo control: 237.4 ± 61.5 p = 0.02 Colesterol Total (mg/dL): Grupo de intervención: 176.5 ± 58.1 Grupo control: 224.6 ± 62.3 p = 0.04 Colesterol LDL (mg/dL): Grupo de intervención: 87.3 ± 30.2 Grupo control: 106.7 ± 35.1 p = 0.05 Colesterol HDL (mg/dL): Grupo control: 70.5 ± 13.2 Grupo de intervención: 68.7 ± 14.3 p = 0.21 |
| Camarena et al. (2022)9 | Mujeres con diabetes gestacional de 18 a 35 años, de 24 y 28 semanas de embarazo País: México | Grupo de intervención: vitamina D (n = 27) grupo placebo (n = 27) | Intervención: 5000 UI de vitamina D por vía oral cada 24 horas comparada con placebo Temporalidad: 8 semanas | Media (IC95%) Vitamina D (ng/mL): Grupo de intervención: 32 (25-37) Grupo control: 27 (17-29) p = 0.006 Resultados principales: HBA1c %: Grupo de intervención: 6.0 (5.5-6.4) Grupo control: 6.1 (5.7-0.3) p = 0.29 Glucosa en ayuno (mg/dL): Grupo de intervención: 99 (83-120) Grupo control: 87 (80-104) p = 0.29 Insulina (µIU/mL): Grupo de intervención: 14 (11-17) Grupo control: 13 (9.3-20) p = 0.79 Índice HOMA-IR: Grupo de intervención: 3.6 (2.7-4.7) Grupo control: 2.6 (1.8-4.8) p = 0.55 Resultados secundarios: Colesterol total (mg/dL): Grupo de intervención: 214 (194-251) Grupo control: 211 (181-223) p = 0.46 Colesterol HDL (mg/dL): Grupo de intervención: 55 (47-63) Grupo control: 45 (39-60) p = 0.025 Colesterol LDL (mg/dL): Grupo de intervención: 100 (72-140) Grupo control: 100 (88-113) p = 0.77 Triglicéridos (mg/dL): Grupo de intervención: 283 (241-302) Grupo control: 218 (180-288) p = 0.08 |
| Mirzaei-Azandaryani et al. (2022)10 | Pacientes con 8 a 10 semanas de embarazo País: Irán | 88 mujeres Grupo de intervención (n = 44) Grupo control (n = 44) | Intervención: 4000 unidades de vitamina D3 en comprimidos. Grupo control: comprimidos de placebo: no reportado Temporalidad:18 semanas | Media (DE) Concentraciones de vitamina D (ng/mL): Grupo de intervención: 32.17 ± 13.20 Grupo control: 26.51 ± 9.99 p = 0.002 Resultados principales: Glucosa en ayuno (mg/dL): Grupo de intervención: 81.97 ± 8.90 Grupo control: 82.37 ± 8.46 p = 0.672 Insulina en ayuno (mg/dL): Grupo de intervención: 7.24 ± 5.11 Grupo control: 8.55 (5.97) p = 0.672 Índice HOMA-IR: Grupo de intervención: 27.29 ± 26.63 Grupo control: 29.85 ± 23.9 p = 0.637 |
HOMA-IR: índice de resistencia a la insulina; LDL: Lipoproteína de baja densidad; HDL: Lipoproteína de alta densidad; HbA1c: Hemoglobina glucosilada; DE: Desviación estándar.
Resultados secundarios
En la evidencia científica analizada se observó que tres de los cinco estudios revisados incluyeron la medición del perfil lipídico, entre ellos el de Yazdchi y colaboradores.8 En ese estudio, al finalizar la intervención, el grupo que recibió suplementación mostró una disminución promedio en las concentraciones de colesterol total de 3 ± 26.90 mg/dL, mientras que el grupo placebo experimentó un aumento de 13.05 ± 20.25 mg/dL; sin embargo, esta diferencia no fue estadísticamente significativa (p = 0.08). En cuanto a los triglicéridos, se registró una reducción de 7.69 ± 84.54 mg/dL en el grupo de intervención y de 1.86 ± 79.71 mg/dL en el grupo placebo, sin diferencias significativas entre ellos (p = 0.85), respecto del colesterol LDL. El grupo de intervención tuvo una reducción promedio de 0.51 ± 22.84 mg/dL, mientras que el grupo placebo mostró un incremento de 10.31 ± 23.33 mg/dL, sin alcanzar significación estadística (p = 0.46) y las concentraciones de colesterol HDL aumentaron ligeramente en el grupo de intervención (0.22 ± 14.41 mg/dL) y disminuyeron en el de placebo (3.57 ± 7.14 mg/dL) (p = 0.18).
Li y colaboradores,11 al concluir el estudio, el grupo de intervención mostró concentraciones significativamente más bajas de triglicéridos (161.8 ± 69.2 mg/dL) que el grupo placebo (237.4 ± 61.5 mg/dL) (p = 0.02). Asimismo, el colesterol total fue menor en el grupo de intervención (176.5 ± 58.1 mg/dL) que en el de placebo (224.6 ± 62.3 mg/dL) (p = 0.04). Las concentraciones de colesterol LDL también fueron inferiores en el grupo de intervención (87.3 ± 30.2 mg/dL) en comparación con el de placebo (106.7 ± 35.1 mg/dL) (p=0.05) y no se observaron diferencias significativas en las concentraciones de colesterol HDL entre uno y otro grupo (intervención: 70.5 ± 13.2 mg/dL; placebo: 68.7 ± 14.3 mg/dL; p = 0.21).
En el estudio de Camarena y coautores9 se evaluaron los efectos de la suplementación con vitamina D en el perfil lipídico de pacientes con diabetes mellitus gestacional. Al finalizar la intervención, las concentraciones de colesterol total mostraron una mediana de 214 mg/dL (rango intercuartílico: 194-251) en el grupo de vitamina D, y de 211 mg/dL (181-223) en el grupo placebo, sin diferencia significativa entre uno y otro grupo (diferencia de 12 mg/dL; IC95%: -17 a 40; p = 0.46), en cuanto al colesterol HDL, las medianas fueron 55 mg/dL (47-63) para el grupo de vitamina D y 45 mg/dL (39-60) para el grupo placebo, con una diferencia significativa de 8.4 mg/dL (IC95%: -0.1-17; p = 0.025), respecto al colesterol LDL, ambos grupos reportaron una mediana de 100 mg/dL, con rangos intercuartílicos de 72 a 140 para el grupo de vitamina D y 88 a 113 para el de placebo, sin diferencia significativa (diferencia de 2.0 mg/dL; IC95%: -19 a 29; p = 0.77) y los triglicéridos mostraron medianas de 283 mg/dL (241-302) en el grupo de vitamina D y 218 mg/dL (180 a 288) en el grupo placebo, sin diferencia significativa entre ambos grupos (diferencia de 52 mg/dL; IC95%: -5 a 92; p = 0.08). Cuadro 4
DISCUSIÓN
En esta revisión se incluyeron cinco estudios clínicos aleatorizados que incluyeron 355 pacientes con diagnóstico de diabetes mellitus gestacional. La duración de las intervenciones varió entre 2 meses y 18 semanas, y la suplementación con vitamina D3 se administró en diferentes presentaciones, incluida la inyección intramuscular, las cápsulas y el yogur.
En cuanto a la resistencia a la insulina, se observaron diferencias significativas en dos estudios con resultados positivos. Mozaffari-Khosravi y colaboradores (2012)7 utilizaron una inyección intramuscular de 300,000 UI de vitamina D3 durante 3 meses, y Li y coautores (2016)11, con 2 porciones de yogur de 100 gramos (500 UI de vitamina D3) durante 16 semanas. Estos autores demostraron que, además de la dosis, el tiempo de suplementación y, quizá, el método de administración pueden influir en el efecto observado. Solo un estudio reportó una variación positiva en las concentraciones de hemoglobina glucosilada. Yazdchi y su equipo (2016)8 indicaron cápsulas con 50,000 UI de vitamina D3 una vez cada dos semanas durante dos meses. Los otros estudios no encontraron diferencias significativas en este parámetro luego de la suplementación. Por último, los desenlaces de la glucosa en ayuno fueron heterogéneos, dos estudios (Yazdchi 2016 y Li y sus correspondientes grupos 2016)8,11 reportaron una reducción significativa en la concentración de glucosa en el grupo que recibió suplementación con vitamina D en comparación con el grupo placebo. Sin embargo, otros tres estudios no encontraron diferencias significativas en esta variable. La falta de consistencia en los hallazgos podría atribuirse a la variabilidad en las dosis utilizadas, el tiempo de suplementación y el estado basal de la vitamina D en las participantes. Solo el estudio de Li y colaboradores (2016)11 reportó una reducción significativa en las concentraciones de insulina en ayuno en el grupo que recibió suplementación con vitamina D en comparación con el grupo placebo (p = 0.03), quizá el efecto observado pueda reflejarse por la forma de suplementación.
En la bibliografía se encontraron investigaciones que han demostrado que la vitamina D3 desempeña un papel decisivo en la regulación de la secreción de insulina y la funcionalidad de las células β pancreáticas. Los estudios en modelos animales han evidenciado que la deficiencia de vitamina D se asocia con una disminución significativa de la secreción de insulina, mientras que su administración restablece esa función. Este efecto se ha atribuido a la expresión del receptor de vitamina D (VDR) y de la enzima α-hidroxilasa en las células de los islotes pancreáticos que permite la activación local del calcitriol y su acción directa en genes clave para el metabolismo. Se ha observado que participa en la transcripción del gen de la insulina al unirse a elementos de respuesta específicos en su promotor, además de restaurar la expresión del transportador de glucosa GLUT2, facilitando la entrada de glucosa a la célula β. Asimismo, el calcitriol interviene en la regulación del calcio intracelular, elemento fundamental para la exocitosis de insulina, al promover la despolarización de la membrana celular y la apertura de canales de calcio tipo L, favorecer la activación de la proteína cinasa A (PKA), y estimular la síntesis de fosfolipasa C (PLC), lo que activa la producción de inositol trifosfato (IP3) y la liberación de calcio desde el retículo endoplásmico. Además, se incrementa la expresión de calbindina, una proteína fijadora de calcio que ayuda a mantener concentraciones intracelulares adecuadas para la función secretora. También la vitamina D3 ha demostrado activar la vía PI3K/AKT al promover la supervivencia y eficiencia funcional de las células β, al tiempo que se ha relacionado con la activación de los receptores nucleares PPAR-γ y PPAR-δ, implicados en la regulación del metabolismo de la glucosa y los lípidos, y en la sensibilidad a la insulina. Incluso se ha documentado que la vitamina D inhibe la vía proinflamatoria TLR4/NFκB al reducir la inflamación sistémica y local en los islotes pancreáticos; además de ejercer efectos protectores frente a la apoptosis, el estrés oxidativo y las respuestas autoinmunitarias, contribuir a preservar la masa y la función de las células β.12,13
En este sentido, Zhang y colaboradores14 investigaron los efectos de la suplementación con vitamina D3 (1600 UI/día) en el metabolismo de la glucosa en personas y ratones prediabéticos, a través de un ensayo clínico aleatorizado, controlado con placebo y un modelo murino con dieta alta en grasas en ratones Kkay. Los autores evaluaron los parámetros glucolipídicos, la inflamación, la función muscular y las vías moleculares. Al finalizar los estudios se evidenció que, en humanos, la vitamina D3mejoró la secreción de insulina y redujo la inflamación. En los ratones, además de mejorar el metabolismo de la glucosa y lípidos, también atenuó las alteraciones musculares y aumentó la capacidad de ejercicio. En el ámbito molecular, la Vitamina D3 inhibió la vía inflamatoria TLR4/NFκB, activó la vía PI3K/AKT y favoreció la homeostasis glucémica.
Está demostrado que la deficiencia de vitamina D se asocia con resistencia a la insulina y con el aumento del índice HOMA-IR. La suplementación con vitamina D ha demostrado reducir el riesgo de resistencia a la insulina y las concentraciones circulantes de insulina, con una correlación inversa entre las concentraciones de vitamina D y HOMA-IR, que se intensifica en sujetos con índices de masa corporal (IMC) elevados.15 Elsheikh y su grupo (2024)16 llevaron a cabo un estudio transversal, retrospectivo, con el objetivo de explorar la relación entre las concentraciones séricas de 25-hidroxivitamina D y marcadores metabólicos en una muestra de 476 adultos saudíes, con límites de endad de 15 y 78 años. Los participantes se clasificaron en tres categorías, según su estatus de vitamina D. Al finalizar el estudio, los autores reportaron una prevalencia significativamente mayor de diabetes en el grupo con deficiencia de vitamina D (18.3%) en comparación con el grupo insuficiente (11.6%) y el grupo suficiente (10.1%).
Algunos mecanismos moleculares subyacentes vinculan la hipovitaminosis D con la resistencia a la insulina, lo que destaca la expresión de receptores de insulina, la producción de citocinas inflamatorias y el polimorfismo del receptor de vitamina D en las células β pancreáticas. Se ha observado que la vitamina D incrementa la expresión de los receptores de insulina en el músculo, hígado y tejido adiposo en donde mejora la sensibilidad a la insulina. Asimismo, la deficiencia de vitamina D aumenta la expresión de citocinas proinflamatorias, lo que contribuye a la resistencia a la insulina en pacientes con obesidad. También podría influir en la sensibilidad a la insulina a través de su acción en la bioenergética mitocondrial y el estrés oxidativo. Se ha observado que su deficiencia se relaciona con una reducción en la expresión de genes implicados en la respiración mitocondrial, lo que deriva en menor producción de ATP y mayor generación de especies reactivas de oxígeno (ROS) que favorecen la disfunción metabólica y la resistencia a la insulina.17
En cuanto al perfil lipídico, el estudio de Li y coautores (2016)11 fue el único que encontró un efecto positivo en una cantidad mayor de variables, entre ellas triglicéridos, colesterol total y colesterol LDL. Por su parte, en el estudio de Camarena y colaboradores (2022)9 se encontró un aumento en la concentración de colesterol HDL en el grupo de intervención. Quizá estos efectos sean un reflejo de la forma de administración de la vitamina D.
Respecto a la participación de la vitamina D en el metabolismo de los lípidos, esta vitamina puede influir en la adipogénesis, lipólisis y lipogénesis, aunque su función varía dependiendo del contexto. Los estudios in vitro han demostrado que promueve la diferenciación de precursores de adipocitos en células mesenquimatosas humanas, estimula la expresión de factores clave como PPARγ y AP2. En modelos animales, la suplementación con vitamina D3 aumentó la grasa subcutánea y visceral, mientras que la administración de calcitriol redujo el peso del tejido adiposo. Los ratones sin receptor de vitamina D tuvieron menor masa adiposa y concentraciones reducidas de triglicéridos y colesterol, con mayor expresión de la proteína UCP1, lo que sugiere un aumento en el gasto energético.18 Elsheikh y coautores (2022),16 además del perfil glucémico, examinaron la asociación entre la situación de la vitamina D y los perfiles lipídicos de los participantes. Los resultados del estudio transversal revelaron que los individuos con concentraciones deficientes de 25(OH)D tuvieron un mayor riesgo de dislipidemia, evidenciado por una mayor concentración de colesterol total ≥ 240 mg/dL (18.9%) y LDL ≥ 160 mg/dL (13.2%), en comparación con quienes tuvieron concentraciones suficientes (5.3% y 6,9%, respectivamente). En el ensayo de Gholamzad y su grupo (2023)19 en 15,600 participantes, aparentemente sanos, se evidenció una asociación significativa entre mayores concentraciones séricas de 25-hidroxivitamina D [25(OH)D] y concentraciones más bajas de colesterol LDL; es decir una correlación inversa entre ambas variables.
Quizá la dosificación y duración de la suplementación hayan influido en algunos efectos observados pues se ha evidenciado que la respuesta puede variar en función del IMC, ingesta de calcio, tipo de vitamina D indicada y el estado previo de la paciente antes de iniciar la suplementación.20 En relación con este último factor, en los estudios analizados se observó que al inicio las pacientes tenían concentraciones basales menores de 35 nmol/L. Mozaffari-Khosravi y coautores (2012)7 reportaron que el 79.2% (n = 19) de las pacientes del grupo de intervención tenían concentraciones basales de 25-hidroxivitamina D inferiores a 35 nmol/L. Al finalizar el estudio en el 20.8% (n = 5) se incrementaron las concentraciones (más de 35 nmol/L) de vitamina D. En contraste, el grupo placebo que inició y continuó hasta el final de la investigación permaneció con concentraciones basales inferiores a 35 nmol/L de 25-hidroxivitamina D. En ese mismo sentido, Yazdchi y colaboradores (2016)8 y Li y su grupo (2016)11 encontraron concentraciones basales de 25-hidroxivitamina D inferiores a 20 ng/mL. Al finalizar los estudios observaron un incremento de la 25-hidroxivitamina D mayor a 20 ng/mL en los grupos de intervención, en comparación con los grupos placebo que permanecieron con concentraciones bajas. Por su parte, Camarena y coautores (2022),9 no encontraron diferencia en las concentraciones basales de 25(OH)D entre grupos; después de la intervención se observó un incremento en las concentraciones de 25(OH)D en el grupo de intervención en comparación con el grupo basal (32 en comparación con 26 ng/mL; p = 0.006, respectivamente). Por último, Mirzaei-Azandaryani y colaboradores (2022)10 incluyeron en en su estudio a pacientess con concentraciones basales de vitamina D inferiores 30 ng/mL; al finalizar la suplementación, el grupo de intervención reportó un aumento en las concentraciones de vitamina D (32.17 ± 13.20 ng/mL); mientras que el grupo placebo no experimentó aumento (26.51 ± 9.99 ng/ml) (p = 0.002).
Esta revisión tiene limitaciones, como las referentes a los pocos estudios que evaluaron las variables de interés y que no todos midieron el perfil lipídico. Hubiera sido valioso incorporar estudios que utilizaran métodos de suplementación alternativos a las cápsulas, como el yogur que, a pesar de contener una dosis más baja, mostró efectos favorables en las variables evaluadas en la revisión. Entre las fortalezas sobresale el apego a los estándares internacionales y un enfoque objetivo que minimiza la probabilidad de resultados falsos positivos; además, solo se incluyeron ensayos clínicos aleatorizados, doble o triple ciego, reconocidos de buena o excelente calidad, evaluados mediante escalas de puntuación PEDro y JADAD.
CONCLUSIONES
La evidencia disponible aún es insuficiente para establecer que la suplementación con vitamina D indicada a pacientes con diabetes mellitus gestacional es eficaz de manera concluyente porque los resultados de los estudios tienen una variabilidad significativa, sobre todo en parámetros como la hemoglobina glucosilada y el perfil lipídico. Entonces, si bien la suplementación con vitamina D podría representar una posibilidad de tratamiento para esas pacientes, es necesario llevar a cabo más estudios que permitan determinar las dosis óptimas, la duración adecuada del tratamiento y sus efectos en indicadores metabólicos. Ello permitirá generar guías claras, basadas en evidencia que respalden su implementación, como parte de un enfoque terapéutico multimodal orientado a mejorar los desenlaces en las madres y sus recién nacidos.