Introducción
El banano (Musa spp. AAA) es una de las frutas más cultivadas y comercializadas en el mundo, desempeñando un papel crucial en la economía agrícola de muchos países tropicales y subtropicales. Este cultivo no solo es vital para la seguridad alimentaria, sino también para el sustento de millones de pequeños agricultores. Sin embargo, el cultivo de banano enfrenta desafíos significativos, incluyendo enfermedades del suelo y plagas que afectan el crecimiento y la productividad de las plantas (Ploetz, 2015). Estas enfermedades, como la Marchitez por Fusarium y la Sigatoka negra, pueden devastar plantaciones enteras, haciendo urgente la búsqueda de soluciones efectivas y sostenibles.
La agricultura moderna está cada vez más enfocada en prácticas sostenibles que minimicen el uso de productos químicos y promuevan el uso de agentes biológicos. En este contexto, los microorganismos benéficos, como Bacillus sp. y Trichoderma spp., han emergido como alternativas prometedoras para el manejo de plagas y enfermedades, así como para la promoción del crecimiento vegetal.
Bacillus sp. es un género de bacterias conocido por su capacidad de promover el crecimiento de las plantas y suprimir patógenos del suelo a través de diversos mecanismos. Estas bacterias pueden producir antibióticos, competir por nutrientes y nichos ecológicos con otros patógenos, y estimular las defensas naturales de las plantas, induciendo resistencia sistémica. Investigaciones han mostrado que Bacillus sp. puede mejorar significativamente el crecimiento y la salud de las plántulas en varios cultivos, incrementando la absorción de nutrientes y la tolerancia a estrés abiótico (Shafi, Tian y Ji, 2017).
Por otro lado, Trichoderma spp. es un grupo de hongos que ha mostrado un potencial considerable en la biocontrol de enfermedades de plantas y en la promoción del crecimiento vegetal. Estos hongos actúan a través de la producción de enzimas hidrolíticas como las esterasas, proteasas, lipasas, amilasas, acilasas y fosfatasas, que degradan las paredes celulares de los patógenos, la competencia por espacio y nutrientes, y la inducción de mecanismos de defensa en las plantas hospedadoras (Harman, Howell, Viterbo, Chet y Lorito, 2004). Además, se ha reportado que Trichoderma spp. en Arabidopsis pudo mejorar la absorción de nutrientes y la tolerancia a estrés abiótico, lo cual es crítico en ambientes de crecimiento adversos.
En el caso específico del cultivo de banano, la aplicación de Bacillus sp. y Trichoderma spp. podría ofrecer una solución dual: mejorar el crecimiento y la salud de las plantas, y controlar patógenos del suelo de manera sostenible. La combinación de estos microorganismos puede proporcionar un efecto sinérgico, aumentando la eficacia de cada uno y proporcionando beneficios adicionales que no se obtendrían con su uso individual.
El objetivo del presente estudio fue evaluar el efecto combinado de Bacillus sp. y Trichoderma spp. sobre el desarrollo de plántulas de banano (Musa spp. AAA) en etapa de vivero, con el fin de determinar si la aplicación conjunta de estos microorganismos benéficos mejora el crecimiento y la salud de las plántulas, proporcionando una estrategia sostenible para el manejo de viveros de banano y contribuyendo a la producción agrícola sostenible. Esta investigación no solo contribuye al conocimiento científico sobre el uso de microorganismos benéficos en la agricultura, sino que también ofrece aplicaciones prácticas para mejorar la productividad y sostenibilidad del cultivo de banano.
Materiales y Métodos
Localización del Lugar de Estudio
La investigación se realizó en la Quinta Herrera en el km 2 de la vía Quevedo - Valencia, ubicada entre las coordenadas geográficas1º01’24.4” S y 79º27’10.5” O, a una altitud de 51 m de altitud bajo una cubierta en invernáculo. El clima del sitio experimental es tropical húmedo, con una temperatura media anual de 24 °C, precipitación media anual de 2510 mm, humedad relativa del 91%. El terreno del sitio experimental presenta topografía plana y drenaje regular.
Material Genético
Las plántulas utilizadas en la investigación fueron obtenidas mediante multiplicación meristemática del material Musa AAA Canvendish (producidas por la empresa Galiltec Ecuador GLTC S.A.). Se seleccionaron plántulas de la misma edad (cuatro semanas) con uniformidad en cuanto a su vigor e indicadores de crecimiento y desarrollándose en un sustrato con buen drenaje rico en materia orgánica (25% tierra de huerto de cacao + 25% de arena + 50% de cascarilla de arroz).
Tratamientos y Diseño Experimental
Los tratamientos consistieron en la aplicación de dos cepas nativas de Trichoderma spp. provenientes del laboratorio de Microbiología de la Universidad Técnica Estatal de Quevedo (Colección de antagonistas del Proyecto PFOC-08-15-2021), que previamente han sido usadas en estudios similares en varios cultivos de la zona con resultados promisorios (T. asperellum y T. yunnanense). Adicionalmente, se evaluaron dos productos comerciales formulados con T. harzianum (TrichoD® Orius Biotech) y B. subtilis (Serenade® Bayer) tal como se muestra en la Cuadro 1. El ensayo se realizó bajo un diseño completamente al azar (DCA), con siete tratamientos en cuatro repeticiones (cada unidad experimental conformada por diez plantas). Las variables de respuesta fueron sometidas al respectivo análisis de varianza, y se utilizó la prueba de Tukey (P ≤ 0.05) para la comparación de las medias de los tratamientos.
Table 1: Description of the treatments evaluated in the research.
| Tratamientos | Dosis |
| T1: T. asperellum | 1 × 1012 esporas ha-1 |
| T2: T. yunnanense | 1 ×1012 esporas ha-1 |
| T3: T. asperellum + T. yunnanense | 1 ×1012 esporas ha-1 |
| T4: B. subtilis (Serenade®) | 1 × 1012 esporas ha-1 |
| T5: T. harzianum (TrichoD®) | 1 × 1010 esporas ha-1 |
| T6: B. subtilis (Serenade®) + T. harzianum (Tricho-D®) | 1 × 1012 esporas ha-1 1 × 1010 esporas ha-1 |
| T7: Control (Agua) | – |
Aplicación de los Tratamientos
Los tratamientos se aplicaron al suelo (drench) usando un volumen de agua de equivalente a 200 litros por hectárea para todos los tratamientos incluyendo el testigo (agua sin producto). Las dosis se aplicaron a las 5, 8 y 11 semanas de edad de las plántulas.
Variables Evaluadas
Altura de plántulas (cm). Se midió la altura de cada plántula desde la base del cormo hasta el ápice de la hoja más joven. Se realizó una medición al inicio del experimento, y luego se realizó evaluaciones cuando las plantas cumplieron 14, 16, 18 y 20 semanas de edad.
Crecimiento de plántulas (cm). Se calculó la diferencia entre la altura al final del ensayo y aquella registrada al inicio del ensayo. Este cálculo permitió identificar cuánto crecieron las plántulas desde la primera hasta la última semana de evaluación dentro del ensayo.
Diámetro del pseudotallo (mm). La medición del diámetro del pseudotallo se realizó utilizando un calibrador vernier digital Stanley modelo 78-440LA. La medida fue tomada a una altura de 5 cm del nivel del suelo, a las 14, 16, 18 y 20 semanas de edad.
Engrose de pseudotallo (cm). Se calculó la diferencia entre el diámetro del pseudotallo al final del ensayo y al inicio del mismo.
Número de hojas por planta. En cada una de las evaluaciones de la altura y diámetro del pseudotallo, se realizó el conteo del número de hojas presentes en cada una de las plántulas evaluadas a las 14, 16, 18 y 20 semanas de edad.
Emisión foliar (número de hojas). Para la evaluación de esta variable, se procedió a llevar un registro del número de hojas emitidas desde el inicio del ensayo hasta su culminación, mediante un conteo de hojas. Luego se promedió de acuerdo a cada unidad experimental.
Índice de clorofila (SPAD). Se evaluó el contenido de clorofila usando un medidor portátil de clorofila SPAD-502 Plus (Konica Minolta), que mide cuantitativamente la intensidad del verde de la hoja (650 a 940 nm) en SPAD. Las mediciones se registraron al inicio del ensayo, luego de la aplicación del 50% de las dosis de los tratamientos y al final del ensayo. Las mediciones se realizaron siempre en el mismo horario (14:00).
Longitud de raíces (cm). En la semana 20 días después de la siembra (DDS) se midió la longitud de las raíces, seleccionando aquellas más largas en cada planta y registrando su medida en centímetros.
Peso fresco radicular (g). Al final del ensayo, se separaron las raíces de la parte aérea y se pesaron.
Peso seco radicular (g). Las raíces de las plántulas utilizadas para evaluar la variable anterior, se llevaron a la estufa a 65 °C por un lapso de 48 horas, tiempo en que alcanzaron peso constante.
Sobrevivencia (%). La sobrevivencia de las plántulas de banano en el ensayo, se calculó aplicando la siguiente fórmula, en donde SPE corresponde a la sobrevivencia de plántulas en el ensayo, NPV es el número de plántulas vivas y TPS es el total de plántulas sembradas:
Análisis Estadístico
Las variables fueron sometidas al respectivo análisis de varianza, y se utilizó la prueba de Tukey (P ≤ 0.05) para la comparación de las medias de los tratamientos. El procesamiento de datos fue realizado en el software estadístico R Statistical Software (R Core Team, 2021).
Resultados y Discusión
Efecto de la Aplicación de Microorganismos Benéficos sobre el Desarrollo Vegetativo (tallo y hojas) de Plantas de Banano en Etapa de Vivero
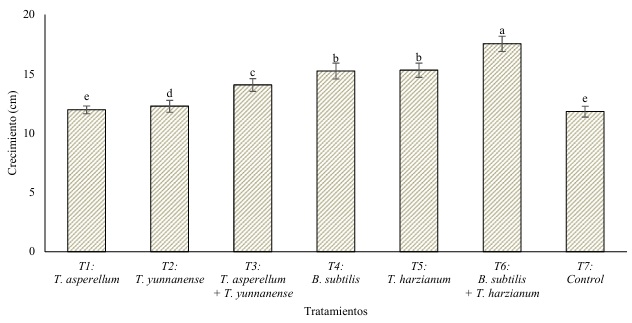
La aplicación de los microorganismos benéficos influyó en la altura, diámetro de pseudotallo y área de foliar de las plantas tratadas. A pesar de que se registraron datos en las semanas 14, 16, 18 y 20 después de la siembra, las diferencias estadísticas entre los tratamientos se observaron en los registros realizados a las 18 y 20 semanas. Esta respuesta indicaría que las plantas requieren al menos siete semanas desde la última aplicación de los tratamientos para mostrar incremento en su desarrollo. Al analizar los resultados obtenidos en la variable altura de planta, la mayor medida se registró en la semana 20 en las plantas tratadas con la combinación de T6 con 52.91 cm (Cuadro 2), tratamiento que, al analizar la diferencia entre el primer y último registro de altura presentó el mayor incremento o crecimiento con 17.54 cm (Figura 1).
Cuadro 2: Altura de plántulas de banano a nivel de vivero en respuesta a los tratamientos en estudio. Table 2: Height of banana seedlings at the nursery level in response to the treatments under study.
Table 2: Color of squash fruit peel (Cucurbita pepo L.) var. ‘Grey Zucchini’s.
| Tratamientos | Diámetro del pseudotallo (mm) | |||||||
| Semana 14 | Semana 16 | Semana 18 | Semana 20 | |||||
| T1: T. asperellum | 35.27 | a | 38.85 | a | 43.16 | b | 47.23 | c |
| T2: T. yunnanense | 35.30 | a | 38.93 | a | 43.54 | b | 47.57 | bc |
| T3: T. asperellum + T. yunnanense | 34.53 | a | 38.56 | a | 43.44 | b | 48.60 | bc |
| T4: B. subtilis | 34.70 | a | 39.27 | a | 44.65 | ab | 49.94 | b |
| T5: T. harzianum | 34.43 | a | 38.99 | a | 44.37 | ab | 49.75 | b |
| T6: B. subtilis + T. harzianum | 35.37 | a | 40.34 | a | 46.60 | a | 52.91 | a |
| T7: Control | 34.87 | a | 38.33 | a | 42.51 | b | 46.68 | c |
| Media | 34.92 | 39.04 | 44.04 | 48.95 | ||||
| Coeficiente de variación (%) | 2.56 | 2.18 | 3.32 | 4.39 | ||||
El impacto positivo de la aplicación combinada de B. subtilis + T. harzianum sugiere que la combinación específica de microorganismos, B. subtilis + T. harzianum, generó un efecto sinérgico que favoreció el desarrollo de las plántulas (Elnahal et al., 2022; Kredics et al., 2024). El incremento en el crecimiento de plantas de banano con la presencia de Trichoderma spp. y Bacillus spp. se puede atribuir a varios factores principales, según Etesami, Ryoung y Glick (2023) estos microorganismos favorecen la absorción de nutrientes al liberar enzimas como quitinasa, glucanasa, proteasa y celulasaque descomponen moléculas de nutrientes en formas más solubles para la planta. Además, de acuerdo a Zaheer et al. (2019), promueven la salud radicular al producir sustancias antimicrobianas que protegen las raíces de enfermedades (Jabborova et al., 2024; Ramírez-Pool, Calderón, Ruiz, Ortiz y Xoconostle, 2024). Zhao et al. (2015), agregan que otro de sus efectos es que desencadenan respuestas hormonales positivas al generar fitohormonas como ácido abscísico, auxinas, giberelinas, entre otras que estimulan el crecimiento (Giordano et al., 2023; Van Hee et al., 2023) y desarrollo de las plantas (Galeano et al., 2024).
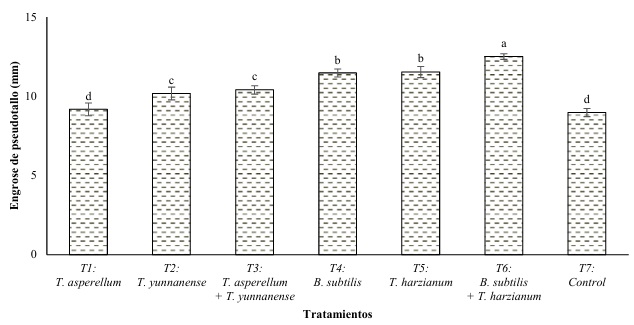
En cuanto al diámetro de pseudotallo, se observó que las plantas tratadas con T6 mostraron un mayor diámetro (43.87 mm) con relación a los otros tratamientos y control (39.83 mm), como se muestra en el (Cuadro 3). El incremento de esta variable (engrose de pseudotallo) entre las semanas 16 y 20 fue de 12.50 mm desde en el T6, seguido de 11.53 mm en el T5 con aplicación de T. harzianum y 11.47 mm de las plantas tratadas con B. subtilis, estadísticamente diferentes del control sin aplicación con 8.97 mm (Figura 2). En estas variables las cepas nativas de Trichoderma (T. asperellum y T. yunnanense) no lograron incrementar el desarrollo de las plántulas, llegando incluso a alcanzar valores similares a los registrados en el control, como es el caso de T. asperellum.Ghasemi, Esmaeili y Mohammadi (2022) y Santana, Vera y Vélez (20231), sostienen que esto podría atribuirse a la capacidad de los microorganismos para fortalecer las paredes celulares o inducir procesos fisiológicos que promueven un desarrollo más robusto de las estructuras del pseudotallo (Hao et al., 2022). La aplicación de microorganismos que mejoran el desarrollo de las plantas, tanto estructural como sanitariamente puede tener consecuencias positivas futuras a nivel de rendimiento o cosecha (Lamichhane, Corrales y Soltani, 2022; Reyes, León y Barrezueta, 2023; Seekham, Kaewsalong, Jantasorn y Dethoup, 2024).
Cuadro 3: Diámetro del pseudotallo de banano a nivel de vivero en respuesta a los tratamientos en estudio.
Table 3: Diameter of banana pseudostem at nursery level in response to the treatments under study.
| Tratamientos | Diámetro del pseudotallo (mm) | |||||||
| Semana 14 | Semana 16 | Semana 18 | Semana 20 | |||||
| T1: T. asperellum | 31.27 | a | 34.37 | a | 36.63 | b | 40.43 | b |
| T2: T. yunnanense | 31.30 | a | 34.47 | a | 37.27 | b | 41.47 | ab |
| T3: T. asperellum + T. yunnanense | 30.53 | a | 34.50 | a | 36.90 | b | 40.93 | b |
| T4: B. subtilis | 30.70 | a | 34.87 | a | 38.20 | ab | 42.17 | ab |
| T5: T. harzianum | 30.43 | a | 34.57 | a | 38.03 | ab | 41.97 | ab |
| T6: B. subtilis + T. harzianum | 31.37 | a | 36.10 | a | 40.20 | a | 43.87 | a |
| T7: Control | 30.87 | a | 33.87 | a | 35.93 | b | 39.83 | b |
| Media | 30.92 | 34.68 | 37.59 | 41.52 | ||||
| Coeficiente de variación (%) | 2.89 | 2.46 | 2.21 | 2.18 | ||||
Promedios con la misma letra en cada columna, no difieren estadísticamente según la prueba de Tukey (P ≤ 0.05).
Means with the same letters in the columns do not differ significantly according to Tukey (P ≤ 0.05).
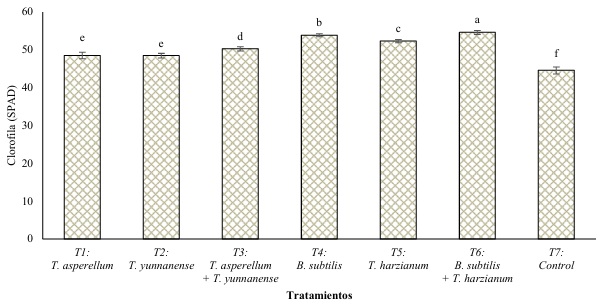
El número de hojas por planta fue estadísticamente superior en el tratamiento T6 con un promedio de 7, 8 hojas (Cuadro 4). Los demás tratamientos no presentaron valores con diferencias importantes con relación al testigo. Al analizar la diferencia entre el número de hojas final y del inicio de los registros (emisión foliar) no se encontraron diferencias entre ninguno de los tratamientos. Sin embargo, al analizar el índice de clorofila en las hojas de las plantas tratadas y sin tratar, se encontró que todos los tratamientos fueron estadísticamente diferentes del control (Figura 3). La cantidad de clorofila fue superior en los tratamientos T6 con 54.62 SPAD y T4 con 53.86 SPAD.
Cuadro 4: Número de hojas por plántula de banano a nivel de vivero en respuesta a los tratamientos en estudio.
Table 4: Number of leaves per banana seedling at the nursery level in response to the treatments under study.
| Tratamientos | Número de hojas por planta | |||||||
| Semana 14 | Semana 16 | Semana 18 | Semana 20 | |||||
| T1: T. asperellum | 3.37 | a | 4.47 | a | 5.83 | a | 7.20 | b |
| T2: T. yunnanense | 3.43 | a | 4.50 | a | 5.87 | a | 7.30 | ab |
| T3: T. asperellum + T. yunnanense | 3.37 | a | 4.50 | a | 5.80 | a | 7.23 | b |
| T4: B. subtilis | 3.53 | a | 4.63 | a | 5.93 | a | 7.30 | ab |
| T5: T. harzianum | 3.37 | a | 4.57 | a | 5.80 | a | 7.43 | ab |
| T6: B. subtilis + T. harzianum | 3.63 | a | 4.87 | a | 6.30 | a | 7.80 | a |
| T7: Control | 3.43 | a | 4.60 | a | 5.97 | a | 6.97 | b |
| Media | 3.45 | 4.59 | 5.93 | 7.32 | ||||
| Coeficiente de variación (%) | 4.56 | 7.33 | 3.45 | 3.76 | ||||
Promedios con la misma letra en cada columna, no difieren estadísticamente según la prueba de Tukey (P ≤ 0.05).
Means with the same letters in the columns do not differ significantly according to Tukey (P ≤ 0.05).
Estos resultados sugieren que la aplicación combinada de las cepas de Bacillus y Trichoderma estimuló el desarrollo y expansión de las hojas (Berg, Rybakova, Grube y Köberl, 2016; Alcedo y Reyes, 2018), contribuyendo al crecimiento foliar robusto de las plántulas (Mao y Jiang, 2021; Sánchez-Miranda, 2022). El crecimiento alcanzado se debe probablemente a una sinergia entre Trichoderma spp. y Bacillus subtilis en el fomento del desarrollo foliar durante la etapa de vivero (Liu, Li, Zhang, Liu y Huang, 2021), al igual que el efecto que los otros microorganismos pudieron haber tenido sobre la actividad fisiológica y en la capacidad de las plantas para generar y mantener hojas saludables (García-Crespo, Arcia, Pérez y Riera, 2012; Zhou, Yang, Wang, Guo y Huang, 2021). La consistencia en los resultados destaca que los microorganismos aplicados (aun en los tratamientos con menores promedios) promueven un desarrollo foliar más abundante y vigoroso en el contexto del vivero de banano (Ahmad et al., 2015; Ortega-Bonilla, Torres, Echeverría y Uribe, 2022). Rodríguez-Hernández et al. (2020) aislaron dos cepas de Bacillus amyloliquefaciens y tres de Bacillus subtilis, las cuales evaluaron en campo en dos híbridos de maíz (Galáctico y AG 614). La inoculación con la cepa Bacillus amyloliquefaciens incrementó el peso fresco de la planta, peso seco, diámetro de tallo, número de elotes, peso fresco de raíz y la longitud de la raíz; por su parte, Bacillus subtilis, incrementó el peso fresco de raíz.
En cuanto a la síntesis y retención de clorofila en las hojas de las plántulas de banano, es posible que tanto B. subtilis como Trichoderma spp. estén activando procesos bioquímicos que mejoran la eficiencia fotosintética (Alfiky y Weisskopf, 2021). Estos microorganismos, según describen Bononi, Chiaramonte, Pnasa, Moitinho y Melo (2020), son conocidos por sus propiedades promotoras del crecimiento y su capacidad para estimular respuestas hormonales en las plantas. Según Castillo, Piug y Cumagun (2019), los microorganismos estudiados pueden llegar a incrementar la producción de clorofila al mejorar la disponibilidad de nutrientes y agua, elementos esenciales para la fotosíntesis (Sánchez et al., 2018; Khatun, Joya, Hoque y Monjil, 2021).
Al analizar los porcentajes de sobrevivencia de las plantas tratadas y no tratadas no se encontraron diferencias estadísticas entre las mismas. Aunque la variabilidad no alcanzó significancia estadística, es notable que la aplicación de microorganismos benéficos no afectó negativamente la sobrevivencia, indicando una adecuada tolerancia de las plántulas a los tratamientos (Agüero et al., 2018).
Efecto de la Aplicación de Microorganismos Benéficios sobre el Desarrollo de Raíces de Plantas de Banano en Etapa de Vivero
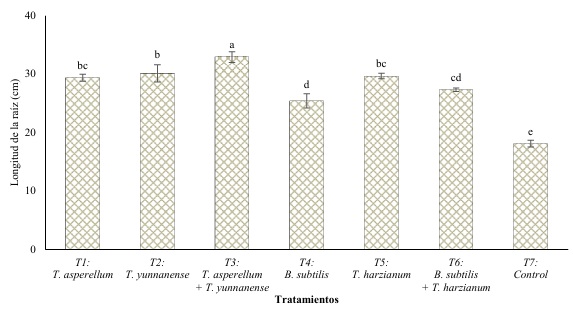
El desarrollo radicular de las plantas tratadas en comparación con las no tratadas (control) fue significativamente superior en todos los tratamientos con los microorganismos benéficos (Figura 4). La mayor longitud de raíces se registró en las plantas tratadas con la combinación de las cepas nativas de T3 con un promedio de 32.93 cm, seguidas del T2 con aplicación de T. yunnanense (30.13 cm). Por su parte, el control registró los valores más bajos con 18.10 cm. Con la aplicación de T3 se presentó mayor peso fresco y seco radicular con 367.93 y 145.84 g, respectivamente (Figura 5). Dichos valores fueron significativamente diferentes de los demás tratamientos quienes registraron pesos húmedos que oscilaron entre 235.53 y 342.03 gramos.
Figura 4: Longitud de la raíz en plántulas de banano durante el tiempo de estudio en respuesta a la aplicación de fertilización biológica. Promedios con la misma letra no difieren estadísticamente según la prueba de Tukey (P ≤ 0.05). Barras de error representan la desviación estándar en cada tratamiento.
Figura 5: Peso fresco y seco de la raíz en plántulas de banano durante el tiempo de estudio en respuesta a la aplicación de fertilización biológica. Promedios con la misma letra no difieren estadísticamente según la prueba de Tukey (P ≤ 0.05). Barras de error representan la desviación estándar en cada tratamiento.
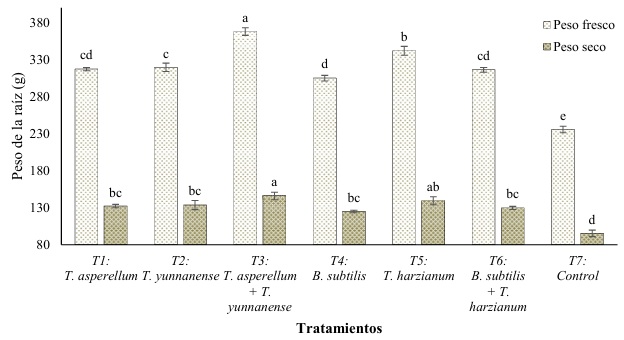
Figura 5. Fresh and dry weight of the root in banana seedlings during the study time in response to the application of biological fertilization. Means with the same letter do not differ statistically according to the Tukey test (P ≤ 0.05). Error bars represent the standard deviation in each treatment.
López, Pelagio y Herrera (2015), sostienen que las cepas nativas de Trichoderma spp. podrían haber desencadenado una serie de respuestas beneficiosas en las raíces de las plántulas de banano. Es bien conocido que el género Trichoderma posee la habilidad para solubilizar nutrientes en el suelo, facilitando así una mayor disponibilidad de elementos esenciales para las plantas (Wang et al., 2016). Esta característica, puede haber contribuido con el desarrollo radicular mejorado observado en T3, ya que un acceso más eficiente a los nutrientes del suelo es crucial para el crecimiento óptimo de las raíces (Du Jardin, 2015). Además, los compuestos promotores de crecimiento que produce Trichoderma spp. (fitohormonas y enzimas), podrían haber estimulado la elongación y proliferación de las raíces (Díaz et al., 2020; Hernández-Melchor et al., 2023), resultando en la longitud de raíz y peso fresco y seco superiores en comparación con otros tratamientos (Thapa, Sotang, Kumari y Joshi, 2020).
Varios autores destacan que las cepas nativas de Trichoderma pueden establecer simbiosis más efectivas y adaptadas al entorno local, maximizando así su impacto beneficioso en el desarrollo radicular de las plantas (Imam y Hassan, 2023; Imran, Abo-Elyousr, Mousa y Saad, 2022). En conjunto, la presencia específica de estas cepas nativas de Trichoderma en el tratamiento T3: T. asperellum y T. yunnanense ha actuado como un componente clave en la biofertilización, promoviendo un sistema radicular robusto que sienta las bases para un crecimiento saludable y sostenible de las plantas de banano en las etapas posteriores del cultivo (Companioni, Domínguez y García, 2019). Karmakar, Gupta, Das, Thattacharya y Saha (2021) encontraron que la especie T. yunnanense tiene el potencial para incrementar el desarrollo radicular, así como también conferir resistencia a enfermedades provocadas por patógenos del suelo. De igual manera, T. asperellum ha sido ampliamente reconocida como una especie de hongo benéfico con propiedades enfocadas en fortalecer el sistema radicular de los cultivos donde es aplicado, al igual que potencia la resistencia a hongos importantes del suelo como Fusarium spp. (El-Komy, Al-Qahtani, Ibrahim, Almasrahi y Al-Saleh, 2022; Sehim, Hewedy, Altammar, Alhumaidi y Abd-Elghaffar, 2023).
Conclusiones
El estudio sobre el efecto combinado de Bacillus sp. y Trichoderma spp. en el desarrollo de plántulas de banano (Musa spp. AAA) en etapa de vivero demuestra que la aplicación de estos microorganismos benéficos puede mejorar significativamente el crecimiento y la salud de las plántulas. Los resultados indican que la combinación de B. subtilis y T. harzianum produce un incremento notable en la altura, diámetro del pseudotallo y área foliar, sugiriendo que estos microorganismos actúan sinérgicamente para potenciar el desarrollo vegetativo.
La investigación también resalta la importancia de un manejo sostenible en la producción agrícola, ya que el uso de bioestimulantes puede reducir la dependencia de insumos químicos, promoviendo prácticas más amigables con el medio ambiente. Además, se observó que las plántulas tratadas mostraron una mayor sobrevivencia y vigor, lo que podría traducirse en una producción más eficiente y sostenible a largo plazo. En conclusión, este estudio no solo aporta al conocimiento científico sobre el uso de microorganismos en la agricultura, sino que también ofrece una estrategia viable para mejorar la productividad en los viveros de banano, contribuyendo así a la sostenibilidad del cultivo y al bienestar económico de los productores.