Introducción
Las dunas costeras se caracterizan por su riqueza de especies y servicios ambientales que proveen (Guadarrama et al., 2014; Jiménez-Orocio, Espejel y Martínez, 2015; Mendoza-González et al., 2021). La dinámica de formación en las dunas se relaciona estrechamente con la erosión eólica y generalmente no presentan evidencias de erosión hídrica (Bolaños-González et al., 2016). Sin embargo, las actividades productivas, recreativas, provisión de servicios y de infraestructura, que ahí se desarrollan, paulatinamente han modificado su estructura y función (Monzón-Bruguera, 2009; Ortega-Rubio, Muñoz, Rivera y Azuz, 2011; García-Dueñas, Castellanos y Miranda, 2023). En México, se carece de una política ambiental de gestión o protección específica, de dicho ambiente lo que ha propiciado la alteración de su capacidad de resiliencia (Quiroz-Villanueva, Cervantes, Olivos y Martínez, 2022; Hernández, Villanueva, Coego, Bao y Sáez, 2023). A su vez, los fenómenos naturales como los ciclones tropicales y el aumento del nivel del mar (Cid-Salinas et al., 2013; Soto, 2018), cambio climático (Ovando-Hidalgo, Tun, Mendoza y Parra, 2020) y la presencia de especies invasoras, como por ejemplo: Scaevola taccada (Castillo-Campos et al., 2022) y Cassytha filiformis (Parra-Tabla, Tun, García y Martínez, 2024) son elementos que amenazan con desaparecer la vegetación de las dunas costeras.
Las especies que conforman la vegetación de dunas costeras son capaces de tolerar condiciones limitantes; ya sea, altos niveles de salinidad y temperatura del suelo, bajas concentraciones de materia orgánica, baja disponibilidad de agua, las cuales limitan su sucesión y disminuyen su diversidad (Mendoza-González et al., 2022). Mientras que las estructuras subterráneas de la vegetación contribuyen a la reducción de la erosión que afecta las dunas (Bryant, Bryant, Sharp, Bell y Moore, 2019; Figlus, Sigren, Feagin y Armitage, 2022). En los suelos de las dunas costeras predomina los hongos formadores de micorrizas principalmente del género Glomus (Wang et al., 2021; Hanlon, 2021; Tenzin, Noirungsee, Runsaeng, Noppradit y Klinnawee, 2022; Greipsson, Stover, Whitney y McElroy, 2024).
La vegetación tienen la capacidad de establecer asociaciones con dichos microorganismos, realzando la resistencia al estrés hídrico, mejoran la adquisición de nutrimentos y brindan protección contra enfermedades, lo que incrementa su supervivencia y establecimiento (Guadarrama-Chávez, Sánchez, Álvarez y Ramos, 2004; Carmona-Escalante, Guadarrama, Ramos, Castillo y Montaño, 2013; Ramos-Zapata, Zapata, Ortíz y Guadarrama, 2011; González-González, Torres, Ortega y Gómez, 2016) y la adquisición de biomasa subterránea (Dong, Hu, Alamusa, Ma y Liu, 2023). En este sentido, es reconocido que la biomasa aérea y subterránea (raíces y tallos enterrados) contribuyen a reducir la erosión (Feagin et al., 2019; De Battisti y Griffin, 2020).
Existe evidencia que señalan las ventajas de emplear la interacción micorrizal en planes de recuperación de sistemas dunares costeros, favoreciendo la adquisición de nutrimentos del suelo, optimización de la capacidad de resistencia al estrés y la defensa contra patógenos (Guadarrama y Ramos, 2020; Carrillo-Saucedo, Puente, Montes y Cruz, 2022; Mendoza-González et al., 2022; Farrer, Van Bael, Clay y Smith, 2022). Inclusive el uso de micorrizas comerciales contribuye a elevar la acumulación de biomasa y cantidad de esporas en los suelos (Luecke, Mejia y Crawford, 2021). Es por ello, que la aplicación de hongos formadores de micorrizas y organismos benéficos como estrategia en la revegetación de las dunas costeras podría contribuir a la recuperación de este sistema biológico degradado; por tanto, en el presente studio-evaluamos la influencia de la aplicación de un consorcio micorrízico comercial (Fosfonat®) sobre el crecimiento y acumulación de biomasa en Scaevola plumieri y Sophora tomentosa, especies de plantas nativas y estabilizadoras de la duna costera.
Materiales y Métodos
Especies de estudio. Scaevola plumieri (L.) Vahl (Goodeniaceae). Arbusto perenne de 0.4 a 2 m de altura. Hojas simples, suculentas, grandes, gruesas y lisas, de 5 a 11 cm de largo y de 2 a 7 cm de ancho, al desprenderse dejan cicatrices en el tallo de color verde amarillento. Flores solitarias zigomórficas, pequeñas y blanquesinas. Fruto carnoso de color azul/morado o negro cuando está maduro de 10 a 15 mm de diámetro (Gutiérrez-Báez, Avendaño y Zamora, 2013). Distribución general: Centroamérica y las Antillas. En México: Tamaulipas, Veracruz, Tabasco, Campeche, Yucatán y Quintana Roo (Herbario virtual; CICY, 2024).
Sophora tomentosa L. (Fabaceae). Arbusto de 3 a 4 m de altura. Hojas alternas, compuestas, foliolos de 13 a 21, ovados, raquis pubescente. Inflorescencia terminal, racimo de 10 a 40 cm, corola amarillo brillante con 5 pétalos, pedicelos pubescentes de 8 a 9 mm de largo. Vainas con cáliz persistente de 5 a 13 cm de largo, entre 5 a 10 semillas subglobosas, color café oscuro (Lonard, Judd y Stalter, 2015). Distribución general: Neotrópico. En México: Tamaulipas, Veracruz, Campeche, Yucatán y Quintana Roo (Herbario virtual; CICY, 2024).
Origen de las semillas. Se obtuvieron frutos de diversos individuos de ambas especies localizados en la duna costera que se ubica en las cercanías a la carretera Champotón-Ciudad del Carmen, Campeche. Se recolectaron frutos maduros de color púrpura intenso de S. plumieri o bien en proceso de fermentación. Mientras que para S. tomentosa se colectaron vainas secas de color castaño, grisáceo. Posteriormente, se seleccionaron semillas que no tuvieran indicios de perturbaciones por pérdida de agua, daños en su cubierta, abertura de micrópilo y de similar tamaño. No se empleó ningún tipo de escarificación química o mecánica.
Diseño del experimento y condiciones experimentales. El experimento tuvo una duración de 197 días (siembra: 16 de noviembre de 2022; cosecha: 1 de junio de 2023) y se desarrolló en un vivero tipo forestal con sombra del 50% (malla de poliestireno), provisto con un sistema de riego por microaspersión. La temperatura promedio al interior del vivero fue de 26.7 °C y humedad relativa de 83.67%, ambas mediciones se realizaron en un termohigrómetro digital Walfront®. Se empleó un diseño experimental completamente al azar, utilizando dos especies nativas de la vegetación de duna costera (Scaevola plumieri y Sophora tomentosa) y dos tratamientos (Consorcio de microorganismos benéficos, Fosfonat®, y Control). Para evitar afectaciones al desarrollo del experimento, durante los meses de marzo a mayo, se humedeció el suelo con agua corriente para mantener la humedad relativa al interior del vivero. Mientras que para evitar daños a las plántulas por hormigas se aplicó cal hidratada (Ca(OH)) mensualmente en el suelo perímetro del vivero. Asimismo, el perímetro del vivero contó con una protección de malla ciclónica galvanizada de 69 × 69 mm × 2.50 m cal. 12.5; para evitar el ingreso de fauna al interior. De igual manera el suelo del vivero conto con malla anti-maleza de polipropileno en color negro (Figura 1).
Para la siembra, se emplearon germinadores forestales tipo banca de 98 unidades tubulares (tubetes), con capacidad de 120 mL; previamente desinfectados con hipoclorito de sodio al 4% durante 1 h, los cuales se llenaron con una mezcla 50:50 v/v de perlita (Multiperl®) y peat moss (CosmoPeat®). Se utilizaron cuatro germinadores (392 tubetes por tratamiento) por especie. Para la inoculación del consorcio comercial se aplicó el producto comercial Fosfonat® (Bactiva), compuesto por 132 esporas g-1 de Glomus intraradices, G. mosseae, G. etunicatum, G. aggregatum y 2 ×109 UFC de bacterias benéficas de Azospirillum brasiliense, Azotobacter chroococcum, Bacillus megaterium y Pseudomonas fluorescens. Durante el desarrollo del experimento, se realizaron tres inoculaciones, previo a la siembra se aplicó inóculo a las semillas de ambas especies del tratamiento Consorcio, sumergiéndolas en una solución al 0.25% (w/v) de inoculante durante 1 h. La segunda aplicación se realizó a los 30 días posteriores a la emergencia, utilizando la misma concentración aplicada en la primera aplicación. Finalmente, a los 60 días después de la siembra, se aplicó la tercera, utilizando una solución al 0.75% (w/v) de inoculante aplicado al sustrato.
Adicionalmente, las plántulas de ambas especies de ambos tratamientos se fertilizaron con el biofertilizante líquido comercial Fertikabil® (Nitrógeno orgánico: 15%, P: 2%, K: 8%, materia orgánica: 32%, pH: 7.5, ácidos fúlmicos: 4%, ácidos húmicos: 8%) en dos concentraciones, la primera fue del 0.5% (v/v) a los 60 días, después de la siembra, aplicándola una vez cada semana durante un mes. Posteriormente, se aplicó el biofertilizante al 11% (v/v), 90 días después de la siembra de las semillas. Este fertilizante se aplicó en forma de nebulización con un aspersor sobre las hojas de las plántulas.
Variables de estudio. Las variables del crecimiento se midieron en intervalos de 15 días (8 de febrero al 20 de mayo de 2023). La altura total, se midió desde el cuello del tallo hasta el ápice utilizando una regla graduada en mm, y por último se realizó el conteo del número de hojas y foliolos (para el caso de S. tomentosa). Al final del experimento se tomó una muestra de 20 plántulas del total, a las cuales se les midió la longitud de las raíces y se disectaron separando hojas, tallo y raíces. Los valores de biomasa, se obtuvieron de manera separada las partes de las plántulas mediante su secado en una estufa de convección Wisconsin Memmert® a una temperatura de 60 °C durante 72 horas. Posteriormente, se pesaron en una balanza digital marca AEAdam® modelo HCB602H (0.01 g).
Análisis estadístico. Las comparaciones de las variables del crecimiento (número de hojas, altura de la plántula y longitud de raíces) y la biomasa acumulada en hojas, tallo y raíces entre los tratamientos fueron realizadas con las pruebas t-Student (t) y Mann-Whitney (U) a un nivel de significancia P < 0.05, los supuestos de normalidad (Shapiro-Wilk) y homogeneidad de varianzas (Levene) se verificaron previo a la aplicación de las pruebas estadísticas con el programa Past versión 4.13 (Hammer y Harper, 2001).
Resultados y Discusión
La emergencia de las plántulas de S. tomentosa inició a los 17 días, mientras que para S. plumieri inició a los 27 días posteriores a la siembra. En el tratamiento Consorcio registramos el 86% de emergencia para S. plumieri y en el Control obtuvimos el 79%. En semillas con tres años de almacenamiento se ha registrado el 65% de emergencia a las 16 semanas posteriores a la siembra (Knevel, Venema y Lubke, 2002). Es posible que las diferencias en los porcentajes de emergencia sean debido a que las semillas utilizadas en el presente experimento se almacenaron por 30 días. Además, cabe señalar que la colecta de frutos se realizó en el mes de octubre del año 2022. Lo cual coincide con los meses (octubre a febrero) de mayor producción de semillas maduras (Knevel y Lubke, 2005).
De manera semejante a la anterior especie, el tratamiento Consorcio la emergencia de S. tomentosa fue del 81% y en el Control se obtuvo el 78%. La latencia de S. tomentosa está condicionada por la capacidad de protección de la semilla y a la abertura del micrópilo como principal barrera ante la pérdida y absorción de agua (Delgado, Souza, Santos y Silveira, 2015). Aunado, las semillas de la especie son frecuentemente afectadas por hongos e insectos depredadores (Nogueira y Arruda, 2006). De manera que los porcentajes de emergencia que se obtuvieron en el experimento pueden atribuirse al periodo de colecta de frutos y su selección. Para ambas especies se eligieron semillas sin indicios de perturbaciones por pérdida de agua, daños externos visibles en su cubierta y evidencia de apertura en el micrópilo en el caso de S. tomentosa. A su vez, el remojo en agua con el inóculo, de las semillas del tratamiento Consorcio, durante 1 h previo a la siembra pudo actuar como una medida de escarificación y promover la pronta germinación y emergencia.
Número de hojas. En ambas especies se encontraron diferencias significativas entre los tratamientos en cuanto al número de hojas a partir de la tercera medición realizada a los 45 días posteriores a la emergencia (Figura 2 a, b). Al final del experimento (90 días) la diferencia promedio entre tratamientos fue de 3.2 hojas para S. plumieri y 1.98 hojas para S. tomentosa. Al respecto, se ha estudiado en condiciones experimentales que la aplicación de fertilizantes químicos conduce a un aumento en el área foliar de S. plumieri (Gilbert, Pammenter y Ripley, 2008). Sin embargo, valores bajos de área foliar pueden ser favorables para mantener el balance hídrico de la especie (Ripley y Pammenter, 2004).
Figura 2: Número de hojas en plántulas de las especies estabilizadoras de duna costera. Los valores indican la media y el error estándar (media ± E. E.). Las letras minúsculas diferentes denotan diferencia significativa (U Mann Withney; P < 0.0001). Las barras grises oscuras representan el tratamiento con fertilización y las barras grises claras el control sin fertilización. Especies: (a) Scaevola plumieri; (b) Sophora tomentosa.
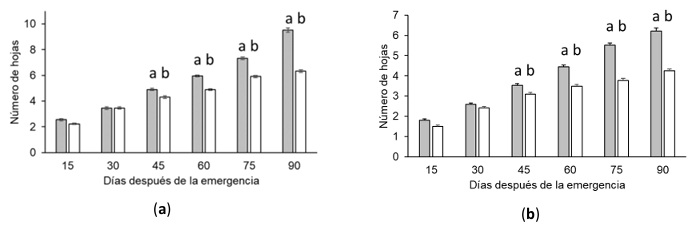
Figure 2: Number of leaves in seedlings of coastal dune stabilizing species. Values indicate the mean and standard error (mean ± S. E.). Different lowercase letters denote significant difference (U Mann Withney; P < 0.0001). Dark gray bars represent the fertilized treatment, and light gray bars represent the unfertilized control. Species: (a) Scaevola plumieri; (b) Sophora tomentosa.
Altura de la planta. Se encontraron diferencias estadísticas significativas entre los tratamientos para ambas especies a los 90 días post-emergencia. En S. plumieri la diferencia entre tratamientos en la media de la altura fue de 13.1 mm en tanto que para S. tomentosa fue de 21.11 mm (Figura 3 a, b). En condiciones naturales los individuos adultos de S. tomentosa muestran dos momentos de máximo desarrollo del tallo (Kuki, Oliva y Pereira, 2008). Asimismo, en condiciones naturales, la aplicación de fertilización química no genera diferencias en la longitud del tallo con respecto a las plantas sin fertilización (Gilbert et al., 2008). Sin embargo, el enterramiento en arena (Gilbert y Ripley, 2008), la orientación de los individuos respecto de la duna (Gilbert, Pammenter y Ripley, 2011) y el desarrollo de la planta en condiciones ambientales con limitaciones en nutrimentos (Gilbert et al., 2008), favorecen el constante crecimiento del tallo de S. plumieri. En playas del pacífico mexicano la especie tiene afinidad a dunas embrionarias y suelos con alta fertilidad (Frías-Ureña et al., 2022). Las diferencias observadas en el crecimiento en ambas especies contribuyen a entender la capacidad de resiliencia de las dunas costeras y la respuesta de la flora de las dunas ante el cambio climático y las especies invasoras y en consecuencia (McGuirk, Kennedy y Konlechner, 2022).
Figura 3: Altura (mm) de las plántulas de especies estabilizadoras de duna costera. Los valores indican la media y el error estándar (media ± E. E). Las letras minúsculas diferentes denotan diferencia significativa (t-Student; P < 0.0001). Las barras grises oscuras representan el tratamiento con fertilización y las barras grises claras el control sin fertilización. Especies: (a) Scaevola plumieri; (b) Sophora tomentosa.
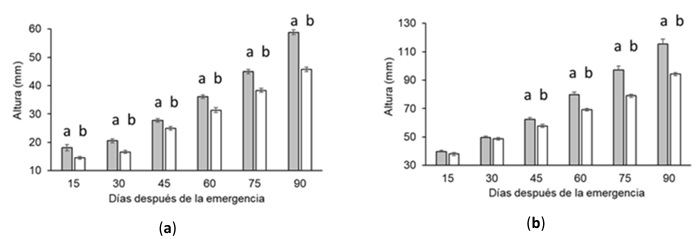
Figure 3: Height (mm) of coastal dune stabilizing species seedlings. Values indicate the mean and standard error (mean ± S. E). Different lowercase letters denote significant difference (t-Student; P < 0.0001). Dark gray bars represent the fertilized treatment, and light gray bars represent the unfertilized control. Species: (a) Scaevola plumieri; (b) Sophora tomentosa.
Longitud de las raíces. Se encontraron diferencias significativas en la longitud de las raíces de ambas especies (Figura 4). La presencia de un extenso sistema de raíces y tallos subterráneos en adición con bajas áreas foliares en S. plumieri le confieren una baja transpiración y demanda de agua (Ripley y Pammenter, 2004). En los nódulos de las raíces de S. tomentosa se han registrado diversas especies de bacterias de los géneros: Bacillus, Brevibacillus, Paenibacillus, Rhizobium y Sinorhizobium; de manera que la especie posee la capacidad de establecer estrechas relaciones simbióticas con microrganismos fijadores de nitrógeno (Toma et al., 2017). La longitud de las raíces pudo estar limitada por el tubete forestal empleado en el experimento. Por lo que, además, de la longitud y biomasa de las raíces es necesario incorporar los rasgos funcionales, p. ej.: densidad del tejido radicular, longitud específica de la raíz, diámetro promedio de la raíz y diámetro de la raíz; a fin de comprender las posibles interacciones entre la vegetación y la dinámica de la duna costera (Walker y Zinnert, 2022).
Figura 4: Longitud de las raíces (cm) de las plántulas de especies estabilizadoras de duna costera. Las barras indican la media y el error estándar (media ± E. E.). Las letras minúsculas diferentes denotan diferencia significativa (t-Student; P < 0.05). Las barras grises representan el tratamiento con fertilización y las barras blancas el control sin fertilización.
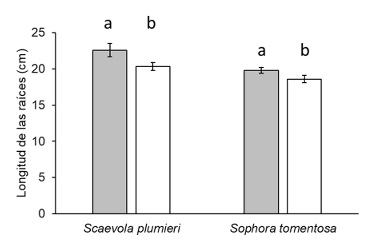
Figure 4: Root length (cm) of coastal dune stabilizing species seedlings. Values indicate the mean and standard error (mean ± S. E). Different lowercase letters denote significant difference (t-Student; P < 0.05). Gray bars represent the fertilized treatment, and white bars represent the unfertilized control.
Biomasa aérea y subterránea. Los tratamientos difieren significativamente en la comparación de la biomasa seca acumulada en hojas, tallo y raíz para S. plumieri y para S. tomentosa en hojas y raíz (Figura 5 a, b). Los efectos de la adición de P, sobre la morfología y biomasa de Scaevola aemula son positivos a niveles por debajo de 20 mg L-1 de P (Burnett, Zhang, Stack y He, 2008). No se conducen a diferencias en el crecimiento del tallo en plantas enterradas en la arena respecto de plantas no cubiertas con arena (Gilbert y Ripley, 2008). En el caso de S. tomentosa su crecimiento en ambientes degradados y con altas concentraciones de sal promueve la ganancia de peso en las raíces de las plántulas (Santos, Goi y Neto, 2001). Además, S. tomentosa puede ser considerada como especie biomarcadora in situ de la calidad ambiental (Kuki et al., 2008). El presente experimento se desarrolló en un vivero forestal y se aplicó un biofertilizante líquido lo que pudo favorecer la adquisición de nutrimentos por el consorcio de microorganismos favoreciendo el crecimiento y la acumulación de biomasa. La adición de nutrimentos potencia la acumulación de biomasa aérea inclusive en condiciones de alta densidad de plantas (Morton et al., 2025). Además, es posible que la acumulación de biomasa observada haya sido debido a la inoculación con el consorcio de microorganismos comercial (Luecke et al., 2021). Sin embargo, la acumulación de biomasa puede ser limitada bajo condiciones de estrés salido (Clark, Busch y Crawford, 2021). Lo anterior, trae consigo la necesidad de implementar experimentos en los cuales el estrés salino sea un factor a evaluar.
Figura 5: Acumulación de biomasa (g) en las plántulas. Las barras indican la media y el error estándar (media ± E. E.). Tratamientos: Consorcio, barras en color gris y Control, barras en color blanco. Las letras minúsculas diferentes denotan diferencia significativa (t-Student; P < 0.0001). Las barras grises oscuras representan el tratamiento con fertilización y las barras grises claras el control sin fertilización. Especies: (a) Scaevola plumieri; (b) Sophora tomentosa.
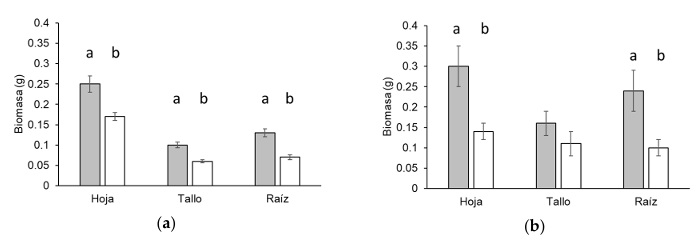
Figure 5: Accumulation of biomass (g) in the seedlings. The bars indicate the mean and standard error (mean ± S. E.). Treatments: Consortium, gray bars and Control, white bars. Lowercase letters denote significant difference (t-Student test P < 0.0001). Dark gray bars represent the fertilized treatment, and light gray bars represent the unfertilized control. Species: (a) Scaevola plumieri; (b) Sophora tomentosa.
Conclusiones
En el presente estudio se encontró que el uso de consorcios de microorganismos (hongos formadores de micorrizas y bacterias benéficas) promueven el crecimiento y acumulación de biomasa en dos especies arbustivas estabilizadoras de la duna costera. La aplicación de microorganismos benéficos durante la etapa de producción de plantas en vivero puede potenciar el éxito de las estrategias de revegetación en ambientes cuyos suelos presentan condiciones limitantes y estresantes como es el caso de las dunas costeras. Los resultados del estudio empleando el Fosfonat® como consorcio micorrízico comercial pueden contribuir como estrategia de restauración y recuperación de la vegetación costera, a fin de aliviar los efectos adversos de la erosión y mitigar los efectos del cambio climático en las zonas costeras del Golfo de México. Los resultados del experimento muestran un incremento de las diferencias entre los tratamientos en cuanto al número de hojas y altura en ambas especies. En futuras investigaciones es necesario incluir otras especies nativas p. ej.: especies pioneras de hábitos rastreros, evaluar rasgos funcionales de las plantas y ampliar el tiempo de los ensayos para alcanzar un mayor desarrollo de las plántulas y evaluar su establecimiento en los sitios potenciales de revegetación. Además, en el diseño de políticas públicas del sector ambiental, programas de recuperación de ecosistemas costeros degradados, se debe considerar el uso de microorganismos benéficos nativos; por un lado, para contribuir al éxito en el establecimiento de las plantas y por otro lado para aliviar la competencia frente a las especies invasoras. Lo anterior, también puede ser aplicado en otros ecosistemas degradados con suelos que presenten condiciones salinas que limitan el crecimiento de las plantas nativas.

















