Introducción
El virus del fruto rugoso marrón del jitomate (ToBRFV) representa una seria amenaza para la producción de jitomate. Este virus fue identificado inicialmente en Israel en 2014 (Solanum lycopersicum) (Luria et al., 2017), y se extendió a Jordania en 2015 (Salem et al., 2016). Desde entonces, su presencia ha aumentado drásticamente. El ToBRFV ha sido detectado en cultivos de jitomate en diversas regiones, como México (Cambrón-Crisantos et al., 2018), Alemania (Menzel et al., 2019), Turquía (Fidan et al., 2019), Reino Unido (Skelton et al., 2019), China (Yan et al., 2019), Países Bajos (Van de Vossenberg et al., 2020), Estados Unidos (Ling et al., 2019), Italia (Panno et al., 2019), Palestina (Alkowni, 2019), Grecia (EPPO, 2019/210), España (EPPO, 2019/238) y Francia (MAA, 2020). En particular, en 2020, se infiltró en invernaderos de chile en Italia y Jordania (Salem et al., 2020; Panno et al., 2020a), mientras que en 2018 también afectó a invernaderos comerciales de pimiento en México (Cambrón-Crisantos et al., 2018). Esta propagación generalizada del ToBRFV a través de los continentes subraya su amenaza sustancial para el cultivo del jitomate. Es por ello que resulta imperativo tomar medidas urgentes para combatir su expansión desenfrenada y proteger los ecosistemas agrícolas.
El ToBRFV, clasificado como un tobamovirus, exhibe una morfología característica en forma de varilla rígida en sus partículas. Su genoma consiste en ARN de cadena sencilla monocatenario (+ARNcs) que alberga cuatro marcos abiertos de lectura (ORF). Dentro de estos ORFs, son ORF1 y ORF2 quienes dirigen la función de la ARN polimerasa dependiente de ARN (RdRp). El ORF3 codifica la proteína de movimiento (MP), mientras que el ORF4 la síntesis de la proteína de la cápside (CP) (Luria et al., 2017). Este virus destaca por la estabilidad de sus partículas, lo que facilita considerablemente su transmisión mecánica. Como consecuencia, las prácticas de cultivo en invernaderos sirven como el principal conducto para su diseminación (Levitzky et al., 2019; Panno et al., 2020b). La robustez de las partículas del ToBRFV amplifica su potencial para propagarse rápidamente, enfatizando la necesidad apremiante de medidas estrictas para restringir su propagación y salvaguardar los ecosistemas de cultivo.
En este contexto, la detección del ToBRFV en plantas se ha abordado mediante una serie de técnicas, que incluyen el ensayo de inmunoabsorción ligado a enzimas (ELISA), la microscopía electrónica de transmisión, la RT-PCR, la secuenciación de segunda generación, la qRT-PCR y la amplificación isotérmica mediada por bucle (LAMP) (Oladokun et al., 2019; Ling et al., 2019; Panno et al., 2019; Sarkes et al., 2020). Estos métodos difieren en cuanto a sus límites de sensibilidad, implicaciones de costos y el nivel de conocimientos necesarios para su ejecución. La elección de la técnica óptima depende de los objetivos de diagnóstico específicos, el tipo de material vegetal examinado, las limitaciones presupuestarias y el tiempo disponible para el análisis. La variedad de técnicas de detección subraya la necesidad de un enfoque a medida que adapte el método elegido a las exigencias particulares del diagnóstico. Este enfoque pragmático garantiza tanto la precisión como la optimización de recursos para combatir la proliferación del ToBRFV.
En México, el Centro Nacional de Referencia Fitosanitaria (CNRF) inicialmente respaldó el uso de técnicas moleculares para la identificación de ToBRFV, específicamente la RT-PCR de punto final utilizando el par de oligonucleótidos ToBRFV F/ToBRFV-R (Rodríguez-Mendoza et al., 2019). No obstante, una reciente actualización de los protocolos de diagnóstico molecular ha introducido mejoras integrales. Los procedimientos revisados ahora incluyen una combinación de RTPCR de punto final, RT-qPCR y RT-qPCR multiplex. Según las últimas directrices publicadas por la CNRF, el diagnóstico del ToBRFV requiere un enfoque integrado, en el cual un resultado positivo debe ser corroborado por al menos dos de las técnicas mencionadas (SENASICA, 2022). Este cambio hacia una estrategia de diagnóstico multifacética subraya la importancia de obtener resultados sólidos y validados de forma cruzada, en línea con las mejores prácticas internacionales. El mayor énfasis en la precisión del diagnóstico es fundamental para contener la propagación del ToBRFV en el panorama agrícola de México.
El propósito de este estudio fue realizar una comparación exhaustiva de diversos protocolos de extracción de ARN para evaluar su eficacia en la detección del ToBRFV. Además, buscamos evaluar el límite de detección de tres pares de oligonucleótidos distintos utilizando metodologías de RT-PCR y RT-PCR anidada. A través de este análisis comparativo, nuestro estudio tuvo como objetivo determinar la combinación más eficaz y sensible de métodos de extracción de ARN y los pares de oligonucleótidos para la detección precisa del ToBRFV. Esta investigación contribuye a mejorar la precisión y fiabilidad de las técnicas de diagnóstico cruciales para gestionar la propagación del ToBRFV en entornos agrícolas.
Material vegetal como fuente de inóculo. Durante septiembre de 2020, se recolectaron plantas de tomate (Solanum lycopersicum), que mostraban clorosis, estrechamiento foliar y mosaicos (síntomas típicos de la infección por ToBRFV) en invernaderos comerciales de Colima, México (Figura 1). La fuente de inóculo dio positivo para ToBRFV por RT-PCR. Con este tejido se inoculó mecánicamente una planta de Nicotiana glutinosa y se observaron lesiones necróticas locales. Posteriormente, se cortó una de estas lesiones para inocular una segunda planta de N. glutinosa. Este proceso se repitió dos veces. Se utilizó una lesión local de la cuarta planta de N. glutinosa para inocular una planta de tomate. A continuación, 30 días después de la inoculación (dpi), se analizó mediante RT-PCR utilizando los oligonucleótidos específicos (ToBRFV-FMX: AACCAGAGTCTTCCTATACTCG-

Figura 1 A-C) En plantas de jitomate saladette recolectadas en invernaderos, se observaron síntomas evidentes de mosaico, deformación foliar y estrechamiento de las hojas. Estas plantas dieron positivo para el virus del fruto rugoso marrón del jitomate (ToBRFV). D-E) Las observaciones visuales en hojas inoculadas de Nicotiana revelaron la presencia de lesiones cloróticas y necróticas localizadas causadas por la infección con ToBRFV. Las plantas utilizadas para el estudio y que resultaron positivas al virus provinieron de Tecomán, Colima, México.
GAA/ ToBRFV-RMX: CTCWCCATCTCTTAATAATCTCCT: 475 pb Región ORF 1-RdRp) y las condiciones descritas por Rodríguez-Mendoza et al. (2018), Cuadro 1. Posteriormente se secuenciaron los fragmentos esperados y se compararon en el GenBank. La fuente de inóculo se incrementó mediante inoculación mecánica sobre plantas de tomate para realizar los diferentes bioensayos de los hospedantes.
Cuadro 1 Oligonucleótidos probados en este estudio para la detección del ToBRFV en jitomate, tomatillo y berenjena.
| Secuencias de nucleótidos de los oligonucleótidos (5’-3’) | Tamaño esperado del fragmento y región para la amplificación por PCR | Condiciones de RT-PCR | Referencias |
|---|---|---|---|
| ToBRFV-FMX: AACCAGAGTCTTCCTATACTCGGAA | 475 pb (ORF 1-RdRp)θ | - 95° 3 minβ. | Rodríguez- Mendoza et al., 2018 |
| -32 ciclos: 95° 50 sΩ, | |||
| ToBRFV-RMX: CTCWCCATCTCTTAATAATCTCCT | 53° 50 s y 72° 55 s. | ||
| -72°C 10 min. | |||
| TobN up3: GGCGYTGCARACIATHGTITAYCA | 400 pbα (ORF 1-RdRp) θ | -95° 3 minα. | Dovas et al., 2004 |
| -4 ciclos: 95° 30 s, | |||
| TobN do4: GTRTTICCIATRAAIGTIGTIACRTC | 51° 30 s y 72° 30 s. | ||
| -26 cycles: 95° 30 s, | |||
| TobN do4G: GCCGATRAAGGTGGTGACRTC | 51° 30 s y 72° 30 s. | ||
| -72°C 10min. | |||
| ToBRFV-F: GAAGTCCCGATGTCTGTAAGG | 842 pb (ORF 3- MP) θ | -95° 3 min. | Ling et al., 2019 |
| -32 ciclos: 95° 50 s, | |||
| ToBRFV-R: TGCCTACGGATGTGTATGA | 53° 50 s y 72° 55 s. | ||
| -72°C 10min. |
θ Sección del gen ToBRFV amplificado, αRT-PCR anidada, βminutos, Ωsegundos.
Evaluación de los métodos de extracción de ARN total. Se sembraron 20 semillas de pimiento morrón y jitomate saladette en cada una de las tres placas Petri asignadas a cada especie de planta. Las semillas se germinaron en placas de Petri con toallas de papel humedecidas con agua destilada estéril. Después de 10 a 20 días, cuando las hojas cotiledonares emergieron y se expandieron, se extrajeron 100 mg de plántulas completas (tallo, hojas y raíz) de cada especie de planta para la extracción de ARN total. Además, se plantaron tres semillas en vasos de espuma de poliestireno de 1 L con turba para la mayoría de cada especie de planta, utilizando una planta como réplica. Las plantas se mantuvieron en un invernadero con ciclos de 12 horas de luz y 12 horas de oscuridad, y temperaturas mínimas de 15 °C y máximas de 32 °C. Después de 45 días, se recolectaron 100 mg de tejido foliar (pedicelos, hojas y brotes) para la extracción de ARN total. Se evaluaron cuatro métodos de extracción de ARN: PlantRNAeasy miniKit®, siguiendo las instrucciones del fabricante; Trizol®, CTAB 2 % y CTAB 2 %-Trizol®, según el protocolo descrito por Jordon-Thaden et al. (2015) con modificaciones menores (véase apéndice 1). La maceración del tejido vegetal (pedicelos, hojas y brotes) se realizó con nitrógeno líquido en un mortero estéril. La cantidad y calidad del ARN extraído se cuantificaron con un Nanodrop 2000®, y se registraron las medidas de absorbancia 260/280 y 260/230.
Evaluación de oligonucleótidos y límite de sensibilidad. Mecánicamente se inocularon tres repeticiones de plántulas de jitomate (S. lycopersicum), berenjena (Solanum melongena) y tomatillo (Physalis ixocarpa). Las inoculaciones se llevaron a cabo al emerger y desarrollarse la primera hoja verdadera (foliolo), y se incluyeron plantas no inoculadas como controles. Todas las plantas se mantuvieron en las condiciones previamente descritas en el invernadero. A los 30 días post inoculación (dpi), cuando las plantas exhibieron síntomas de clorosis y mosaico, se procedió a la extracción de ARN total mediante el protocolo CTAB-Trizol previamente mencionado. La calidad y cantidad del ARN extraído se verificaron con un Nanodrop 2000® y se ajustó la concentración final a 300 ng µL-1. A continuación, se realizaron diluciones seriadas de cada extracción de ARNt ajustadas a 10, 1, 0,1, 0,01, 0,001 y 0,0001 ng µL-1. Se probaron los pares de oligonucleótidos específicos descritos por Ling et al. (2019) y Rodríguez-Mendoza et al. (2018), y reportados por Dovas et al. (2004) (Cuadro 1). Optamos por este protocolo debido a su mayor rendimiento en concentración de nanogramos en comparación con el uso de Trizol y el kit, a la vez que resultaba más rentable. Se siguieron las especificaciones descritas en los protocolos para cada par de oligonucleótidos.
Evaluación de los métodos de extracción de ARN total. En nuestra comparación de metodologías, observamos que las plántulas de tomate y pimiento presentaron una concentración significativamente superior de ARN total (Figura 2). Notablemente, el protocolo CTAB-Trizol mostró el resultado más destacado en términos de nanogramos por microlitro, alcanzando la concentración más alta (966 ng μL-1). En contraste, el Kit de aislamiento de ARN exhibió la concentración más baja (29 a 101 ng μL-1) entre los métodos evaluados (Figura 2).
Evaluación de oligonucleótidos y límite de sensibilidad. Nuestros hallazgos delinean los diferentes límites de sensibilidad de diferentes conjuntos de oligonucleótidos en la detección de ToBRFV utilizando ARN total extraído de plantas de jitomate, tomatillo y berenjena (Cuadro 2). Específicamente, los oligonucleótidos diseñados por Ling et al. (2019) mostraron la capacidad de detectar el virus hasta una concentración de 0.01 ng µL-1 en muestras de tomate y tomatillo. Por el contrario, su sensibilidad en muestras de ARN de berenjena se manifestó a una concentración superior de 1 ng µL-1. Paralelamente, los oligonucleótidos desarrollados por Rodríguez-Mendoza et al. (2018) mostraron un límite de detección de 0.1 ng µL-1 en tomate y 0.01 ng µL-1 en tomatillo. Independientemente de la selección de oligonucleótidos, el umbral de sensibilidad para la detección del virus en muestras de berenjena residió consistentemente en 1 ng µL-1.
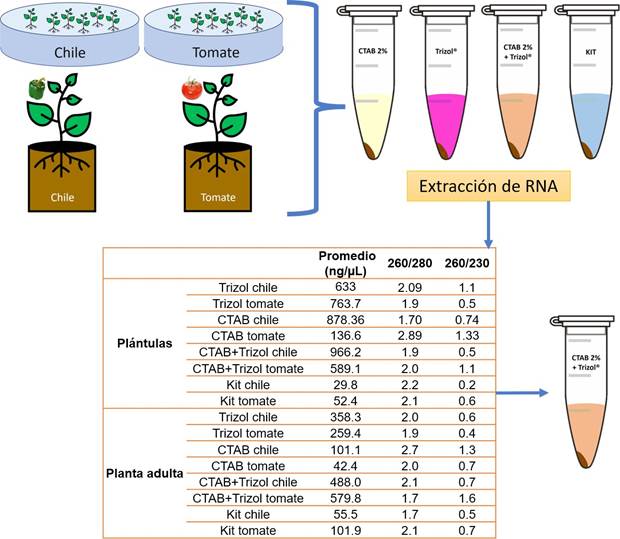
Figura 2 La evaluación de los métodos de extracción de ARN total implicó la comparación de su eficacia y rendimiento, medidos a través de lecturas de absorbancia en un espectrofotómetro Nanodrop 2000®. De los métodos probados, que incluyeron Trizol®, CTAB 2 % y CTAB 2 %-Trizol®, el protocolo CTAB 2 %-Trizol® demostró producir la concentración más elevada de ARN total, mientras que el kit de aislamiento de ARN resultó en la concentración más baja. Estos datos fueron registrados mediante mediciones de absorbancia a longitudes de onda de 260/280 y 260/230. El Nanodrop 2000® se utilizó para cuantificar la concentración de ARN extraído y evaluar su calidad a través de estas relaciones de absorbancia. Los resultados señalan que el protocolo CTAB 2 %-Trizol® fue especialmente efectivo en la extracción de ARN de alta calidad de las muestras de plantas, lo que lo convierte en una opción adecuada para análisis moleculares posteriores.
Cuadro 2 Comparación de referencias de oligonucleótidos, fuentes vegetales y límites de detección de ARN en la fuente de material vegetal infectado.
| Referencias para oligonucleótidos | Fuente de Material Vegetal Infectado | Límite de Concentración Detectada de ARN Total (ng μL-1) |
|---|---|---|
| Rodriguez-Mendoza et al., 2018. | Jitomate | 0.1000 |
| Jitomate | 0.0100 | |
| Jitomate | 1.0000 | |
| Ling et al., 2019. | Tomatillo | 0.0100 |
| Tomatillo | 0.0100 | |
| Tomatillo | 1.0000 | |
| Dovas et al., 2004. | Berenjena | 0.0001 |
| Berenjena | 0.0010 | |
| Berenjena | 1.0000 |
En particular, se destacó un aumento notable en los umbrales de sensibilidad al emplear la técnica RT-PCR anidada con el conjunto de oligonucleótidos propuesto por Dovas et al. (2004) en muestras de jitomate y tomatillo. Esta optimización permitió la identificación de un alto nivel de sensibilidad en la detección del ToBRFV, alcanzando 0.0001 ng µL-1 en tomate, 0.001 ng µL-1 en tomatillo y 1 ng µL-1 en muestras de berenjena (Cuadro 2, Figura 3). Estas sutiles variaciones en los umbrales de sensibilidad subrayan la importancia de la selección cuidadosa de los oligonucleótidos y la aplicación de la amplificación RT-PCR anidada para optimizar la capacidad de detección del ToBRFV en diversas especies de plantas.
Se han desarrollado diversos métodos de extracción de ARN con un objetivo central: producir concentraciones óptimas de ARN de alta calidad. Este objetivo adquiere especial relevancia al considerar que los tejidos vegetales suelen albergar cantidades significativas de sustancias potencialmente interferentes, tales como compuestos fenólicos, polisacáridos, pigmentos y RNasas (Wang et al., 2009). La diversidad del contenido fenólico en las plantas está sujeta a variaciones determinadas por factores como la fase de desarrollo y la exposición a influencias ambientales bióticas y abióticas. En el caso de las hojas de tomate, el contenido de fenoles puede disminuir con el avance de la edad de la planta. Sin embargo, es importante destacar que la composición de varios compuestos fenólicos puede experimentar variaciones dinámicas a lo largo de las distintas etapas de desarrollo de la hoja (Dadáková et al., 2020). Esta compleja interacción entre las técnicas de extracción de ARN y la composición diversa de los tejidos vegetales enfatiza la importancia de elegir métodos apropiados para asegurar la obtención de muestras de ARN confiables y representativas para los análisis subsiguientes.
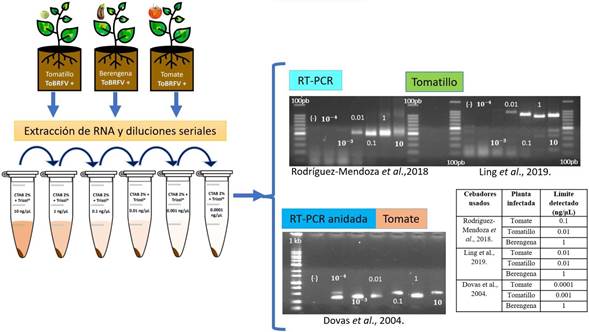
Figura 3 Evaluación y sensibilidad de los oligonucleótidos PCR. Análisis electroforético en geles de agarosa al 1.5 % de los productos de RT-PCR y RT-PCR anidada (tamaño esperado de los oligonucleótidos de Ling 842 pb; tamaño esperado de los oligonucleótidos de Rodríguez-Mendoza 475 pb; tamaño esperado de los oligonucleótidos de Dovas 400 pb). (-): agua esterilizada en lugar de ARN. 100pb= 100pb DNA Ladder (Invitrogen®). 1Kb= 1000 pb DNA ladder (Promega®). 10-3 y 10-4 = 0.001 y 0.0001 ng µL-1.
Los compuestos polifenólicos participan de manera significativa en complejas interacciones, formando intrincados agregados moleculares con proteínas y ácidos nucleicos. Esta propensión a crear complejos de gran peso molecular complica aún más el proceso de extracción. Simultáneamente, la presencia de polisacáridos agrava la situación, ya que tienden a coprecipitar con el ARN en la ejecución de protocolos de extracción basados en alcohol. Este fenómeno resulta en la persistencia de contaminantes polisacáridos en el producto final de ARN extraído, afectando su integridad (Salzman et al., 1999).
La eficacia de los métodos CTAB y Trizol trasciende su rentabilidad. Estos métodos han sido ampliamente adoptados en diversas especies y tejidos vegetales, siempre arrojando resultados favorables (Gambino et al., 2008). La notable calidad y pureza del ARN, junto con la naturaleza rápida y económica de estas técnicas de extracción, las convierten en opciones especialmente adecuadas para la detección de virus (Mathioudakis et al., 2020). El método CTAB destaca por facilitar la extracción rápida de ARN de tejidos desafiantes, eliminando la necesidad de utilizar productos químicos peligrosos (Chang et al., 1993). Es importante señalar que, aunque el método Trizol produce extracciones de ARN de alta calidad, también extrae ADN simultáneamente. La combinación de Trizol con la extracción mediante CTAB mejora aún más la calidad de la extracción de ARN total.
La calidad y la concentración del ARN extraído ejercen un profundo impacto en la precisión y la confiabilidad de diversos estudios moleculares de plantas, como la RT-PCR (Gambino et al., 2008) y el análisis de la expresión génica (Toni et al., 2018). Sin embargo, en el marco de ensayos de detección a gran escala, la elección de un método de extracción de ARN también se ve influenciada por consideraciones de costo. En este sentido, metodologías como CTAB y Trizol emergen como opciones rentables en comparación con los kits disponibles comercialmente. La versatilidad y eficacia de los métodos CTAB y Trizol se extienden a diversas especies y tejidos vegetales, ofreciendo resultados sistemáticamente favorables (Gambino et al., 2008). Estos métodos presentan la doble ventaja de obtener ARN puro y de alta calidad de manera rápida y económica, lo que los posiciona como especialmente beneficiosos para la detección acelerada de virus (Mathioudakis et al., 2020).
Nuestros resultados evidencian de manera clara la variabilidad en los límites de sensibilidad presentados por cada par de oligonucleótidos en las diferentes especies vegetales. Es probable que este fenómeno se deba a las variaciones en los niveles de expresión y concentración del patógeno en las distintas plantas hospedantes. De manera interesante, la berenjena mostró límites de sensibilidad consistentes, independientemente del conjunto de oligonucleótidos utilizado. En el caso del tomatillo, tanto los oligonucleótidos de Ling como los de Rodríguez-Mendoza exhibieron límites de sensibilidad equivalentes, mientras que para el tomate, los oligonucleótidos de Ling demostraron una sensibilidad diez veces mayor. Específicamente, los oligonucleótidos de Ling están meticulosamente diseñados para apuntar a la región de la proteína de cubierta, mientras que los de Rodríguez-Mendoza detectan la región RdRp. Una observación destacada por Magaña-Álvarez et al. (2021) subraya el rendimiento superior de los oligonucleótidos dirigidos a la proteína de cubierta en la detección del ToBRFV en plantas de tomate en comparación con los oligonucleótidos dirigidos a la RdRp.
Se ha corroborado que la PCR anidada, a pesar de requerir más tiempo y recursos, ofrece una sensibilidad y fiabilidad superiores en comparación con la PCR convencional (Shin et al., 2004). Como podría esperarse, los oligonucleótidos de Dovas exhibieron una sensibilidad impresionante, siendo cien veces mayor en jitomate y diez veces mayor en tomatillo. En resumen, nuestros resultados destacan que, bajo las condiciones experimentales específicas, el protocolo óptimo de detección para ToBRFV se configura como el método de extracción de ARN CTAB-Trizol emparejado con la RT-PCR anidada utilizando los oligonucleótidos delineados por Dovas et al. (2004).
En conclusión, hemos llevado a cabo una comparación exhaustiva de diversos protocolos moleculares para la detección del virus del fruto rugoso marrón del jitomate (ToBRFV) en hospedantes solanáceos. Dada la amenaza significativa que representa el ToBRFV para la producción mundial de tomate, la detección temprana y precisa se vuelve crucial para mitigar su impacto. Nuestro estudio evaluó tanto métodos de extracción de ARN como distintos pares de oligonucleótidos PCR específicos, buscando determinar su eficacia en la detección del virus.
Entre los diversos protocolos analizados, el método que demostró mayor sensibilidad para la detección del ToBRFV fue la combinación del protocolo de extracción de ARN CTAB-Trizol junto con la PCR anidada utilizando los oligonucleótidos descritos por Dovas et al. (2004). Estos resultados resaltan la importancia de seleccionar combinaciones adecuadas de protocolos de extracción y amplificación para alcanzar niveles óptimos de sensibilidad y precisión en la detección del ToBRFV.
En última instancia, esperamos que nuestros hallazgos contribuyan a mejorar la exactitud de las técnicas de diagnóstico esenciales para gestionar la propagación del ToBRFV en entornos agrícolas, ofreciendo así una herramienta valiosa en la lucha contra esta amenaza para la producción de tomate a nivel mundial.















