
Las plantas medicinales de México como fuente de compuestos activos contra la leishmaniasis
Mexican medicinal plants as source of active compounds against leishmaniasis
María Adelina Jiménez-Arellanes,1 Lorena Alamilla-Fonseca,2 Gabriel Alfonso Gutiérrez-Rebolledo1
1 Unidad de Investigación Médica en Farmacología, Hospital de Especialidades, CMN Siglo XXI, IMSS.
]]> 2 Laboratorio de Inmunoparasitología, Unidad de Medicina Experimental, Facultad de Medicina, Universidad Nacional Autónoma de México.
Correspondencia:
Dra. Adelina Jiménez Arellanes
U.I.M. en Farmacología, Hospital de Especialidades, CMN
Siglo XXI, IMSS.
Av. Cuauhtémoc 330, Col. Doctores 06720, Delg.
Cuauhtémoc, México, D.F.
Tel. 56 27 69 00 ext 21367
Emal: adelinajim08@prodigy.net.mx
Fecha de recepción: 05 de febrero de 2014
Fecha de recepción de modificaciones: 30 de junio de 2014
Fecha de aceptación: 07 de julio de 2014
Resumen
La leishmaniasis es una enfermedad emergente no controlada y endémica de 98 países. Anualmente se registran 2 millones de tipo cutánea, 500,000 de tipo visceral y 60,000 mueren por esta causa. En México se conoce como úlcera del chiclero y se presenta en 22 estados. El tratamiento es con fármacos antimoniales pentavalentes de alto costo y muy tóxicos. Una alternativa es la búsqueda de moléculas activas en las plantas medicinales, donde se reporta que dihidrocorinanteina, corinanteina y corinanteidina resultaron activos contra L. major; harmano, pleiocarpina, buchtienina, luteolina y quercetina fueron activos contra L. donovani. En México se han evaluado aproximadamente 25 plantas medicinales siendo las más activas y las más investigadas Tridax procumbens, Lonchocarpus xuul y Pentalinon andrieuxii, de las cuales han aislado los compuestos activos cuyo CI50 < 30 µg/mL contra L. mexicana.
Palabras clave: plantas medicinales, leishmaniasis, compuestos naturales activos.
Abstract
]]> Leishmaniasis is considered as an uncontrolled emerging disease and is endemic in 98 countries. Anually, is registered about 2 million cases of cutaneous, 500,000 cases of visceral-type and 60,000 persons die. In Mexico it is known as Chiclero's ulcer and is reported in 22 states. For its treatment, pentavalent antimonial drugs are administered, these drugs cause severe side effects are high cost and drug resistance cases have been reported. One alternative to currently available drugs is the search for active molecules in medicinal plants, dihydrocorynantheine, corynantheine and corynantheidine were active against Leishmania major; harmane, pleiocarpine, buchtienine, luteolin and quercetin are active against L. donovani. In Mexico has been evaluated about 25 medicinal plants being the most active and most investigated Tridax procumbens, Lonchocarpus xuul and Pentalinon andrieuxii. From these plants have been isolated the active compounds with IC50 <30 µg/mL.Key words: Medicinal plants, leishmaniasis, active natural compounds.
Introducción
La leishmaniasis es causada por diferentes especies de Leishmania y está clasificada por la Organización Mundial de la Salud (OMS) dentro de las enfermedades emergentes con categoría uno y no controladas, también es considerada por este organismo como una de las seis enfermedades tropicales más importantes. Es endémica en 98 países (tropicales y subtropicales) y es más frecuente en hombres. Hoy en día se estima que en el mundo existen 20 millones de personas infectadas, 350 millones están en riesgo y se reporta una incidencia de dos a tres millones de nuevos casos por año.1,2
Al año se presenta de 1.5 a 2 millones de casos de leishmaniasis cutánea (la forma más frecuente y afecta tanto a niños como adultos), 500,000 casos de tipo visceral y 60,000 personas mueren por esta última causa. En México, el principal agente causal es L. mexicana, su presencia se ha reportado en 22 estados y es considerada endémica en Coahuila, Nuevo León, Tamaulipas, Veracruz, Tabasco, Campeche, Yucatán, Quintana Roo, Chiapas, Oaxaca, Guerrero, Michoacán, Jalisco, Nayarit, San Luis Potosí, Morelos, Puebla e Hidalgo, en donde comúnmente se le conoce como "úlcera de los chicleros.3-6 Recientemente se han reportado casos de coinfección leshmaniasis con VIH/SIDA, los cuales son de pobre pronóstico. La infección por este parásito depende en gran media del estado del sistema inmunológico.6
En la actualidad, para tratar la leishmaniasis se emplean fármacos de primera elección como estibogluconato sódico conocido comercialmente como Pentostam y el antimoniato de meglumine (nombre comercial Glucantime). Una siguiente opción es el isotianato de pentamidina (nombre comercial pentamidina), la anfotericina B (Fungizona o Ambisome), miltefosina y sulfato de paramomicina (Aminosidina); aunque esta última opción no es muy empleada en México y no es muy efectivo cuando se administra oralmente.
Los fármacos antimoniales fueron desarrollados hace más de 70 años y ya no son muy efectivos debido a la fármaco resistencia que ha desarrollado el parásito,2,6-8 aunado al escaso desarrollo en este tipo de medicamentos. Estos fármacos provocan severos efectos secundarios como insuficiencia renal, pancreatitis, mialgia, neuropatía periférica, hepatotoxicidad y cardiotoxicidad, aunado a que el tratamiento es prolongado (por más de 30 días, dependiendo de la evolución del paciente), la administración es por vía parenteral, son caros, no siempre efectivos por la resistencia del parásito a los medicamentos disponibles, en ocasiones el paciente no tiene acceso a los sistemas de salud y no pueden utilizarse en personas que padecen insuficiencia renal, hepática o cardiaca; ni en aquellas con tuberculosis.6
Actividad leishmanicida de plantas medicinales y de compuestos puros
El desarrollo de medicamentos para tratar enfermedades parasitarias como la leishmaniasis ha sido escaso, debido a que estas enfermedades se presentan con mayor frecuencia en países en vías de desarrollo y a las industrias farmacéuticas no les reditúa mayores ganancias debido a que tienen que desarrollar medicamentos de bajo costo para que sean accesible a la población de condición socioeconómica baja.6,9 Una alternativa a los fármacos sintéticos es la búsqueda de moléculas activas en fuentes naturales como las plantas medicinales utilizadas en el tratamiento de la leishmaniasis, por su uso ancestral, por su contenido de compuestos y diversidad estructural.6 Además, la OMS ha enfatizado la urgente necesidad por desarrollar nuevos fármacos para el tratamiento de la leishmaniasis.2
]]> En este sentido, podemos mencionar que las plantas medicinales biosintetizan numerosos metabolitos secundarios, por lo que pueden constituir una fuente importante de agentes leishmanicidas.9 Los productos naturales han jugado y juegan un papel importante en la terapéutica actual; entre 1981 al 2006 se obtuvieron 1184 nuevos fármacos de origen natural y el 28% de estos provinieron de plantas. Por otro lado, el 24 % de los nuevos fármacos sintéticos presentan como molécula base o bien son derivados de moléculas activas obtenidas de plantas medicinales.6,10 Otro reporte indica que entre el 2000 y 2005, se introdujeron al mercado 23 nuevos fármacos de origen natural, los cuales presenta diversidad estructural y biológica. Por lo que, los productos naturales constituyen una riqueza inconmensurable de estructuras químicas que han sido y seguirán siendo una fuente importante de nuevos fármacos o bien pueden constituir moléculas prototipo para el desarrollos de nuevas sustancias activas.11,12 Algunos ejemplos de principios activos obtenidos de plantas medicinales y que se utilizan en la terapéutica actual son paclitaxel (aislado de Taxus brevifolia), camptotecina (aislado de Camptohteca acuminata), vinblastina y vincristina (aislados de Catharanthus roseus), estos compuestos son utilizados hoy en día en la terapia de diversos tipos de cáncer.La morfina (aislados de Papaver somniferum) es empleado como analgésico; el clorhidrato de apomorfina (derivado de la morfina) y el bromuro de galantamina (alcaloide aislado de Galanthus nivalis) son utilizados en el tratamiento de la enfermedad del Parkinson. La codeína (aislado de P. somniferum) es empleada como antitusígeno. Otros ejemplos importantes lo constituyen el bromuro de tiotropio (es un derivado de la atropina aislada de Atropa belladona) y se utiliza para el tratamiento de broncoespasmos asociados al EPOC (enfermedad pulmonar obstructiva crónica), la nitisona aislado de Callistemon citrinus, esta sustancia es empleada en la tirosinemia tipo 1 hereditaria.12
Sobre el desarrollo de compuestos activos contra Leishmania, a la fecha solo cuatro moléculas son candidatos potenciales para el desarrollo de fármacos antileishmania (estas sustancias están en fase I/II de investigación) como la miltefosine (alquilfosfolípido) que se usa en la India desde 2002 y en Colombia fue autorizado en el 2005 y está en fase clínica de investigación para determinar su posible uso a nivel mundial,2 paranomicina (aminoglicósido), la 8-aminoquinolina sitamaquina y la berberina (este último es un alcaloide de origen vegetal, aislado de Beberis vulgaris), este compuesto es empleado para este padecimiento desde hace más de 50 años y se ha demostrado su actividad in vitro e in vivo.6,13,14 Recientemente, algunos metabolitos secundarios como naftoquinonas, lignanos, neolignanos, alcaloides, chalconas y triterpenos han sido reportados con actividad leishmanicida.15-17
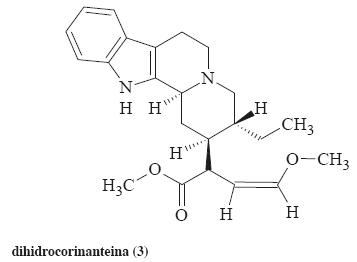
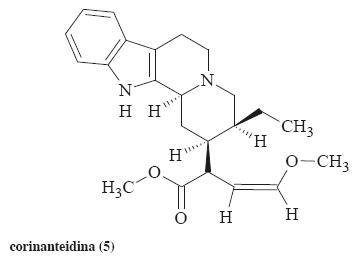
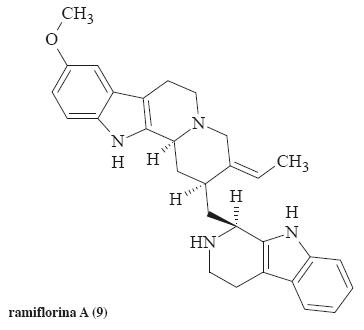
Dentro de estos metabolitos secundarios destacan algunos alcaloides aislados de especies vegetales que han demostrado significativa actividad leishmanicida in vitro. Algunos ejemplos son la isoguattouregidina (1), alcaloide indólico aislado de Guatteria foliosa que mostró una concentración inhibitoria media (CI50) = 100 µg/mL contra L. donovani y L. amazonensis; la coronaridina (2, aislado de Peschirea australis) mostró una CI50 = 12 µg/mL contra L. amazonensis. Los alcaloides indólicos aislados de Corynanthe pachyceras, identificados como dihidrocorinanteina (3), corinanteina (4) y corinanteidina (5) resultaron activos contra L. major con CI50~30 µM. Los alcaloides indólicos: harmano (6), pleiocarpina (7) y buchtienina (8) aislados de la corteza y hojas de Kopsia griffithii fueron activos contra promastigotes de L. donovani mostrando una CI50 = 6.25, 25 y 1.56 µg/mL, respectivamente;16-18 la desventaja es que estos alcaloides han sido evaluados en diferentes cepas de Leishmania y en diferentes estadios y ninguno de estos compuestos está en investigación clínica. Otros alcaloides activos fueron la ramiflorina A y B, (9 y 10, aislados de Aspidosperma ramiflorum), estos compuestos mostraron una dosis letal media (DL50) = 16.3 y 4.9 µg/mL contra promastigotes de L. amazonensis.16 El alcaloide 4-hidroxi-1-tetralona (11) aislado de la corteza de Ampelocera edentula, resultó activo contra promastigotes de L. brazilensis, L. amazonensis y L. donovani, mostrando CI50 = 10 µg/mL.19








Por otro lado, existen otros trabajos que describen la actividad in vitro de extractos de plantas medicinales como Ambrosia miratima y Acacua nilotica con valores de IC50 < 8 µg/mL;20 pero de estas especies vegetales no han aislado los compuestos responsables de la actividad. El extracto etanólico de las hojas y las fracciones de diclorometano y cloroformo de Azadirachta indica mostraron una CI50 = 38, 3.9 y 1.2 µg/mL contra promastigotes de L. amazonensis, respectivamente y contra amastigotes, la CI50 fue de 9.8, 1.1 y 0.6 µg/mL.9
La fracción rica en ácido torméntico (12), ácido 2α,3 β-dihidroxiursan-12-en-28-oico (13), ácido 2α,3 β-dihidroxiolean-12-en-oico (14), ácido ursólico (15) y ácido oleanólico (16) de Pourouma guianensis resultó muy activa contra promastigotes de L. amazonensis mostrando una CI50 = 100 µg/mL; además, el ácido ursólico (15) y ácido oleanólico (16), fueron también muy activos contra los amastigotes intracelulares (CI50 = 27 y 11 µg/mL, respectivamente). Estos compuestos resultaron más activos que el glucantime (CI50= 83 µg/mL).15 Una revisión adicional describe que las flavonas luteolina (17) y quercetina (18) (aisladas de Vitex negundo y Fagopyrum esculentum) fueron activas contra amastigotes de L. donovani, mostrando una CI50 = 12.5 y 45.5 µM; la chalcona identificada como licochalcona A (19, aislada de Glycyrrhiza sp) mostró una CI50 = 0.9 µg/mL (2.7 µM) contra amastigotes de L. donovani y contra promastigotes de L. major mostró un CI50 = 7.2 µg/mL (21 µM).








La 2',6'-dihidroxi-4'-metoxichalcona (20, aislada de Piper aduncum) inhibe el crecimiento de promastigotes y amastigotes intracelulares de L. amazonensis, las dosis efectiva media (DE50) fueron de 0.5 µg/mL (1.9 µM) y de 24 µg/mL (89 µM), respectivamente. La formulación de este compuesto (440 µg) con nanopartículas poliméricas y administrada por 42 días a ratones BALB/c infectados con L. amazonensis redujó en un 53% las úlceras cutáneas y el compuesto puro redujó sólo el 23%.17,21 Un glucosecoiridoide, amarogentina (21) aislado de Swertia chirata fue evaluado in vivo junto con dos formulaciones (liposomal y niosomal) en ratones infectados con L. donovani; la formulación niosomal-amarogentina redujó en un 90% la carga de parásito en el bazo de los animales tratados.17,22


La plumbagina (22), naftoquinona aislada de la corteza de Pera benensis resultó muy activo contra promastigotes y amastigotes intracelulares de L. donovani (CI50 = 0.21 µM); estudios in vivo demostraron que la plumbagina retardó el desarrollo de L. amazonensis y L. venezuelensis. El tratamiento local de una simple lesión con 8,8'-biplumbagina (23) resultó mejor que el tratado con glucantime (fármaco de referencia). Además, la plumbagina (22) y 8,8'-biplumbagina (23) fueron muy activas in vitro contra amastigotes de L. amazonensis y contra promastigotes de L. brazilensis, L. amazonensis y L. donovani mostrando valores de CI90 = 5 µg/mL.17,23-25
]]>

Las saponinas mesabalides III (24) y VI (25), obtenidas de Maesa balansae resultaron muy activas contra amastigotes intracelulares de L. infantum (CI50 = 7 y 14 ng/mL, respectivamente); a pesar de mostrar importante actividad leishmanicida, estos compuestos resultaron altamente citotóxicos, por lo que no constituyen candidatos a seguir investigando. La saponina esteroidal racemósido A (26, aislada de Asparagus racemosus) induce apoptosis en promastigotes y amastigotes de L. donovani y mostró valores de CI50 = 1.31 y 0.61 µg/mL, respectivamente.17 La α- y β-hederina (27, 28) y hederacholchisido A (29) obtenidos de Hedera hélix mostraron actividad leishmanicida, siendo el compuesto 29 el más activo, cuya CI50 fue de 1.2 y 0.053 µM contra promastigotes y amastigotes intracelulares de L. infantum, respectivamente.17 La diospirina (30) fue aislada de Euclea natalensis y resultó activa contra promastigotes de L. donovani.26,27







Como se puede observar, en la literatura se describen diversos tipos de metabolitos secundarios aislados de plantas medicinales que tiene importante actividad leishmanicida; sin embargo, algunos compuestos activos resultaron tóxicos, por lo que no constituyen candidatos para seguir investigando.
]]> En el caso de México, para tratar la leishmaniasis se emplea diversas especies vegetales y algunos tratamientos no convencionales. Por ejemplo, utilizan termoterapia que consiste en aplicar aceite de automóvil caliente vertido directamente en la lesión, aplican monedas o utensilios de metal al rojo vivo, huesos de animales calientes o el foco caliente colocadas sobre la úlcera y también emplean la crioterapia que consiste en colocar hielo sobre la lesión. En algunas ocasiones llegan a emplear polvo de penicilina sobre la herida o usan pomadas antifúngicas (como el miconazol, ketoconazol o itraconazol). También suelen utilizar ácido acético, ácido bórico, ácido sulfúrico (ácido de batería de carro), alcohol, formalina, peróxido de hidrógeno, alumbre, sulfato de cobre entre otros14,28 Sí bien estos tratamientos solo deforman y agudizan la inflamación, los pacientes siguen estos métodos al no saber que se trata de una parasitosis y que requiere de atención médica profesional. Algunas especies vegetales que son empleadas comúnmente en México para tratar la lieshmaniasis se describen en la Tabla 1.14,29
A pesar que en México se emplean diversas plantas medicinales para tratar principalmente las infecciones cutáneas provocadas por Leishmania; a la fecha, existen escasos trabajos que exploran la actividad in vitro y/o in vivo de estas. Peraza-Sánchez y col. describen la evaluación in vitro de los extractos metanólicos de 18 plantas medicinales del estado de Yucatán contra promastigotes de L. mexicana y encontraron que los extractos de Aphelandra scabra (hojas), Byrsonima bucidaefolia (corteza), B. crassifolia (corteza), Clusia flava (hojas), Cupania dentata (corteza), Diphysa carthagenensis (hojas), Dorstenia contrajerva (planta completa), Milleria quinqueflora (raíz), Tridax procumbens (planta completa) y Vitex gaumeri (corteza) fueron los más activos, mostrando una CI50 < 50 µg/mL.30 Este mismo grupo evaluó 15 extractos, fracciones y algunos compuestos puros obtenidos de Urechites andrieuxii (Sin. Pentalinon andrieuxii), Colubrina greggii, Dorstenia contrajerva y Tridax procumbens. Un compuesto identificado como NCG-5C y la fracción DCG-3A (de baja polaridad) aislados de C. greggii y la fracción de baja polaridad TPZ-24 aislada de T. procumbes fueron los más activos contra L. aethiopica; los cuales mostraron una DL50 de 62.4, 7.2 y 18.5 µg/mL contra promastigotes, respectivamente y la DL50 contra amastigotes fue de 94.2, 27.1, 95.2 µg/mL; en este trabajo también evaluaron los mismos extractos y compuestos puros contra L. major y L. tropica pero resultaron poco activos.2 El extracto metanólico de T. procumbens y el compuesto 3(S)-16,17-didehidrofalcarinol u oxilipina (31) inhibieron el crecimiento de promastigotes de L. mexicana mostrando un CI50 = 3 y 0.478 µg/mL, respectivamente. Además la oxilipina pura (31) resultó activa contra amastigotes (estadio intracelular) de L. mexicana.31,32 Recientemente, Gamboa-León y col. han descrito que el extracto MeOH de la planta total de T. procumbens mezclado con el extracto acuoso liofilizado de Allium sativa (bulbos) reduce significativamente las lesiones cutáneas provocada con promastigotes de L. mexicana (Hd18-MHET/MX/97/Hd18) en ratones hembras CD-1, al ser tratados por dos semanas con la mezcla de extractos. Los extractos por separados también redujeron la formación de lesiones en menor porcentaje que la mezcla. 33

Por otro lado, este grupo describe que el extracto MeOH de las hojas y raíces de Urechites andrieuxii (sin. Pentalinon andrieuxii) colectado en Champoton, México (colecta I) fue el más activo contra promastigotes de L. braziliensis, L. amazonensis y L. donovanii,30 también resultaron activos contra promastigotes de L. mexicana.34,35
La fracción hexánica obtenida del extracto MeOH de las raíces de P. andrieuxxii fue evaluada en el modelo in vivo de leishmaniasis cutánea, en ratones machos C57BL/6 infectados con promastigotes de L. mexicana. La aplicación tópica de 10 µg de la fracción hexánica por 6 semanas redujo significativamente el tamaño de las lesiones respecto al vehículo.
También esta fracción inhibió el crecimiento de promastigotes L. mexicana in vitro, mostrando una CI50= 43.04 µg/mL, en macrófagos infectados con amastigotes, la CI50= 4.1 µg/mL y en células dendríticas infectadas con amastigotes de L. mexicana la CI50 fue de 11.06 µg/mL.36 De la fracción hexánica activa, obtenida por proceso de partición a partir del extracto MeOH (activo) de las raíces de U. andrieuxii (sin. P. andrieuxxii) aislaron colestra-4,20,24-trien-3-ona o pentalinosterol (32), 24- metilcolesta-4-24(28)-dien-3-ona (33), colest-4-en-3-ona (34), 6,7-dihidroneridienona (35) y neridienona (36), los cuales inhibieron el crecimiento de promastigotes de L. mexicana, mostrando una CI50 <30 µg/mL; estos compuestos (32-36) junto con colest-5,20,24-trien-3β-ol (37) resultaron más activos contra amastigotes de L. mexicana (CI50 < 14.5 µg/mL), estas evaluaciones fueron realizadas in vitro.37 Del extracto EtOH de las hojas de P. andrieuxxii aislaron el ácido betulínico, el cual resulto inactivo contra L. amazonensis, L. braziliensis, mostrando un CI50 >200 µM.38
]]>





El extracto hexánico a 10 µg/mL de las raíces de P. andrieuxii fue el más activo contra promastigotes de L. mexicana, el efecto observado fue similar al glucantime (control positivo); los parásitos fueron completamente destruidos a las 100 h de tratamiento. Los extracto de Hex:AcOEt, AcOEt y EtOH también resultaron activos, ya que provocaron el 75% de mortalidad a 10 µg/mL.39
La flavona 6 (38) y la isocordoina (39, chalcona) aisladas de Lonchocarpus sp. fueron activos contra L. braziliensis, L. donovani y L. amazonensis, presentado valores de CI50 <40 µg/mL.40 De las raíces de L. xuul aislaron dos chalconas, la isocordoina (39) y 2',4'-dihidroxy-3'-(γ,γ-dimetilalil)-dihidrochalcona (40) y fueron probadas contra promatigotes de L. mexicana. Estos compuestos presentaron una CI50 = 7.7 y 66.5 µM, respectivamente, en este trabajo también evaluaron la actividad de algunos derivados semisintéticos, los cuales resultaron más activos que los compuestos naturales, por ejemplo el derivado acetilado, 2',4'-diacetoxi-3'-(3-metilbut-2-enil)-chalcona (41) presentó una CI50 = 3.10 µM.41




Conclusiones
A la fecha son escasas las especies medicinales de México que han sido evaluadas para determinar su potencial leishmanicida; de las investigaciones realizadas sólo tres especies medicinales (Tridax procumbens, Lonchocarpus xuul y Pentalinon andrieuxii) han mostrado una significativa actividad in vivo contra L. mexicana y se consideran candidatos potenciales. De estas especies activas se han aislado ocho compuestos activos [oxilipina, isocordoina, 2',4'-dihidroxy-3'-(γ,γ-dimetilalil)-dihidrochalcona, colestra-4,20, 24-trien-3-ona o pentalinosterol, 24-metilcolesta-4-24(28)-dien-3-ona, colest-4-en-3-ona, 6,7-dihidroneridienona, neridienona y colest-5,20,24-trien-3 β-ol], los cuales mostraron una CI50 >30 µg/mL contra L. mexicana; sin embargo, se desconoce el potencial real de los mismos ya que sólo se tiene la evaluación in vitro contra promastigotes y/o amastigotes de L. mexicana. Además se ha descrito que algunos extractos orgánicos han resultado activos contra otras especies de Leishmania (L. braziliensis, L. donovani y L. amazonensis), pero no se reportan los compuestos responsables de la actividad. Dado el problema que representa las infecciones provocadas por especies de Leishmania, aunado al problema de la fármaco resistencia y a los efectos secundarios que provocan los fármacos actuales, es necesario redoblar esfuerzos para continuar investigando otras especies medicinales y poder encontrar compuesto activos que coadyuven al tratamiento de la enfermedad o bien encontrar moléculas prototipo para el desarrollo de fármacos con mecanismo de acción diferentes a los existentes.
Referencias
1. Domínguez-Carmona DB, Escalante-Erosa F, García-Sosa K, Ruiz-Pinell G, Gutierrez-Yapu D, Chan-Bacab MJ, Giménez-Turba A, Peña-Rodríguez LM. Antiprotozoal activity of betulinic acid derivatives. Phytomedicine. 2010; 17(5):379-382. doi: 10.1016/j.phymed.2009.08.002. [ Links ]
2. Getti G, Durgadoss O, Domínguez-Carmona D, Martin-Quintal Z, Peraza-Sanchez S, Peña-Rodriguez LM, Humber D. Leishmanicidal activity of Yucatecan medicinal plants on Leishmania species responsible for cutaneous leishmaniasis. J Parasitol. 2009; 95(2):456–460. doi:10.1645/GE-1675.1. [ Links ]
]]>3. Arjona-Jiménez G, Villegas N, López-Céspedes A, Marín C, Longoni SS, Bolio-González ME, Rodríguez-Vivas RI, Sauri-Arceo CH, Sánchez-Moreno Hyg. Prevalence of antibodies against three species of Leishmanial (L. mexicana, L. braziliensis, L. infantum) and possible associated factors in dogs from Mérida,Yucatán, Mexico. Trans R Soc Trop Med. 2012; 106(4):252-258. [ Links ]
4. Bero J, Hannaert V, Chataigné G, Hérent MF, Quetin-Leclercq J. In vitro antitrypanosomal and antileishmanial activity of plants used in Benin in traditional medicine and bio-guided fractionation of the most active extract. J Ethnopharmacol. 2011; 137(2):998-1002. [ Links ]
5. Varela-M RE, Villa-Pulgarin JA, Yepes E, Müller I, Modolell M, Muñoz DL, Robledo SM, Muskus CE, López-Abán J, Muro A, Vélez ID, Mollinedo F. In vitro and in vivo efficacy of ether lipid edelfosine against Leishmania spp. and SbV-resistant parasites. PLoS Negl Trop Dis. 2012; 6(4):e1612. [ Links ]
6. Wink M. Medicinal plants: a source of antiparasitic secondary metabolites. Molecules. 2012; 17(11):12771-12791. doi:10.3390/molecules171112771. [ Links ]
7. Basselin M, Denise H, Coombs GH, Barrett MP. Resistance to pentamidine in Leishmania mexicana involves exclusion of the drug from the mitochondrion. Antimicrob Agents Chemother. 2002; 46(12):3731-3738. [ Links ]
]]>8. Chow LM, Volkman SK. Plasmodium and Leishmania: the role of MDR genes in mediating drug resistance. Exp Parasitol. 1998; 90(1):135-141. [ Links ]
9. Carneiro SM, Carvalho FA, Santana LC, Sousa AP, Neto JM, Chaves MH. The cytotoxic and antileishmanial activity of extracts and fractions of leaves and fruits of Azadirachta indica (A Juss). Biol Res. 2012; 45(2):111-116. doi: 10.1590/S0716-97602012000200002. [ Links ]
10. Newman DJ, Cragg GM. Natural products as sources of new drugs over the last 25 years. J Nat Prod. 2007; 70(3):461-177. [ Links ]
11. Balunas MJ, Kinghorn AD. Drug discovery from medicinal plants. Life Sci. 2005; 78(5):431-441. [ Links ]
12. Chin YW, Balunas MJ, Chai HB, Kinghorn AD. Drug discovery from natural sources. AAPSJ. 2006; 8(2):E239-253. [ Links ]
]]>13. Galdo A. A propósito de un caso de Botón de Oriente en primera infancia. Med Rev Mex. 1934; 14(225):388-396. [ Links ]
14. Chan-Bacab MJ, Peña-Rodriguez LM. Plant natural products with leishmanicidal activity. Nat Prod Rep. 2001; 18(6):674-688. [ Links ]
15. Torres-Santos EC, Lopes D, Oliveira RR, Carauta JP, Falcao CA, Kaplan MA, Rossi-Bergmann B. Antileishmanial activiy of isolater triterpenoids form Pourouma guianensis. Phytomedicine. 2004; 11(2-3):114-120. [ Links ]
16. Mishra BB, Kale RR, Singh RK, Tiwari VK. Alkaloids: Future prospective to combat leishmanisis. Fitoterapia. 2009; 80(2):81-90. doi: 10.1016/j.fitote.2008.10.009. [ Links ]
17. Polonio T, Efferth T. Leishmaniasis drug resistance and natural products (review). Int J Mol Med. 2008; 22(3):277-286. doi:10.3092/ijmm_00000020. [ Links ]
]]>18. Bhuwan BM, Rakesh KS, Srivastava A, Tripathi VJ, Vinod K. Fighting against Leishmaniasis:Search of Alkaloids as future true potential anti-leishmanial agentes. Mini-Rev Med Chem. 2009; 9(1):107-123. [ Links ]
19. Fournet A, Barrios AA, Muñoz V, Hocquemiller R, Roblot F, Cavé A. Antileishmanial activity of a tetralone isolated from Ampelocera edentula, a Bolivian plants used as a treatment for cutaneous leishmaniasis. Planta Med. 1993; 60(1):8-12. [ Links ]
20. Eltayeb A, Ibrahim K. Potential antileishmnial effect of three medicinal plants. Indian J Pharm Sci. 2012; 74(2):171-174. doi:10.4103/0250-474X.103856. [ Links ]
21. Torres-Santos EC, Rodrigues JMJr, Moreira DL, Kaplan MA, Rossi-Bergmann B. Improvement of in vitro and in vivo antileishmanial activities of 29,69-dihidroxy-49-methoxychalcone by entrapment in poly(D,L-lactide) nonoparticles. Antimicrob Agents Chemother. 1999; 43(7):1776-1778. [ Links ]
22. Medda S, Mukhopadhyay S, Basu MK. Evaluation of the in vivo activity and toxicity of amarogentin, an antileishmanial agent, in both liposomal and niosomal forms. J Antimicrob Chemother. 1999; 44(6):791-794. [ Links ]
]]>23. Fournet A, Barrios AA, Muñoz V, Hocquemiller R, Cavé A. Effect of natural naphtoquinones in BALB/c mice infected with Leishmania amazonensis and L. venezuelensis. Trop Med Parasitol. 1992a; 43(4):219-222. [ Links ]
24. Fournet A, Angelo A, Muñoz V, Roblot F, Hocquemiller R, Cavé A. Biological and chemical studies of Pera benensis, a Bolivian plant used in folk medicine as a treatment of cutaneous leishmaniasis. J Ethnopharmacol. 1992b; 37(2):159-164. [ Links ]
25. Hazra B, Saha AK, Ray R, Roy DK, Sur P, Banerjee A. Antiprotozoal activity of diospyrin towards Leishmania donovani promastigotes in vitro. Trans R Soc Trop Med Hyg. 1987; 81(5):738-741. [ Links ]
26. Ray S, Hazra B, Mittra B, Das A, Majumder HK. Diospyrin, a bisnaphtoquinone a novel inhibitor of type I DNA topoisomerase of Leishmania donovani. Mol Pharmacol. 1998; 54(6):994-999. [ Links ]
27. Lall N, Meyer JJ. Inhibition of drug-sensitive and drug-resistant strains of Mycobacterium tuberculosis by diospyrin, isolated from Euclea natalensis. J Ethnopharmacol. 2001; 78(2-3):213-216. [ Links ]
]]>28. Uribarren BT. Leishmaniasis. 2013. http://www.facmed.unam.mx/deptos/microbiologia/parasitologia/leishmaniosis.html Acceso 3 Sep 201. [ Links ]
29. Chan-Bacab MJ, Balanza E, Deharo E, Muñoz V, García RD, Peña-Rodríguez LM. Variation of leishmanial activity in four population of Urechites andrieuxii. J Ethnopharmacol. 2003; 86(2-3):243-247. [ Links ]
30. Peraza-Sánchez SR, Cen-Pacheco F, Noh-Chimal A, May-Pat F, Simá-Polanco P, Dumonteil E, García-Miss MR, Mut-Martín M. Leishmanicidal evaluation of extracts from native plants of the Yucatan peninsula. Fitoterapia. 2007; 78(4):315-318. [ Links ]
31. Martín-Quintal Z, Moo-Puc R, González-Salazar F, Chan-Bacab MJ, Torres-Tapia LW, Peraza-Sanchéz SR. In vitro activity of Tridax procumbens against promastigotes of Leishmania mexicana. J Ethnopharmacol. 2009; 122(3):463-467. doi: 10.1016/j.jep.2009.01.037. [ Links ]
32. Martín-Quintal Z, García Miss dR, Mut-Martin M, Matus-Moo A, Torres-Tapia LW, Peraza-Sánchez SR. The lieshmanicidal effect of (3S)-16,17-didehidrofalcarinol, an oxylipin isolated from Tridax procumbes, is independent of NO production. Phytohter Res. 2010; 24(7):1004-1008. doi: 10.1002/ptr.3052. [ Links ]
]]>33. Gamboa-Leon R, Vera-Ku M, Peraza-Sanchez SR, Ku-Chulim C, Horta-Baas A, Rosado-Vallado M. Antileishmanial activity of a mixture of Tridax procumbens and Allium sativum in mice. Parasite. 2014; 21:15. doi: 10.1051/parasite/2014016. [ Links ]
34. Viscencio GS, Tamay PM, Issac AP, Lezama, CM. Toxicidad in vitro de extractos de Urechites andrieuxii Muell-Arg, en contra de L. mexicana. Memorias de la III Reunión de Investigación Química en el Sureste de México, Mérida, Yucatán. 1995; 93. [ Links ]
35. Adebayo OL, Suleman D, Samson AA. Natural products in Antileishmanial drug discovery: a review. JASR. 2013; 3(2):157-173. [ Links ]
36. Lezama-Dávila CM, Pan L, Isaac-Márquez AP, Terrazas C, Oghumu S, Isaac-Márquez R, Pech-Dzib M, Barbi J, Calomeni E, Parinandi N, Kinghorn AD, Satoskar AR. Pentalinon andrieuxii Root Extract is Effective in the Topical Treatment of Cutaneous Leishmaniasis Caused by Leishmania mexicana. Phytother Res. 2014; 28(6):909-16. doi: 10.1002/ptr.5079. [ Links ]
37. Pan L, Lezama-Davila CM, Isaac-Marquez AP, Calomeni EP, Fuchs JR, Satoskar AR, Kinghorn AD. Sterols with antileishmanial activity isolated from the roots of Pentalinon andrieuxii. Phytochemistry. 2012; 82:128-35. doi: 10.1016/j.phytochem.2012.06.012. [ Links ]
]]>38. Domínguez-Carmona DB, Escalante-Erosa F, García-Sosa K, Ruiz-Pinell G, Gutierrez-Yapu D, Chan-Bacab MJ, Giménez-Turba A, Peña-Rodríguez LM. Antiprotozoal activity of betulinic acid derivatives. Phytomedicine. 2010; 17(5):379-382. doi: 10.1016/j.phymed.2009.08.002. [ Links ]
39. Lezama-Dávila CM, Isaac-Márquez AP, Zamora-Crescencio P, Uc-Encalada Mdel R, Justiniano-Apolinar SY, del Angel-Robles L, Satoskar A, Hernández-Rivero L. Leishmanicidal activity of Pentalinon andrieuxii. Fitoterapia 2007; 78(3):255-257. [ Links ]
40. Borges-Argáez R, Balnbury L, Flowers A, Giménez-Turba A, Ruiz G, Waterman PG, Peña-Rodríguez LM. Cytotoxic and antiprotozoal activity of flavonoids from Lonchocarpus spp. Phytomedicine. 2007; 14(7-8):530-533. [ Links ]
41. Borges-Argáez R, Vela-Catzín T, Yam-Puc A, Chan-Bacab MJ, Moo-Puc RE, Cáceres-Farfán M. Antiprotozoal and cytotoxic studies on some isocordoin derivatives. Planta Med. 2009; 75(12):1336-1338. doi: 10.1055/s-0029-1185670. [ Links ]
]]>