Evaluación del metabolismo óseo pre y postrasplante renal en niños y adolescentes
Pre and post-renal transplant bone mineral metabolism in children and adolescents
Daniel Díaz-Barriga,1* Ana María Hernández-Sánchez,2 Yazmín Rico-Argüello,1 Lourdes Matilde Ortiz-Vázquez,2 Rubén Aldana-Vergara,2 Luis Velásquez-Jones,1
Saúl Valverde-Rosas,1 Francisco Velásquez-Forero,2 Mara Medeiros1,2
1 Departamento de Nefrología, ]]>
2 Laboratorio de Investigación en Nefrología y Metabolismo Mineral Óseo Hospital Infantil de México Federico Gómez
* Becario PUIS-UNAM
México D.F., México
Autor de correspondencia: Dra. Mara Medeiros
Correo electrónico: medeiro.mara@gmail.com
Fecha de recepción: 05-02-13
Fecha de aceptación: 05-03-13
Resumen
Introducción. La enfermedad renal crónica presenta efectos sobre el tejido óseo que se conocen como enfermedad renal crónica-trastorno mineral óseo. Los pacientes con trasplante renal también presentan trastornos óseos, aun con la función normal del injerto. Se han atribuido a los medicamentos inmunosupresores (esteroides e inhibidores de calcineurina). Por lo anterior, es necesario conocer la prevalencia y evolución de trastorno mineral óseo pre y postrasplante renal en los niños. El objetivo de este trabajo fue describir la prevalencia y el tipo de alteraciones de metabolismo mineral pretrasplante y su evolución postrasplante.
Métodos. El estudio fue aprobado por el Comité de Ética e Investigación del hospital. Se obtuvo el consentimiento informado de todos los participantes. Participaron pacientes con enfermedad renal crónica menores de 18 años, estudiados para recibir un primer trasplante renal. Al momento del trasplante, así como a los 6 y a los 12 meses postrasplante, se realizó la antropometría completa y se colectó sangre para determinar creatinina, niveles en valle de tacrolimus, calcio, fósforo, magnesio y fosfatasa alcalina. Se midió la hormona paratiroidea intacta (PTH) al momento del trasplante.
Resultados. Se incluyeron 31 pacientes con edad promedio de 14.6 ± 3.2 años y predominio del sexo femenino (52%). Todos recibieron inducción con basiliximab y triple esquema con prednisona, micofenolato de mofetilo y tacrolimus. En cuanto a los valores de PTH, 51.6% tuvieron cifras pretrasplante <150 pg/ml (sugestivo de lesiones óseas de bajo remodelamiento); 38.7%, >300 pg/ml (sugestivo de alto remodelamiento); y tan sólo 9.6% tuvieron PTH en los valores recomendados. Al comparar los valores pre y postrasplante, la creatinina sérica disminuyó en forma significativa, no hubo diferencia en el calcio sérico y fosfatasa alcalina, pero se encontró una disminución significativa en fósforo y magnesio. Doce pacientes (38.7%) presentaron hipofosfatemia postrasplante. Diez pacientes (32%) cursaron con hipomagnesemia. Todos incrementaron el valor z de peso en forma significativa. La función renal tuvo correlación positiva con el calcio sérico y negativa con el fósforo y el magnesio (p <0.05). Los niveles de tacrolimus tuvieron una correlación negativa con el magnesio sérico (r =-0.431, p <0.0001).
Conclusiones. La velocidad de filtración glomerular al momento del trasplante tuvo una correlación negativa con el fósforo sérico basal y la concentración de tacrolimus, con el magnesio sérico. El crecimiento fue mejor en los pacientes que no presentaron hipofosfatemia durante el postrasplante. Es necesario vigilar y tratar oportunamente las alteraciones minerales en el postrasplante renal.
Palabras clave: trasplante renal, metabolismo mineral óseo, osteodistrofia, enfermedad renal crónica.
Abstract
Background. Information regarding chronic kidney disease-mineral bone disorder (CKD-MBD) in children who undergo renal transplant is scarce. Despite successful renal transplantation, bone disorders have been described and attributed to immunosuppressive drugs (steroids and calcineurin inhibitors). Therefore, it is important to determine the prevalence and outcome of bone mineral disorders pre- and post-renal transplant. The aim was to describe the prevalence and type of bone mineral disorders in children pre-renal transplant and outcomes.
]]> Methods. The Institutional Review Board and Ethics Committee approved the study. Signed consent/assent was obtained from all participants. Patients <18 years of age and under investigation for a first renal transplant were invited to participate. At transplant and 6 and 12 months after transplantation, anthropometric data were collected and blood samples were collected for serum creatinine, slope levels of tacrolimus, serum calcium, phosphorus, magnesium and alkaline phosphatase. Intact parathyroid hormone (PTH) was measured before transplant.Results. Thirty-one patients were included with a mean age of 14.6 ± 3.2 years. Females represented 52%. All received induction with basiliximab and triple maintenance therapy with prednisone, mycophenolate mofetil and tacrolimus. Pre-transplant PTH values were <150 pg/ml in 51.6%, suggestive of low turnover bone lesions, 38.7% had PTH >300 pg/ml, suggestive of high turnover bone lesions and only 9.6% had PTH between 150 and 300 pg/ml. When pre- and post-transplant studied parameters were compared, serum creatinine was statistically lower during follow-up. No difference was found in serum calcium and alkaline phosphatase, but magnesium and phosphorus values were significantly lower after transplant. Twelve patients (38.7%) had post-transplant hypophosphatemia and required supplementation. Ten patients (32%) had hypomagnesemia, seven of them with concomitant hypophosphatemia. Z-score for weight increased significantly after renal transplant; nevertheless, only patients with no hypophosphatemia during follow-up improved their Z-score for height. Glomerular filtration rate had a positive correlation with serum calcium and a negative correlation with phosphorus and magnesium (p <0.05). Tacrolimus slope levels had a significantly negative correlation with serum magnesium (r =-0.431, p <0.0001).
Conclusions. Glomerular filtration rate had a negative correlation with serum phosphorus at transplant. Tacrolimus slope levels had a negative correlation with magnesium serum values. Patients with no hypophosphatemia during the first year had better growth than those with hypophosphatemia. It is important to monitor and opportunely treat bone mineral disorders in children who undergo transplantation.
Key words: renal transplant, bone mineral metabolism, osteodystrophy, chronic kidney disease.
Introducción
La enfermedad renal crónica tiene efectos sobre el hueso que se conocen como osteodistrofia renal (ODR). La enfermedad ósea presenta un amplio espectro ya que aparece desde etapas iniciales de la enfermedad renal.1 La gravedad de la afección ósea tiende a asociarse con la gravedad y duración de la enfermedad renal. En los niños, si la osteodistrofia no se trata en forma apropiada y oportuna, se presentan deformidades óseas y trastornos en el patrón de crecimiento.2 A medida que disminuye la función renal se deteriora la homeostasis mineral, con cambios en los niveles sanguíneos de calcio y fósforo, así como de hormonas como la paratohormona (PTH), la 25-hidroxivitamina D (25OHD), la 1,25-dihidroxivitamina D (125OH2D3) y otros metabolitos de la vitamina D, el factor de crecimiento de fibroblastos (FGF-23) y la hormona de crecimiento.3
La guía internacional KDIGO recomienda el uso del término ''enfermedad renal crónica-trastorno mineral óseo'' para describir el síndrome clínico amplio que comprende las alteraciones minerales (metabolismo de calcio, fósforo o PTH), óseas (alteraciones en el recambio óseo, mineralización, crecimiento lineal o fuerza) y calcificaciones cardiovasculares que se desarrollan como complicaciones de la enfermedad renal crónica. También recomienda que el término ''osteodistrofia renal'' se limite a la descripción de la patología ósea asociada con la enfermedad renal. La evaluación y el diagnóstico definitivo de ODR requieren de una biopsia ósea, utilizando un sistema de clasificación que se basa en parámetros de alteración en la modelación y la remodelación óseas.4
Después de un trasplante renal (TR) exitoso los trastornos del metabolismo de calcio se corrigen parcial o totalmente; sin embargo, puede persistir el hiperparatiroidismo secundario. Además, puede presentarse enfermedad ósea inducida por disfunción tubular o relacionada con los medicamentos inmunosupresores.5 Estudios en adultos han mostrado que los pacientes con TR tienen niveles de PTH, calcio y osteocalcina más elevados que los sujetos controles, así como hipofosfatemia, consistente con la persistencia de hiperparatiroidismo secundario. Esto se presenta aun en aquellos pacientes con velocidad de filtración glomerular (VFG) normal, lo cual indica que otros factores, además de la función renal, participan en la persistencia del hiperparatiroidismo. Estos podrían ser el tiempo y gravedad de la uremia, el tamaño de las paratiroides antes del trasplante, una pobre involución de las paratiroides hipertróficas debida a una alteración en la depuración del exceso de células por apoptosis, el tipo de crecimiento paratiroideo, ya que el tipo nodular se asocia con una distribución menos uniforme en los receptores de calcitriol que el tipo hiperplasia difusa, ocasionando una menor inhibición con calcitriol.6 Algunos pacientes tienen un crecimiento monoclonal del tejido paratiroideo, por lo que puede no darse la involución de las glándulas después de que se corrigieron los factores que condicionaron el hiperparatiroidismo secundario.7 Los medicamentos inmunosupresores empleados para prevenir el rechazo pueden tener efectos sobre el hueso. En el caso particular de los glucocorticoides, se sabe que condicionan la pérdida de hueso, principalmente de tipo trabecular. A dosis modestas, consideradas en el rango fisiológico, incrementan el riesgo de fracturas osteoporóticas.8 Dentro de los efectos directos de los glucocorticoides sobre el hueso se encuentran el incremento en la osteoclastogénesis, cambios en la duración del osteoclasto, la diferenciación de célula hematopoyética a osteoclasto, el acortamiento de la vida de los osteoblastos maduros y osteocitos, la disminución en la función osteoblástica y la transcripción de IGF 1. También tienen efectos indirectos que afectan el metabolismo mineral como la resistencia al calcitriol, la disminución en la absorción intestinal de calcio, la hipercalciuria y el hipogonadismo.
El efecto de los inhibidores de calcineurina (ciclosporina y tacrolimus) ha sido ampliamente estudiado en modelos animales, donde se observa una pérdida significativa de la masa trabecular y cortical ósea después de semanas de tratamiento. Este efecto es reversible y dependiente de la dosis. En la histomorfometría se encuentra alto remodelamiento.9 Tanto tacrolimus como ciclosporina inducen la pérdida renal de calcio y magnesio e inhiben la activación del receptor de vitamina D.10 Existen pocos estudios en adultos y en niños que evalúen el metabolismo mineral pre y post TR. En nuestro país se ha reportado el predominio de adinamia ósea en 16 pacientes adultos con función renal normal biopsiados 84 meses postrasplante.11
]]> Koch-Nogueira y colaboradores reportaron que 41 pacientes con trasplante prediálisis tuvieron niveles de PTH menores que los niños con diálisis, tanto pretrasplante como a los tres meses post-TR, todos con función normal del injerto. Aquéllos con hiperparatiroidismo secundario más grave tuvieron una menor involución de las paratiroides post-TR.12Sánchez y colaboradores realizaron una biopsia ósea metabólica en 47 niños a los 3.2 ± 1.7 años post-TR. El 23% presentó hiperparatiroidismo; 66%, hueso normal; y 11%, lesiones adinámicas. Los niveles séricos de PTH no predijeron la lesión ósea.13
El objetivo del presente estudio fue describir la prevalencia y el tipo de alteraciones de metabolismo mineral pretrasplante y su evolución postrasplante en niños.
Métodos
Se realizó un estudio descriptivo, prospectivo, aprobado por el Comité de Ética e Investigación del hospital (protocolo HIM 2010/006). Se obtuvo el consentimiento informado de todos los participantes. Se invitaron a participar pacientes con enfermedad renal crónica menores de 18 años que estuvieran siendo evaluados para recibir un primer trasplante renal.
Al momento del trasplante, así como a los 6 y a los 12 meses postrasplante, se realizó la antropometría (peso, talla) y se colectó sangre para determinar niveles de creatinina, calcio, fósforo, magnesio y fosfatasa alcalina. Se determinaron los niveles de PTH intacta al momento del trasplante por inmunoquimioluminiscencia. Los niveles en valle de tacrolimus se midieron por inmunoensayo de quimioluminiscencia (ARCHITECT System, Abbott, Abbott Park IL).
Se consideró hipofosfatemia e hipocalcemia cuando las cifras de fósforo y calcio sérico se encontraron por debajo de los valores recomendados para la edad (según las guías KDOQI)14 e hipomagnesemia cuando las cifras de magnesio sérico fueron menores de 1.5 mg/dl.15
Función renal
La función renal pretrasplante y postrasplante renal se valoró por estimación de la velocidad de filtración glomerular (eVFG) de acuerdo con la fórmula de Schwartz:
eVFG (ml/min/1.73 m2)= kL/ Scr (mg/dl),
]]> donde L: talla en centímetros, Scr: creatinina sérica, k: valor de la constante (0.55 para niños y niñas adolescentes o 0.7 para varones adolescentes).16-18 Se eliminaron los pacientes que perdieron el injerto renal antes de 6 meses.Análisis estadístico
Se realizó estadística descriptiva. Los datos se expresaron como promedio + desviación estándar para variables con distribución normal, y medianas con rangos para variables con distribución libre. Los cambios bioquímicos pre y postrasplante se analizaron con ANOVA de muestras repetidas. También se analizaron los valores pre y post-TR con t de Student, o bien con la prueba de rangos de Wilcoxon según la distribución de la variable. Se hizo un análisis de la correlación entre los niveles séricos de tacrolimus, la velocidad de filtración glomerular y las variables bioquímicas estudiadas. Se consideró una p <0.05 como estadísticamente significativa. Se utilizó el programa Graph Pad Prism Versión 5.0 para Mac Os X.
Resultados
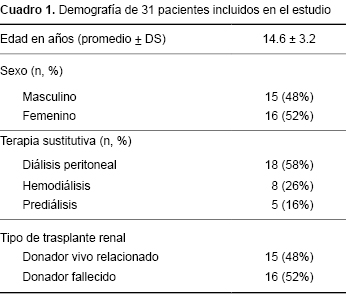
Se incluyeron 31 pacientes. La edad promedio fue de 14.5 ± 3.5 años. Predominó el sexo femenino (52%). De los 31 pacientes, 18 tenían diálisis peritoneal (58%); ocho, hemodiálisis (25%); y cinco pacientes recibieron trasplante prediálisis (16%) (Cuadro 1). Al momento del trasplante todos los pacientes recibían terapia sustitutiva con multivitaminas: 26/31 recibían eritropoyetina, 30/31 recibían carbonato de calcio como quelante de fosfato y 29/31 tratamiento con calcitriol. Este tratamiento se suspendió al día siguiente del trasplante renal. Todos recibieron inducción con basiliximab y triple esquema con prednisona, micofenolato de mofetilo y tacrolimus. Una paciente cambió a ciclosporina antes de tres meses debido a que presentó diabetes mellitus postrasplante.

]]>
Las variables bioquímicas estudiadas al momento del trasplante renal, así como a los 6 y 12 meses de seguimiento, se muestran en el Cuadro 2. Como se esperaba, los niveles de creatinina sérica y la eVFG mejoraron en forma significativa en todos los pacientes.
El calcio sérico incrementó de 8.86 ± 1.4 mg/dl al trasplante a 9.46 ± 0.5 mg/dl a los 6 meses post-TR y a 9.47 ± 0.6 mg/dl a los 12 meses post-TR (p =0.01). En contraste, el fósforo y el magnesio disminuyeron en forma significativa.
Al momento del trasplante renal, 12 pacientes presentaban hipocalcemia, con calcio sérico total menor de 8.8 mg/dl (en promedio 7.5 ± 0.9 mg/dl), y tres pacientes presentaban hipercalcemia, con calcio sérico superior a 10.3 mg/dl. En el seguimiento, tres pacientes presentaron hipocalcemia no tan acentuada (8.5 ± 0.2 mg/dl). La velocidad de filtración glomerular tuvo una correlación positiva con el calcio sérico (Figura 1A) y negativa con el fósforo (Figura 1 B) y magnesio séricos (p < 0.05, Figura 1C).
Se encontró una correlación negativa entre los niveles de tacrolimus y magnesio sérico (Figura 2A), así como entre calcio y fósforo sérico (Figura 2B) y positiva entre fósforo y magnesio sérico (Figura 2C) y fosfatasa alcalina versus magnesio sérico (Figura 2D). No se observó relación entre los niveles de tacrolimus y otras variables estudiadas, ni entre la dosis ponderal de prednisona a los 6 y 12 meses con las variables estudiadas (no se muestran resultados).
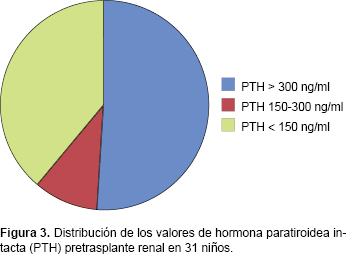
Antes del trasplante renal se observó que 16 pacientes presentaban valores de PTH < 150 ng/ml (51.6%), lo que sugería adinamia ósea; 12 pacientes (38.8%) presentaron un estado de hiperparatiroidismo con valores de PTH > 300 ng/ml; y sólo tres pacientes (9.6%) presentaron PTH en los límites recomendados (entre 150 y 300 ng/ml) (Figura 3).
]]>
Doce pacientes presentaron hipofosfatemia durante el seguimiento y 10 hipomagnesemia. Ameritaron tratamiento sustitutivo con sales de fosfato y magnesio.
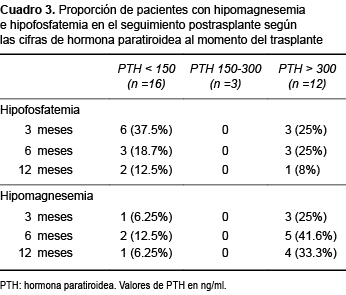
La proporción de pacientes con hipofosfatemia e hipomagnesia postrasplante se muestra en el Cuadro 3. Los pacientes con niveles recomendados de PTH no presentaron hipofosfatemia o hipomagnesemia durante el seguimiento. Los pacientes con niveles bajos de PTH tendieron a presentar hipofosfatemia, mientras que los que tenían niveles de PTH mayores de 300 pg/ml tendieron a presentar hipomagnesemia. Sin embargo, la diferencia no resultó estadísticamente significativa.
]]>
A los 12 meses postrasplante, tres pacientes persistían con hipofosfatemia y cinco con hipomagnesemia (Cuadro 3).
En cuanto al crecimiento, todos los pacientes mejoraron el valor Z de peso en forma significativa, aunque no se observó mejoría en la talla (Cuadro 4). Estos resultados no cambian si los pacientes se estratifican según las cifras de PTH basales.
Al clasificar a los pacientes entre los que presentaron hipofosfatemia postrasplante y los que no, los niños que no desarrollan hipofosfatemia sí presentaron un incremento significativo en el valor Z de talla. En ambos grupos se observó un incremento significativo en el peso (Cuadro 4).
Discusión
La enfermedad renal crónica ocasiona múltiples alteraciones en el metabolismo mineral, que son de especial importancia en la edad pediátrica. Cuando los niños están creciendo, deben ganar la masa ósea que tendrán en la edad adulta, por lo que se considera un periodo crítico para la salud ósea.
En el presente trabajo se observó que, en el momento del trasplante renal, únicamente 9.6% de los pacientes presentaron valores de PTH en el rango recomendado para la enfermedad renal terminal. La PTH comienza a aumentar desde que cae la velocidad de filtración glomerular por debajo de 60 ml/min/1.73m2SC.1 La hiperfosfatemia contribuye al hiperparatiroidismo secundario, ya que disminuye tanto la 1, 25 dihidroxivitamina D como los niveles de calcio ionizado, además de ser un estímulo directo para la secreción de PTH.19 Para el tratamiento del hiperparatiroidismo secundario se cuenta con los análogos de la vitamina D. El más ampliamente utilizado por su bajo costo es el calcitriol; sin embargo, el tratamiento con dosis excesiva de calcitriol y el uso de quelantes de fosfato con calcio favorecen el desarrollo de la enfermedad ósea de bajo remodelamiento, como al parecer sucedió con estos pacientes, ya que 51.6% presentó niveles de PTH por debajo de 150 pg/ml al momento del trasplante.4
La hipofosfatemia contribuye al desarrollo de hiperparatiroidismo secundario y se ha relacionado con la mortalidad. En niños, la hipofosfatemia lleva al raquitismo y al retraso en el crecimiento.14 En el presente trabajo es evidente que aquellos pacientes que desarrollaron hipofosfatemia en el postrasplante, no crecieron de forma adecuada después de 12 meses, sin importar la duración de la hipofosfatemia.
La velocidad de filtración glomerular tuvo una correlación positiva con la cifra de calcio sérico y negativa con el fósforo, como se ha descrito en otros estudios que han evaluado el metabolismo mineral óseo en pacientes con enfermedad renal.4 Es importante considerar que, a pesar de que los pacientes incluidos en el presente estudio tuvieron un trasplante renal exitoso, la eVFG a los 12 meses fue de 88 ± 19 ml/min/1.73m2SC, por lo que, en forma inexorable, irán perdiendo función renal a largo plazo, y continuarán siendo enfermos renales crónicos.
Encontramos también que existe una correlación negativa entre los niveles de tacrolimus y el magnesio sérico. Cabe mencionar que la dosis de tacrolimus se ajustó para alcanzar los valores en valle objetivo entre 5 y 10 ng/ml, según el tiempo postrasplante. La hipomagnesemia se ha relacionado con el uso de inhibidores de calcineurina.20 Tanto la ciclosporina como el tacrolimus aumentan la excreción urinaria de magnesio, al parecer por un efecto inhibitorio sobre el receptor de vitamina D y, de manera independiente, de los niveles de PTH.21 Este efecto es más pronunciado con la ciclosporina.10 La presencia de hipomagnesemia se ha asociado con el desarrollo de diabetes mellitus postrasplante.22
]]> Se considera que es necesario vigilar y tratar oportunamente las alteraciones minerales en el postrasplante renal. Algunos pacientes pueden requerir análogos de vitamina D diferentes del calcitriol, así como quelantes de fosfatos sin calcio para evitar lesiones de bajo remodelamiento. Otros pueden requerir tratamientos como bifosfonatos. Es deseable contar con la información que proporciona la biopsia ósea con doble marcaje de tetraciclina. Se requieren más estudios para evaluar las posibles intervenciones y sus efectos sobre el hueso, el crecimiento, la función del injerto y el riesgo cardiovascular a largo plazo.Agradecimientos
El proyecto agradece a la Dirección de Investigación y a las Becas PUIS-UNAM por el apoyo otorgado al alumno Daniel Díaz Barriga.
REFERENCIAS
1. Hruska KA, Choi ET, Memon I, Davis TK, Mathew S. Cardiovascular risk in chronic kidney disease (CKD): the CKD-mineral bone disorder (CKD-MBD). Pediatr Nephrol 2010;25:769-778. [ Links ]
2. Klaus G, Watson A, Edefonti A, Fischbach M, Rönnholm K, Schaefer F, et al. Prevention and treatment of renal osteodystrophy in children on chronic renal failure: European guidelines. Pediatr Nephrol 2006;21:151-159. [ Links ]
]]>3. Moe S, Drüeke T, Cunningham J, Goodman W, Martin K, Olgaard K, et al. Definition, evaluation, and classification of renal osteodystrophy: a position statement from Kidney Disease: Improving Global Outcomes (KDIGO). Kidney Int 2006;69:1945-1953. [ Links ]
4. Kidney Disease: Improving Global Outcomes (KDIGO) CKD-MBD Work Group. KDIGO clinical practice guideline for the diagnosis, evaluation, prevention, and treatment of Chronic Kidney Disease-Mineral and Bone Disorder (CKD-MBD). Kidney Int Suppl 2009;113:S1-S130. [ Links ]
5. Alshayeb HM, Josephson MA, Sprague SM. CKD-mineral and bone disorder management in kidney transplant recipients. Am J Kidney Dis 2013;61:310-325. [ Links ]
6. Fukuda N, Tanaka H, Tominaga Y, Fukagawa M, Kurokawa K, Seino Y. Decreased 1,25-dihydroxyvitamin D3 receptor density is associated with a more severe form of parathyroid hyperplasia in chronic uremic patients. J Clin Invest 1993;92:1436-1443. [ Links ]
7. Arnold A, Brown MF, Ureña P, Gaz RD, Sarfati E, Drüeke TB. Monoclonality of parathyroid tumors in chronic renal failure and in primary parathyroid hyperplasia. J Clin Invest 1995;95:2047-2053. [ Links ]
]]>8. van Staa TP, Cooper C, Leufkens HG, Bishop N. Children and the risk of fractures caused by oral corticosteroids. J Bone Miner Res 2003;18:913-918. [ Links ]
9. Epstein S, Dissanayake IR, Goodman GR, Bowman AR, Zhou H, Ma Y, et al. Effect of the interaction of parathyroid hormone and cyclosporine A on bone mineral metabolism in the rat. Calcif Tissue Int 2001;68:240-247. [ Links ]
10. Gouadon E, Lecerf F, German-Fattal M. Differential effects of cyclosporin A and tacrolimus on magnesium influx in Caco2 cells. J Pharm Pharm Sci 2012;15:389-398. [ Links ]
11. Velasquez-Forero F, Mondragón A, Herrero B, Peña JC. Adynamic bone lesion in renal transplant recipients with normal renal function. Nephrol Dial Transplant 1996;11(suppl 3):58-64. [ Links ]
12. Koch Nogueira PC, David L, Cochat P. Evolution of secondary hyperparathyroidism after renal transplantation. Pediatr Nephrol 2000;14:342-346. [ Links ]
]]>13. Sanchez CP, Kuizon BD, Goodman WG, Gales B, Ettenger RB, Boechat MI, et al. Growth hormone and the skeleton in pediatric renal allograft recipients. Pediatr Nephrol 2002;17:322-328. [ Links ]
14. National Kidney Foundation. KDOQI Clinical Practice Guidelines for Bone Metabolism and Disease in Children with Chronic Kidney Disease. Disponible en: https://www.kidney.org/professionals/kdoqi/guidelines_pedbone/index.htm [ Links ]
15. Kelepouris E, Agus ZS. Hypomagnesemia: renal magnesium handling. Semin Nephrol 1998;18:58-73. [ Links ]
16. Schwartz GJ, Brion LP, Spitzer A. The use of plasma creatinine concentration for estimating glomerular filtration rate in infants, children, and adolescents. Pediatr Clin North Am 1987;34:571-590. [ Links ]
17. Schwartz GJ, Furth SL. Glomerular filtration rate measurement and estimation in chronic kidney disease. Pediatr Nephrol 2007;22:1839-1848. [ Links ]
18. Schwartz GJ, Haycock GB, Spitzer A. Plasma creatinine and urea concentration in children: normal values for age and sex. J Pediatr 1976;88:828-830. [ Links ]
19. Torregrosa JV, Bover J, Cannata Andía J. Spanish Society of Nephrology recommendations for controlling mineral and bone disorder in chronic kidney disease patients (S.E.N.-M.B.D.). Introduction. Nefrologia 2011;31(suppl 1):1-2. [ Links ]
20. Dimke H, Monnens L, Hoenderop JG, Bindels RJ. Evaluation of hypomagnesemia: lessons from disorders of tubular transport. Am J Kidney Dis 2012. PMID 23201160. doi: 10.1053/j.ajkd.2012.07.033 [ Links ]
21. Lee CT, Ng HY, Lien YH, Lai LW, Wu MS, Lin CR, et al. Effects of cyclosporine, tacrolimus and rapamycin on renal calcium transport and vitamin D metabolism. Am J Nephrol 2011;34:87-94. [ Links ]
22. Van Laecke S, Van Biesen W, Verbeke F, De Bacquer D, Peeters P, Vanholder R. Posttransplantation hypomagnesemia and its relation with immunosuppression as predictors of new-onset diabetes after transplantation. Am J Transplant 2009;9:2140-2149. [ Links ]
]]>