Utilidad de la proteína C reactiva para el diagnóstico de infección bacteriana en el paciente pediátrico con cáncer, fiebre y neutropenia
Usefulness of C-reactive protein in the diagnosis of bacterial infection in the pediatric patient with cancer, fever and neutropenia
Martín Penagos-Paniagua,1 Miguel Ángel Villasís-Keever,2 María Guadalupe Miranda-Novales,1 Andrea Tapia-Marcial,3 Hugo Rivera-Márquez,4 Roberto Bernaldez-Ríos,5 Enrique Lopez Aguilar,4 Fortino Solórzano-Santos1
1 Servicio de Infectología, Centro Médico Nacional Siglo XXI Instituto Mexicano del Seguro Social México D.F., México.
]]> 2 Unidad de Investigación en Epidemiología Clínica, Centro Médico Nacional Siglo XXI Instituto Mexicano del Seguro Social México D.F., México.3 Laboratorio de Inmunología, Centro Médico Nacional Siglo XXI Instituto Mexicano del Seguro Social México D.F., México.
4 Servicio de Oncología, Centro Médico Nacional Siglo XXI Instituto Mexicano del Seguro Social México D.F., México.
5 Servicio de Hematología, Unidad Médica de Alta Especialidad, Hospital de Pediatría, Centro Médico Nacional Siglo XXI Instituto Mexicano del Seguro Social México D.F., México.
Autor de correspondencia:
Dr. Fortino Solórzano Santos
Correo electrónico: fortino.solorzano@imss.gob.mx
Fecha de recepción: 24-05-12 ]]> Fecha de aceptación: 05-09-12
RESUMEN
Introducción. El diagnóstico de infección bacteriana en el paciente con cáncer, fiebre y neutropenia se dificulta debido a una pobre respuesta inflamatoria. Se han realizado evaluaciones con reactantes de fase aguda, como la proteína C reactiva, con resultados variables. El objetivo de este trabajo fue calcular la sensibilidad, especificidad, valores predictivos positivos y negativos y razones de verosimilitud de la proteína C reactiva para el diagnóstico de infección bacteriana en pacientes con cáncer y neutropenia febril.
Métodos. Se realizó el estudio de la prueba diagnóstica. Se incluyeron pacientes pediátricos con cáncer, y neutropenia (<500 NA/mm3). La proteína C reactiva se cuantificó por nefelometría. Los episodios se clasificaron en cuatro grupos: grupo I, infección microbiológicamente documentada; grupo II, infección clínicamente documentada; grupo III, fiebre por otras causas; y grupo IV, pacientes con neutropenia sin fiebre. Se realizó el cálculo de sensibilidad, especificidad, valores predictivos positivos y negativos, curvas operantes del receptor y razones de verosimilitud. Para la comparación de variables cuantitativas se emplearon la U de Mann-Whitney y Kruskal-Wallis y para variables cualitativas, χ2.
Resultados. Se incluyeron 127 episodios que se distribuyeron en: 29, 47, 20 y 31 episodios para los grupos I, II, III y IV, respectivamente. Las medianas de la proteína C reactiva fueron 282 mg/L para el grupo I, 205 mg/L grupo II, 27.3 mg/L grupo III y 5.1 mg/L para el grupo IV (p < 0.001). Con la proteína C reactiva de 60 mg/L se obtuvo una sensibilidad de 94%, especificidad de 94%, valor predictivo positivo 96% y valor predictivo negativo 92%; razón de verosimilitud para un resultado positivo 15.6 y de 0.06 para resultado negativo.
Conclusiones. La proteína C reactiva es una prueba útil y económica para el diagnóstico de infección bacteriana en el paciente con cáncer, fiebre y neutropenia.
Palabras clave: proteína C reactiva, cáncer, neutropenia, infección bacteriana, fiebre.
ABSTRACT
]]> Background. Diagnosis of bacterial infection in the patient with cancer, fever and neutropenia is difficult due to the poor inflammatory response. Several evaluations of acute phase reactants such as C-reactive protein (C-RP) have been performed with diverse results. The aim of this study was to calculate the sensitivity, specificity, positive predictive value (PPV) and negative predictive value (NPV), and likelihood ratios (LR) for C-RP in the diagnosis of bacterial infection of patients with cancer, neutropenia and fever.Methods. We carried out a diagnostic test study. Pediatric patients with cancer and neutropenia (<500 NA/mm3) were selected. C-RP was determined by nephelometry. Episodes were classified into the following groups: group I: microbiologically documented infection; group II: clinically documented infection; group III: fever of unknown origin; group IV: patients with neutropenia without fever. Sensitivity, specificity, PPV, NPV, receiving operating curves (ROC) and LR were calculated. Mann-Whitney U test and Kruskal-Wallis test were used for comparison of quantitative variables. For qualitative variables, χ2 test was used.
Results. There were 127 episodes distributed as follows: 29, 47, 20 and 31 for groups I, II, III and IV, respectively. Median of C-RP values were 282 mg/L for group I, 205 mg/L group II, 27.3 mg/L group III and 5.1 mg/L group IV (p <0.001). With a C-RP value of 60 mg/L, we obtained a sensitivity of 94%, specificity 94%, PPV 6% and NPV 92%. LR for a positive test was 15.6 and LR for a negative test was 0.06.
Conclusions. C-RP is a useful and economically feasible test for diagnosis of bacterial infection in patients with cancer, neutropenia and fever.
Key words: C-reactive protein, cancer, neutropenia, bacterial infection, fever.
INTRODUCCIÓN
En los pacientes con cáncer la fiebre es un signo común. En 60 a 70% de los casos tiene origen infeccioso. Otras causas de fiebre son la actividad de la enfermedad, los efectos adversos de ciertos fármacos, la reacción transfusional o la crisis adrenal. Cuando la fiebre se presenta durante un periodo de neutropenia (neutrófilos absolutos <500/mm3), el riesgo de infección grave es mayor, por lo que se recomienda el uso de antimicrobianos empíricos de amplio espectro durante estos episodios.1 Los signos y síntomas de infección en estos pacientes son pocos, por lo que constituye un reto establecer oportunamente el diagnóstico correcto de la infección.24
Con la finalidad de precisar el diagnóstico se han utilizado pruebas no bacteriológicas, como la determinación de reactantes de fase aguda, entre los que se incluye la proteína C creativa (PCR). A nivel sérico, la PCR se eleva cuando hay daño tisular y en presencia de infecciones bacterianas. Los procesos neoplásicos, la quimioterapia, las transfusiones de derivados sanguíneos incrementan poco su concentración.5-8
El análisis cuantitativo de la PCR se ha considerado de ayuda por algunos autores desde el siglo pasado. En un estudio con pacientes inmunocompetentes e inmunocomprometidos, empleando un valor de corte de 20 mg/L, Peltola y Jaakkola obtuvieron una sensibilidad de 89% y especificidad de 77% para discriminar entre infección bacteriana y viral.9 Santolaya y colaboradores obtuvieron una sensibilidad de 100% y especificidad del 76.6% con un valor de PCR de 40 mg/L en 75 niños con cáncer.10 En otro estudio con pacientes adultos, con el mismo valor de corte, la sensibilidad fue de 100% aunque la especificidad fue muy baja (7%). Los valores de corte en estos estudios fueron seleccionados en forma arbitraria.11
]]> Por otro lado, hay estudios que consideran la prueba como de poca utilidad. Con un nivel de corte de 50 mg/L, Riikonen y colaboradores observaron una especificidad de 100%, con una sensibilidad del 24%.12 Katz y colaboradores, al evaluar niveles entre 20 y 100 mg/L, observaron una sensibilidad de 22 a 71% y especificidad entre 32 al 71%, lo que sugirió que las variaciones se realcionaron con el microorganismo aislado.13 Recientemente, algunos autores la han empleado para guiar el tratamiento antimicrobiano.14,15 Sin embargo, el número de pacientes incluidos en estos trabajos no permite generalizar su aplicación para todos los centros que atienden niños con cáncer.El objetivo de este estudio fue evaluar la utilidad de la cuantificación de la PCR en niños con cáncer, neutropenia y fiebre, mediante el cálculo de la sensibilidad, la especificidad, los valores predictivos negativo y positivo y las razones de verosimilitud. Además, obtener el mejor valor para diferenciar entre los pacientes con infección microbiológica o clínicamente documentada y los niños con fiebre de origen no infeccioso.
MÉTODOS
El estudio se realizó en el Hospital de Pediatría del Centro Médico Nacional Siglo XXI, Instituto Mexicano del Seguro Social, que es un centro de atención médica de tercer nivel. Se incluyeron niños con leucemia, linfoma o tumores sólidos que ingresaron con fiebre y neutropenia grave en un período de dos años. Para el grupo de comparación se incluyeron pacientes con neutropenia sin fiebre. Se excluyeron los pacientes que recibieron tratamiento antimicrobiano una semana previa al episodio de neutropenia y fiebre, los sometidos a procedimientos quirúrgicos cinco días previos al inicio de fiebre, pacientes con desnutrición de tercer grado, enfermedad o insuficiencia hepática. Se eliminaron los pacientes en quienes la toma de muestra para PCR no se realizó en el momento de la obtención de sangre para hemocultivos. Los hemocultivos se procesaron de acuerdo a las normas internacionales (American Society of Microbiology).16
La fiebre se definió como temperatura única de ≥38.3°C o temperatura axilar o bucal de 38°C por más de 4 horas. Se consideró neutropenia grave cuando la cifra de neutrófilos absolutos (NA) fue menor o igual a 500/mm3. A los pacientes con fiebre se les realizó historia clínica y examen físico completos. Se obtuvieron al menos dos hemocultivos periféricos y, en su caso, uno más a través del catéter venoso central; al mismo tiempo, se tomó 1.0 mL de sangre para la determinación de PCR. Después de la toma de cultivos, se inició el esquema antimicrobiano empírico con ceftazidima (150-200 mg/kg/día) y amikacina (20 mg/ kg/día). Las modificaciones al esquema antimicrobiano fueron realizadas por los médicos tratantes, quienes desconocían los niveles de PCR en cada paciente. Se evaluó al paciente diariamente hasta la remisión del episodio de fiebre y neutropenia.
Para la cuantificación de la PCR se requirió una muestra de 0.5 mL de plasma. La formación del complejo formado por anticuerpos específicos y PCR se detectó por refracción de luz por nefelometría (Nephelometer 100-analyzer, Behring Co, Marburg, Alemania). La cantidad de se determinó en mg/L. Para la confiabilidad de las mediciones, se almacenaron alícuotas de las muestras en congelación a -70°C y la cuantificación de PCR se realizó por duplicado; se obtuvo una correlación de r = 0.96 (rho de Spearman) en las mediciones pareadas. De manera adicional con cada serie de muestras se midieron controles Reuma IV/T, SL/1 y 2 para controlar la precisión y exactitud de la prueba. También se realizaron auditorías por laboratorios externos. El procedimiento lo realizó un químico, quien desconocía la condición y diagnósticos de los pacientes.
Los pacientes fueron distribuidos en cuatro grupos, de acuerdo con su condición clínica:
Grupo I. Infección microbiológicamente documentada. Crecimiento bacteriano o fúngico en cultivos de sitios estériles, con o sin foco infeccioso identificado.
Grupo II. Infección clínicamente documentada. Paciente con datos clínicos de infección, sin aislamiento de un microorganismo causal.
]]> Grupo III. Fiebre no asociada a infección. Episodio de fiebre, sin evidencia clínica o microbiológica de infección, con remisión de la sintomatología sin asociación con el inicio del esquema de antibiótico o cuando se determinó que la fiebre se atribuyó a la actividad neoplásica.Grupo IV. Pacientes sin fiebre. Este grupo estuvo compuesto por pacientes con cáncer, que en el momento de la evaluación cursaban con neutropenia grave, pero sin fiebre o evidencia clínica de algún proceso infeccioso. Este grupo conformó el grupo control.
Tamaño de la muestra
Se calculó para un valor de p < 0.05, sensibilidad y especificidad estimadas del 80% [(P = 0.80), 1 - P = 0.20] y amplitud total del intervalo para la proporción de ± 0.20, con lo que se estimó un tamaño mínimo de la muestra de 124 pacientes.
Aspectos éticos
El estudio se clasificó como de riesgo mínimo. Fue aprobado por el Comité Local de Ética e Investigación del Hospital de Pediatría, Centro Médico Nacional Siglo XXI. Se solicitó consentimiento verbal a los padres o tutores de los pacientes para la toma de muestras para la PCR.
Análisis estadístico
Debido a que las variables cuantitativas no tuvieron distribución normal, se utilizó estadística no paramétrica. Se empleó la mediana (Md) y los límites intercuartílicos (Liq = percentiles 25-75) como medidas de tendencia central y dispersión, respectivamente. La prueba U de Mann-Whitnney y prueba de Kruskal-Wallis se utilizaron para la comparación de variables cuantitativas entre dos o más grupos, respectivamente. La x2 o la prueba exacta de Fisher se emplearon para comparar variables cualitativas. Para evaluar la correlación entre las mediciones de la PCR que se procesaron por duplicado, se realizó la prueba de rho de Spearman. Para estas pruebas, un valor de p ≤ 0.05 se consideró significativo.
Para determinar la utilidad de la PCR se realizó análisis de Bayes. Los pacientes del grupo I y II se consideraron los verdaderos positivos y a los de los grupos III y IV como los verdaderos negativos. Los mejores niveles de sensibilidad y especificidad se establecieron con curvas de las características operantes del receptor (COR). Con cada uno de los niveles de corte se realizaron los cálculos para los valores predictivos positivo y negativo, así como para razones verosimilitud y probabilidad a posteriori. Para cada valor de sensibilidad, especificidad y valores predictivo positivo y negativo se calcularon intervalos de confianza al 95% (IC95%).17 El análisis estadístico se realizó con el programa SPSS 18.0 (SPSS IBM, USA).
]]> RESULTADOS
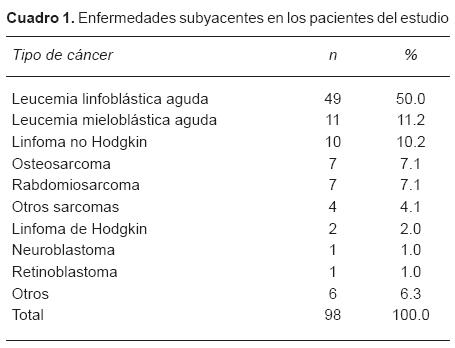
Se incluyeron 112 pacientes en total, de los cuales se excluyeron 14, es decir, quedaron 98 sujetos para el análisis final. La edad promedio fue de 9.3 ± 3.9 años. Con respectao al sexo, fueron 57 hombres (58.2%) y 41 mujeres (41.8%). El 61.2% de los pacientes tenía diagnóstico de leucemia, siendo la leucemia linfoblástica aguda la más común (Cuadro 1). Se encontraban en recaída de su enfermedad de base 42 pacientes.

Episodios
De los 98 pacientes, se analizaron en total de 127 episodios, que se distribuyeron en los cuatro grupos (Cuadro 2). Del grupo total, la mediana para la última dosis de quimioterapia fue de 15 días (Liq 9-21) y la mediana para los días de fiebre previa al ingreso fue de 1 día (Liq 1-2).
El grupo I estuvo integrado por 29 episodios. Los microorganismos más comúnmente aislados fueron Staphylococcus aureus, Klebsiella pneumoniae y Escherichiacoli (25.8, 16.1 y 13 %, respectivamente). En dos episodios se obtuvo aislamiento de Candida. En dos episodios se aislaron dos microorganismos diferentes.
El grupo II incluyó 47 episodios. En 29 se encontró el foco infeccioso localizado (Ila) y en 18 no se localizó la infección (Ilb). De las enfermedades diagnosticadas en el subgrupo Ila predominaron celulitis (n= 7, 16.6%), colon neutropénico (n= 6, 14.3%), neumonía (n= 6, 14.3%) y gastroenteritis aguda (n= 6, 14.3%). La mediana para la remisión de la fiebre fue de 2 días (Liq 1.5-4.5). En el grupo de pacientes sin foco infeccioso (IIb), la mediana para la remisión de la fiebre también fue de 2 días (Liq 2-3). En un paciente hubo remisión de la fiebre al día 7 y en otro al día 14 de iniciado el tratamiento antimicrobiano.
En el grupo III se incluyeron 20 episodios de fiebre y neutropenia no relacionados con infección; en siete (36.8%), se documentó que la causa de la fiebre fue secundaria a la recaída de la enfermedad principal. La mediana para la remisión de la fiebre fue de un día (Liq 1-5) y no hubo relación con el inicio del tratamiento antimicrobiano empírico.
En el grupo IV se incluyeron 31 episodios. En el momento de la evaluación, la mayoría se encontraba recibiendo quimioterapia antineoplásica.
]]> Valores de PCRLa mediana de la PCR para el grupo I fue de 282 mg/L (Liq 174.3-385.5); para el sub-grupo Ila de 198 (Liq 127.4267), para el sub-grupo Ilb de 178 (Liq 119-221), para el grupo III fue de 27.3 mg/L (Liq 12.3-55.2) y para el grupo IV de 5.1 mg/L (Liq 2.4-13.3) (Cuadro 2).
Cuando se compararon los valores de PCR entre grupo I y II, no se encontraron diferencias significativas (p = 0.06) y tampoco entre los subgrupos IIa y IIb (p = 0.23), por lo que se consideraron como un solo grupo (pacientes con infección [I, IIa y IIb]). El grupo de los pacientes sin infección lo constituyeron los grupos III y IV. Las medianas para los valores de PCR en el grupo de pacientes con infección fue de 201 mg/L (Liq 136.5-300.3) y de 12.0 (Liq 2.8-29.5) para el grupo de pacientes sin infección (p < 0.0001).
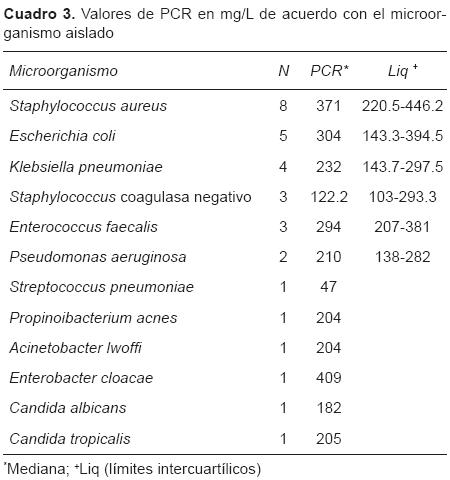
Al comparar los niveles de PCR con el microorganismo aislado en los pacientes del grupo I, se observó que las medianas de la prueba fueron más altas para S. aureus (371 mg/L, Liq 220.5-446.2), E. coli (304 mg/L, Liq 143.3-394.5) y E. faecalis (294 mg/L, Liq 207381), aunque no se observaron diferencias significativas (p = 0.35) (Cuadro 3).
Análisis de la prueba diagnóstica
De acuerdo con las curvas de las características operantes del receptor (COR) para la identificación de una infección bacteriana, el nivel de corte óptimo de PCR fue de 60 mg/L. En este punto, la sensibilidad (S) fue de 94% (IC95% 89-99%), la especificidad (E) de 94% (IC95% 88100%), el valor predictivo positivo (VPP) de 96% (IC95% 92-100%) y para el valor predictivo negativo (VPN) de 92% (IC95% 85-99%). Considerando el nivel de PCR de 60 mg/L, al comparar el grupo de pacientes con infección vs el grupo III, y el grupo de infectados vs el grupo IV, los valores de S, E, VPP y VPN se mantuvieron altos.
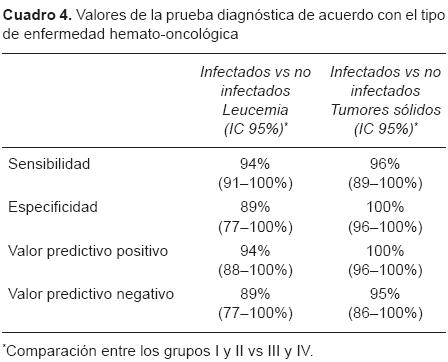
Cuando se evaluó la utilidad de la prueba de PCR con el valor de 60 mg/L en los pacientes con leucemia y con tumores sólidos, los valores de S, E, VPP y VPN fueron más altos (Cuadro 4).
]]>
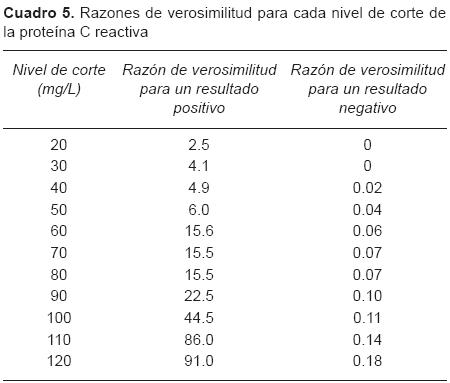
Las razones de verosimilitud a los diferentes niveles de corte se muestran en el Cuadro 5. Con un nivel de PCR mayor a 60 mg/L, la razón de verosimilitud fue de 15.6 y de 0.06 para un nivel inferior a este valor. Se observa que con un resultado de PCR menor de 30 mg/L, ningún paciente cursó con infección, mientras que con una cifra superior de 100 mg/L todos resultaron infectados.
DISCUSIÓN
El origen de la fiebre en el paciente neutropénico constituye un problema diagnóstico y terapéutico. Dependiendo de la serie consultada, cerca de 70% de los pacientes en estas condiciones cursan con infección; en el resto, la fiebre puede estar asociada con transfusiones, administración de quimioterápicos, antimicrobianos o necrosis tumoral.1,2 La fiebre puede ser el único signo de infección grave, dado que su respuesta inflamatoria es mínima o nula.4
Por la alta morbilidad y mortalidad asociada a las infecciones en el paciente con neutropenia grave, se recomienda la administración de esquemas antimicrobianos de amplio espectro. Sin embargo, su uso puede propiciar la inducción de resistencias microbianas, sobreinfecciones fúngicas, efectos secundarios e incremento de costos de atención.18
Dada la baja identificación del agente etiológico de la infección mediante las pruebas rutinarias para diagnóstico microbiológico (cultivos, serología, detección de antígeno) en este tipo de pacientes, son necesarias otras pruebas de diagnóstico, como los biomarcadores, que apoyen el diagnóstico clínico, reúnan características de rapidez, bajo costo, alta sensibilidad y especificidad y que no sean alteradas por la enfermedad de base, transfusiones o quimioterapia.19,20
La PCR es quizá el biomarcador más evaluado en diferentes estudios. Sin embargo, en un meta-análisis reciente20 se consideró que su uso no debe recomendarse, ya que existe heterogeneidad e inconsistencias en los estudios revisados, además de que los resultados como prueba para discriminar entre pacientes con y sin infección no son concluyentes.
]]> En este estudio de evaluación de una prueba diagnóstica fase V21 se incluyeron 98 pacientes con características clínicas basales idénticas entre los grupos, sin conocer la causa de la fiebre en el momento de su evaluación. Los grupos I y II se consideraron como pacientes con infección. Al analizar en forma conjunta los grupos III y IV como pacientes sin infección, los valores de la prueba diagnóstica mantuvieron sensibilidad y especificidad elevadas. Al utilizar el nivel de corte de 60 mg/L, elegido por curvas operantes del receptor, la sensibilidad y especificidad de la prueba fueron de 94%, y los valores predictivos superiores al 90%, los cuales mejoraron al separar a los pacientes de acuerdo con el tipo de cáncer. Dada la prevalencia de infección de 79%, se probaron a diferentes puntos de corte los niveles de proteína C reactiva para determinar las probabilidades a posteriori. A un nivel de corte de 60 mg/L, la probabilidad de tener infección en sujetos con sospecha clínica y con resultado positivo fue de 98%, y de no tenerla de 2% para los pacientes con PCR negativa y con baja sospecha de infección. Adicionalmente, se encontró que a ese mismo nivel de corte de PCR, la razón de verosimilitud señaló que es 15.6 veces más probable encontrar un resultado positivo en pacientes con infección. Por otro lado, un paciente con un resultado negativo de la prueba (< 60 mg/L) tiene menos de una décima de probabilidad (0.06) de presentarse en un paciente con infección. A un nivel de PCR inferior a 30 mg/L, ninguno de los pacientes con neutropenia y fiebre, cultivos negativos y sin foco infeccioso cursó con infección. De la misma manera, todos los pacientes con un nivel superior de 100 mg/L presentaron infección bacteriana. Tal como se reporta en otros estudios, los valores de la PCR en los sujetos con infección se encontraron elevados a pesar de la neutropenia.22,23 Los pacientes del grupo IV (neutropenia sin fiebre) en general, recibían algún tipo de quimioterapia antineoplásica y sus valores de PCR fueron bajos (Md 5.1, Liq 2.4-13.3).Por otro lado, aunque los niveles de la PCR en el grupo de pacientes con fiebre asociada a causas no infecciosas (III) fueron más altos que los encontrados en los pacientes con neutropenia y sin fiebre (IV), su intervalo de confianza 95% no se interpoló con el de los pacientes infectados (p < 0.001), por lo que es posible que la actividad tumoral o las infecciones virales no detectadas eleven en forma discreta los niveles de PCR, pero no alcanzan los valores de los pacientes con infección bacteriana.24 No se encontraron diferencias significativas en los niveles de PCR entre los grupos por definición de la infección, ya fuera clínica o microbiológicamente documentada (Grupo I y II) (p = 0.06).
Algunos autores han realizado evaluaciones en las que la PCR sirve como factor de decisión para determinar la suspensión o mantenimiento del tratamiento antimicrobiano. En neonatos, Ehl y colaboradores eligieron un nivel de PCR de 10 mg/L. Cuando el valor era superior y se sospechaba sepsis, continuaron los antibióticos. Si la PCR era baja, en ausencia de respuesta inflamatoria sistémica o sospecha clínica de sepsis, el tratamiento se suspendía. Los desenlaces fueron satisfactorios y la frecuencia de recaídas fue baja (3/176), el valor predictivo negativo fue de 99% (IC95% 95.4-99.9%). Sin embargo, los resultados se consideran aún preliminares.25 En niños neutropénicos con fiebre, Santolaya y colaboradores realizaron una evaluación con PCR a un nivel de corte de 40 mg/L, apoyada en características clínicas. La tasa de casos con falla terapéutica fue también baja. Sin embargo, la población estudiada fue pequeña.14 Aquino y colaboradores catalogaron a los pacientes neutropénicos con fiebre como de "alto riesgo" de desarrollar infecciones graves al presentar una de las siguientes características: diagnóstico reciente o recaída, apariencia clínica de enfermedad, NA <200/ mm3 o neutropenia prolongada (>7 días).26 Los pacientes de "bajo riesgo" usualmente están en remisión y su estado general es bueno, además de que sus hemocultivos son negativos, tienen tendencia a la remisión de la fiebre y evidencia de recuperación medular. Hasta el momento no existe una recomendación para utilizar un valor definido de PCR para continuar o suspender los antimicrobianos en un paciente con cáncer, fiebre y neutropenia.20
Dada la evaluación global de la prueba diagnóstica y considerando las razones de probabilidad que en estudios previos no se habían calculado, podemos concluir que la prueba fue útil en los pacientes pediátricos con cáncer que se atienden en este hospital de tercer nivel para distinguir entre los pacientes con infección y los sujetos con fiebre asociada a causas no infecciosas.
REFERENCIAS
1. Freifeld AG, Bow EJ, Sepkowitz K, Boeckh MJ, Ito JI, Mullen CA, et al. Clinical Practice Guideline for the use of antimicrobial agents in neutropenic patients with cancer: 2010 update by the Infectious Diseases Society of America. Clin Infect Dis 2011;52:e56-e93. [ Links ]
2. Pizzo PA, Robichaud KJ, Wesler R, Commers J. Fever in the pediatric and young adult patient with cancer. A prospective study of 1001 episodes. Medicine (Baltimore) 1982;161:153-165. [ Links ]
]]>3. González-Galnares M, Guiscafré-Gallardo H, Vargas-de la Rosa R, Bernaldez-Ríos R, Farfán-Castro J, Barrón-Uribe C, et al. Infección en el niño con inmunodeficiencia. Lineamientos sobre su prevención y asistencia. Rev Med IMSS 1983;21:207-217. [ Links ]
4. Meckler G, Lindemulder S. Fever and neutropenia in pediatric patients with cancer. Emerg Med Clin North Am 2009;27:525-544. [ Links ]
5. Pourcyrous M, Bada HS, Korones SB, Baselski V, Wong SP. Significance of serial C-reactive protein responses in neonatal infection and other disorders. Pediatrics 1993;92:431-436. [ Links ]
6. Pepys MB. C-reactive protein fifty years on. Lancet 1981;1:653-657. [ Links ]
7. Jaye DL, Waites KB. Clinical applications of C-reactive protein in pediatrics. Pediatr Infect Dis J 1997;16:735-747. [ Links ]
]]>8. Kawamura M, Nishida H. The usefulness of serial C-reactive protein measurement in managing neonatal infection. Acta Paediatr 1995;84:10-13. [ Links ]
9. Peltola H, Jaakkola M. C-reactive protein in early detection of bacteremic versus viral infections in immunocompetent and compromised children. J Pediatr 1988;113:641-646. [ Links ]
10. Santolaya MA, Cofre J, Beresi V. C-reactive protein: a valuable aid for the management of febrile children with cancer and neutropenia. Clin Infect Dis 1994,18:589-595. [ Links ]
11. Manian FA. A prospective study of daily measurement of C-reactive protein in serum of adults with neutropenia. Clin Infect Dis 1995;21:114-121. [ Links ]
12. Riikonen P, Jalanko H, Hovi L, Saarinen UM. Fever and neutropenia in children with cancer: diagnostic parameters at presentation. Acta Paediatr 1993;82:217-225. [ Links ]
]]>13. Katz JA, Mustafa MM. Management of fever in granulocytopenic children with cancer. Pediatr Infect Dis J 1995;12:330-337. [ Links ]
14. Santolaya ME, Villarroel M, Avendaño LF, Cofré J. Discontinuation of antimicrobial therapy for febrile, neutropenic children with cancer: a prospective study. Clin Infect Dis 1997;25:92-97. [ Links ]
15. Avabratha KS, Rau AT, Venkataravanamma P, Rau A. Significance of C-reactive protein during febrile neutropenia in pediatric malignancies. Indian Pediatr 2009;46:797-799. [ Links ]
16. Clinical and Laboratory Standards Institute (CLSI). Principles and Procedures for Blood Cultures. Approved Guideline. CLSI document M47-A. Pennsylvania: CLSI; 2007. [ Links ]
17. Sackett D, Straus SE, Richardson WS, Rosenberg W, Haynes RB. Evidence-Based Medicine. How to Practice and Teach EBM. New York: Churchill Livingston; 2000. p. 67. [ Links ]
]]>18. Hathorn JW, Lyke K. Empirical treatment of febrile neutropenia: evolution of current therapeutic approaches. Clin Infect Dis 1997;24(suppl 2):S256-S265. [ Links ]
19. Pritchard-Jones K, Kaatsch P, Steliarova-Foucher E, Stiller CA, Coebergh JWW. Cancer in children and adolescents in Europe: developments over 20 years and future challenges. Eur J Cancer 2006;42:2183-2190. [ Links ]
20. Phillips RS, Wade R, Lehrnbecher T, Stewart LA, Sutton AJ. Systematic review and meta-analysis of the value of initial biomarkers in predicting adverse outcome in febrile neutropenic episodes in children and young people with cancer. BMC Med 2012;10:6. [ Links ]
21. Nierenberg AA, Feintesin AR. How to evaluate a diagnostic marker test. Lessons from the rise and fall of dexamethasone suppression test. JAMA 1988;259:1699-1702. [ Links ]
22. Riikonen P, Saarinen UM, Teppo AM, Metsärinne K, Fyhrquist F, Jalanko H. Cytokine and acute-phase reactant levels in serum of children with cancer admitted for fever and neutro-penia. J Infect Dis 1992;166:432-436. [ Links ]
]]>23. Secmeer G, Devrim I, Kara A, Ceyhan M, Cengiz B, Kutluk T, et al. Role of procalcitonin and CRP in differentiating a stable from deteriorating clinical course in pediatric febrile neutropenia. J Pediatr Hematol Oncol 2007;29:107-111. [ Links ]
24. El-Maghraby SM, Moneer MM, Ismail MM, Shalaby LM, El-Mahallawy HA. The diagnostic value of C-reactive protein, interleukin-8, and monocyte chemotactic protein in risk stratification of febrile neutropenic children with hematologic malignancies. J Pediatr Hematol Oncol 2007;29:131-136. [ Links ]
25. Ehl S, Gering B, Bartmann P, Högel J, Pohlandt F. C-reactive protein is a useful marker for guiding duration of antibiotic therapy in suspected neonatal bacterial infection. Pediatrics 1997;99:216-222. [ Links ]
26. Aquino VM, Tkaczewski I, Buchanan GR. Early discharge of low-risk febrile neutropenic children and adolescents with cancer. Clin Infect Dis 1997;25:74-78. [ Links ]
]]>