Anticuerpos anti-HLA y rechazo agudo del injerto renal en los niños
Anti-HLA antibodies and acute renal graft rejection in children
Rubén Arturo Galeas,1 Rebeca Gomezchico-Velasco,2 Saúl Valverde,1 Guillermo Ramón-García,3 Luis Velásquez-Jones,1 Benjamín Romero-Navarro,1 Ana María Hernández,4 Arindal Vargas,4 Claudia de Leo,5 Mara Medeiros4
1 Departamento de Nefrología
]]> 2 Subdirección de Pediatría Ambulatoria3 Departamento de Patología
4 Laboratorio de Investigación en Nefrología y Metabolismo Mineral, Hospital Infantil de México Federico Gómez
5 Laboratorio de Trasplante, Instituto Nacional de Ciencias Médicas y Nutrición Salvador Zubirán, México D.F., México
Autor de Correspondencia:
Dra. Mara Medeiros Domingo
Correo electrónico: medeiro.mara@gmail.com
Fecha de recepción: 05-04-10. ]]> Fecha de aceptación: 12-08-10.
Resumen
Introducción. A pesar de que las nuevas terapias inmunosupresoras han mejorado notablemente la evolución clínica de los trasplantes renales, los rechazos agudo y crónico siguen limitando la sobrevida a largo plazo del injerto. En base a lo anterior, el objetivo de este estudio fue determinar la presencia de anticuerpos séricos contra antígenos de histocompatibilidad (HLA) clase I y clase II en niños con rechazo agudo del injerto renal.
Métodos. Se realizó un estudio clínico prospectivo en pacientes con trasplante renal que presentaron rechazo agudo del injerto. Se les tomó muestra de suero al momento de la biopsia renal, misma que fue utilizada para la detección de anticuerpos contra antígenos HLA de clase I y II por ensayo basado en equipo fuoroanalizador (Luminex) y microperlas cubiertas con antígenos clase I y clase II de One Lambda.
Resultados. De 21 pacientes estudiados, 17 pacientes (81%), fueron diagnosticados con rechazo celular y cuatro (19%) con rechazo agudo mediado por anticuerpos.
El tiempo post-trasplante promedio de presentación del rechazo humoral agudo fue de 18.7 meses y para el rechazo celular de 36.7 meses.
Once pacientes (52.3%) presentaron anticuerpos específicos contra el donador. Los anticuerpos contra antígenos HLA clase I donador específicos se encontraron en seis pacientes, siendo más frecuente el rechazo agudo mediado por anticuerpos (humoral), donde todos los pacientes tuvieron anti HLA clase I con Chi cuadrada (P =0.004). En cuanto a los anticuerpos inespecíficos, el 95.2% de los pacientes desarrollaron este tipo de anticuerpos.
Conclusiones. El 95% de los niños con rechazo del injerto renal presentan anticuerpos anti HLA, específicos y/o no específicos contra el donador. Los anticuerpos anti HLA donador específicos clase I se presentan con mayor frecuencia en el rechazo humoral.
Palabras clave: rechazo mediado por anticuerpos, rechazo celular, rituximab, plasmaféresis, globulina intravenosa, metilprednisolona.
]]>Abstract
Background. Although new immunosuppressive therapies have signifcantly improved the clinical progression of kidney transplants, acute and chronic rejection continue to limit long-term graft survival. Despite this, the aim of the study was to determine the presence of human leukocyte antigen (HLA) antibodies class I and class II in children with acute renal graft rejection.
Methods. Patients with graft rejection were included in the study. A serum sample for anti-HLA antibody measurement class I and II by Luminex was taken at the time of renal biopsy.
Results. Seventeen patients (81%) had cellular rejection and four (19%) antibody-mediated rejection. Mean post-transplant time of rejection was 18.7 months and 36.7 months for humoral rejection and cellular rejection, respectively. Eleven patients (52.3%) had donor specific (DS) antibodies. Anti-HLA class I DS was found in six patients including the four patients with humoral rejection (Fisher exact test p =0.004); 95.2% had non-DS antibodies.
Conclusions. Of the children with acute renal graft rejection, 95% have anti HLA antibodies (DS and/or non-DS). Anti-HLA DS class I are more frequent in humoral rejection.
Key words: antibody mediated rejection, cellular rejection, rituximab, plasmapheresis, intravenous inmmunoglobulin, metilprednisolone.
Introducción
A pesar de que las nuevas terapias inmunosupresoras han mejorado notablemente la evolución clínica de los trasplantes renales (TR), los rechazos agudo y crónico siguen limitando la sobrevida a largo plazo del injerto.
]]> El sistema inmune del receptor puede dañar el injerto a través de diversos mecanismos que se sobreponen.El rechazo hiperagudo, manifestado por trombosis intravascular, isquemia y falla del injerto inmediata, es mediado por anticuerpos preformados contra antígenos del sistema mayor de histocompatibilidad (HLA). El rechazo agudo del injerto se caracteriza por una disminución súbita de la función del injerto renal acompañada de infiltración de mononucleares con o sin inflamación vascular, puede se precipitado por células T y/o aloanticuerpos y ocasiona pérdida del injerto si no se trata. El rechazo crónico, definido como un deterioro lento y progresivo en la función renal asociado a arteriopatía del injerto y fibrosis, puede estar mediado por células T y/o anticuerpos anti-injerto formados post-trasplante, que interactúan con componentes del sistema inmune innato en conjunción con una variedad de factores no inmunes.1
La inmunidad celular ha sido extensamente estudiada en los trasplantes de órganos por ser considerada el mecanismo efector de mayor importancia en el rechazo agudo; de hecho, la mayor parte de los esquemas inmunosupresores de inducción y mantenimiento están dirigidos directamente a los linfocitos T.2
En los últimos años se ha obtenido evidencia del papel fundamental que juegan las células B y sus productos, los anticuerpos, en la patogénesis del rechazo agudo. Estos pacientes suelen presentar rechazo severo resistente a la terapia convencional en contra de células T.3,4
Este tipo de rechazo puede representar una respuesta anamnésica a aloantígenos del donador, o bien, reflejar la presencia de niveles bajos de anticuerpos preformados que no se detectan por las técnicas de pruebas cruzadas habituales, incluyendo la presencia de anticuerpos anti-células endoteliales. endoteliales.5
En un estudio de casos y controles, Zhu y cols. encontraron que 97% de los pacientes presentan anticuerpos anti-HLA al momento de disfunción del injerto vs 48% de los controles, pacientes con trasplante renal seguidos el mismo periodo de tiempo y con función estable del injerto.6
El diagnóstico del rechazo humoral no siempre es fácil. En el estudio realizado por Mauiyyedi y cols., en 67 pacientes que presentaron rechazo agudo renal en los primeros tres meses posttrasplante, 30% tuvo un componente humoral evidenciado por el depósito del fragmento de complemento C4d en la biopsia.7 Puede ser que no se detecten anticuerpos específicos para el donador y aun así el injerto está siendo rechazado. La ausencia de anticuerpos puede reflejar su fijación en el injerto; en estos casos se espera que los anticuerpos anti-donador sean evidentes en el estudio histopatológico. Sin embargo, aún la inmunopatología puede no revelar anticuerpos en el injerto. Esto debido a la mayor habilidad de los vasos sanguíneos de depurar anticuerpos y complejos inmunes.8 La tinción para C4d en el tejido renal, principalmente en los capilares peritubulares, es un indicador muy sensible de la activación de la vía clásica del complemento que ocurre en el rechazo agudo humoral.9
El objetivo de este estudio fue determinar la presencia de anticuerpos séricos anti- HLA clase I y clase II generales y donador específicos en niños con rechazo agudo del injerto renal.
Métodos
]]> Se realizó un estudio clínico prospectivo en el Hospital Infantil de México Federico Gómez en el que se incluyeron pacientes con trasplante renal que presentaron rechazo agudo del injerto en el periodo comprendido de marzo de 2006 a abril de 2009, a los cuales se les tomó muestra de suero al momento de la biopsia renal, misma que fue utilizada para la detección de anticuerpos contra antígenos HLA de clase I y II. El estudio fue aprobado por los Comités de Ética e Investigación, con firma de consentimiento informado (Protocolo HIM/2006/030, SSA 686).El diagnóstico de rechazo agudo se realizó por biopsia renal según la Clasificación de Banff.10
En todas las biopsias renales se hizo inmunohistoquímica para C4d.
Se estudiaron 21 pacientes, de los cuales diecisiete pacientes fueron catalogados como rechazo celular y fueron tratados con bolos de metilprednisolona a 10 mg/kg/dosis por tres a cinco días consecutivos.
Cuatro pacientes tuvieron diagnóstico de rechazo agudo mediado por anticuerpos, de los cuales tres fueron tratados con sesiones de plasmaféresis cada tercer día con recambio de un volumen de plasma de 90-120 min y reposición con albúmina al 5%. Después de la sesión de plasmaféresis recibieron inmunoglobulina G intravenosa (IgG IV) 500 mg/kg en infusión lenta y rituximab (anticuerpo monoclonal anti-CD20) a dosis de 375 mg/m2/semana, en dos dosis. El tratamiento inmunosupresor de mantenimiento se continuó a las dosis habituales.
Una paciente fue catalogada como rechazo celular resistente a esteroides y recibió 5 bolos de metilprednisolona; posteriormente, globulina antilinfocito por 10 dosis a 1.5 mg/kg. Al hacer, en forma retrospectiva, la detección de anticuerpos vs. donador se encontró que además tenía la presencia de anticuerpos clase I contra donador y C4d positivo en la biopsia renal por lo que, para fines del estudio, se catalogó como rechazo humoral agudo.
La función renal fue evaluada mediante la determinación de creatinina sérica y estimación de la velocidad de filtración glomerular (VFG) por la fórmula de Schwartz:
eVFG (ml/min/1.73 m2) = kL/Scr (mg/dL), donde:
L: talla en centímetros, Scr: creatinina sérica, k: constante con valor de 0.55 para niños y adolescentes femeninas y de 0.7 para varones adolescentes.11-13
Esta fórmula, si bien se diseñó para estimar la función renal de riñones nativos, también se utiliza en pacientes con trasplante renal.14
]]>Análisis de anticuerpos anti-HLA por Luminex
La determinación de anticuerpos anti HLA clase I y II se realizó mediante ensayo basado en equipo fluoroanalizador LAB Scan 100 (Luminex, Austin, Tx) y las microperlas cubiertas con antígenos clase I y clase II (LABScreen® Single Antigen HLA Class I-combi y LABScreen® Single Antigen HLA Class II, One Lambda Inc., Canoga Park, California USA). Con esta tecnología de fase sólida, únicamente una molécula de HLA producida por tecnología recombinante se une a una perla y permite detectar las especificidades de los anticuerpos en suero en forma muy precisa, ya que elimina las reacciones falsas positivas debidas a anticuerpos no dirigidos contra HLA e identifica los anticuerpos reactivos a uno o más epítopes dominantes.15,16 Siguiendo las recomendaciones del fabricante, 40mL de suero del paciente se incuban con las microperlas recubiertas por antígenos HLA durante media hora; posteriormente, se lavan y se remueve el anticuerpo no unido. Después, las perlas se incuban durante 30 minutos con anticuerpos anti-IgG humano para finalmente ser colocadas en el fluoroanalizador. Se incluye siempre un control negativo. Se utilizó el software HLA-Visual de One Lambda para obtener el análisis de datos.
Resultados
Se incluyeron 21 pacientes en el estudio. La demografía se muestra en la Tabla 1. Catorce fueron del sexo masculino, con una edad promedio de 15.7 años. Diecisiete recibieron el órgano de donador vivo relacionado y cuatro de donador fallecido. Diecisiete pacientes (81%), fueron diagnosticados como rechazo celular y cuatro (19%) como rechazo agudo mediado por anticuerpos (humoral).
El tiempo post-trasplante promedio de presentación del rechazo humoral agudo fue de 18.7 meses y para el rechazo celular de 36.7 meses.
El tiempo de seguimiento promedio posterior al trasplante renal fue de 54.1 meses en el grupo de pacientes con rechazo celular y de 37.7 meses en los pacientes con rechazo humoral agudo. En cuanto al esquema de inmunosupresión, dieciocho pacientes recibieron inducción con Anti-CD25 (Basiliximab o Daclizumab). Diecisiete pacientes (81%) recibieron tacrolimus, micofenolato de mofetilo y prednisona. Dos pacientes (9.5%) recibieron ciclosporina, azatioprina y prednisona; dos pacientes (9.5%) recibieron inmunosupresión sin esteroide que incluye tratamiento con daclizumab (Zenapax) por seis meses para alcanzar una dosis acumulada de 10mg/kg, tacrolimus y micofenolato de mofetilo. Uno de ellos presentó rechazo celular IIA posterior al cual se introdujo esteroide a su esquema de tratamiento en forma permanente. Dentro de este estudio, el 52.3% de los pacientes (11/21) presentaron anticuerpos específicos contra el donador, de los cuales 19% (4/21) fue contra antígenos HLA clase I, 23.8% (5/21) contra antígenos HLA clase II y 9.5% (2/21) presentaron anticuerpos contra ambos tipos de antígenos.
En la Tabla 2 se detallan las incompatibilidades que tenía cada trasplante, las especificidades de los anticuerpos anti-HLA encontrados, el tipo de rechazo agudo presentado, la presencia o no de C4d en el tejido renal, el tiempo de seguimiento y la velocidad de filtración glomerular en el último seguimiento. En tres pacientes no se cuenta con el HLA del receptor (pacientes 16, 17 y 18) ya que no es un requisito para recibir un injerto de donador fallecido,17 y en nuestro país los órganos se asignan sin considerar el HLA; sin embargo, se sabe que el donador del paciente 17 tenía el HLA A2 para el cual el paciente desarrolló anticuerpos.
Una paciente presentó pérdida del injerto por falta de adherencia terapéutica no asociada a la formación de anticuerpos específicos contra el donador (paciente 10, Tabla 2). Un paciente no desarrolló ningún tipo de anticuerpos a pesar de tener rechazo celular IIA (paciente 11, Tabla 2). Una paciente fue receptora de un segundo injerto renal (paciente 21, Tabla 2).
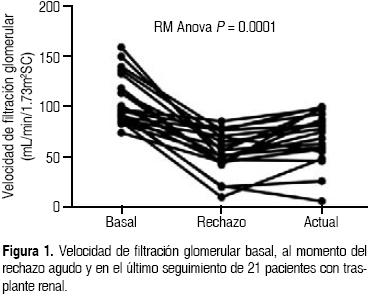
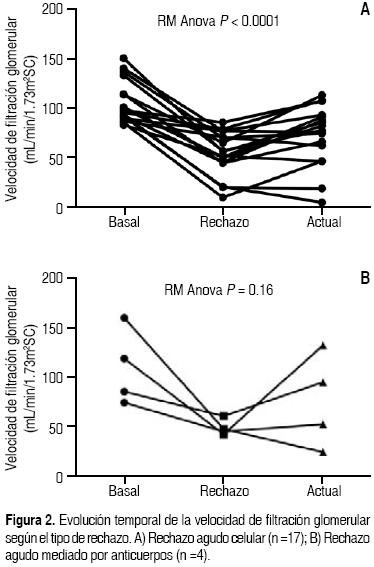
]]> Los niveles de creatinina sérica y la velocidad de filtración glomerular fueron analizados al momento del egreso posterior al trasplante (creatinina basal), en el momento del rechazo agudo y durante el último seguimiento en la consulta externa, con un tiempo de seguimiento promedio post-trasplante de 45.9 ± 11.6 meses. En forma global, hubo un aumento significativo de la creatinina durante el episodio de rechazo y un valor basal de 0.9 mg/dL y aumento a 1.5 mg/dL en el último seguimiento (Tabla 3).La VFG se encuentra disminuida al momento del rechazo en ambos grupos, y si bien mejora después del tratamiento antirrechazo, no se recupera el valor basal. La diferencia del valor basal vs el de seguimiento es más pronunciada en los pacientes con rechazo celular, probablemente porque una paciente de ese grupo perdió el injerto (Figuras 1 y 2). En la Figura 3 se muestra el depósito de C4d mediante inmunohistoquímica en el endotelio de los capilares peritubulares.


Anticuerpos anti-HLA donador específicos
Once pacientes presentaron anticuerpos anti-HLA donador específicos (52.3%). Los anticuerpos contra antígenos HLA clase I donador específicos se encontraron en seis pacientes; el rechazo más frecuente fue el rechazo agudo mediado por anticuerpos, donde todos los pacientes tuvieron anti-HLA clase I con P = 0.002 por prueba exacta de Fisher (Tabla 4).
]]> Dos de estos pacientes que presentaron rechazo humoral también formaron anticuerpos contra antígenos HLA de clase II donador específicos. Dos pacientes con rechazo celular presentaron anticuerpos donador específicos contra antígenos HLA clase I (9.5%). Ninguno de estos pacientes formó anticuerpos anti-HLA clase II (Tabla 2).De los cinco pacientes con rechazo celular que formaron anticuerpos específicos contra antígenos HLA de clase II ninguno presentó anticuerpos contra antígenos de clase I (Tablas 2 y 3).
Anticuerpos anti-HLA inespecíficos
En cuanto a los anticuerpos inespecíficos el 95.2% (20/21) de los pacientes desarrollaron este tipo de anticuerpos. El 76.4% (13/17) de pacientes con rechazo celular fue contra ambas clases de HLA; dos pacientes (11.7%) presentaron anticuerpos para antígenos HLA de clase I y un paciente (5.8%) para antígenos HLA de clase II (Tabla 2). Todos los pacientes con rechazo agudo mediado por anticuerpos presentaron anticuerpos no específicos contra antígenos de clase I; de estos, dos presentaron también anticuerpos para antígenos HLA clase II (50%). Un paciente del grupo rechazado no presentó anticuerpos inespecíficos al momento del rechazo (paciente 11, Tabla 2).
Discusión
La disfunción del injerto, evaluada por la elevación de la creatinina sérica o por disminución de VFG en un paciente con trasplante renal, es el primer elemento para la sospecha de rechazo agudo del injerto renal. El estándar de oro para el diagnóstico definitivo es la biopsia renal.
El rechazo celular agudo es el tipo de rechazo más frecuente. El porcentaje de pacientes con rechazo humoral agudo no varía con respecto a otras series donde se encuentra en el 20-30% de los episodios de rechazo agudo del injerto.18,19
La formación de anticuerpos donador específicos contra antígenos HLA de clase I y clase II posterior al trasplante se ha relacionado con el rechazo mediado por anticuerpos, el rechazo crónico y la menor sobrevida del injerto.20 Diversos autores han sugerido la vigilancia postrasplante de anticuerpos anti-HLA donador específicos, los cuales son útiles para la detección de pacientes en riesgo de rechazo agudo y crónico de corazón, pulmón y riñón.19,21,22 Los anticuerpos dirigidos contra otras especificidades también pueden participar en el daño inmunológico contra el injerto.6,23,24
]]> En nuestro estudio encontramos que el 95.2% (20/21) de los pacientes tienen anticuerpos anti-HLA en el episodio de rechazo agudo contra antígenos HLA de clase I y II donador específicos y no específicos, que incluyen una amplia variedad de especificidades como son HLA–A, B, CW para los clase I y DR, DQ y DP para los clase II. Los títulos altos de anticuerpos donador específicos se han reportado hasta en el 95% de los casos con C4d positivo, valor que disminuye en 50% en los casos de C4d negativo.19Desafortunadamente, no sabemos cuántos de nuestros pacientes tenían anticuerpos inespecíficos previos al trasplante renal.
Morales–Buenrostro y cols. reportaron un grupo de 196 pacientes mexicanos con TR con injerto funcional, de los cuales 22% presentó anticuerpos anti-HLA. La presencia de anticuerpos, aunque no se sabe si eran donador específico o no, tuvo un impacto negativo en la sobrevida del injerto.25
Al realizar el análisis entre la presencia de anticuerpos donador específicos con el tipo de rechazo presentado, encontramos una fuerte asociación con el rechazo agudo mediado por anticuerpos ya que todos los pacientes con rechazo humoral presentaron anticuerpos contra antígenos HLA de clase I y 50% presentó anti-HLA clase II. Estos resultados son consistentes con los reportados por otros autores que encontraron títulos elevados de estos anticuerpos al momento del rechazo mediado por anticuerpos.26
Crespo y cols. reportaron un grupo de 81 pacientes adultos con TR que presentaron rechazo, de los cuales los que respondieron a esteroides no tuvieron anticuerpos donador específicos, mientras que 37% de los pacientes que no respondieron al tratamiento tuvieron anti-HLA donador específicos.27
Los anticuerpos donador específicos contra antígenos HLA de clase II se encontraron en 33.3% (7/21) de nuestros pacientes. Burns y cols. reportan la presencia de estos anticuerpos en 16% de los casos al momento del rechazo.28
En cuanto a la tinción C4d, únicamente fue positiva en los pacientes con rechazo humoral, todos ellos con anticuerpos donador específicos, lo que resulta similar a lo reportado por otros autores donde esta tinción se encuentra positiva hasta en el 95% de los casos con rechazo humoral agudo.29,30 Crespo y cols. reportaron que 6% de los pacientes al momento del rechazo agudo sin presencia de anticuerpos donador específicos, presentaron C4d en capilares peritubulares.27 En nuestra serie ningún paciente del grupo de rechazo celular tuvo C4d positivo en la biopsia; sin embargo, de los pacientes catalogados como rechazo celular, dos tuvieron anticuerpos anti-HLA clase I donador específicos y cinco pacientes tuvieron anti-HLA clase II donador específicos. La principal causa de pérdida de injerto a largo plazo es el rechazo humoral crónico. El endotelio vascular de la microcirculación renal es el blanco principal del rechazo mediado por anticuerpos, que al unirse a los antígenos HLA y otros expresados en endotelio inician una cascada de acciones entre las que destacan la inflamación vascular y la activación del sistema del complemento, lo que finalmente conducen a daño endotelial con aumento en la coagulación.31
Se ha reportado que en algunos pacientes el C4d puede ser negativo en la biopsia renal y aún así presentar rechazo crónico mediado por anticuerpos; esto se evidencia por el aumento en la expresión génica de transcritos asociados a endotelio, como endotelina, factor de von Wille-brand, trombomodulina, caderina 5, selectina E, molécula de adhesión celular plaquetas-endotelio 1, entre otros.32
Un importante hallazgo en este estudio es que 75% (3/4) de los pacientes que presentaron rechazo mediado por anticuerpos fueron resistentes al tratamiento con esteroides; sin embargo, respondieron al tratamiento con rituximab, plasmaféresis e inmunoglobulina. Por otro lado, la paciente que fue tratada sólo con bolos de metilprednisolona presentó una notable disminución en la VFG con respecto a su basal. La remoción de anticuerpos a través de plasmaféresis se ha utilizado tanto en tratamiento previo al trasplante en pacientes sensibilizados o bien en aquéllos con rechazo humoral, asociado o no a otras terapias.33
El rituximab es un anticuerpo monoclonal quimérico dirigido contra el antígeno CD20 que se encuentra en los linfocitos pre-B y B maduros, pero no en las células plasmáticas. Es una inmunoglobulina IgG1 k que tiene secuencias murinas en las regiones variables pesadas y ligeras, y secuencias humanas en las regiones constantes. Al unirse al CD20 en los linfocitos B, desencadena reacciones inmunológicas que provocan la lisis de las células B. Los mecanismos posibles de la lisis celular son la citotoxicidad dependiente del complemento y la toxicidad dependiente de anticuerpos.34,35
]]> Se ha propuesto también el uso de globulina intravenosa para el tratamiento del rechazo agudo humoral.34 Como las inmunoglobulinas naturales, la IgIV se puede fijar a factores de complemento y así prevenir el daño a tejidos mediado por la cascada de complemento, como sucede en casos de dermatomiositis.36,37En cuanto al tratamiento del rechazo celular, todos los pacientes recibieron de 3 a 5 bolos de metilprednisolona aunque, si bien la creatina sérica disminuyó de los valores alcanzados en el episodio de rechazo, es evidente que no logra regresar la función renal a los valores basales en el seguimiento. La presentación de un rechazo agudo es un factor conocido de deterioro en la supervivencia del injerto. Se recomienda utilizar OKT3 o globulina antilinfocito en aquellos casos que no responden a los esteroides y tratar al paciente en forma permanente con esteroides si el tratamiento inicial no los incluía.38
Llama la atención que 88% (15/17) de los niños con rechazo agudo de tipo celular tuvieron anticuerpos no específicos contra antígenos HLA.
Estos datos sugieren que la presencia de anticuerpos anti-HLA clase I y clase II, tanto donador específicos como no específicos, están relacionados con el rechazo agudo y la menor sobrevida del injerto. Desafortunadamente no contamos con un grupo control de pacientes con trasplante renal y función estable del injerto, que deberá ser considerado en estudios posteriores.
Agradecimientos
El proyecto recibió apoyo de Fondos Federales Protocolo HIM/2006/030, SSA 686.
Agradecemos a Lourdes Ortiz del Laboratorio de Investigación en Nefrología y Metabolismo Mineral, por su colaboración en el procesamiento y congelación de las muestras de suero.
Referencias
]]>1. Bumgardner G. Evidence for multiple allograft rejection mechanisms within the same experimental system. Curr Opin Organ Transplant 2005;10:20-27. [ Links ]
2. Suthanthiran M, Strom TB. Renal transplantation. N Engl J Med 1994;331:365-376. [ Links ]
3. Gloor J, Cosio F, Lager DJ, Stegall MD. The spectrum of antibody-mediated renal allograft injury: implications for treatment. Am J Transplant 2008;8:1367-1373. [ Links ]
4. Heeger PS, Fairchild RL. Taking aim at a moving target: the complexity of immune-mediated organ rejection. Curr Opin Organ Transplant 2005;10:3-8. [ Links ]
5. Obata F, Yoshida K, Ohkubo M, Ikeda Y, Taoka Y, Takeuchi Y, et al. Contribution of CD4+ and CD8+ T cells and interferon-gamma to the progress of chronic rejection of kidney allografts: the Th1 response mediates both acute and chronic rejection. Transpl Immunol 2005;14:21-25. [ Links ]
]]>6. Zhu L, Lee PC, Everly MJ, Terasaki PI. Detailed examination of HLA antibody development on renal allograft failure and function. Clin Transpl 2008:171-187. [ Links ]
7. Mauiyyedi S, Crespo M, Collins AB, Schneeberger EE, Pascual MA, Saidman SL, et al. Acute humoral rejection in kidney transplantation: II. Morphology, immunopathology, and pathologic classification. J Am Soc Nephrol 2002;13:779-787. [ Links ]
8. Watschinger B, Pascual M. Capillary C4d deposition as a marker of humoral immunity in renal allograft rejection. J Am Soc Nephrol 2002;13:2420-2423. [ Links ]
9. Böhmig GA, Exner M, Habicht A, Schillinger M, Lang U, Kletzmayr J, et al. Capillary C4d deposition in kidney allografts: a specific marker of alloantibody-dependent graft injury. J Am Soc Nephrol 2002;13:1091-1099. [ Links ]
10. Solez K, Colvin RB, Racusen LC, Haas M, Sis B, Mengel M, et al. Banff 07 classification of renal allograft pathology: updates and future directions. Am J Transplant 2008;8:753-760. [ Links ]
]]>11. Schwartz GJ, Brion LP, Spitzer A. The use of plasma creatinine concentration for estimating glomerular filtration rate in infants, children, and adolescents. Pediatr Clin North Am 1987;34:571-590. [ Links ]
12. Schwartz GJ, Furth SL. Glomerular filtration rate measurement and estimation in chronic kidney disease. Pediatr Nephrol 2007;22:1839-1848. [ Links ]
13. Schwartz GJ, Haycock GB, Spitzer A. Plasma creatinine and urea concentration in children: normal values for age and sex. J Pediatr 1976;88:828-830. [ Links ]
14. Ulibarri B, Martinez–Duncker C, Camarrillo C, Guadarrama EO, García P, Munoz AR, et al. Comparison of 99m Tc DTPA vs five methods to estimate glomerular filtration rate in children with renal transplantation. Pediatric Oncall 2009;6:67-70. [ Links ]
15. Everly MJ, Terasaki PI. Monitoring and treating posttransplant human leukocyte antigen antibodies. Hum Immunol 2009;70:655-659. [ Links ]
]]>16. Gebel HM, Moussa O, Eckels DD, Bray RA. Donor-reactive HLA antibodies in renal allograft recipients: considerations, complications, and conundrums. Hum Immunol 2009;70:610-617. [ Links ]
17. Cantú G, Sales F, Reyes A, Rodríguez-Ortega G, Medeiros M. En Hospitales de México: criterios de asignación de riñón de pacientes fallecidos. Persona Bioética 2009;13:20-34. [ Links ]
18. Michaels PJ, Fishbein MC, Colvin RB. Humoral rejection of human organ transplants. Springer Semin Immunopathol 2003;25:119-140. [ Links ]
19. Zhang Q, Liang LW, Gjertson DW, Lassman C, Wilkinson AH, Kendrick E, et al. Development of posttransplant antidonor HLA antibodies is associated with acute humoral rejection and early graft dysfunction. Transplantation 2005;79:591-598. [ Links ]
20. Lee PC, Zhu L, Terasaki PI, Everly MJ. HLA-specific antibodies developed in the first year posttransplant are predictive of chronic rejection and renal graft loss. Transplantation 2009;88:568-574. [ Links ]
]]>21. Billen EV, Christiaans MH, Lee J, van den Berg-Loonen EM. Donor-directed HLA antibodies before and after transplantectomy detected by the luminex single antigen assay. Transplantation 2009;87:563-569. [ Links ]
22. Stastny P, Lavingia B, Fixler DE, Yancy CW, Ring WS. Antibodies against donor human leukocyte antigens and the outcome of cardiac allografts in adults and children. Transplantation 2007;84:738-45. [ Links ]
23. Hourmant M, Cesbron-Gautier A, Terasaki PI, Mizutani K, Moreau K, Meurette A, et al. Frequency and clinical implications of development of donor-specific and non-donor-specific HLA antibodies after kidney transplantation. J Am Soc Nephrol 2005;16:2804-2812. [ Links ]
24. Morales-Buenrostro LE, Rodríguez-Romo R, de Leo-Cervantes C, López M, Pérez-Garrido J, Uribe-Uribe N, et al. HLA and MICA antibodies: further evidence of their impact on graft loss two years after their detection. Clin Transpl 2006:207-218. [ Links ]
25. Morales-Buenrostro LE, Rodríguez-Romo R, de Leo-Cervantes C, López M, Pérez-Garrido J, Uribe-Uribe N, et al. Evidence on the role of HLA and MICA antibodies in renal graft loss. Gac Med Mex 2008;144:315-322. [ Links ]
]]>26. Halloran PF, Wadgymar A, Ritchie S, Falk J, Solez K, Srinivasa NS. The significance of the anti-class I antibody response. I. Clinical and pathologic features of anti-class I-mediated rejection. Transplantation 1990;49:85-91. [ Links ]
27. Crespo M, Pascual M, Tolkoff-Rubin N, Mauiyyedi S, Collins AB, Fitzpatrick D, et al. Acute humoral rejection in renal allograft recipients. I. Incidence, serology and clinical characteristics. Transplantation 2001;71:652-658. [ Links ]
28. Burns JM, Cornell LD, Perry DK, Pollinger HS, Gloor JM, Kremers WK, et al. Alloantibody levels and acute humoral rejection early after positive crossmatch kidney transplantation. Am J Transplant 2008;8:2684-2694. [ Links ]
29. Magil AB, Tinckam KJ. Focal peritubular capillary C4d deposition in acute rejection. Nephrol Dial Transplant 2006;21:1382-1388. [ Links ]
30. Poduval RD, Kadambi P V, Josephson MA, Cohn RA, Harland RC, Javaid B, et al. Implications of immunohistochemical detection of C4d along peritubular capillaries in late acute renal allograft rejection. Transplantation 2005;79:228-235. [ Links ]
]]>31. Sis B, Halloran P F. Endothelial transcripts uncover a previously unknown phenotype: C4d-negative antibody-mediated rejection. Curr Opin Organ Transpl 2010;15:42-48. [ Links ]
32. Sis B, Jhangri GS, Bunnag S, Allanach K, Kaplan B, Halloran PF. Endothelial gene expression in kidney transplants with alloantibody indicates antibody-mediated damage despite lack of C4d staining. Am J Transplant 2009;9:2312-2323. [ Links ]
33. Lehrich RW, Rocha PN, Reinsmoen N, Greenberg A, Butterly DW, Howell DN, et al. Intravenous immunoglobulin and plasmapheresis in acute humoral rejection: experience in renal allograft transplantation. Hum Immunol 2005;66:350-358. [ Links ]
34. Jordan SC, Vo AA, Toyoda M, Tyan D, Nast CC. Post-transplant therapy with high-dose intravenous gammaglobulin: applications to treatment of antibody-mediated rejection. Pediatr Transplant 2005;9:155-161. [ Links ]
35. Pescovitz MD. The use of rituximab, anti-CD20 monoclonal antibody, in pediatric transplantation. Pediatr Transplant 2004;8:9-21. [ Links ]
]]>36. Basta M, Dalakas MC. High-dose intravenous immunoglobulin exerts its beneficial effect in patients with dermatomyositis by blocking endomysial deposition of activated complement fragments. J Clin Invest 1994;94:1729-1735. [ Links ]
37. Lutz HU, Stammler P, Jelezarova E, Nater M, Späth PJ. High doses of immunoglobulin G attenuate immune aggregate-mediated complement activation by enhancing physiologic cleavage of C3b in C3bn-IgG complexes. Blood 1996;88:184-193. [ Links ]
38. Kidney Disease: Improving Global Outcomes (KDIGO) Transplant Work Group. KDIGO clinical practice guideline for the care of kidney transplant recipients. Am J Transplant 2009;9(Suppl 3):S1-S155. [ Links ]
]]>