
Liberación de sustancias lipofílicas a partir de nanocápsulas poliméricas
Fabiola Chávez, Blanca Inés Olvera, Adriana Ganem, David Quintanar*
División de Estudios de Posgrado (Tecnología Farmacéutica), Facultad de Estudios Superiores Cuautitlán, Universidad Nacional Autónoma de México, Av. 1° de Mayo s/n, Cuautitlán Izcalli, Estado de México C.P. 54704, Tel: 5623-2065; Fax: 5871-0650. E-mail: ganemq@hotmail.com
Recibido el 8 de mayo del 2002.
Aceptado el 2 de diciembre del 2002.
Resumen
Se prepararon nanocápsulas (NC) con talla < 500 nm por la técnica de emulsificación-difusión con alta tasa de encapsulación y eficiencia del proceso. Evaluaciones isopícnicas indicaron que la proporción octil metoxicinamato:acetato ftalato de celulosa (OMC:CAP) 5:2 es la óptima para la encapsulación. La estructura vesicular de las NC fue evidenciada por una técnica directa de MEB sin uso de congelamiento y fractura. La liberación de OMC de las NC fue evaluada por la técnica de celda de permeación. Se encontró que el mecanismo de transporte es de tipo no fickiano y el tipo de liberación es dependiente del tiempo, de acuerdo al modelo semi-empírico dM / dt = ktn-1. La liberación del OMC no pudo ser descrita por un modelo tricompartimental. Los resultados indican que la liberación obedece a una cinética de primer orden.
Palabras clave: Nanocápsulas, nanopartículas, octil metoxicinamato, emulsificación-difusión, liberación de activos.
Abstract
Size < 500 nm nanocapsules (NC) were prepared using the emulsification-diffusion technique with high encapsulation rate and process efficiency. Isopycnic evaluations showed that the ratio octyl methoxicinnamate:cellulose acetate phthalate (OMC:CAP) 5:2 is the optimal for encapsulation. The NC vesicular structure was made evident by a direct MEB technique without use of freeze-fracture. The OMC release from the NC was evaluated through the permeation cell technique. It was found that the transport mechanism is non-fickian and the release rate depends on time, according to the semi-empiric model dM / dt = ktn-1. The OMC release was not described through a tricompartmental model. The results indicate that the release responds to a first order kinetics.
Key words: Nanocapsules, nanoparticles, octyl methoxycinnamate, emulsification-diffusion, drug release.
Introducción
]]> La nanotecnología es una nueva área que involucra entre otros aspectos el diseño y la manufactura de componentes con dimensiones submicrónicas. La nanotecnología está teniendo implicaciones muy importantes en diferentes áreas de la química y biología y se piensa que las próximas tres décadas estarán marcadas por espectaculares avances en dicha área [1].Una de las potenciales aplicaciones para los sistemas dispersos nanoparticulados es su uso como vectores coloidales o acarreadores de entidades químicas con actividad biológica (principios activos). Varios son los grupos de investigación que se basan en la idea de diseñar nuevos sistemas farmacéuticos con capacidad de entrega de un activo en un sitio específico, a una velocidad y régimen de dosificación óptimos [2], con lo que se podría evitar o minimizar los efectos secundarios o adversos que se presentan con frecuencia al administrar una forma farmacéutica convencional. Por medio de estos sistemas también se podría proteger la entidad química de interés y prolongar su estancia en el organismo, como ya se ha mencionado en diversas publicaciones [3-6].
En las nanopartículas (sólidos coloidales entre 10-8 y 10-7 m) podemos diferenciar dos grandes grupos: Las nanoesferas (NE) y las nanocápsulas (NC), las cuales difieren principalmente en su constitución, ya que mientras que las NE están formadas de una densa matriz polimérica, las NC se componen de una membrana polimérica que recubre un centro líquido oleoso. Desde el punto de vista farmacéutico, las NC son atractivas porque su cavidad central basada en aceite, permite un alto nivel de encapsulación para sustancias lipofílicas [7-9]. En cuanto a los métodos de preparación de NC se distinguen los siguientes: a) polimerización interfacial, que involucra una reacción de polimerización que ocurre en la interfase entre los nanoglóbulos de aceite que contienen la sustancia activa y una fase acuosa; b) desplazamiento de solvente, que consiste en disolver una fase oleosa y el polímero de recubrimiento en un solvente polar (p. ej. acetona). Esta fase se vierte a una fase acuosa bajo agitación magnética, formándose las NC debido a la rápida difusión de la fase orgánica en la acuosa, lo que provoca una emulsificación espontánea. La subsecuente agregación del polímero sobre las nanogotas de aceite provocará la formación del sistema vesicular; c) emulsificación-difusión, es un proceso en el que se forma una emulsión aceite/agua entre un solvente parcialmente soluble en agua (el cual ha sido previamente saturado y contiene disueltos al polímero y sustancia activa), y una fase acuosa saturada del solvente generalmente con uno o varios estabilizantes. La adición de agua a la emulsión provoca el rompimento del equilibrio y la salida del solvente a la fase continua con la subsecuente agregación del polímero sobre el aceite en forma de NC.
Se han utilizado varios métodos para evaluar la liberación in vitro de la entidad contenida en los sistemas nanoparticulados, pudiéndose mencionar: i) difusión en celdas con membranas artificiales o biológicas, ii) técnica de difusión en bolsas de diálisis, iii) técnica de saco de diálisis inversa, iv) ultra-centrifugación, v) ultrafiltración y vi) técnica de centrifugación-ultrafiltración.
En 1994, Kreuter y cols. [2] mencionan que el mecanismo de liberación, coeficiente de difusión, velocidad de biodegradación y medio biológico son los factores principales que determinan la velocidad de liberación del activo.
Del estudio de la liberación de sustancias incluidas en NC resaltan dos grandes propuestas: a) que la liberación se lleve a cabo por un proceso de difusión y b) que se lleve a cabo por un proceso de erosión y ruptura de la pared polimérica de las NC. En el presente estudio se utilizaron celdas de permeación vertical tipo Franz para determinar el mecanismo y tipo de liberación de un modelo de molécula activa (filtro solar), para lo cual se prepararon lotes con diferentes cantidades de polímero como material membrana, sin y con la adición de plastificante.
Resultados y discusión
Los lotes de NC preparados por la técnica de emulsificación-difusión presentaron una alta eficiencia del proceso (no hay formación de agregados) y una alta tasa de encapsulación del octil metoxicinamato (OMC), pues durante los lavados correspondientes no se presentó aceite sin encapsular, lo que nos indica que prácticamente todo el polímero y el filtro solar se transformaron en NC. La talla de partícula promedio se muestra en la Tabla 1, donde se observa que la cantidad de polímero y la adición de plastificante producen tan sólo pequeños cambios en la talla de partícula.
La forma real de las NC puede observarse claramente en la Fig. 1, donde queda de manifiesto la estructura vesicular de este tipo de sistemas, pues en el acercamiento es posible visualizar la cavidad que había sido ocupada por aceite. Es importante señalar que es la primera vez que se revela la estructura capsular de las NC por un método de microscopía electrónica de barrido (MEB) sin recurrir a métodos de criofractura. De acuerdo al mecanismo propuesto por el método de emulsificación-difusión [8-9], la formación de las NC se debe a que durante el paso de difusión del solvente (parcialmente miscible al agua), se forman regiones locales de super-saturación en la interfase glóbulo / medio de disolución de la emulsión o/w previamente obtenida, de donde se desprenden nuevos glóbulos ("protonanopartículas") que son estabilizados por el alcohol polivinílico (PVAL), produciéndose el acomodo del polímero en torno al aceite, lo que da como resultado la estructura vesicular del sistema al término de la difusión.
]]>
Con la finalidad de seleccionar el método de evaluación para la liberación, se realizaron tanto ensayos por ultracentrifugación como por celda de permeación. La Fig. 2 muestra la tendencia obtenida al trabajar con las NC cargadas de solución oleosa saturada de colorante violeta no. 2. En este caso, el método de ultracentrifugación resultó ser invasivo para los sistemas vesiculares. La tendencia prácticamente constante podría ser explicada por las condiciones usadas en la obtención de las muestras. Con 20,000 rpm durante 10 min se indujo la ruptura de la membrana nanocapsular de los sistemas, resultando así, la liberación rápida del colorante; sin embargo, de no hacerlo de esa forma, no se habría separado la pastilla del sobrenadante para tomar la muestra.

Debido a lo expuesto anteriormente, la ultracentrifugación no fue un método adecuado para seguir la liberación del activo encapsulado, por lo que se optó por el método de celdas de permeación verticales tipo Franz, el cual resulta ser un método no invasivo ya que permite la difusión del permeante a través de una membrana sin afectar la estructura de la membrana polimérica de la NC.
El método de densidad isopícnica (utilizando marcadores de densidad conocida) permitió conocer la proporción OMC:CAP con la que se obtiene la óptima encapsulación del filtro solar, siendo la proporción 5:2 la adecuada para la encapsulación del aceite, pues cantidades mayores de OMC revelaron que una parte del aceite se encontraba libre [10]. Por lo tanto se prepararon 4 sistemas con 0.2, 0.3, 0.5 y 0.8 g de CAP, respectivamente.
Los perfiles de liberación en porcentaje de OMC se muestran en las Figs. 3 y 4, para todos los sistemas trabajados. Como puede verse, la forma exponencial de las curvas, indica que no se tuvo una liberación de orden cero, además, la diferencia para los 4 sistemas pudiera asociarse al grosor de la pared nanocapsular. Es decir, que a mayor cantidad de polímero, la pared fue más gruesa y por ende, la cantidad liberada a un cierto tiempo resultó menor con respecto a los sistemas con menor proporción de CAP. Esto pudo apreciarse mejor alrededor de las 200 h de iniciada la liberación. Cabe señalar que la disminución en la velocidad de liberación al transcurrir el tiempo, puede ser explicada por un decremento en el gradiente de concentración de OMC que se genera entre el interior de las NC y el medio de disolución, quedando de manifiesto que el proceso de difusión es esencial en la liberación. Otro aspecto importante es que cerca de las 400 h, las curvas presentaron la tendencia a igualarse para todos los sistemas, y esto podría sugerir que al mismo tiempo que se presentó el proceso de difusión, se llevó a cabo la degradación y ruptura del polímero constituyente de la pared nanocapsular. De esta manera, hacia el final de la liberación, tal proceso fue el responsable de la salida del filtro solar contenido en los sistemas antes señalados.


Los sistemas que contenían al agente plastificante (dibutil sebacato o DBS), se comportaron prácticamente de la misma forma, y solo podemos señalar que los puntos iniciales en las curvas, hacia la mitad de la liberación, guardaron una tendencia lineal más uniforme.
Al analizar los resultados con el modelo semi-empírico que se muestra en la ecuación 1 [11-12], en el que se toman en cuenta los datos hasta el 60 % de la cantidad total liberada, se obtuvieron las Figs. 5 y 6, que muestran una tendencia lineal en todos los casos.



Recordando que dMt / dt representa la velocidad de liberación, k es una constante y t es el tiempo; el valor obtenido para el exponente difusional n de dicho modelo, es el que proporciona información acerca del mecanismo y tipo de liberación implicados tal y como se muestra en la Tabla 2 [9]. De acuerdo a los valores de la Tabla 3 y a lo estipulado por dicho modelo en la Tabla 2, este exponente tuvo un valor entre 0.6 y 1.0 en todos los casos, por lo que se puede decir que el mecanismo propuesto es no fickiano (anómalo), y el tipo de liberación es dependiente de una fracción del tiempo. La diferencia que produjo la adición del DBS a cada sistema fue un pequeño aumento en el valor de n en todos los casos, sugiriendo que podría existir una proporción adecuada CAP-DBS que controlaría la liberación en esta primera parte del proceso, pudiéndose llegar a un orden cero (n = 1) y que por lo tanto la liberación fuera independiente del tiempo (caso II). Cuando los resultados de la liberación fueron tratados con un modelo utilizado en sistemas matriciales, el modelo de Higuchi (ecuación 2), donde Mt corresponde a la cantidad de activo liberada al tiempo t y k es una constante, se obtuvieron las Figs. 7 y 8, así como la Tabla 4, donde se pudo observar que no existe una tendencia lineal en los sistemas trabajados.
]]>



Se puede decir que este modelo no describe adecuadamente el proceso de difusión que ocurre del interior de las NC hacia el medio de disolución, pues en nuestro caso, la cantidad liberada (Mt) no depende de la raíz cuadrada del tiempo, como sucede en un dispositivo matricial, en el cual, el grosor de la capa hidrodinámica de difusión va en aumento al transcurrir el tiempo.
En un estudio de la liberación de sustancias contenidas en NC realizado por Ammoury y cols. en 1989 y 1990 [13-15], se consideró un sistema tricompartimental donde el fármaco se disuelve o divide entre las fases lipofílica e hidrofílica de un sistema disperso, pero separado de la solución "sink" (solución con una concentración del activo menor al 15% de su solubilidad en el medio de disolución) por una membrana de diálisis la cual no es paso limitante del proceso general. Se asume que la difusión del activo a través de la membrana obedece la primera ley de Fick. Las características matemáticas del modelo se basan en asumir que el principio activo se reparte en tres compartimientos, los cuales son: las nanocápsulas, la fase acuosa interna y la solución "sink" (donde se toman las muestras). La ecuación 3 corresponde a dicho modelo, donde k12 es la constante de velocidad de partición de primer orden entre la fase interna oleosa y la fase externa acuosa en el compartimiento donador ó la constante de liberación de primer orden del activo a través de la delgada membrana de polímero de las NC; k23 es la constante de velocidad de primer orden de permeación a través de la membrana; M es la masa; C es la concentración y V es el volumen (referido a un compartimiento en particular); 0 se refiere al tiempo cero y ∞ al tiempo infinito. Los símbolos α y β se definen de acuerdo a las ecuaciones 4 y 5.

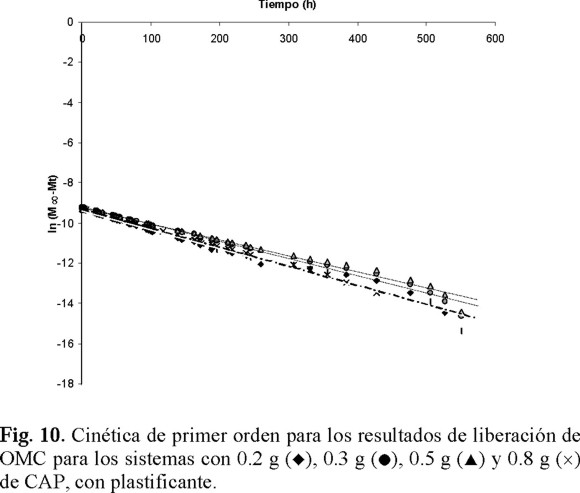
En cuanto al tipo de cinética a la que se ajustaron nuestros resultados, se encontró que corresponden a una cinética de primer orden, como lo muestran las Figs. 9 y 10. Esto implica que la liberación de la sustancia lipofílica modelo depende de la concentración del mismo en el sistema. Cabe señalar que se obtuvo una pequeña disminución en el valor de la constante de primer orden en los sistemas que incluían plastificante respecto a los que no lo contenían (Tabla 5), posiblemente debido a que el DBS le confirió mayor resistencia mecánica a la pared nanocapsular, con lo que se retrasó la ruptura de dicha pared.

Parte experimental
Preparación de los lotes de NC
Se prepararon lotes de NC con y sin plastificante, por la técnica de emulsificación-difusión recientemente patentada por Quintanar-Guerrero y cols. [9] y comentada en la introducción. Brevemente, se emulsificaron 20 mL de una solución de CAP y OMC en butanona (Fluka, USA) saturado de agua, en 40 mL de una solución acuosa de PVAL (Mowiol 4-88, Glomarza, México) al 5 %. La dispersión se agitó por 10 minutos a 2500 rpm con agitador de propela de hélice convencional. Se agregaron 80 mL de agua sin saturar para provocar la difusión y la agregación de las NC. Se utilizaron diferentes cantidades de CAP: 0.2, 0.3, 0.5 y 0.8 g (Vita Drug S.A. de C.V., México) y una fija (0.4 mL) de OMC (Escalol 557, Multiquim, México). Para las NC con DBS (Helm de México), éste se adicionó en un 20% (p/p) con respecto a la cantidad de polímero en la fase orgánica. Una vez obtenidas las NC, el exceso de agua y el solvente orgánico fueron eliminados a presión reducida. Se realizaron 3 lavados sucesivos por ultracentrifugación y las NC se diluyeron en un volumen total de 10 mL con agua destilada. La talla de partícula se determinó por medio del Nanosizer N4 Plus, CoulterTM (Florida, USA).
]]> Las NC cargadas de violeta no. 2 (sólo lotes sin plastificante) se prepararon de acuerdo al proceso antes descrito, utilizando 0.5 mL de solución saturada de colorante violeta no. 2 (D&C violeta no. 2, Kingfisher® Colours, England) en Miglyol® 840 (propilenglicol dicaprilato / caprato, Hüls AG, Germany); 400 mg del polímero biodegradable ácido poliláctico-coglicólico (PLGA, Resomer® RG 502, 50:50 Boehringer Ingelheim, Germany) en 30 mL de acetato de etilo (J. T. Banker Analized® Reactivo, USA) saturado con agua y 60 mL de PVAL 5 % (p/v) en agua saturada de acetato de etilo.Determinación de la proporción OMC:CAP óptima
Se determinó la densidad experimental de OMC (1.03 g / cm3) y de CAP (1.11 g / cm3) por el método de igualación de densidades con sistemas de glicerina:agua en diferentes proporciones. Se preparó un sistema de proporción 30:70 con densidad intermedia (1.08 g / cm3), con el fin de determinar la proporción OMC:CAP para obtener la óptima encapsulación del filtro solar en el polímero por el método isopícnico. Se utilizaron tubos de centrífuga en los cuales se colocó una pequeña cantidad de diferentes lotes de NC, se centrifugaron durante 3 h a 15,000 rpm en la ultracentrífuga OptimaTM LE-80K (Beckman, USA) y se observó en cual sistema no se presentaba aceite sin encapsular.
Microscopía electrónica de barrido
En la obtención de las micrografías las partículas se sometieron a estrés para provocar su ruptura. Se realizó la fijación de las NC adsorbidas en membranas de 0.22 µm (Millipore, USA), sumergiéndolas en tetróxido de osmio al 1 % durante 2 h, seguido de la deshidratación en gradientes de etanol (70, 80, 90 y 100 %). Después se realizó el recubrimiento con oro (≅ 20 nm) y se observaron las NC con el Microscopio Electrónico de Barrido JSM-25 SII (JEOL, Japón). La técnica fue optimizada en un trabajo previo (16).
Estudios de liberación
Liberación de colorante por ultracentrifugación
Se colocaron simultáneamente 10 sistemas con 330 µL de la suspensión de NC (llevándolos a 7 mL con Tween ® 80 al 20 %; Polisorbato 80, ICI Surfactants) en agitación magnética moderada a 37 °C. Las muestras fueron obtenidas centrifugando a 20,000 rpm durante 10 min. El sobrenadante se leyó en un Espectrofotómetro DU®-64 (Beckman, USA) a λ = 582 nm (longitud de máxima absorción para violeta no. 2).
Liberación de filtro solar por celda de permeación
Los ensayos de liberación de OMC se llevaron a cabo en una celda de permeación estática bicompartimental vertical tipo Franz (Fig. 11). En el compartimiento donador se adicionaron las NC en 2 mL de solución de Brij® 58 (polioxietilen(20)cetil éter) al 5 % (p/v); por su parte, el compartimiento receptor contenía un volumen de 2 mL del medio de disolución, Brij 58 al 5 %. Ambos compartimentos estaban separados por una membrana de 0.1 µm de poro (Advantec MFS, Inc., Japón), lo que permitió el paso de la sustancia liberada sin que las NC pudieran atravesarla. Las celdas se mantuvieron en un baño de agua a 37 °C, con agitación magnética constante a una velocidad moderada. Las muestras fueron colectadas tomando todo el volumen del compartimiento receptor (mismo que se reponía en cada ocasión) y fueron leídas en el espectrofotómetro a = 305 nm (longitud de onda de máxima absorción del OMC), usando como blanco el mismo medio de disolución. Todas las proporciones fueron analizadas por triplicado.
]]>
Conclusiones
Se optimizó la técnica de emulsificación-difusión para encapsular el filtro solar OMC, observándose que la proporción OMC:CAP 5:2 es la adecuada para obtener una alta tasa de encapsulacion y eficiencia del proceso. La talla de partícula promedio indica que todos los sistemas miden menos de 500 nm. La estructura vesicular de estos sistemas fue evidenciada por primera vez por una técnica de MEB por fijación con tetróxido de osmio sin requerir criofractura de la dispersión. En ensayos de liberación, el método de ultracentrifugación resultó ser invasivo para las NC. La liberación de OMC llevada a cabo por el método de celda de permeación vertical tipo Franz no obedece al modelo tricompartimental, ni a una liberación del tipo de sistemas matriciales (del modelo de Higuchi, t1/2). El valor de n del modelo semi-empírico indica un mecanismo de liberación de tipo no fickiano (anómalo) y una liberación dependiente de una fracción del tiempo. Por otro lado, los resultados se ajustan a una cinética de liberación de primer orden, dependiente de la concentración de OMC en el sistema. La variación en la cantidad de OMC liberado de los distintos sistemas, sugiere que la proporción de polímero influye en el grosor de la pared nanocapsular y que por lo tanto, a mayor cantidad de CAP se tiene una membrana nanocapsular más gruesa. La adición del plastificante (DBS), durante el proceso de formación de las NC produjo disminución en el valor de la constante de primer orden, retrasando la liberación del filtro solar.
Agradecimientos
Los autores agradecen a CONACyT (proyecto J27741-M) y a la UNAM (proyecto PAPIIT IN214000) por el apoyo para la realización de este proyecto. Asimismo agradecemos la asistencia técnica del Sr. Rodolfo Robles de la Sección de Microscopía Electrónica de la FES Cuautitlán y al Ing. Draucin Jiménez del taller de soplado de vidrio de la FES Cuautitlán.
Referencias
]]>1. Drexler K. Nanotechnology (Engines of creation), Anchor Books, New York, 1986. [ Links ]
2. Kreuter J., in: Colloidal Drug Delivery Systems, Kreuter J., Ed., Marcel Dekker, Inc., New York, USA, 1994, 219-315. [ Links ]
3. Damgé C.; Michael C.; Aprahamian M.; Couvreur P.; Devissaguet J. P. J. Control. Rel. 1990, 13, 233-239. [ Links ]
4. Lowe J .P.; Temple S. C. J. Pharm. Pharmacol. 1994, 46, 547-552. [ Links ]
5. Aboubakar M.; Couvreur P.; Pinto-Alphandary H.; Gouritin B.; Lacour B.; Farinotti R.; Puisieux F.; Vauthier C. Drug Dev. Research 2000, 49, 109-117. [ Links ]
]]>6. Fawaz F.; Bonini F.; Guyton M.; Lagueny A. M.; Fessi H.; Devissaguet J. P. Int. J. Pharm. 1996, 133, 107-115. [ Links ]
7. Quintanar-Guerrero D.; Allémann E.; Fessi H.; Doelker E. Drug Dev. Ind. Pharm. 1998, 24, 1113-1117. [ Links ]
8. Quintanar-Guerrero D. Tesis Doctoral N° 2950 Universidad de Ginebra, Suiza, 1997.
9. Quintanar-Guerrero D.; Allémann E., Fessi H.; Doelker E. French Patent Appl. 97 09 672 1997. [ Links ]
10. Olvera M. B.; Villalobos G. R.; Escobar Ch. J. J.; López C. M.; Ganem R. A.; Quintanar G. D. Rev. Mex. Cien. Farm. 2001, 32, 81. [ Links ]
11. Masaro L.; Zhu X. Prog. Polym. Sci. 1999, 24, 731-775. [ Links ]
12. Narasimhan B.; Mallapragada S. K.; Peppas N. A., in: Encyclopedia of Controlled Drug Delivery, Vol. 2, Mathiowitz, E., Ed., John Wiley & Sons., Inc., New York, 1999, 921-935. [ Links ]
13. Ammoury N.; Fessi H.; Devissaguet J. P.; Puisieux F.; Benita S. J. Pharm. Sci. 1990, 79, 763-767. [ Links ]
14. Ammoury N.; Fessi H.; Devissaguet J. P.; Puisiex F.; Benita S. Proceed. Intern. Symp. Control Rel. Bioact. Mater., 1989, 16, 544-545. [ Links ]
15. Ammoury N.; Fessi H.; Devissaguet J. P.; Puisiex F.; Benita S. S. T. P. Pharma 1989, 5, 647-651. [ Links ]
16. Chávez-Monroy F., Tesis Licenciatura QFB Facultad de Estudios Superiores Cuautitlán-UNAM, 2002.
]]>