Estimación de la permeabilidad al vapor de agua en películas a base de quitosán
Verónica Trejo, Nidia Aragón y Patricia Miranda*
Sección de Biotecnología, Coordinación General de Estudios de Posgrado, Facultad de Estudios Superiores Cuautitlán, Universidad Nacional Autónoma de México, Av. Quetzalcóatl s/n, Campo 1, Cuautitlán Izcalli, Estado de México 5474, México.
Recibido el 6 de noviembre del 2000.
Aceptado el 8 de diciembre del 2000.
Resumen
El quitosán como componente estructural forma películas hidrofílicas con propiedades de permeabilidad deficientes para ser empleadas en la industria de alimentos; el presente trabajo tiene como objetivo estimar la permeabilidad al vapor de agua en películas de quitosán modificadas con sorbitol y polietilenglicol al 0.7 y 1.4 %, y ácido esteárico y láurico al 0.3 y 0.8 %. Aplicando el método modificado de Mc-Hugh, el índice de permeabilidad con relación al peso, grosor y área; tanto las presiones parciales corregidas como el grosor afectan la permeabilidad. Las películas obtenidas con soluciones de quitosán al 2 % más sorbitol 0.7 % muestran una permeabilidad al vapor de agua (WVP) de 2.539 g mm / m2 kPa, más adecuada para su uso.
Palabras clave: Quitosán, películas hidrofílicas, permeabilidad, vapor de agua.
Abstract
Chitosan as structural component of hydrophilic films shows deficient permeability properties for its application in the food industry. The objective of this contribution is to estimate the permeability to the water vapor in modified chitosan films containing sorbitol and polyethylene glycol at concentrations of 0.7 and 1.4 % as well as stearic and lauric acids at 0.3 and 0.8 %. Applying the modified method of Mc-Hugh, the permeability coefficient considered weight, thickness and area; the corrected water vapor partial pressures and thickness affect the permeability. The 2.539 g mm / m2 kPa water vapor permeability of chitosan films obtained from 2 % chitosan solutions containing 0.7 % sorbitol was the most adequate for its application.
Keywords: Chitosan, hydrophilic films, permeability, water vapor.
Introducción
]]> El quitosán como material alternativo de películas flexibles biodegradables presenta propiedades funcionales similares a las tradicionales derivadas de productos petroquímicos (polietileno, polivinilo). Tanto el quitosán como otros polímeros son capaces de actuar como barreras selectivas entre el medio y el alimento generando ambientes modificados en cuanto a la concentración de gases y vapores (vapor de agua, oxígeno, etileno etc.). Sin embargo la permeabilidad al vapor de agua no es una de las propiedades inherentes de estas películas de tipo hidrofílico, las cuales tienden a retener el agua en su estructura lo cual conduce al hinchamiento de la misma, generando un funcionamiento ineficiente [1]. Debido a esto, se ha optado por integrar a su estructura agentes plastificantes y ácidos grasos, impartiendo con ello flexibilidad a la vez que se incrementa la movilidad del polímero, implicando con ello la modificación en los valores de permeabilidad al vapor de agua. El presente estudio tiene por objeto evaluar la permeabilidad al vapor de agua WVP de películas elaboradas a partir de una solución de quitosán al 1 y 2 %, de soluciones de quitosán al 1 y 2 % más sorbitol y polietilenglicol a dos concentraciones 0.7 y 1.4 %, y de soluciones de quitosán al 1 y 2 % más los ácidos grasos esteárico y láurico a concentraciones de 0.3 y 0.8 %.
Antecedentes
El quitosán es un poliaminosacárido lineal de alto peso molecular, cuyos grupos funcionales están disponibles para reacciones químicas; se comporta como un polielectrólito en agua a pH's ácidos, ya que presenta una alta densidad de carga positiva atribuida a las unidades de glucosamina, por lo que interactúa fuertemente con estructuras aniónicas como: proteínas, polisacáridos y otras moléculas de carga negativa [2].
Para la formación de las películas se debe garantizar la total solubilidad del quitosán en agua acidificada [3].
Las películas empleadas como empaques para alimentos deben cumplir con características básicas de transferencia de vapor de agua y de gases. A este respecto se plantean dos mecanismos de transferencia de masa: el fluído capilar y el de difusión activada; en el primer caso las moléculas permeantes pasan a través de un medio altamente poroso, a diferencia de la difusión activada en donde la solubilización de los agentes penetrantes es bajo un gradiente de concentración, por lo que en estas películas el transporte de masa incluye la adsorción, la difusión y la desorción [4]. Este fenómeno para el caso de películas de quitosán ha sido poco estudiado, por lo que se requiere integrar el conocimiento de transferencia en películas hidrofílicas, considerando la ley de Fick y la ley de Henry, arribando con ello al cálculo de permeabilidad al vapor de agua a través del método modificado de Mc-Hugh [5].
Metodología
Para evaluar la permeabilidad al vapor de agua (WVP) se seleccionó el método desecante de la técnica gravimétrica de la ASTM E-96,88, modificada por Mc-Hugh y colaboradores en 1993, en la cual indirectamente se obtiene la permeabilidad cuantificando el índice de movimiento de vapor de agua a través de la película mediante los cambios de peso debido a la transferencia de humedad. En esta técnica se cuenta con dos cámaras: la de ambientación y la de prueba, previo a la determinación de la WVP fue necesario realizar la implementación de ambas cámaras.
Cámara ambiental
]]> De acuerdo a lo establecido en la técnica modificada de Mc-Hugh se definieron las condiciones de operación: 1) velocidad de aire 182 m / min. (500 ft / min.); 2) Temperatura 23-32 °C; 3) Humedad Relativa (HR) 95 ± 2 %. Se implementó una cámara (sellada) hermética de 40 cm de ancho × 40 cm de alto y 40 cm de profundidad, a la cual se le adaptó un ventilador marca Rotron modelo MXA-3 de tipo axial en la parte superior central, con impulso de aire hacia la parte posterior, las velocidades de aire alcanzadas se monitorearon en cuatro puntos diferentes de la cámara con la ayuda de un anemómetro , obteniéndose un perfil de velocidades de aire de la cámara por un período de 4 h.El registro de temperatura se manejó con un higrotermómetro, el cual se instaló en la pared derecha en el primer tercio de la cámara, se tomaron lecturas cada media hora por 8 h.
De forma consecuente se monitoreó la humedad relativa (HR), sin embargo para lograr 95 ± 2 % fue necesario un abastecimiento continuo de agua para obtener esta condición, se cubrieron las paredes de la cámara con telas absorbentes y se instaló una manguera calibre 0.003 × 0.006 m perforada cada 10 cm en la periferia superior, la administración de agua fue manual, lográndose así la humedad relativa especificada.
Cámara de Prueba
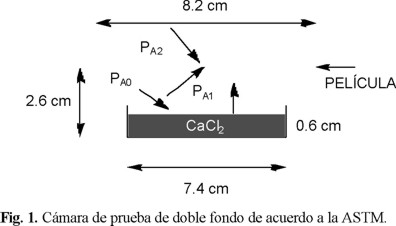
Según especificaciones de la ASTM E-96,88 [6]; se optó por el diseño de caja de doble fondo con área de 8.2 cm2, de profundidad total 2.6 cm, usando como bastidor una banda de caucho de 1.5 cm de ancho.

Para la construcción de la cámara se utilizó plexiglas de 3 mm de espesor, cumpliendo con las características deseadas de ser no corrosivo, resistente, impermeable al agua y ligero.
La película se sujetó a la cámara de prueba colocando el bastidor y sellando con silicón para mantener las condiciones de hermeticidad dentro de la caja de prueba y 0 % de humedad relativa (HR), adicionando previamente al sellado cloruro de calcio anhidro (CaCl2) tamizado y secado a peso constante a 200 °C.
Elaboración de las películas
Para la preparación de las películas se elaboraron soluciones de quitosán a dos concentraciones 1 y 2 % (p/v), utilizando quitosán extraído a partir de caparazón de camarón, obtenido por la técnica de desacetilación química [7]. Para obtener una disolución de quitosán al 1 y 2 %, se disolvió éste en ácido acético al 1 %, con ayuda de un agitador magnético por 15 min. En algunos casos fue necesario centrifugar la disolución para eliminar el aire incorporado. Posteriormente se vertieron 20 ml de la disolución de quitosán sobre una placa de acrílico de 9 mm de espesor y un área de 12.3 cm2 previamente lavada con alcohol y colocada en una superficie nivelada con el objeto de obtener un grosor homogéneo. Las disoluciones de quitosán proyectadas sobre el acrílico se dejaron secar por 8 h a temperatura ambiente y humedad relativa de 55 % obteniéndose de esta forma las películas. En el caso de las películas elaboradas con quitosán más los agentes modificadores de la estructura, se procedió de forma similar, se elaboraron las soluciones de quitosán y posteriormente se adicionó sorbitol y polietilenglicol a concentraciones de 0.7 y 1.4 % (p/v) para el sorbitol y (p/p) para el polietilenglicol. Estas mezclas se homogenizaron por 20 min con agitador magnético; los ácidos esteárico y láurico, se incorporaron a concentraciones de 0.3 y 0.8 % (p/v). De igual forma 20 ml de estas mezclas se vertieron en placas de acrílico y se dejaron secar bajo las condiciones anteriores. Posteriormente las películas formadas se desprendieron con ayuda de una navaja, valorándose su grosor y peso. Para el primero con ayuda de un vernier (0.001 in de precisión), se tomaron cuatro mediciones por película obteniéndose la media. Para la determinación de los pesos se usó una balanza analítica. Inmediatamente después fueron transferidas a la cámara para iniciar la valoración de la permeabilidad (WVP).
]]> Determinación de la WVPSellada la cámara de prueba con la película, se colocó en la cámara ambiental a las condiciones estandarizadas de humedad relativa, T° y velocidad de aire; la cámara de prueba fue extraída rápidamente de la ambiental registrando la ganancia de peso, después de haberse establecido el estado estacionario aproximadamente durante 2 h. La toma de lecturas fue cada 2 h hasta cubrir 12 h.
Los datos fueron tratados y sustituidos en la siguiente secuencia de ecuaciones [5]:

En donde:
WVTR o CTVA = Indice de transferencia al vapor de agua o coeficiente de transmisión de vapor de agua
dm / dt = Flux = diferencia de masa a través del tiempo
A = área de la película

En donde:
]]> PA2 = presión sobre la película que ejercen las condiciones de la cámara ambiental, kPaPA1 = presión a la cual esta sujeta la película al interior de la cámara de prueba, kPa

En donde:
PA0 = presión que se ejerce en la superficie del CaCl2 como resultado de la temperatura y aw del mismo
R = constante universal de los gases
T = temperatura experimental en K
Z = Δ Z altura de aire estancado entre la película y el desecante
D = difusividad a la T experimental, m/s

Resultados
La ASTM asume que la resistencia a la transferencia de masa en la cámara de prueba es despreciable en ambos lados de la película, en el caso de las películas hidrofílicas esto es falso, ya que presentan una baja transferencia, por lo que se induce la convección del aire a velocidades de 182 m / min [8]. La media de los datos de la cámara de ambientación en dos sitios, posterior izquierda y derecha fueron de 199.9 y 201.4 m / min. respectivamente, con desviaciones estándar de 0.18 a 0.29.
Respecto a la temperatura, la variación de los datos fue de 24-36.6 °C, quedando en el intervalo establecido por la norma ASTM, E-96,88. La HR registrada varió entre 90-97 con una media de 95.8 %, siendo evaluada cada 10 minutos completando 30 datos, quedando establecido el acondicionamiento de la cámara ambiental: velocidad de aire 200.6 m / min, T° 24.7 ± 10 °C, y HR 95 ± 2 %.
Referido a la cámara de prueba el acondicionamiento quedó sujeto al manejo del desecante a peso constante (4 h), y la forma en que se sujetó la película a evaluar en primera instancia con el bastidor de polimetilmetacrilato y posteriormente con una banda de plástico flexible de 1 cm de grosor.
Valoración de la permeabilidad al vapor de agua
En la determinación de la permeabilidad al vapor de agua WVP y habiendo optado por el método modificado de Mc-Hugh [5], se obtiene la WVP cuantificando el índice de movimiento o transferencia de vapor de agua a través de la película mediante los cambios de peso, realizando una regresión lineal de la ganancia de peso vs. tiempo y calculando la pendiente, misma que al dividirse entre el área de la película resulta el WVTR (índice de permeabilidad al vapor de agua) consecuentemente el cociente que resulta de dividir el WVTR entre las presiones parciales define la Permeanza, misma que al multiplicarse por el espesor dará la WVP.
Para el cálculo de la permeabilidad al vapor de agua (WVP) de películas hidrofílicas, se conceptuaron 3 etapas: la primera definida a través del índice o coeficiente de difusión en donde el agua es adsorbida de la zona de más alta HR externa difundiéndose hacia la película. La segunda sucede al integrarse a ésta, generándose una diferencia de presiones parciales en la estructura de la misma (matriz), en donde influye principalmente el grosor y el área de la película. En la tercera fase se da el fenómeno de desorción, considerando el área de la lámina en donde se presenta la menor HR interna. De tal manera se iniciará la discusión del WVTR índice o coeficiente de difusión; dado que para cada película en particular se tienen diferentes características dependiendo de sus componentes en este caso quitosán solo, quitosán más sorbitol y PEG, quitosán más ácidos grasos estéarico y láurico.
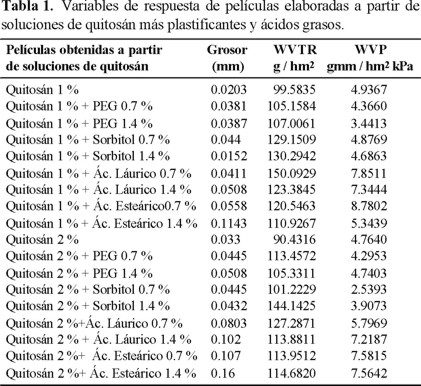
Para las películas obtenidas a partir de una solución al 1 y 2 % de quitosán se obtuvieron grosores del orden 0.01 a 0.16 mm, (Tabla 1) coincidiendo con lo citado en la bibliografía en donde se reportan grosores de 0.017 mm para películas laminadas de quitosán; sin embargo, no se define la concentración de quitosán empleada para su preparación [9].
]]>
Cuando se trata de películas obtenidas de una solución de quitosán 1 % cuya estructura fue modificada con polietilenglicol a concentraciones de 0.7 y 1.4 % los grosores fueron de 0.038 mm; mientras que para quitosán a la concentración 2 % en promedio el valor fue de 0.047 mm. Al incorporar sorbitol los grosores obtenidos fueron de alrededor de 0.0367 mm.
En el caso de los ácidos grasos (estéarico y láurico) a ambas concentraciones y con soluciones de quitosán al 1 % los grosores fueron de 0.04 hasta 0.1 mm; situación similar se presentó con soluciones de quitosán al 2 % en donde los valores varían de 0.08 a 0.16 mm.
Es importante señalar la relación del grosor con el coeficiente o índice de permeabilidad, ya que el grosor se modifica cuando se utilizan plastificantes o ácidos grasos; es decir que aunque el objetivo era disminuir el grado de hidrofílicidad el resultado final de la conformación polimérica fue diferente para cada caso.
Así los índices de permeabilidad al vapor de agua se observaron dentro del intervalo 90.43-150.09 g / hm2 (Tabla 1); sin embargo, el WVTR de las películas de quitosán 1 y 2 %, se incrementó con la incorporación del plastificante, destacando la de quitosán más sorbitol al 1.4 %, ya que este es un poliol con varios grupos funcionales, lo que implica un mayor grado de reacción con la cadena polimérica debido a su habilidad de reducir enlaces de hidrógeno internos, reduciendose así las fuerzas intermoleculares e incrementando la movilidad de las cadenas del quitosán, todo esto influyendo en la modificación estructural de la red polimérica permitiendo el libre paso de agua generando con ello el fenómeno de adsorción [10].
Para el caso de PEG 0.7 % con solución de quitosán al 1 % en el que parece que los sitios de acción fueron menores, reduciendo la distribución molecular a lo largo de la matriz de quitosán, lo que supone un menor acomodo y por lo tanto una reducción de fuerzas intermoleculares en comparación con el Sorbitol al 1.4 %. Sucedió lo mismo al observar los valores de Quitosán 2 % con PEG 0.7 % y 1.4 %, aunque el grosor fue ligeramente mayor, se expresó el aumento en el índice de permeabilidad, en otras palabras disminuyó la barrera para el paso del agua [11].
Los ácidos grasos debido a su naturaleza hidrofóbica, tienen la función de bloquear el transporte de humedad a través de la película, impartiendo no solo hidrofobicidad a la misma, sino incluso formando grandes intersticios a lo largo de la cadena polimérica constituyendo una red complicada debido a las diferentes posibilidades de interaccionar con el quitosán [12].
Las películas de quitosán más ácidos tanto láurico como esteárico presentaron un efecto antiplastificante sobre las mismas, realzando el efecto de quebrantamiento y opacidad de éstas [13].
Respecto al índice de permeabilidad para las películas con ácidos grasos se notó un comportamiento inversamente proporcional con el grosor casi en todos los casos, es decir a menores grosores se incrementó el WVTR (Tabla 1); este efecto se atribuye a las propiedades fisicoquímicas de los componentes en este caso ácidos grasos y quitosán, si bien está reportado que la composición de una película, la orientación de las moléculas y el acomodo estructural que se dé en la formación de la misma, son determinantes para su interacción con el vapor de agua [14].
La permeanza es la expresión en algunos casos de la permeabilidad al vapor de agua cuando se observa una variabilidad marcada en los grosores de las películas, ya que está definida a través del índice de permeabilidad al vapor de agua dividido entre las presiones parciales al interior de la película [15]. Las concentraciones tanto de ácido graso y quitosán realzan el efecto del grosor y consecuentemente las barreras para el paso del agua serán mayores por lo tanto el WVTR se vió disminuido (Tabla 1).
]]> El resultado final del fenómeno de permeabilidad al vapor de agua en las películas de quitosán más plastificantes fueron de 2.53 a 4.87 g mm / hm2 kPa, siendo los valores más altos en las películas obtenidas a partir de soluciones de quitosán al 1 % más sorbitol 0.7 % y soluciones de quitosán al 2 % más PEG al 1.4 % (Tabla 1).A diferencia de los datos obtenidos para los índices o coeficientes de permeabilidad, los valores de WVP's de las películas de quitosán más ácidos grasos tienen una relación directamente proporcional con el grosor coincidiendo con lo descrito por Mc-Hugh y [16], Tabla 1.
Los valores de permeabilidad variaron de 5.34 a 8.78 g mm / hm2 kPa; resaltando el valor de WVP para películas preparadas con soluciones de quitosán al 1 % y ácido esteárico al 0.3 % las cuales dan el valor mas alto.
Al comparar los valores de permeabilidad al vapor de agua, de películas con quitosán más ácidos grasos, el efecto en la disminución de la misma, en ninguno de los casos se presenta a humedades relativas altas, coincidiendo con lo establecido por algunos autores [16].
En términos generales se puede decir que la permeabilidad al vapor de agua en películas a base de quitosán se ve incrementada con la adición de agentes plastificantes y ácidos grasos comparadas con las películas de quitosán.
Conclusiones
1. El método modificado de Mc-Hugh 1993 permitió la valoración adecuada en tiempos y movimientos de las películas elaboradas a base de soluciones de quitosán.
2. El grosor de las películas de quitosán más plastificantes es proporcional al WVTR.
3. Para las películas de quitosán más ácidos grasos, la relación con el grosor es inversa al WVTR.
]]> 4. La permeabilidad al vapor de agua de las películas de quitosán se incrementa notablemente con la adición de los ácidos grasos.5. La adición de sorbitol y polietilenglicol a las películas de quitosán modifica las características físicas y por tanto los índices de permeabilidad al vapor de agua (WVTR)
6. La permeabilidad al vapor de agua en películas obtenidas a partir de soluciones de quitosán al 2 % más sorbitol al 0.7 y 1.4 % presentan los valores más pequeños.
Bibliografía
1. Park, J. H.; Weller, L.C.; Vergano, J.P. and Testin, R.F., J. Food Sci. 1993, 58, 1361. [ Links ]
2. Draget, K. I.; Varum, K.M.; Smidsrod, O. Advances in Chitin and Chitosan (C.J. Brine, P.A. Sandoford, and J.P. Zikakis, eds), Elsevier Applied Science, New York, 1991, 604. [ Links ]
3. Austin, P.R., Solvents and purification of chitin, US Patent 3, 892, 731 (1975). [ Links ]
4. Chao, R. R.; Rizvi Syed, S.H., in: Food and Packaging interactions, American Chemical Society, 1988. [ Links ]
5. Mc-Hugh, T. H.; Avena Bustillos, R.; Krochta, J.M. J. Food Sci. 1993, 58, 899-903. [ Links ]
6. ASTM, 1996. Annual Book of ASTM Standards. Philadelphia, Association of Standard Testing Methods. [ Links ]
7. Sixto, B.A.; Soto, A. M., Tesis FES-C, UNAM, 1996.
8. Mc-Hugh, T. H.; Krochta, J. M., in: Edible Films and Coatings to Improve Food Quality, Baldwin, E.; Krochta, J. M. and Nisperos-Carreido, M. O. Ed., Lancaster, PA. Technomic Publishing Co. 1994, 139-187. [ Links ]
]]>9. Hoagland, P.D.; Parris, N.; J. Agric Food Chem. 1996, 44, 1915-1919. [ Links ]
10. Gontard, N.; Guilbert, S.; Cuq, J.L. J. Food Sci. 1993, 58, 206-211. [ Links ]
11. Mc-Hugh, T. H.; Krochta, J. M. J. Agric. Food Chem. 1994, 42, 841-845. [ Links ]
12. Avena-Bustillos, R. J.; Krochta, J. M. J. Food Eng. 1994, 21, 197-214. [ Links ]
13. Sherwin C., The water vapor barrier of whey protein fatty acid emulsion edible films, 1998: http://fscn.che.umn.edu/FScNStudents/Homepages/csherwin/research.htm [ Links ]
14. Gordon, L.R., Food Packaging, Principles and Practice, Mariel Dekker Inc., 1992. [ Links ]
15. Koelsch, C. M.; Labuza, T. P. Lebensmittel-Wissenschaft-und-Technologie 1992, 25, 404-411. [ Links ]
16. Mc-Hugh, T. H.; Krochta J. M. J. Food Proc. and Preservation 1994, 18, 173-188. [ Links ]
]]>