El ribosoma: lo que nos ha enseñado su estructura1
The ribosome: what we learned from its structure
Tzvetanka D. Dinkova y Estela Sánchez de Jiménez2
2 Departamento de Bioquímica, Facultad de Química, Universidad Nacional Autónoma de México, UNAM.
]]>Resumen
Hace 150 años se publicó la teoría de Darwin sobre la evolución que dice: "Las características de un organismo son hereditarias y sujetas a cambios al azar; los cambios que permiten al organismo mejorar sus opciones de supervivencia, se conservarán en las futuras generaciones". El Premio Nobel en Química 2009 fue otorgado a tres científicos que aportaron la última pieza requerida para conocer cómo funciona en realidad la teoría de Darwin a nivel atómico. El primer premio Nobel en este sentido fue uno de los más famosos en la historia: el otorgado en 1962 a Francis Crick, James Watson y Maurice Wilkins por el modelo atómico de la doble hélice de ADN. El segundo fue el otorgado en el 2006 a Roger Kornberg por la estructura de la ARN polimerasa que copia la información de ADN a ARN. El tercero, otorgado este año a Ada Yonath, Thomas Steitz y Venkatraman Ramakrishnan por la estructura cristalina de alta resolución del ribosoma – una de las maquinarias celulares más complejas – que completa el camino de la información genética, permitiéndonos conocer cómo el lenguaje de ADN/ARN se convierte en proteínas que garantizan el correcto funcionamiento celular.
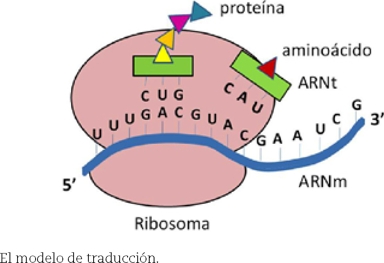
En los años sesenta se sucedieron varios descubrimientos clave para determinar que la información genética codificada a nivel de ADN es primero copiada a ARN mensajero (ARNm) y luego exportada fuera del núcleo. En el citoplasma, los ribosomas y los ARN de transferencia (ARNt) decodifican la información a secuencia de aminoácidos formando una proteína. El código genético fue completamente elucidado y sólo restaba conocer cómo funcionan a nivel químico estas moléculas para garantizar un proceso tan asombrosamente preciso, rápido y eficiente que además se ha conservado desde las bacterias hasta los humanos.
Abstract
The Darwin evolution theory published 150 years ago stated:"All organism features are hereditary and subject to random changes; those changes allowing a greater chance for the organism to survive will be carried out in further generations". The 2009 Nobel Prize in Chemistry was awarded to three scientists for their contribution with the third piece of evidence showing how actually the Darwin theory functions at the atomic level. The first piece contributed in the same puzzle was one of the most famous Nobel prizes in history: the one awarded in 1962 to Francis Crick, James Watson y Maurice Wilkins for the atomic model of ADN double helix. The second one was the 2006 Nobel Prize awarded to Roger Kornberg for solving the structure of ARN polymerase and how it copies the information from ADN to ARN. The third one, awarded this year to Ada Yonath, Thomas Steitz and Venkatraman Ramakrishnan for the high resolution crystal structure of the ribosome – one of the most complex cellular machineries – completes the flux of genetic information, showing us how the language codified in ADN/ARN is converted to proteins that precisely control the correct cell functioning.
Keywords: Nobel Prize, ribosome, structure, translation, antibiotics.
El modelo de traducción
]]> Muchos químicos, bioquímicos y físicos dedicaron sus esfuerzos durante los siguientes años a la búsqueda de respuestas sobre cómo funciona el ribosoma, considerado como el núcleo catalítico de la célula, la máquina de producción de proteínas, un enlace tangible con los orígenes de la vida. El ribosoma es una macromolécula que consiste de ARN ribosomal y proteínas. Para la síntesis de proteínas, el ribosoma debe contener un programa que le permita transformar el ARNm en la secuencia de aminoácidos de la proteína, reconocer los aminoácidos como sustrato para la síntesis, y proporcionar energía química para formar el enlace entre los aminoácidos.
El ribosoma está compuesto por dos subunidades, una subunidad pequeña y otra grande. La subunidad pequeña en humanos está formada por una molécula de ARN y 32 proteínas. La subunidad grande consiste de tres moléculas de ARN y alrededor de 46 proteínas. Cada subunidad está compuesta por miles de nucleótidos y miles de aminoácidos, que a su vez están formados por cientos de miles de átomos. Para conocer cómo funciona esta máquina era necesario contar con información de su estructura, es decir establecer la ubicación exacta de cada uno de los átomos en el ribosoma. Dada la complejidad del ribosoma, muchos científicos de los años ochenta consideraban que sería imposible obtener tales datos para esta partícula ribonucleoproteica.
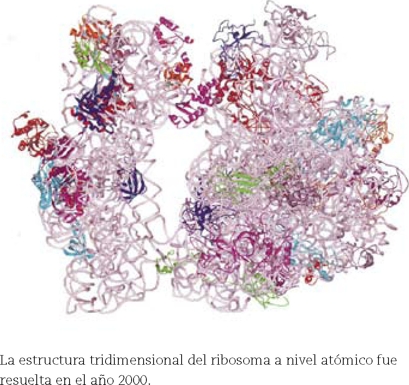
A finales de los setenta, Ada Yonath del Instituto Weizmann en Israel decidió tratar de generar estructuras cristalográficas por rayos X del ribosoma. Para ello era imprescindible contar con cristales adecuados que permitieran aportar patrones precisos de las moléculas en su estructura. Mientras más complejas las moléculas en solución, más difícil es obtener cristales de alta calidad, y en este caso se trataba de un complejo de muchas moléculas. A pesar de la dificultad del reto, la Dra. Yonath obtuvo en los años ochenta, colaborando en Berlín con el pionero de los estudios ribosómicos, el Dr. H.G. Wittmann, los primeros cristales de ribosomas que a pesar de no cumplir con los requisitos de calidad, fueron un paso crucial hacia el objetivo. Le tomó varios años más lograr la generación de cristales adecuados para obtener las imágenes estructurales que le valieron el premio Nobel (Harms et al., 2001). Ada Yonath, fue la pionera que se atrevió a iniciar la exploración de un terreno árido y desconocido, y mostró la posibilidad de conocer el ribosoma a nivel atómico. Varios grupos de científicos la siguieron en este enfoque, entre ellos, Thomas Steitz y Venkatraman Ramkrishnan.

Thomas Steitz de la Universidad de Yale, Estados Unidos, era ya un reputado biólogo estructural que abordó el problema del ribosoma en los años noventa, en colaboración con Peter Moore, también conocido por sus investigaciones acerca del ribosoma. Estos investigadores tuvieron la brillante idea de utilizar para la estructura modelos del ribosoma obtenidos por criomicroscopía electrónica en el equipo del Dr. Joachim Frank, de la Universidad de Albany, lo que resultó fundamental para resolver el problema de la orientación o fase angular del ribosoma. En 1998 Thomas Steitz publicó la primera estructura cristalográfica de la subunidad grande del ribosoma a resolución de 9 Årmströng (Ban et al., 1998). Todavía no era posible ver átomos individuales pero fue un hito decisivo.
Venkatraman Ramakrishnan, el más joven de los tres galardonados, participó en la resolución de la estructura de la subunidad pequeña del ribosoma y proporcionó un modelo molecular que explicaba el proceso de decodificación de los ARNm y cómo a nivel atómico esta subunidad mide la distancia en el apareamiento entre el codón en el ARNm y el anticodón en el ARNt para permitir la asociación estable solamente del ARNt portador del aminoácido correspondiente al codón correcto. Estos trabajos fueron realizados con gran éxito en el MRC de Cambridge, Inglaterra.
De esta manera, los grupos dirigidos por los tres galardonados publicaron en el año 2000 y 2001, la estructura cristalográfica de las dos subunidades ribosómicas de organismos procariontes, lo que es un hito incuestionable en biología estructural (Ban et al., 2000; Clemons Jr. et al., 2001; Harms et al., 2001).
La existencia de enfermedades debidas a alteraciones ribosómicas realza la importancia biomédica del trabajo galardonado, aunque el impacto más valioso en este campo radica en que el ribosoma es el punto de anclaje de un número importante de antibióticos que se unen específicamente a partes de su estructura y bloquean su función, paralizando de esta forma la producción de proteínas y con ellas las funciones celulares y la vida de los organismos. Es importante mencionar que los ribosomas de microorganismos procarióticos, entre los que se encuentran muchos agentes infecciosos para el ser humano, son los receptores de la mayoría de los antibióticos actualmente conocidos. Además, y posiblemente más prometedora, es la aplicación de la información ahora disponible de la estructura diferencial de los ribosomas procariontes de los eucariontes, a fin de diseñar nuevos antibióticos que mejoren la actividad de los existentes, eviten en algunos casos la aparición de resistencias o eliminen los efectos secundarios que algunos manifiestan. La notable inversión de recursos en este tipo de estudios que se está llevando a cabo, incluso la creación de empresas específicamente dedicadas a explorar estas posibilidades, subraya la relevancia de la información proporcionada por los trabajos de investigación básica de quienes fueron galardonados.
]]>Bibliografía
Ban, N., Freeborn, B., Nissen, P., Penczek, P., Grassucci, R. A., Sweet, R., Frank, J., Moore, P. B. and Steitz T. A., A 9 Å resolution X-ray crystallographic map of the large ribosomal subunit, Cell, 93(7), 1105-15, 1998. [ Links ]
Ban, N., Nissen, P., Hansen, J., Moore, P. B. and Steitz, T. A., The complete atomic structure of the large ribosomal subunit at 2.4 Å resolution, Science, 289(5481), 905-20, 2000. [ Links ]
Clemons Jr., W. M., Brodersen, D. E., McCutcheon, J. P., May, J. L. C., Carter, A. P., Morgan-Warren, R. J., Wimberly, B. T. and Ramakrishnan, V., Crystal structure of the 30 S ribosomal subunit from Thermus thermophilus: purification, crystallization and structure determination, Journal of Molecular Biology, 310(4), 827-43, 2001. [ Links ]
Harms, J., Schluenzen, F., Zarivach, R., Bashan, A., Gat, S., Agmon, I., Bartels, H., Franceschi, F. and Yonath, A. High resolution structure of the large ribosomal subunit from a mesophilic eubacterium, Cell, 107(5), 679-88, 2001. [ Links ]
]]>Nota
1 Artículo solicitado a las doctoras Dinkova y Sánchez por el Director de Educación Química.
]]>