
Efecto de preparados minerales sobre el crecimiento y desarrollo in vitro de Moniliophthora roreri (Cif. & Par.) Evans*
Effect of mineral preparations on growth and in vitro development of Moniliophthora roreri (Cif. & Par.) Evans
Lyda Esperanza Ochoa Fonseca1, Sandra Isabel Ramírez González2§, Orlando López Báez3, José Luis Moreno Martínez1 y Saúl Espinosa Zaragoza5
1 Universidad Autónoma de Chiapas-Facultad de Ciencias Agrícolas Campus IV. Entronque Carretera Costera y Estación Huehuetán, C. P. 30660. Tel: 964 6270128. (lyda.ochoa.23@gmail.com; jolumo@gmail.com).
]]> 2 Universidad Autónoma de Chiapas-Laboratorio de Agrotecnologías, AUDES Cacao-Chocolate. Campus Ciudad Universitaria, km 8 carretera Terán-Ejido Emiliano Zapata. Tuxtla Gutiérrez, Chiapas. Tel: 961 6178000 ext. 1725 y 1722.3 Universidad Autónoma de Chiapas, México. Laboratorio de Agrotecnologías, AUDES Cacao-Chocolate. Campus Ciudad Universitaria, km 8 carretera Terán-Ejido Emiliano Zapata. Tuxtla Gutiérrez, Chiapas. Tel: 961 6178000 ext. 1725 y 1722. (olopez@unach.mx).
5 UniversidadAutónoma de Chiapas, México. Facultad de Ciencias Agrícolas Campus IV. Entronque Carretera Costera y Estación Huehuetán, C. P. 30660. Tel: 964 6270128. (saulez1@gmail.com). §Autora para correspondencia: sanirg@yahoo.com.
* Recibido: septiembre de 2014
Aceptado: enero de 2015
Resumen
El presente estudio se desarrolló con el objetivo de evaluar en condiciones de laboratorio, la actividad fungicida sobre Moniliophthora roreri de los preparados minerales: caldo visosa (CV), caldo bordelés más permanganato de potasio (CBP), caldo bordelés más sulfato de zinc y sulfato de magnesio (CBS), caldo de bicarbonato de sodio (BiS), caldo silicosulfocálcico (SSC) y polisulfuro de calcio (PC). Se realizaron dos bioensayos. En el primero, el efecto inhibitorio sobre el crecimiento del hongo se evaluó mediante la técnica de difusión en agar, los compuestos fueron probados en cinco concentraciones (50, 40, 30, 20 y 10% v/v). En el segundo, mediante la técnica de cultivo en medio líquido en tubos de ensayo se determinó el efecto sobre la formación y germinación de esporas del hongo; el medio de cultivo consistió de una solución de agua más extracto de cacao (1:1 v/v) a la cual se adicionaron esporas del hongo y 50% (v/v) de cada preparado mineral. Con excepción del BiS al 10%, el crecimiento micelial fue inhibido total o parcialmente por los demás preparados minerales, presentando diferencias estadísticamente significativas con el testigo. Los preparados SSC y PC fueron los más eficaces inhibiendo 100% de crecimiento micelial aún en la concentración de 10%. La prueba en medio líquido mostró que a las 96 horas los preparados SSC y PC fueron los más eficaces, llegando a reducir el número de esporas en 98.2 y 79.9% respectivamente; solo se presentó germinación de esporas en el tratamiento testigo. Se observó la formación de esporas en los tratamientos BiS en todas las concentraciones y en el testigo, pero ningún preparado mineral permitió la germinación de esporas.
Palabras clave: Theobroma cacao L., Moniliasis, agricultura orgánica.
]]>Abstract
The present study was developed with the aim to evaluate the fungicidal activity of mineral preparations on Moniliophthora roreri under laboratory conditions: broth visosa (CV), Bordeaux mixture plus potassium permanganate (CBP), Bordeaux mixture plues zinc sulfate and sulfate magnesium (CBS), broth sodium bicarbonate (BiS), broth silicosulfocálcico (SSC) and calcium polysulfide (PC). Two bioassays were performed; in the first, the inhibitory effect on fungal growth was assessed by the agar diffusion method, the compounds were tested at five concentrations (50, 40, 30, 20 and 10% v / v). In the second, through the cultivation technique cultivation in liquid medium in test tubes, the effect on formation and germination of fungus spores was determined; The culture medium consisted of a solution of cocoa extract plus water (1:1 v / v) to which fungus spores and 50% (v / v) ofeach mineral preparation were added. With the exception of BiS at 10%, mycelial growth was inhibited completely or partially by the other mineral preparations, showing statistically significant differences with control. SSC and PC preparations were the most effective in inhibiting 100% mycelial growth even at 10% concentration. The test showed that in liquid medium at 96 hours the SSC and PC preparations were the most effective, reducing up to 98.2 and 79.9% of spores respectively; spore germination was only present in control treatment. Spore formation in BiS treatments at all concentrations and in control was observed, but no mineral preparations allowed spore germination.
Keywords: Theobroma cacao L., Moniliasis, organic agriculture.
Introducción
La moniliasis (Moniliophthora roreri (Cif. & Par.) Evans es una de las enfermedades que generan mayores pérdidas en el cultivo de cacao (Theobroma cacao L.), llegando a ser hasta de 100% si las condiciones climáticas son favorables y los árboles son altamente susceptibles a la enfermedad (Phillips et al, 2005; López et al, 2006). En las regiones productoras de México el manejo de este fitopatógeno es básicamente de tipo cultural, a través de la poda de los árboles y la remoción de frutos enfermos. Si se aplica de forma rigurosa, el manejo cultural ha demostrado ser una alternativa efectiva en otros países (Soberanis et al, 1999; Krauss et al, 2003; Jaimes y Aranzazu, 2010); sin embargo, factores como el costo o la escasez de mano de obra para realizar estas prácticas y la existencia de plantaciones de avanzada edad con árboles de porte alto, hacen que se requiera de nuevas alternativas complementarias para mejorar la eficiencia tanto en protección del cultivo, como en términos económicos.
Desde hace más de un siglo se conoce el efecto positivo que tienen diferentes productos a base de sales inorgánicas y otros compuestos de origen natural (aquí se denominan preparados minerales) en el control de numerosos problemas fitosanitarios (Deliopoulos et al, 2010). Reuveni y Reuveni (1995) señalan algunas ventajas de estos productos como su bajo costo, la baja toxicidad para mamíferos y en general, un buen perfil de seguridad para el hombre y el ambiente; además es importante señalar que el uso de estos preparados minerales es aceptado en el marco de las normas de producción orgánica (Reglamento (CE) núm. 834/2007 y USDA-NOP).
Uno de los preparados minerales más conocidos es el caldo bordelés, que se ha empleado con éxito para controlar Phytophthora palmivora en el cacao (Hislop, 1963; Adejumo, 2005), además se han obtenido buenos resultados sobre diferentes fitopatógenos con otros productos, como el bicarbonato de sodio (Dik et al, 2003; Dessalegn et al, 2013) y el polisulfuro de calcio (Holb y Schnabel, 2008; Jamar et al, 2010); este último fue probado para el control de M. roreri, encontrándose que in vitro redujo el número de conidias hasta 74% y en campo logró bajar la incidencia a 0.53%, frente a 21% en el tratamiento con manejo cultural y 69.6% en el testigo sin manejo (Ramírez et al, 2011a).
Actualmente hay un incremento sostenido en la demanda de cacao orgánico, sin embargo la oferta es insuficiente (The International Cocoa Organization, 2006; Centro Agronómico Tropical de Investigación y Enseñanza, 2010), lo cual plantea la necesidad de desarrollar alternativas para el control de la moniliasis, aceptadas dentro de la normatividad de producción orgánica y que presenten una buena relación beneficio/costo para el productor. En este sentido, preparados a base de minerales pueden ser una opción promisoria, por lo cual el presente estudio se planteó como objetivo evaluar la efectividad de seis preparados minerales para inhibir el crecimiento micelial, la formación y la germinación de esporas de M. roreri, en condiciones de laboratorio.
]]>Materiales y métodos
Los ensayos fueron conducidos en el Laboratorio de Agrotecnologías de la Agencia Universitaria para el Desarrollo -AUDES Cacao-Chocolate, ubicado en Ciudad Universitaria de la Universidad Autónoma de Chiapas, en Tuxtla Gutiérrez, Chiapas, México.
Los preparados minerales evaluados fueron: caldo visosa (CV); caldo bordelés más permanganato de potasio (CBP); caldo bordelés más sulfato de zinc y sulfato de magnesio (CBS); caldo de bicarbonato de sodio (BiS); caldo silicosulfocálcico (SSC) y polisulfuro de calcio (PC). Los cinco primeros se elaboraron siguiendo la composición y procedimientos descritos por Restrepo (2007) y para el PC, se aplicó el procedimiento descrito por Ramírez et al. (2011a); se utilizaron elementos y compuestos grado analítico.
El hongo se aisló de un fruto de cacao infectado en estado de mancha chocolate procedente del municipio de Tecpatán, Chiapas, México y se mantuvo en medio de cultivo compuesto por extracto de cacao, agar y agua destilada, a una temperatura de 26 °C (±2°C).
Para determinar el efecto de los preparados minerales sobre el patógeno se realizaron dos ensayos, uno mediante la técnica de difusión en agar y otro en medio líquido.
Prueba de difusión en agar. Se preparó el medio de cultivo según la composición indicada anteriormente para el mantenimiento del hongo, pero se reemplazó una parte del agua destilada por el correspondiente volumen de preparado mineral, dependiendo de la concentración a evaluar: 50, 40, 30, 20 y 10% (v/v), excepto en el testigo (TES) sin preparado. Una vez solidificado el medio, se realizó la siembra de M. roreri procedente de un cultivo de 12 días de edad, para lo cual se usó un sacabocado y se depositó el inóculo en el centro de cada caja Petri de 50 mm. Cada 24 h durante 12 días se midió el diámetro de crecimiento micelial (mm); el día 13, con una cámara de Neubauer se realizó el conteo del número de esporas formadas y germinadas, para lo cual se hizo un raspado del crecimiento fúngico de cada caja Petri y se diluyó con agua destilada. El diseño experimental fue completamente al azar con siete tratamientos consistentes en los seis preparados minerales más un testigo únicamente con el medio de cultivo y cinco repeticiones, la unidad experimental consistió de una caja Petri.
Prueba en medio líquido. Se preparó una solución madre con esporas obtenidas de un cultivo de 12 días de sembrado, para lo cual se realizó un raspado superficial del contenido de siete cajas Petri de 50 mm en un Erlenmeyer, se agregaron 117 mL de extracto de cacao, 117 mL de agua destilada y dos gotas de Tween 80, esta solución se sometió a agitación en vortex por una hora. Se marcaron 15 tubos de ensayo (repeticiones) por tratamiento y en cada uno se agregaron 5 mL de solución madre y 5 mL del preparado mineral a evaluar; en el tratamiento testigo se agregó agua destilada en vez de preparado mineral. Los tubos de ensayo se agitaron hasta homogenizar la solución y se incubaron en oscuridad a 26 ± 2 °C. Cada 24 h y hasta las 96 h después de inoculación se realizó el conteo del número de esporas totales y germinadas en cámara de Neubauer. En cada momento de conteo se evaluaron tres tubos por tratamiento realizando tres lecturas en cada tubo. Se usó un diseño completamente al azar con siete tratamientos y 15 repeticiones por tratamiento.
A los datos obtenidos en las dos pruebas se les realizó análisis de varianza y comparación de medias a través de la prueba de Tukey. El análisis estadístico se realizó con el programa Statistical Analysis System (SAS)® versión 9.1 para Windows.
]]> Resultados y discusión
a) Prueba de difusión en agar
En el Cuadro 1 se presentan los resultados del diámetro de crecimiento micelial de M. roreri, 12 días después de la siembra (dds) y exposición a los preparados minerales; la prueba de Tukey mostró que existen diferencias estadísticamente significativas entre todos los tratamientos y el testigo (TES). En la Figura 1 se aprecia el aspecto de las colonias en las cajas Petri; el color del medio en los tratamientos SSC y PC se debe a su composición.

Los mejores resultados se obtuvieron con el SSC y el PC, ya que en todas las concentraciones el crecimiento micelial fue nulo. Estos resultados coinciden con los reportados por Ramírez et al. (2011a) para el PC y demuestran mayor eficacia que productos de síntesis química como el Clorotalonil y Azoxystrobin en los estudios realizados por Torres et al. (2013) y Quevedo (2012). El primero de estos autores encontró una inhibición de 96% en el crecimiento micelial con Azoxystrobin (1 250 mg/L) y el segundo reportó valores de 67% para Clorotalonil y 78% para Azoxystrobin (dosis de 1 000 mg/L).
En los tratamientos CV, CBP y CBS la inhibición del crecimiento micelial incrementó a medida que la concentración del preparado mineral fue mayor; en concentraciones de 50 al 30% lograron inhibir completamente el crecimiento micelial y al 20% ejercieron una inhibición de más de 60% por lo cual se consideran productos con potencial para el control de M. roreri. Por su parte, el Bi S en todas las concentraciones ejerció el menor efecto inhibitorio sobre el hongo y a la concentración más baja (10%) promovió su crecimiento superando al testigo; un efecto similar fue reportado por Mills et al. (2004), quienes encontraron que el bicarbonato de sodio estimuló el crecimiento micelial de Verticillium albo-atrum.
En el Cuadro 2 se presentan los resultados del número de esporas formadas; se puede observar que con excepción de los tratamientos BiS y testigo, los demás inhibieron totalmente la formación de éstas estructuras. En el tratamiento BiS el número de esporas mL-1 se incrementó a medida que disminuyó la concentración del preparado y al 10% superó ligeramente al testigo, sin presentar diferencia estadísticamente significativa con éste. En los tratamientos CV, CBP y CBS aunque se observó formación de micelio a concentraciones de 10 y 20% (Cuadro 1), no se presentó formación de esporas; este efecto antiesporulante es muy importante ya que las esporas son las únicas estructuras del patógeno que pueden causar infección de los frutos.
En las cinco concentraciones todos los preparados minerales inhibieron la germinación de esporas, ésta solo se presentó en el testigo con un promedio de 3.27 x 105 esporas germinadas mL-1, que corresponden al 0.28% del total. En estudios in vitro, esta inhibición total sobre la germinación de M. roreri, ha sido reportada para pocos productos, entre ellos el fungicida de síntesis química Azoxystrobin (450 ppm) (Torres et al, 2013) y aceites esenciales de Lippia origanoides, Lippia citriodora y Lippia alba en concentraciones de 600 a 1 000(μg mL-1 (Lozada et al, 2012). Dado que el tubo germinativo es la estructura encargada de penetrar e iniciar la infección del fruto, la inhibición de la germinación de las esporas es un mecanismo de acción indispensable en los productos para el control de M. roreri, pues impiden que las esporas depositadas en la superficie del fruto lleven a cabo la infección. Estadísticamente hubo una correlación positiva y significativa (r= 0.77) entre las variables crecimiento micelial y número de esporas, pero no entre estas dos variables y el número de esporas germinadas.
Prueba en medio líquido. El objetivo de esta prueba fue establecer si además de impedir la germinación, los preparados minerales tienen la capacidad de causar mortalidad a esporas ya formadas. En el Cuadro 3 se presentan los resultados del número de esporas contabilizadas en los tubos de ensayo a las 0, 24, 48, 72 y 96 h después de inoculación. En los tratamientos SSC, PC, CBS y CBP se observó reducción en el número de esporas a medida que transcurrió el tiempo. Desde el primer conteo (hora 0) los preparados SSC y PC indujeron mortalidad de esporas, presentando diferencia estadísticamente significativa con el testigo. Esta tendencia se mantuvo en todas las horas de evaluación, llegando a ocasionar la muerte de 98.2 y 79.9% de las esporas respectivamente, a las 96 h; un valor similar es reportado por Ramírez et al. (2011a) para el PC que en condiciones in vitro redujo el número de esporas en 74.7% a las 72 h.
]]> Los tratamientos CBP y CBS mostraron una eficacia intermedia, llegando a reducir el número de esporas en 45.5 y 42.8% respectivamente, a las 96 h; con excepción de las 0 h, en los demás conteos presentaron diferencia estadísticamente significativa con el testigo. De acuerdo con los resultados de otros estudios, los componentes de estos dos preparados minerales han inducido el desarrollo de resistencia hacía varias enfermedades fungosas en diferentes cultivos (Tomlinson y Hunt, 1987; Huber y Wilhelm, 1988; Rouxel et al., 1990) y pueden incrementar el rendimiento pues mejoran su nutrición. Este último efecto fue reportado por Siller (1958), en un estudio sobre control de enfermedades en cacao indica que con la aplicación de caldo bordelés se obtuvo un promedio de 53 frutos sanos por árbol al año, mientras que al adicionarle sulfato de zinc este número se elevó a 61 frutos, atribuyendo dicho incremento a la corrección de una deficiencia de zinc. Tomando en cuenta estos resultados se sugiere evaluar el CBP y CBS contra M. roreri en condiciones de campo.Los tratamientos BiS y CV mostraron un efecto muy bajo o nulo e incluso en algunas horas el número de esporas fue ligeramente superior al testigo, aunque sin presentar diferencias estadísticamente significativas con éste. Estos resultados en conjunto con los de la prueba de difusión en agar indicarían un efecto fungistático más no fungicida por parte de estos dos preparados minerales. En relación con el número de esporas germinadas, solo se presentaron en el testigo, alcanzando un valor máximo de 14.2 x 104 a las 48 h. Se ratifican así los resultados obtenidos en la prueba de difusión en agar, respecto a la inhibición total que ejercen los cinco preparados sobre la germinación de las esporas.
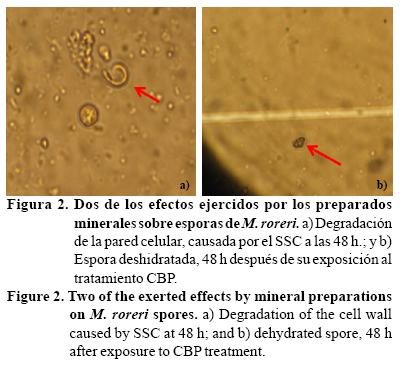
Acerca de los mecanismos de acción de los preparados minerales sobre el patógeno, complementario a la inhibición de la esporulación y formación de micelio que se observó en la prueba de difusión en agar, durante la prueba en medio líquido fue posible observar inhibición de la germinación de esporas y muerte causada por el rompimiento de las paredes celulares (Figura 2a) y deshidratación (Figura 2b). A nivel in vitro y en campo se han documentado estos mismos efectos sobre diferentes fitopatógenos para varios de los elementos y compuestos que componen los seis preparados minerales: bicarbonato de sodio (Yildirim et al, 2002), azufre (Khan y Kulshrestha, 1991; Williams et al., 2002; Williams y Cooper, 2004), polisulfuro de calcio (Montag et al, 2005; Holb y Schnabel, 2008; Ramírez et al, 2011a) y sulfato de cobre (Mills et al, 2004; Montag et al, 2006), entre otros. Por otra parte, es conocido que algunos de estos minerales inducen resistencia en las plantas, lo cual puede reducir la incidencia y severidad del daño en campo. En el caso del caldo silicosulfocálcico, uno de sus componentes es la ceniza vegetal que contiene cantidades variables de silicio, la inducción de resistencia por este elemento ha sido ampliamente documentada en diversos cultivos (Chérif et al., 1994; Fauteux et al., 2005; Qin y Tian, 2005).
La moniliasis constituye el principal problema fitosanitario que enfrenta la producción de cacao en Centro y Sur América, causando un alto impacto socioeconómico y ambiental; atendiendo al hecho de que en esta región se encuentran los materiales genéticos de mayor calidad para la industria chocolatera, es muy importante desarrollar una oferta tecnológica de bajo impacto ambiental para el manejo de esta enfermedad. El uso de fungicidas de síntesis química no ha mostrado resultados contundentes, en algunos casos atribuibles al escaso control del hongo y en otros a una relación beneficio/costo desfavorable para el productor, sobre todo en plantaciones con baja productividad; a lo anterior se suma la contaminación ambiental que estos productos ocasionan, por lo cual no son permitidos dentro de los sistemas de producción orgánica.
A causa de esta situación y teniendo en cuenta el incremento en la demanda de cacao orgánico, en años recientes se viene enfatizando la búsqueda de alternativas de bajo impacto ambiental, tales como el uso de organismos antagonistas (Bailey et al, 2008; Melnick et al, 2011), extractos vegetales (Ramírez et al., 2011b; Lozada et al., 2012; Ramírez et al, 2013) y en menor medida, aunque no de menor potencial, los preparados a base de minerales (Krauss et al, 2010: Ramírez et al., 2011a).
La eficacia de estos últimos sobre diversos patógenos motivó su evaluación para el control de la moniliasis y los resultados presentados demuestran que el PC y el SSC son productos promisorios, que requieren ser validados en condiciones de campo. Es de resaltar que estos dos productos se elaboran con materiales accesibles y de bajo costo: cal y azufre y ceniza vegetal, lo cual incrementa las posibilidades de adopción de estas tecnologías por parte de pequeños cacaocultores.
Conclusiones
]]> El caldo silicosulfocálcico y el polisulfuro de calcio causaron la mayor mortalidad de esporas e inhibición del crecimiento micelial y de la formación y germinación de esporas de M. roreri in vitro, superando resultados obtenidos con productos de síntesis química en otros estudios.El caldo bordelés complementado con permanganato de sodio o con sulfato de zinc y sulfato de magnesio, aunque inferiores en eficacia al caldo silicosulfocálcico y al polisulfuro de calcio, ejercen inhibición sobre el crecimiento, esporulación y germinación de esporas de M. roreri in vitro.
Se observaron cuatro mecanismos de acción antifúngica de los preparados minerales sobre M. roreri: a) inhibición de la formación y crecimiento de micelio; b) inhibición de la formación de esporas; c) inhibición de la germinación de esporas; y d) muerte de las esporas ocasionada por deshidratación y degradación de la membrana celular, con la consecuente lisis.
Literatura citada
Adejumo, T. 2005. Crop protection strategies for major diseases of cocoa, coffee and cashew in Nigeria. Afr. J. Biotechnol. 4(2): 143-150. [ Links ]
Bailey, B.; Bae, H.; Strem, M.; Crozier, J.; Thomas, S.; Samuels, G.; Vinyard, B. and Holmes, K. 2008. Antibiosis, mycoparasitism, and colonization success for endophytic Trichoderma isolates with biological control potential in Theobroma cacao. Biological Control. 46:24-35. [ Links ]
Centro Agronómico Tropical de Investigación y Enseñanza (CATIE). 2010. Estudio de mercado cacao amigable con la biodiversidad de Centroamérica. Costa Rica. 198 p. [ Links ]
Chérif, M.; Asselin,A. and Bélanger, R. 1994. Defense responses induced by soluble silicon in cucumber roots infected by Phytium spp. Mol. Plan Pathol. 84(3):236-242. [ Links ]
Deliopoulos, T.; Kettlewell, P. and Hare, M. 2010. Fungal disease suppression by inorganic salts: a review. Crop Protection. 29:1059 -1075. [ Links ]
Dessalegn, Y.; Ayalew, A. and Woldetsadik K. 2013. Integrating plant defense inducing chemical, inorganic salt and hot water treatments for the management of postharvest mango anthracnose. Postharvest Biol. Technol. 85:83-88. [ Links ]
Dik, A.; van der Gaag, D. ans van Slooten, M. 2003. Efficacy of salts against fungal diseases in glasshouse crops. Comm. Agric. Appl. Biol. Sci. 68(4):475-485. [ Links ]
Fauteux, F.; Rémus, W.; Menzies J. and Bélanger, R. 2005. Silicon and plant disease resistance against pathogenic fungi. FEMS Microbiology Letters. 249(1):1-6. [ Links ]
Hislop, E. 1963. Studies on the chemical control of Phytophthora palmivora (Butl.) Butl. on Theobroma cacao L. in Nigeria. Ann. Appl. Biol. 52(3):465-480. [ Links ]
Holb, I. and Schnabel, G. 2008. A detached fruit study on the post-inoculation activity of lime sulfur against brown rot of peach (Moniliniafructicola). Australasian Plant Pathol. 37:454-459. [ Links ]
Huber, D. and Wilhelm, N. 1988. The role ofmanganese in resistance to plant diseases. In: manganese in soils and plants. Graham, R.; Hannam, R. and Uren, N. (Eds). KluwerAcademic Publishers. Dordrecht, The Netherlands. 155-173 pp. [ Links ]
Jaimes, Y. y Aranzazu, F. 2010. Manejo de las enfermedades del cacao (Theobroma cacao L.) en Colombia, con énfasis en monilia (Moniliophthora roreri). Corporación Colombiana de Investigación Agropecuaria (Corpoica). Colombia. 90 p. [ Links ]
Jamar, L.; Cavelier, M. and Lateur, M. 2010. Primary scab control using a "during-infection" spray timing and the effect on fruit quality and yield in organic apple production. Biotechnol. Agron. Soc. Environ. 14(3):423-439. [ Links ]
Khan, M. and Kulshrestha, M. 1991. Impact of sulphur dioxide exposure on conidial germination of powdery mildew fungi. Environ. Pollution. 70(1):81-88. [ Links ]
Krauss, U.; Hoopen, M.; Hidalgo, E.; Martínez, A.; Arroyo, C.; García, J.; Portuguez, A. y Sánchez, V. 2003. Manejo integrado de la moniliasis (Moniliophthora roreri) del cacao (Theobroma cacao) en Talamanca, Costa Rica. Agroforestería en las Américas. 10(37-38):52-58. [ Links ]
Krauss, U.; Hidalgo, E.; Bateman, R.; Adonijah, V.; Arroyo, C.; García, J.; Crozier, J.; Brown, N.; ten Hoopen, M. and Holmes, K. 2010. Improving the formulation and timing of application of endophytic biocontrol and chemical agents against frosty pod rot (Moniliophthora roreri) in cocoa (Theobroma cacao). Biological Control. 54:230-240. [ Links ]
López, O.; Ramírez, S.; González, O.; Ramírez M., Lee, V.; Méndez, J.; Alvarado, A. y Gehrke, M. 2006. Diagnóstico y técnicas para el manejo de la moniliasis del cacao. Universidad Autónoma de Chiapas, Universidad Pedagógica y Tecnológica de Colombia, Fundación Produce Chiapas. 40 p. [ Links ]
Lozada, B.; Herrera, L.; Perea, J.; Stashenko, E. y Escobar, P. 2012. Efecto in vitro de aceites esenciales de tres especies de Lippia sobre Moniliophthora roreri (Cif. y Par.) Evans et al., agente causante de la moniliasis del cacao (Theobroma cacao L.). Acta Agron. 61(2):102-110. [ Links ]
Melnick, R.; Suárez, C.; Bailey, B. and Backman, P. 2011. Isolation of endophytic endospore-forming bacteria from Theobroma cacao as potential biological control agents of cacao diseases. Biol. Control. 57:236-245. [ Links ]
Mills, A.; Platt, H. and Hurt, R. 2004. Effect of salt compounds on mycelial growth, sporulation and spore germination of various potato pathogens. Postharvest Biol. Technol. 34:341-350. [ Links ]
Montag, J.; Schreiber, L. and Schönherr, J. 2005. An in vitro study on the postinfection activities of hydrated lime and lime sulphur against apple scab (Venturia inaequalis). J. Phytopathol. 153(7-8):485-491. [ Links ]
Montag, J.; Schreiber, L. and Schönherr, J. 2006. An in vitro study of the nature of protective activities of copper sulphate, copper hydroxide and copper oxide against conidia of Venturia inaequalis. J. Phytopathol. 154(7-8):474-481. [ Links ]
Phillips, W.; Castillo, J.; Krauss, U.; Rodríguez, E. and Wilkinson, M. 2005. Evaluation of cacao (Theobroma cacao) clones against seven Colombian isolates of Moniliophthora roreri from four pathogen genetic groups. Plant Pathol. 54:483-490. [ Links ]
Qin, G. and Tian, S. 2005. Enhancement of biocontrol activity of Cryptococcus laurentii by silicon and the possible mechanisms involved. Biol. Control. 95(1):69-75. [ Links ]
Quevedo, I. 2012. Evaluación de fungicidas sistémicos y de contacto en el control de la moniliasis (Moniliophthora roreri) del cacao (Theobroma cacao). Tesis Maestría en Ciencias. Colegio de Posgraduados, México. 72 p. [ Links ]
Ramírez, S.; López O.; Guzmán, T.; Munguía, S. y Moreno, J. 2011a. El polisulfuro de calcio en el manejo de la moniliasis Moniliophthora roreri (Cif & Par) Evans et al. del cacao Theobroma cacao L. Tecnología en Marcha. 24(4):10-18. [ Links ]
Ramírez, S.; López, O.; Guzmán, T.; Munguía, S. y Espinosa, S. 2011b. Actividad antifúngica in vitro de extractos de Origanum vulgare L., Tradescantia spathacea Swartz y Zingiber officinale Roscoe sobre Moniliophthora roreri (Cif & Par) Evans etal. Tecnología en Marcha. 24(2):3-17. [ Links ]
Ramírez, S.; López, O.; Guzmán, T.; Munguía, S.; Moreno, J. y Espinosa. S. 2013. Biofungicidas de origen vegetal una alternativa para el manejo de la moniliasis del cacao en México. In: Memorias VII Congreso de la Red Latinoamericana de Ciencias Ambientales. San Carlos, Costa Rica. 46 p. [ Links ]
Reglamento (CE). 2007. Número 834-2007 del consejo, sobre producción y etiquetado de los productos ecológicos. Consejo de la Unión Europea. Diario Oficial de la Unión Europea. http://eur-lex.europa.eu/legal-content/es/all/?uri=celex:32007r0834. [ Links ]
Restrepo, J. 2007. Manual práctico el A, B, C de la agricultura orgánica y harina de rocas. 1ª (Ed.). Servicio de Información Mesoamericano sobre Agricultura Sostenible -SIMAS. Nicaragua. 262 p. [ Links ]
Reuveni, M. and Reuveni, R. 1995. Efficacy of foliar application of phosphates in controlling powdery mildew fungus on field-grown winegrapes: effects on cluster yield and peroxidase activity in berries. J. Phytopathol. 143:21-25. [ Links ]
Rouxel, T.; Kollmann, A. and Bousquet, J. 1990. Zinc suppresses sirodesmin PL toxicity and protects Brassica napus plants against the blackleg disease caused by Leptosphaeria maculans. Plant Sci. 68(1):77-86. [ Links ]
Siller, L. 1958. Effect on cacao of urea, zinc and bordeaux mixture foliar sprays. The 7th Inter-American Cacao Conference. Colombia. 187-91 pp. [ Links ]
Soberanis, W.; Ríos, R.;Arevalo, E.; Zuñiga, L.; Cabezas, O. and Krauss, U. 1999. Increased frequency of phytosanitary pod removal in cacao (Theobroma cacao) increases yield economically in eastern Peru. Crop Protection. 18:677-685. [ Links ]
The International Cocoa Organization (ICCO). 2006. A study on the market for organic cocoa. Executive committee. One hundred and thirtieth meeting, London. 12 p. [ Links ]
Tomlinson, J. and Hunt, J. 1987. Studies on watercress chlorotic leaf spot virus and on the control of the fungus vector (Spongospora subterranea) with zinc. Ann. Appl. Biol. 110(1):75-88. [ Links ]
Torres, M.; Ortiz, C.; Téliz, D.; Mora, A. y Nava, C. 2013. Efecto del Azoxystrobin sobre Moniliophthora roreri, agente causal de la Moniliasis del cacao (Theobroma cacao). Rev. Mex. Fitopatol. 31(1):65-69. [ Links ]
USDA-NOP. 2014. The National Organic Program standards of the United States Department of Agriculture. http://www.ecfr.gov/cgi-bin/text-idx?SID=497deb86f6aac6df9cf42574955a1cfb&node=7:3.1.1.9.32&rgn=div5. [ Links ]
Williams, J.; Hall, S.; Hawkesford, M.; Beale, M. and Cooper R. 2002. Elemental sulfur and thiol accumulation in Tomato and defense against a fungal vascular pathogen. Plant Physiol. 128(1):150-159. [ Links ]
Williams, J. and Cooper, R. 2004. The oldest fungicide and newest phytoalexin -a reappraisal of the fungitoxicity of elemental sulphur. Plant Pathol. 53:263-279. [ Links ]
Yildirim, I.; Onogur, E. and Irshad, M. 2002. Investigations on the efficacy of some natural chemicals against Powdery Mildew [Uncinula necator (Schw.) Burr.] of Grape. J. Phytopathol.150(11-12):697-702. [ Links ]
]]>