Correlación de la farmacocinética con la farmacodinamia del tacrolimus en el tratamiento de pacientes pediátricos con trasplante renal
Correlation between pharmacokinetics and pharmacodynamics of tacrolimus in the treatment of pediatric renal transplant patients
Enrique Omar Guadarrama-Díaz,1* María Inés del Pilar García-Roca,2 Herlinda Reyes-Pérez,3 Mara Medeiros1,2
1 Departamento de Nefrología
2 Laboratorio de Investigación en Nefrología y Metabolismo Mineral Óseo ]]>
3 Laboratorio Central
Hospital Infantil de México Federico Gómez
México, D.F., México
* Becario CONACYT
Autor de correspondencia: Dra. Mara Medeiros
Correo electrónico: medeiro.mara@gmail.com
]]> Fecha de recepción: 11-02-13
Resumen
Introducción. El tacrolimus se emplea como inmunosupresor en pacientes con trasplante renal. La monitorización farmacodinámica es una estrategia para conocer el efecto biológico real. El objetivo de este trabajo fue determinar la correlación entre la concentración de tacrolimus y la expresión génica de factor de necrosis tumoral alfa (TNF-α) en pacientes con trasplante renal.
Métodos. Se realizó un estudio transversal y experimental en niños con trasplante renal con tres meses de evolución. Se obtuvieron muestras de sangre para realizar la farmacocinética de tacrolimus y la expresión génica de TNF-α. Se llevó a cabo PCR en tiempo real para determinar la expresión del gen TNF-α y el gen de control interno 18S. Se determinó el genotipo de CYP3A5 mediante secuenciación directa.
Resultados. Se estudiaron seis pacientes con una mediana de edad de 14.5 años. Se encontró una correlación negativa entre la concentración de tacrolimus por punto de farmacocinética y la media correspondiente de la expresión génica de TNF-α. Hubo tendencia a la disminución de TNF-α ante niveles altos de tacrolimus.
Conclusiones. Existe una correlación negativa entre la concentración de tacrolimus y la expresión génica de TNF-α. La expresión de TNF-α no se modificó según el genotipo de CYP3A5.
Palabras clave: tacrolimus, farmacocinética, farmacodinamia, TNF-α, trasplante renal, inmunosupresión.
]]> Abstract
Background. Tacrolimus is a widely used immunosuppressant in renal transplant patients. Drug monitoring is performed by measuring trough levels. Pharmacodynamic monitoring is used to evaluate the biological effect.
The aim of the study was to determine the relationship between tacrolimus area-under concentration vs. time curve (AUC) and the gene expression of tumor necrosis factor alpha (TNF-α) in children with renal transplant.
Methods. An experimental, cross-sectional study was performed in children with renal transplant at 3 months after transplant. An 8-h pharmacokinetic-pharmacodynamic profile was obtained. Gene expression of TNF-α and internal control of 18s rRNA was performed by real-time PCR. CYP3A5 genotype was obtained by direct sequencing.
Results. Six patients were included with a median age of 14.5 years. A negative correlation was found between tacrolimus pharmacokinetics and TNF-α gene expression. There was a trend of low TNF-α with high tacrolimus blood levels.
Conclusions. There is a negative correlation between tacrolimus concentration and TNF-α gene expression. TNF-α gene expression was not modified by CYP3A5 genotype.
Key words: tacrolimus, pharmacokinetics, pharmacodynamics, TNF-α, renal transplant, immunosuppression.
Introducción
El trasplante renal es el mejor tratamiento para pacientes pediátricos con enfermedad renal crónica terminal (ERCT), ya que no solamente resuelve la sintomatología urémica sino también permite una mejoría significativa del retardo del crecimiento esquelético, maduración sexual, desempeño cognitivo y psicosocial. La calidad de vida del paciente pediátrico con un injerto renal funcional siempre es superior a cualquier método dialítico existente.1
]]> El tratamiento con trasplante ofrece mejor supervivencia que la diálisis en cualquier grupo de edad de pacientes pediátricos. Se describe hasta 95% de supervivencia del injerto a 5 años del trasplante, mientras que los pacientes sometidos a procedimientos dialíticos presentan una supervivencia de 80%.El tacrolimus (Tac) es un medicamento con estrecho índice terapéutico que se emplea para prevenir el rechazo en los trasplantes de órganos sólidos. Requiere un cuidadoso manejo en el ajuste de la dosis empleada para obtener niveles terapéuticos. Ejerce su mecanismo de acción mediante la unión a una proteína intracelular llamada proteína de unión a FK (FKBP-12, del inglés FK binding protein 12). Una vez formado el complejo de FKBP-tacrolimus junto con calcio, se produce la inhibición selectiva de la calcineurina, enzima que normalmente actúa como una fosfatasa de ciertas proteínas nucleares reguladoras. Una de ellas es el factor nuclear de linfocitos T activados (NFAT) que, en condiciones normales, al ser desfosforilado, pasa a través de la membrana nuclear. De esta manera se inhibe la expresión de diversos genes involucrados en la activación de las células T, incluyendo el gen de la interleucina 2 (IL-2), su receptor, el interferón gamma (IFN-γ), el factor estimulante de colonias de granulocitos y macrófagos (GM-CSF), el factor de necrosis tumoral alfa (TNF-α) y los protooncogenes H-ras y c-myc. Al mismo tiempo se lleva a cabo la promoción del factor transformador de crecimiento beta (TGF-β), que también inhibe a la IL-2, con la consiguiente disminución en la proliferación de linfocitos T citotóxicos y la limitación en la producción de citocinas. Sin embargo, también provoca el desarrollo de fibrosis intersticial, que es la principal causa de nefrotoxicidad relacionada con los inhibidores de la calcineurina. El grado de inhibición de la actividad de la calcineurina y la producción de IL-2 podría reflejar el balance entre una inmunosupresión excesiva o deficiente.2,3
El tacrolimus es metabolizado por sistemas enzimáticos microsomales del citocromo P-450 IIIA (CYP3A4 y CYP3A5) hallados tanto en el tracto gastrointestinal como en el hígado. La dosis de tacrolimus requerida para alcanzar niveles terapéuticos depende del tipo de polimorfismo en la enzima CYP3A5. Aquellos pacientes que expresan la enzima, requieren dosis mayores.4
El monitoreo terapéutico del tacrolimus se lleva a cabo determinando las concentraciones mínimas, también conocidas como niveles en valle. Sin embargo, esto ha sido cuestionado, ya que se presentan algunos casos de toxicidad y rechazo, aun cuando las concentraciones mínimas se encuentran dentro del límite considerado como aceptable. Diversos estudios han demostrado una adecuada correlación entre la concentración en sangre y el área bajo la curva (ABC) de concentración plasmática contra tiempo, y que dicha correlación puede mejorar mediante el uso de diferentes tiempos de muestreo.2,5-7 Cabe destacar que la monitorización farmacocinética no refleja la actividad biológica del fármaco.
En los últimos años se ha propuesto la monitorización farmacodinámica como una nueva estrategia para proveer información acerca del efecto biológico específico ejercido por el mecanismo de acción del tacrolimus.8
Sobre vigilancia farmacodinámica se tienen varios reportes para ciclosporina (CsA), otro inhibidor de la calcineurina, y se ha reportado que la concentración máxima (Cmáx) -que se alcanza aproximadamente a las 2 horas- se relaciona con el nivel de inmunosupresión medido como inhibición de calcineurina en linfocitos.9
Giese y colaboradores, en 2004, mostraron que existe una correlación entre el nivel de CsA en sangre y la supresión de IL-2, TNF-α y GM-CSF hasta de 85%, lo que representa un enfoque para evaluar la efectividad biológica de CsA, permitiendo individualizar el régimen inmunosupresor.10
La monitorización farmacodinámica se aplica como un método adicional para brindar información acerca del impacto biológico de la CsA en pacientes trasplantados, de tal manera que la inhibición de calcineurina en linfocitos se correlaciona de manera inversa con las concentraciones sanguíneas de CsA. La máxima inhibición de calcineurina ocurre dos horas posteriores a la toma inicial en 90% de los pacientes.11-13 Se han realizado estudios farmacodinámicos con Tac en población adulta, y se ha sugerido que la expresión residual de los genes regulados por NFAT podría ser un método farmacodinámico para monitorizar a pacientes con trasplante renal tratados con Tac, ya que se puede identificar baja o alta inmunosupresión con base en su relación con la presencia de infecciones o rechazo agudo al injerto.14
El objetivo del presente trabajo fue determinar la correlación existente entre el área bajo la curva (ABC) de la concentración plasmática del Tac contra el tiempo y la expresión génica de TNF-α regulado por NFAT, en niños con trasplante renal.
Métodos
]]> Se realizó un estudio transversal experimental analítico, aprobado por las Comisiones de Investigación y Ética del Hospital Infantil de México Federico Gómez (protocolo HIM 2011/026, SSA 949).Se invitó a participar a pacientes pediátricos del Hospital Infantil de México Federico Gómez (HIMFG) de cualquier sexo y grupo etáreo, con diagnóstico de enfermedad renal crónica terminal y trasplante renal con un mínimo de seis meses de evolución posterior al evento quirúrgico.
Criterios de inclusión
• Pacientes de cualquier sexo y edad entre 3 y 18 años con 3 meses de trasplante renal en HIMFG
• Inmunosupresión establecida con tacrolimus
• Función estable del injerto (nivel sérico de creatinina ≤0.3 mg/dl al egreso del trasplante renal, sin
alteración metabólica, clínicamente estable)
• Sin ajustes en la terapia inmunosupresora tres meses previos a la toma de la muestra
• Sin infección aparente al momento del estudio
• Participación voluntaria en el estudio mediante una carta de consentimiento informado del padre o tutor y de asentimiento de cada niño
Criterios de exclusión
]]> • Pacientes con trasplante renal con administración de tacrolimus en dosis diferentes en cada toma o intervalo de administración diferente a cada 12 horas
• Administración concomitante de fármacos que alteren las concentraciones plasmáticas de tacrolimus, con excepción de verapamilo
• Pacientes con hepatopatías de cualquier índole
Criterios de eliminación
• Pacientes con alteración de pruebas de función hepática al momento del estudio o niveles elevados de colesterol o triglicéridos, que pudieran generar alteraciones en la medición plasmática de tacrolimus y otros parámetros séricos
• Pacientes con infecciones recientes o con sospecha de cualquier tipo de infección que pudiera modificar el nivel de inmunosupresión
Se registraron las siguientes variables: edad, sexo, exploración física completa, esquema y dosis de inmunosupresión completo en dosis ponderal, tratamiento concomitante con antihipertensivos, profilaxis antimicrobiana y aportes de electrolitos.
Con respecto a la farmacocinética y farmacodinamia, se llevó a cabo en un intervalo de 8 horas en todos los pacientes, desde la toma inicial del fármaco a las 8:00 am hasta las 4:00 pm. Se tomaron seis puntos de muestreo a diferentes tiempos (a las 0, 1, 2, 4, 6 y 8 h).
En cada punto se procesó una muestra de 4 a 5 ml de sangre total en un tubo con EDTA. En cada muestra fue determinada la concentración plasmática de tacrolimus, así como la expresión génica de TNF-α. Adicionalmente, en la primera muestra se llevó a cabo el procedimiento para la obtención de ADN a partir de leucocitos, y la posterior determinación del genotipo para CYP3A5. Las muestras fueron almacenadas a 4ºC hasta su procesamiento para la determinación de niveles plasmáticos. El resto se llevó a cultivo celular. En la muestra 0 se tomó también creatinina sérica y pruebas de función hepática. La velocidad de filtración glomerular se estimó con la fórmula de Schwartz.15-17
]]> Determinación de niveles de tacrolimusLa determinación se realizó en sangre total, mediante un kit comercial (Architect System, Abbot, IL) para análisis inmunoenzimático por partículas (CMIA).
Preparación de las muestras
La sangre contenida en tubos de EDTA se estimuló con 1 ml de RPMI-1640 (medio de cultivo), suplementado con 10% de suero fetal bovino y antibióticos, además de 100 ng/ml de acetato forbol miristato (PMA) y 5 mg/ml de ionomicina (Sigma, St. Louis, MO) por 3 horas. Posteriormente, se centrifugó por 15 seg a 10,000 rpm en estufa de CO2 a temperatura controlada de 37 ºC. Después de la lisis de glóbulos rojos y separación del sobrenadante, se almacenó a -70 ºC. Se llevó a cabo el lavado de glóbulos blancos con solución salina estéril en dos ocasiones, para su posterior almacenamiento en combinación con el reactivo RNA later (Ambion), a -70 ºC hasta el momento de extracción de ácido ribonucleico (ARN).
La extracción de ARN de glóbulos blancos se realizó con un kit comercial (RNAeasy mini kit, Qiagen). Posteriormente se realizó transcripción reversa para obtención del cDNA. La cuantificación de expresión del gen TNF-α y el gen de control interno 18s rRNA, se llevó a cabo mediante PCR en tiempo real, equipo PCR-TR 7500 (Applied Biosystems), con amplificación de secuencias mediante sondas comerciales (Applied Biosystems). La concentración del transcrito para los genes blanco fue calculada a partir de una curva estándar.
Determinación de genotipo
Se realizó mediante la extracción directa de DNA, para su posterior amplificación por PCR, purificación y secuenciación, según se ha descrito previamente.4
Análisis estadístico
Por medio de estadística de tipo descriptiva, se llevó a cabo la determinación del promedio y desviación estándar de aquellos datos con distribución normal. En variables sin distribución normal se realizó el cálculo de medianas y rangos (mínimo y máximo).
Para algunas variables se realizó el cálculo de proporciones.
]]> Para el cálculo de correlación se realizó la prueba P de Spearman, al contar con distribución anormal de la población de estudio mediante el programa Graph Pad Prism Versión 5.0. Para determinar la comparación existente entre el genotipo que expresa y el que no expresa el gen CYP3A5 con parámetros farmacocinéticos, se utilizó la U-Mann-Whitney en SPSS versión 16.Resultados
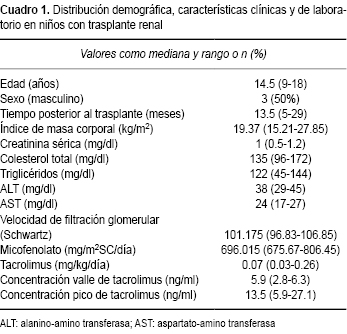
Se evaluaron seis pacientes (Cuadro 1). La mediana de edad fue de 14.5 años con valor mínimo de 9 años y máximo de 18 años. La mediana de tiempo posterior al trasplante de 13.5 meses con valor mínimo de 5 meses y máximo de 29 meses.

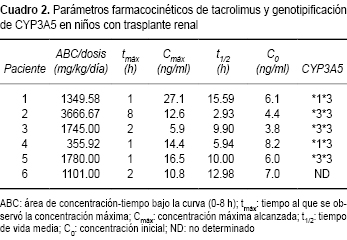
Los resultados del estudio farmacocinético se muestran en el Cuadro 2.
]]>
En la curva de concentración plasmática de tacrolimus y expresión génica de TNF-α contra tiempo (promedio y error estándar), se observa que existe una tendencia a la disminución de los niveles de TNF-α ante los niveles más altos de tacrolimus (Figura 1). Cabe destacar la amplia desviación estándar en cada punto, que obedece al escaso número de pacientes.
]]>

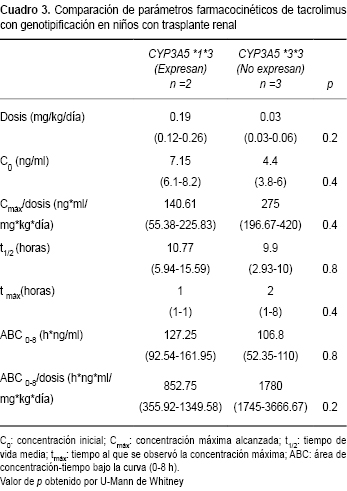
De los pacientes incluidos en el estudio, se llevó a cabo determinación de genotipo para CYP3A5 solamente en cinco, ya que en uno de ellos no se contó con una muestra adecuada y se obtuvo una lectura errónea del secuenciador. En tres casos no se observó expresión del citocromo (homocigotos GG-*3*3), y en dos casos la expresión del mismo (heterocigoto AG-*1*3). Se muestra la distribución del genotipo por grupos en comparación con la farmacocinética en cada paciente (Cuadro 3). No se encontraron diferencias estadísticamente significativas en las variables estudiadas, según el genotipo de CYP3A5. Sin embargo, los pacientes que expresaron la proteína requirieron dosis mayores de tacrolimus.
]]> La expresión génica fue determinada con el número de copias por microgramo de ARN de TNF-α, normalizado con el gen control de 18s rRNA. Se muestra la dispersión de puntos de la totalidad de pacientes del LN de TNF-α/18s rRNA contra las concentraciones de tacrolimus en todos los puntos de la farmacocinética considerando el tiempo de administración. Hubo correlación negativa entre la concentración de tacrolimus y la expresión de TNF-α, con r =-0.07, sin alcanzar diferencia estadísticamente significativa. Se observó que, en efecto, la concentración de TNF-α disminuye en tanto las concentraciones de tacrolimus son mayores, con los más altos niveles al inicio del estudio farmacocinético
Tomando en consideración las medias de concentración de cada punto de la farmacocinética con respecto al LN TNF-α /18s rRNA, se observó que en la dispersión de puntos existe una correlación negativa entre la concentración de tacrolimus de manera global por punto de farmacocinética con respecto a la media correspondiente al mismo punto de LN TNF-α. Aplicando r de Spearman se obtuvo r =-0.498 con p =0.17 (Figuras 2 y 3).

]]>

Discusión
Los resultados obtenidos son similares a los reportados por Sommerer y colaboradores en estudios realizados en adultos. En ellos, se comparó la farmacocinética con la farmacodinamia de inhibidores de calcineurina en cuanto a una correlación inversa entre la administración de CsA o Tac con la determinación de expresión génica de citocinas inflamatorias.11-14 En el presente estudio no se observó una asociación significativa entre ambos parámetros. Tampoco fue posible recolectar suficiente muestra para generar normalidad y significancia estadística en la distribución. Sin embargo, la metodología fue la adecuada para la determinación de la farmacocinética y el cultivo celular para la extracción de RNA y posterior cuantificación de expresión génica. Es interesante mencionar que, según la literatura, hay evidencia de que la vigilancia de los inhibidores de calcineurina con niveles plasmáticos aislados no es suficiente para la individualización de la dosis por paciente y que el factor genético, con identificación de polimorfismos de CYP3A5 y MDR1, además de parámetros farmacocinéticos completos y la expresión génica de genes producidos por linfocitos, es fundamental para la prevención de rechazo agudo, infecciones, nefrotoxicidad y disfunción del injerto a largo plazo.
Es importante considerar que, en el presente estudio, el número de pacientes incluido fue escaso, por lo que las diferencias no resultaron estadísticamente significativas. Sin embargo, se observó la tendencia a una correlación inversa con respecto a los niveles de tacrolimus en comparación con la expresión de TNF-α.
Es necesario realizar estudios de este tipo en población mexicana con mayor número de pacientes pediátricos para determinar el potencial de la cuantificación de la expresión génica como parámetro farmacodinámico de vigilancia del tacrolimus, con la finalidad de lograr la individualización de la inmunosupresión.
Financiamiento
Este proyecto fue financiado con Fondos Federales, protocolo HIM/2011/026
REFERENCIAS
1. Danovich GM. Handbook of Kidney Trasnplantation. Philadelphia: Lippincott Williams & Wilkins; 2010. [ Links ]
2. Alberú-Gómez J, Morales-Buenrostro LE, Abbud-Filho M. Trasplantomecum Renal. Barcelona: Permanyer; 2011. [ Links ]
3. Reyes-Pérez H, Medeiros-Domingo M. Uso de tacrolimus en pediatría. Bol Med Hosp Infant Mex 2006;63:276-285. [ Links ]
4. García-Roca P, Medeiros M, Reyes H, Rodríguez-Espino BA, Alberú J, Ortiz L, et al. CYP3A5 polymorphism in Mexican renal transplant recipients and its association with tacrolimus dosing. Arch Med Res 2012;43:283-287. [ Links ]
]]>5. Midtvedt K, Fauchald P, Bergan S, Høieggen A, Hallan S, Svarstad E, et al. C2 monitoring in maintenance renal transplant recipients: is it worthwhile? Transplantation 2003;76:1236-1238. [ Links ]
6. Einecke G, Mai I, Fritsche L, Slowinski T, Waiser J, Neumayer HH, et al. The value of C2 monitoring in stable renal allograft recipients on maintenance immunosuppression. Nephrol Dial Transplant 2004;19:215-222. [ Links ]
7. Morris RG, Russ GR, Cervelli MJ, Juneja R, McDonald SP, Mathew TH. Comparison of trough, 2-hour, and limited AUC blood sampling for monitoring cyclosporin (Neoral) at day 7 post-renal transplantation and incidence of rejection in the first month. Ther Drug Monit 2002;24:479-486. [ Links ]
8. Sommerer C, Giese T, Meuer S, Zeier M. New concepts to individualize calcineurin inhibitor therapy in renal allograft recipients. Saudi J Kidney Dis Transpl 2010;21:1030-1037. [ Links ]
9. Halloran PF, Helms LM, Kung L, Noujaim J. The temporal profile of calcineurin inhibition by cyclosporine in vivo. Transplantation 1999;68:1356-1361. [ Links ]
]]>10. Giese T, Zeier M, Schemmer P, Uhl W, Schoels M, Dengler T, et al. Monitoring of NFAT-regulated gene expression in the peripheral blood of allograft recipients: a novel perspective toward individually optimized drug doses of cyclosporine A. Transplantation 2004;77:339-344. [ Links ]
11. Sommerer C, Konstandin M, Dengler T, Schmidt J, Meuer S, Zeier M, et al. Pharmacodynamic monitoring of cyclosporine A in renal allograft recipients shows a quantitative relationship between immunosuppression and the occurrence of recurrent infections and malignancies. Transplantation 2006;82:1280-1285. [ Links ]
12. Sommerer C, Giese T, Schmidt J, Meuer S, Zeier M. Ciclosporin A tapering monitored by NFAT-regulated gene expression: a new concept of individual immunosuppression. Transplantation 2008;85:15-21. [ Links ]
13. Sommerer C, Morath C, Giese T, Meuer S, Zeier M. Activity of nuclear factor of activated T cells is independent of the number of peripheral lymphocytes in FTY720-treated patients. Transplant Proc 2008;40:1416-1418. [ Links ]
14. Sommerer C, Zeier M, Meuer S, Giese T. Individualized monitoring of nuclear factor of activated T cells-regulated gene expression in FK506-treated kidney transplant recipients. Transplantation 2010;89:1417-1423. [ Links ]
]]>15. Schwartz GJ, Haycock GB, Spitzer A. Plasma creatinine and urea concentration in children: normal values for age and sex. J Pediatr 1976;88:828-830. [ Links ]
16. Schwartz GJ, Brion LP, Spitzer A. The use of plasma creatinine concentration for estimating glomerular filtration rate in infants, children, and adolescents. Pediatr Clin North Am 1987;34:571-590. [ Links ]
17. Schwartz GJ, Furth SL. Glomerular filtration rate measurement and estimation in chronic kidney disease. Pediatr Nephrol 2007;22:1839-1848. [ Links ]
]]>