
Study for rehabilitation of a vinasses treatment plant using a polyacrylamide (PAM) polymer flocculant
Gilberto ÍÑIGUEZ y Rosaura HERNÁNDEZ
Universidad de Guadalajara, Departamento de madera, celulosa y papel. Km 15.5 carretera Guadalajara–Nogales. Las Agujas, Municipio de Zapopan, Jalisco. Apartado Postal 52–93. C.P. 45020, Guadalajara, Jalisco
Recibido octubre 2009
Aceptado julio 2010
RESUMEN
Se realizó un tratamiento primario por coagulación/floculación a vinazas tequileras para la rehabilitación de una planta de tratamiento; para ello se utilizó una poliacrila mida catiónica (PAM) como floculante. Se realizaron pruebas iniciales de laboratorio para conocer la concentración necesaria de PAM para obtener una buena formación de flóculos, por lo que se aplicaron concentraciones de 200, 300, 400, 500, 600, 700 y 800 mg de floculante/L de vinazas. Posteriormente se realizaron seis corridas por lote en un contenedor de 798 L para la coagulación/floculación de las vinazas. Los flóculos formados fueron recuperados en un separador cilíndrico rotatorio. La concentración de floculante fue entre 400 y 800 mg/L de vinazas. Por separado, en un tanque de acero inoxidable se recolectaron las vinazas tratadas. En cada corrida se determinó el pH, sólidos sedimentables, sólidos totales, sólidos suspendidos totales, sólidos disueltos totales y demanda química oxígeno a las vinazas con y sin tratamiento. También se realizó un balance entre los volúmenes de vinazas por tratar y de flóculos recuperados y vinazas tratadas. Con base en los parámetros estudiados y el rango de dosis utilizado, se encontró que a mayor dosis de floculante, mayor remoción de contaminantes, con una capacidad de recuperación de hasta 45.4 kg de flóculos/100 L de vinazas tratadas al utilizar 700 mg de floculante/L de vinazas. Con los resultados obtenidos se determinaron las condiciones más importantes de operación de la planta.
Palabras clave: vinazas de tequila, poliacrilamida, floculación, separación de sólidos.
ABSTRACT
This paper reports the results of a coagulation/flocculation study for the primary treatment of tequila vinasse, with the intention of rehabilitating a treatment plant using a cationic polyacrylamide (PAM) polymer flocculant. The PAM concentration required to obtain the required floc formation was determined with seven different flocculant concentrations (200, 300, 400, 500, 600, 700 y 800 mg/L). In a second experiment, six pilot–scale batch runs were conducted in a 798–liter container using PAM concentrations of between 400 and 800 mg/L of vinasse. The flocculated solids were separated in a rotating screen separator and the treated vinasse collected in a 327–liter stainless steel tank. For each batch run, the parameters pH–value, settleable solids, total solids, total suspended solids, total dissolved solids and chemical oxygen demand were evaluated for both treated and non–treated vinasse. In addition, the balance between the untreated vinasse volume as related to the recovered flocculated solids and the residual liquid vinasse was determined. Based on the observed parameters within the range of the PAM concentrations used, it was concluded that the higher the floculant dose, the higher the removal of vinasse pollutants, recovering up to 43.7 L of flocs/100 L of treated vinasse when 700 mg of PAM/L of vinasse was used. These results proved very useful for optimizing the operational condition of the vinasse treatment plant.
Key words: tequila vinasses, polyacrylamide, flocculation, solids separation.
INTRODUCCIÓN
]]> La industria tequilera es de gran importancia económica para México y principalmente para el estado de Jalisco, donde se localiza la mayoría de las empresas certificadas para la fabricación de tequila. En 2008, el Consejo Regulador del Tequila (CTR 2008) tenía reportadas 146 destilerías de tequila entre grandes, medianas, pequeñas y micros. A pesar de la crisis económica que se vive en México, este sector industrial ha presentado un aumento considerable en su producción en los últimos cinco años, de 97.2 millones de litros de tequila en 2003, a 231.2 millones de litros reportados en septiembre de 2008 (40 % Alc. Vol., CTR 2008). La creciente producción de tequila trae consigo el aumento de subproductos como el bagazo y las vinazas. De acuerdo a Cedeño (1995), se generan 1200 g de bagazo y entre 7 y 10 L de vinazas por litro de tequila. De acuerdo a lo anterior, para septiembre de 2008 se generaron entre 1618 y 2312 millones de litros de vinazas.Las vinazas son las aguas residuales producto de la destilación del tequila; tienen un alto contenido de materia orgánica, con una demanda química de oxígeno (DQO) superior a 38 215 mg/L y sólidos totales (ST) superiores a 21 883 mg/L, y poseen pH bajo, de 3.5–3.9 (Íñiguez y Peraza 2007). Se descargan a una temperatura de 90 °C, lo que las convierte en un contaminante térmico. Su color probablemente se deba al pigmento café oscuro de las melanoidinas, la presencia de fenoles, caramelo y melanina, propios del licor de destilerías de melazas (Sirianuntapiboon et al. 1988, Godshall 1999, Kalavathi et al. 2001), que se pueden formar por las reacciones amino–carbonil de Maillar (Wedzicha y Kaputo 1992) al hidrolizar por calentamiento los azúcares de las pencas de agave.
El alto contenido de materia orgánica y el color reducen la penetración de luz en ríos, lagos y lagunas, haciendo que disminuya la actividad fotosintética de organismos acuáticos; esto disminuye la concentración de oxígeno disuelto, lo que causa un deterioro de la vida acuática. Por otro lado, utilizar los suelos para la disposición final de las vinazas tequileras sin tratamiento alguno puede favorecer la presencia de organismos patógenos para algunos cultivos. Amador (2002) reportó que el uso de vinazas tequileras en riego de plantas de agave (Agave tequilana weber var. Azul) facilitó la presencia de bacterias fitopatógenas en plantas atacadas por Fusarium oxysporum y Fusarium solani. En vinazas de la destilación del alcohol etílico, Bautista y Durán de Bazúa (1998) concluyeron que es mejor someterlas a un tratamiento biológico para después aplicarlas en suelos, debido a que las formas químicas del carbono son moléculas con propiedades coloidales que mejoran las propiedades físicas, químicas y biológicas de los suelos.
Actualmente, las autoridades intentan frenar el impacto ambiental de la industria tequilera y obligan a los responsables a que tomen medidas para disminuir la contaminación. La ley establece (SEMARNAT 1996) que para descargar aguas residuales en un cuerpo de agua, éstas no deben contener más de 150 mg/L de DBO5, 150 mg/L de sólidos suspendidos totales (SST) y 1 mL/L de sólidos sedimentables (SS), valores que las vinazas tequileras rebasan por mucho, lo que puede provocar costosas multas y, en última consecuencia, el cierre de las instalaciones. Depende de las condiciones, pero por lo general, el tratamiento de aguas residuales –como es el caso de las vinazas tequileras– debe incluir como primer paso la separación de sólidos, constituidos principalmente por partículas de agave (celulosa y pectinas), células de levaduras, así como proteínas y algunos ácidos orgánicos (Cedeño 1995).
Pocas compañías tequileras, en particular las grandes, realizan actualmente algunos esfuerzos para cumplir con la norma ambiental de descarga. Sin embargo, las tecnologías implementadas, como la termoevaporación y la ósmosis inversa, distan mucho de ser sustentables; de cualquier manera, estos procesos requieren forzosamente de un pretratamiento para la remoción de sólidos sedimentables y suspendidos. El objetivo del presente trabajo consistió en realizar los estudios pertinentes que sirvieran de base para la rehabilitación de una planta de tratamiento de vinazas tequileras. El tratamiento estudiado fue por coagulación/floculación a fin de reducir la carga orgánica que dificulta el manejo y procesos posteriores de tratamiento, o la saturación por materia orgánica en suelos que entorpecería el aprovechamiento de nutrientes.
MATERIALES Y MÉTODOS
Origen de las vinazas
Vinazas atípicas. Las vinazas que se utilizaron para el presente estudio son consideradas atípicas por la forma en que se extraen los jugos de las cabezas de agave. El proceso es el siguiente: en la fábrica de tequila que facilitó el estudio, las cabezas de agave son cocidas a 110 °C durante 36 horas en 5 hornos de mampostería, 3 hornos de 50 toneladas cada uno y 2 de 25 toneladas. Después del cocimiento, las cabezas de agave pasan por una desgarradora (Molinos Onofre®) consistente en una pequeña flecha provista de varias hileras de cortadoras a manera de "cabezas de hacha" alineadas horizontalmente, con otra hilera de cabezas de hachas colocada en forma fija frente a la flecha en movimiento. De la desgarradora, el material destrozado pasa por dos desmeduladoras en serie, consistentes en cilindros de acero inoxidable con un eje central provisto de varias aspas para facilitar el desprendimiento de la médula y el transporte del material destrozado de un extremo a otro. Los mismos cilindros están provistos, a lo largo de la parte alta, de llaves de agua para la extracción de los azúcares fermentables mediante el lavado del material destrozado. La parte baja de los cilindros está provista de una malla por donde salen los jugos en conjunto con la médula desprendida de las fibras del agave. Al final de los dos cilindros se encuentra una prensa de rodillos para extraer lo más posible de azúcares a las fibras de agave. El jugo extraído pasa a fermentación y destilación, de donde se obtuvieron las vinazas para ser tratadas conforme a la figura 1.
Vinazas típicas. Las vinazas típicas provienen por lo general del siguiente proceso: las cabezas de agave son cocinadas en hornos de mampostería o autoclaves, para luego pasarse por una desgarradora con las mismas características de la descrita en el párrafo anterior. Después de la desgarradora, el material destrozado pasa por una serie de molinos a manera de rodillos donde el material destrozado es lavado con agua y exprimido para extraer al máximo los azúcares fermentables para la elaboración del tequila.
]]> Pruebas de laboratorioLas pruebas de laboratorio se realizaron con vinazas atípicas recolectadas de la fosa de captación, provista de un inyector de aire para asegurar la homogeneidad y el mezclado de las mismas durante la toma de muestras o extracción de la fosa.
Tamaño de partícula. Para el análisis físico del tamaño de partículas de las vinazas tequileras se utilizaron cinco cribas de aro de laboratorio (20.3 cm de diámetro por 7.6 cm de altura) con aberturas de malla de 0.25, 0.50, 1.0, 1.98 y 4.76 mm. Por cada una de ellas se pasó un litro de muestra de vinazas. Se determinó el contenido de sólidos totales (ST, mg/L) de las muestras, antes y después de pasarse por la criba, para establecer la relación de ST retenidos por tamaño de abertura de la malla.
Pruebas de floculación. Para las pruebas iniciales de floculación se utilizó un floculante patentado de poliacrilamida catiónica [PAM (SNF Floerger®), Francia]. La viscosidad de la PAM fue de 1190 cps, viscosidad UL de 5.55 cps y el porcentaje de sólidos no volátiles de 50.6 %. Se utilizaron concentraciones de 200, 300, 400, 500, 600, 700 y 800 mg de floculante/L de vinazas. En vasos de precipitados de plástico de 2 L se mezclaron lentamente con una propela a aproximadamente 30 revoluciones por minuto (rpm) durante 10 minutos, muestras de 1 L de vinazas con pequeñas cantidades de PAM hasta alcanzar la concentración final deseada de acuerdo a la dosis aplicada.
Pruebas de neutralización. Las pruebas de neutralización se realizaron con muestras de vinazas con y sin tratamiento. Para ello se utilizó hidróxido de sodio (NaOH) y cal viva (CaO). El volumen de las muestras fue de 1 L, que se mantuvo en agitación constante en una parrilla de agitación magnética durante la aplicación del reactivo hasta alcanzar valores de pH por arriba de 10. Por cada adición de reactivo se registraron los gramos añadidos, así como los cambios de pH; para dichas mediciones se utilizó un potenciómetro Hanna (modelo 211 de Hanna Instruments, Portugal).
Pruebas piloto
La figura 1 presenta en forma esquemática el desarrollo de las pruebas piloto por lote. Este esquema consistió de las siguientes partes: fosa recolectora de vinazas, tanque de coagulación/floculación, filtro rotatorio y tanque de vinazas tratadas. Las características de los equipos fueron las siguientes: tanque de coagulación/floculación de acero inoxidable de 798 L de capacidad, con fondo cónico (39°) y una válvula de descarga de 7.62 cm de diámetro en la parte baja para conectarse con un separador cilíndrico rotatorio a través de un tubo de PVC (Íñiguez y Peraza 2007). Del separador, el líquido filtrado fue recolectado en un tanque de acero inoxidable de 327 L de capacidad. En el tanque de coagulación/floculación, las vinazas se mezclaron con el floculante con la ayuda de un difusor en forma de cruz, hecho con tubos de cobre (1.6 cm de diámetro) perforados por una de las caras; por medio de un compresor de 6 galones y 1.5 HP, se distribuyó el aire en el fondo del tanque. El separador de acero inoxidable tenía 63 cm de diámetro y 1.22 m de largo, provisto de una malla de 0.2 mm de abertura. El cilindro rotatorio estaba soportado en un par de flechas movidas por un motor de 0.5 HP. La velocidad del cilindro fue de 12 rpm.
Corridas en planta piloto
Para los estudios por lote se realizaron seis corridas, la primera, segunda y sexta con 700, 800 y 400 mg de floculante/L de vinazas respectivamente y la tercera, cuarta y quinta con 600; en cada una de ellas se trabajó de la siguiente manera: las vinazas homogeneizadas en la fosa de captación se bombearon hasta el contenedor de coagulación/floculación, de donde se tomó una muestra de 5 litros de vinazas sin tratar una vez mezcladas con aireación. La adición del floculante hasta la dosis deseada (400, 600, 700 y 800 mg de floculante/L de vinazas) se hizo por medio de la abertura de una llave de paso del contenedor mientras las vinazas eran mezcladas con aire. Después de la adición del floculante, el líquido se dejó decantar durante 45 minutos antes de abrir la llave para la separación de flóculos en el separador cilíndrico rotatorio; el tiempo de descarga fue de 30 minutos. Del sobrenadante se tomaron muestras para el análisis químico posterior (SS, ST, SST, SDT –sólidos disueltos totales–, y DQO). En cada una de las corridas se tomaron muestras de vinazas con y sin tratamiento para el análisis de pH, SS, ST, SST, SDT y DQO. En cada corrida se hizo un balance entre el volumen de vinazas sin tratar y el volumen de flóculos recuperados y vinazas tratadas. De una muestra compuesta de flóculos recuperados se determinó el contenido de agua, nitrógeno total Kjeldahl (NTK), cenizas, materia orgánica, carbono orgánico total, pH, conductividad, total de P, K, Ca, Mg, Na, Cu, Be, Al, Ba, Cd, Cr, Pb, Co, Fe, Mn, Mo, Ni, Ag, Zn, Sb, Tl y V.
Análisis químico
]]> Para el análisis de SS las muestras se vertieron en conos Imhoff de un litro para dejarse sedimentar durante 45 minutos. Se utilizó una varilla de vidrio para retirar los sólidos floculados pegados en las paredes del cono, dejando reposar los flóculos por 15 minutos más para completar una hora de prueba. Los resultados se leyeron y reportaron en mL/L (APHA 1992). Los ST se determinaron mediante el calentamiento y secado de muestras, calculándolos en mg/L al comparar el peso inicial con el final (APHA 1992). Para medir la concentración de SST se pesaron filtros de fibra de vidrio, puestos previamente a peso constante; se colocaron los filtros en un embudo de filtración sujeto a vacío y se pasó un volumen conocido de la muestra a través de los filtros, posteriormente se secaron en una estufa, se enfriaron y se pesaron. La concentración de SST se calculó con base en la diferencia del peso previo y posterior al secado (APHA 1992). Los resultados se reportaron en mg/L. Los SDT se calcularon por la diferencia de los ST y SST (APHA 1992). La DQO fue determinada mediante un sistema de reflujo y un método colorimétrico (APHA 1992). Para medir la temperatura de las muestras se utilizó un termómetro de mercurio de escala Celsius de 0 a 150 °C, el cual se sumergió en la muestra; cuando la columna de mercurio se estabilizó, se tomó la lectura. Los valores de pH fueron determinados con un potenciómetro Hanna (modelo 21 Hanna Instruments, Portugal) en escala de unidades estándar de 0 a 14. Para los flóculos, el contenido de agua se determinó mediante el secado de una muestra por 24 h a 105 °C, comparando el peso inicial y final; el resultado se reporta en % (AOAC 1990). El NTK se determinó de acuerdo a la técnica descrita por la AOAC (1990), utilizando mezcla selénica como catalizador y ácido bórico a 4 % para captar el amoniaco. Para el análisis de cenizas se puso una muestra de peso conocido en una mufla a 550 °C por 2 h; el peso del material residual se consideró como el contenido de cenizas. El material volátil fue considerado como materia orgánica (Bateman 1970). El pH y la conductividad de las muestras sólidas fueron determinados de extractos en agua en una relación peso/volumen 1:5 (CWMI 1995). El pH se midió con un potenciómetro Hanna y la conductividad se determinó con un medidor modelo 407303 Extech, Instruments. El carbono orgánico total (COT) fue calculado mediante la siguiente ecuación (Golueke 1977):
El total de P, K, Ca, Mg, Na, Cu, Be, Al, Ba, Cd, Cr, Pb, Co, Fe, Mn, Mo, Ni, Ag, Zn, Sb, Tl y V, fue determinado por espectroscopía de emisión atómica en plasma, acoplado inductivamente en un espectrómetro de emisión atómica (modelo FMA–03), previa digestión de las muestras con agua regia de acuerdo a la técnica descrita por el TMECC (2001).
RESULTADOS Y DISCUSIÓN
Vinazas
De acuerdo a los datos recabados en la fábrica de tequila de donde se tomaron las vinazas para su estudio, la relación de L de vinazas generados/L de tequila producido fue de 10–10.7, a diferencia de Cedeño (1995) de 7–10 L de vinazas/L de tequila. Esta tequilera produce entre 7000 y 8000 L de tequila/día y genera entre 75 000 y 80 000 L de vinazas/día. Las descargas de vinazas provienen de cuatro alambiques de destilación, tres de los cuales tienen una capacidad de 5000 L cada uno (con una descarga por unidad aproximada de 3500 L de vinazas por corrida) y otro de 2500 L (con una descarga aproximada de 1500 L de vinazas por corrida).
Las características de las vinazas utilizadas en este estudio fueron las siguientes: pH 3.6, SS 943 mL/L, ST 38 473 mg/L, SST 14 138 mg/L, SDT 24 335 mg/L, DQO 55 916 mg/L.
Pruebas de laboratorio
Pruebas de floculación. En la figura 2 se presentan los resultados gráficos de cómo evolucionó la coagulación y formación de flóculos conforme se incrementaba la adición de PAM (200, 300, 400, 500, 600, 700 a 800 mg/L) en vinazas tequileras con pH de 3.8 y una concentración de ST de 39 630 mg/L. Íñiguez y Peraza (2007), trabajando en pruebas de laboratorio con muestras de 500 mL de vinazas, encontraron buenas formaciones de flóculos con concentraciones de PAM de 20 a 180 mg/L, pero con concentraciones de SS y ST de 150 mL/L y 26 267 mg/L, respectivamente. En pruebas con 200 L de vinazas de cinco fábricas diferentes de tequila, también tuvieron buenas formaciones de flóculos utilizando 200 mg/L de PAM, al tener concentraciones de SS desde 72 hasta 400 mL/L y de ST desde 21 883 hasta 41 578 mg/L. En vinazas con 900 mL/L de SS y 56 900 mg/L de ST se utilizó una concentración de 400 mg/L de PAM para tener una buena formación de flóculos, con remociones de SS y ST de 99.3 y 49.5 %, respectivamente.
]]>
Análisis físico de partículas. La figura 3 presenta el porcentaje de sólidos totales (ST) recuperados de muestras de vinazas sometidas a pruebas de filtración en mallas con abertura de 0.25, 0.50, 1.0, 1.98 y 4.76 mm. Como se puede observar en la figura, entre más cerrada es la malla, mayor es el porcentaje de ST recuperados, de tal manera que al utilizar una malla con una abertura de 0.25 mm se recuperó hasta 20.3 % de los ST; sin embargo, existe el inconveniente de una lenta velocidad de drenado, lo cual dificultaría la operación en planta para la remoción de ST. En cambio, como se puede apreciar en esta misma figura, al utilizar el floculante PAM, se recuperó hasta 45 % de los ST con la misma abertura de malla (0.25 mm) sin problemas de drenado, lo cual justifica su utilización para la remoción de una parte importante de los ST.

Pruebas de neutralización. La figura 4 presenta los cambios de pH para vinazas con y sin la adición de PAM al añadirse hidróxido de sodio (NaOH) y cal viva (CaO). Las vinazas para esta prueba tuvieron un pH de 3.8 y una concentración de ST de 23 519 mg/L (vinazas tratadas con PAM) y 39 630 mg/L (vinazas no tratadas). Las vinazas sin PAM necesitaron de mayores cantidades de NaOH y CaO para alcanzar valores de pH 11, lo que significa que el contenido de sólidos en las vinazas influye en el mayor consumo de reactivos. Por otro lado, para alcanzar valores de neutralización (pH 7) en las vinazas con y sin tratamiento, se requirió de menor cantidad de CaO que de NaOH, a pesar de que el segundo era grado reactivo. Para alcanzar pH 7 en vinazas tratadas con PAM, se requirieron 1.26 g/L de CaO y 1.7 g/L de NaOH. En cambio, en vinazas no tratadas con PAM, se requirieron 1.5 g/L de CaO y 1.95 g/L de NaOH. Esto definitivamente favorece la neutralización de vinazas al utilizar menos reactivo de un compuesto químico más barato. En la neutralización de vinazas obtenidas de la producción de alcohol a partir de la fermentación de mieles finales de caña de azúcar, Bermúdez et al. (2000) reportaron resultados inversos, ya que para neutralizar sus muestras de vinazas se requirió de menor cantidad de sosa cáustica que de cal viva (4.98 y 10 g/L, respectivamente).

Pruebas en planta piloto
Tratamiento por lote. El cuadro I presenta los resultados de seis corridas realizadas en las pruebas de planta piloto; se determinó la temperatura de las vinazas antes de la adición del floculante, así como pH, SS, ST, SST, SDT y DQO antes y después del tratamiento con diferentes dosis de PAM. En las corridas se consideró el volumen de vinazas tratadas para determinar el volumen de sólidos floculados recuperados y por diferencia conocer el volumen remanente de vinazas para neutralizarse o ser tratadas en un proceso posterior. También se determinó el peso de sólidos floculados separados, así como su contenido de humedad.
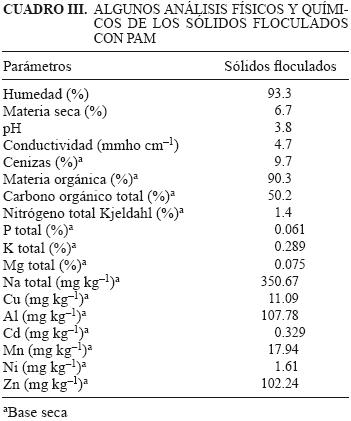
]]> El cuadro II presenta una síntesis de los resultados obtenidos en las seis corridas. De acuerdo con los resultados, en la figura 5 se ilustra la relación entre la concentración de ST y SS de las vinazas sin tratamiento, donde se aprecia que esta relación no es lineal: una alta concentración de ST no necesariamente implica tener una alta concentración de SS. En una muestra con 57 407 mg/L de ST se tuvo un valor de SS de 740 mL/L; en cambio con otra de 31 666 mg/L de ST, se tuvo inclusive un valor mayor de SS (850 mL/L). Estos resultados dan una idea de la heterogeneidad de las vinazas y lo poco práctico que es remover ST por simple sedimentación; en cambio, con la adición de PAM, la situación puede cambiar al removerse un buen porcentaje de los ST por floculación, con la obvia inclusión de los SS. El cuadro III presenta algunos análisis físicos y químicos que se les practicaron a los sólidos recuperados con el floculante PAM. Como era de esperarse estos sólidos contienen una gran cantidad de agua (93.3%) lo que puede dificultar su manejo posterior, sin embargo, pueden integrarse al proceso de compostaje del bagazo de agave, ya que la mayorías de las plantas de tequila han optado por este sistema de disposición del bagazo. Si a lo anterior se agrega el contenido de materia orgánica y elementos como N, P, K, Mg, Na, Cu, Al, Cd, Mn, Ni y Zn que contienen los sólidos recuperados, significa que la adición de estos sólidos al bagazo de agave mejorará las condiciones de compostaje y la calidad de la composta al final del proceso.
La figura 6 presenta la relación de dosis de PAM (mg/L), concentración y remoción de los ST en muestras de vinazas. En la figura se aprecia que a mayor dosis de PAM (mg/L), mayor remoción de ST; aparentemente, la concentración de ST en las vinazas sin tratamiento no influye en la remoción, ya que teniendo la misma dosis de floculante, en la cuarta corrida se removieron 12 185 mg/L (concentración inicial, 31 666 mg/L) y en la quinta 10 240 mg/L (concentración inicial, 57 407 mg/L).

La figura 7 presenta la relación de dosis de PAM (mg/L), concentración y remoción de los SS (mL/L) en muestras de vinazas. Se aprecia también que a mayor concentración de SS, mayor remoción, habiendo aplicado a las muestras la misma dosis de floculante. En las corridas 3, 4 y 5 –teniendo una concentración inicial de SS en vinazas de 927, 850 y 740 mL/L– se removieron 847, 818 y 707 mL/L, respectivamente.
]]>
La figura 8 presenta la relación de dosis de PAM (mg/L), concentración y remoción de la DQO (mg/L) en muestras de vinazas. Al igual que en los casos anteriores, a mayor dosis de floculante (mg/L), mayor remoción de DQO (mg/L). En este caso, los valores de remoción tuvieron que ver con la concentración inicial de la DQO (mg/L), de tal manera que con la misma dosis de PAM, a mayor concentración de DQO (mg/L), mayor valor de remoción. En las corridas 3, 4 y 5, en muestras con una DQO de 51 462, 41 280 y 87 123 mg/L, se removieron 13 205, 8600 y 23 323 mg/L, respectivamente.

La figura 9 presenta la relación de dosis de PAM (mg/L), concentración y remoción de los SST (mg/L). En esta figura se aprecia que la remoción de SST (mg/L) se vio influenciada también por el valor de la dosis del PAM (mg/L), de tal manera que a mayor dosis, mayor remoción de SST (mg/L), sin aparente influencia de la concentración inicial en las muestras de vinazas. En las corridas 3, 4 y 5, en donde se utilizó la misma dosis de PAM (mg/L), se tuvieron remociones (10 549, 11 674 y 10 029 mg/L, respectivamente) relativamente proporcionales a las concentraciones de SST (12 398, 13 063 y 10 917 mg/L, respectivamente).

La figura 10 presenta la relación de la dosis de PAM (ppm) y los sólidos floculados recuperados/100 L de vinazas. Como prueba de los resultados anteriores –en los que se vio que a mayores dosis de PAM (mg/L), mayores remociones de SS (mL/L), ST (mg/L), DQO (mg/L) y SST (mg/L)–, en esta figura se presenta que a mayor dosis de PAM, mayor recolección de L o kg de sólidos floculados/100 L de vinazas tratadas. En el tratamiento con 700 mg/L de PAM se recolectaron 43.7 L de sólidos/100 L de vinazas, mientras que con 400 mg/L se recolectaron 28.3 L. Por otro lado, en la figura 11 se muestra que a mayor dosis de floculante y mayor recolección de sólidos floculados/100 L de vinazas tratadas, menor volumen de vinazas remanentes por neutralizar.


Datos de operación para la planta de tratamiento. La planta tratadora de vinazas tiene una una fosa de captación de 88 m3 (4 × 2.65 × 8.3 m; profundidad, ancho y largo, respectivamente) y una generación de vinazas de 80 m3/día, por lo que no hay limitante para la captación de las aguas residuales. Se han acondicionado seis celdas de coagulación/floculación con una capacidad total de 15.6 m3. Cada celda cuenta con un sistema de desagüe individual, por lo que se tendrán que llenar y vaciar 5.1 veces para cumplir la carga de aguas residuales generadas. Esto implica que en una jornada de trabajo de ocho horas, el llenado y vaciado de las fosas se tendrá que realizar en 1.5 horas y la capacidad del separador de los sólidos tendrá que ser de 173 L/min. Si se considera que se generan 43.7 L de sólidos floculados por cada 100 L vinazas tratadas, se deberá contar con un sistema de recolección, traslado y disposición en compostaje de sólidos floculados de 75.6 L/min. Para la captación de vinazas tratadas se cuenta con una fosa de 56 m3 (2.45 × 3.86 × 5.96 m; profundidad, ancho y largo, respectivamente), pero dado que la generación de vinazas tratadas con 700 mg/L de PAM será de 58 080 L, se requerirá remover algunos litros de vinazas en una jornada de ocho horas. Los requerimientos para la neutralización de 58 080 L de vinazas remanentes de la floculación serán del orden de 73.2 kg de CaO (ver figura 4).
CONCLUSIONES
Los resultados obtenidos en esta investigación, en concordancia con experiencias previas, indicaron que para la óptima aplicación del floculante PAM y la eficiente remoción de contaminantes, es importante homogeneizar lo más posible las vinazas antes de iniciar el tratamiento de coagulación/floculación. Aplicar un exceso de floculante, aparte de la repercusión económica, trae consigo la formación de un flóculo pegajoso y de poca consistencia. La formación de un buen flóculo facilitó la separación de sólidos y líquido mediante la filtración. La neutralización de vinazas tratadas con PAM resultó más económica con CaO que con NaOH. La relación en la concentración de ST y SS en vinazas sin tratamiento, demostró que una alta concentración de ST no necesariamente implica tener una alta concentración de SS. Por otro lado en este trabajo se demostró que a mayor dosis de floculante, mayor remoción de ST, SS, SST y DQO, lo que significó una mayor recolección de L o kg de sólidos floculados/100 L de vinazas tratadas. La aplicación del floculante PAM a vinazas tequileras para la remoción de la mayor carga orgánica puede ser una alternativa técnica y económicamente viable, sobre todo para vinazas con alto contenido de SS y ST.
AGRADECIMIENTOS
Los autores expresan su agradecimiento al Ing. Carlos A. Hernández Ramos, dueño de la fábrica de tequila La Cofradía, por las facilidades y beca otorgadas para la realización de este trabajo de investigación.
]]> REFERENCIAS
Amador M. (2002). Efecto de vinazas en agave tequilero en la nutrición y su relación con problemas fitosanitarios. Tesis de Licenciatura. Departamento de fitotecnia. Universidad Autónoma Chapingo. Chapingo, Estado de México, México. [ Links ]
AOAC (1990). Official methods of analysis. 15a. ed. Association of Official Analytical Chemists. Washington, EUA. 11–18 pp. [ Links ]
APHA (1992). Standard methods for the examination of water and wastewater. 18a. ed. American Public Health Association, Washington, EUA. Secciones 5–8, 5–9. [ Links ]
Bateman J.V. (1970). Nutrición animal. Manual de métodos analíticos. Herrero Hermanos, México. pp. 146–149. [ Links ]
Bautista Z.F. y Durán de Bazúa C. (1998). Análisis del beneficio y riesgo potenciales de la aplicación al suelo de vinazas crudas y tratadas biológicamente. Rev. Int. Contam. Ambient. 14, 13–19. [ Links ]
Bermúdez S., Hoyos H. y Rodríguez P. (2000). Evaluación de la disminución de la carga contaminante de la vinaza de destilería por tratamiento anaerobio. Rev. Int. Contam. Ambient. 16, 103–107. [ Links ]
Cedeño C. M. (1995). Tequila production. Crit. Rev. Biotechnol. 15, 1–11. [ Links ]
CRT (2008). Consejo Regulador del Tequila. http://www.crt.org.mx. 06/11/2008. [ Links ]
CWMI (1995). Monitoring compost pH. Cornell Waste Management Institute. [en línea] http://cwmi.css.cornell.edu/composting.htm ~Large Scale Composting/Siting and Operation/Monitoring compost pH 29/10/2008. [ Links ]
Godshall M.A. (1999). Removal of colorants and polysaccharides and the quality of white sugar. En: Proceedings of the 6th International Symposium of the Association Andrew van Hook (AvH). Marzo 25, 1999. Reims, Francia, pp. 28–35. [ Links ]
Golueke C.G. (1977). Biological processing: composting and hydrolysis. En: Handbook of solid waste management (D.G. Wilson, Ed.). Van Nostrand Reinhold, Nueva York, pp. 197–225. [ Links ]
Íñiguez G. y Peraza F. (2007). Reduction of solids and organic load concentrations in tequila vinasses using a polyacrylamide (PAM) polymer flocculant. Rev. Int. Contam. Ambient. 23, 17–24. [ Links ]
Kalavathi D.F., Uma L. y Subramanium G. (2001). Degradation and metabolization of the pigment–melanoidin in distillery effluent by the marine cyanobacterium Oscillatoria boryana BDU 92181. Enzyme Microb. Tech. 29, 246–251. [ Links ]
SEMARNAT (1996). NOM–001–ECOL.SEMARNAT. Establece los límites máximos permisibles de contaminantes en las descargas de aguas residuales en aguas y bienes nacionales. Diario Oficial de la Federación. 11 de diciembre de 1996. [ Links ]
Sirianuntapiboon S., Somchai P., Ohmomo S. y Atthasampunna P. (1988). Screening of filamentous fungi having the ability to decolourize molasses pigments. Agric. Biol. Chem. 52, 387–392. [ Links ]
TMECC (2001). Method 04.12–E. Test methods for the examination of composting and compost. [en línea]. http://tmecc.org/tmecc 25/07/2009. [ Links ]
Wedzicha, B.L. y Kaputo M.T. (1992). Melanoidins from glucose and glycine: composition, characteristics and reactivity towards sulphite ion. Food Chem. 43, 359–367. [ Links ]
]]>