DESARROLLO DE UN MODELO EXPERIMENTAL PARA LA CARACTERIZACIÓN DE LA RESPUESTA FUNCIONAL DEL CORIOAMNIOS HUMANO
CLAUDIA VERÓNICA ZAGA CLAVELLINA
Dirección de Investigación, del Instituto Nacional de Perinatología (INPer).
ROSARIO LÓPEZ VANCELL
Departamento de Medicina Experimental, Facultad de Medicina, Universidad Nacional Autónoma de México, México, D.F.
ROLANDO MAIDA CLAROS ]]> Departamento de Neonatología del INPer.
JORGE BELTRÁN MONTOYA
Departamento de Ginecología y Obstetricia, del INPer Instituto Nacional de Perinatología, México, México, D.F.
FELIPE VADILLO ORTEGA
Dirección de Investigación, del Instituto Nacional de Perinatología (INPer).
Correspondencia
Dr. Felipe Vadillo Ortega
Instituto Nacional de Perinatología,
Montes Urales 800, Lomas de Virreyes, México, D.F. 11000 ]]>
Tel. y fax.: 5520-0034
Correo electrónico: felipe.vadillo@uia.mx
Recibido: 25 de mayo de 2004
Aceptado: 22 de junio de 2004
RESUMEN
Objetivo: Este estudio fue diseñado para validar y caracterizar un modelo de cultivo de membranas corioamnióticas (MC) humanas que permita mantenerlas íntegras, viables y reproducir su capacidad de respuesta como tejido, que separa al compartimiento materno-fetal ante diversos estímulos asociados al proceso infeccioso.
Material y métodos: Se utilizaron MC de mujeres con 37-40 semanas de gestación, sin trabajo de parto activo, ni señales clínicas y/o microbiológicas de infección cervicovaginal. Las MC fueron sujetadas a una placa de cultivo tipo transwell, que permitió la formación de dos compartimentos independientes delimitados por la membranas que se mantuvieron en cultivo 96 h, se evaluó la integridad estructural mediante resistencia eléctrica transepitelial y análisis histológico. La funcionalidad se midió estimulando de manera independiente o cunjunta amnios y/o corion con 500 ng/mL de lipopolisacárido o 5 ng/mL de IL-1β y cuantificando la secreción de TNFα por ELISA y de Metaloproteasa-9 (MMP-9) por zimografía, respectivamente.
Resultados: Las diferentes poblaciones celulares de las MC se mantuvieron metabólicamente viables en el cultivo; los parámetros de integridad indicaron que no presentan cambios morfo-estructurales significativos. El estímulo con IL-1β induce secreción diferencial de MMP-9, que en corion alcanzó su máximo a la 4 h y en amnios a las 24 h. La estimulación selectiva con lipopolisacárido indujo la síntesis diferencial de TNFα, siendo el corion el principal productor con aproximadamente 60%.
Conclusiones: El sistema de cultivo de MC propuesto, permite estudiar cuantitativa y cualitativamente la contribución de las distintas poblaciones celulares del corioamnios en la respuesta ante el estímulo diferencial con agentes inmunológico-infecciosos.
ABSTRACT
Objective: This study was designed to validate and characterize a culture model of human choriamniotic membranes (HCM) that keeps their viability, integrity and capacity to reproduce a response to several stimulus associated to an infectious process, as the tissue that separates the fetal and maternal compartment.
Material and methods: We use HCM obtained after delivery by elective cesarean section. Women with 37-40 weeks of gestation without evidence of active labor or presence of clinical an microbiological signs of intrauterine/vaginal infection. The membranes were mounted in transwell devices, allowing testing two independent compartments (chorion and amnion) by physically separating the upper and lower chambers. 500 ng/mL of lipopolysaccharide was added to amniotic or chorionic surface and secretions of TNFα was measured in both compartments by specific enzyme-linked immunosorbent assays and Metalloproteinase-9 (MMP-9) secretions after stimulation with 5 ng/mL of IL-1β.
Results: The viability test showed that the different cellular populations of the HCM keep their metabolic viability along 96 h of culture. The integrity parameters showed that the stay without morphologic and structural changes. Functional markers showed that membranes responded differentially to IL-1β stimulus; production of MMP-9 in chorion reached its maximum value at 4 h, while amnion reached it at 24 h. The selective stimulation of chorioamnion with lipopolysaccharide induced a differential synthesis of TNFα; the chorion was the principal producer with approximately 60% of total TNFα.
Conclusions: The experimental model allows to study qualitatively and quantitatively the contribution of different cellular regions of the HCM, and its response to differential stimulation with immunologic agents.
KEY WORDS: Fetal membranes, chorion, amnion, intrauterine infection, IL-1β, TNFα.
INTRODUCCIÓN
]]> El embrión humano desarrolla durante el embarazo tejidos extraembrionarios accesorios que incluyen a la placenta y a las membranas corioamnióticas (MC), que en conjunto proveen al producto de diferentes mecanismos de intercambio, protección y control de las relaciones con su medio ambiente. Las MC delimitan la cavidad amniótica y están constituidas por dos capas histológicas adosadas, denominadas amnios y corion, cada una de las cuales está formada por diferentes tipos celulares embebidos en una prominente matriz extracelular, cuyo principal componente es la colágena, de la cual derivan su fuerza y elasticidad. 1Las MC son una identidad anatómica sumamente compleja y dinámica que secretan diferentes sustancias hacia el líquido amniótico y son capaces de responder a diferentes señales bioquímicas provenientes tanto del producto como de la madre. 2
Uno de los eventos que caracteriza a las etapas tardías del trabajo de parto normal es la ruptura de las MC, que junto con las contracciones uterinas y la dilatación del cuello del cérvix, preceden a la expulsión del producto. En la mayoría de los partos, las membranas permanecen íntegras hasta que el cuello uterino desarrolla dilatación avanzada, sin embargo, en algunas mujeres la ruptura de estas estructuras se presenta en ausencia de todos los demás eventos que caracterizan el trabajo de parto, situación que se denomina ruptura prematura de membranas (RPM). Esta patología obstétrica se presenta en pacientes con más de 20 semanas de embarazo y complica entre 5 y 10% del total de los embarazos en todo el mundo. 2,3
Tanto el mecanismo normal que condiciona la ruptura de las MC, como el que promueve la RPM son aún poco entendidos; sin embargo, a lo largo de los últimos años se ha conformado un panorama explicativo más extenso que permite entender que la RPM tiene un origen multifactorial. 4-7
Dentro de los factores que se han asociado de manera más directa con el desarrollo de la RPM, destaca la presencia de una infección cervico-vaginal o intrauterina, que puede explicar hasta la tercera parte del total de los embarazos complicados con RPM. 8Existen suficientes evidencias de que los microorganismos patogénicos existentes en cérvix y vagina pueden ascender hacia la región coriodecidual y eventualmente penetrar a la cavidad amniótica. En cada uno de estos puntos de contacto se disparan una red de señales que coordinan la defensa contra la infección, pero desafortunadamente, también producen daño colateral a las MC que podría terminar en RPM. 9 Parte de estas señales incluyen la secreción de citocinas, tales como: IL-1β, TNFα, IL-8 e IL-6 las cuales a su vez inducen la producción de factores uterotónicos como prostaglandinas E2 (PGE2) y F 2α (PGE 2α ) 10,11 y de metaloproteasas de matriz extracelular (MMP, por sus siglas en inglés) como la colagenasa tipo IV de 92 kDa o MMP-9 y la colagenasa IV de 72 kDa o MMP-2. A estos últimos mediadores se les considera como los efectores del daño a las MC, ya que su actividad alterada resulta en la degradación de la matriz extracelular que mantiene la arquitectura del corioamnios. 12,13 Sin embargo, y a pesar del avance en el entendimiento de la fisiopatogenia de la RPM, no es claro aún cómo, cuándo y en qué magnitud contribuyen, cada una de las poblaciones celulares de las MC, en la producción de los diferentes mediadores funcionales que median las respuestas que al final se manifiestan en RPM. Por lo anterior, decidimos diseñar, validar y estandarizar un sistema de cultivo de MC que permita mantenerlas íntegras, viables y funcionales, de modo que corion y amnios puedan ser estimulados con componentes del proceso infeccioso e inflamatorio en forma simultánea, independiente y selectiva, y poder así analizar la respuesta funcional de ambas regiones.
MATERIAL Y MÉTODOS
1. Cultivo de membranas corioamnióticas humanas.
Se utilizaron membranas corioamnióticas de mujeres con indicación de cesárea, con edades gestacionales entre 37 y 40 semanas, sin evidencia de trabajo de parto activo ni antecedentes o características clínicas y/o microbiológicas de infección cervicovaginal, coriodecidual y/o intraamniótica. Este proyecto fue evaluado y aprobado por los Comités de Investigación y Ética del Instituto Nacional de Perinatología (Código 212250-06101).
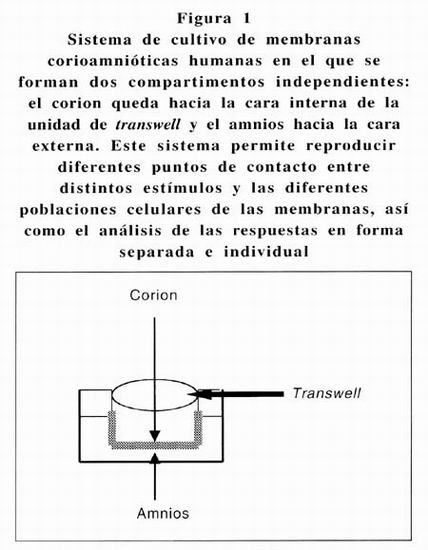
Las membranas fueron transportadas al laboratorio en Medio de Tagle modificado por Dulbecco (DMEM) estéril (Gibco BRL, Bethesda, USA), en condiciones de esterilidad. Fueron lavadas en solución Hanks 1X (Gibco BRL, Bethesda, USA) para remover los coágulos adheridos; posteriormente fueron cortadas manualmente en discos de 18 mm de diámetro y colocadas sobre una pieza de Transwell® (Costar, Acton, USA) de 12 mm de diámetro, en donde fueron sujetadas con una liga de silicón estéril. Con este sistema se formaron dos cámaras independientes, en donde el corion quedó hacia la cara superior y el amnios hacia la cara inferior, lo que permitió estimular y analizar en forma selectiva la respuesta en ambos lados de la membrana.
]]> En cada una de las dos cámaras se puso 1 mL de medio de cultivo DMEM suplementado con 10% de suero fetal bovino (SFB), 1 mm de piruvato de sodio, 100 U/mL de penicilina, 100 μg/mL de estreptomicina y 10 μg/mL de anfotericina B/Gibco, BRL, Bethesda, USA).Los explantes se incubaron a 37 ºC en una atmósfera con 5% de CO 2 ; el medio suplementado con SFB se recambió cada 24 h, por un periodo de 48 h. De 20 a 24 h antes de los experimentos, los explantes fueron cultivados en DMEM suplementado, con 0.2% de hidrolizado de lactoalbúmina (LAH), 1 mM de piruvato de sodio, 100 U/mL de penicilina, 100 μg/mL de estreptomicina y 10 μg/mL de anfotericina B (Gibco, BRL, Bethesda, USA).
2. Pruebas de validación del modelo.
a) Viabilidad
Fue determinada con una prueba colorimétrica, la técnica está basada en la transformación mediante una deshidro-genasa mitocondrial del compuesto azul de tetrazolio (XTT) en una sal de formazán, esta conversión sólo puede ser hecha por células metabólicamente activas 14 (Boeh-tinger, Manheim Germany). Brevemente: 200 μL de una mezcla del reactivo (acoplador de electrones - sal XTT 1:50) fueron agregados al medio de cultivo, en el que se encontraban las membranas, por un periodo de 1 h a 37 ºC. La conversión metabólica fue evidenciada por el cambio de color en el medio, el cual fue cuantificado espectrofotométricamente a 475 mm. La prueba se hizo en ambas caras de las membranas montadas en el transwell
b) Integridad
Para medir la integridad física y permeabilidad de las membranas en cultivo se calculó la resistencia eléctrica trans-epitelial/RET). 15 En esta técnica se utilizó como soporte un filtro de nitrocelulosa de 13 mm de diámetro, sobre el que se colocó el explante entre dos cámaras de Lucita® (llenas de medio DMEM) de una cámara de Ussing (UNAM, México); una vez montada la membrana y mediante dos electrodos de plata, se aplicó un pulso de 20 μAmp en la cara del corion y la deflexión del voltaje fue medida en la cara amniótica. La RET fue medida cada 24 h, por un periodo de cuatro días de cultivo. Los cálculos se hicieron con base en la Ley de Ohm y la contribución del filtro y del medio fueron restadas.
R = ∆V (14.135)Ω [cm] 2
Donde:
]]> R = Resistencia∆V = Voltaje final (Vf) - Voltaje inicial (Vi)
14.135 = Constante resultado de la relación entre el área total sometida a la corriente (0.02827 cm 2 ) y el amperaje (20x10 -6 amp).
c) Funcionalidad
Para determinar la capacidad de las MC para responder a estímulos funcionales, fueron estimuladas selectivamente con 5 ng/mL de IL-1β (R&D Systems, Minneapolis, USA) en corion y amnios, para poder cuantificar el efecto de esta citocina sobre la secreción al medio y actividad de la MMP-9, la cual se midió a través de un curso temporal a las 2, 4, 8, 12 y 24 h después del estímulo inicial mediante zimograma (ver detalle de la técnica más adelante).
3. Microscopía
La integridad anatómica del tejido fue analizada a lo largo de la 96 h que duró el periodo de cultivo. Las mismas membranas utilizadas para medir la RET fueron fijadas en buffer de Karnovsky, pH 7.3 (cacodilato de sodio 0.1M, glutaraldehído al 2.5%) y posteriormente incluidas en EPON; se hicieron cortes semifinos de 1μm, que fueron analizados mediante microscopía de luz.
4. Estimulación de las membranas en cultivo con lipopolisacárico (LPS)
Con el fin de estabilizar el tejido después de la manipulación y antes de la estimulación, los explantes fueron preincubados por 48 h con DMEM-SFB. Después de este tiempo fueron estimulados con 500 ng/mL de LPS de Escherichia coli 055:B5 (Sigma, St. Louis, USA).
Cada experimento montado en el sistema de Transwell incluyó las siguientes modalidades de estimulación por triplicado: Basales: Membranas control las cuales tanto corion como amnios fueron tratados únicamente con 100 μ1 de solución salina (vehículo); Ambos : El LPS fue añadido simultáneamente a ambos compartimientos, Corion: El LPS fue añadido únicamente a la cara del corion y, Amnios : El LPS fue añadido únicamente al compartimento en contacto con el amnios.
]]> Los medios de ambas cámaras fueron colectados 24 h después y se guardaron a -70 ºC hasta su uso. La concentración de proteínas en todas las muestras fue calculada con el método de Bradford.5. ELISA
La concentración de TNFα en el medio de cultivo fue cuantificada mediante ELISA tipo sandwich en microplacas de 96 pozos (Nunc Maxisorp, Denmark). La citosina se inmovilizó con 500 ng/pozo de anticuerpo monoclonal anti TNFα humana (R&D Systems, Minneapolis, USA), las placas fueron incubadas a 4 ºC toda la noche. El anticuerpo que no se unió fue removido lavando la placa con buffer de fosfatos a pH 7.4 con 0.05% de Tween 20 (PBS-Tween). La microplaca fue bloqueada con 300 μl por pozo de PBS con 1% de BSA, 5% de sacarosa y 0.05% de NaN 3 por 3 h a temperatura ambiente (TA). Se hizo una curva estándar usando TNFα recombinante humana (R&D Systems, Minneapolis, U.S.A.); la sensibilidad de la curva fue de 3.91 pg/mL en un intervalo lineal de 5.0 a 500 pg/mL. 100 μL de cada estándar o muestra fueron incubados toda la noche a 4 ºC, las microplacas se lavaron nuevamente tres veces y se incubaron con 25 ng/pozo del anticuerpo policlonal-biotinilado correspondiente (R&D Systems, Minneapolis, USA), por 2 h a TA, después de lavar tres veces la microplata, ésta fue incubada con 9.0 ng/pozo de conjugado streptavidina/fosfatasa alcalina (Gibco BRL, Bethesda, U.S.A.) por 1.5 h a 37 ºC; para generar la reacción colorimétrica que fue leída a 450 nm en un lector de microplacas (DYNATECH MR 500), se agregaron a cada pozo 100 μg de p-nitrofenilfosfato como substrato (Sigma, St. Louis, USA).
6. Zimografía
La presencia y actividad de la MMP-9 se hizo mediante un ensayo de zimografía. Los geles de poliacrilamida al 8% se copolimerizaron con gelatina a una concentración de 1 mg/mL. La electroforesis se corrió a un amperaje constante de 10 mA por gel, en condiciones no desnaturalizantes; se usaron 0.5 μg de proteína por muestra en cada experimento. Fue incluido en cada gel un estándar de actividad para MMP-2 y MMP-9 obteniendo de una línea celular U937 de promielocitos (ATCC, Tockville, MD, U.S.A.). Los geles se lavaron en una solución al 2.5% de tritón X-100 por 30 minutos y posteriormente se incubaron durante 18 h a 37 ºC en buffer de actividad a pH 7.4 (50 mM Tris base, 0.15 M NaCl, 20 mM CaCl 2 y 0.02% de azida de sodio). Los geles se tiñeron con azul de coomasie R-250.
Para cuantificar la actividad gelatinolítica de la MMP-9, a cada gel se le hizo un análisis de densitometría con el software NIH-Image v1.6 8 (NIH, Bethesda, USA). La actividad lítica es estimada como el área de cada banda.
7. Análisis estadístico
La comparación entre los diferentes grupos se hizo mediante prueba de Kruskal-Wallis en las que una p ≤ 0.05 fue considerada significativa, todos los experimentos se hicieron por quintuplicado.
RESULTADOS
]]> Al utilizar el sistema de cultivo de las membranas corioamnióticas sobre la unidad de Transwell permitió la formación de dos compartimentos independientes (Figura 1). De esta forma se pudieron hacer las diferentes pruebas de validación y la estimulación con LPS, logrando, así, analizar el comportamiento del corion y del amnios por separado.
La prueba de viabilidad mostró que las poblaciones celulares, tanto del corion como del amnios, se mantuvieron viables y metabólicamente activas durante las 96 h que duró el periodo de cultivo (Figura 2).

La prueba que permitió evaluar la integridad de las membranas demostró que a lo largo de los cuatro días, las membranas no presentaron diferencias significativas en los valores de RET (Figura 3).

]]> Las mismas membranas que fueron utilizadas para la prueba de RET fueron procesadas mediante técnicas histológicas estándar y permitieron comprobar que las diferentes regiones que las conforman, mantuvieron la arquitectura estructural típica de un corio-amnios íntegro (Figura 4).

El corion secretó MMP-9 en respuesta al estímulo con IL-1β (Figura 5A). El análisis densitométrico de la zimografía indicó que, comparado con las condiciones control (0 h), el corion incrementó al doble la cantidad de enzima secretada después de 4 h, concentración que se mantuvo sin cambio hasta las 24 h.

El amnios respondió en forma proporcional al tiempo del estímulo, presentando el máximo hasta las 24 h, tiempo en el que secretó hasta siete veces más enzima, comparado con el control (0 h) (Figura 5B).
Comparado con los controles, la estimulación de las membranas con LPS indujo producción significativa de TNFα en ambos compartimentos; sin embargo, el LPS indujo en el corion una respuesta de hasta dos veces mayor que la que presentó la región del amnios (Figura 6).
]]>

DISCUSIÓN
Existe suficiente evidencia en la literatura para establecer la relación causal entre la respuesta a un proceso infeccioso en el tracto genital femenino y el desarrollo de RPM. 8,9 A este respecto, la respuesta de los diferentes componentes del corioamnios, a productos bacterianos y estímulos inmunológicos o infecciosos, ha sido demostrada en distintos estudios, los cuales se han enfocado a preparaciones celulares de corion y amnios 16 o membranas enteras, 17 en donde no se han preservado las relaciones e integridad anatómica de las mismas. En estos estudios, células aisladas del corion, estimuladas con IL-1, TNFα o LPS, respondieron produciendo IL-816 y citocina (que también es secretada como respuesta a la estimulación directa con estreptoco del grupo B). 18
En un estudio similar, preparaciones celulares de amnios tratadas con IL-1β, TNFα o LPS, producen IL-6; 16 también se ha demostrado que el contacto directo con Streptococcus agalactiae, Escherichia coli, Bacilus fragilis, Mycoplasma hominis o Streptococcus aureus , induce a estas células a biosintetizar IL-6 e IL-8, pero no otras citocinas proinflamatorias como TNFα o IL-1β. 19
Otros reportes han mostrado que membranas enteras pueden expresar diferentes citocinas en respuesta a la estimulación con LPS, en donde, a nivel de la trascripción se favorece la expresión del ARNm de IL-1β, exclusivamente del lado del corion; sin embargo, la proteína se logra inmunolocalizar en ambas caras de la membrana. 17
Es en este punto en el que es clara la ventaja de contar con un modelo experimental in vitro , en el cual las membranas en cultivo se mantengan íntegras y viables para mantener las distintas vías de señalización intra-membranosas, así como la arquitectura estructural que existen in vivo . De esta forma, se puede analizar, cualitativa y cuantitativamente la contribución específica de las diferentes poblaciones de las membranas fetales a una red de respuestas que se entablan ante un ambiente inflamatorio.
Existen antecedentes que demuestran que las posibilidades de análisis de las diferentes respuestas son más amplias y completas en modelos en los que las MC se mantienen íntegras. Por ejemplo, de esta forma se pudo demostrar que diversas citocinas pueden atravesar las MC de un extremo a otro 20,21 y que, el estímulo con distintos productos bacterianos en un lado de la membrana se traduce en la síntesis de prostaglandinas en la cara opuesta. 22
El modelo que presentamos en este artículo preserva íntegras, viables y funcionales a las membranas; al mismo tiempo que mantiene la disposición anatómica y espacial que las identifica, como una barrera física entre el útero materno y el producto. Una consideración importante para la evaluación de este modelo es la conservación de la estructura mecánica durante el periodo de cultivo, lo que fue evaluado de dos maneras: la primera, siguiendo cambios en la conductancia del tejido con RET y que de existir pérdida de la continuidad estructural, debería reflejarse como disminución súbita de la resistencia al paso de la corriente; y la segunda, mediante la verificación de manera directa la permanencia de la estructura histológica.
Tal y como se demostró, la resistencia al paso de la corriente eléctrica de las membranas no se modificó durante el periodo de observación, lo anterior correlacionó con el aspecto histológico, que aunque mostró algunos cambos en la celularidad, no mostró modificaciones compatibles con la formación de espacios de pérdida de solución.
Todo lo anterior implica que en este sistema de cultivo, tanto corion como amnios forman compartimentos separados e independientes, tal y como sucede in vivo . Este modelo permite entonces, estimular selectivamente una o ambas caras de la membrana y analizar la respuesta simultánea o independiente de todas las poblaciones celulares que la conforman. Por otro lado, la evidencia de que las membranas reducen activamente al compuesto XTT, confirma que éstas mantienen su viabilidad durante el periodo experimental, lo que también se refuerza con la demostración de que son capaces de responder al estímulo con LPS, sintetizando TNFα.
]]> Las membranas responden al estímulo con LPS, secretando cantidades variables de TNFα en ambas regiones de la membrana, secreción que aparentemente depende del sitio inicial que fue estimulado con la endotoxina. La secreción de TNFα es dirigida mayoritariamente por el corion, sin embargo, el amnios reveló tener una capacidad intrínseca para secretar este factor proinflamatorio, lo que contradice otros estudios en los que no se ha logrado caracterizar al amnios, como un tejido capaz de producir esta citocina. 19 En nuestro estudio no evaluamos directamente la expresión de los ARNm de TNFα, por lo que no es posible concluir si la síntesis de la citosina se puede atribuir a un solo tejido o explicar la aparición de la proteína en ambos lados de la membrana, como una consecuencia del tráfico transmembranal de la mismaPor otro lado, las membranas responden a IL-1β secretando MMP-9 al medio, y con ello se pone en evidencia un mecanismo mediante el cual un miembro elemental de la red de citocinas, sintetizadas en respuesta a un estímulo infeccioso, favorece la síntesis y secreción de un mediador de la degradación del tejido conectivo del corioamnios, y de este modo, entender la progresión hacia la ruptura de las membranas. 1,2,13 Un hecho que es necesario destacar es que durante las condiciones del ensayo realizado nunca fue posible detectar la forma activa de la MMP-9 y los cambios encontrados deben ser referidos a la forma de proenzima de la MMP-9 (proMMP-9). Sin duda, el mecanismo de activación de esta enzima es un proceso más complejo que no ha sido caracterizado aún.
Este modelo experimental permite también hacer una correlación entre los diferentes marcadores funcionales y las distintas estructuras celulares que conforman el corioamnios, permitiendo potencialmente caracterizar la respuesta secuencial de los diferentes tipos celulares ante estímulos selectivos en ambas caras de la membrana, y aunque este modelo fue originalmente diseñado para estudiar al corioamnios en un ambiente que reproduce la respuesta inflamatoria, el potencial de uso es muy amplio, ya que permite evaluar estímulos de distinta naturaleza y analizar claramente cuál es la respuesta específica de las distintas regiones de las membranas fetales.
Este proyecto fue financiado por CONACYT Salud 2002 C01-7036.
REFERENCIAS
1. Parry S, Strauss JF. Premature rupture of the fetal membranes. N Engl J Med 1998; 338: 663-8. [ Links ]
2. Bryant-Greenwood Gd. The extracellular matrix of the human fetal membranes: Structure and function. Placenta 1998; 19: 1-11. [ Links ]
3. Narcio-Reyes ML, Polo E, Tejero E, López S, Casanueva E. Etiología y sintomatología de la infección cervicovaginal en pacientes embarazadas y su relación con la incidencia de la ruptura prematura de membranas. Perinatol Reprod Hum 1994; 8: 207-11. [ Links ]
4. Shubert PJ, Diss E, Iams JD. Etiology of preterm premature rupture of membranes. Obstet Gynecol Clin North Am 1992; 19: 251-63. [ Links ]
5. Keelan JA, Coleman M, Mitchel MD. The molecular mechanisms of term and preterm labor: recent progress and clinical implications. Clin Obstet Gynecol 1997; 40: 460-78. [ Links ]
6. Mercer BM. Preterm premature rupture of the membranes: etiology and implications for treatment. Prenat Neonat Med 1998; 3: 91-7. [ Links ]
7. Woods JR. Reactive oxygen species and preterm premature rupture of membranes. A Review. Placenta 2001; 15(Suppl A): S38-S34. [ Links ]
8. Asrat T. Intra-amniotic infection in patients with preterm prelabor rupture of membranes. Pathophysiology, detection, and management. Clinic Perinatol 2001; 28: 735-51. [ Links ]
9. Romero R, Mazor M, Wu YK, Sirtori M, Oyarzun E, Mitchell MD, Hobbins JC. Infection in the pathogenesis of preterm labor. Sem Perinatol 1988; 12: 262-79. [ Links ]
10. Mitchel MD, Branch DW, Lundin-Schiller S, Romero RJ, Dynes RA, Dudley DJ. Immunologic aspects of preterm labor. Sem Perinat 1991; 15: 210-24. [ Links ]
11. Goldenberg RL, Andrews WW, Hauth JC. Markers of preterm birth. Prenat Neonat Med 1998; 3: 43-6. [ Links ]
12. Fortunato SJ, Menon R, Lombardi SJ. Collagenolytic encimes (gelatinases) and their inhibitors in human amniochorionic membrane. Am J Obstet Gynecol 1997; 177: 731-41. [ Links ]
13. Maymon E, Romero R, Pacora P, Gervasi MT, Gomez R, Edwin SS, Yoon BH. Evidence of in vivo differential bioavailability of the active forms of matrix metalloproteinases 9 and 2 in parturition, spontaneous rupture of membranes, and intra-amniotic infection. Am J Obstet Gynecol 2000; 183: 887-94. [ Links ]
14. Gerlier D, Thomasset N. Use of MTT colorimetric assay to measure cell activation. J Immunol Methods 1986; 94: 57-63. [ Links ]
15. López-Vancell R, Montfort I, Pérez-Tamayo R. Galactose-specific adhesin and cytotoxycity of Entamoeba histolytica . Parasito Res 2000; 86: 226-31. [ Links ]
16. Mitchell DM, Trautman MS, Dudley DJ. Cytokine networking in the placenta. Placenta 1993; 14: 249-75. [ Links ]
17. Menon R, Swan KF, Lyden TW, Rote NS, Fortunato SJ. Expression of inflammatory cytokines (interleukin-1β and interleukin-6) in amniochorionic membranes. Am J Obstet Gynecol 1995; 172: 493-500. [ Links ]
18. Dudlye DJ, Edwin SS, Dangerfield A, Van Waggoner J, Mitchell MD. Regulation of cultured human chorion cell chemokine production by group B streptococci and purified bacterial products. Am J Reprod Immunol 1996; 36: 264-8. [ Links ]
19. Reisenberger K, Egarter C, Knöfler M, Schiebel I, Gregor H, Hirschl AM, Heinza G, Husslein P. Cytokine and prostaglandin production by amnion cells in response to the addition of different bacteria. Am J Obstet Gynecol 1998; 178: 50-3. [ Links ]
20. Kent ASH, Sullivan MHF, Elder MG. Transfer of cytokines through human fetal membranes. J Reprod Fertil 1994; 110: 81-4. [ Links ]
21. Steimer B, Elder MG, Visón S, Opri F, Weitzel HK, Sullivan MHF. Transfer of interleukin-8 through human fetal membranes in vitro. Med Sci Res 1998; 26: 63-6. [ Links ]
22. Rajasingam D, Bennett R, Alvi SA, Elder MG, Sullivan MHF. Stimulation of prostaglandin production from intact human fetal membranes by bacteria and bacterial products. Placenta 1998; 19: 301-6. [ Links ] ]]>