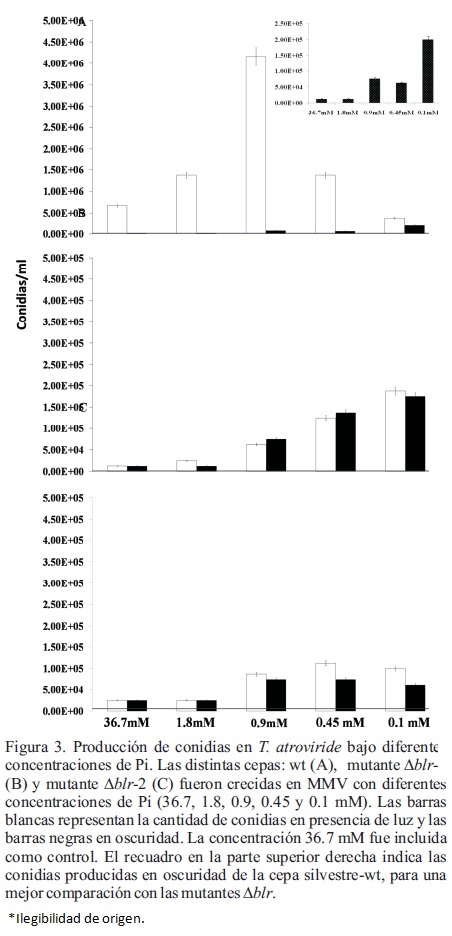
Efecto de la limitación de fosfato sobre la conidiación de Trichoderma atroviride y mutantes ciegas a la luz
The influence of phosphate limitation on conidiation in Trichoderma atroviride and light blind mutants
Macario Osorio-Concepción1, Sergio Casas-Flores2, Carlos Cortés-Penagos1
]]> 1 Facultad de Químico Farmacobiología, Universidad Michoacana de San Nicolás de Hidalgo, Tzintzunzan 173, Col. Matamoros, C.P. 58420, Morelia, Michoacán. México.
2 IPICYT, División de Biología Molecular. Camino a la Presa San José, No. 2055, Col. Lomas 4a. Sección C.P. 78216, San Luis Potosí, México.
* Autor para correspondencia:
Carlos Cortés Penagos neocccs@yahoo.com
Recibido 21 de octubre 2012;
Aceptado 19 de mayo 2013.
Abstract
]]> Molecular events associated with photoconidiation of Trichoderma are regulated by the BLR-1 and BLR-2 protein complex, where the first plays an essential role as sensor, and both function as a transcriptional factor. Null mutant strains of blr genes in T. atroviride are unable to respond to light stimulation and are then considered blind mutants. Limited concentration of essential nutrients in the media is a condition that triggers conidiation in T. atroviride. In the present study we show the influence of limited concentration of inorganic phosphate (Pi) in the media on photoconidiation in T. atroviride and two blr null mutants. All strains tested showed the development of conidial structures when low levels of Pi (0.1 mM) were present in the absence of light. The data showed that sensing environmental cues such as phosphate limitation is independent of BLR proteins pathway.Key words: Hypocrea, blr mutants, nutrition, morphogenesis, sporulation.
Resumen
Los eventos moleculares asociados a la conidiación inducida por luz en Trichoderma están regulados por el complejo formado por las proteínas BLR-1 y BLR-2, donde la primera actúa como fotorreceptor y ambas tienen actividad como factor de transcripción. Las cepas mutantes nulas en los genes blr de T. atroviride pierden la capacidad de responder al estímulo luminoso y son consideradas "mutantes ciegas". La limitación de algunos nutrientes esenciales también desencadenan la conidiación en T. atroviride. La influencia de bajas concentraciones de fosfato inorgánico (Pi) en el medio de cultivo sobre la fotoconidiación de la cepa silvestre y las mutantes blr de T. atroviride fue probada. Todas las cepas utilizadas mostraron el desarrollo de conidias bajo concentraciones limitantes de Pi (hasta 0.1 mM) en ausencia de la luz. Los resultados indican que la limitación de Pi es un factor desencadenante del proceso de conidiación a través de una vía independiente a la mediada por las proteínas BLR.
Palabras clave: Hypocrea, mutantes blr, nutrición, morfogénesis, esporulación.
Introducción
El género Trichoderma Pers. es un ascomiceto del orden Hypocreales que comprende una gran diversidad de especies saprobias, con un ciclo de vida prioritariamente asexual. Este tipo de reproducción se lleva a cabo a través de un programa de diferenciación de hifas que culmina con la formación de conidias. Las conidias, caracterizadas por su forma ovoide y pigmentación verde, se originan en fiálides dispuestas en conidióforos ramificados típicos de la especie (Rosen et al., 1974). La conidiación en Trichoderma puede ser estimulada por factores que propician un ambiente de estrés, como son: exposición a la luz, estrés nutricional, cambios en el pH del medio, daño o herida micelial (Horwitz et al., 1985; Nemcovic et al., 2008; Casas-Flores et al., 2004, 2006; Steyaert et al., 2010).
La formación de conidias inducidas por la luz en Trichoderma atroviride P. Karst. ha sido estudiada a nivel morfológico y genético (Horwitz et al., 1985; Schmoll et al., 2010). Es conocido que la aplicación de un pulso de luz sobre una colonia que creció en la oscuridad estimula el desarrollo de conidias justo en el sitio donde incidió el pulso, formando un anillo de conidiación característico (Betina, 1984). De los primeros eventos moleculares inducidos por la luz en T. atroviride están: el incremento en los niveles de AMPc intracelular, la activación de la enzima adenilato ciclasa, la fosforilación de proteínas, cambios en el potencial de membrana, variaciones en los niveles de ATP y la transcripción diferencial de genes (Gresík et al., 1988, 1991; Kolarova et al., 1992; Nemcovic et al., 1998; Sulova et al., 1990; Berrocal-Tito et al., 2000). La respuesta al estímulo luminoso en T. atroviride está regulada por las proteínas BLR-1 y BLR-2 (Blue Light Regulator), ortólogas a las proteínas WC-1 y WC-2 (White Collar) descritas en Neurospora crassa (Casas-Flores et al., 2004; Castellanos et al., 2010). Por la homología que presenta la proteína BLR-1 con WC-1 de N. crassa se ha propuesto que ésta actúa como fotorreceptor, pero se requiere de ambas proteínas para conformar el sistema activo de fotorecepción en Trichoderma. El complejo BLR-1/BLR-2 (BLRC) interactúa con el ADN a través de los dominios de dedo de zinc tipo GATA que contienen, regulando así la expresión génica (Ballario et al., 1996; Liu et al., 2003; Casas-Flores et al., 2004). Las cepas de T. atroviride nulas en los genes codificantes de las proteínas BLR-1 y BLR-2 (Δblr-1 y Δblr-2) pierden la capacidad de fotoconidiar, su desarrollo colonial se caracteriza por un micelio hialino sin conidias. Así, estas mutantes son consideradas "ciegas" al estímulo luminoso (Casas-Flores et al., 2004; Castellanos et al., 2010). El estrés nutricional también induce la formación de conidias en T. atroviride. Casas-Flores et al. (2006) analizaron el efecto de la limitación de fuentes de carbono (C) y nitrógeno (N) bajo un fondo genético mutante nulo para blr. El estrés por limitación de la fuente de N promovió la conidiación en las dos mutantes Δblr de forma similar a la cepa silvestre; este resultado demostró la independencia de las rutas de transducción entre la percepción de luz y de la limitación de este nutriente. Por otra parte, cuando la fuente de C fue limitada en ausencia de luz, sólo la cepa silvestre de T. atroviride generó los conidióforos típicos de la especie, no así las mutantes nulas. Este trabajo demostró la relación dependiente entre las vías de transducción para el estrés luminoso mediada por las proteínas BLR y aquellas relacionadas con la percepción del estrés nutricional de la fuente de C. Otro factor relacionado con la activación de eventos de diferenciación morfológica en T. atroviride y que hasta el momento no ha sido documentado es la limitación de fuentes de fósforo (P).
]]> El fosfato inorgánico (Pi) es un elemento nutricional importante para el crecimiento y diferenciación de todos los sistemas biológicos, considerado como limitante ya que el 95% de este ión se encuentra en forma de fosfato insoluble (Kang et al., 2002). Entre sus funciones biológicas están: a) elemento estructural en ácidos nucleicos y fosfolípidos; b) activación de metabolitos intermediarios; c) componente en la cascada de transducción de señales., d) regulación enzimática. La asimilación de este elemento está regulada por las proteínas transportadoras de fosfato (PHO) a través de dos sistemas de afinidad: 1) un sistema de baja afinidad expresado constitutivamente en altas concentraciones de Pi y 2) un sistema de alta afinidad inducido en condiciones escasas de Pi (Rausch et al., 2002). Los organismos como Saccharomyces cerevisiae, Escherichia coli, Aspergillus nidulans y N. crassa presentan genes pho implicados en la asimilación y transporte de Pi disponible en su entorno, los cuales operan bajo los sistemas de afinidad descritos. En N. crassa se han identificado los genes preg, pgov, nuc-2, nuc-1 que controlan el mecanismo molecular de la respuesta a la limitación de Pi, entre los cuales el gen nuc-1 codifica para un activador transcripcional que regula a los genes pho necesarios para la asimilación del Pi. La proteína NUC-1 presenta algunas características estructurales que le permiten llevar a cabo su función, tales como un dominio para su translocación al núcleo, dominios de unión a DNA y de interacción con factores de transcripción y dominios que responden a señales reguladoras (Mitchell y Tjian, 1989; Kang y Metzenberg, 1990). En este sistema, el producto del gen nuc-2 (NUC-2) detecta la concentración de Pi e inhibe la función del complejo PREG/PGOV para liberar a la proteína NUC-1 facilitando su translocación al núcleo (Peleg et al., 1996).El genoma de T. atroviride posee 2 genespho-5 y un pho-4 que codifican proteínas transportadoras de fosfato de alta afinidad, además de los genes preg, nuc-1, nuc-2 que codifican para una ciclina, un activador transcripcional y una proteína con repetidos de ankirina respectivamente. Estos genes son ortólogos a los descritos para N. crassa y podrian de igual forma regular los eventos moleculares de la respuesta al déficit de Pi (http://genome.jgi-psf.org/Triat2/Triat2.home.html). La capacidad de solubilizar y utilizar al ión fosfato ha sido estudiada en varias especies del género Trichoderma y representa una ventaja de adaptación ambiental para el género (Altomare et al., 1999; Rawat et al., 2011). Sin embargo, poco se sabe sobre el efecto que tiene este ión sobre la producción de conidias o de las rutas de transducción asociadas a la regulación del fenómeno de captación de Pi en Trichoderma.
Con el fin de lograr un mejor entendimiento sobre las bases moleculares de la conidiogénesis en Trichoderma, inducida por condiciones de estrés nutricional, en el presente trabajo se evaluó el papel y el efecto del déficit de Pi en la conidiación de T. atroviride y la posible relación entre su vía de señalización y aquella de respuesta a la luz mediada por las proteínas BLR.
Materiales y métodos
Microorganismos
Se utilizaron las cepas del hongo T. atroviride: cepa silvestre IMI206040 y sus mutantes blr (Δblr-1 y Δblr-2) (Casas-Flores et al., 2004).
Preparación del Medio Mínimo de Vogel (MMV)
El Medio de Vogel (MV) se preparó como una solución stock 50X según lo reportado (Vogel, 1965) sin incorporar las fuentes de P, C y N. El Medio Mínimo de Vogel (MMV) utilizado en los ensayos se preparó con (g/L): MV 1X, dextrosa 18, NH4Cl 5.3, agar bacteriológico 1.5. La fuente de Pi (KH2PO4) se agregó a partir de una solución stock con una concentración 1 M para tener una concentración final en el medio de 36.7, 1.8, 0.9, 0.45 y 0.1 mM.
]]>Cultivo y propagación de las cepas
Se colocó un bloque de micelio de cada cepa de T. atroviride en cajas con medio PDA (Papa Dextrosa Agar) para generar preinóculos que se incubaron en la oscuridad por 48 horas a 28 °C. Los bloques de micelio de los preinóculos se transfirieron al MMV con diferentes concentraciones de Pi con o sin papel celofán estéril según el ensayo a realizar (cuantificación de conidias o producción de biomasa). La manipulación de las cepas se realizó con luz roja de seguridad utilizando un filtro LEE # 183. Los cultivos se incubaron a 28 ° C en la oscuridad por 48 horas.
Ensayos de fotoinducción
A las colonias de T. atroviride con 48 horas de crecimiento en la oscuridad se les aplicó un pulso de luz blanca por 15 minutos. Para los ensayos de conidiación los cultivos se incubaron a 28 ° C por 48 horas posterior al pulso de luz.
Determinación de crecimiento
El micelio de las colonias de T. atroviride crecidas en MMV sobre papel celofán, se colectó cada 24 horas (de distintas cajas) hasta completar 96 horas y se colocó en un papel filtro a peso constante. El peso seco de la biomasa expresado en mg de micelio se obtuvo por diferencia de pesos.
]]> Determinación de la cantidad de conidias por fotoinducción
Para colectar las conidias producidas en cada colonia de Trichoderma se agregaron 5 mL de agua destilada y se raspó el micelio con una espátula. La suspensión se filtró a través de una gasa para separar las conidias de micelio. La cuantificación se llevó a cabo en una cámara de Neubauer. El número de conidias se calculó con la siguiente fórmula: (No. Conidias) (5) (10000) = No. Total de conidias/mL.
Resultados
Morfología colonial y microscópica de T. atroviride cepas silvestre y mutantes Δblr bajo condiciones limitantes de Pi
La conidiación en organismos fúngicos puede ser activada por múltiples factores abióticos que generan una condición de estrés (daño mecánico, pH, pulso de luz y el estrés nutricional). Con la finalidad de evaluar la conidiación de T. atroviride ante un ambiente condicionado por déficit de Pi se evaluó la formación de conidias inducida por un pulso de luz. En concentraciones estándar para este ión equivalente a 36.7 mM, previamente descrita para N. crassa, la colonia silvestre de Trichoderma desarrolló un anillo de conidias bien definido, mientras que bajo condiciones de oscuridad se observó crecimiento exclusivamente micelial (Figura 1A y B) como había sido reportado previamente (Betina, 1984; Horwitz et al., 1985). La disminución en la concentración de Pi en el medio (1.8, 0.9, 0.45 y 0.1 mM) no tuvo efecto en la respuesta de la cepa silvestre al estímulo luminoso, en todos los casos la formación de conidias fue en la zona donde recibió el pulso. En la concentración 0.1 mM de Pi, el anillo de conidiación mostró una ligera disminución de la pigmentación verde característica (Figura 1A). La morfología de las colonias de la cepa silvestre crecidas en la oscuridad en condiciones limitantes de Pi no mostró indicios de conidiación, en todos los casos se observaron colonias formadas por micelio hialino (Figura 1B). La morfología microscópica de la cepa silvestre de T. atroviride en condiciones estándar de Pi y después de haber recibido el pulso de luz se caracterizó por la presencia de hifas hialinas septadas y abundantes conidióforos ramificados, mismos que estuvieron ausentes bajo condiciones de oscuridad (Figura 2B y C). Al observar el comportamiento de esta cepa en condiciones limitadas de Pi y en presencia de luz, la formación de conidióforos se mantuvo presente aunque disminuida en los medios conteniendo 0.45 y 0.1 mM de Pi (Figura 2C). Resultó interesante la presencia de conidióforos en los cultivos en oscuridad, mismos que fueron evidentes en las concentraciones de 0.9, 0.45 y 0.1 mM de Pi (Figura 2B).
El análisis de fotoinducción en las mutantes Δblr bajo condiciones estándar y limitantes del ión fosfato mostró en el plano macroscópico, colonias con abundante micelio hialino. En ningún caso se observó el desarrollo del anillo de conidias que presentó la cepa silvestre (Figura 1B). Bajo condiciones de oscuridad, la limitación de Pi no tuvo efecto en ambas mutantes, las colonias se caracterizaron por un desarrollo micelial homogéneo y la ausencia de conidias (Figura 1A). Las colonias de las mutantes Δblr en la condición de 0.1 mM de Pi tuvieron un desarrollo escaso comparado con las otras concentraciones limitadas, independientemente de la exposición al estímulo de luz (Figura 1A y B). La observación al microscopio de las mutantes Δblr crecidas en la oscuridad o expuestas a un pulso de luz en concentraciones limitantes de Pi mostró la formación de conidióforos y conidias, estas estructuras no fueron observadas en las concentraciones de 36.7 mM y de 1.8 mM de Pi (Figura 2B y C).
Producción de conidias inducida por un estímulo luminoso en las cepas silvestre y mutantes Δblr de T. atroviride bajo condiciones limitantes de Pi
El estímulo luminoso es una de las condiciones desencadenantes de la formación de conidias en T. atroviride y con el propósito de evaluar la magnitud del efecto entre este estímulo y el ambiente de estrés propiciado por la limitación de Pi, así como una comparación cuantitativa entre la cepa silvestre y las mutantes ciegas a la luz, se determinó el número de conidias generadas en las diferentes concentraciones de Pi en el medio de cultivo (36.7, 1.8, 0.9, 0.45 y 0.1 mM).
]]> En la concentración estándar descrita para el medio de Vogel (36.7 mM), la cepa silvestre de T. atroviride generó después del pulso de luz, 6.75E+05 conidias/mL (Figura 3A). Al reducir la concentración de Pi 20 veces en el medio de cultivo (1.8 mM) la concentración de conidias incrementó al doble, esto es 1.38E+06 conidias/mL. La mayor concentración de conidias producidas por la fotoinducción en la cepa silvestre obtuvo en la concentración 0.9 mM de Pi en el medio (4.16E+06 conidias/mL) (Figura 3A). Por otra parte, la limitación del ión fosfato hasta 0.1 mM tuvo un efecto negativo en la producción de conidias alcanzando una concentración de 3.63E+05 conidias/mL. En la cepa silvestre de T. atroviride, al crecer en condiciones de oscuridad, la producción de conidias incrementó de manera proporcional a la limitación de Pi en el medio, de 1.25E+04 conidias/mL en la concentración de 36.7 mM a 2.25E+05 conidias/mL en la condición más limitada (0.1mM) (Figura 3A). El comportamiento de las cepas Δblr fue similar entre ellas, esto es, la producción de conidias incrementó en aquellos cultivos con concentraciones de Pi limitadas. La cepa Δblr-1 alcanzó el número máximo de conidias de 1.5E+05 en presencia de 0.1 mM de fosfato, esta respuesta fue independiente de la exposición de la colonia al pulso de luz (Figura 3B). Por otra parte, la mutante Δblr-2 generó un número menor de conidias, en el intérvalo de 5.0E+04, pero su formación resultó independiente de la exposición a la luz (Figura 3B).
Producción de biomasa de las cepas silvestre y mutantes Δblr de T. atroviride bajo condiciones limitantes de Pi
Con el fin de demostrar el efecto de la limitación del ión Pi sobre el crecimiento de T. atroviride, se cuantificó la biomasa producida en cada una de las colonias de acuerdo a lo descrito en materiales y métodos. La biomasa producida por la cepa silvestre en condiciones estándar de fosfato (36.7 mM) fue de 148.3 y 160.2 mg con o sin la exposición a un pulso de luz respectivamente (Figura 4A). Una concentración de 1.8 mM de Pi no tuvo efecto sobre la producción de biomasa, donde alcanzó 147.4 mg (Figura 4B). Por otra parte, una concentración de 0.1 mM de fosfato en el medio disminuyó la cantidad de biomasa producida, la cantidad fue de 26.7 mg en la condición de oscuridad y 27.2 mg después del pulso de luz (Figura 4C). La diferencia en esta condición de crecimiento (0.1 mM) es de 6 veces menor con respecto a la biomasa cuantificada en la condición estándar de Pi.
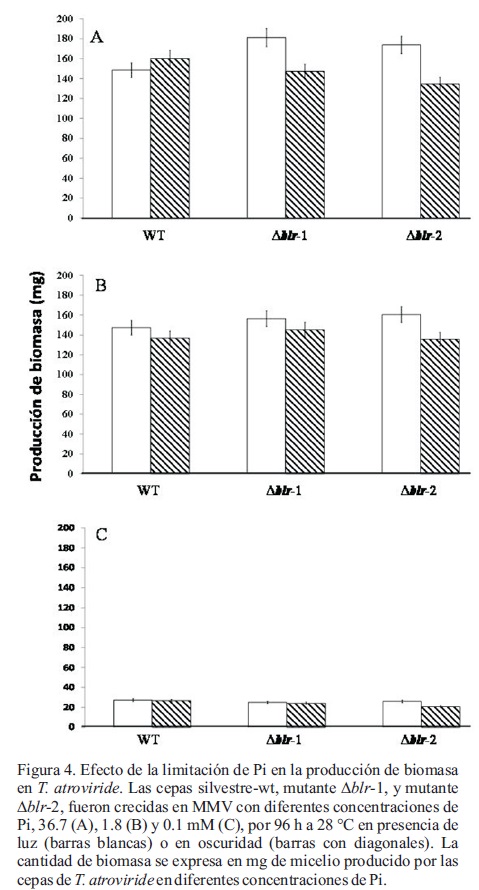
Al evaluar el crecimiento de las mutantes Δblr en condiciones estándar de Pi y después de 96 h de incubación, la biomasa alcanzó 156 y 145 mg después del estímulo de luz o sin él respectivamente (Figura 4A). Una condición de 1.8 mM del ión fosfato no tuvo efecto sobre la producción de biomasa en ambas mutantes. Sin embargo, la biomasa producida disminuyó a 22 mg en la condición de 0.1 mM de Pi para las mutantes Δblr, similar a la biomasa cuantificada en la cepa silvestre en la misma concentración de Pi (Figura 4B y C).
]]> Discusión
La formación de conidias en T. atroviride representa un fenómeno morfogenético complejo pero interesante desde el punto de vista de la biología celular de este hongo. Muchos son los factores descritos como determinantes para desencadenar este programa genético. La sola exposición de Trichoderma a un pulso de luz blanca induce la formación de conidias. Varios estudios sugieren que la fotomorfogénesis depende del estado metabólico de las hifas en crecimiento, composición del medio de cultivo y de la especie de Trichoderma empleada (Steyaert et al., 2010 b, c). En este sentido, el fosfato como nutriente esencial podría tener un impacto sobre la fotoconidiación de estas especies de hongos.
Con esto en mente, se analizó el efecto de la concentración del ión Pi, definida a partir de la utilizada en el medio de Vogel para N. crassa, sobre la conidiación de la cepa silvestre de T. atroviride. Una concentración de 0.9 mM o menor de fosfato en el medio de cultivo promovió la formación de conidióforos y conidias. El desarrollo de estas estructuras fue independiente de la exposición a la luz (Figura 2B y C) evidenciando que la sola limitación de este ión es inductora de la conidiación en Trichoderma. Bajo estas condiciones de limitación de Pi y ausencia del estímulo luminoso, las cepas mutantes Δblr, definidas como "ciegas" a la luz, fueron capaces de conidiar, demostrando que la conidiación mediada por estrés nutricional de fosfato no depende de las proteínas BLR previamente asociadas a la fotoconidiación de T. atroviride (Figura 2B y C). La conidiación inducida por la limitación de fosfato en las cepas mutantes sólo se hizo evidente a través de la observación microscópica ya que la morfología de la colonia no evidenció ningún cambio observándose micelio hialino abundante en condiciones de luz y oscuridad (Figura 1). Es posible que la escasa formación de conidióforos en las mutantes Δblr sea el resultado de una vía de señalización inducida solamente por el déficit de Pi. Esto sugiere que la vía de señalización generada por la luz a través de las proteínas BLR para la formación de conidias, se suma a la señal de estrés nutricional como se observó en la cepa silvestre crecida bajo una condición de 0.9 mM de Pi en el medio y la aplicación de un pulso de luz. Al analizar el efecto conjunto de los dos estímulos (luminoso y nutricional) sobre el crecimiento colonial de la cepa silvestre de T. atroviride, no se observaron cambios a nivel macroscópico. En la concentración más baja de Pi utilizada (0.1mM), se observó un anillo de conidias muy escaso (Figura 1A). A pesar de que la limitación de Pi indujo la formación de conidióforos y conidias en las cepas mutantes Δblr, la aplicación del pulso de luz no generó un cambio en su colonia, siendo en todos los casos sólo micelio hialino. El número de conidias producidas en ambas cepas mutantes en condiciones limitadas de Pi en presencia o ausencia de luz no tuvo diferencia alguna entre estas dos condiciones manteniendo una tendencia de aumento directamente proporcional al deficit de Pi (Figura 3B y C). Este comportamiento ante estrés nutricional coinciden con los datos de Casas-Flores et al (2004, 2006) donde las mutantes Δblr formaron conidias por la limitación de N en el medio de cultivo, demostrando la independencia de las rutas de transducción entre la percepción de luz y de la limitación de este nutriente. Nuestros resultados prueban que la privación de Pi simula un ambiente de estrés e induce la conidiación a través de una vía independiente a las proteínas BLR. Es probable que el mecanismo molecular de esta respuesta esté regulada por proteínas similares a las descritas e identificadas en N. crassa, como es el caso del activador transcripcional NUC-1 (Kang y Metzenberg. 1990). Las mutantes Δblr no forman conidios igual que la cepa silvestre en respuesta a los dos factores de estrés, esto sugiere la activación de una vía de señalización alterna generada únicamente por déficit de Pi y confirma la importancia de la vía mediada por las proteínas BLR para alcanzar el nivel de conidiación de la cepa silvestre. Es posible que estas dos vías convergan en algún punto de la cascada de señalización del proceso de conidiación, esto explicaría el aumento en el número de conidias generadas por cepa silvestre al crecer en una condición de 0.9 mM de Pi y en presencia de la luz (Figura 3A).
La determinación del número de conidias en la cepa silvestre de Trichoderma mostró que además del efecto potenciador de la luz sobre el de la limitación del ión fosfato, la concentración estándar de 36.7 mM contenida en la formulación original del medio de Vogel tiene un efecto negativo sobre la producción de conidias, ya que una concentración 40 veces menor de este ión (0.9 mM) es capaz de producir 6 veces más conidias en presencia de luz (Figura 3A). De acuerdo con este resultado es posible establecer que la concentración óptima para la conidiación de T. atroviride en un medio definido como el de Vogel es de no más de 1.0 mM de fosfato como KH2PO4. De esta forma, las condiciones reales de limitación del fosfato como nutriente estarían por debajo de dicha concentración. Esto se demuestra con el resultado del ensayo mostrado en la figura 4B, donde el crecimiento a una concentración de 1.8mM de Pi (20 veces menos que la condición estándar) de la cepa silvestre y mutantes de Trichoderma no se ve afectado. Por el contrario, al utilizarse 0.1 mM de fosfato la producción de biomasa se redujo de 15 a 18% de lo obtenido en la concentración de 36.7 mM. Este comportamiento coincide con el reporte realizado por Rawat et al. (2011), donde el crecimiento micelial de Trichoderma fue deficiente en fuentes de Pi como lo observado en Saccharomyces (Freese et al., 1981). La disminución de biomasa posiblemente se debe a la disminución de los niveles intracelulares de Pi que condiciona la síntesis de ATP, la síntesis nucleótidos y de fosfolípidos, además del efecto negativo sobre la fosforilación de proteínas, todos estos procesos necesarios para regular el metabolismo energético y el desarrollo celular. Así, bajo condiciones limitantes de Pi algunas funciones celulares permanecen activas con el objetivo de mantener el crecimiento hasta que las condiciones nutricionales sean favorables.
Los datos presentados constituyen el primer reporte que muestra a la limitación del ión fosfato como un factor de estrés desencadenante del programa de conidiación en T. atroviride. Es posible que el déficit de este ión se traduzca en un cambio en el estado redox intracelular como se ha sugerido para otros nutrientes esenciales (Casas-Flores et al., 2006; Friedl et al., 2008). La respuesta de este estímulo no parece estar ligada a la actividad de las proteínas BLR, previamente asociadas con la fotoconidiación, sin embargo la vía que señaliza el deficit de Pi podría interactuar con aquella asociada a la percepción de luz en algún otro elemento que permita amplificar la señal y desencadenar la producción de conidias en T. atroviride.
Agradecimientos
El presente trabajo fue apoyado por el proyecto SEP-CONACYT 83798 otorgado a Alfredo Herrera-Estrella y Sergio Casas-Flores. Macario Osorio Concepción recibió una beca de maestría del CONACYT, con número de becario 226637.
Literatura citada
]]>Altomare, C., W.A. Norvell,T. Bjorkman, G.E. Harman, 1999. Solubilization of Phosphates and Micronutrients by the Plant-Growth-Promoting and Biocontrol Fungus Trichoderma harzianum Rifai 1295-22. Applied and Environmental Microbiology 65: 2926-2933. [ Links ]
Betina, V., 1984. Photoinduced conidiation in Trichodermia Viride. Indian Journal of Microbiology 2:55-68. [ Links ]
Brotman Yariv, J., A.V. Gupta Kapuganti, 2010. Trichoderma Current Biology 20: 9. [ Links ]
Casas-Flores, S., M. Rios-Momberg, M. Bibbins, P. Ponce Noyola, A. Herrera-Estrella 2004. BLR-1 and BLR-2 are key regulatory elements for photoconidiation and mycelial grown in T. atroviride. Microbiology 150: 3561-3569. [ Links ]
Casas-Flores, S., M. Rios-Momberg, T. Rosales-Saavedra, P. Martinez-Hernandez, V. Olmedo-Monfil, A. Herrera-Estrella, 2006. Cross talk between a fungal blue-light perception system and the cyclic AMP signaling pathway. Eukaryotic Cell 5: 499-506. [ Links ]
]]>Castellanos, F., M. Schmoll, P. Martínez, D. Tisc, C.P. Kubicek, A. Herrera-Estrella, E.U. Esquivel-Naranjo, 2010. Crucial factors of the light perception machinery and their impact on growth and cellulase gene transcription in Trichoderma reesei. Fungal Genetic and Biology47: 468-476. [ Links ]
Freese, E.B., M. Chu, E. Freese, 1982. Initiation of yeast sporulation by partial carbon, nitrogen or phosphate deprivation. Journal of Bacteriology 149: 840-851. [ Links ]
Friedl, M.A., C.P. Kubicek, I.S. Druzhinina, 2008. Carbon source dependence and photostimulation of conidiation in Hypocrea atroviridis. Applied and Environmental Microbiology 74: 245-250. [ Links ]
Horwitz, B.A., J. Gressel, S. Malkin, 1985. Photoperception mutants in Trichoderma: mutants that sporulate in response to stress but not light. Current Genetics 9:605-613. [ Links ]
Kang, S., R.L. Metzenberg, 1990. Molecular analysis of nuc-1+, a gene controlling phosphorus acquisition in Neurospora crassa. Molecular and Cellular Biology 10: 5839-5848. [ Links ]
]]>Mitchell, P.J., R. Tjian, 1989. Transcriptional regulation in mammalian cells by sequence-specific DNA binding proteins. Science 245: 371378. [ Links ]
Nemcovic, M., L. Jakubikova, I. Viden, V. Farkas, 2008. Induction of conidiation by endogenous volatile compounds in Trichoderma spp. Fems Microbiology Letters 284: 231-236. [ Links ]
Peleg, Y., R. Addison, R. Aramayo, R.L. Metzenberg, 1996. Translocation of Neurospora crassa transcription factor Nuc-1 into the nucleus is induced by phosphorus limitation. Fungal Genetic and Biology 20: 185-191. [ Links ]
Rausch, C., M. Bucher, 2002. Molecular mechanisms of phosphate transport in plants. Planta 216: 23-37. Rekha, R., T. Lakshmi, 2011. Effect of abiotic stress on phosphate solubilization by biocontrol fungus Trichoderma sp. Current Microbiology 62:1521-6. [ Links ]
Schmoll, M., E.U. Esquivel-Naranjo, A. Herrera-Estrella, 2010. Trichoderma in the light of day: physiology and development.Fungal Genetic and Biology 47: 909-916. [ Links ]
]]>Steyaert, J.M., R.J. Weld, A. Mendoza-Mendoza, A. Stewart, 2010. Reproduction without sex: conidiation in the filamentous fungus Trichoderma. Microbiology 156:2887-900. [ Links ]
Steyaert, J.M., R.J. Weld, A. Stewart, 2010. Isolate-specific conidiation in Trichoderma in response to different nitrogen sources. Fungal Biology114: 179-188. [ Links ]
Kang,S.C., C.G. Ha, T.G. Lee, D. K. Maheshwari, 2002. Solubilization of insoluble inorganic phosphates by a soil-inhabiting fungus Fomitopsis sp. Current Science 82: 439-412. [ Links ]
]]>