
24 h de resuspensión, la EPC0 fue rebasada, indicando la movilización del P de la superficie hacia el interior de las partículas (etapa lenta). La adsorción fue el proceso dominante en los experimentos y, al aumentar la cantidad de sedimento resuspendido, los procesos de adsorción-desadsorción se acentuaron. Al comparar los flujos no conservativos de PID obtenidos con el modelo de LOICZ y los obtenidos en los experimentos de resuspensión, se observa que la adsorción del PID por las partículas puede generar una subestimación de ~20% de la heterotrofía neta del sistema, ya que la remoción de PID por adsorción enmascara su adición por la respiración neta de la comunidad.]]>
Contribución de la resuspensión de sedimentos a los flujos no conservativos de fósforo inorgánico disuelto en Bahía San Quintín, Baja California: Una estimación experimental
Contribution of sedimentary resuspension to non-conservative fluxes of dissolved inorganic phosphorus in San Quintín Bay, Baja California: An experimental estimate
M.C. Ortiz-Hernández1, VF. Camacho-Ibar1*, J.D. Carriquiry1, S.E. Ibarra-Obando2 y L.W. Daesslé1
1 Instituto de Investigaciones Oceanológicas, Universidad Autónoma de Baja California Ensenada. Baja California, México. *E-mail: vcamacho@uabc.mx
]]> 2 Centro de Investigación Científica y de Educación Superior de Ensenada. Ensenada, Baja California, México.
Recibido en octubre de 2002;
Aceptado en julio de 2003.
Resumen
Procesos abióticos como la resuspensión sedimentaria pueden contribuir a los flujos no conservativos del fósforo inorgánico disuelto (PID) en sistemas someros como Bahía San Quintín (BSQ), ya que los sedimentos resuspendidos pueden adsorber o desadsorber fósforo inorgánico. Se determinó en el laboratorio, mediante experimentos de adsorción-desadsorción, la contribución de los sedimentos en suspensión a las concentraciones del PID observadas en la columna de agua de BSQ variando el tipo de sedimento (arena fina y limo arenoso) en suspensión y su concentración, la concentración inicial de PID y el tiempo de resuspensión. En la primera etapa del proceso de adsorción (etapa rápida), ocurrida antes de las 10 h, se observó la concentración de fósforo en equilibrio (EPC0, por sus siglas en inglés). En sedimentos expuestos a > 24 h de resuspensión, la EPC0 fue rebasada, indicando la movilización del P de la superficie hacia el interior de las partículas (etapa lenta). La adsorción fue el proceso dominante en los experimentos y, al aumentar la cantidad de sedimento resuspendido, los procesos de adsorción-desadsorción se acentuaron. Al comparar los flujos no conservativos de PID obtenidos con el modelo de LOICZ y los obtenidos en los experimentos de resuspensión, se observa que la adsorción del PID por las partículas puede generar una subestimación de ~20% de la heterotrofía neta del sistema, ya que la remoción de PID por adsorción enmascara su adición por la respiración neta de la comunidad.
Palabras clave: PID, adsorción-desadsorción, LOICZ, isoterma de adsorción, Bahía San Quintín.
Abstract
]]> Abiotic processes like sedimentary resuspension may contribute to non-conservative fluxes of dissolved inorganic phosphorus (DIP) in shallow systems like San Quintín Bay (SQB), because suspended particles may adsorb or desorb inorganic phosphate. The contribution of suspended sediments to DIP concentrations in SQB was determined in the laboratory through adsorption-desorption experiments with two types of sediments (fine sand and sandy silt), and different concentrations of suspended particles, the initial concentration of DIP and resuspension time. The zero equilibrium phosphate concentration (EPC0) was observed during the first step of the adsorption process (fast step), which occurred before 10 h. The EPC0 was exceeded after 24 h of resuspension, indicating the diffusion of P from the surface toward the interior of particles (slow step). Adsorption was the dominant process in the experiments, and the intensity of adsorption-desorption was emphasized with an increase in the amount of resuspended particles. From the comparison of the non-conservative fluxes of DIP estimated using the LOICZ model with those estimated with resuspension experiments, we conclude that adsorption may lead to an underestimation of ~20% of net heterotrophy in SQB calculated with the LOICZ model, as excess respiration leads to a net release of DIP to the water column, but adsorption by particles masks this net release.Key words: DIP, adsorption-desorption, LOICZ, adsorption isotherm, San Quintín Bay.
Introducción
Bahía San Quintín (BSQ) es una laguna costera altamente productiva de Baja California (México) que exporta fósforo inorgánico disuelto (PID) hacia el mar adyacente durante la mezcla por mareas (Álvarez-Borrego y Chee-Barragán, 1976; Camacho-Ibar et al., 1999, 2003). Camacho-Ibar et al. (2003) aplicaron el modelo de balances biogeoquímicos propuesto por el Proyecto de Interacciones Tierra-Océano en la Zona Costera (LOICZ por sus siglas en inglés) para determinar el metabolismo neto del ecosistema (MNE = producción primaria bruta menos respiración de la comunidad) en BSQ, con base en el cálculo de los flujos no conservativos de PID (Gordon et al., 1996). Estos autores encontraron que BSQ es un cuerpo de agua generador neto de PID (i.e., los flujos no conservativos de PID son positivos), lo que implica que éste es un sistema heterótrofo neto (Camacho-Ibar et al., 2003). Sin embargo, esta conclusión presupone que los flujos no conservativos de PID representan un balance entre el consumo de PID por fotosíntesis y su regeneración por respiración de la comunidad. Esto implica que interacciones no biológicas del PID, como la adsorción hacia o la desadsorción desde las partículas en suspensión, se consideran despreciables comparadas con los procesos biológicos.
Las concentraciones de PID en ecosistemas acuáticos pueden ser controladas por procesos de adsorción o desadsorción. Froelich (1988) postuló que el ión ortofosfato interactúa con la superficie de las partículas en suspensión de tal forma que, cuando las concentraciones de PID se elevan, las partículas adsorben el fósforo (P), mientras que cuando las concentraciones de PID bajan, el P de las partículas se desadsorbe para compensar esta disminución en la columna de agua. Este proceso puede ser importante tanto en ríos (Carignan y Vaithiyanathan, 1999; Webster et al., 2001) como en ecosistemas estuarinos (Pratska et al., 1998) donde, en casos como el del Estuario Scheldt (Holanda), los flujos no conservativos de PID en alguna sección del estuario, y/o durante alguna época del año, pueden ser totalmente controlados por procesos de adsorción-desadsorción (Zwolsman, 1994).
La intensidad de las reacciones de adsorción o desadsorción de P está controlada por variables como el pH, la salinidad, el potencial redox, la concentración de PID, y el tipo y cantidad de sedimento en suspensión (Pomeroy et al., 1965; Froelich, 1988; Zwolsman, 1994). Los sedimentos acuáticos pueden ser ricos en P si presentan una fracción importante de limos y arcillas, ya que por su menor tamaño estas partículas presentan una mayor área superficial, además de que los óxidos de Fe y Al que las recubren son capaces de adsorber grandes cantidades de P (McManus et al., 1997; Matthiesen et al., 2001). La fracción lábil de Fe tiene mayor afinidad por el P ya que esta fase amorfa es más reactiva y su área superficial es mayor que las fases cristalinas (Danen-Louwerse et al., 1993; Langmuir, 1997; Sei et al., 2002).
La retención y liberación del P asociado con partículas ha sido descrita por Barrow (1983) como un mecanismo en dos etapas: la primera es un proceso rápido y generalmente reversible de adsorción-desadsorción sobre la superficie de las partículas que ocurre en minutos a horas; la segunda es la reubicación del P adsorbido en la superficie hacia sitios menos activos del interior de las partículas, en un proceso de difusión lenta que ocurre en días a meses.
El análisis de isotermas de adsorción es comúnmente utilizado para determinar la intensidad del proceso de adsorción-desadsorción. Las isotermas de adsorción son una representación gráfica de la relación entre la concentración del adsorbato (sustancia en solución que es adsorbida al adsorbente) y la cantidad adsorbida, en condiciones de equilibrio, a temperatura constante (Langmuir, 1997). Uno de los modelos que mejor se ajustan a datos de los experimentos con sedimento limo arenoso, es el de Freundlich, el cual se describe con la siguiente ecuación:

Otro parámetro importante que se obtiene de las isotermas es la concentración de fósforo en el equilibrio (por sus siglas en inglés se expresa como EPC0; Froelich, 1988) cuando ΔPd = 0, y es la concentración a la cual los sólidos despliegan su máxima capacidad de amortiguamiento. La pendiente de la recta formada por los datos alrededor de EPC0 corresponde al coeficiente de adsorción lineal (Kads; L g-1). El Kads proporciona información sobre la capacidad de amortiguamiento de la concentración de PID por las partículas resuspendidas; los sólidos con una alta capacidad presentan valores altos de Kads (Froelich, 1988).
La cantidad de sedimento resuspendido (Cp) es una variable importante asociada con el proceso de adsorción-desadsorción, ya que Cp es un indicador de la concentración de los sitios superficiales activos disponibles para la adsorción. Se ha observado que la capacidad de amortiguamiento de las partículas decrece al aumentar Cp, lo cual ha sido denominado "efecto de concentración de las partículas" (Di Toro et al., 1986; Honeyman et al., 1988; Herut et al., 1999). Dicho efecto se puede deber a: (1) que el equilibrio entre las fases disuelta y particulada no se ha alcanzado, (2) la competencia entre las partículas para ocupar sus sitios activos con el PID, ó (3) la presencia de coloides en la fase determinada como disuelta (Stumm, 1992).
En el presente trabajo se determinó experimentalmente la contribución de los procesos de adsorción-desadsorción por la resuspensión de sedimentos superficiales de BSQ a los flujos no conservativos del PID, y el impacto de dicha contribución en el cálculo del MNE obtenido para esta laguna costera mediante el modelo de LOICZ.
Materiales y métodos
Se recolectaron sedimentos superficiales en zonas arenosas y limosas de la bahía, mediante buceo autónomo, con un nucleador de plexiglas de 10 cm de diámetro. Para los experimentos se preparó una muestra compuesta mezclando los 2 cm superficiales de sedimentos de tres sitios aparentemente arenosos con otra muestra compuesta mezclando sedimentos de tres sitios aparentemente limosos. Con un analizador de partículas Horiba LA-910 se determinó que la composición granulométrica de las mezclas correspondía a arena fina (media = 140 µm) y limo arenoso (media = 80 µm). Entre la información generada con este instrumento se encuentra el área superficial específica, la cual representa la suma total del área superficial de las partículas en una muestra, por unidad de volúmen, suponiendo que las partículas son esféricas y con superficie lisa. Para cada muestra compuesta se determinó el contenido total de carbono con un analizador elemental LECO-CNHS y se realizó una descripción mineralógica mediante la observación al microscopio petrográfico de frotis preparados con la técnica descrita por Rothwell (1989). Además, se determinaron el contenido total de hierro y el de manganeso (Fe-T y Mn-T) tras una digestión con ácido nitrico, fluorhídrico y perclórico (Thompson y Walsh, 1989), así como el hierro y manganeso extraíbles con bicarbonato-ditionito (Fe-BD y Mn-BD), presentes como oxihidróxidos amorfos (Hupfer et al., 1995). Las determinaciones de Fe y Mn en los extractos se hicieron a la flama con un espectrómetro de absorción atómica Varian SpectrAA 220FS. También se determinó el contenido total de P, así como el asociado a las fracciones lábiles (fracciones extraíbles con cloruro de amonio y bicarbonato-ditionito) siguiendo el protocolo de extracción secuencial de fósforo particulado descrito por Hupfer et al. (1995).
Se realizaron experimentos de adsorción-desadsorción para los dos tipos de sedimento con las siguientes Cp de sedimento seco: 1, 0.5, 0.25 y 0.1 g L-1 (para facilitar la visualización de los resultados reportamos únicamente los casos de condiciones extremas de Cp). El valor de Kads para una Cp de 0.01 g L-1 se obtuvo por extrapolación con la tendencia de los datos en la relación de Kads vs. Cp. La extrapolación fue necesaria porque no fue posible realizar experimentos de adsorción-desadsorción con valores de Cp similares a las condiciones naturales ya que el límite de detección del método para determinar PID no hubiera permitido observar sus cambios a lo largo de los experimentos. El sedimento se añadió en húmedo a 200 mL de agua de océano abierto (0.2 ± 0.03 µM de PID), filtrada (0.2 µm), esterilizada con UV y con pH ~8.0 (proporcionada por el Dr. Doug Masten, ODF-SCRIPPS). El agua de mar se fortificó previamente con una solución estándar de KH2PO4 para obtener concentraciones aproximadas de 0, 0.5, 1, 2, 4 y 8 µM de PID. Los matraces se mantuvieron en un baño con agitación constante a 150 rpm y temperatura controlada a 20°C, el pH osciló a lo largo de los experimentos entre 7.9 y 8.2; se añadió azida de sodio (concentración final de 0.1%; Morin y Morse, 1999) para evitar cambios en las concentraciones de PID asociados con la actividad bacteriana. De cada experimento se extrajo una alícuota inicial al t = 0 y posteriormente alícuotas de 20 mL a los 5, 10, 15, 30, 180 y 600 min; para los experimentos con 1 y 0.25 g L-1 se extrajeron muestras adicionales a los 1440 (24 h) y 2880 (48 h) minutos. Las muestras fueron filtradas (GF/F) y el PID se determinó por colorimetría (Strickland and Parsons, 1972) con un espectrofotómetro UV/visible Cary 50 y una celda de 10 cm, con un límite de detección de 0.03 µM.
Se determinaron los valores de ΔPd, ΔPs, EPC0 y Kads, se graficaron las isotermas de adsorción y se ajustaron los datos a la ecuación de adsorción de Freundlich. Los datos obtenidos fueron extrapolados a la concentración máxima de sólidos suspendidos reportados en BSQ para así estimar la contribución abiótica bajo condiciones similares a las observadas en el medio natural. Se obtuvo una estimación de la capacidad de las partículas para amortiguar el P mediante el cálculo de Ω = 1 + Cp x Kads, donde Ω (adimensional) describe la capacidad de respuesta de las partículas para proveer o remover PID, y es función de las características texturales y mineralógicas de las partículas y las condiciones fisicoquímicas del sistema. Un valor de Ω = 1 implica que los sedimentos resuspendidos no tienen efecto sobre las variaciones en la concentración de PID (Webster et al., 2001).
]]> Resultados
Composición química y mineralógica
El contenido de arcillas fue menor a 8% en ambos tipos de muestras, pero el contenido total de lodos (fracción de limos + arcillas) fue cuatro veces mayor en el limo arenoso (tabla 1). En consecuencia, el área superficial, el contenido de carbono total, así como los contenidos de P, Fe y Mn en la fase lábil del limo arenoso fueron mayores que en la arena fina. Sin embargo, los contenidos totales de P, Fe y Mn fueron similares en ambos tipos de sedimento y mucho mayores que en la fase reactiva, lo que indica que la mayor parte del total de estos elementos se encuentra asociada a las fases no reactivas. Mineralógicamente, la arena fina estuvo compuesta principalmente por cuarzo >> plagioclasa (predominantemente cálcica como la oligoclasa) > ortoclasa > biotita, así como fragmentos de roca y abundantes minerales pesados, especialmente horblenda, piroxenos y magnetita. El limo arenoso se distinguió de la arena fina por su mayor abundancia relativa de biotita y magnetita, y por la presencia de agregados arcillosos, ausentes en la arena fina.
Experimentos de adsorción-desadsorción
Los valores ΔPd para limo arenoso con 1 g L-1 variaron en el intervalo de 0 a 6 µM, lo que indica que el proceso de adsorción fue más intenso bajo estas condiciones experimentales (fig. 1a). Sólo en los experimentos con 1 g L-1 de arena fina y concentraciones de PID < 1 µM (fig. 1c) se observó la predominancia del proceso de desadsorción a lo largo de todo el experimento (los valores negativos de ΔPd indican desadsorción). En los experimentos con 0.1 g L-1, para ambos tipos de sedimento (fig. 1b, d), los valores de ΔPd son, en general, más cercanos al cero comparados con los valores observados para 1gL-1; es decir, la magnitud de la adsorción y la desadsorción decrece y es más constante cuando Cp disminuye.
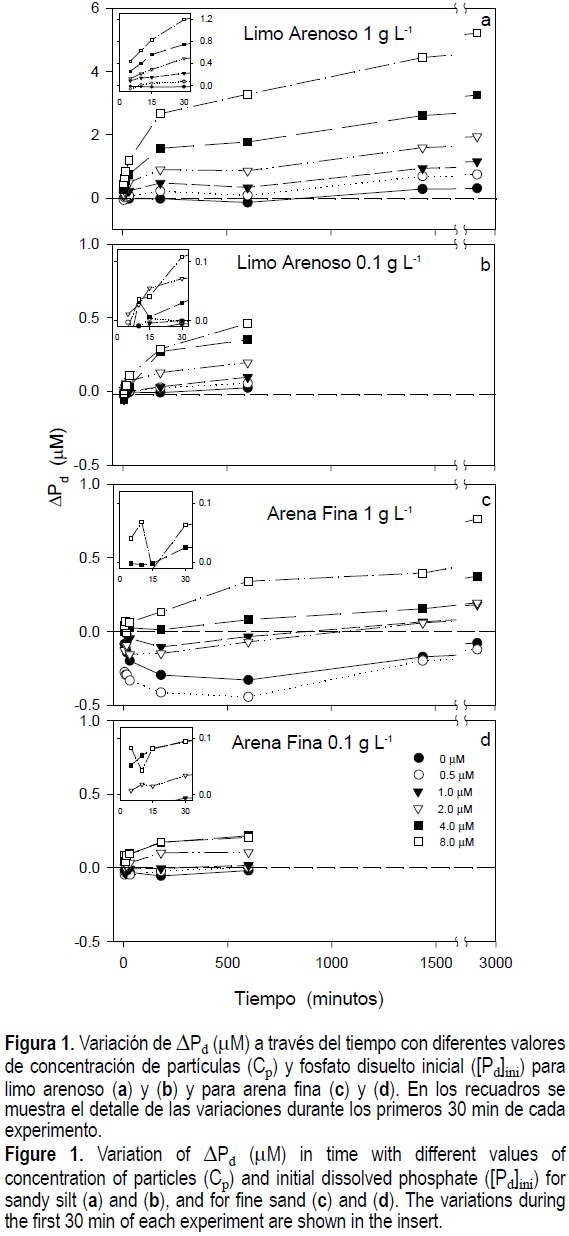
La pendiente de los datos cambió notoriamente entre los 180 y 600 min en muchos de los experimentos (fig. 1). Este cambio, particularmente claro en los experimentos con 1 g L-1 de limo arenoso (fig. 1a), indica que la etapa rápida del proceso de adsorción concluye entre las 3 y 10 h. Por lo anterior, las isotermas de adsorción (fig. 2) se construyeron con los datos para las 10 h. Para valores de Cp de 0.1 g L-1, con ambos tipos de sedimento las isotermas de adsorción mostraron un comportamiento tendiente a asintótico, a concentraciones mayores de 4 µM (fig. 2); esta tendencia no se observó para las Cp de 1 g L-1. Los valores de EPC0 para arena fina con 1 y 0.1 g L-1 fueron, respectivamente, ~3 y ~0.6 µM (fig. 2a); para limo arenoso con 1 g L-1 el valor EPC0 fue ~0.5 µM. En el caso del limo arenoso con 0.1 g L-1 no se obtuvo el valor de EPC0 ya que ningún valor de ΔPs intersectó la abscisa (fig. 2b). Con la disminución de Cp los valores de Kads para arena fina se incrementaron en todos los experimentos, mientras que para limo arenoso las Kads variaron poco entre el experimento con 1 g L-1 y el experimento con 0.1 g L-1 (tabla 2). La ecuación que describe la tendencia de los valores de las Kads en función de las Cp (fig. 3) fue utilizada para calcular la Kads correspondiente a una Cp de 0.01 g L-1. La Kads calculada para arena fina fue 6.24 L g-1, mientras que la Kads estimada para limo arenoso fue 0.91 L g-1 (fig. 3). Al disminuir Cp de 1 a 0.1 g L-1 los valores de Ω para arena fina se mantuvieron constantes, alrededor de 1.1, mientras que para limo arenoso estos valores disminuyeron de 1.9 a 1.1 (tabla 2).
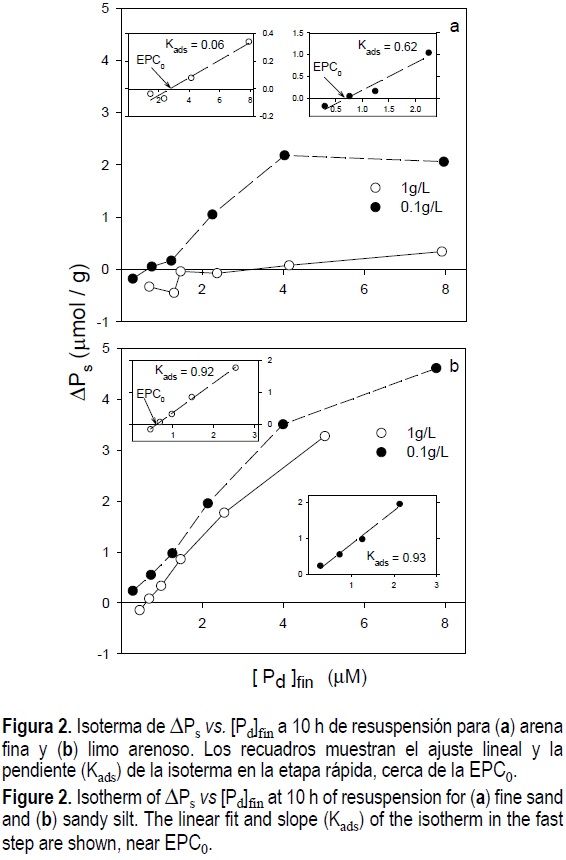

Los valores de ΔPs mostrados en la figura 2 fueron calculados para la isoterma tipo Freundlich comparando los valores predichos con los valores observados (fig. 4). Los mejores ajustes se obtuvieron para el limo arenoso (fig. 4c y 4d) con una r2 = 0.91 para 1 g L-1 y una r2 = 0.98 para 0.1 g L-1. La arena fina (fig. 4a, b) presentó una r2 = 0.54 con 0.1 g L-1, mientras que los valores negativos de ΔPs en arena fina con 1gL-1 no permitieron realizar el ajuste completo.
Discusión
Los resultados obtenidos con los experimentos de adsorción-desadsorción mostraron que la adsorción es el efecto dominante de las partículas en suspensión sobre el PID, especialmente cuando se presentan partículas finas en concentraciones altas (fig. 1a). Se observó que la remoción de PID se incrementa al aumentar Cp, por efecto de una mayor disponibilidad de sitios superficiales activos para la adsorción de P. El valor relativamente alto de Ω para limo arenoso con Cp de 1g L-1 (Ω = 1.9; tabla 2) indica una mayor capacidad de respuesta para el amortiguamiento de PID debido al mayor número de sitios activos disponibles. Sin embargo, con valores bajos de Cp (i.e., 0.1 g L-1 y el extrapolado a 0.01 g L-1) se observaron valores de Ω ~ 1, sugiriendo una probable saturación de los sitios activos. En contraste con el limo arenoso, los valores de Ω para arena fina son similares para todas las concentraciones de partícula, lo cual indica una capacidad menor para responder a las variaciones de PID, independientemente de la cantidad de partículas que se resuspendan. En este caso, las arenas finas tienen un área superficial menor y un número más limitado de sitios activos que se saturan rápidamente. Lo anterior sugiere que en BSQ la resuspensión sedimentaria, particularmente de partículas finas, favorece la adsorción de PID y que es más efectivo el amortiguamiento del PID al incrementarse la Cp. La desadsorción de P solamente ocurriría a lo largo de un periodo entre 0 y 48 h de resuspensión en presencia de concentraciones elevadas de arena fina resuspendida (1 g L-1) y concentraciones relativamente bajas, < 1 µM, de PID (fig. 1c); también puede presentarse desadsorción para concentraciones de PID entre 1 y 2 µM y periodos menores de 10 h (fig. 1c). Sin embargo, es poco probable que en BSQ se presente de manera natural esta concentración de partículas, ya que la cantidad máxima promedio reportada de sólidos suspendidos es ~0.014 g L-1 (Lara-Lara et al., 1980; García-Esquivel et al., 2003). Lo anterior sugiere que el proceso de desadsorción de P, a partir de las partículas resuspendidas, contribuye poco a mantener las concentraciones de PID en el intervalo de 1 a 5 µM, comúnmente observado en la columna de agua de esta laguna costera (Camacho-Ibar et al., 2003).
Los datos experimentales sugieren que la etapa rápida del proceso de adsorción ocurrió durante las primeras 10 h de resuspensión (fig. 1). Desde los primeros minutos de los experimentos el limo arenoso con Cp de 1 g L-1 presentó una mayor capacidad que la arena fina para adsorber PID, sin embargo, aún después de 600 min continuó el incremento en los valores de ΔPd con ambos tipos de sedimento (fig. 1a, c). Esto sugiere que la capacidad de amortiguamiento rápido de los sedimentos resuspendidos fue rebasada entre los 180 y 600 min, para posteriormente continuar con la etapa lenta del proceso de adsorción. Durante esta etapa, el P adsorbido en los sitios activos superficiales se moviliza por difusión lenta hacia el interior de las partículas (Froelich, 1988). Los valores máximos de ΔPd fueron observados durante la etapa lenta para limo arenoso a las 48 h, y su magnitud fue ~5 veces mayor que los máximos para la arena fina (fig. 1a, c). Sin embargo, es poco probable que en BSQ ocurra una adsorción de esta magnitud, ya que se requeriría mantener en resuspensión partículas en una concentración de 1 g L-1 por un periodo de 2 días.
Los experimentos con Cp de 0.1 g L-1 para ambos tipos de sedimento mostraron, en general, valores positivos de ΔPd pero muy cercanos a cero comparados con los datos para Cp de 1 g L-1 (fig. 1). En estos casos, el efecto de la concentración de PID en la magnitud de la adsorción fue menos evidente, indicando que el número de sitios activos fue menor y, en consecuencia, estaban mas cercanos a la saturación que en los experimentos con Cp elevadas. Con estos resultados se infiere que la magnitud de la adsorción es aún menor bajo concentraciones de partículas similares a las encontradas naturalmente en BSQ (Cp ~ 0.01 g L-1).
Este trabajo es una aproximación empírica para evaluar la magnitud de los procesos de adsorción-desadsorción de P en BSQ. Las diferencias en la capacidad de adsorción entre ambos tipos de sedimento se pueden explicar en función del diferente número de sitios activos como resultado de sus diferencias en el tamaño de grano, variable a partir de la cual se calculó el área superficial. Sin embargo, es importante aclarar que el área superficial disponible para la adsorción no sólo es función del tamaño de grano, sino también de la composición mineralógica de las partículas sedimentarias. Se ha documentado que, en contraste con la caolinita, otras arcillas como la illita y la montmorillonita tienen una mayor capacidad para adsorber P, ya que estas últimas tienen una mayor área superficial por su mayor contenido de oxihidróxidos amorfos de Fe (Edzwald et al., 1976; Sei et al., 2002). En este estudio, los agregados arcillosos observados al microscopio en el limo arenoso coinciden con los descritos para esta laguna costera por Gorsline y Stewart (1962), por lo que están probablemente constituídos por una mezcla de illita y montmorillonita. Sin embargo, Sei et al. (2002) reportaron diferencias en la capacidad de adsorción de P entre sedimentos dominados por un mismo tipo de arcilla, la caolinita, y esta diferencia se explicó cualitativamente en función del diferente contenido de óxido de Fe entre depósitos sedimentarios. En nuestro estudio, el contenido total de P, Fe y Mn fue similar en ambos tipos de sedimentos (tabla 1), lo cual indica que el contenido total de P y Fe no ayuda a explicar las diferencias en la capacidad de adsorción observadas; esto se debe probablemente a que un alto porcentaje (> 80%) del total de estos elementos se encuentra asociado a las fases minerales refractarias que no participan en los procesos de adsorción-desadsorción. En contraste, el limo arenoso presentó 50% más Fe y 3 veces más Mn en la fase sensible a redox que la arena fina. Esto indica que la mayor concentración de óxidos amorfos de Fe en los sedimentos finos de este estudio puede ayudar a explicar cualitativamente, mas no cuantitativamente, las diferencias en la capacidad de adsorción observadas en los experimentos de adsorción-desadsorción. Ya que el proceso dominante en este estudio fue la adsorción, el contenido ligeramente mayor de P en el extracto de bicarbonato-ditionito del limo arenoso (tabla 1) no ayuda a explicar la mayor capacidad de adsorción de PID de este tipo de sedimentos.
Las isotermas de adsorción de la figura 2 muestran el denominado "efecto de concentración de las partículas" (Honeyman et al., 1988). Este efecto fue más evidente en la arena fina, ya que los valores de Kads fueron aproximadamente 10 veces mayores con 0.1 g L-1 que con 1 g L-1 (fig. 2a). En este caso la adsorción por unidad de masa de sedimento se favoreció al disminuir la cantidad de sedimento presente, lo cual indica una posible competencia entre las partículas por el PID. En contraste, el limo arenoso presentó Kads similares, lo que indica que no hubo diferencias claras en la capacidad de adsorción de P al variar la Cp (fig. 2b). Este comportamiento puede explicar los mejores ajustes de la isoterma tipo Freundlich para el sedimento limo arenoso (fig. 4), ya que este modelo considera que no hay límite en el número de sitios activos para la adsorción y se ajusta mejor a partículas heterogéneas de sistemas naturales (Stumm, 1992).
]]> Efecto de la adsorción extrapolado para toda la BSQLa contribución de la adsorción a los flujos no conservativos de P en escala de toda la BSQ fue calculada a partir del valor de Kads para una Cp de 0.01 g L-1 (tabla 3). Con este valor de Kads se calculó APd para 0.01 g L-1 a partir de la relación APd = ΔPs x Cp, donde ΔPs se obtiene a partir de ΔPs = Kads x [Pd]fin. El valor utilizado de [Pd]fin fue de 2 µM, ya que éste es un valor promedio razonable a escala de toda la laguna (Camacho-Ibar et al., 2003).
Para el caso del limo arenoso, el valor utilizado de Kads fue de 0.91 L g-1, ya que para este tipo de sedimento la Kads es aparentemente independiente del valor de Cp (fig. 3). En contraste, la arena fina mostró un incremento en Kads al disminuir Cp (fig. 3), obteniéndose por extrapolación un valor de Kads de 6.3 L g-1 para una Cp de 0.01 g L-1. En la figura 3 se observa que los cambios en Kads para Cp < 0.1 g L-1 son más drásticos, y que pequeños cambios en el valor del exponente en la ecuación pueden resultar en cambios importantes en el valor extrapolado de Kads. Es necesario aclarar que, si bien la Kads incrementa al disminuir Cp, el valor de EPC0 decrece al disminuir Cp debido a la saturación de los sitios activos de estas partículas. En la figura 5 se observa que el valor de EPC0 para una Cp de 0.1 g L-1 es ~0.6 µM, mientras que el valor de EPC0 extrapolado para una Cp de 0.01 g L-1 fue ~0.08 µM (recuadro fig. 5). Esta observación indica que con valores de PID de ~0.1 µM las partículas de arena fina se saturan, por lo que es poco probable que con concentraciones de PID ~2 µM, típicas de BSQ, dichas partículas adsorban PID al resuspenderse. Debido a esto, el valor de [Pd]fin zutilizado para calcular el efecto de la resuspensión de arena fina fue 0.08 µM.
El valor calculado de ΔPd para arena fina fue menor que para limo arenoso, siendo 0.005 mmol m-3 y 0.02 mmol m-3, respectivamente (tabla 3); es decir, que las partículas resuspendidas del limo arenoso en BSQ pueden contribuir en mayor medida a la adsorción y tendrían la capacidad de remover de la columna de agua ~0.02 milimoles por cada m-3. Siendo el volumen total de BSQ ~ 90 x 106 m-3, las partículas de limo arenoso tendrían la capacidad de remover ~1700 moles de PID por día; esto ocurriría si el evento de resuspensión se mantuviera durante ~10 h con una Cp de 0.01 g L-1, a lo largo de toda la bahía. En cambio las partículas resuspendidas de arena fina tendrían la capacidad de remover ~450 moles de PID por día bajo las mismas condiciones de Cp en resuspensión y tiempo. Para el limo arenoso, la cantidad de PID potencialmente removida por adsorción representa ~25% del flujo no conservativo de PID de ~+7000 mol d-1, calculado con el modelo de LOICZ para datos de verano de 1996 (Camacho-Ibar et al., 1997), mientras que para arena fina corresponde a ~6% de dicho flujo. El signo positivo en el flujo refleja una adición neta de P inorgánico a la columna de agua, e indica que la suma de todas las reacciones internas de adición de PID (i.e., remineralización por respiración y desadsorción) es mayor que la suma de las reacciones internas de remoción (i.e., fotosíntesis y adsorción).
Si las partículas resuspendidas fueran limo arenoso, al excluir del flujo no conservativo total la remoción de PID asociada con la adsorción, se obtiene un flujo no conservativo de ~+8700 mol d-1 asociado exclusivamente con procesos biológicos. Es decir, por efecto de la adsorción, los flujos no conservativos de PID utilizados como indicadores del MNE han inducido una subestimación no mayor de ~20% en la magnitud de la heterotrofía neta de BSQ (Camacho-Ibar et al., 1997). Sin embargo, es posible que esta subestimación sea menor ya que la magnitud de la adsorción calculada experimentalmente representa posiblemente una sobreestimación de las condiciones de Cp, y tiempos de resuspensión que se puedan presentar de manera natural.
En contraste con los estuarios, BSQ es una laguna costera hipersalina donde las propiedades fisicoquímicas del agua no favorecen los flujos no conservativos abióticos del P en la columna de agua. En un estuario típico donde se mezcla agua dulce con agua de mar se presentan intensos gradientes en variables fisicoquímicas como el pH, el Eh y la salinidad, los cuales inducen la adsorción o la desadsorción de PID (Benitez-Nelson, 2000). Por ejemplo, la desadsorción del P se favorece por el incremento del pH porque induce un aumento en la repulsión electrostática debido a los cambios en la especiación del P de H2PO4- a HPO42-, y cambios en la carga de los oxihidróxidos de Fe (Zwolsman, 1994). En contraste, la mezcla por mareas, la carencia de aportes de un río, y la permanente oxigenación de la columna de agua (y los sedimentos superficiales) en BSQ minimizan los gradientes horizontales y verticales de pH, Eh y salinidad, limitando su contribución como variables importantes en los procesos de adsorción-desadsorción. Por lo tanto, la magnitud de los aportes abióticos a los flujos no conservativos de PID en BSQ está determinada esencialmente por el tipo de partículas y el tiempo que éstas se mantienen en resuspensión.
Agradecimientos
Se agradece al CONACYT el financiamiento al proyecto 25030-T y la beca doctoral a M.C. Ortiz (becaria No. 57593); y el apoyo SEP-FOMES 1999 para adquirir el espectrofotómetro y el analizador de tamaño de partículas. Se agradece a Víctor Macías (IIO-UABC) y a Vicente Guerrero-Herrera (Agromarinos) su apoyo durante el trabajo de campo. A Arturo Siqueiros y Enrique Navarro su apoyo en los análisis de Fe y Mn. A Arturo Martín Barajas por permitir el uso del microscopio petrográfico del Depto. de Geología del CICESE. A Doug Masten, del Oceanographic Data Facility - Institución Oceanográfica SCRIPPS, el abastecimiento del agua de mar baja en nutrientes. Un agradecimiento especial para Ian T. Webster (CSIRO-Australia) por su apoyo en el análisis de las isotermas.
]]> Referencias
Álvarez-Borrego, S. y Chee-Barragán, A. (1976). Distribución superficial de fosfatos y silicatos en bahía San Quintín, BC. Ciencias Marinas, 3(1): 51-61. [ Links ]
Barrow, N.J. (1983). A mechanistic model for describing the sorption and desorption of phosphate by soil. J. Soil Sci., 34: 733-750. [ Links ]
Benitez-Nelson, C.R. (2000). The biogeochemical cycling of phosphorus in marine systems. Earth-Science Rev., 51: 109-135. [ Links ]
Camacho-Ibar, V.F., Carriquiry, J.D. and Smith, S.V. (1997). Bahía San Quintín, Baja California (a teaching example). In: Comparison of Carbon, Nitrogen and Phosphorus Fluxes in Mexican Coastal Lagoons. LOICZ Reports and Studies No.10, pp. 9-15. [ Links ]
Camacho-Ibar, V.F., Carriquiry, J.D. and Smith, S.V. (1999). Bahía San Quintín, Baja California: N/P budgets within compartments in a coastal lagoon. In: Mexican and Central American Coastal lagoon Systems: Carbon, Nitrogen and Phosphorus Fluxes. LOICZ Reports and Studies No. 13, pp 65-78. [ Links ]
Camacho-Ibar, V.F., Carriquiry, J.D. and Smith, S.V. (2003). Non-conservative P and N fluxes and net ecosystem production in San Quintin Bay, Mexico. Estuaries (in press). [ Links ]
Carignan, R. and Vaithiyanathan, P. (1999). Phosphorus availability in the Paraná floodplain lakes (Argentina): Influence of pH and phosphate buffering by fluvial sediments. Limnol. Oceanogr., 44: 1540-1548. [ Links ]
Danen-Louwerse, H., Lijklema, L. and Coenraats, M. (1993). Iron content of sediment and phosphate adsorption properties. Hydrobiologia, 253: 311-317. [ Links ]
Di Toro, P.M., Mahony, J.D., Kirchgraber, P.R., O'Byrne, A.L., Pasquale, L.R. and Piccirilli, D.C. (1986). Effects of nonreversibility, particle concentration and ionic strength on heavy metal sorption. Environ. Sci. Technol., 20: 55-61. [ Links ]
Edzwald, J.K., Toensing, D.C. and Leung, M. Ch-Y. (1976). Phosphate adsorption reactions with clay minerals. Environ. Sci. Technol., 10: 485-490. [ Links ]
Froelich, P.N. (1988). Kinetic control of dissolved phosphate in natural rivers: A primer on the phosphate buffer mechanism. Limnol. Oceanogr., 33: 649-668. [ Links ]
García-Esquivel, Z., González-Gómez, M.A., Ley-Lou, F. y Mejía-Trejo, A. (2003). Potencial ostrícola del brazo oeste de Bahía San Quintín: Biomasa actual y estimación preliminar de la capacidad de carga. Cienc. Mar. (este volumen). [ Links ]
Gordon, D.C., Boudreau, P.R., Mann, K.H., Ong, J.E., Silvert, W., Smith, S.V., Wattayakorn, G., Wulff, F. and Yanagi, T. (1996). LOICZ (Land-Ocean Interactions in the Coastal Zone) biogeochemical modelling guidelines. LOICZ Reports and Studies No. 5, pp. 1-96. [ Links ]
Gorsline, D.S. and Stewart, R.A. (1962). Benthic marine exploration of Bahia de San Quintin, Baja California, 1960-61. Marine and quaternary geology. Pac. Nat., 3(8): 281-319. [ Links ]
Herut, B., Zohary, T., Robarts, R.D. and Kress, N. (1999). Adsorption of dissolved phosphate onto loess particles in surface and deep Eastern Mediterranean water. Mar. Chem., 64: 253-265. [ Links ]
Honeyman, B.D., Balistrieri, L.S. and Murray, J.W. (1988). Oceanic trace metal scavenging: The importance of particle concentration. Deep-Sea Res., 35: 227-246. [ Links ]
Hupfer, M., Gachter, R. and Giovanoli, R. (1995). Tansformation of phosphorus species in settling seston and during early sediment diagenesis. Aquat. Sci., 57: 305-324. [ Links ]
Langmuir, D. (1997). Aqueous Environmental Geochemistry. Prentice Hall, 560 pp. [ Links ]
Lara-Lara, J.R., Álvarez-Borrego, S. and Small, L.F. (1980). Variability and tidal exchange of ecological properties in a coastal lagoon. Estuar. Coast. Mar. Sci., 2: 613-617. [ Links ]
Matthiesen, H., Leipe, T. and Calado-Laima, M.J. (2001). A new experimental setup for studying the formation of phosphate binding iron oxides in marine sediments. Preliminary results. Biogeochemistry, 52: 79-92. [ Links ]
McManus, J., Berelson, W.M., Coale, K.H., Johnson, K.S. and Kilgore, T.E. (1997). Phosphorus regeneration in continental margin sediments. Geochim. Cosmochim. Acta, 61: 2891-2907. [ Links ]
Morin, J. and Morse, J.W. (1999). NH4+ release from resuspended sediments in the Laguna Madre estuary. Mar. Chem., 65, 97-110. [ Links ]
Pomeroy, L.R., Smith, E.E. and Grant, C.M. (1965). The exchange of phosphate between estuarine water and sediments. Limnol. Oceanogr., 10: 167-172. [ Links ]
Pratska, K., Sanders, R. and Jickells, T. (1998). Has the role of estuaries as sources or sinks of dissolved inorganic phosphorus changed over time? Results of a Kd study. Mar. Pollut. Bull., 36: 718-728. [ Links ]
Rothwell, R.G. (1989). Minerals and Mineraloids in Marine Sediments. An Optical Identification Guide. Elsevier Applied Science, USA, 279 pp. [ Links ]
Sei, J., Jumas, J.C., Oliver-Fourcade, J., Quiquampoix, H. and Staunton, S. (2002). Role of iron oxides in the phosphate adsorption properties of kaolinites from the Ivory Coast. Clays Clay Min. 50: 217-222. [ Links ]
Strickland, J.D.H. and Parsons, T.R. (1972). A Manual of Sea Water Analysis. 2nd ed. Fisheries Research Board of Canada, Ottawa, 310 pp. [ Links ]
Stumm, W. (1992). Chemistry of the Solid-Water Interface. Processes at the mineral-water interface in natural systems. John Wiley, USA., 428 pp. [ Links ]
Thompson, M. and Walsh, J.N. (1989). The Handbook of Inductively Coupled Plasma Spectrometry. 2nd ed. Blackie, Glasgow, 273 pp. [ Links ]
Webster, I.T., Ford, P.W. and Hancock, G. (2001). Phosphorus dynamics in Australian lowland rivers. Mar. Freshwater Res., 52: 127-137. [ Links ]
Zwolsman, J. (1994). Seasonal variability and biogeochemistry of phosphorus in the Scheldt Estuary, south-west Netherlands. Estuar. Coast. Shelf Sci., 39: 227-248. [ Links ]
]]>